文档内容
化学试题
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 S
32 Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 I 127 Ba 137
一、选择题(本大题共 25小题,每小题 2分:共 50分。每小题列出的四个备选项中只有一个
是符合题目要求的,不选、多选、错选均不得分)
1. 下列消毒剂的有效成分属于盐的是
A. 高锰酸钾溶液 B. 过氧乙酸溶液 C. 双氧水 D. 医用酒精
2. 下列物质属于强电解质的是
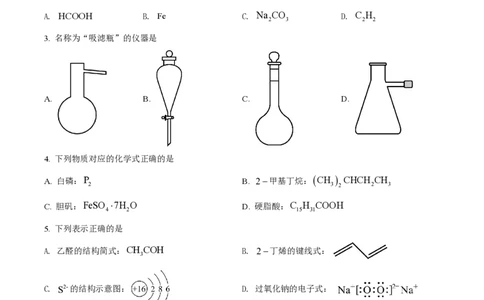
A. HCOOH B. Fe C. Na CO D. C H
2 3 2 2
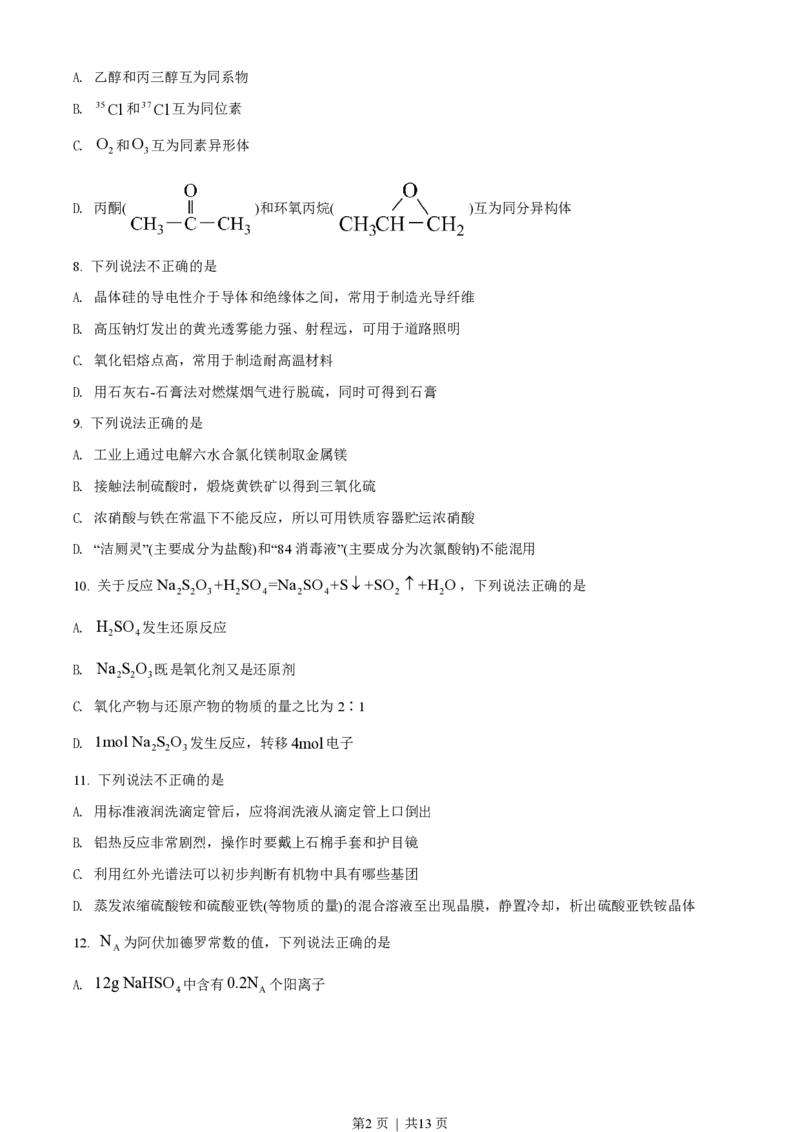
3. 名称为“吸滤瓶”的仪器是
A. B. C. D.
4. 下列物质对应的化学式正确的是
A. 白磷:P B. 2-甲基丁烷: CH CHCH CH
2 3 2 2 3
C. 胆矾:FeSO ×7H O D. 硬脂酸:C H COOH
4 2 15 31
5. 下列表示正确的是
A. 乙醛的结构简式:CH COH B. 2-丁烯的键线式:
3
C. S2-的结构示意图: D. 过氧化钠的电子式:
6. 下列说法不正确的是
A. 油脂属于高分子化合物,可用于制造肥皂和油漆
B. 福尔马林能使蛋白质变性,可用于浸制动物标本
C. 天然气的主要成分是甲烷,是常用的燃料
D. 中国科学家在世界上首次人工合成具有生物活性的蛋白质——结晶牛胰岛素
7. 下列说法不正确的是
第1页 | 共13页A. 乙醇和丙三醇互为同系物
B. 35Cl和37Cl互为同位素
C. O 和O 互为同素异形体
2 3
D. 丙酮( )和环氧丙烷( )互为同分异构体
8. 下列说法不正确的是
A. 晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
B. 高压钠灯发出的黄光透雾能力强、射程远,可用于道路照明
C. 氧化铝熔点高,常用于制造耐高温材料
D. 用石灰右-石膏法对燃煤烟气进行脱硫,同时可得到石膏
9. 下列说法正确的是
A. 工业上通过电解六水合氯化镁制取金属镁
B. 接触法制硫酸时,煅烧黄铁矿以得到三氧化硫
C. 浓硝酸与铁在常温下不能反应,所以可用铁质容器贮运浓硝酸
D. “洁厕灵”(主要成分为盐酸)和“84消毒液”(主要成分为次氯酸钠)不能混用
10. 关于反应Na S O +H SO =Na SO +S¯+SO +H O,下列说法正确的是
2 2 3 2 4 2 4 2 2
A. H SO 发生还原反应
2 4
B. Na S O 既是氧化剂又是还原剂
2 2 3
C. 氧化产物与还原产物的物质的量之比为2∶1
D. 1mol Na S O 发生反应,转移4mol电子
2 2 3
11. 下列说法不正确的是
A. 用标准液润洗滴定管后,应将润洗液从滴定管上口倒出
B. 铝热反应非常剧烈,操作时要戴上石棉手套和护目镜
C. 利用红外光谱法可以初步判断有机物中具有哪些基团
D. 蒸发浓缩硫酸铵和硫酸亚铁(等物质的量)的混合溶液至出现晶膜,静置冷却,析出硫酸亚铁铵晶体
12. N 为阿伏加德罗常数的值,下列说法正确的是
A
A. 12g NaHSO 中含有0.2N 个阳离子
4 A
第2页 | 共13页B. 11.2L乙烷和丙烯的混合气体中所含碳氢键数为3N
A
C. 8g CH 含有中子数为3N
4 A
D. 0.1mol H 和0.1mol I 于密闭容器中充分反应后,HI分子总数为0.2N
2 2 A
13. 下列反应的离子方程式不正确的是
A. 盐酸中滴加Na SiO 溶液:SiO2-+2H+=H SiO ¯
2 3 3 2 3
B. Na CO 溶液中通入过量SO :CO2-+2SO +H O=2HSO-+CO
2 3 2 3 2 2 3 2
C. 乙醇与K CrO 酸性溶液反应:3CH CH OH+2Cr O2-+16H+ ¾¾®3CH COOH+4Cr3++11H O
2 2 7 3 2 2 7 3 2
D. 溴与冷的NaOH溶液反应:Br +OH-=Br-+BrO-+H+
2
14. 下列说法不正确的是
A. 植物油含有不饱和高级脂肪酸甘油酯,能使溴的四氯化碳溶液褪色
B. 向某溶液中加入茚三酮溶液,加热煮沸出现蓝紫色,可判断该溶液含有蛋白质
C. 麦芽糖、葡萄糖都能发生银镜反应
D. 将天然的甘氨酸、丙氨酸、苯丙氨酸混合,在一定条件下生成的链状二肽有9种
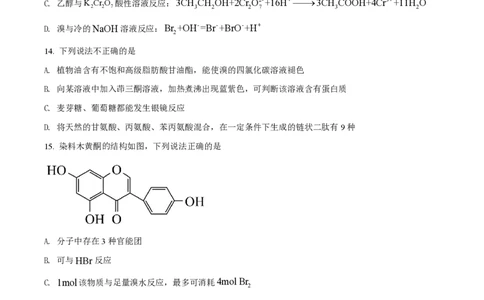
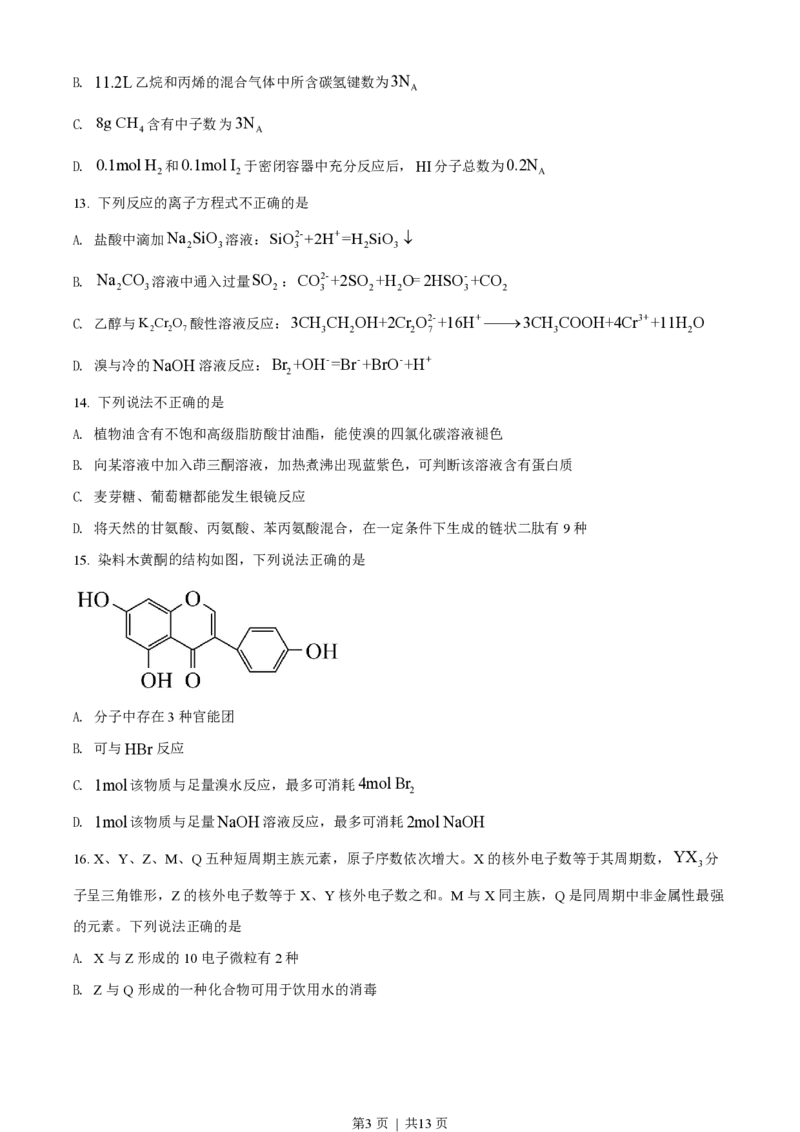
15. 染料木黄酮的结构如图,下列说法正确的是
A. 分子中存在3种官能团
B. 可与HBr反应
C. 1mol该物质与足量溴水反应,最多可消耗4mol Br
2
D. 1mol该物质与足量NaOH溶液反应,最多可消耗2mol NaOH
16. X、Y、Z、M、Q五种短周期主族元素,原子序数依次增大。X的核外电子数等于其周期数,YX 分
3
子呈三角锥形,Z的核外电子数等于X、Y核外电子数之和。M与X同主族,Q是同周期中非金属性最强
的元素。下列说法正确的是
A. X与Z形成的10电子微粒有2种
B. Z与Q形成的一种化合物可用于饮用水的消毒
第3页 | 共13页C. M Z与MQ的晶体类型不同
2
D. 由X、Y、Z三种元素组成的化合物的水溶液均显酸性
17. 25℃时,苯酚 C H OH 的K =1.0´10-10,下列说法正确的是
6 5 a
A. 相同温度下,等pH的C H ONa和CH COONa溶液中,c
C H
O-
>c
CH
COO-
6 5 3 6 5 3
B. 将浓度均为0.10mol×L-1的C H ONa和NaOH溶液加热,两种溶液的pH均变大
6 5
C. 25℃时,C H OH溶液与NaOH溶液混合,测得pH=10.00,则此时溶液中
6 5
c C H O- =cC H OH
6 5 6 5
D. 25℃时,0.10mol×L-1的C H OH溶液中加少量C H ONa固体,水的电离程度变小
6 5 6 5
18. 标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H O H O H O
2 2 2 2 2
能量/kJ×mol-1 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g)=H O (g)计算出H O 中氧氧单键的键能为214kJ×mol-1。下列说法不正确的是
2 2 2 2
A. H 的键能为436kJ×mol-1
2
B. O 的键能大于H O 中氧氧单键的键能的两倍
2 2 2
C. 解离氧氧单键所需能量:HOOc Cl- >c CH COO- >cCH COOH
3 3
24. 尖晶石矿的主要成分为MgAl O (含SiO 杂质)。已知:
2 4 2
MgAl O (s)+4Cl (g)=MgCl (s)+2AlCl (g)+2O (g) ΔH>0。该反应难以发生,但采用“加炭氯化法”
2 4 2 2 3 2
可以制备MgCl 和AlCl ,同时还可得到副产物SiCl (SiCl 沸点为58℃,AlCl 在180℃升华):
2 3 4 4 3
高温
MgAl O (s)+4C(s)+4Cl (g) MgCl (s)+2AlCl (g)+4CO(g)。下列说法不正确的是
2 4 2 2 3
A. 制备时要保持无水环境
B. 输送气态产物的管道温度要保持在180℃以上
C. 氯化时加炭,既增大了反应的趋势,又为氯化提供了能量
D. 为避免产生大量CO ,反应过程中需保持炭过量
2
25. 亚硝酸钠俗称“工业盐”,其外观、口感与食盐相似,人若误服会中毒。现将适量某样品(成分为亚硝酸
钠或氯化钠)溶于水配成溶液,分别取少量该溶液于试管中进行实验。下列方案设计、现象和结论都正确的
是
方案设计 现象和结论
先加入少量KClO 溶液,再加AgNO 溶液和足量稀硝酸, 若产生白色沉淀,则样品为亚硝酸
3 3
A
钠
振荡
第6页 | 共13页B 加到少量KMnO 溶液中,再加硫酸酸化,振荡 若溶液褪色,则样品为亚硝酸钠
4
C 先加到少量FeCl 溶液中,再加入稀盐酸酸化,振荡 若溶液变黄色,则样品为亚硝酸钠
2
若产生白色沉淀,则样品为亚硝酸
D 先加入少量Na SO 溶液,再加入BaCl 溶液和稀硝酸,振荡
2 3 2
钠
A. A B. B C. C D. D
二、非选择题(本大题共 6小题,共 50分)
26. 回答下列问题:
(1)乙醇的挥发性比水的强,原因是_______。
(2)金属氢化物是应用广泛的还原剂。KH的还原性比NaH的强,原因是_______。
27. 联合生产是化学综合利用资源的有效方法。煅烧石灰石反应:
CaCO (s)=CaO(s)+CO (g) ΔH=1.8´102kJ×mol-1,石灰石分解需要的能量由焦炭燃烧提供。将石灰
3 2
石与焦炭按一定比例混合于石灰窑中,连续鼓入空气,使焦炭完全燃烧生成CO ,其热量有效利用率为
2
50%。石灰窑中产生的富含CO 的窑气通入氨的氯化钠饱和溶液中,40%的CO 最终转化为纯碱。已知:
2 2
焦炭的热值为30kJ×g-1(假设焦炭不含杂质)。请回答:
(1)每完全分解100kg石灰石(含CaCO 90%,杂质不参与反应),需要投料_______kg焦炭。
3
(2)每生产106kg纯碱,同时可获得_______kg CaO(列式计算)。
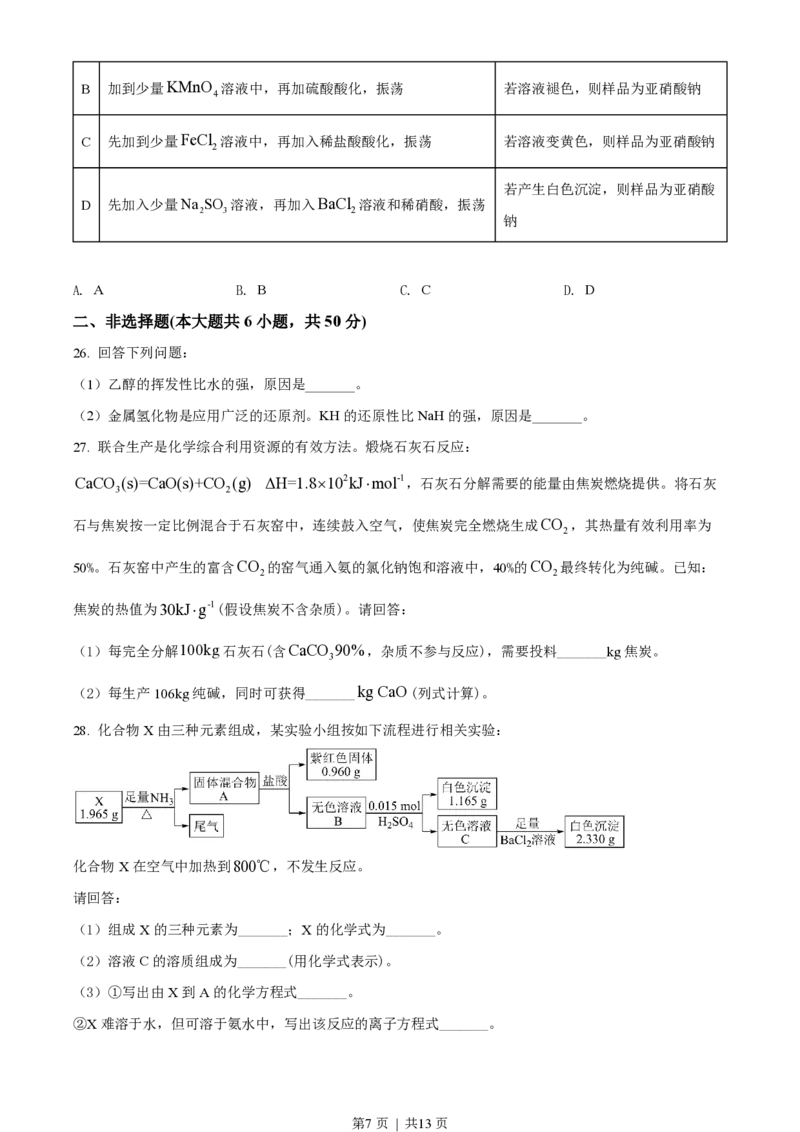
28. 化合物X由三种元素组成,某实验小组按如下流程进行相关实验:
化合物X在空气中加热到800℃,不发生反应。
请回答:
(1)组成X的三种元素为_______;X的化学式为_______。
(2)溶液C的溶质组成为_______(用化学式表示)。
(3)①写出由X到A的化学方程式_______。
②X难溶于水,但可溶于氨水中,写出该反应的离子方程式_______。
第7页 | 共13页(4)设计实验,检验尾气中相对活泼的2种气体_______。
29. 主要成分为H S的工业废气的回收利用有重要意义。
2
(1)回收单质硫。将三分之一的H S燃烧,产生的SO 与其余H S混合后反应:
2 2 2
3
2H S(g)+SO (g)ˆˆ† S (s)+2H O(g)。在某温度下达到平衡,测得密闭系统中各组分浓度分别为
2 2 ‡ˆˆ 8 8 2
cH S=2.0´10-5mol-1×L-1、cSO =5.0´10-5mol×L-1、cH O=4.0´10-3mol×L-1,计算该温度下
2 2 2
的平衡常数K=_______。
(2)热解H S制H 。根据文献,将H S和CH 的混合气体导入石英管反应器热解(一边进料,另一边
2 2 2 4
出料),发生如下反应:
Ⅰ 2H S(g) 2H (g)+S (g) ΔH =170kJ×mol-1
2 ƒ 2 2 1
Ⅱ CH (g)+S (g)ˆˆ†CS (g)+2H (g) ΔH =64kJ×mol-1
4 2 ‡ˆˆ 2 2 2
总反应:
Ⅲ 2H S(g)+CH (g)ˆˆ†CS (g)+4H (g)
2 4 ‡ˆˆ 2 2
投料按体积之比VH S:VCH =2:1,并用N 稀释;常压,不同温度下反应相同时间后,测得H 和
2 4 2 2
CS 体积分数如下表:
2
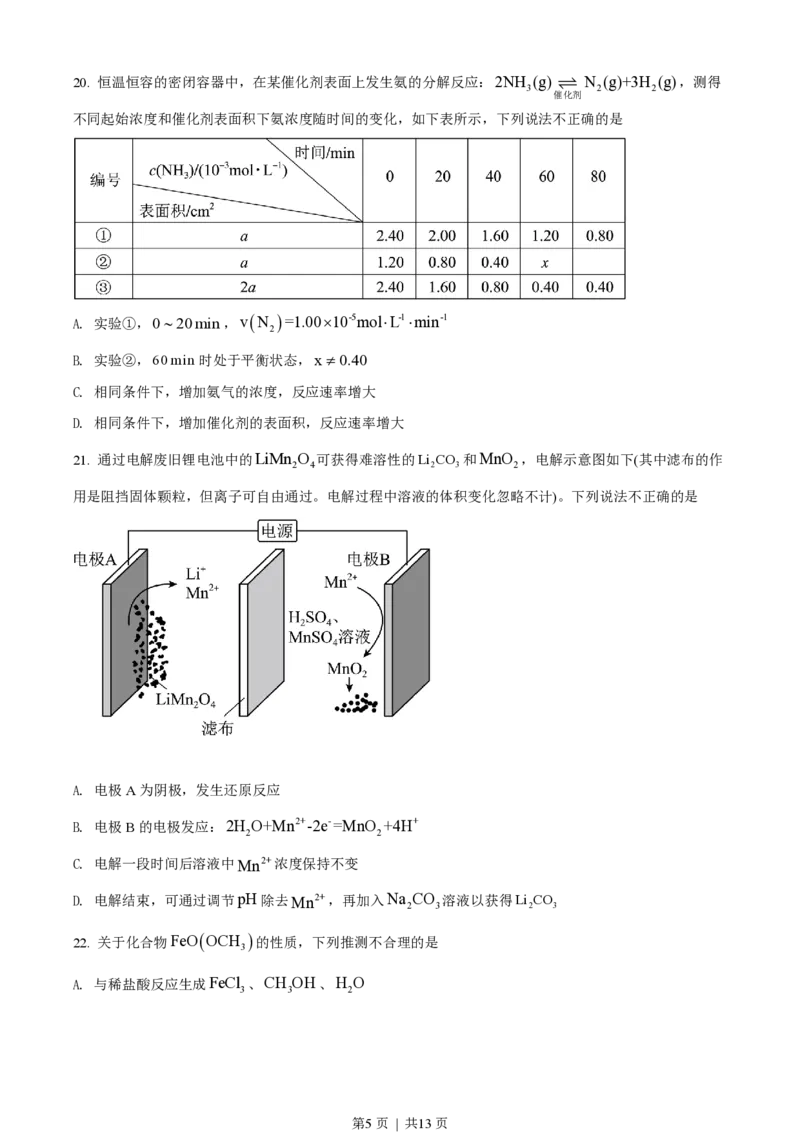
温度/℃ 950 1000 1050 1100 1150
H /V(%) 0.5 1.5 3.6 5.5 8.5
2
CS /V(%) 0.0 0.0 0.1 0.4 1.8
2
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代N 作稀释气体,对实验结果几乎无影响
2
B.其他条件不变时,温度越高,H S的转化率越高
2
C.由实验数据推出H S中的S-H键强于CH 中的C-H键
2 4
D.恒温恒压下,增加N 的体积分数,H 的浓度升高
2 2
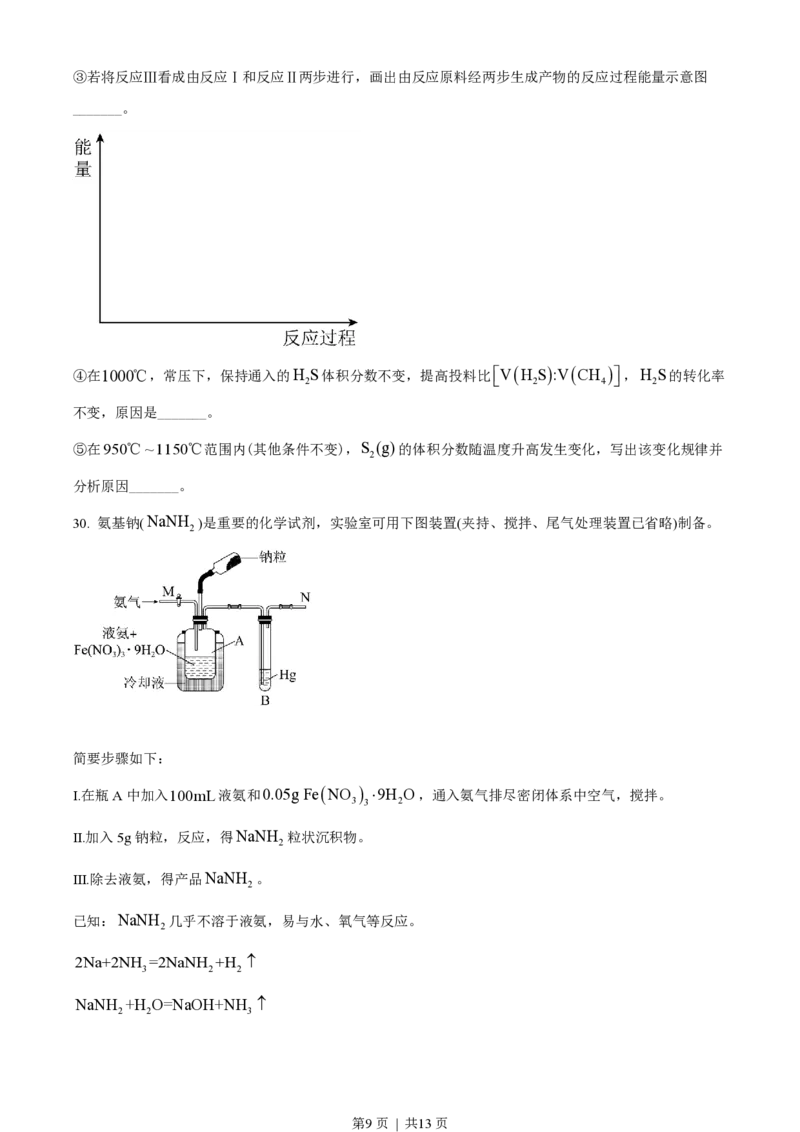
第8页 | 共13页③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意图
_______。
④在1000℃,常压下,保持通入的H
2
S体积分数不变,提高投料比é
ë
VH
2
S:VCH
4
ù û,H
2
S的转化率
不变,原因是_______。
⑤在950℃~1150℃范围内(其他条件不变),S (g)的体积分数随温度升高发生变化,写出该变化规律并
2
分析原因_______。
30. 氨基钠(NaNH )是重要的化学试剂,实验室可用下图装置(夹持、搅拌、尾气处理装置已省略)制备。
2
简要步骤如下:
Ⅰ.在瓶A中加入100mL液氨和0.05g FeNO ×9H O,通入氨气排尽密闭体系中空气,搅拌。
3 3 2
Ⅱ.加入5g钠粒,反应,得NaNH 粒状沉积物。
2
Ⅲ.除去液氨,得产品NaNH 。
2
已知:NaNH 几乎不溶于液氨,易与水、氧气等反应。
2
2Na+2NH =2NaNH +H
3 2 2
NaNH +H O=NaOH+NH
2 2 3
第9页 | 共13页4NaNH +3O =2NaOH+2NaNO +2NH
2 2 2 3
请回答:
(1)FeNO ×9H O的作用是_______;装置B的作用是_______。
3 3 2
(2)步骤Ⅰ,为判断密闭体系中空气是否排尽,请设计方案_______。
(3)步骤Ⅱ,反应速率应保持在液氨微沸为宜。为防止速率偏大,可采取的措施有_______。
(4)下列说法不正确的是_______。
A. 步骤Ⅰ中,搅拌的目的是使FeNO ×9H O均匀地分散在液氨中
3 3 2
B. 步骤Ⅱ中,为判断反应是否已完成,可在N处点火,如无火焰,则反应己完成
C. 步骤Ⅲ中,为避免污染,应在通风橱内抽滤除去液氨,得到产品NaNH
2
D. 产品NaNH 应密封保存于充满干燥氮气的瓶中
2
(5)产品分析:假设NaOH是产品NaNH 的唯一杂质,可采用如下方法测定产品NaNH 纯度。从下
2 2
列选项中选择最佳操作并排序_______。
准确称取产品NaNH xg®()®()®()®计算
2
a.准确加入过量的水
b.准确加入过量的HCl标准溶液
c.准确加入过量的NH Cl标准溶液
4
d.滴加甲基红指示剂(变色的pH范围4.4~6.2)
e.滴加石蕊指示剂(变色的pH范围4.5~8.3)
f.滴加酚酞指示剂(变色的pH范围8.2~10.0)
g.用NaOH标准溶液滴定
h.用NH Cl标准溶液滴定
4
i.用HCl标准溶液滴定
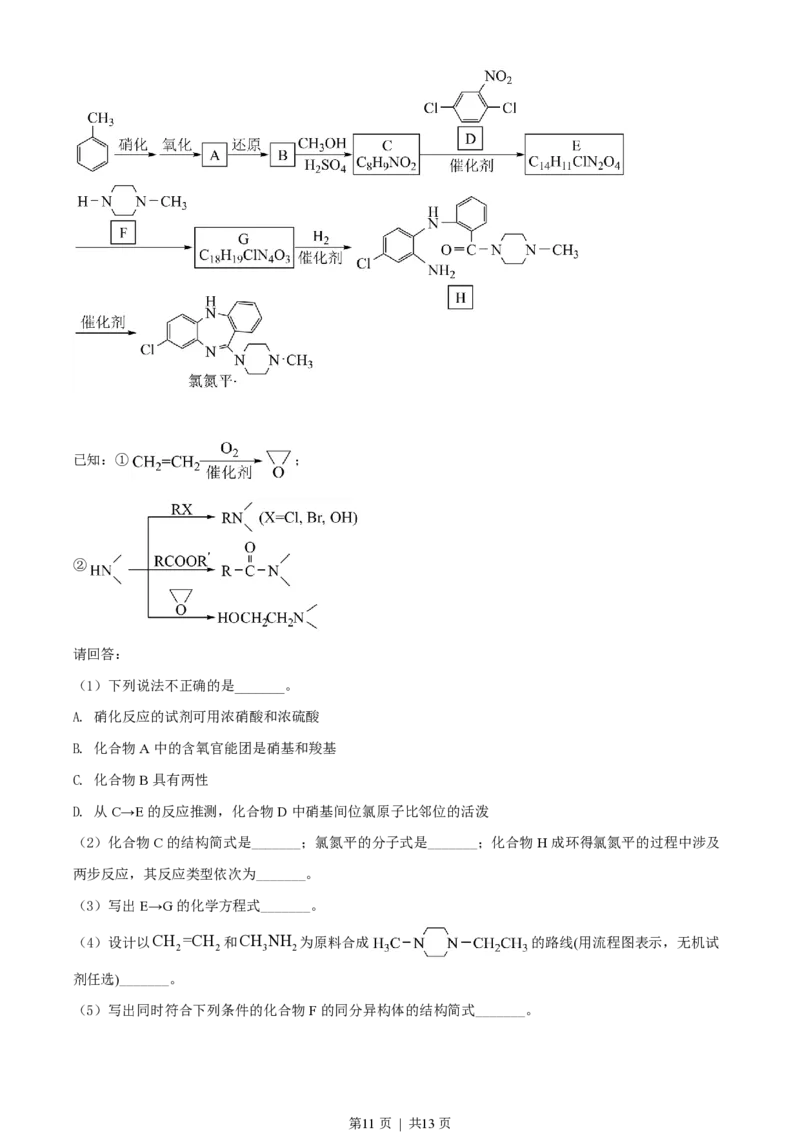
31. 某研究小组按下列路线合成药物氯氮平。
第10页 | 共13页已知:① ;
②
请回答:
(1)下列说法不正确的是_______。
A. 硝化反应的试剂可用浓硝酸和浓硫酸
B. 化合物A中的含氧官能团是硝基和羧基
C. 化合物B具有两性
D. 从C→E的反应推测,化合物D中硝基间位氯原子比邻位的活泼
(2)化合物C的结构简式是_______;氯氮平的分子式是_______;化合物H成环得氯氮平的过程中涉及
两步反应,其反应类型依次为_______。
(3)写出E→G的化学方程式_______。
(4)设计以CH =CH 和CH NH 为原料合成 的路线(用流程图表示,无机试
2 2 3 2
剂任选)_______。
(5)写出同时符合下列条件的化合物F的同分异构体的结构简式_______。
第11页 | 共13页①1H-NMR 谱和IR谱检测表明:分子中共有3种不同化学环境的氢原子,有N-H键。
②分子中含一个环,其成环原子数³4
第12页 | 共13页第13页 | 共13页