文档内容
2023 学年第二学期初中毕业班模拟考试(一)
化学
本试卷分两部分共 8页,20小题,满分 90分。用时 60分钟。
注意事项;
1.答卷前,参加测试学生务必用黑色字迹的钢笔或签字笔将自己的学校、姓名、考生号、试
室号、座位号填写在答题卡上。
2.选择题每小题选出答案后,用 2B铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改
动,用橡皮擦干净后,再选涂其他答案。答案不能答在试卷上。
3.非选择题必须用黑色字迹的钢笔或签字笔作答,答案必须写在答题卡各题目指定区域内相
应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。
不按以上要求作答的答案无效。
4.参加测试学生必须保持答题卡的整洁。测试结束后,将试卷和答题卡一并交回。
可能用到的相对原子质量:H:1C:12O:16Mg:24S:32Ca:40
第一部分选择题(共 42分)
一、选择题。(本题包括 14小题,每小题 3分,满分 42分。在每小题给出的四个选项中,
只有一项是符合题目要求。)
1.中华文明源远流长,太阳神鸟金饰、透雕龙凤纹重环玉佩、蚕丝素纱单衣、青铜纵目面具等,都是文化
瑰宝,下列说法不正确的是( )
A.太阳神鸟依旧色泽金黄是因为金的化学性质稳定
B.将天然玉石雕刻成玉佩,发生的是物理变化
C.蚕丝属于有机合成材料
D.青铜属于混合物
2.中国大力推进生态文明建设,下列做法不
.
利
.
于
.
生态保护的是( )
A.生活垃圾——露天焚烧 B.工业废水——处理排放
C.废旧金属——回收处理 D.农药化肥——合理使用
3.空气是人类宝贵的自然资源,下列关于空气的说法不正确的是( )
A.工业上通过分离液态空气的方法可得到N B.稀有气体中的He可用于飞艇
2
C.CO 是植物光合作用的重要原料 D.硫在氧气中燃烧的产物是SO
2 3
4.化学元素与人体健康息息相关,下列说法正确的是( )
A.过量摄入碘元素会引起甲状腺肿大
B.油脂是重要的营养物质,可大量摄入油脂
C.西红柿中含有丰富的蛋白质
D.食用甲醛溶液浸泡保鲜的水产品有利健康
5.劳动创造美好生活,下列家务劳动涉及的化学知识不正确的是( )
选项 家务劳动 化学知识
学科网(北京)股份有限公司A 用干布和带油的布依次擦拭被淋湿的自行车 隔绝空气和水
B 用炉具清洁剂清洗抽油烟机 炉具清洁剂中的NaOH能与油脂反应
C 用白醋除去热水瓶中的水垢 白醋能与碳酸盐反应
D 用草木灰( K CO )给大豆施肥 K CO 是复合肥料
2 3 2 3
6.对下列宏观事实的微观解释,合理的是( )
A.澄清石灰水显碱性:溶液中含氢氧根离子
B.臭氧在一定条件下可转化为氧气:原子种类发生变化
C.水蒸发为水蒸气:水分子体积变大
D.气球越吹越大:压强越大,分子间隔越大
7.镧元素在元素周期表中的相关信息如下图所示,下列有关说法不正确的是( )
A.La3+的核外电子数为54 B.一个镧原子的质量为138.9g
C.镧属于金属元素 D.镧的原子序数为57
8.用如图装置进行实验。通入O 前,白磷均不燃烧;通入O 后,甲中白磷不燃烧,乙中白磷燃烧。下列
2 2
说法不正确的是( )
已知:白磷的着火点为40°C;红磷的着火点为240°C。
A.该实验能验证可燃物燃烧需要与O 接触
2
B.该实验能验证可燃物燃烧需要温度达到着火点
C.若将乙中的白磷换成红磷,能验证可燃物燃烧需要与O 接触
2
D.若将O 换为N ,甲、乙中白磷均不能燃烧
2 2
9.燃料是人类社会重要的能源,下列说法不正确的是( )
A.汽车燃料改用压缩天然气可减少对空气的污染
B.炒菜时油锅着火,应立即用水浇灭
C.燃气灶火焰出现黄色,锅底出现黑色时,可增大灶具进风口
D.乙醇(
C H OH
)在空气中完全燃烧只生成二氧化碳和水
2 5
学科网(北京)股份有限公司10.学习小组以“水”为主题展开研究,下列有关说法不正确的是( )
A.试管a收集的气体是氢气
B.试管b收集的气体可用于炼钢、气焊等
C.电解水和水蒸发都属于化学变化
D.电解水的微观实质是分子分成原子,原子重新组合成新的分子
11.科学家用H 为原料消耗航天员呼出的CO 。该转化反应的微观示意图如下所示,下列说法正确的是
2 2
( )
A.该反应属于置换反应
B.反应前后的氧化物共有3种
C. 和 按个数比1:1进行该反应
D.该反应中消耗的 和生成的 的质量比为1:2
12.某课外活动小组制作了如下简易净水器,关于该净水器的说法正确的是( )
A.能除去水中的色素和异味 B.能起到杀菌消毒的作用
C.能将自来水转化为蒸馏水 D.能除去水中的所有杂质
13.镍(Ni)的金属活动性与铁相近,镍元素在化合物中常见+2价,下列预测正确的是( )
A.NiO能与NaOH反应生成Ni(OH)
2
B.NiCO 能与盐酸反应产生CO
3 2
C.Ni不能与稀硫酸反应产生H
2
学科网(北京)股份有限公司D.NiSO 溶液中的少量杂质CuSO 可加入Fe粉除去
4 4
14.关于下列实验的说法,不正确的是( )
A.实验①:小木棍上沾了浓硫酸的部位变黑,说明浓硫酸有腐蚀性
B.实验②:滴加稀盐酸后,试管外壁发烫,说明镁与稀盐酸反应放出热量
C.实验③:反应前后总质量相等,说明该反应符合质量守恒定律
D.实验④:氢气流吹出泡泡,说明氢气密度比空气大
第二部分非选择题(共 48分)
二、非选择题。(本题包括 6小题,共 48分。)
15.(7分)铁及其化合物在生产生活中有广泛应用。
(1)高铁酸钾( K FeO )是新型净水剂,K FeO 中Fe的化合价是_________。根据化合物的分类,
2 4 2 4
K FeO 属于________。推测高铁酸的化学式是__________。
2 4
(2)缺铁性贫血,其中“铁”是指____________(填“单质”或“元素”)。补铁剂FeCO 读作__________,它
3
可由碳酸铵和硫酸亚铁通过复分解反应可制得,写出该反应的化学方程式________。
(3)Fe(OH) 易转化为Fe(OH) ,存在反应4Fe(OH) +X+2H O=4Fe(OH) ,则X的化学式是
2 3 2 2 3
_______。
16.(9分)我国古代科技璀璨夺目,金属的冶炼和使用历史悠久。
(1)铁和铜在自然环境中都能被腐蚀,下列事实能说明铁比铜活泼的是_______(填字母)。
A.历史上铜比铁使用更早
B.铁制容器不能盛放硫酸铜溶液
C.FeCl 中Fe的化合价为+3,CuCl 中Cu的化合价为+2
3 2
(2)在兵马俑彩绘中发现了绝美“中国紫”,其原料有石绿(一种铜锈)和一氧化铅等。
Cu、O 、CO 与物质R共同作用生成铜锈[Cu (OH) CO ,难溶于水],则物质R一定含有_______元
2 2 2 2 3
素:铜锈中含有的原子团有OH−和_______(写离子符号);预测铜锈能与_______(填物质类别)反应。
(3)“乌铜走银”是一种独特的铜制工艺品技艺。乌铜是一种合金,乌铜经锻打、碾压可成不同厚度的乌铜
片,说明乌铜具有良好的_________。
(4)在乌铜表面的黑色物质主要是氧化铜。利用稀硫酸和铁从氧化铜中得到铜单质可通过以下两种方案
实现:
学科网(北京)股份有限公司方案一:FeH2 SO4→H CuO→Cu
2 ∆
方案二:CuOH2 SO4→CuSO Fe→Cu
反应I 4 反应II
①上述两种方案中较优的是_________,理由:______________;
②方案二中反应I的反应现象:_______________;
(5)乌铜的废料经初步处理后可得到AgNO 和Cu ( NO ) 的混合溶液。若向其中加入一定重的金属锌
3 3 2
粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的溶质是___________(写化学式)。
17.(8分)硫酸是一种重要的化工原料。
(1)下列硫酸的性质中,属于酸的共同性质的是____________(填字母)。
A.稀硫酸和镁粉反应 B.稀硫酸能使紫色石蕊溶液变红
C.稀硫酸和氢氧化钡溶液反应 D.稀硫酸和氯化钡溶液反应
(2)在稀硫酸中加入足量镁粉恰好完全反应,将反应后溶液中和液面上方存在的微观粒子的种类在图中
补充完整。(粒子数目不作要求;不考虑空气、水。)
(3)向滴有酚酞溶液的氢氧化钠溶液中,逐滴滴加稀硫酸至足量,当观察到____________的现象,证明
溶液中____________,可判断NaOH和H SO 发生了反应。
2 4
(4)甲同学将氢氧化钠溶液与稀硫酸混合,然后检验了混合液中含有Na+和SO2−,他据此认为该反应是
4
NaOH和H SO 发生了反应,且生成Na SO 。你认为甲同学是否找到了反应发生的证据?请说出你的
2 4 2 4
观点并阐述理由,___________。
(5)往氢氧化钡溶液中逐滴滴加稀硫酸至过量,测得溶液的温度变化如图a所示,溶液的电导率变化如
图b所示。(溶液的电导率越大,导电能力越强。)
①结合图像a分析,该反应过程是___________(填“放热”或“吸热”)过程。
②结合图像b分析溶液中离子变化的情况,请说明该反应发生的证据为:___________。
学科网(北京)股份有限公司图a 图b
18.(7分)海洋吸收是实现“碳中和”的途径之一,其原理是利用CO 在水等溶剂中的溶解性来吸收
2
CO 。某实验小组围绕CO 在水和食盐水(模拟海水)中溶解情况开展以下实验。
2 2
【任务一】配制一定溶质质量分数的食盐水
备注:20°C时,NaCl的溶解度为36.0g,水的密度为1.0g/mL
(1)配制食盐水,配制方案如下,请补充a、b数据。
序号 食盐水中NaCl的质量分数 NaCl质量(g) 水的体积(mL)
1 5% 5.0 95.0
2 10% 10.0 a
3 26.47%(饱和食盐水) b 100.0
【任务二】制备CO
2
相同条件下,用下图所示装置,分别用排水法、排食盐水法收集100mL CO 后,移出导管。保持量筒在
2
水槽中位置不变,每隔一段时间观察并记录量筒内CO 的体积。所测数据如下表。
2
时间/h
0 0.5 3 6 24
CO 体积/mL
2
1 排水法时CO 体积 100 96 79.5 59 2
2
2 排5%食盐水法时CO 体积 100 98 86.5 73.5 20.5
2
3 排10%食盐水法时CO 体积 100 98.5 90.5 x 55
2
学科网(北京)股份有限公司4 排饱和食盐水法时CO 体积 100 100 99.5 98.5 90.5
2
(2)仪器c的名称___________。
(3)实验室制取CO 的化学方程式____________________。
2
(4)根据上表分析:相同条件下,在24h时吸收CO 最多的实验是以__________(填字母)为吸收液。
2
A.水 B.5%食盐水 C.10%食盐水 D.饱和食盐水
(5)表格中x的数值可能为___________(填字母)。
A.58 B.70.5 C.82.5 D.92.5
(6)上图制取CO 的发生装置,还可用于下列物质的制备的是__________(填字母)。
2
A.加热KMnO 制O
4 2
B.用锌粒和稀硫酸制H
2
C.用二氧化锰和过氧化氢溶液制O
2
D.加热碱石灰和氯化铵混合物制NH
3
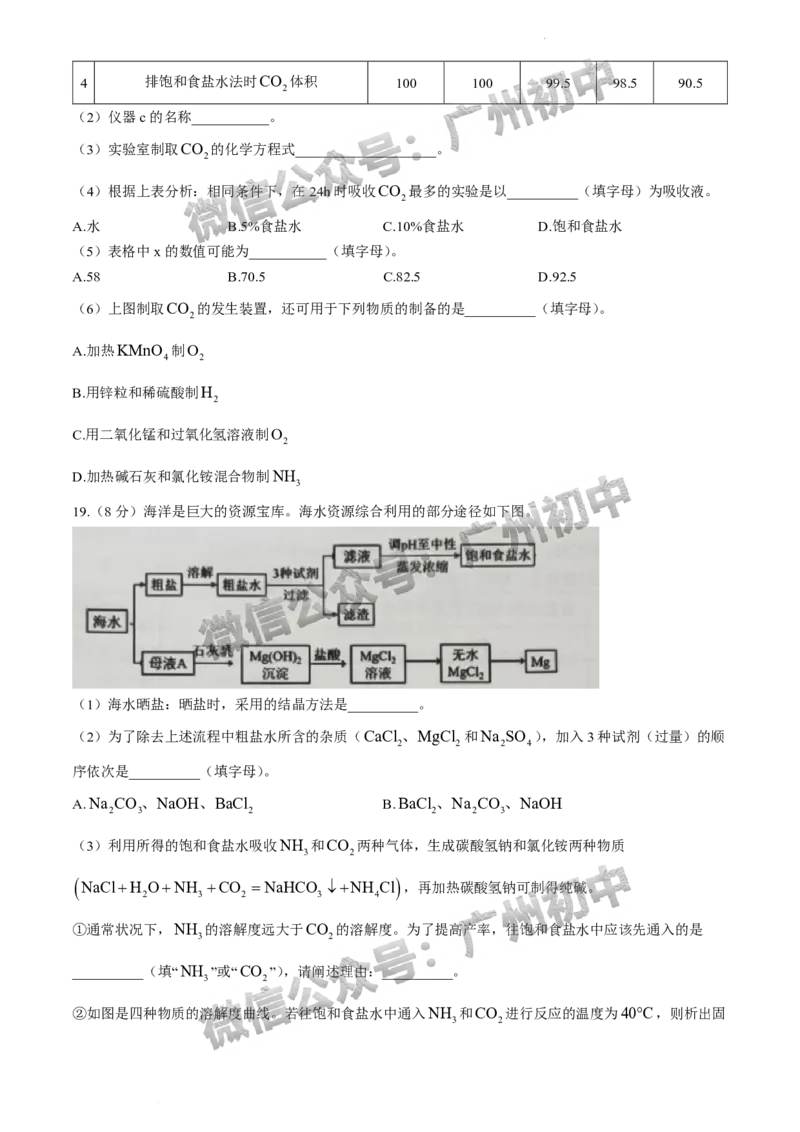
19.(8分)海洋是巨大的资源宝库。海水资源综合利用的部分途径如下图。
(1)海水晒盐:晒盐时,采用的结晶方法是__________。
(2)为了除去上述流程中粗盐水所含的杂质(CaCl 、MgCl 和Na SO ),加入3种试剂(过量)的顺
2 2 2 4
序依次是__________(填字母)。
A.Na CO、NaOH、BaCl B.BaCl 、Na CO、NaOH
2 3 2 2 2 3
(3)利用所得的饱和食盐水吸收NH 和CO 两种气体,生成碳酸氢钠和氯化铵两种物质
3 2
( )
NaCl+H O+NH +CO = NaHCO ↓+NH Cl ,再加热碳酸氢钠可制得纯碱。
2 3 2 3 4
①通常状况下,NH 的溶解度远大于CO 的溶解度。为了提高产率,往饱和食盐水中应该先通入的是
3 2
__________(填“NH ”或“CO ”),请阐述理由:__________。
3 2
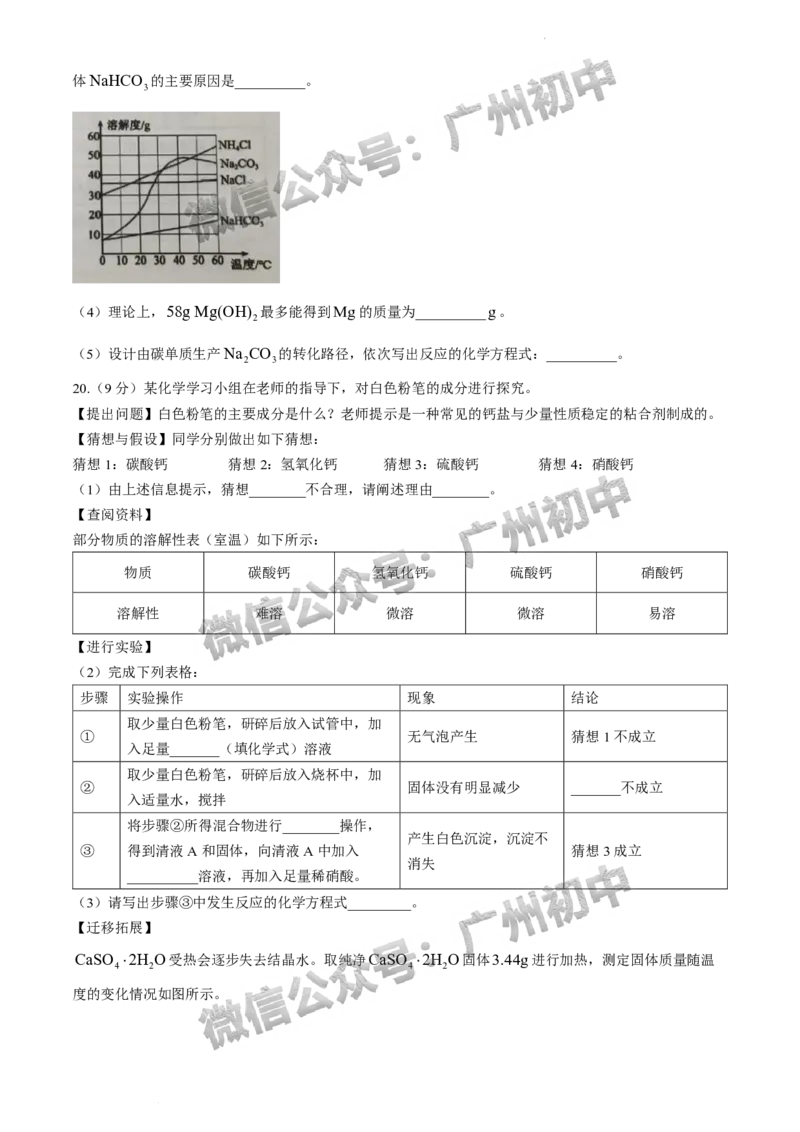
②如图是四种物质的溶解度曲线。若往饱和食盐水中通入NH 和CO 进行反应的温度为40°C,则析出固
3 2
学科网(北京)股份有限公司体NaHCO 的主要原因是__________。
3
(4)理论上,58g Mg(OH) 最多能得到Mg的质量为__________g。
2
(5)设计由碳单质生产Na CO 的转化路径,依次写出反应的化学方程式:__________。
2 3
20.(9分)某化学学习小组在老师的指导下,对白色粉笔的成分进行探究。
【提出问题】白色粉笔的主要成分是什么?老师提示是一种常见的钙盐与少量性质稳定的粘合剂制成的。
【猜想与假设】同学分别做出如下猜想:
猜想1:碳酸钙 猜想2:氢氧化钙 猜想3:硫酸钙 猜想4:硝酸钙
(1)由上述信息提示,猜想________不合理,请阐述理由________。
【查阅资料】
部分物质的溶解性表(室温)如下所示:
物质 碳酸钙 氢氧化钙 硫酸钙 硝酸钙
溶解性 难溶 微溶 微溶 易溶
【进行实验】
(2)完成下列表格:
步骤 实验操作 现象 结论
取少量白色粉笔,研碎后放入试管中,加
① 无气泡产生 猜想1不成立
入足量_______(填化学式)溶液
取少量白色粉笔,研碎后放入烧杯中,加
② 固体没有明显减少 _______不成立
入适量水,搅拌
将步骤②所得混合物进行________操作,
产生白色沉淀,沉淀不
③ 得到清液A和固体,向清液A中加入 猜想3成立
消失
__________溶液,再加入足量稀硝酸。
(3)请写出步骤③中发生反应的化学方程式_________。
【迁移拓展】
CaSO ⋅2H O受热会逐步失去结晶水。取纯净CaSO ⋅2H O固体3.44g进行加热,测定固体质量随温
4 2 4 2
度的变化情况如图所示。
学科网(北京)股份有限公司[CaSO ⋅2H O的相对分子质量为172]
4 2
(4)D点固体的化学式是________。
(5)T ~T °C温度段加热固体可产生两种常见气体,其中一种气体是形成酸雨的主要物质之一,则D~E
3 4
段发生反应的化学方程式为_________。
学科网(北京)股份有限公司