【2026年南方台江苏专用教辅电子版化学培优word讲义第9讲镁、铝、铜及其化合物

备考导航
|
复习目标 |
1. 了解镁、铝、铜单质及其重要化合物的性质、用途。 2. 掌握从海水中提镁的工艺流程及原理。 3. 了解氢氧化铝的制备方法。 4. 掌握用铝土矿制备铝的工艺流程及原理。 |
|
熟记网络 |
|
|
|
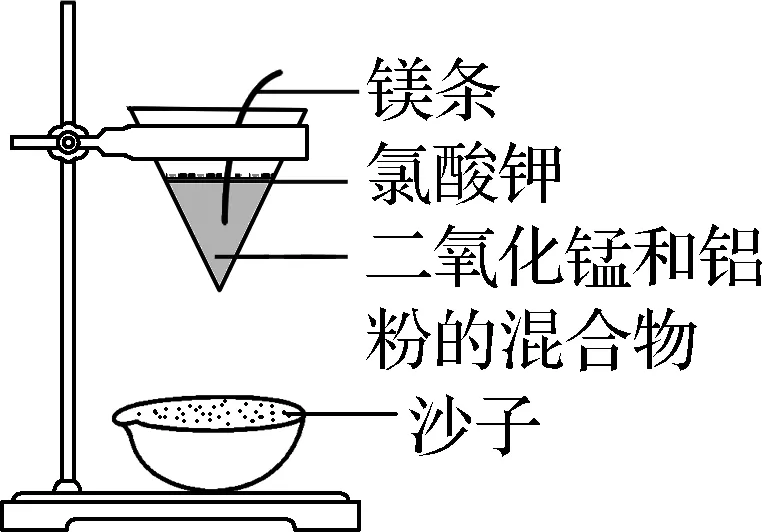
|
|
|
|
|
课前自测 |
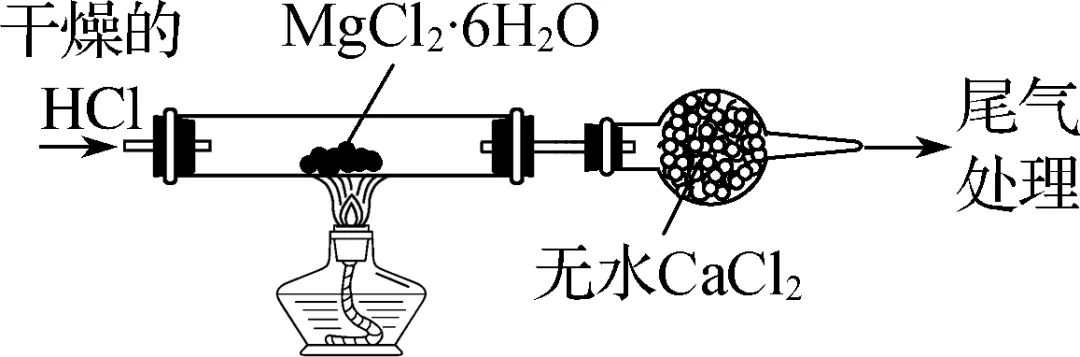
判断正误(正确的打“√”,错误的打“×”)。 (1)MgO和Al2O3都属于两性氧化物(×) (2)(2024·如东期末)Mg分别在空气和氧气中燃烧,生成相同的产物(×) (3) (2024·苏州期末)Mg有强还原性,故可用于钢铁的电化学防护(√) (4)常温下,铝遇浓硝酸或浓硫酸时会发生钝化(√) (5)向盛有少量Mg(OH)2沉淀的试管中加入适量饱和NH4Cl溶液,振荡,白色沉淀溶解(√) (6)向Al2(SO4)3溶液中逐滴加入NaOH溶液至过量,先生成白色沉淀,后沉淀消失,说明Al(OH)3具有酸性(√) (7)向Cu(OH)2固体中分别滴加盐酸和氨水;向Al(OH)3固体中分别滴加盐酸和烧碱溶液,固体均溶解,Cu(OH)2和Al(OH)3均为两性氢氧化物(×) (8)在稀硫酸中加入少量Cu2O(s),溶液由无色变为蓝色并有红色固体生成,反应中Cu2O既作氧化剂又作还原剂(√) (9)(2024·如东中学)用图1装置制取无水MgCl2(√)
图1 图2 (10)(2024·如东中学)用图2装置制取金属锰(√) (11) (2024·前黄中学二检)将Mg(HCO3)2溶液与过量的NaOH溶液混合:Mg(HCO3)2+2NaOH===MgCO3↓+Na2CO3+2H2O(×) (12) (2024·姜堰中学)可溶性铝盐净水原理:2Al3++3H2O===Al2O3+6H+(×) (13) (2023·前黄·姜堰·如东·沭阳四校联考)AlCl3(aq)――→HCl气流△无水AlCl3电解Al (×) (14) (2023·句容中学)CuSO4过量NaOHaqCu(OH)2――→葡萄糖△Cu2O(√) |

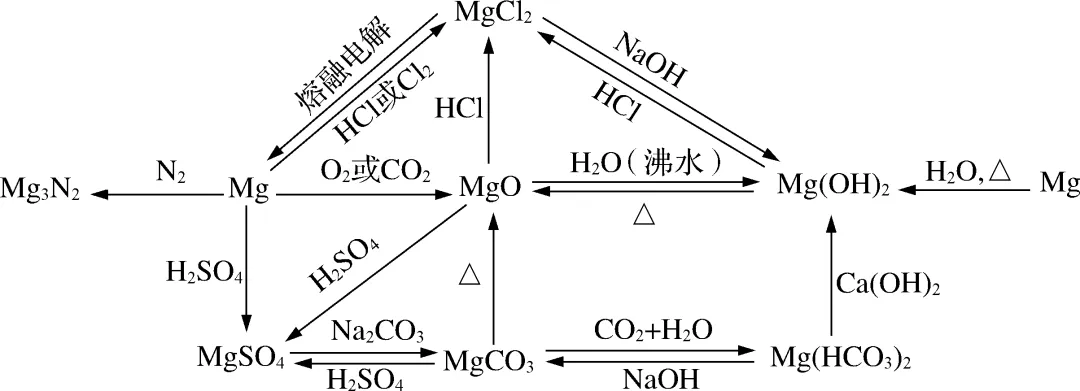
考点1 镁 海水制镁
知 识 梳 理
1. 与氧气反应(写化学方程式,下同):
2Mg+O2点燃2MgO(发出耀眼的白光,生成白色固体)。
2. 与氮气反应:3Mg+N2点燃Mg3N2
(镁在空气中燃烧得到的是MgO和Mg3N2的混合物)。
Mg3N2+6H2O===3Mg(OH)2+2NH3↑。
3. 与盐酸(或稀硫酸)反应(写离子方程式):Mg+2H+===Mg2++H2↑。
4. 与二氧化碳反应:2Mg+CO2点燃2MgO+C(镁着火不能用CO2灭火器灭火)。
5. 与盐溶液反应:Mg+2NH4Cl===MgCl2+2NH3↑+H2↑。
6. 与水反应:Mg+2H2O△Mg(OH)2+H2↑(镁与冷水反应缓慢,与沸水反应迅速)。
1. MgO(碱性氧化物)与酸反应(写离子方程式):MgO+2H+===Mg2++H2O。
2.Mg(OH)2
(1)中强碱,难溶于水,能溶于酸、NH4Cl溶液:
Mg(OH)2+2H+===Mg2++2H2O;
Mg(OH)2+2NH4Cl===MgCl2+2NH3·H2O。
(2)溶解度小于碳酸镁
MgCO3+H2O△Mg(OH)2+CO2↑
由于Mg(OH)2的溶解度比MgCO3小,故水垢的主要成分中,含镁化合物是Mg(OH)2,而非MgCO3。
(3)不稳定,受热易分解
Mg(OH)2△MgO+H2O
3. Mg2 (OH)2CO3
Mg2+与Na2CO3溶液反应生成碱式碳酸镁[Mg2 (OH)2CO3]沉淀:
2Mg2++2CO2-3+H2O===Mg2(OH)2CO3↓+ CO2↑。

常见的含镁物质的用途
|
物质 |
镁 |
镁铝合金 |
氧化镁 |
氢氧化镁 |
|
用途 |
信号弹和焰火 |
制造火箭、导弹、飞机部件 |
耐高温材料 |
阻燃剂 |
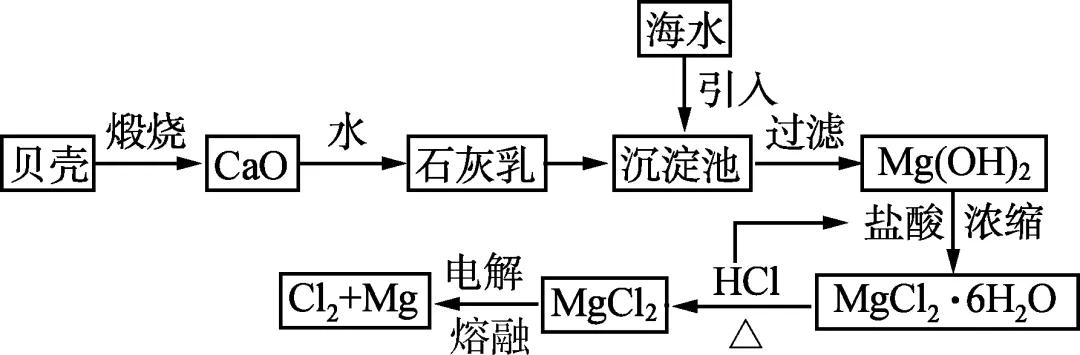
基本步骤及主要反应的化学方程式:
①制石灰乳:CaCO3高温CaO+CO2↑、
CaO+H2O===Ca(OH)2。
②沉淀:MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2。
③酸化:Mg(OH)2+2HCl===MgCl2+2H2O。
④蒸发结晶,析出MgCl2·6H2O
⑤脱水:MgCl2·6H2O△MgCl2+6H2O↑

通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风