【2026年南方台江苏专用教辅电子版化学培优word讲义高考特训18化学工艺流程(非选择题)

高考特训18 化学工艺流程(非选择题)
1. (2023·常熟检测)纳米铁在废水处理、材料研发等领域有重要应用。以某钛白粉厂副产品(主要含FeSO4,还含有TiOSO4、CoSO4、NiSO4等杂质)为原料制备纳米铁的流程如下:
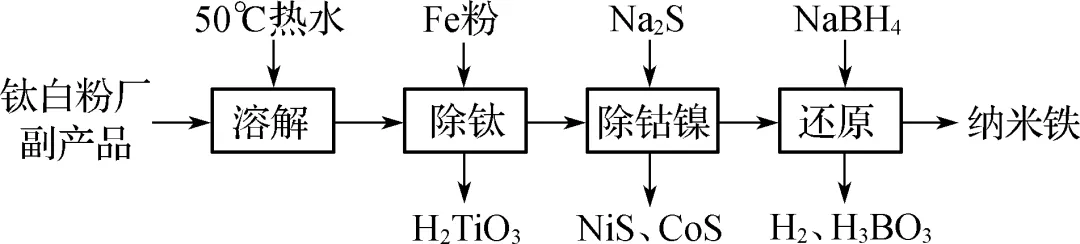
已知:Ksp\rc\)(\a\vs4\al\co1(CoS)=1.8×10-22,Ksp\rc\)(\a\vs4\al\co1(NiS)=1.0×10-21,Ksp\rc\)(\a\vs4\al\co1(FeS)=4.0×10-17,Ksp\a\vs4\al\co1(CuOH2)=2.0×10-20。当溶液中离子浓度小于1.0×10-5 mol/L时,认为该离子沉淀完全。TiOSO4在溶液中以TiO2+和SO2-4形式存在。
(1) 结合离子方程式解释“除钛”时加入铁粉的作用:TiO2+水解生成H2TiO3的反应为TiO2++2H2OH2TiO3+2H+,加入铁粉消耗H+,促进水解正向进行,使TiO2+转化为难溶的H2TiO3而除去。
(2) “除钴镍”完全后,溶液中c\rc\)(\a\vs4\al\co1(Fe2+)的最大值为0.4mol/L。
(3) “还原”时NaBH4与FeSO4以物质的量之比2∶1反应,写出该反应的化学方程式:2NaBH4+FeSO4+6H2O===7H2↑+2H3BO3+Fe↓+Na2SO4。
(4) 用纳米铁去除废水中的Cu2+。常温下,选择Cu2+初始浓度为2×10-4 mol/L的废水,控制纳米铁用量相同,测得Cu2+去除率随初始pH的变化如图所示。写出初始pH在3~6内Cu2+去除率随初始pH增大缓慢上升,而初始pH在6~7内Cu2+去除率随初始pH增大快速上升的原因:初始pH在3~6范围内,pH上升,c\rc\)(\a\vs4\al\co1(H+)减小,与H+反应的铁减少,更多的铁与Cu2+反应,Cu2+去除率缓升;初始pH在6~7范围内,除了铁与Cu2+反应外,pH上升,c\rc\)(\a\vs4\al\co1(OH-)增大,Cu2+沉淀生成Cu(OH)2,Cu2+去除率迅速上升
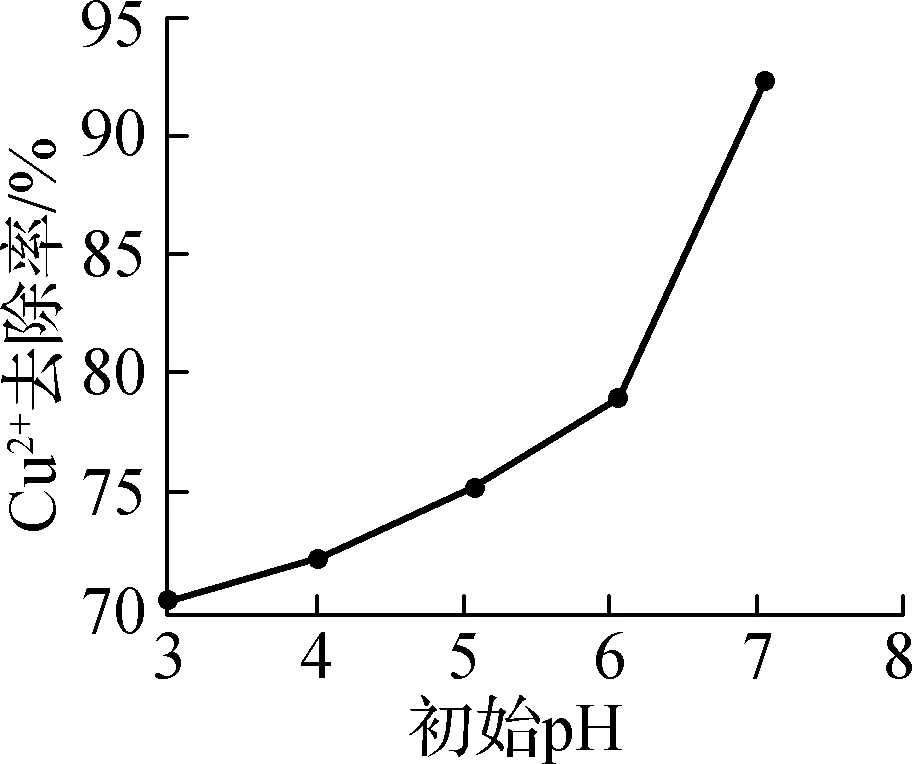
【解析】 (2) 当溶液中离子浓度小于1.0×10-5mol/L时,认为该离子沉淀完全,由Ksp\rc\)(\a\vs4\al\co1(CoS)=1.8×10-22、Ksp\rc\)(\a\vs4\al\co1(NiS)=1.0×10-21可知CoS更难溶,故当Ni2+沉淀完全时Co2+也已完全沉淀,Ni2+沉淀完全时溶液中c\rc\)(\a\vs4\al\co1(S2-)=\rc\)(\a\vs4\al\co1(NiS))c\b\lc\(\rc\)(\a\vs4\al\co1(Ni2+))=1.0×10-211.0×10-5mol/L=1.0×10-16mol/L,溶液中Fe2+浓度最大值为c(Fe2+)=KspFeScS2-=4.0×10-171.0×10-16mol/L=0.4 mol/L。(3) 2 mol NaBH4还原1 mol FeSO4时,NaBH4中氢由-1价升至H2中的0价,失去8 mol电子,1 mol FeSO4转化为纳米铁得2 mol电子,故有H2O参加反应且+1价的氢得6 mol电子生成H2,共生成7 mol H2,反应的化学方程式为2NaBH4+FeSO4+6H2O===7H2↑+2H3BO3+Fe↓+Na2SO4。(4) c\rc\)(\a\vs4\al\co1(H+)较大时,H+与铁粉反应消耗铁,初始pH在3~6范围内,随pH上升,c\rc\)(\a\vs4\al\co1(H+)减小,与H+反应的铁减少,更多的铁与Cu2+反应,Cu2+去除率缓升;Cu2+初始浓度为2×10-4 mol/L,开始沉淀的c(OH-)=2×10-202×10-4)mol/L=10-8 mol/L,pH=6,故pH>6时Cu2+开始沉淀,Cu2+去除率迅速上升。
2. (2024·丹阳中学)钕铁硼磁铁因其超强的磁性被誉为“永磁之王”。一种从钕铁硼废料[含钕(Nd,质量分数为28.8%)、Fe、B]中提取氧化钕的工艺流程如下:
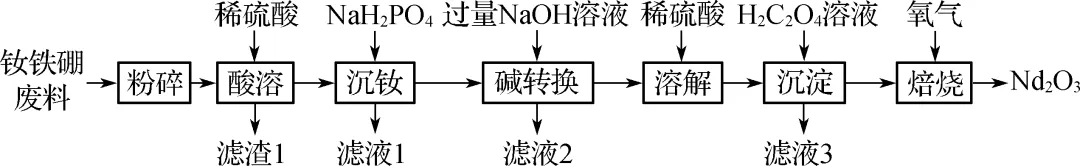
已知:Nd稳定的化合价为+3;金属钕的活动性较强,能与酸发生置换反应;Nd(H2PO4)3难溶于水;硼不与稀硫酸反应,但可溶于氧化性酸。
(1) “酸溶”时,不可将稀硫酸换为浓硫酸的原因是浓硫酸会与硼反应从而引入了杂质离子,同时还会生成SO2等污染气体。
(2) 在常温下“沉钕”,当Nd(H2PO4)3完全沉淀时pH为2.3,溶液中c(Fe2+)=2 mol/L。
①写出“沉钕”的化学方程式:6NaH2PO4+Nd2(SO4)3===2Nd(H2PO4)3↓+3Na2SO4。
②“沉钕”完全时,无(填“有”或“无”)Fe(OH)2沉淀生成{常温下,Ksp[Fe(OH)2]=8.0×10-16}。
③“酸溶”后需调节溶液的pH=1,若酸性太强,“沉钕”不完全,试分析其原因:若酸性太强,H+与H2PO-4反应生成H3PO4,导致H2PO-4浓度太小,沉淀不完全。
(3) “焙烧”沉淀Nd2(C2O4)3·10H2O时生成无毒气体,该反应的化学方程式为2[Nd2(C2O4)3·10H2O]+3O2焙烧2Nd2O3+ 12CO2+20H2O。
(4) 热重法是测量物质的质量与温度关系的方法。草酸钕晶体[Nd2(C2O4)3·10H2O,式量为732]的热重曲线如图所示,加热到450℃时,只剩余一种盐,该盐的化学式为Nd2O2CO3(计算过程见解析)。
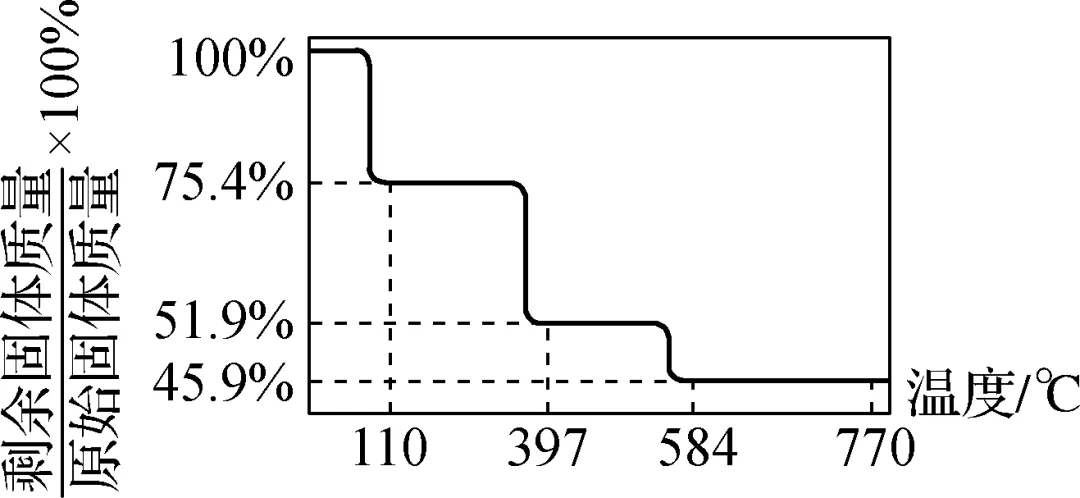
【解析】 (1) 根据题给信息可知,硼不与稀酸反应但是可溶于氧化性酸,若加入浓硫酸,浓硫酸会与硼反应,引入了杂质离子,同时还会生成SO2,污染空气。(2) ②Q=c(Fe2+)·c2(OH-)=2.0×\a\vs4\al\co1(\f(10-1410-2.3))2=2×10-23.4<8.0×10-16=Ksp[Fe(OH)2],则无Fe(OH)2沉淀生成 (4) 由题给信息,Mr[Nd2(C2O4)3·10H2O]=732,其中结晶水的相对分子质量为180,固体残留率:732-180732×100%≈75.4%,此时残留固体为Nd2(C2O4)3;固体残留率由75.4%→51.9%时,相对分子质量减少172,设Nd2(C2O4)3分解减少x个C(x<6)和y个O(x、y为正整数),则12x+16y=172,解得x=1y=10)(舍去)、x=5y=7),该盐的化学式为Nd2O2CO3。
3. (2023·扬州中学)以粉煤灰浸取液(含Al3+、Li+、Mg2+、Cl-等)为原料制备电极材料LiFePO4的实验流程如图:
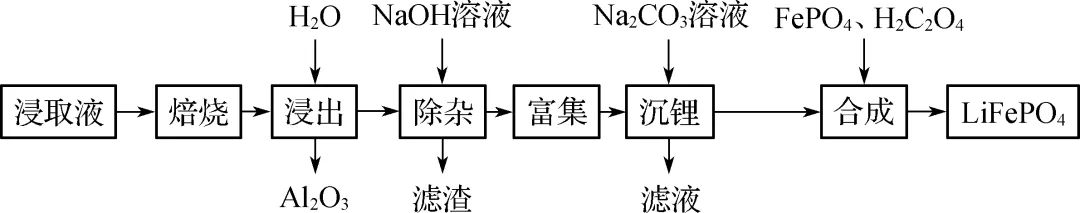
(1) “焙烧”过程中AlCl3最终转化为Al2O3和HCl(填化学式)。
(2) “浸出”后的滤液中主要含Li+、Mg2+、Cl-等。已知Ksp[Mg(OH)2]=5.5×10-12,欲使c(Mg2+)≤5.5×10-6mol/L,“除杂”需要调节溶液的pH不低于11。
(3) 离子筛法“富集”锂的原理如图1所示。在碱性条件下,离子筛吸附Li+容量较大,其可能原因为在碱性条件下,OH-与离子筛中H+反应,使离子筛留出更多“空位”,能吸附更多Li+。
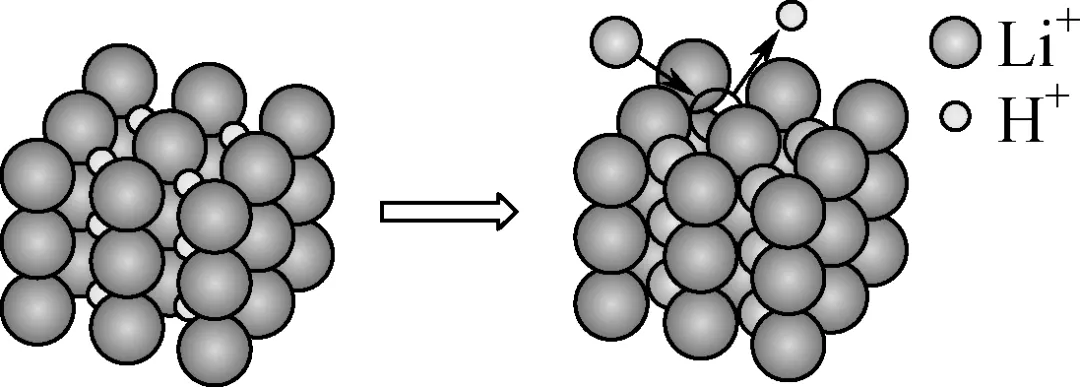
图1 图2
(4) 已知Li2CO3的溶解度曲线如图2所示。“沉锂”反应1h,测得Li+沉淀率随温度升高而增加,其原因有随温度升高,“沉锂”反应速率加快,相同时间内Li2CO3沉淀量增大;随温度升高,Li2CO3溶解度减小,Li2CO3沉淀量增大。
(5) “合成”在高温下进行,其化学方程式为Li2CO3+H2C2O4+2FePO4高温2LiFePO4+H2O+3CO2↑。
【解析】 (1) “焙烧”浸取液过程中,AlCl3水解最终转化为Al2O3和HCl。(2) Ksp[Mg(OH)2]=c(Mg2+)·c2(OH-)=5.5×10-12,欲使c(Mg2+)≤5.5×10-6 mol/L,则此时溶液中c(OH-)≥Ksp[MgOH2]cMg2+)=5.5×10-125.5×10-6) mol/L=1×10-3 mol/L,c(H+)=KwcOH-=10-141×10-3 mol/L=1×10-11 mol/L,故需要调节溶液的pH不低于11。(3) 离子筛中含有H+和Li+,碱性条件下,OH-与离子筛中H+反应,使离子筛留出更多“空位”,能吸附更多Li+。(4) 温度越高,Li2CO3溶解度越小,越易产生沉淀;“沉锂”发生反应:2Li++CO2-3===Li2CO3↓,温度越高,反应速率越大,相同时间内产生Li2CO3的量越大,故“沉锂”反应1 h,测得Li+沉淀率随温度升高而增加。
4. (2024·如东中学)某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+),实现镍、钴、镁元素的回收。
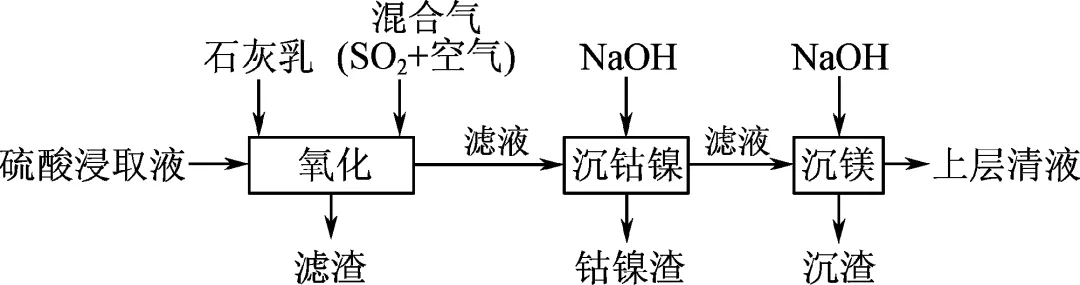
(1) 在一定温度下,用硫酸浸取已粉碎的镍钴矿时,提高浸取速率的方法为适当增大硫酸浓度(答案合理即可)(答出一条即可)。
(2) “氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5),写出H2SO5
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风




