【2026年南方台江苏专用教辅电子版化学培优word讲义第3讲离子反应

备考导航
|
复习目标 |
1. 了解电解质及其分类,掌握强电解质、弱电解质的本质区别。 2. 理解电解质在水溶液中的电离以及电解质溶液的导电性。 3. 了解离子反应的概念,了解离子反应发生的条件,能正确书写离子方程式。 4. 掌握离子共存的条件,会判断溶液中离子能否大量共存。 5. 掌握常见离子的检验,能根据实验现象推断溶液中所含离子的种类。 |
|
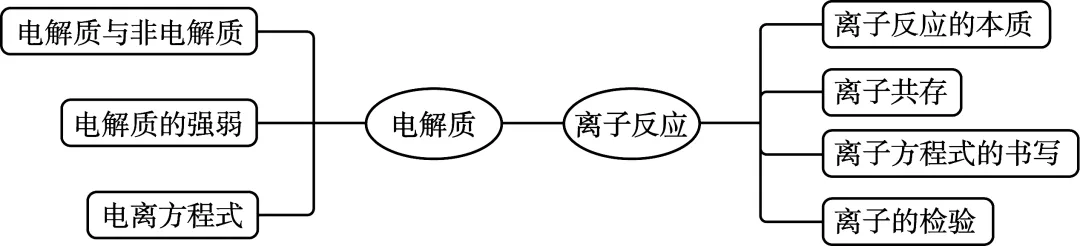
熟记网络 |
|
|
课前自测 |
判断正误(正确的打“√”,错误的打“×”)。 (1) (2017·江苏卷)无色透明的溶液中:Fe3+、Mg2+、SCN-、Cl-能大量共存(×) (2) (2018·江苏卷)0.1 mol/L HCl 溶液中:Ba2+、K+、CH3COO-、NO-3能大量共存(×) (3) (2019·江苏卷)0.1 mol/L FeCl2溶液中:K+、Mg2+、SO2-4、MnO-4能大量共存(×) (4) (2022·辽宁卷)H2S电离:H2S2H+ + S2-(×) (5) (2023·海门调研)H2O2氧化酸性废水中的Fe2+:2Fe2++H2O2===2Fe3++2OH-(×) (6) (2024·徐州模拟)向某溶液X中滴加少量稀盐酸,再滴加几滴Ba(NO3)2溶液,出现白色沉淀,该溶液中含有SO2-4(×) (7) (2024·徐州模拟)K+的检验:用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,观察火焰颜色变化(×) (8) (2023·常熟)检验溶液X中含有CO2-3或HCO-3:向溶液X中加入稀硫酸,并将产生的无色气体通入澄清石灰水中,观察是否有沉淀生成(×) (9) (2023·海门调研)检验溶液中是否存在NH+4:向某溶液中加入氢氧化钠溶液并加热,观察产生的气体能否使蓝色石蕊试纸变色(×) (10) 取少量某溶液于试管中,加稀盐酸酸化,再加入FeCl2溶液,若溶液变黄色且试管上部产生红棕色气体,则该溶液中含有NO-2(×) |

考点1 电解质与电离方程式
知 识 梳 理
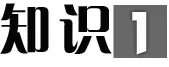
1. 强电解质:完全电离,用“===”连接。
如:H2SO4===2H++SO2-4
2. 弱电解质:部分电离,用“”表示。
如:NH3·H2O NH+4+OH-
3. 多元弱酸:分步电离,以第一步电离为主。
如:H2SO3H++HSO-3、
HSO-3H++SO2-3
4. 多元弱碱:分步电离,但一步书写。
如:Cu(OH)2Cu2++2OH-
5. 酸式盐的书写方法
(1) 弱酸的酸式盐在溶液中完全电离,生成酸式酸根离子和阳离子。
如:NaHC2O4===Na++HC2O-4、
HC2O-4H++C2O2-4
(2) 强酸的酸式盐在水溶液中完全电离。
如:NaHSO4===Na++H++SO2-4
典 题 悟 法
 BD(填字母)。
BD(填字母)。
A. NaHCO3在水溶液中的电离:NaHCO3===Na++H++CO2-3
B. 硼酸在水中的电离方程式:H3BO3+H2O[B(OH)4]-+H+
C. 草酸的电离方程式:H2C2O4C2O2-4+2H+
D. 液氨电离可表示为2NH3NH+4+NH-2
【解析】 HCO-3不能拆开,A错误;H2C2O4是弱酸,分步电离,C错误。
考点2 离子方程式的书写
知 识 梳 理
 “拆分”
“拆分”
1. 单质、气体、氧化物、弱电解质(弱酸、弱碱、水等)、络合物{如Fe(SCN)3、[Ag(NH3)2]+}、弱酸的酸式根离子、难溶盐不能拆分成离子。
2. 强酸(如HCl、H2SO4、HNO3、HBr、HI、HClO4等)、强碱[如KOH、NaOH、Ca(OH)2、Ba(OH)2等]、绝大多数可溶性的盐拆分成离子。
(1) 钾盐、钠盐、铵盐、硝酸盐、磷酸二氢盐等都易溶于水。
(2) 氯化物中,AgCl难溶于水。硫酸盐中,PbSO4、BaSO4难溶于水,CaSO4、Ag2SO4微溶于水。
(3) 碳酸盐、亚硫酸盐、磷酸盐和硅酸盐,除钾盐、钠盐、铵盐外都难溶于水,如BaCO3、BaSO3、Ca3(PO4)2等难溶于水。
(4) 硫化物中,除K2S、Na2S、(NH4)2S、BaS外均难溶于水。
(5) 银盐中,AgCl、AgBr、AgI、Ag2S、Ag3PO4、Ag2CO3等都难溶。
3. 微溶物[如Ca(OH)2、CaSO4、MgCO3、Ag2SO4]的处理
(1) 生成物中有微溶物时,微溶物不拆。
(2) 反应物中微溶物处于溶液状态(稀溶液),拆成离子,如澄清石灰水中的“Ca(OH)2”拆成“Ca2++2OH-”。
(3) 反应物中微溶物处于固态或悬浊液状态时,仍写化学式。如石灰乳中的“Ca(OH)2”不拆分。
1. 检查离子反应是否符合反应原理。
2. 检查化学式拆分是否正确。
3. 多重反应,检查是否漏写离子反应。
4. 检查物质的量的关系是否正确(少量与过量)。
5. 检查离子方程式左右两边是否符合原子守恒、电荷守恒、得失电子守恒。
6. 检查各项物质的化学计量数是否为最简整数比。
7. 检查反应是否完全进行(“===”“”),反应条件、气体和沉淀符号是否遗漏等。
典 题 悟 法

 Ⅷ族元素,物理性质和化学性质比较相似。一般情况下,在化合物中常见的价态为+2和+3,Co(Ⅲ)和Ni(Ⅲ)有强氧化性,酸性条件下能将Cl-氧化成Cl2。向Ni(Ⅱ)盐的溶液中加入过量的氨水,可以生成稳定的蓝色配离子[Ni(NH3)6]2+。下列指定反应的离子方程式正确的是(B)
Ⅷ族元素,物理性质和化学性质比较相似。一般情况下,在化合物中常见的价态为+2和+3,Co(Ⅲ)和Ni(Ⅲ)有强氧化性,酸性条件下能将Cl-氧化成Cl2。向Ni(Ⅱ)盐的溶液中加入过量的氨水,可以生成稳定的蓝色配离子[Ni(NH3)6]2+。下列指定反应的离子方程式正确的是(B)
A. Co2O3溶于浓盐酸:Co2O3+6H+===2Co3++3H2O
B. 将Ni(OH)2溶于氨水:Ni(OH)2+6NH3·H2O===[Ni(NH3)6]2++2OH-+6H2O
C. 向FeCl3溶液中滴加少量NaHCO3溶液:2Fe3++3CO2-3===Fe2(CO3)3↓
D. NaClO在浓碱溶液中将Fe(OH)3氧化成FeO2-4:2Fe(OH)3+3ClO-===2FeO2-4+3Cl-+H2O+4H+
【解析】 Co(Ⅲ)有强氧化性,酸性条件下能将Cl-氧化成Cl2,Co2O3溶于浓盐酸反应生成氯气和Co2+:Co2O3+6H++2Cl-===2Co2++3H2O+Cl2↑ ,A错误;Ni(OH)2溶于氨水得到[Ni(NH3)6]2+,B正确;向FeCl3溶液中滴加少量NaHCO3溶液,Fe3+和HCO-3发生双水解反应生成Fe(OH)3沉淀和CO2:Fe3++
通过网盘分享的文件:南方凤凰台·2026全国一轮电子稿等7个文件
链接: https://pan.baidu.com/s/1Q8yIZ6J_EF4Bq61Fj8yz8w?pwd=4321 提取码: 4321
–来自百度网盘超级会员v8的分享
 夜雨聆风
夜雨聆风