AI赋能破耐药困局:苯基乙酸苯胺衍生物2g精准阻断铜绿假单胞菌QS系统!
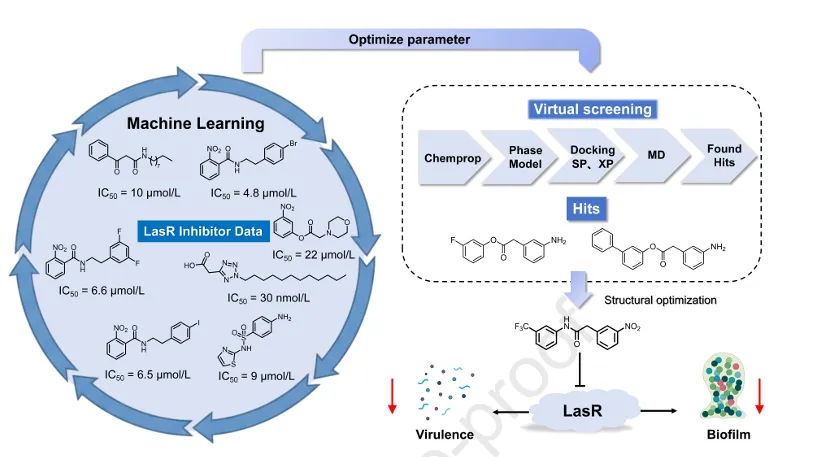
面对铜绿假单胞菌(P. aeruginosa)等超级细菌构筑的坚固生物膜“堡垒”,传统抗生素往往束手无策。由于群体感应(QS)系统——尤其是核心调控蛋白LasR——主导着生物膜的形成与毒力表达,靶向QS成为了极具前景的“反毒力”策略。近期,广东工业大学生物医药学院郑俊霞教授团队、暨南大学药学院刘君教授和徐俊教授团队在药学顶刊 Acta Pharmaceutica Sinica B上发表重磅成果:他们通过一套精密的机器学习(ML)筛选管线,成功挖掘出一款极具临床转化潜力的先导化合物——苯基乙酸苯胺衍生物2g。
一、 冲出“维度灾难”:ML多模型联用与SAR优化精准锁定先导分子
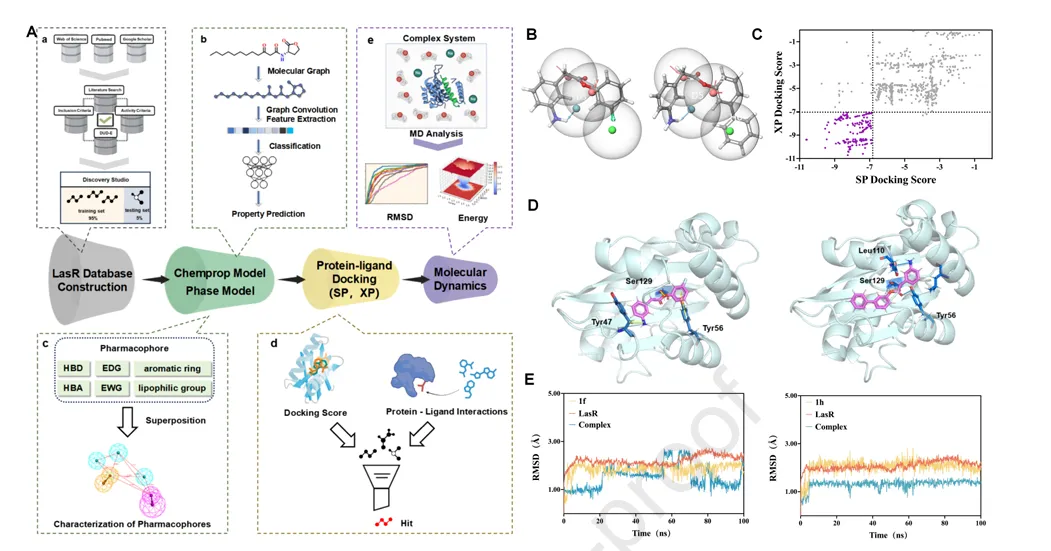
在浩瀚的化学空间中寻找具备高LasR抑制活性的分子,无异于大海捞针。研究团队没有盲目试错,而是构建了一套所向披靡的“AI筛选漏斗”:他们整合图神经网络(GNN)、药效团模型、分子对接及100纳秒的分子动力学模拟,对内部化合物库进行了层层过滤。从初始的4万余个分子中,AI精准捕获了两个高分 hits。
以此为核心模板,团队展开了系统的结构-活性关系(SAR)优化。他们敏锐地发现,苯环上吸电子基团(特别是三氟甲基 -CF3)的引入能极大提升生物膜抑制活性。历经多轮合成与生物学评价,活性飙升的明星分子化合物2g脱颖而出。晶体紫染色实验证实,2g抑制生物膜的IC50高达 0.14±0.08 μmol/L,效力远超阳性对照阿奇霉素,且它本身不具备任何杀菌活性(MIC >256 μmol/L),巧妙规避了传统抗生素带来的选择性压力。
二、 直击“细菌中枢”:靶向降解LasR蛋白并重编程毒力网络
2g的神奇之处在于它扮演了“特洛伊木马”的角色。深入的机制探究揭示,2g能直接与LasR蛋白发生高亲和力结合(KD = 38.97 μmol/L),并促进LasR的降解。这一釜底抽薪的打击,直接瘫痪了细菌的QS通讯网络。
转录组学(RNA-seq)数据进一步佐证,2g能选择性地沉默LasR调控的毒力基因通路。在它的干预下,铜绿假单胞菌的“武器库”被迫关闭:标志性毒力因子绿脓菌素(pyocyanin)的合成大幅锐减,细菌的运动性(motility)也受到显著压制。这意味着,2g虽然不直接杀死细菌,却成功将致命的致病菌“驯化”为高敏感状态,使其丧失免疫逃逸与定植能力,为后续抗生素的介入扫清了障碍。
三、 跨越“耐药鸿沟”:体内外千倍协同重振经典抗生素雄风
一项理想的抗感染辅助疗法,必须在动物模型中经得起实战检验。研究团队在小鼠皮肤伤口感染模型中给出了令人窒息的答卷:当2g与传统抗生素联用时,产生了极其强大的协同增效作用!具体而言,它竟能将环丙沙星(Cip)和妥布霉素(Tob)的有效剂量分别惊人地降低1000倍和500倍。
更令人振奋的是,在长期 evolutionary 压力下,2g处理组极少诱发耐药突变。配合其优秀的口服生物利用度(26.8%)和极宽的安全窗口(100 μmol/L下无细胞毒性或溶血现象),这些特质共同铸就了2g作为新一代抗感染佐剂的巨大临床转化价值。
综上所述,这项研究完美诠释了“AI筛选+经典药物化学”的双剑合璧。化合物2g的发现不仅是对抗铜绿假单胞菌的一记重拳,更为解决全球抗生素耐药性危机提供了可迁移的崭新范式。未来,随着这类“反毒力”策略的成熟,人类有望在与超级细菌的博弈中,重新夺回失去的主动权。
原文链接:https://doi.org/10.1016/j.apsb.2026.03.048