好题推荐 | 中考化学压轴真题|中考培优
【原题呈现】
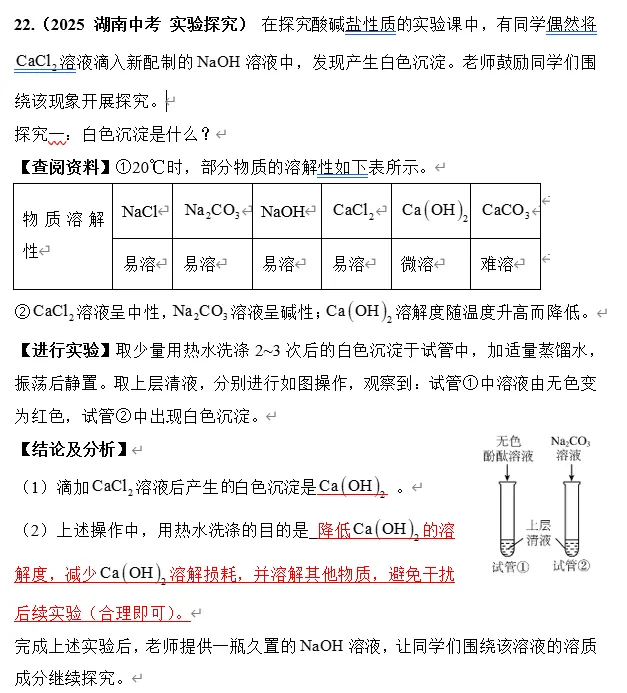
2025年湖南中考真题


【参考答案】

【考点定位】
(1)酸碱盐的化学性质:NaOH、Na₂CO₃、Ca (OH)₂、CaCO₃的性质
(2)物质溶解性与溶解度特性:Ca (OH)₂溶解度随温度升高而减小
(3)离子检验:CO₃²⁻检验:CaCl₂/BaCl₂ 产生白色沉淀; OH⁻检验:酚酞变红。
(4)久置 NaOH 变质问题:与 CO₂反应生成 Na₂CO₃
(5)实验方案评价与改进:除杂、排除干扰、控制变量。
【命题意图】
(1)以异常实验现象创设情境,考查发现问题—猜想—实验—结论的科学探究思路。
(2)考查严谨实验思维:除尽干扰离子、排除溶液本身碱性的影响。
(3)强化证据推理:用现象支撑结论,不主观臆断。
(4)落实核心素养:科学态度、实证意识、实验评价与优化能力。
【答案解析】
(1)滴加溶液后产生白色沉淀是______。题目特意强调为新制NaOH溶液,目的想说明此时溶液中溶质仅为NaOH,暂不考虑Na₂CO₃,所以先排除Na₂CO₃与CaCl₂反应产生CaCO₃沉淀,再根据查阅资料Ca(OH)₂微溶于水,说明题目在引导学生考虑CaCl₂与NaOH反应,运用复分解反应相互交换成分反应的特征,CaCl₂与NaOH反应生成Ca(OH)₂与NaCl,再根据Ca(OH)₂微溶于水,且其溶解度随温度升高而降低。用热水洗涤沉淀后,上层清液能使酚酞变红(显碱性),说明沉淀中含Ca(OH)₂。答案:Ca(OH)₂(或氢氧化钙)。
(2) 用热水洗涤的目的是______。Ca(OH)₂的溶解度随温度升高而降低,用热水洗涤可减少沉淀中Ca(OH)₂的溶解,同时洗去表面附着的NaCl等可溶性杂质,避免对后续实验产生干扰。所以答案是:除去沉淀表面附着的可溶性杂质,同时减少Ca(OH)₂的溶解。
(3)步骤①中加入CaCl₂溶液过量的目的是______。久置NaOH溶液可能含Na₂CO₃,Na₂CO₃与CaCl₂反应生成CaCO₃沉淀。加入过量CaCl₂可将溶液中所有的Na₂CO₃完全反应除去,防止其对后续NaOH的检验(酚酞变红)产生干扰。答案:将溶液中的Na₂CO₃完全除去,避免对NaOH的检验造成干扰
(5)优化实验方案。首先要看清题意,优化思路的目的是证明猜想Ⅱ,根据第(4)小题的分析,产生的白色沉淀可能为CaCO₃和Ca(OH)₂,不能根据产生白色沉淀证明Na₂CO₃的存在,从而锁定目标是如何证明Na₂CO₃的存在,要证明有Na₂CO₃,就需要证明有CaCO₃沉淀产生,所以答案是:取久置的溶液,加入足量CaCl₂溶液后,产生白色沉淀,过滤,向白色沉淀中加入足量稀盐酸,若观察到有气泡冒出,说明原溶液中有Na₂CO₃(合理即可),再根据加入酚酞变红,证明猜想Ⅱ成立。
【易错警示】
(1)没有理解题意,按照常规思路答题,认为白色沉淀就是CaCO₃;
(2)热水洗涤目的答错,基础知识不熟练,此题对可溶性物质与难溶性物质分类的实验操作的理解要求较高,不容易想到答案;
(3)不会对实验方法不严谨的分析,不能根据题意结合题中提出的异常现象答题,获取信息,分析信息,运用信息能力不足,采用常规思路此题难以答出;
(4)方案改进解答问题,不能充分理解题意,分析出题意图,导致答题方向错误。根据题意写出操作、现象与结论,许多学生会出现表述不规范的问题。
【方法小结】
本题为是对NaOH变质问题的探究,但是不属常规探究,而是针对异常现象的探究,对于酸碱盐“异常现象”探究学习方法小结如下:
(1)审题为先,破除定势。不被惯性思路带偏,精准抓取题眼与题目提供的查阅资料信息,不默认“正常反应”,从源头避免判断失误。
(2)基础扎实,精准对标。夯实酸碱盐核心反应与常见离子检验基础知识。先定“标准理论”,再核“实际现象”,通过精准对比锁定异常突破口。
(3)思维突破,多维归因。跳出单一反应框架,不忽视隐形变量。全面排查药品纯度、用量顺序、离子干扰、环境影响,构建严密分析网络。
(4)证据推理,以证立论。拒绝主观感觉,以事实为依据。遵循“现象→猜想→验证→结论”逻辑链,用严谨实验证据说话,有理有据、由表及里,完成深度探究。
核心口诀:常规看“应然”,异常看“实然”;
解题靠套路,探究凭证据。

 如有疑问可以在评论区留言,我们将耐心解答,觉得有用别忘了点赞+推荐,分享给身边需要的同学,一起坚持刷题、稳步提分!
如有疑问可以在评论区留言,我们将耐心解答,觉得有用别忘了点赞+推荐,分享给身边需要的同学,一起坚持刷题、稳步提分! 夜雨聆风
夜雨聆风