文档内容
让更多的孩子得到更好的教育
中考总复习:常见的酸和碱及其通性(提高)
撰稿:熊亚军 审稿:李伟
【考纲要求】
1.掌握常见的酸及酸的通性,知道浓盐酸、浓硫酸的特性以及浓硫酸的稀释方法。
2.掌握常见的碱及碱的通性,重点掌握氢氧化钠和氢氧化钙的性质。
3.会用酸碱指示剂检验溶液的酸碱性。
【知识网络】
浓盐酸:是无色有刺激性气味的液体,有挥发性和腐蚀性
物理性质 浓硫酸:是无色粘稠油状液体,有吸水性,易溶于水,溶解时放出大量热,
有强烈的腐蚀性
①紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色
②与活泼 Zn+HSO=ZnSO+H↑
2 4 4 2
金属反应 Fe+2HCl=FeCl+H↑
2 2
化学性质 ③与金属 FeO+6HCl=2FeCl+3HO
2 3 3 2
氧化物反应 CuO+HSO=CuSO+HO
2 4 4 2
常见的酸 ④与碱 NaOH+HCl=NaCl+HO
2
反应 Ca(OH)+HSO=CaSO+2HO
2 2 4 4 2
⑤与某些 HCl+AgNO=AgCl↓+HNO
3 3
盐反应 HSO+BaCl=BaSO↓+2HCl
2 4 2 4
浓硫酸特性:吸水性、脱水性、强氧化性
浓硫酸稀释方法:一定要把浓硫酸沿着器壁慢慢地注入水里,并不断地用玻璃棒搅拌
用 盐酸:除锈,制造其他化工产品,胃液中的主要成分,帮助消化
途 硫酸:干燥剂,广泛用于生产化肥、农药、火药、染料及金属除锈
氢氧化钠:俗名火碱、烧碱、苛性钠,易潮解,易溶于水且放热,有强腐蚀性
物理性质 氢氧化钙:俗名熟石灰、消石灰,微溶于水
① 紫色石蕊试液遇碱溶液变蓝色,无色酚酞试液遇碱溶液变红色
②与非金属 2NaOH+SO=NaSO+HO
2 2 3 2
氧化物反应 Ca(OH)+CO=CaCO↓+HO
2 2 3 2
常见的碱 化学性质 ③与酸 NaOH+HCl=NaCl+HO
2
反应 Ca(OH)+HSO=CaSO+2HO
2 2 4 4 2
④与某些 3NaOH+FeCl=Fe(OH)↓+3NaCl
3 3
盐反应 2NaOH+CuSO=Cu(OH)↓+NaSO
4 2 2 4
用 氢氧化钠:干燥剂,广泛用于制肥皂、石油、造纸、纺织和印染等
途 氢氧化钙:建筑业、农业上改良酸性土壤等
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共8页让更多的孩子得到更好的教育
【考点梳理】
考点一、酸碱指示剂和溶液的酸碱性
常用的酸碱指示剂:
溶液 酸性溶液(例:盐酸) 中性溶液(例:食盐 碱性溶液(例:氢氧化
指示剂 水) 钠溶液)
紫色石蕊试液 变红色 不变色 变蓝色
无色酚酞试液 不变色 不变色 变红色
【要点诠释】
1.酸碱指示剂与酸或碱的溶液作用时,变色的是指示剂,而不是酸或碱。指示剂与酸或碱的作用是化学变
化。
2.碱只有溶于水后才能使指示剂变色,固态碱或不溶于水的碱不能使指示剂变色,因为使指示剂变色的
是能自由运动的OH-。
考点二、几种常见的酸和碱
1.盐酸、硫酸的物理性质及用途:
盐酸(HCl) 硫酸(HSO)
2 4
颜色、状 无色液体,有刺激性气味。常用浓盐酸中HCl无色粘稠的油状液体。实验室常用浓
物
态、气味、的质量分数为36%~37%,密度为1.19g/cm3 硫酸的溶质质量分数为98%,密度为
理
密度 1.84g/cm3
性
打开瓶盖 浓盐酸在打开瓶盖后瓶口上方会出现白雾 无明显现象
质
后的现象
盐酸是一种重要的化工产品。用于金属表面除硫酸是一种重要的化工原料。用于生
锈、制造药物(如盐酸麻黄素、氯化锌)等;人产化肥、农药、火药、染料、冶炼金属、
用途
体胃液中也含有少量的盐酸,可以帮助消化 精炼石油和金属除锈等;利用浓硫酸
的吸水性,实验室中常用它做干燥剂
2.浓盐酸的特性:挥发性。打开盛装浓盐酸的试剂瓶盖,会在瓶口出现白雾,这是浓盐酸中挥发出的氯化
氢气体与空气中的水蒸气结合形成盐酸小液滴产生的现象,并不是白烟。
3.浓硫酸的特性:吸水性、脱水性和腐蚀性。吸水性是浓硫酸的物理性质,脱水性是浓硫酸的化学性质。脱
水性是浓硫酸将由C,H,O等元素组成的化合物(一般是有机物)里的H,O元素的原子数以2∶1的比例从
化合物中夺取出来,使化合物脱水而发生碳化现象。
4.氢氧化钠和氢氧化钙的物理性质、用途及制备原理:(高清课堂《酸、碱和盐的复习(一)》四)
氢氧化钠(NaOH) 氢氧化钙(Ca(OH))
2
俗称 火碱、烧碱、苛性钠 熟石灰、消石灰
白色固体,易溶于水,易潮解,溶解时放出大量
物理性质 白色固体,微溶于水
的热。NaOH固体有吸水性
重要的化工原料,应用于肥皂、石油、造纸、纺织用于建筑业,制烧碱、漂白粉的原料;用
用途 和印染等工业。生活中用的炉具清洁剂中就含有于农业改良酸性土壤、配制农药波尔多
氢氧化钠,用以去除油污。可做干燥剂 液
制备原理 Ca(OH)+NaCO=CaCO↓+2NaOH CaO + HO =Ca(OH)
2 2 3 3 2 2
5.氢氧化钠的特性:吸水性、腐蚀性。生石灰和氢氧化钠固体都是碱性干燥剂(它们的混合物叫碱石灰),
可以干燥H、O、N、NH 等气体,但不能干燥CO、SO、HCl等酸性气体。
2 2 2 3 2 2
【要点诠释】
1.在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中,并不断搅拌。切不可将水倒进浓硫酸中。
2.称量氢氧化钠时,不能将氢氧化钠放在纸片上,而应放在玻璃器皿中称量,因为氢氧化钠易吸收水分而
潮解,且有较强的腐蚀性。
考点三、酸的通性
酸的通性可归纳为以下五点:(高清课堂《酸、碱和盐的复习(一)》三)
化学性质 盐酸 硫酸
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共8页让更多的孩子得到更好的教育
与指示剂作用 紫色石蕊试液遇酸变红色,无色酚酞试液遇酸不变色
与金属反应 Zn+2HCl=ZnCl + H↑ Zn+HSO=ZnSO+H↑
2 2 2 4 4 2
与金属氧化物反应 FeO+6HCl=2FeCl+3HO CuO+HSO=CuSO+HO
2 3 3 2 2 4 4 2
与盐反应 NaCO+2HCl=2NaCl+HO+CO↑ HSO+BaCl=BaSO↓+2HCl
2 3 2 2 2 4 2 4
与碱反应 HCl+NaOH=NaCl+HO HSO+2NaOH=NaSO+2HO
2 2 4 2 4 2
【要点诠释】
1.酸具有相似的化学性质是因为酸溶液中都存在相同的氢离子。
2.探究酸的化学性质,要学会对实验现象进行观察、分析和总结。
(1)金属Mg、Zn、Fe 、Cu分别与HCl,HSO 作用,只有Cu不反应(无现象),其余都能反应(有气体生成),
2 4
且产生气体的速率最快的是Mg,其次依次是Zn、Fe,由此可知这4种金属的活动性由强到弱的顺序依次
是Mg>Zn>Fe>Cu。
(2)观察酸与其他物质反应的现象,要重点关注以下几个方面:①反应物中若有固体,是否溶解。②生成
物中是否有气体、沉淀。③反应前后溶液的颜色是否改变。其中溶液颜色的变化有一定的规律:
a.溶液中有Fe2+,一般显浅绿色(如Fe与HCl,HSO 反应,溶液由无色变成浅绿色)。
2 4
b.溶液中有Fe3+,一般显棕黄色(如铁锈与HSO,HCl反应,红色铁锈溶解,溶液由无色变成棕黄色)。c.
2 4
溶液中有Cu2+,一般显蓝色(如CuO与HSO,HCl反应,黑色的CuO粉末溶解,溶液由无色逐渐变成蓝色)。
2 4
d.若反应前后溶液中无Fe2+,Fe3+,Cu2+,一般为无色,溶液颜色没有变化。
考点四、碱的通性
碱的通性可归纳为以下四点:
化学性质 氢氧化钠 氢氧化钙
与指示剂作用 紫色石蕊试液遇碱变蓝色,无色酚酞试液遇碱变红色
与非金属氧化物反应 CO+ 2NaOH = NaCO + HO CO + Ca(OH) =CaCO↓+ HO
2 2 3 2 2 2 3 2
与盐反应 2NaOH+CuCl=Cu(OH)↓+2NaCl Ca(OH)+NaCO=CaCO↓+2NaOH
2 2 2 2 3 3
与酸反应 HCl+NaOH=NaCl+HO 2HCl+Ca(OH)=CaCl+2HO
2 2 2 2
【要点诠释】
1.碱具有相似的化学性质是因为碱溶液中都存在相同的氢氧根离子。
2.NaOH必须密封保存,盛装强碱液的试剂瓶不能用玻璃塞而要用橡胶塞或软木塞封口。实验时,吸收CO
2
或酸性气体常用NaOH溶液而不用Ca(OH) 溶液,因为NaOH的溶解度远大于Ca(OH) 的溶解度,相同体积
2 2
的NaOH溶液吸收气体的能力比Ca(OH) 溶液的吸收能力强得多。
2
3.碱与盐的反应,除了要满足复分解反应条件外,碱和盐还必须可溶。
【典型例题】
类型一、考查酸碱指示剂及其应用
1.所示的实验不能得出的信息是( )
A.A烧杯中酚酞溶液变红,C烧杯中浓氨水没有变色
B.A烧杯内的酚酞溶液变红,说明分子在不断运动
C.A烧杯内的酚酞溶液变红,B烧杯内的酚酞溶液没有变色,说明使酚酞溶液变红的粒子是氨分子
D.该实验说明:温度越高,分子运动越快
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共8页让更多的孩子得到更好的教育
【思路点拨】根据分子运动的性质和酚酞遇碱溶液能变红的性质分析。浓氨水能挥发出氨气,氨气溶于水
形成氨水呈碱性。此对比实验是在相同温度下进行的。
【答案】D
【解析】A烧杯中酚酞溶液变红,C烧杯中浓氨水没有变色;A烧杯内的酚酞溶液变红,是因为氨气分子运
动的结果,说明分子在不断运动;A烧杯内的酚酞溶液变红,B烧杯内的酚酞溶液没有变色,说明空气的分
子不能使酚酞溶液变红,使酚酞溶液变红的粒子是氨分子;该实验是在相同温度下进行的,不能说明温度
越高,分子运动越快。故选D。
【总结升华】通过对比实验得出结论,是化学学习中常用的一种方法,要注意控制好变量,从而得到正确的
实验结论。
举一反三:
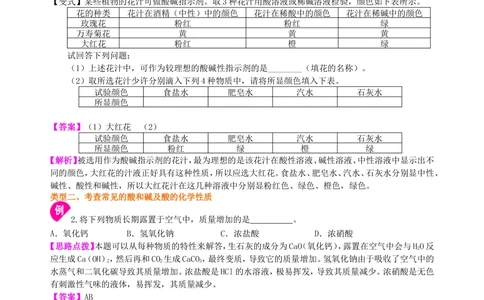
【变式】某些植物的花汁可做酸碱指示剂。取3种花汁用酸溶液或稀碱溶液检验,颜色如下表所示。
花的种类 花汁在酒精(中性)中的颜色 花汁在稀酸中的颜色 花汁在稀碱中的颜色
玫瑰花 粉红 粉红 绿
万寿菊花 黄 黄 黄
大红花 粉红 橙 绿
试回答下列问题:
(1)上述花汁中,可作为较理想的酸碱性指示剂的是________(填花的名称)。
(2)取所选花汁少许分别滴入下列4种物质中,请将所显颜色填入下表。
试验颜色 食盐水 肥皂水 汽水 石灰水
所显颜色
【答案】(1)大红花 (2)
试验颜色 食盐水 肥皂水 汽水 石灰水
所显颜色 粉红 绿 橙 绿
【解析】被选用作为酸碱指示剂的花汁,最为理想的是该花汁在酸性溶液、碱性溶液、中性溶液中显示出不
同的颜色,大红花的汁液正好具有这种性质,所以应选大红花。食盐水、肥皂水、汽水、石灰水分别显中性、
碱性、酸性和碱性,所以大红花汁在这几种溶液中分别显粉红色、绿色、橙色,绿色。
类型二、考查常见的酸和碱及酸的化学性质
2.将下列物质长期露置于空气中,质量增加的是 。
A.氧化钙 B.氢氧化钠 C.浓盐酸 D.浓硝酸
【思路点拨】本题可以从每种物质的特性来解答,生石灰的成分为CaO(氧化钙),露置在空气中会与HO反
2
应生成Ca(OH),然后再和CO 生成CaCO,最终变质,导致它的质量增加。氢氧化钠由于吸收了空气中的
2 2 3
水蒸气和二氧化碳导致其质量增加。浓盐酸是HCl的水溶液,极易挥发,导致其质量减少。浓硝酸是无色
有刺激性气味的液体,易挥发,其质量减少。
【答案】AB
【解析】氧化钙露置在空气中吸水等导致其质量增加;氢氧化钠露置在空气中,易吸水发生潮解,又能与空
气中的二氧化碳反应导致其质量增加;浓盐酸具有挥发性,露置在空气中质量减少;浓硝酸易挥发,露置
在空气中质量减少。
【总结升华】浓盐酸、浓硫酸和浓硝酸是三大强酸。(1)浓盐酸具有较强的挥发性,挥发出来的氯化氢会和
空气中的水蒸气结合,形成盐酸的小液滴,扩散在空气中,所以浓盐酸在打开瓶盖后瓶口上方会出现白雾,
因此盐酸要储存在密封容器当中,否则盐酸的质量会逐渐下降,浓度也会下降。(2)市售浓硝酸质量分数
约为65%,密度约为1.4g/cm3,沸点为83℃;因浓硝酸不稳定,在光照和遇热时易分解,故实验室里常将浓
硝酸盛放在棕色试剂瓶中(避光),且放置于冷暗处。(3)浓硫酸是一种高沸点(338℃)难挥发的强酸,易
溶于水,能以任意比与水混溶;浓硫酸溶解时放出大量的热,因此浓硫酸稀释时应该“酸入水,沿器壁,慢
慢倒,并用玻璃棒不断搅拌”,切不可将水倒进浓硫酸中。浓盐酸、浓硝酸和浓硫酸的对比如下表:
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共8页让更多的孩子得到更好的教育
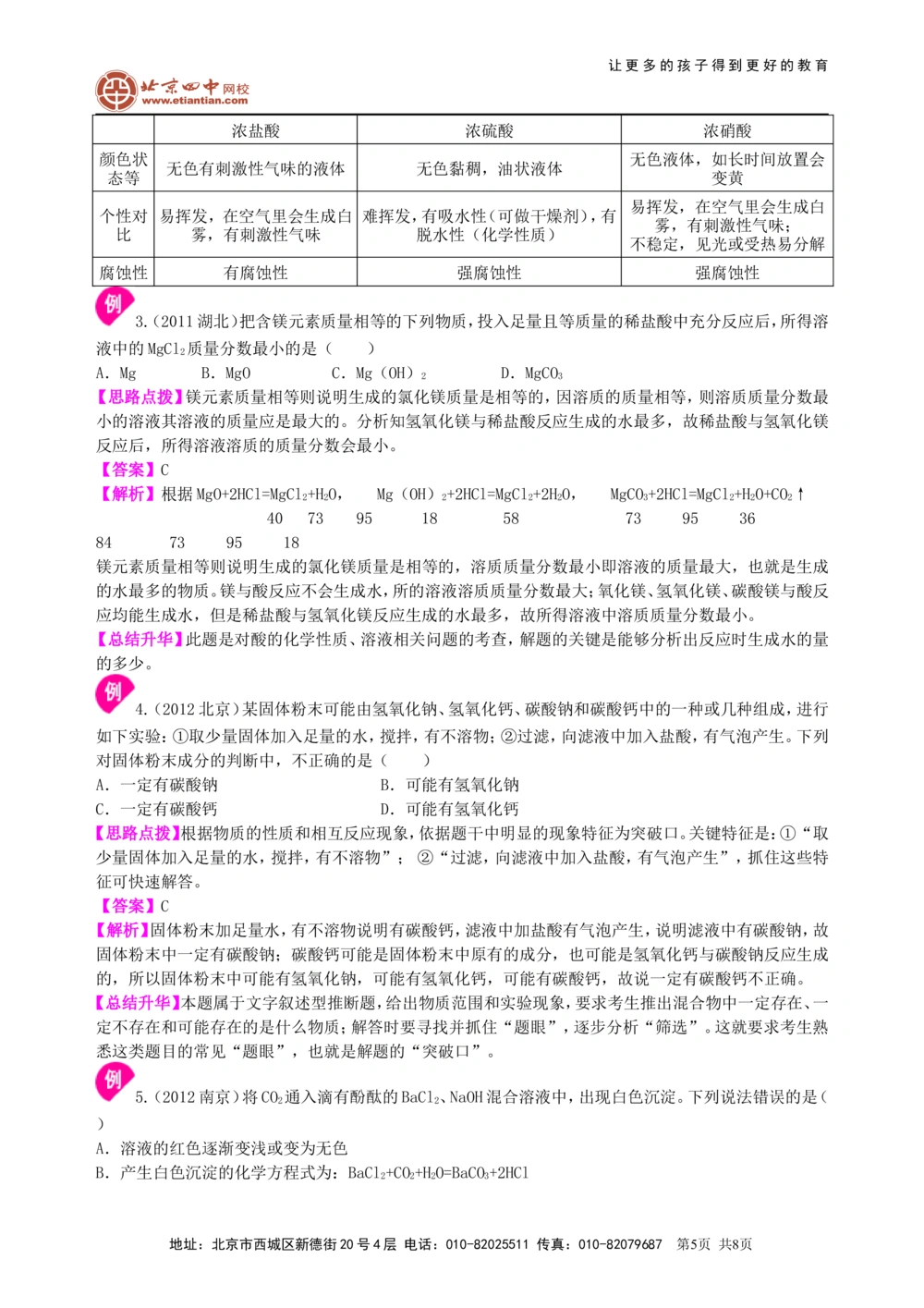
浓盐酸 浓硫酸 浓硝酸
颜色状 无色液体,如长时间放置会
无色有刺激性气味的液体 无色黏稠,油状液体
态等 变黄
易挥发,在空气里会生成白
个性对 易挥发,在空气里会生成白 难挥发,有吸水性(可做干燥剂),有
雾,有刺激性气味;
比 雾,有刺激性气味 脱水性(化学性质)
不稳定,见光或受热易分解
腐蚀性 有腐蚀性 强腐蚀性 强腐蚀性
3.(2011湖北)把含镁元素质量相等的下列物质,投入足量且等质量的稀盐酸中充分反应后,所得溶
液中的MgCl 质量分数最小的是( )
2
A.Mg B.MgO C.Mg(OH) D.MgCO
2 3
【思路点拨】镁元素质量相等则说明生成的氯化镁质量是相等的,因溶质的质量相等,则溶质质量分数最
小的溶液其溶液的质量应是最大的。分析知氢氧化镁与稀盐酸反应生成的水最多,故稀盐酸与氢氧化镁
反应后,所得溶液溶质的质量分数会最小。
【答案】C
【解析】根据MgO+2HCl=MgCl+HO, Mg(OH)+2HCl=MgCl+2HO, MgCO+2HCl=MgCl+HO+CO↑
2 2 2 2 2 3 2 2 2
40 73 95 18 58 73 95 36
84 73 95 18
镁元素质量相等则说明生成的氯化镁质量是相等的,溶质质量分数最小即溶液的质量最大,也就是生成
的水最多的物质。镁与酸反应不会生成水,所的溶液溶质质量分数最大;氧化镁、氢氧化镁、碳酸镁与酸反
应均能生成水,但是稀盐酸与氢氧化镁反应生成的水最多,故所得溶液中溶质质量分数最小。
【总结升华】此题是对酸的化学性质、溶液相关问题的考查,解题的关键是能够分析出反应时生成水的量
的多少。
4.(2012北京)某固体粉末可能由氢氧化钠、氢氧化钙、碳酸钠和碳酸钙中的一种或几种组成,进行
如下实验:①取少量固体加入足量的水,搅拌,有不溶物;②过滤,向滤液中加入盐酸,有气泡产生。下列
对固体粉末成分的判断中,不正确的是( )
A.一定有碳酸钠 B.可能有氢氧化钠
C.一定有碳酸钙 D.可能有氢氧化钙
【思路点拨】根据物质的性质和相互反应现象,依据题干中明显的现象特征为突破口。关键特征是:①“取
少量固体加入足量的水,搅拌,有不溶物”; ②“过滤,向滤液中加入盐酸,有气泡产生”,抓住这些特
征可快速解答。
【答案】C
【解析】固体粉末加足量水,有不溶物说明有碳酸钙,滤液中加盐酸有气泡产生,说明滤液中有碳酸钠,故
固体粉末中一定有碳酸钠;碳酸钙可能是固体粉末中原有的成分,也可能是氢氧化钙与碳酸钠反应生成
的,所以固体粉末中可能有氢氧化钠,可能有氢氧化钙,可能有碳酸钙,故说一定有碳酸钙不正确。
【总结升华】本题属于文字叙述型推断题,给出物质范围和实验现象,要求考生推出混合物中一定存在、一
定不存在和可能存在的是什么物质;解答时要寻找并抓住“题眼”,逐步分析“筛选”。这就要求考生熟
悉这类题目的常见“题眼”,也就是解题的“突破口”。
5.(2012南京)将CO 通入滴有酚酞的BaCl、NaOH混合溶液中,出现白色沉淀。下列说法错误的是(
2 2
)
A.溶液的红色逐渐变浅或变为无色
B.产生白色沉淀的化学方程式为:BaCl+CO+HO=BaCO+2HCl
2 2 2 3
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共8页让更多的孩子得到更好的教育
C.反应后的溶液中一定有NaCl
D.反应过程中,溶液里的BaCl、NaOH的质量分数均减小
2
【思路点拨】将CO 通入滴有酚酞的BaCl、NaOH的混合溶液中,二氧化碳与氢氧化钠先反应,生成的碳酸
2 2
钠再与氯化钡反应。
【答案】B
【解析】因为氢氧化钠属于碱,能使酚酞变红;通入二氧化碳后,二氧化碳与氢氧化钠反应生成碳酸钠和水,
碳酸钠再与氯化钡反应生成碳酸钡沉淀和氯化钠,所以碱性会减弱或消失,故溶液的红色逐渐变浅或变
为无色,故A说法正确。产生白色沉淀的化学方程式为:BaCl+NaCO=BaCO↓+2NaCl,故B错。二氧化碳与
2 2 3 3
氢氧化钠反应生成碳酸钠和水,碳酸钠再与氯化钡反应生成碳酸钡沉淀和氯化钠,所以最后溶液中一定
含有氯化钠,故C说法正确。根据反应化学方程式可知BaCl、NaOH都是反应物,它们都在不断减少,所以
2
质量分数在不断减小,故D说法正确。
【总结升华】解答本题关键是要知道二氧化碳先与氢氧化钠反应,生成碳酸钠和水,碳酸钠再与氯化钡反
应生成碳酸钡沉淀和氯化钠,再进一步进行分析即可。
6.(2012山东)如图是我市某校学生设计的“硫燃烧现象及酸雨危害模拟实验”装置图。实验操作
步骤为:①连接仪器,装好药品;②将玻璃棒下端在酒精灯上烧红,迅速伸入广口瓶中点燃硫粉;③向锥形
瓶中注入双氧水;④硫粉完全燃烧后,用注射器向广口瓶中喷水。下列描述错误的是( )
A.“酸雨”使绿叶变黄,锌粒、镁片表面产生气泡
B.实验结束时,应用注射器向装置中注入NaOH溶液以吸收剩余的SO 气体
2
C.A装置中的注射器的作用相当于分液漏斗
D.可以观察到,硫在氧气中燃烧发出蓝紫色火焰,并产生大量白烟
【思路点拨】本题是有一定难度的综合性题目。熟悉酸雨对植物的危害、二氧化硫气体的吸收方法、硫的燃
烧现象等知识,以及正确分析实验装置的特点是解题的关键。
【答案】D
【解析】“酸雨”中的酸可以腐蚀绿叶,使叶片发黄;镁和锌与“酸雨”中的酸反应生成氢气,故A描述正
确;用NaOH溶液可吸收剩余的SO 气体,防止SO 气体产生污染,故B正确;A装置中的注射器的作用是随
2 2
时添加液体,相当于分液漏斗,故C正确;硫在氧气中燃烧发出蓝紫色火焰,产生有刺激性气味的气体,而
不是产生大量白烟,故D错误。
【总结升华】化石燃料燃烧产生的烟、CO、SO、NO 等污染物被排放到大气中,不仅影响空气的质量,而且氮
2 2
和硫的氧化物溶解于雨水中形成酸雨。酸雨的pH小于5.6。酸雨对建筑物、动植物、金属制品都有腐蚀性。
一般情况下用氢氧化钠溶液来吸收二氧化硫,以减少酸雨发生的次数。
举一反三:
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共8页让更多的孩子得到更好的教育
【变式1】(2012湖北)如图中甲、乙、丙是三种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,
则甲、乙、丙三种物质可能为( )
A.Cu、Ca(OH)、CaCO B.Mg、CaCO、NaHCO
2 3 3 3
C.Fe、CuO、Cu(OH) D.Zn、FeO、NaNO
2 2 3 3
【答案】C
【解析】根据盐酸的化学性质进行分析,盐酸能与某些金属、金属氧化物、碱和某些盐发生化学反应。
铜在氢的后面,不与盐酸发生化学反应,故A错误。这三种物质都能与盐酸发生化学反应,镁属于金属单
质,碳酸钙和碳酸氢钠属于盐,不符合题意,故B错误。这三种物质都能与盐酸反应,铁属于金属,氧化铜
属于金属氧化物,氢氧化铜属于碱,故C正确。硝酸钠不能与盐酸发生化学反应,故D错误。
【变式2】是关于铜及其化合物的知识网络图,“→”表示一种物质转化成另一种物质。A,B,C分别是不
同类别的铜的化合物,其中A物质为黑色粉末,B物质易溶于水。
(1)写出下列物质的化学式:A:________,C:________。
(2)写出①的基本反应类型:________;写出②的化学方程式:________。
【答案】(1)CuO Cu(OH)
2
(2)化合反应 CuSO +BaCl ==BaSO ↓+CuCl [或CuSO +Ba(NO)==BaSO ↓+Cu(NO )]
4 2 4 2 4 3 2 4 3 2
【变式3】某化学实验室有一瓶失去标签的碱溶液,可能是氢氧化钠溶液或氢氧化钙溶液;小王同学认为
是氢氧化钙溶液。请你按小王同学的猜想,进行下列实验探究,并按要求填写下表:
猜 结论与相应的化学方程式
实验步骤 实验现象
想 (若不反应可不写化学方程式)
方案Ⅰ:
该溶液是_______________,
可 用试管取约2mL该溶液,向
_____________ 化学方程式:
能 其中滴加几滴
__________________________
是 ____________溶液
氢
氧
化
方案Ⅱ:(选用与方案Ⅰ
钙 该溶液是_______________,
不同类别的其他物质)
溶 _____________ 化学方程式:
____________________
液 __________________________
____________________
【答案】方案Ⅰ:碳酸钠 生成白色沉淀 氢氧化钙溶液
NaCO+ Ca(OH)= CaCO↓+2NaOH
2 3 2 3
方案Ⅱ:用试管取约2mL该溶液,向其中通入二氧化碳气体
生成白色沉淀 氢氧化钙溶液 Ca(OH) + CO = CaCO↓+ HO
2 2 3 2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共8页让更多的孩子得到更好的教育
【解析】氢氧化钠与二氧化碳反应生成碳酸钠和水,反应现象不明显;而氢氧化钙与二氧化碳反应生成碳
酸钙沉淀和水,所以可以用二氧化碳鉴别氢氧化钠和氢氧化钙。氢氧化钠和碳酸钠不反应,氢氧化钙却与
碳酸钠反应生成碳酸钙沉淀,所以也可以用碳酸钠来鉴别氢氧化钠和氢氧化钙。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第8页 共8页