| ||
| ||
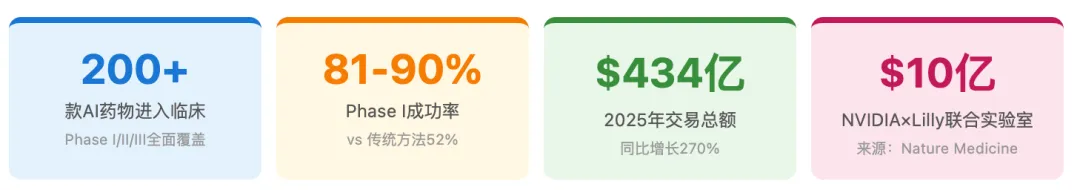
 ▲ AI与生物医药的深度融合正在重塑制药行业格局 | ||
2026年1月12日,JPMorgan医疗健康大会首日,全球市值最高的制药巨头礼来(Eli Lilly)与全球市值最高的科技巨头英伟达(NVIDIA),在旧金山湾区共同宣布:未来五年内,双方将联合投资10亿美元,建设AI药物研发联合创新实验室。 | ||
这不是一个孤立的新闻。这只是2025-2026年AI与生物医药深度融合浪潮中,最具标志性的一声回响。 | ||
事实上,过去两年,AI在生物医药领域的进展已经不是"新闻",而是历史。
| ||
一、真实数据:AI正在创造看得见的临床价值 | ||
许多人听到"AI制药",第一反应是"这还早"。但数据不讲情怀,只讲事实。截至2025年12月,全球已有超过200款由AI设计或辅助开发的药物分子进入临床试验阶段,其中Phase I 94个、Phase II 56个、Phase III 15个。这不是未来,这是现在进行时。 | ||
2026年3月BioMed Nexus发布的统计报告显示:AI发现化合物的Phase I临床成功率估计在81%至90%之间,而传统药物发现方法的Phase I成功率仅约52%;AI方法的Phase II成功率约65%至75%,传统方法仅30%至45%。 | ||
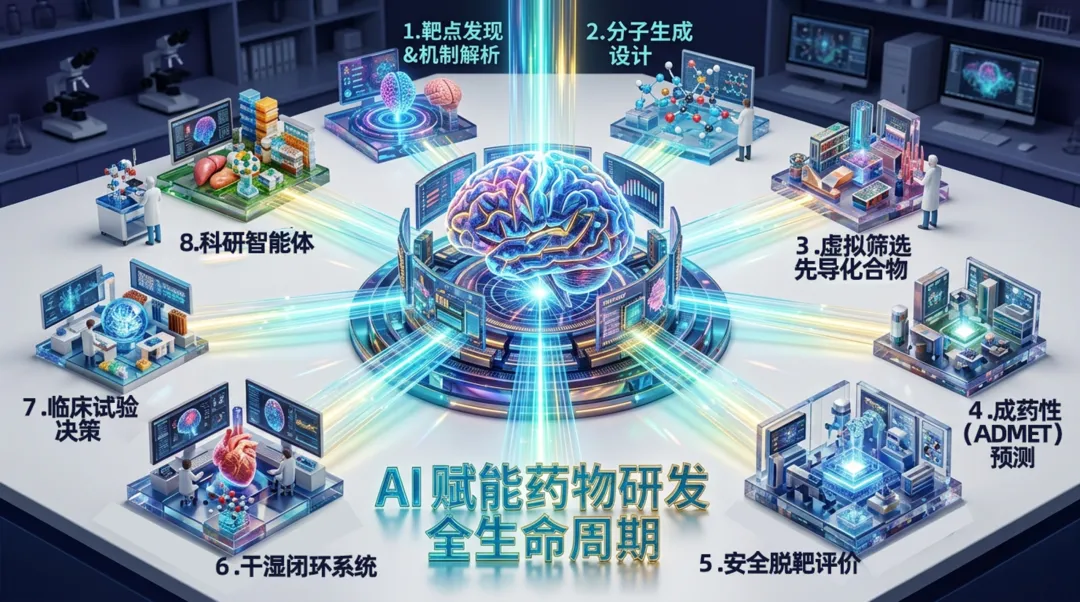 ▲ AI正在以数据驱动的方式革新临床试验的各个环节
| ||
📌 数据来源:Axis Intelligence (2025.12) · BioMed Nexus (2026.03) · 深智药询 (2026.03) | ||
二、标志性临床突破:从"理论上可行"到"临床数据说话" | ||
案例一:英矽智能(Insilico Medicine) — 首个完全由AI发现的药物分子 | ||
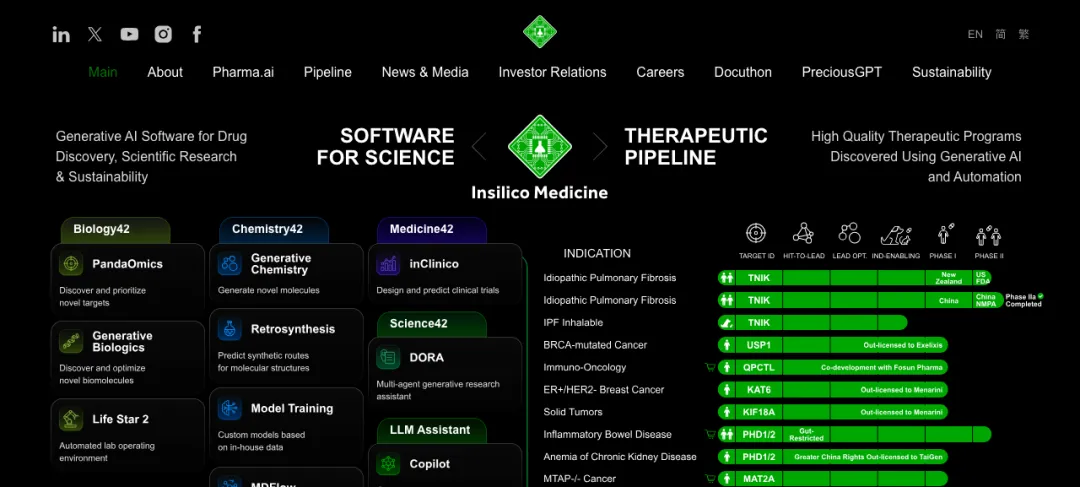 ▲ 端到端AI药物发现平台 | ||
Rentosertib(ISM001-055)是全球第一个从靶点发现到分子设计全程由AI主导的药物。2025年6月,其IIa期临床结果发表于《Nature Medicine》:针对特发性肺纤维化(IPF),60mg剂量组治疗12周后,用力肺活量(FVC)改善达98.4毫升,而安慰剂组反而恶化62.3毫升——差距超过160毫升。 | ||
从靶点发现到提名临床前候选药物,英矽智能仅用了18个月,而传统方法通常需要3至5年。2026年3月,礼来追加投入,总金额达27.5亿美元(首付1.15亿美元+里程碑付款),共同开发口服GLP-1类药物管线。 | ||
案例二:Recursion Pharmaceuticals — AI+高通量实验的工业级范式 | ||
 ▲ Recursion:AI驱动的药物发现操作系统 | ||
Recursion的核心竞争力在于将AI与大规模自动化实验深度整合——每周可完成数百万次的细胞实验,用真实的生物学数据训练模型,再用模型指导下一轮实验。这种"生成—验证—再生成"的闭环,使 Recursion 的研发效率远超传统药企。 2025年,其与基因泰克(Genentech/Roche)达成合作,首付款即达1.5亿美元,潜在总金额超过5亿美元。 | ||
案例三:Generate:Biomedicines — 生成式AI设计全新蛋白质药物 | ||
 ▲ 生成式AI正在设计自然界中从未存在过的全新蛋白质药物 | ||
Generate:Biomedicines是生成式AI在生物医药领域最激进的应用——不再是从现有分子库中筛选,而是让AI"凭空生成"自然界中从未存在过的全新蛋白质作为药物。 2024年,其在Nature杂志发表论文,展示了如何用AI在实验室中测试42,000多种AI生成的蛋白质,并成功识别出多个具有高结合亲和力的候选物。 2026年初,Flagship Pioneering追加投资,使其估值突破30亿美元。 | ||
三、底层逻辑:为什么是现在?三大技术奇点同时到来 | ||

▲ AI与机器人自动化的融合正在重塑药物研发流程 | ||
AlphaFold 3是一个划时代的技术里程碑。蛋白质是生命的基础,理解其三维结构是药物设计的根基——而AlphaFold 3让我们第一次能够以原子级精度预测几乎任何生物分子的结构。 2024年诺贝尔化学奖授予David Baker(从头设计蛋白质)、Demis Hassabis和John Jumper(AlphaFold),正是对这一技术浪潮的正式加冕。 | ||
AI制药的三个底层条件——足够好的模型、足够多的数据、足够便宜的算力——在2024-2025年首次同时成熟。三条曲线交汇,形成了一个不可逆转的拐点。
| ||
▲ AlphaFold 3:原子级精度的蛋白质结构预测 | ||
更重要的是,DeepMind已宣布将AlphaFold 3的能力开源,任何人都可以免费使用。这一决定的意义不亚于互联网的开源——它让全球的研究者和药企站在了同一起跑线上,极大加速了整个领域的创新。 | ||
四、资本用脚投票:$434亿交易额背后的真实逻辑 | ||
 ▲ 科技与制药的跨界融合正在吸引海量资本 | ||
资本从不相信情怀,只相信数据。2025年AI药物发现领域的总交易金额达到434亿美元,同比增长超过270%。这不是风险投资的小打小闹,这是制药巨头和科技巨头的战略级投入。 | ||
礼来27.5亿美元牵手英矽智能、罗氏5亿美元下注Recursion、英伟达10亿美元建联合实验室——每一个数字背后都是严格的ROI计算。 | ||
这些交易有一个共同点:首付比例高、里程碑设置清晰、退出路径明确。制药公司正在用行动表明:AI制药已经不是"要不要做"的问题,而是"怎么做得更快"的问题。 | ||
五、中国机遇:全球AI制药格局中的独特位置 | ||
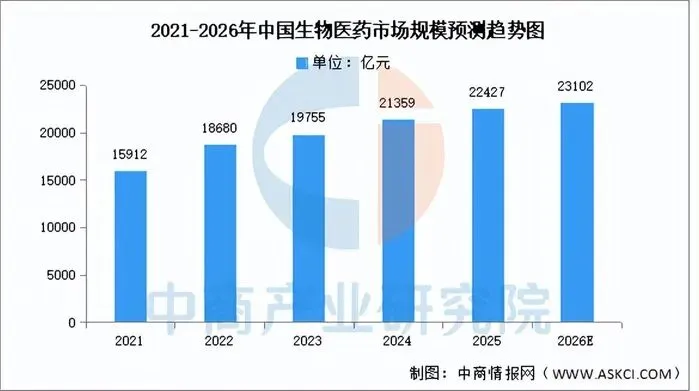 ▲ 中国生物医药研究正在快速崛起 | ||
在全球AI制药版图中,中国有自己的独特优势。 | ||
📊 数据优势:14亿人口带来的庞大患者数据和丰富的临床资源,让中国在真实世界数据和多中心临床试验方面具有天然优势(当然,中国医疗数据的标准化程度低、跨院融合难是巨大阻碍)。 | ||
⚡ 速度优势:中国的biotech公司决策快、执行快、迭代快——同样的临床试验,中国团队往往能比欧美同行更快完成患者入组。 | ||
🔗 生态优势:从CRO到临床PI到医院,中国已经建立了全球最完整的制药产业链。 | ||
但短板同样明显:底层数据库建设、原创算法能力、核心算力基础设施、顶级基础研究人才,与美国仍有差距。这也是为什么我们看到越来越多的中国AI制药公司选择在美国设立研发中心、与国际药企建立合作——取长补短,开放共赢。 | ||
六、人才缺口:这不是瓶颈,这是机遇 | ||
 ▲ 跨学科复合型人才是AI制药行业的核心竞争力 | ||
整个行业最大的瓶颈,不是钱,不是技术,而是人。这个领域需要的是"π型人才"——两个领域都有深度,同时还能在两者之间搭桥。具体来说,以下几类人才最为稀缺:
| ||
这些岗位的薪资水平已经显著高于纯互联网或纯生物医药岗位。以美国市场为例,Senior AI Scientist in Drug Discovery的年薪中位数已超过35万美元,总包(含股权)可达50万美元以上。而在国内,头部AI制药公司同样在极具竞争力的薪酬抢夺人才。 | ||
七、监管进化:FDA的拥抱与审慎 | ||

▲ 监管框架正在与AI技术同步进化 | ||
监管机构的态度是AI制药能否大规模落地的关键变量。FDA已经明确表示:不要求企业单独为AI申请审批,而是将AI作为工具纳入现有审评框架。 2024年5月,FDA发布了《AI/ML驱动的药物及生物制品监管框架》,明确了AI在药物研发全流程中的应用规范。 | ||
值得注意的是,2025年FDA批准了首个完全由AI设计分子结构的新药进入临床试验,这是监管历史上的重要里程碑。 FDA的审评员们正在学习理解AI的工作逻辑,而AI公司也在主动与监管机构沟通,了解审批要求。 这种双向互动,正在构建一个更高效、更科学的监管生态。 | ||
八、喧嚣后的冷思考:当前面临的核心挑战 | ||
尽管 AI 在药物研发中展现了惊人的潜力,但要实现真正的"工业化产出",行业仍需跨越几座大山: | ||
| ||
| ||
| ||
| ||
 ▲ AI正在解锁生命的无限可能 | ||
| ||
2026年1月英伟达与礼来的10亿美元握手,不是起点,也不是终点。它是这个时代最清晰的信号:生物医药与AI的融合,已经从"是否会发生"的讨论阶段,进入了"以什么速度、什么规模发生"的实施阶段。 | ||
对于生物医药研究者,AI是百年来最重要的技术杠杆。对于AI从业者,生物医药是少数几个还在快速增长、数据壁垒极高、且对AI工具的需求正在爆发的领域之一。 | ||
📚 参考来源:Axis Intelligence · BioMed Nexus · Nature Medicine · 深智药询 © 2026 · 齐云龙 · AI与生物医药系列 |
 夜雨聆风
夜雨聆风