
在生命科学研究中,发现一个新颖的疾病相关靶点往往能带来一篇高影响力论文。然而,目前单纯的发病机制类研究,已陷入常规化困境—数量扎堆、实验设计相似(多围绕靶点-通路-疾病表型的验证循环)。即便靶点新颖,也容易因缺乏突破性延伸而难以在众多研究中脱颖而出。事实上,阐明发病机制只是解码疾病的第一步,靶点的核心价值与突破性意义,最终要落脚于能否设计出改变疾病进程的精准治疗药物。遗憾的是,大量研究止步于靶点发现阶段,未能推动靶点向实际治疗产品转化。据报道,人类基因组约2万个蛋白编码基因中,潜在可成药基因约3000个,但成功转化为FDA批准药物的靶点不足700个,而当前国内药物研发资源竟高度集中在不超过20个明星靶点上(如PD-1/PD-L1、KRAS等)。这使得大量具有生物学价值的靶点长期处于“沉睡”状态,不仅造成一些科研资源的浪费,也让肿瘤、自身免疫病等领域中大量未被满足的临床需求。
近年来AI技术的全面爆发,正为这一困境带来范式革新。由AI驱动的靶点药物开发,不仅能大幅缩短药物发现的周期、降低研发成本,还能精准预测靶点分子可成药性(ADMET)、高效破解难成药靶点的转化瓶颈,更能从零创造出高亲和力结合的全新小分子。而那些未被开发的数千个靶点,恰恰为AI技术的落地应用提供了海量素材与广阔发挥空间。在成果层面,有望实现“创新性论文+核心专利+产业化潜力”的三重收益,推动研究从实验室走向应用。在更广阔的的层面上,这不仅有助于突破前沿生物医药技术壁垒,更能加速科学发现向临床治疗产品的转化,将基础研究成果转化为惠及民众健康的公共产品。
例如,2024年英矽智能利用生成式AI技术仅用18天,就成功设计出了针对TNIK靶点的潜在临床新药INS018_055,研究成果发表在A small-molecule TNIK inhibitor targets fibrosis inpreclinical and clinical models。此外,清华大学智能产业研究院2026年首篇Science,开发了AI驱动的超高通量药物虚拟筛选平台DrugCLIP,构建了已知最大规模的蛋白-配体筛选数据库,可开放获取,相关研究成果见Deep contrastive learning enables genome-wide virtual screening。这极大降低了早期药物发现壁垒,为冷门但重要靶点的研究提供了有力支撑。
接下来,小编梳理了AI在靶点研究中的几个极具潜力的研究方向,旨在为不同领域的科研工作者提供交叉创新的思路,让您的课题既保持前沿新颖性,又具备明确的转化前景。
集思慧远深耕AI辅助药物开发领域,能够为您提供从靶点分析、虚拟筛选、SRP等分子实验验证、机制解析以及方案设计的全链条专业服务与协作支持。选择我们,让AI赋能您的靶点研究,在生物医药创新赛道上抢占先机、脱颖而出!

1.虚拟筛选
根据一个疾病靶点,可使用中药单体库、天然产物库,借助AI从中筛选出与靶点高效结合的中药单体或天然产物分子。也可使用FDA批准药物库从中挖掘已上市药物,从而拓展现有药物新适应症(老药新用),缩短研发周期、降低临床风险。该技术适用于药学老师、药企、中医药、天然产物研究领域或临床医生、临床科研人员。
2.已知配体多目标优化
先导化合物药物优化是新药研发中的核心环节,其常存在活性不足、选择性差或ADMET性质不佳等问题。使用AI可预测这些特性并指导结构修饰,以提升活性与成药性等,从而显著降低后期临床试验的失败风险。这块适配中医药大学、中医类医院、临床药学及创新药企等。
3.难成药靶点PROTAC/DUBTAC研究
对于蛋白-蛋白互作界面、GPCR变构位点、内在无序蛋白和无明确活性口袋等难成药靶点,使用AI生成与这些靶点结合的高亲和力分子,并可辅助PROTAC降解剂、DUBTAC稳定剂开发(与PROTAC作用相反的双功能分子,通过去除靶蛋白上的泛素链稳定蛋白质)。这块聚焦药物化学/药学、药企等。
4.从头生成特定功能分子
需要设计具有特殊功能如高特异性、低免疫原性等的分子如环肽、抗体、酶等。这块比较适合药企、生物制药、合成生物学和药学科研人员等。
下面,请大家和集思慧远一起来具体了解下AI在这些方向上的应用。
方向一:虚拟筛选
原理:从靶蛋白的三维结构出发,研究靶蛋白结合位点的特征性质以及它与小分子化合物之间的相互作用模式,根据与结合能相关的亲合性打分函数对蛋白和小分子化合物的结合能力进行评价,最终从大量的化合物分子中挑选出结合模式比较合理的、预测得分较高的化合物,用于后续的生物活性测试。
应用场景:针对已知或新发现的疾病靶点,从百万级化合物库中高通量筛选高活性候选分子。
案例1—基于已知靶点的天然产物筛选+SPR验证+功能/作用机制验证
已知CD133是一个有前景的泛癌靶点,因其结构复杂及肿瘤异质性,急需设计有效靶向CD133的药物。2025年10月2日,清华大学马少华联合暨南大学张玉波团队基于Transformer的CPI筛选模型,筛选出两种天然产物靶向CD133—重楼皂苷V(PP10)和重楼皂苷H(PP24),在多种肿瘤模型中显示出显著抗癌效果。

发文思路:
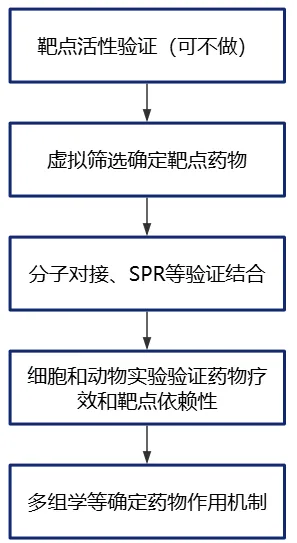
案例2—基于靶点的药物重定位(老药新用)+SPR验证+细胞/动物验证疗效
治疗炎症性肠病的P2Y14R拮抗剂口服利用度不佳。因此,苏州大学田盛/李环球教授团队从DrugBank中选取FDA批准和在研药物,作为药物筛选库。并基于P2Y14R结构进行虚拟筛选,最终锁定氯霉素琥珀酸酯。随后通过细胞/动物实验证实其抗炎及肠屏障保护作用。

发文思路:
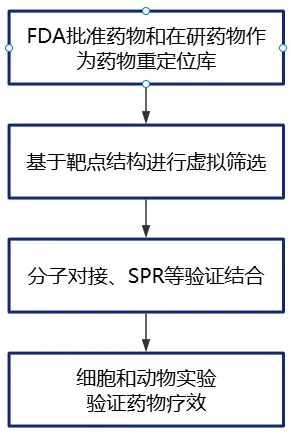
方向二:先导化合物从头生成与优化
De novo:根据已知三维结构的靶蛋白-配体和约束条件(例如期望的活性/选择性、理化性质、安全性、可合成性等),从无到有生成潜在药物分子。
应用场景:全新靶点的候选物启动、设计特殊功能分子(如环肽、抗体等)、难成药靶点的全新分子设计
分子优化:通过改进已有化合物结构,增强其药效、选择性、药代动力学和安全性,最终使其成为候选药物。结构修饰包含骨架跃迁(改变核心结构,保持原有活性)、连接子设计(连接弱结合亲和力片段,形成更高活性的化合物)、片段替换(替换特定基团,以提升亲和力)和侧链修饰(保留活性优势骨架,并修改侧链以增强药效)。
应用场景:成药性综合优化、活性增强优化和结构创新
案例—基于已知靶点的先导物从头生成与结构优化+SPR验证+疗效分析
TYR(酪氨酸酶)是黑色素合成中的关键限速酶,但现有TYR抑制剂活性差、皮肤渗透性差、存在安全风险等。来自杭州师范大学药学院的白仁仁教授团队联合沈阳药科大学基于SAC算法的强化学习模型,整合化学反应模板库+分子构建块库,生成兼具靶点亲和力、成药性和合成可行性的分子。从700个AI生成分子中筛选17个进行合成验证,发现先导化合物V对TYR的抑制活性最强。对化合物V进行结构修饰后,V-24活性最佳(较V提升600-2300倍),药物性质最优,在细胞/斑马鱼/3D皮肤模型中显著抑制黑色素产生。

发文思路:
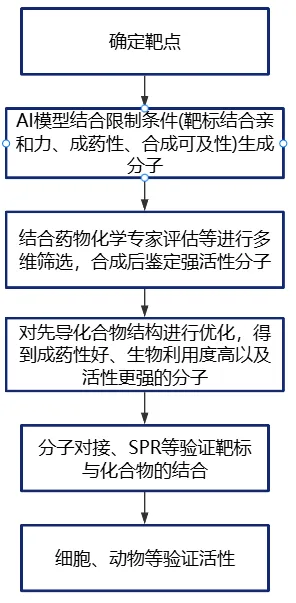
方向三:难成药靶点PROTAC/DUBTAC开发
难成药靶点:指难以用传统小分子抑制的蛋白靶点,包括GTP酶、蛋白-蛋白相互作用、转录因子等,此前PROTAC是研发此类药物常用策略之一。同样,AI也被用于设计靶向难成药的高亲和力结合剂,因此其可作为靶蛋白配体,用于构建新型PROTAC分子。
案例—基于已知靶点的PROTAC分子开发+降解特异性+活性验证
PKMYT1是一种合成致死性癌症靶点,但当前PKMYT1抑制剂存在毒性大、药效差以及突变耐药性问题。2025年11月28日,英矽智能结合现有PKMYT1抑制剂的关键优势特征,使用AI生成了全新PKMYT1抑制剂,并设计了双功能PROTAC分子D16-M1P2。该分子可高效降解PKMYT1,并发挥酶抑制活性,在临床前模型中展现出强大的抗肿瘤活性。
同样有应用潜力的是DUBTAC(去泛素化酶靶向嵌合体)分子的设计,该分子由靶蛋白配体、去泛素化酶配体和Linker三部分组成,其作用与PROTAC相反—通过去除靶蛋白上的泛素链来稳定蛋白质。2025年12月17日,中国药科大学药学院的徐盛涛教授团队开发了针对p53 Y220C的DUBTAC分子A1,其通过构象修复+去泛素化稳定双重功效,在体内外均展现强效抗癌活性。因此,由AI设计的针对靶点的特异性分子也可作为关键元件用于设计新型DUBTAC分子。

方向四:从头生成特定功能分子
1.基于靶点生成多肽、环肽
(1)多肽:与小分子化合物相比,肽类药物因高靶向特异性、易代谢、潜在毒性/生产成本和免疫原性低等优点而受到广泛关注。
应用场景:需设计特异性强或组织穿透性等特定功能的抑制剂
生成模型及原理:
RFdiffusion模型:输入靶蛋白晶体结构,定义结合位点并指导RFdiffusion模型迭代去噪生成与之互补的肽骨架,随后ProteinMPNN优化氨基酸序列,AlphaFold 3预测复合物结构。
PepMLM模型:将靶蛋白序列与已知结合肽结合,并掩蔽肽序列,让蛋白语言模型ESM-2准确揭露掩蔽肽序列,训练完成后就可以根据靶蛋白序列(无需靶蛋白结构)生成全新的肽结合剂。
Transformer模型:通过从蛋白质数据库中获取蛋白互作数据去训练AI。输入靶标表面信息,模型生成理论相互作用界面,并在预先计算的电荷支架库中进行匹配搜索。经Rosetta FastDesign模块优化骨架后,获得候选的靶标结合多肽分子。
案例-基于靶点的多肽生成+BLI/CO-IP验证+机制验证+活性分析
GSDMD-NT介导的过度焦亡诱导炎症疾病,因其孔道体积大、表面光滑且结构高度动态化,传统方法难以筛选有效抑制剂。2025年9月15日,陆军军医大学大坪医院王淦/曾灵研究员团队基于Transformer模型生成靶向GSDMD-NT孔道的多肽SK56,可延缓细胞焦亡,减轻脓毒症。并且多肽SK56已被授予国家发明专利(专利受理号:202310315378X)。
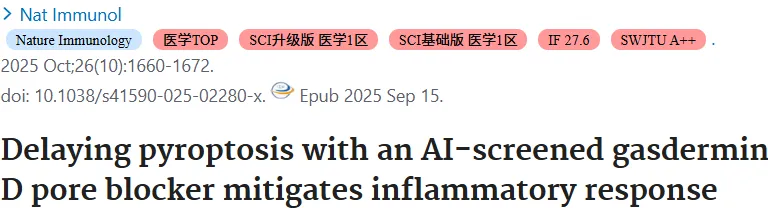
发文思路:
(2)环肽:相比于小分子,环肽更易靶向蛋白-蛋白互作界面。相比于线性肽,环肽稳定性、亲和力和透膜性更佳。
应用场景:难成药靶点以及特定功能需求研究
模型及原理:RFpeptides模型:在RFdiffusion中引入循环相对位置编码生成多样大环肽骨架,利用ProteinMPNN优化氨基酸序列、AfCycDesign结构预测与Rosetta物理打分进行严格筛选。
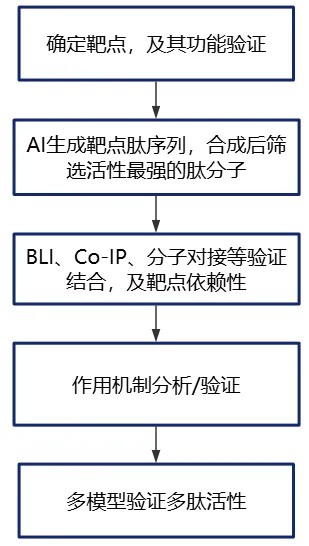
案例—基于靶点的大环肽生成+SPR/X-ray验证
传统大环肽开发方法成本高、效率低,且尚无可靠的方法设计精准结合蛋白质的大环肽。2025年6月20日,David Baker团队开发了环状肽设计模型RFpeptides,针对4种靶点仅需测试≤20条设计大环肽,便能获得高亲和力结合物。即使是未知实验结构的全新靶蛋白也能生成高准确性、高成功率的大环肽。

研究思路
2.基于已知靶点生成抗体
抗体:凭借其高特异性、强靶向性、安全性和长效性等优势,被广泛用于肿瘤、自身免疫性疾病、慢性炎症及感染性疾病等。
应用场景:需长效、靶向性强或高亲和力等功能需求的结合剂
模型及原理:
RFantibody模型(Nature):模型训练采用蛋白质数据库中已知抗体-抗原复合物结构数据。训练时,向模型提供被“加噪”的抗体结构、靶标3D结构、表位信息以及抗体框架序列和结构模板,在保持框架的完整性情况下使模型去噪过程中专注于设计CDR环和抗体-靶标对接姿态。训练完成后,AI能生成与输入框架匹配、且能针对指定表位形成新型CDR环的抗体结构,再经ProteinMPNN优化CDR区氨基酸序列、微调RoseTTAFold2筛选设计抗体,即可生成原子级精度的抗体结合剂(参考文献:Atomically accurate de novo design of antibodies with RFdiffusion)。
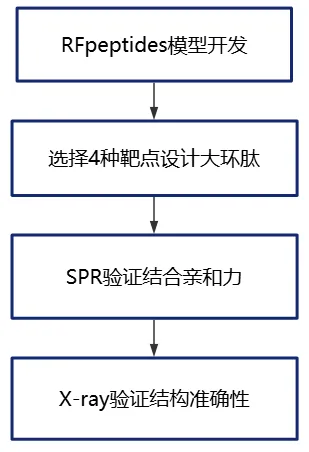
MAGE(Cell)模型:使用包含18,507对抗体-抗原序列对作为训练数据库,对预训练的通用蛋白质语言模型Progen2-base进行微调,使其学习什么样的抗体序列能结合什么样的靶抗原。训练完成后,MAGE模型只需输入靶抗原氨基酸序列,即可生成成对人源重轻链(VH-VL)抗体序列(参考文献:Generation of antigen-specific paired-chain antibodies using large language models)。
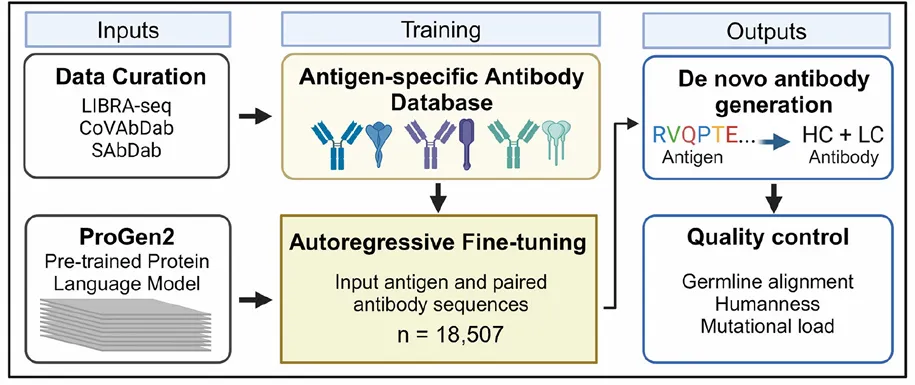
案例—基于靶点的抗体生成+SRP/冷冻电镜验证
传统抗体开发方法依赖动物免疫或噬菌体展示库或大规模随机库筛选,不仅耗时费力,还难以实现对抗原表位的精准识别。2025年11月5日,David Baker团队开发了RFantibody模型,成功设计出针对疾病靶点(流感血凝素、艰难梭菌毒素B等)的VHH和scFv,酵母表面展示、SRP和冷冻电镜证实设计抗体的原子级结构精度和表位特异性。
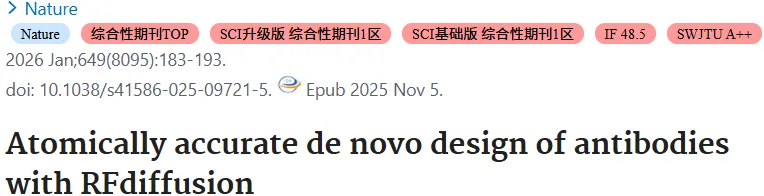
研究思路:
3.基于已知靶点生成酶
酶:生物体内重要的调控工具,广泛应用于食品、医药、化工和环境修复等领域。
应用场景:试剂盒用酶、工业用酶、疾病蛋白水解酶、代谢酶等
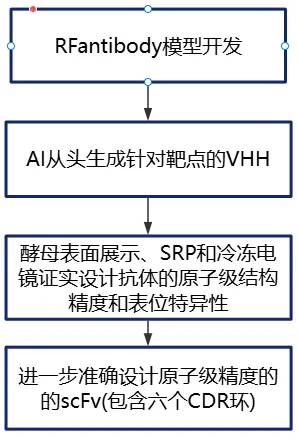
模型及原理:Proteus2模型,整合UniRef50预训练蛋白语言模型与结构解码目标,以蛋白数据库实验结构和AlphaFold2预测结构为训练数据进行双模态基序支架训练,序列和结构条件被视为独立的掩码轨道,利用几何感知的序列语义控制结构生成。给定目标序列和预定义催化基序结构后,基于两步封装策略,模型生成包围催化谷氨酸(负责激活水分子的通用碱)的蛋白质骨架,稳定催化碱基并预包裹底物。随后围绕氧负离子孔构建支架,形成一个夹钳样结构,从而牢牢包裹底物肽段,最大化底物结合特异性。生成骨架后,用LigandMPNN优化蛋白序列,AlphaFold3验证。
案例—基于靶点的金属蛋白酶生成+质谱/FRET验证酶切割位点和催化效率
淀粉样蛋白-β(Aβ)的异常聚集是阿尔茨海默病的核心病理特征,但主流单抗疗法不能直接降解Aβ,且其天然酶底物特异性差,也无法按需改造切割位点。2026年1月6日,西湖实验室人工智能药物设计核心实验室的曹龙兴课题组开发了基于流的生成模型Proteus2,研究针对Aβ病理聚集区的3个特异性切割位点,成功设计并验证了5种高特异性酶(DP720-S1、DP622-S2),催化效率提升10^7倍。该方法可扩展至丝氨酸或半胱氨酸蛋白酶,为阿尔茨海默病治疗提供催化降解新思路,同时推动精准蛋白质操控工具的开发。

研究思路
文章总结
综上所述,AI技术正从根本上改变靶点研究的传统路径,为突破“内卷”困局、跨越转化瓶颈提供了系统性解决方案,包括虚拟筛选、先导化合物优化、难成药靶点PROTAC/DUBTAC开发,以及环肽、抗体、酶等特定功能分子。对于渴望突破研究瓶颈、抢占转化先机的科研团队而言,选择上述AI驱动的研究方向,是通往高分成果与产业落地的高效路径。
集思慧远深耕AI辅助药物开发领域,能够为您提供从靶点分析、虚拟筛选、SRP等分子实验验证、机制解析以及方案设计的全链条专业服务与协作支持。选择我们,让AI赋能您的靶点研究,在生物医药创新赛道上抢占先机、脱颖而出!

往期推荐 ·
IF=44.5 张泽民院士领衔!CRISPR+单细胞技术联手筛选锁定ADAM12靶点调控TGF-β/IFN-I信号轴机制,重塑肿瘤微环境攻克免疫治疗耐药
注:本文原创表明为原创编译,非声张版权,侵删!
关于集思慧远
1.基因/转录/蛋白/代谢/微生物等常规高通量组学及单细胞和空间转录组等时空组学;
2.表观组学:WGBS/Ribo-seq/CUT&Tag/ATAC-seq/Hi-c/m6A/m5C/ac4C等各类修饰)的表观遗传研究,助力新靶点发现、药物作用机制研究及疾病表观调控机制探索;
3.蛋白修饰:磷酸化、乙酰化、泛素化、乳酸化、组蛋白甲基化等修饰
4.专业的医学方案整体设计,利用生物信息学对公共数据进行深入挖掘分析,并提供干湿结合实验;
5.新靶点发现及验证服务,通过ABPP/TPP/DARTS等技术加速小分子药物靶点发现;
6.难成药靶点降解剂开发技术PROTAC;
7.基于AI的药物筛选/设计/优化/抑制剂开发等;
8.无需抗体的临近标记(PLA)技术提供蛋白互作研究。
9.纳米材料递送药物系统开发,定制化纳米载体设计与制备,解决药物靶向递送至病灶组织/细胞等药物递送难题。
 夜雨聆风
夜雨聆风