

关注我们,点亮星标,精彩内容尽在掌握!



研究背景
细胞作为生命体结构与功能的基本单元,其结构、功能与动态生命活动的观测,是阐明生命本质、开展生物医学与病理学研究的核心基础。活细胞大多呈无色透明状态,其关键特征信息主要编码在光波的相位中,而常规成像探测器仅能记录光强振幅,无法直接获取相位分布。早期研究中,荧光染色与化学标记成为细胞结构观测的主要手段,通过特异性染料实现结构对比度增强与动态过程成像。然而,这类方法不仅会因外源性染料干扰细胞正常生理状态,还会因光毒性与光漂白限制成像质量与观测时长,难以满足活细胞长时程、无损伤观测的核心需求[1-3]。
差分相衬显微成像(Differential Phase Contrast, DPC)作为无标记定量相位成像的代表技术,具有鲁棒性强、算法简洁、兼容传统明场显微镜等优势[4-6]。自上世纪80年代发现非对称照明可将相位信息转化为光强衬度后[7],经过数十年的技术迭代与理论完善,2015年Tian等人对DPC进行了系统的理论阐述[8]。传统四帧DPC通过多轴照明优化实现了高质量相位重建,但多帧采集的模式会因高速运动活细胞的形态变化引入严重的运动伪影,大幅降低重构精度。近年来,活细胞动态过程研究的不断深入,推动定量相位成像技术向毫秒级高速成像方向发展,单帧DPC成像也成为领域内的研究热点。
现有单帧DPC技术主要采用多通道复用策略,将多轴照明下的多帧信息编码至单次曝光的不同通道(如波长、偏振),再通过信号分离恢复信息[9-14]。这类方案虽将曝光降至单次,却降低了有效空间分辨率,易引入像素混叠与色串扰,且本质上仍依赖多轴信息复用,存在严重的数据采样冗余。目前,学界尚未从信息论和最小数据冗余角度探明DPC相位重建的理论极限。更关键的是,单帧DPC图像对应的相位传递函数(PTF)在照明对称轴上响应严格为零,会导致该方向相位信息完全丢失,直接反卷积无法实现完整相位重建。如何从信息缺失的单帧输入中实现频谱补全,成为真正意义上实现单帧DPC成像的核心瓶颈。
本文亮点
针对上述难题,研究团队提出了基于支持域约束(Support-Domain Constraint)的单帧差分相衬显微成像技术(SDC-DPC),研究成果以“Single-shot quantitative differential phase contrast microscopy based on support-domain constraint”为题发表于APL Photonics,并被选作Featured Article。
图1 论文被APL Photonics选作Featured Article
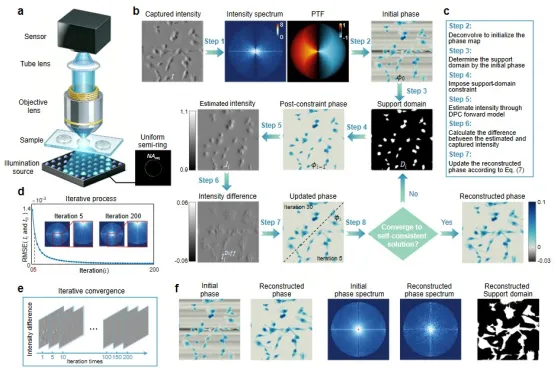
图2 SDC-DPC算法原理流程图。(a)均匀半环照明下的实验装置。(b)SDC-DPC算法的工作流程图。(c)(b)中几个步骤的具体说明。(d)仿真光强与采集光强的RMSE收敛曲线。(e)迭代过程中的光强误差收敛情况。(f)初始输入与重构输出之间的迭代对比
如图2所示,该方法的核心创新在于以下四点:1)单帧重建算法框架:提出了基于支持域约束的单帧差分相衬成像迭代算法,基于物体局部连续与背景相位值为零的先验假设,仅利用传统四帧DPC技术25%的数据量,无需照明复用策略,便实现了单帧曝光下的高精度定量相位重建;2)最优PTF评价体系:建立了适用于单帧DPC的相位传递函数均匀性评价指标,综合考量传递函数的相位信息总量与分布均匀性,通过五种照明模式的系统仿真对比,确定均匀半环照明为单帧DPC的最优照明方案;3)缺失频谱补偿能力:将空域支持域约束引入迭代相位重建框架,有效补偿了单帧PTF固有的频谱零值区域与弱响应信息,解决了单轴照明下的相位信息丢失问题,实现了无方向性伪影的各向同性分辨率成像;4)高速动态成像性能:对未染色HeLa细胞实现了20帧/秒、长达2小时的连续动态观测,可精准捕捉悬浮颗粒3秒内的快速运动轨迹与速度变化,完全消除了传统四帧DPC的多帧运动伪影,静态区域重构精度与四帧DPC几乎一致,且达到了非相干衍射极限的理论分辨率,有望在监测细胞生理过程、药物筛选和病理分析等方面展现出更大的应用潜力。
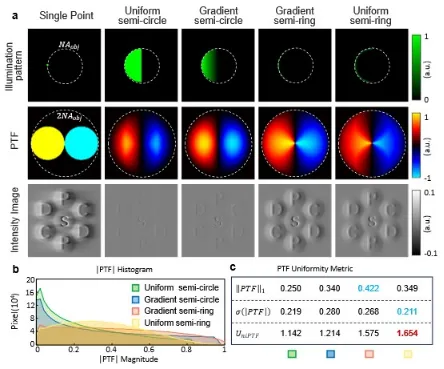
图3 在五种照明模式下的相位传递函数的数值仿真及其均匀性评估。(a)五种照明模式下的光源图案、仿真PTF的模值与相位:单点照明、均匀半圆形照明(半径R)、梯度半圆形照明(半径R)、梯度半环形照明(宽度0.01R)和均匀半环形照明(宽度0.01R)。(b)后四种照明模式下|PTF|幅值的直方图分布。(c)对应PTF的最优化评价指标计算
为优化单帧DPC的相位传递性能,研究团队建立了全新的PTF均匀性评价指标,以求解单帧成像的最佳照明方案。之后,团队针对单点照明、均匀半圆照明、梯度半圆照明、梯度半环照明、均匀半环照明五种模式下的PTF进行了系统数值模拟,结果如图3所示,五种单帧PTF均在非对称轴上响应为零,会导致对应方向相位信息丢失。相较于其他照明模式,均匀半环照明可在提升PTF空间分布均匀性的同时,兼顾低频响应强度与高频信息覆盖,其幅值接近零的像素点最少,可降低解卷积过程对正则化的依赖,避免噪声放大。定量指标计算结果显示,均匀半环照明的均匀性指标值最高(1.675),被确定为单帧SDC-DPC算法的最优照明方案。
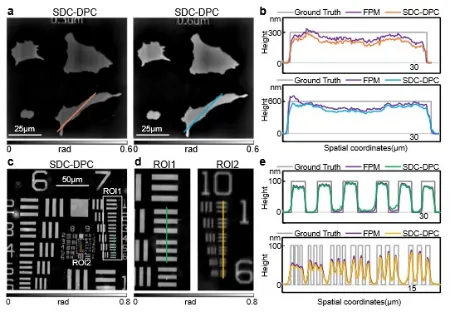
图4 仿细胞模型与纯相位USAF分辨率靶标的实验结果。(a)仿细胞模型的相位成像结果。(b)沿(a)中橙色与蓝色线条所示的相位值分布。(c)纯相位USAF分辨率靶标的相位成像结果。(d)对应(c)中绿色(ROI 1)黄色(ROI 2)线条所示子区域的局部放大图。(e)沿(d)中绿色与黄色线条的相位值分布
随后,研究团队通过细胞仿片与纯相位USAF分辨率靶标开展实验,验证SDC-DPC算法的分辨率性能与成像精度。如图4所示,实验以相同样品下12帧FPM的重构结果作为基准对照,对比发现SDC-DPC的重建结果与基准曲线高度吻合,证明其单帧成像的相位重建质量与多帧FPM基准相当。纯相位分辨率靶标的测试结果显示,SDC-DPC重建图像无方向性伪影与分辨率损失,具备优异的各向同性成像特性,可清晰分辨靶标第10组第4单元的结构,对应的最小可分辨特征尺寸为328nm,精准达到了该成像系统的理论衍射极限分辨率。
最后,研究团队以未染色的人宫颈癌细胞(HeLa细胞)为研究对象,开展了时长2小时、帧率20帧/秒的动态活细胞成像实验,全面验证SDC-DPC的实际应用性能。实验结果如图5所示,SDC-DPC在活细胞静态区域实现了与12帧FPM、四帧DPC相当的重构质量,达到了系统理论分辨率。针对视场内快速运动的悬浮颗粒,四帧DPC出现了严重的运动伪影与形态畸变,而SDC-DPC则精准还原了颗粒的瞬时形态,清晰捕捉到其3秒内的运动轨迹与速度变化。实验证明,基于单帧成像的SDC-DPC方法,可实现活细胞的高分辨率、长时程定量相位成像,在动态生物学观测中具备显著的应用优势。
图5 HeLa细胞在2小时内的SDC-DPC相位重建实验结果。
总结与展望
本研究提出了基于支持域约束的单帧差分相衬相位成像方法SDC-DPC,解决了传统DPC技术依赖多帧采集、难以适配高速动态活细胞成像的核心问题。通过优化的均匀半环照明提升了PTF的均匀性,结合空域支持域约束的迭代重建框架,有效补偿了单帧PTF缺失的频谱信息,仅用传统方法25%的数据量,即可实现无照明复用的单次曝光高帧率定量相位成像。实验结果表明,SDC-DPC在静态样品上实现了与传统四帧DPC相当的重建精度与衍射极限分辨率,针对动态活细胞样品,可完全消除多帧运动伪影,成像帧率提升4倍,结合帧间初始化策略与GPU加速,可实现20帧/秒的实时重建。该方法为动态无标记活细胞显微研究开辟了新的技术路径,有望在细胞生理过程监测、药物筛选、病理分析等领域实现广泛应用。未来,该方法可结合物理驱动的深度学习框架,进一步提升密集样品成像的鲁棒性,拓展其应用场景。
参考文献
[1] Y. Park, C. Depeursinge, and G. Popescu, "Quantitative phase imaging in biomedicine," Nat. Photonics 12, 578-589 (2018).
[2] C. J. Mann, L. Yu, C.-M. Lo, and M. K. Kim, "High-resolution quantitative phase-contrast microscopy by digital holography," Opt. Express 13, 8693-8698 (2005).
[3] G. Popescu, T. Ikeda, R. R. Dasari, and M. S. Feld, "Diffraction phase microscopy for quantifying cell structure and dynamics," Opt. Lett. 31, 775-777 (2006).
[4] M. Chen, L. Tian, and L. Waller, "3D differential phase contrast microscopy," Biomed. Opt. Express 7, 3940-3950 (2016).
[5] B. Seong, I. Kim, T. Moon, M. Ranathunga, D. Kim, and C. Joo, "Untrained deep learning-based differential phase-contrast microscopy," Opt. Lett. 48, 3607-3610 (2023).
[6] Y. Fan, J. Sun, Y. Shu, Z. Zhang, Q. Chen, and C. Zuo, "Accurate quantitative phase imaging by differential phase contrast with partially coherent illumination: Beyond weak object approximation," Photonics Res. 11, 442-455 (2023).
[7] F. Zernike, "How I discovered phase contrast, " Science 121, 345-349 (1955).
[8] L. Tian and L. Waller, "Quantitative differential phase contrast imaging in an LED array microscope," Opt. Express 23, 11394-11403 (2015).
[9] Y. Fan, J. Sun, Q. Chen, X. Pan, M. Trusiak, and C. Zuo, "Single-shot isotropic quantitative phase microscopy based on color-multiplexed differential phase contrast," APL Photonics 4, 121301 (2019).
[10] D. Lee, S. Ryu, U. Kim, D. Jung, and C. Joo, "Color-coded LED microscopy for multi-contrast and quantitative phase-gradient imaging," Biomed. Opt. Express 6, 4912-4922 (2015).
[11] W. Lee, J.-H. Choi, S. Ryu, D. Jung, J. Song, J.-S. Lee, and C. Joo, "Color-coded LED microscopy for quantitative phase imaging: Implementation and application to sperm motility analysis," Methods 136, 66-74 (2018).
[12] Z. F. Phillips, M. Chen, and L. Waller, "Single-shot quantitative phase microscopy with color-multiplexed differential phase contrast (cDPC),"PLOS ONE,12, e0171228 (2017).
[13] S. Liu, C. Zheng, Q. Hao, X. Li, and S. Zhang, "Single-shot quantitative differential phase contrast imaging combined with programmable polarization multiplexing illumination," Opt. Lett. 48, 3559-3562 (2023).
[14] R. Kalita, W. Flanagan, J. Lightley, S. Kumar, Y. Alexandrov, E. Garcia, M. Hintze, M. Barkoulas, C. Dunsby, and P. M. W. French, "Single-shot phase contrast microscopy using polarisation-resolved differential phase contrast," J. Biophot. 14, e202100144 (2021).

团队介绍

南京理工大学智能计算成像实验室(SCILab: www.scilaboratory.com)隶属于南京理工大学光学工程国家一级重点学科带头人陈钱教授领衔的“光谱成像与信息处理”教育部长江学者创新团队、首批“全国高校黄大年式教师团队”。实验室学术带头人左超教授为教育部长江学者特聘教授、国际光学工程学会会士(SPIE Fellow)、美国光学学会会士(Optica Fellow)、英国物理学会会士(IOP Fellow),入选科睿唯安全球高被引科学家。实验室致力于研发新一代计算成像与传感技术,在国家重大需求牵引及重点项目支持下开展新型光学成像的机理探索、工程实践以及先进仪器的研制工作,并开拓其在生物医药、智能制造、国防安全等领域的前沿应用。研究成果已在SCI源刊上发表论文300余篇,其中53篇论文被选作Light、Optica、AP、PhotoniX等期刊封面论文,30篇论文入选ESI高被引/热点论文,论文被引2.3万余次。获中国光学工程学会技术发明奖一等奖、江苏省科学技术奖基础类一等奖、日内瓦国际发明展“特别嘉许金奖”等。培养研究生7人获全国光学工程优秀博士论文/提名奖,6人获中国光学学会王大珩光学奖,10人入围Light全国光学博士生学术竞赛全国百强,获“挑战杯”、“创青春”、“研电赛”全国金奖十余次,“互联网+”全国总冠军。师生双创事迹得到央视《焦点访谈》、人民网、新华网、光明日报、中国教育电视台等百余家媒体报道,社会辐射影响广泛。

文章信息
Single-shot quantitative differential phase contrast microscopy based on support-domain constraint
Tingxiang Xiong, Yefeng Shu, Ran Ye, Maciej Trusiak, Malgorzata Kujawinska, Jiasong Sun, Yao Fan, Chao Zuo
APL Photonics 11, 046107 (2026)
https://doi.org/10.1063/5.0314921

扫描二维码 查看原文

期刊介绍
APL Photonics促进以光子学为基础的基础性、应用性和多学科研究。通过强大的编辑流程,我们的目标是出版高质量的研究成果,代表重大的突破、新的理解、或具有长期影响的前瞻性文章。我们的使命是为国际光子学和更广泛的学术共同体提供公开访问的资源。
关于AIP出版社
美国物理联合会出版社(AIP 出版社)是美国物理联合会(AIP)旗下的非营利独资出版社。AIP 出版社的使命是在物理和相关科学领域开展学术出版活动,以支持AIP的慈善、科学和教育目标。我们也代表出版合作伙伴进行出版活动,以帮助其积极推进自身的使命。
访问主页:https://publishing.aip.org/
相关文章推荐
APP | 南京邮电大学王永进教授团队:氮化镓通感一体化全光芯片
 夜雨聆风
夜雨聆风