▼ 做您定制的类似分析,请与刘老师联系。
不做实验,也能发IF10+SCI?正在悄悄流行的文献计量分析,不仅是“论文捷径”,更是“基金申请外挂”!

引言
癌症仍然是全球最严峻的公共健康挑战之一,2022年全球新发病例约2000万例,死亡人数达970万例。预计到2050年,年发病人数可能超过3500万例,死亡人数将达到1800万例。尽管手术、化疗和放疗等传统治疗手段在一定程度上提高了患者生存率,但许多癌症——尤其是实体肿瘤——仍难以治愈,这主要归因于肿瘤的免疫逃逸、转移扩散以及对常规治疗的耐药性。在此背景下,治疗性癌症疫苗作为一种有前景的策略逐渐受到关注,其目标是激活机体免疫系统以识别并清除恶性肿瘤细胞。然而,尽管经过数十年的研究,癌症疫苗的临床转化仍面临诸多挑战,包括抗原递送效率不足、免疫原性较弱以及向淋巴组织迁移能力有限等问题。
纳米技术为解决这些关键瓶颈提供了变革性思路。纳米材料具有尺寸可调、表面性质可控及结构模块化等特性,可用于优化抗原稳定性、增强抗原呈递细胞(APCs)的摄取能力,并协同递送佐剂以增强免疫反应。脂质纳米颗粒(LNPs)、聚合物胶束、树枝状大分子以及无机纳米结构等平台能够精确调控药物释放动力学,并可通过功能化修饰实现对特定免疫细胞亚群的主动靶向。值得注意的是,脂质纳米颗粒包裹的mRNA疫苗在抗击严重急性呼吸综合征冠状病毒2(SARS-CoV-2)中的里程碑式成功,极大推动了类似纳米平台在癌症免疫治疗中的应用探索,加速了早期临床试验的开展(见原文表1)。近年来的研究进展还包括基于新抗原的个体化纳米疫苗、类病毒颗粒支架以及融合光热治疗与免疫激活的混合系统,体现了纳米技术与肿瘤免疫学日益深入的融合。
尽管该领域呈现出爆发式增长,但基于纳米材料的癌症疫苗研究具有高度跨学科和分散性的特点,涉及材料科学、肿瘤免疫学、药物工程及生物信息学等多个领域。这种碎片化特征带来了诸多挑战:研究者往往局限于各自的细分领域开展工作,缺乏对全球研究趋势的系统性与全景式认知,从而阻碍了对新兴热点、核心研究者及潜在合作机会的识别。现有综述虽然具有一定价值,但通常聚焦于特定技术或治疗方向,难以提供对该领域随时间演变过程及未来发展方向的定量、纵向解析。
在本研究中,我们基于 Web of Science 核心合集(WoSCC)数据库,对2000年至2024年间纳米材料基癌症疫苗研究进行了系统的文献计量与趋势分析。通过整合共被引分析、关键词突现检测、合作网络构建及时间线可视化等方法,系统刻画了该领域在结构与时间维度上的演化过程。本研究作为首个针对纳米材料基癌症疫苗的综合性文献计量与可视化分析,利用先进的可视化技术揭示其主题演进与临床转化路径。研究结果为科研人员、临床医生及政策制定者提供了重要参考,有助于推动科学研究与临床应用的协同发展。

该文2026年发表于International Journal of Surgery,最新JCR影响因子(2025发布,2024数据):约 8–10(常见≈8+), JCR: Q1
▼ 想发表自己的文献计量分析论文?点击👇获得更多高质量文献计量分析模板。

(👆经典文献计量分析模板,持续更新中)
以下分为三个方面进行解读。
一. 检索策略
1. 数据收集与检索策略
本研究采用预设检索策略,对 WoSCC 数据库进行系统性检索,检索式如下:
TS =(nanodot* OR nanoparticle* OR nanomaterial* OR nanotube* OR nanosheet* OR “quantum dot” OR nanofiber OR nanosphere* OR nanorod* OR nanocrystal* OR nanocomposite* OR nanodevice* OR nanocluster* OR nanotechn* OR nanocarrier* OR nanowire* OR nanoliposome* OR nanoemulsion* OR nanoconjugate* OR nanogels* OR nanodiamond* OR nanoporou* OR nanosilver* OR nanopore* OR nanomicell* OR nano size* OR nanomedicine* OR nanofibrou)AND TS =(“Tumor” OR “Neoplasm” OR “Tumors” OR “Neoplasia” OR “Neoplasias” OR “Cancer” OR “Cancers” OR “Malignant Neoplasm” OR “Malignancy” OR “Malignancies” OR “Malignant Neoplasms” OR “Neoplasm, Malignant” OR “Neoplasms, Malignant” OR “Benign Neoplasms” OR “Benign Neoplasm” OR “Neoplasms, Benign” OR “Neoplasm, Benign”)AND TS =(“Vaccine” OR “vaccination*”)。
本研究设定检索时间范围为2000年1月1日至2024年6月30日。仅纳入英文发表的同行评议论文(articles)及综述(reviews)。
2. 文献计量分析工具
本研究运用 CiteSpace 和 VOSviewer 软件以及 HistCite 提供多项关键指标用于评估文献影响力。此外,Alluvial 流图是一种用于展示类别间关系及演变过程的可视化方法,适用于时间序列或多维数据分析。
二.主要结果
1. 发文分布
科学文献的时间演化能够定量反映各研究领域的知识积累过程,为评估学科发展提供关键指标。本研究通过系统检索,共纳入3910篇关于纳米材料基肿瘤疫苗的相关文献,其中包括2415篇研究论文和1495篇综述文章,涉及15,863位作者、3265家研究机构,发表于720种期刊,覆盖98个学科类别。
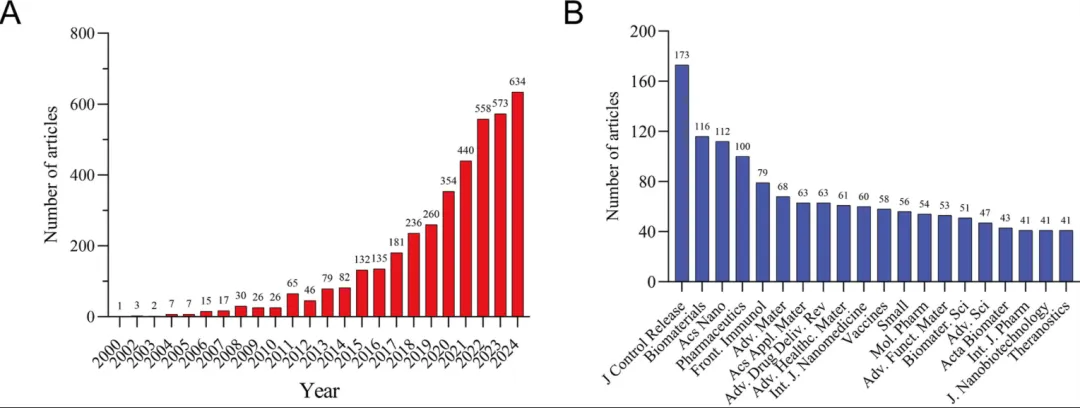
年度发文量变化趋势如图1A所示。2000年仅有1篇关于纳米材料基癌症疫苗的文献发表,2001年增至3篇。在2000年至2010年期间,该领域发文量较低,年均约13.4篇。自2011年至2019年进入稳步增长阶段;2020年以后发文数量进一步加速增长,并于2024年达到峰值,共计634篇。
如图1B所示,Journal of Controlled Release 以173篇发文量位居首位,其次为 Biomaterials(116篇)和 ACS Nano(112篇)。图中展示了该领域发文量排名前20的期刊,可为研究人员在选择投稿期刊时提供重要参考。
2. 共被引网络分析
共被引网络分析揭示了2000—2024年间纳米材料基癌症疫苗原始研究的知识演化过程(图2)。该网络由1296个节点和5876条连线构成,显示出该领域内高度紧密的学术关联性。
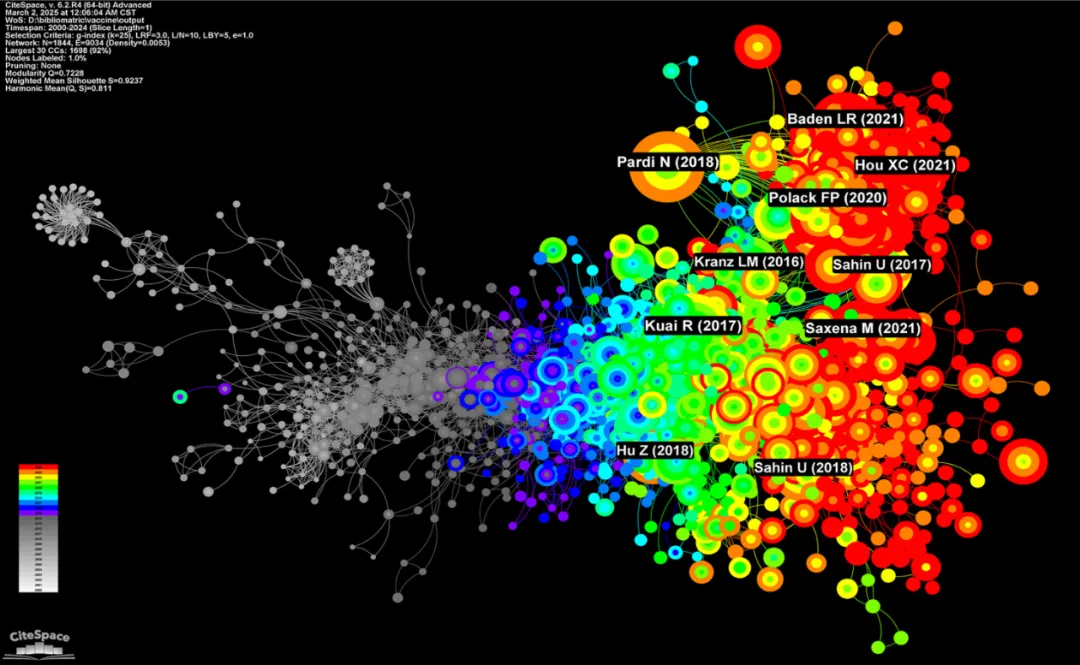
基于时间维度分析,可将该领域的发展划分为三个阶段:
- 奠基阶段(2000—2010年,灰色节点)
:网络连接最为密集,节点度分布最高,构成该领域的概念基础; - 分化阶段(2011—2017年,蓝色节点)
:随着网络模块化程度的提高,研究逐渐呈现出专业化分支; - 成熟阶段(2018—2024年,彩色节点)
:形成了清晰的研究聚类与显著的群体结构,体现出学科专业化与跨学科融合并存的发展特征。
共被引分析进一步识别出10篇具有代表性的关键文献,这些研究因其较高的引用频次而对纳米材料基癌症疫苗领域产生了重要影响,构成了该领域的知识核心。这些研究群体之间的融合与分化特征将在后续的时间线分析中进一步呈现。表2(此处只显示原文表格中的部分)列出了该领域最具影响力的里程碑式文献。其中,被引频次最高的三篇代表性研究包括:
“Designer vaccine nanodiscs for personalized cancer immunotherapy” “A STING-activating nanovaccine for cancer immunotherapy”[50] “Cancer Cell Membrane-Coated Nanoparticles for Anticancer Vaccination and Drug Delivery” 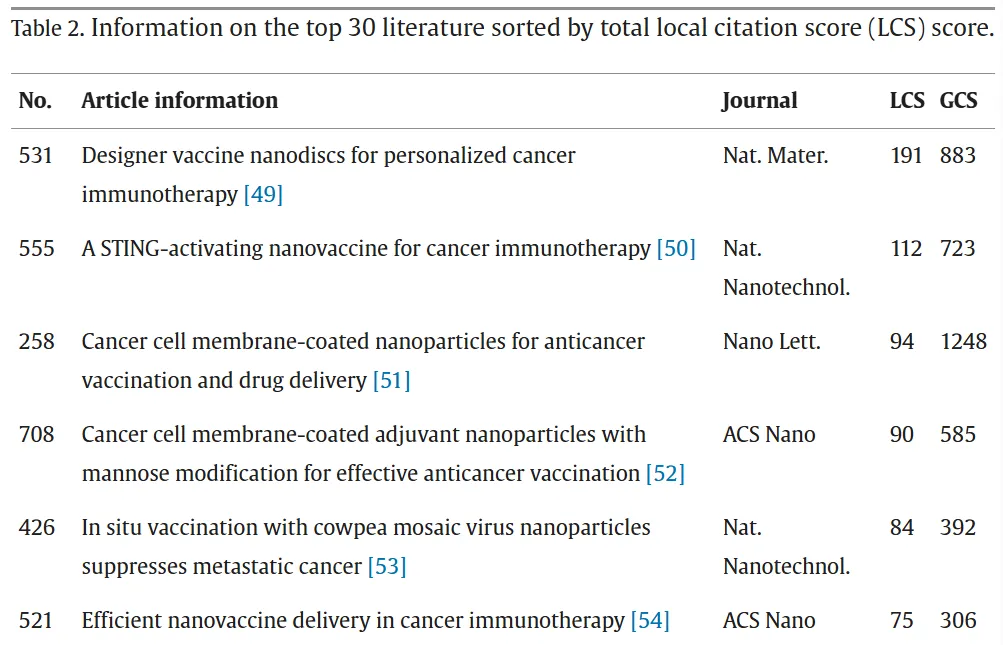
这些高被引研究共同塑造了癌症纳米疫苗领域的发展格局。其中,基于纳米盘(nanodisc)的平台实现了个体化新抗原递呈并诱导持久的T细胞免疫反应;STING激活型纳米疫苗显著增强了先天免疫与适应性免疫反应;而肿瘤细胞膜包裹纳米颗粒则通过整合抗原呈递与药物递送,实现了多功能一体化设计。总体而言,这些研究确立了癌症疫苗开发中的关键范式,即个体化设计、先天免疫激活以及多功能递送系统的协同融合。
3. 科学合作
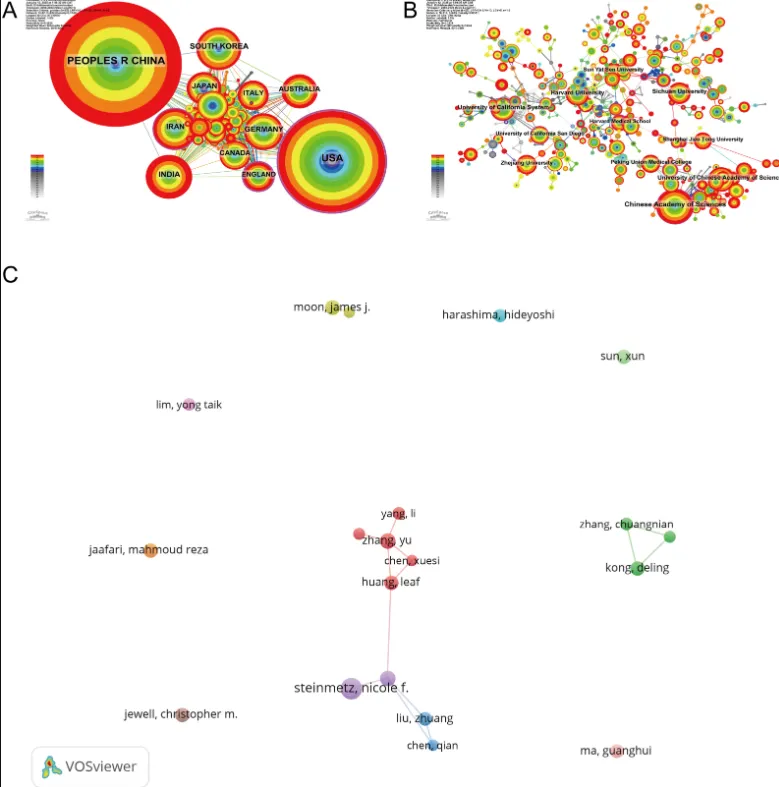
图3展示了在国家、机构及作者层面的广泛科研合作关系,表现为节点与连线构成的密集网络结构。
国际合作网络(图3A)由87个国家和652条合作连线构成,其中中国、美国、印度、韩国和伊朗是最活跃的参与者。中国在纳米材料基癌症疫苗领域的发文量位居首位,而美国在国际合作强度方面处于领先地位。值得注意的是,中美合作构成了国际科研合作网络的核心,体现了中国在该领域的重要贡献及其日益增强的全球影响力。
在机构层面(图3B),合作网络包含516个研究机构及675条合作关系,其中中国科学院处于主导地位,其次为加利福尼亚大学系统、中国科学院大学和四川大学。
作者合作网络(图3C)则揭示了该领域的核心研究者群体。补充材料表S1列出了按共现频次排名的前10个国家、机构及作者。
4. 引文突现分析
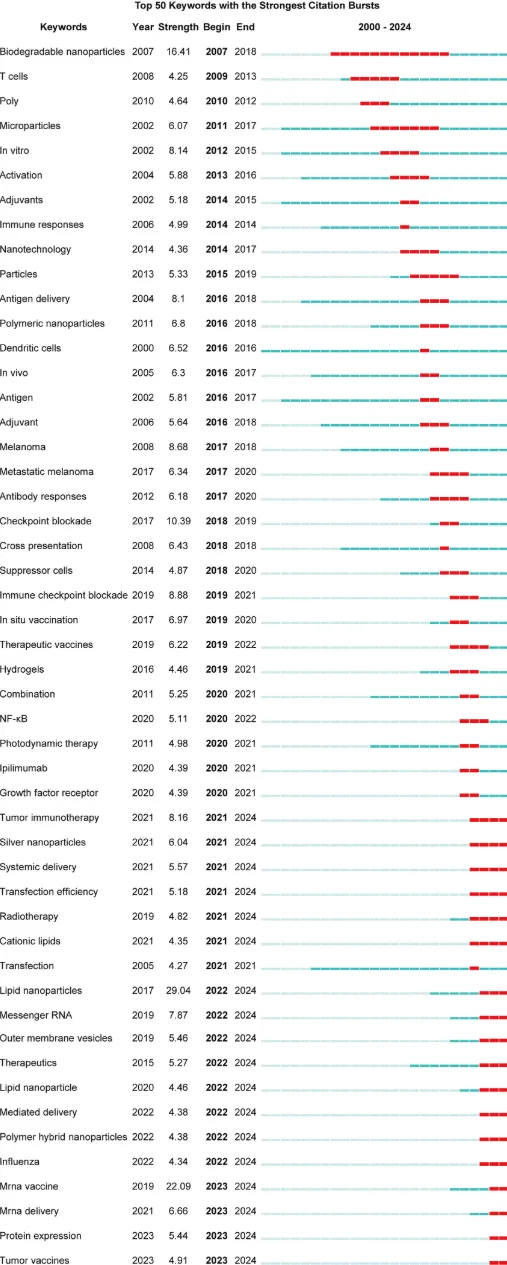
2000年至2024年的引文突现分析显示,在98个相关学科中,有90个学科呈现出显著的研究活跃度(图4)。在时间可视化图中,蓝色线段表示整个研究时间范围,而红色线段表示引文突现阶段,并标注其起止时间。
按时间顺序列出的引文突现强度最高的前50个学科中,“生物化学研究方法(Biochemical Research Methods)”在2018—2019年期间表现出最强的突现强度(强度=5.7)。值得注意的是,引文突现模式随时间推移呈现出学科多样性不断增加的趋势,具体表现为以下学科的阶段性突现:
生物化学与分子生物学(2004—2005年) 内分泌与代谢(2007—2011年) 传染病学(2010—2015年) 遗传学与遗传(2017—2018年) 放射学、核医学与医学影像(2020年) 公共、环境与职业健康(2023—2024年)
这一时间演化过程表明,该研究领域正呈现出日益增强的多学科交叉特征。
最新数据(2024年)显示,共有20个学科仍处于引文突现活跃期(见表S2),其中以“仪器与仪表(Instruments & Instrumentation,2022—2024年)”、“公共、环境与职业健康(2023—2024年)”以及“分析化学(Chemistry Analytical,2022—2024年)”为代表。
这些突现不仅反映了方法学创新的不断涌现,也体现了该领域临床相关性的持续增强。总体来看,这些变化表明,纳米材料基癌症疫苗研究正从以实验室基础研究为主,逐步向更广泛的转化研究及群体健康应用方向发展。
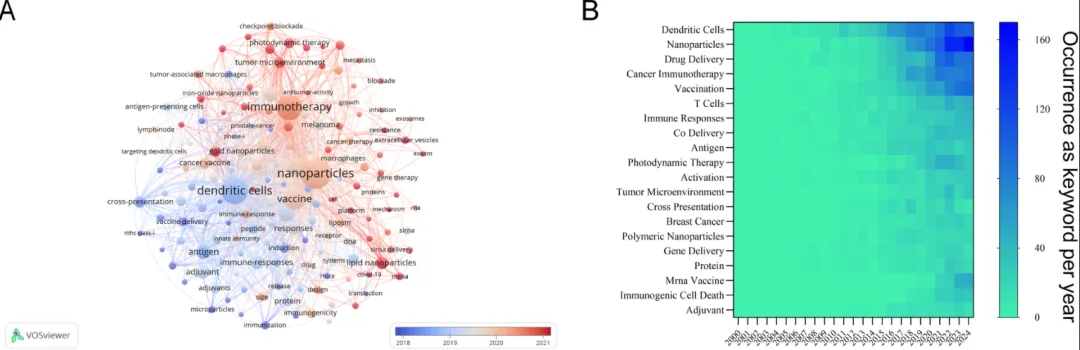
关键词时间线分析共识别出154个高度相关的关键词,这些关键词来源于文献中的关键词字段,并进行了可视化展示(图6A)。通过由蓝色—灰色—红色构成的颜色渐变表示关键词的平均出现年份,从而反映过去二十年癌症疫苗研究的时间演化过程。
在出现频率最高的前20个关键词中,2015年之前整体出现频率较低,此后呈现逐步上升趋势,尤其是在2020年之后增长更加明显(图6B)。值得注意的是,“树突状细胞(dendritic cells)”、“纳米颗粒(nanoparticles)”、“mRNA疫苗(mRNA vaccine)”以及“癌症免疫治疗(cancer immunotherapy)”等关键词的关注度显著提升,凸显其在当前研究发展中的核心地位。
6. 参考文献突现分析
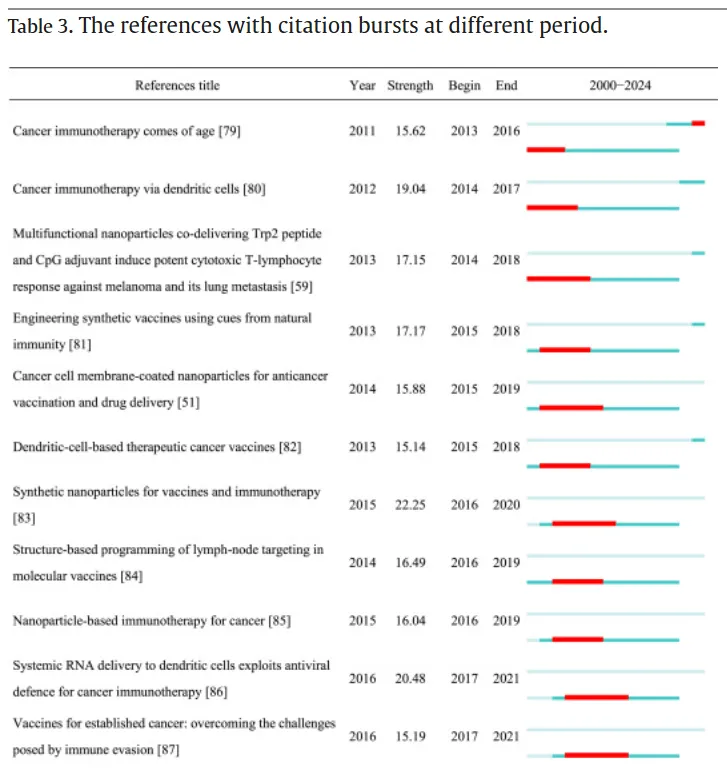
本研究的文献计量分析在2000—2024年期间共识别出1295篇具有显著引文突现的文献。表3(原文表格中的部分)列出了被引频次最高的前30篇文献,并按总引用次数进行排序。这些具有代表性的研究构成了纳米材料基癌症疫苗领域的知识基础,其引文突现强度范围为14.41至29.08。
总体而言,这些关键文献显著推动了癌症疫苗领域的发展。相关研究阐明了树突状细胞与新抗原在抗肿瘤免疫反应中的核心作用,从而为疫苗的理性设计提供了重要理论框架。同时,mRNA技术平台与纳米材料递送系统的进步显著提升了抗原递呈效率与免疫原性,加速了癌症疫苗从机制研究向临床应用转化的进程。
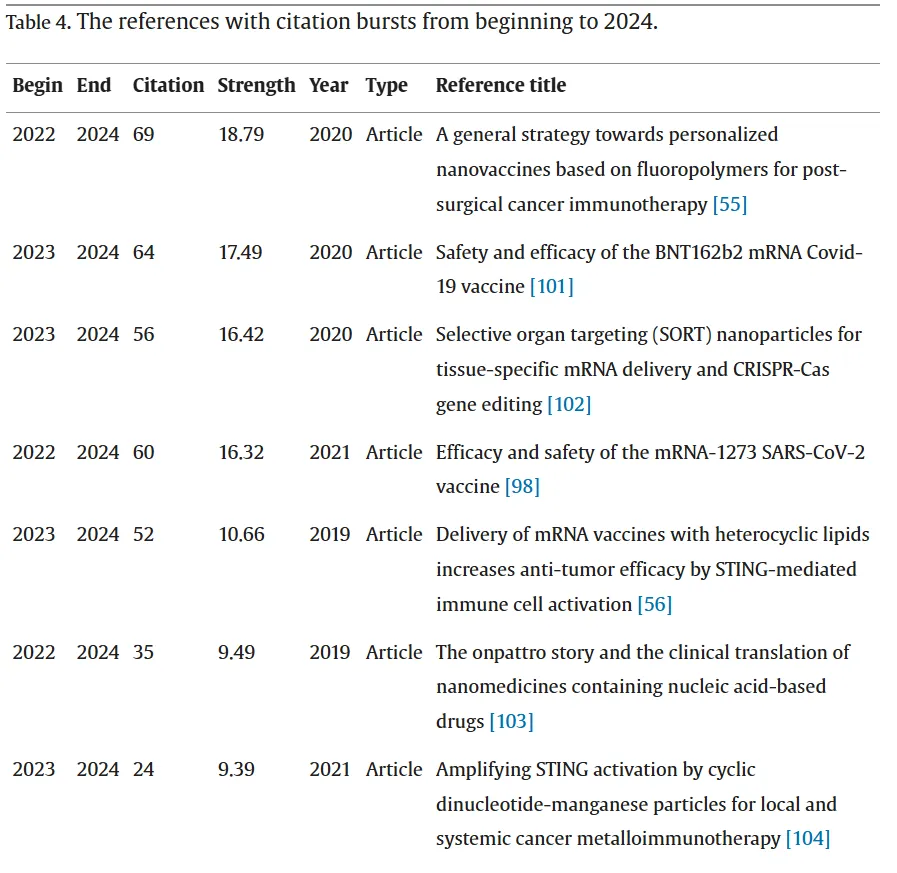
我们的分析自2024年以来共识别出345篇引文突现文献,表4(原文表格中的部分)列出了按突现强度指数排序的前20篇原创研究论文。值得注意的是,这些文献几乎在发表后即进入引文突现阶段(通常为发表后1–2年内)。
这些近期出现引文突现的研究反映了癌症纳米疫苗领域的前沿进展。多种新型平台不断涌现,包括氟聚合物体系、肿瘤细胞膜包裹纳米颗粒、DNA纳米器件以及个体化新抗原疫苗等,均表现出在增强抗原递呈、逆转免疫抑制以及诱导持久T细胞免疫反应方面的显著优势。
与此同时,前沿递送技术也在不断发展,例如器官选择性纳米颗粒、靶向淋巴结的脂质纳米颗粒(LNPs)以及新一代脂质材料,这些技术显著提升了组织特异性与免疫原性。此外,mRNA疫苗及核酸纳米药物的临床验证,以及先天免疫通路的激活,共同加速了其在肿瘤学领域的临床转化潜力。
7. 关键词共现分析
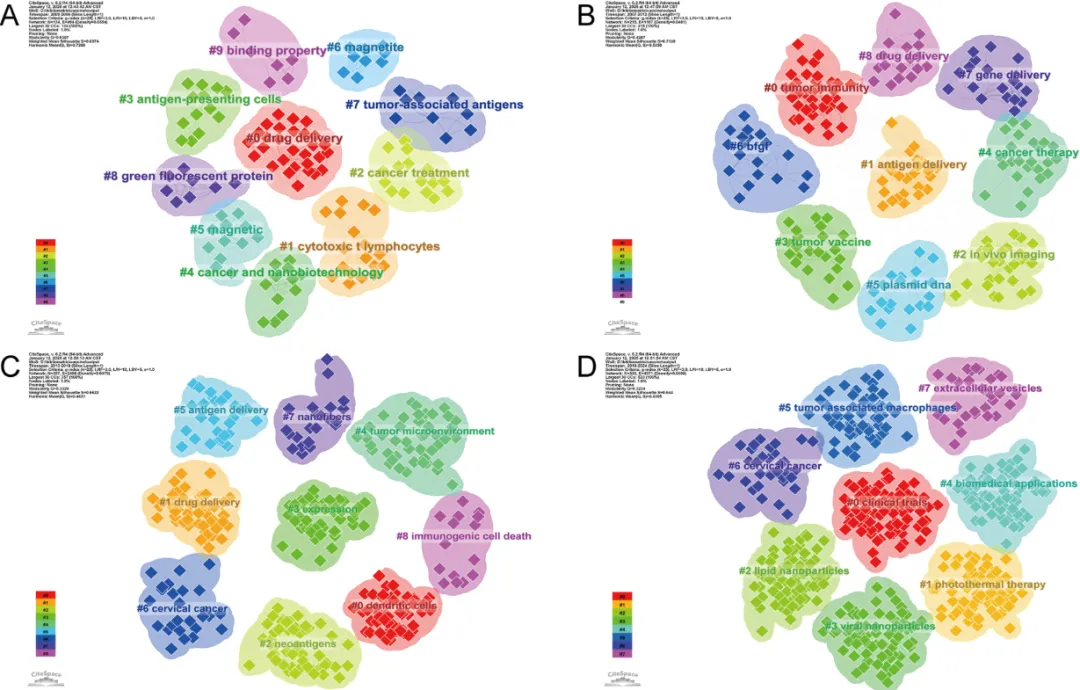
关键词共现分析揭示了该研究领域内的重要概念关联,有助于识别纳米材料基癌症疫苗研究中的关键主题聚类,从而界定各主要研究子领域。基于时间维度,本研究将过去二十年的发展划分为四个五年阶段(图7)。
在初始阶段(2000–2006年,共35篇文献)中,共识别出10个聚类,包括#0“药物递送(drug delivery)”、#1“细胞毒性T淋巴细胞(cytotoxic T lymphocytes)”以及#2“癌症治疗(cancer treatment)”(图7A)。
随后各阶段呈现出指数级增长:
- 2007–2012年(210篇文献)
:形成9个聚类,包括#0“肿瘤免疫(tumor immunity)”、#1“抗原递送(antigen delivery)”、#2“体内成像(in vivo imaging)”(图7B); - 2013–2018年(845篇文献)
:同样形成9个聚类,主要包括#0“树突状细胞(dendritic cells)”、#1“药物递送(drug delivery)”以及#2“新抗原(neoantigens)”(图7C); - 最新阶段(2019–2024年,2819篇文献)
:形成8个聚类,突出显示了新兴研究热点,如#0“临床试验(clinical trials)”、#1“光热治疗(photothermal therapy)”以及#2“脂质纳米颗粒(lipid nanoparticles)”(图7D)。
尽管“药物递送”和“纳米生物技术”等长期研究主题持续存在,但“病毒纳米颗粒”、“肿瘤相关巨噬细胞”以及“细胞外囊泡”等新兴研究方向正迅速发展并获得广泛关注。
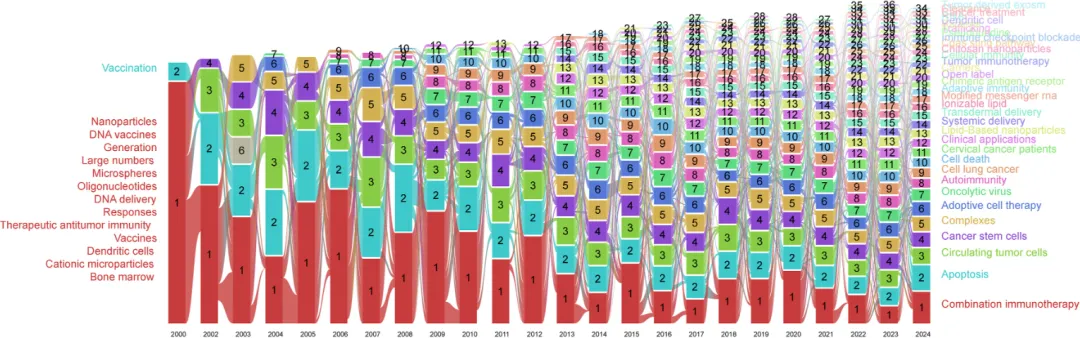
8. 关键词冲积流可视化分析
图8展示了基于关键词共现模式的研究模块动态重组过程,揭示了不同主题聚类如何随着时间推移通过分化与融合不断演化。
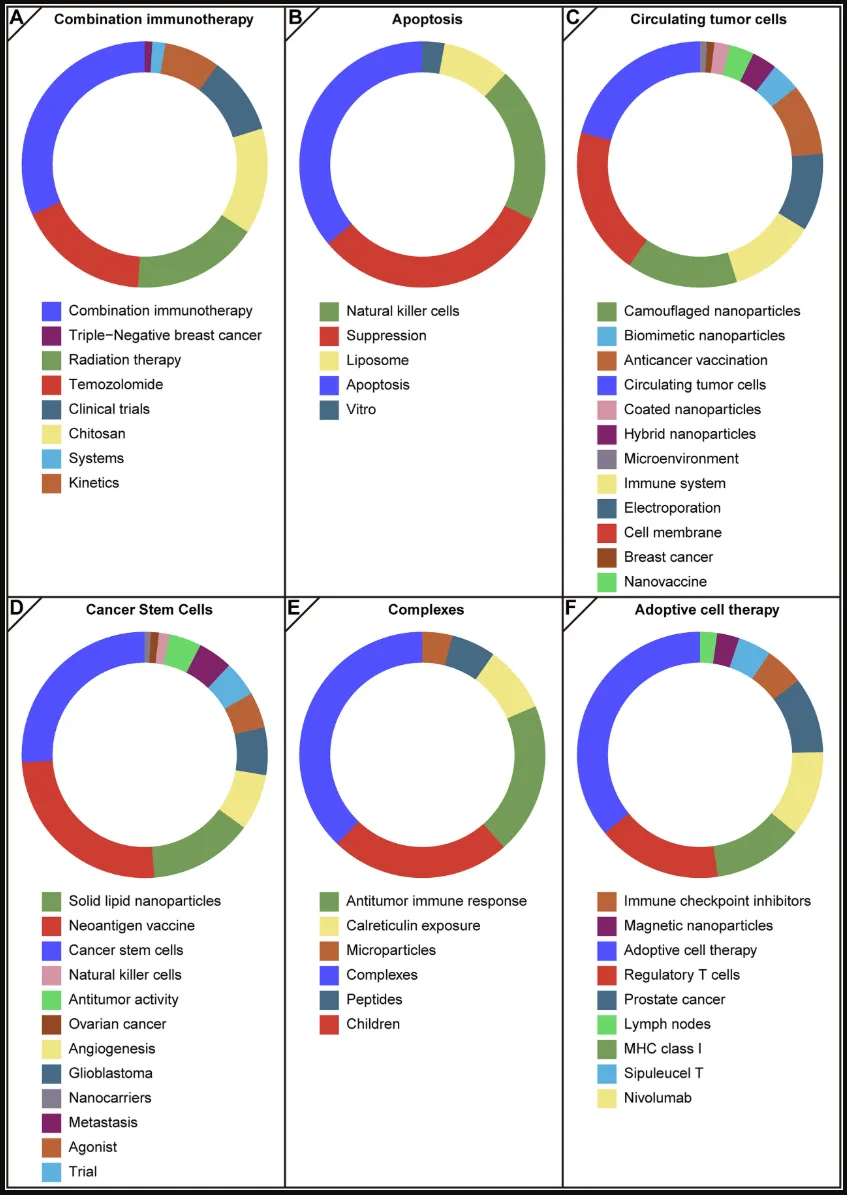
本研究识别出2024年的六大主导研究模块(图9):
- 联合免疫治疗(Combination immunotherapy)
(替莫唑胺、放疗、壳聚糖;8个关键词),显示出持续的临床转化潜力; - 凋亡调控(Apoptosis regulation)
(NK细胞、脂质体;5个关键词),反映了对程序性细胞死亡机制的持续关注; - 循环肿瘤细胞靶向(Circulating tumor cell targeting)
(伪装纳米颗粒、电穿孔;12个关键词),代表新兴的精准递送策略; - 肿瘤干细胞策略(Cancer stem cell strategies)
(新抗原疫苗、胶质母细胞瘤;12个关键词),强调应对肿瘤异质性的研究方向; - 分子复合体系(Molecular complexes)
(儿科应用、钙网蛋白;6个关键词),体现了专门化制剂开发趋势; - 过继性细胞治疗(Adoptive cell therapy)
(纳武利尤单抗、前列腺癌;9个关键词),展示了免疫检查点治疗的协同效应。
这些研究模块,尤其是在**联合治疗策略(模块1与模块6)以及靶向递送系统(模块3与模块4)**方面的融合趋势,预计将在未来数年(至2029年)持续引领纳米材料基癌症疫苗研究的发展方向,因为它们有望解决治疗耐药性及肿瘤微环境调控等关键问题。
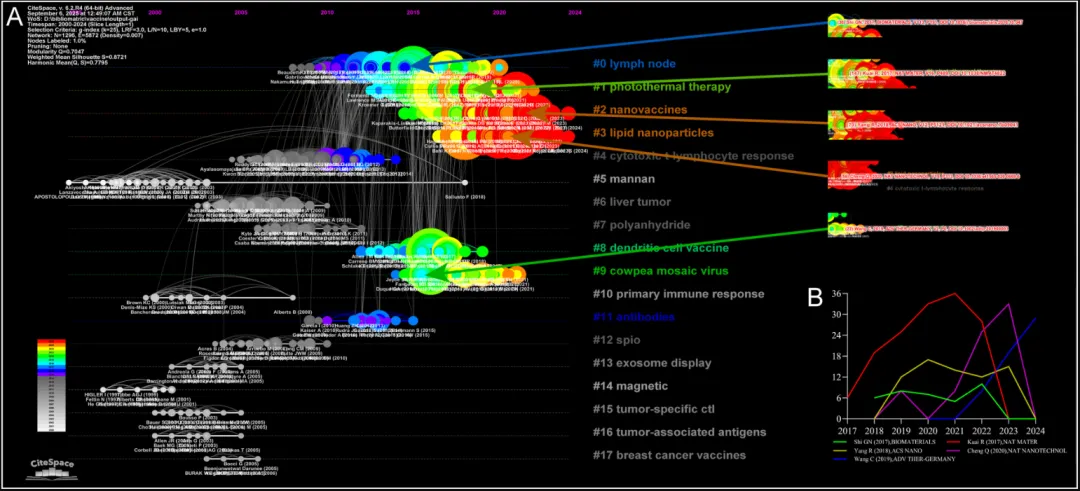
9. 参考文献时间线可视化分析
基于引文时间跨度构建的时间线可视化,为区分新兴主题、经典主题及衰退主题提供了系统性分析框架。在纳米材料基癌症疫苗研究领域中,时间图谱(图10A)共包含18个聚类,并按规模由大到小排列。
其中,经典研究主题包括聚类#4(细胞毒性T淋巴细胞反应)、#8(树突状细胞疫苗)以及#11(抗体)。尽管这些方向已不再处于研究前沿,但由于其在不同研究聚类之间具有广泛的连接性,仍然作为重要的知识基础发挥作用。
相比之下,聚类#5(甘露聚糖)、#7(聚酸酐)、#13(外泌体展示)以及#14(磁性相关研究)代表逐渐衰退的研究方向,其特征为跨聚类联系较弱且缺乏持续的发展动力。
与此同时,聚类#0(淋巴结)、#1(光热治疗)、#2(纳米疫苗)、#3(脂质纳米颗粒)以及#9(豇豆花叶病毒)被识别为新兴研究前沿。这些方向自出现以来持续保持活跃,并展现出较强的发展潜力,有望引领未来研究趋势。相关新兴聚类的详细信息见表S5。
此外,一些关键性文献(以大红色圆圈节点表示)在网络中作为引文枢纽(图10B)发挥重要作用,具有持续的跨学科影响力,并推动各研究子领域的演化与发展。
三. 讨论
1. 纳米材料重塑癌症免疫反应级联
从机制层面来看,关键词与共被引分析表明,纳米材料通过在免疫反应级联的多个关键环节进行干预,彻底改变了癌症疫苗的设计模式。传统癌症疫苗常存在抗原稳定性差、免疫原性不足以及向次级淋巴器官迁移能力有限等问题,从而限制其诱导强效且持久抗肿瘤免疫反应的能力。纳米载体凭借其可调控的理化特性(如粒径、形状、表面电荷及生物降解性),能够实现对体内分布、细胞摄取及胞内处理过程的精准调控。
纳米载体最重要的优势之一在于其能够显著提高肿瘤相关抗原(TAAs)或新抗原的稳定性与生物利用度。通过保护抗原肽或核酸免受体内酶降解,纳米载体可延长抗原半衰期并提高递送效率。这一点对于mRNA疫苗尤为关键,因为其本身极不稳定,必须依赖脂质纳米颗粒(LNPs)包裹以实现有效递送。文献计量分析亦证实了这一趋势:“脂质纳米颗粒”在近年关键词突现中强度最高(29.04,2022–2024),而“mRNA疫苗”排名第二(22.09,2023–2024),表明LNP递送体系已成为2020年后的主导研究前沿。
除稳定作用外,纳米载体还可促进抗原靶向递送至抗原呈递细胞(APCs),尤其是树突状细胞(DCs),从而启动适应性免疫反应。常见策略包括利用甘露糖、抗DEC-205抗体或适配体等配体修饰纳米颗粒表面,实现对DC特异性受体的靶向结合。纳米疫苗被摄取后进入内体,经主要组织相容性复合体(MHC)I类与II类途径递呈抗原,从而同时激活CD8+细胞毒性T细胞与CD4+辅助T细胞,形成协同抗肿瘤免疫反应。研究表明,壳聚糖或PLGA纳米颗粒可显著增强DC成熟与抗原呈递能力,提高干扰素γ分泌及效应T细胞肿瘤浸润水平。文献计量结果中“树突状细胞”持续突现并作为核心节点出现,也进一步印证了其基础性作用。
刺激响应型纳米平台是另一重要前沿,其能够响应肿瘤微环境(TME)中的特定信号(如酸性pH、高谷胱甘肽、基质金属蛋白酶及活性氧)实现精准释放。此类系统在体循环中保持稳定,而在肿瘤或淋巴组织中被激活,从而提高时空靶向性并减少脱靶效应。例如,利用氧化还原敏感或pH敏感材料可实现抗原与佐剂的定向释放,从而增强免疫激活并克服肿瘤免疫抑制。
多功能纳米平台的代表性研究包括:
Kuai等开发的类HDL纳米盘,可高效递送新抗原并诱导强烈CD8+ T细胞反应; Luo等提出的STING激活型纳米疫苗,可桥接先天与适应性免疫并增强免疫检查点治疗效果。
这些研究不仅机制意义重大,也在共被引分析中占据核心地位,构成该领域的知识支柱。
此外,联合治疗策略日益受到关注,如纳米疫苗联合免疫检查点抑制剂、TLR激动剂或光热/光动力治疗等,实现“原位疫苗化”效应。近年来出现的混合纳米结构整合了靶向递送、抗原呈递及微环境调控,体现出系统级免疫调控设计理念。
2. 转化前景与发展方向
尽管LNP平台在当前研究中占据主导地位,但其过度集中可能限制技术多样性。病毒样颗粒(VLPs)、自组装肽、纳米凝胶及DNA纳米结构等替代体系在免疫模拟及安全性方面具有独特优势,但仍处于较早期阶段。
文献计量分析还显示,该领域科研合作呈现明显区域化特征,国际协作不足,尤其是中西方之间合作有限。这种碎片化限制了标准化体系的建立与临床转化进程。
此外,尽管前临床研究迅速增长,但进入后期临床阶段的研究较少,主要瓶颈包括:
制备复杂、难以规模化 批间稳定性差 GMP生产成本高 纳米特性难以标准化控制
监管层面亦存在挑战:现有疫苗规范难以适配纳米体系,缺乏统一评价标准,影响IND审批与产业投资。
3. 未来纳米疫苗创新战略路径
未来发展可从五个关键方向推进:
1️⃣ 人工智能驱动疫苗设计
AI/机器学习可用于抗原预测、纳米材料设计及免疫反应模拟,加速疫苗开发流程。
2️⃣ 模块化纳米平台
“即插即用”设计可实现抗原、佐剂与递送系统灵活组合,适应个体化治疗需求。
3️⃣ 肿瘤微环境响应系统
开发对TME敏感的纳米疫苗,实现精准释放与免疫激活。
4️⃣ 全球监管与标准统一
建立纳米疫苗专属评价体系与国际标准,促进临床转化。
5️⃣ 国际合作与资源整合
推动跨国协作,如中美联合开发模式,以实现优势互补与加速转化。
编者按
纳米材料基癌症疫苗正处于由机制探索迈向临床转化的关键阶段。未来研究亟需在“多学科融合”与“可转化性”之间实现平衡。一方面,应加强对肿瘤微环境、免疫调控网络及抗原递呈机制的系统整合,推动从单一功能纳米平台向多功能协同系统转变,实现递送、激活与调控的一体化设计。另一方面,需突破当前转化瓶颈,重点关注规模化制备、质量一致性及标准化评价体系的建立,以提升临床可行性。
同时,人工智能与数据驱动方法有望重塑疫苗设计范式,通过精准筛选新抗原、优化纳米结构及预测免疫反应,加速研发流程。此外,应强化跨区域与跨学科合作,推动数据共享与国际标准统一,减少重复研究并提升整体效率。未来的发展不仅取决于技术创新,更依赖于工程化能力与协同体系的构建。唯有实现从“概念验证”到“临床落地”的跨越,纳米疫苗才能真正释放其在肿瘤免疫治疗中的潜力。
原文链接:
广而告之:
如果您也需要对自己公司的产品或者对自己研究的领域做系统梳理,可以找美国Healsan恒祥医学科技做文献计量分析。并可同时获赠五个仅Healsan™大数据才有的福利:
文献检索老师参与学员选题的文献检索; 完成分析后,免费使用SCI论文神器10天,以完成论文撰写; 作者撰写好之后,获得免费查重; 作者投稿前,获得免费的选刊服务。

(点击👆,获得持续的医学大数据分析报告)
 |  |
 |  |
 |  |
 |  |
(点击👆图片,进入自己感兴趣的专辑。或点击“资源”,浏览本公众号所有资源)
 夜雨聆风
夜雨聆风