⚠️下载肿瘤指南幻灯等万份资料,点击肿瘤指南幻灯资料库

推荐阅读

【历年CSCO指南及更新幻灯;肺癌、乳腺癌、肠癌等PPT;WCLC、ESMO、ASCO会议幻灯;免疫治疗幻灯;肿瘤基因检测等】获取方法:点击下方卡片,前往【指南幻灯资料库】,对话框回复【CSCO】,获取万份资料
日前,国内领先的AI新药发现公司德睿智药与澳门大学、英国帝国理工学院组成的联合研究团队,在国际顶级学术期刊《Nature Biomedical Engineering》(《自然-生物医学工程》,影响因子26.8)发表了题为“DeepDrugDiscovery identifies blood-brain barrier permeable autophagy enhancers for Alzheimer's disease”的重磅研究论文。
该研究建立了一个整合百万级化合物信息与多重预测模块的AI中药及天然产物活性成分发现平台,并将其用于阿尔茨海默病相关候选小分子的虚拟筛选。
通过计算筛选、成药性评估和跨物种实验验证,研究团队最终筛获具备进一步开发潜力的天然产物来源小分子化合物。
对AI制药行业而言,这项研究的价值不只在于发现候选分子,更在于验证了一条面向复杂中枢神经系统疾病的早期药物发现路径。
研究背景:AD药物研发的高壁垒
作为一种机制复杂、临床转化难度极高的神经退行性疾病,阿尔茨海默病(AD)一直是全球药物研发中的高风险领域。当前,全球阿尔茨海默病患者已逾5000万,但该领域治疗手段长期进展缓慢。
细胞自噬功能障碍是AD的重要病理特征之一。
自噬可以理解为细胞内部的“清道夫系统”,负责清除异常蛋白和受损细胞成分。当这一系统失衡,β淀粉样蛋白和过度磷酸化tau蛋白等有害物质便可能在脑内沉积。因此,开发自噬增强剂被视为具有前瞻性的治疗方向。
但这一方向也面临明显挑战。现有自噬增强剂多依赖mTOR(哺乳动物雷帕霉素靶蛋白)通路,而mTOR是人体代谢调控的重要枢纽,直接干预可能带来脱靶效应,并干扰正常生理稳态。
同时,血脑屏障、AD发病机制复杂以及脑内自噬标志物不足,共同构成了该领域药物研发的核心障碍,堪称“死亡之谷”。
DeepDrugDiscovery:重塑早期筛选范式
面对这一高难度场景,研究团队搭建了DeepDrugDiscoveryAI驱动筛选平台,试图对脑疾病药物发现流程进行系统性重构。
研究团队首先应用DeepDrugDiscovery平台,对澳门大学百万级天然产物及中药化合物库中的116万个化合物进行筛选。借助GPU加速的分子注意力机制,平台完成50×1,155,606的大规模相似性矩阵计算,并初步筛出6834个命中物。
随后,团队进一步应用德睿智药ADMET Ranker™图神经网络/图Transformer预测模块,对候选分子的血脑屏障穿透、Caco-2、MDCK、LogD、pKa、溶解度等关键成药性指标进行联合评估,将候选范围缩小至449个高潜力分子。
再结合针对FKBP12、mTOR kinase及FKBP12-mTOR复合体的分子对接和商业可得性验证,最终确定15个候选化合物进入实验阶段。
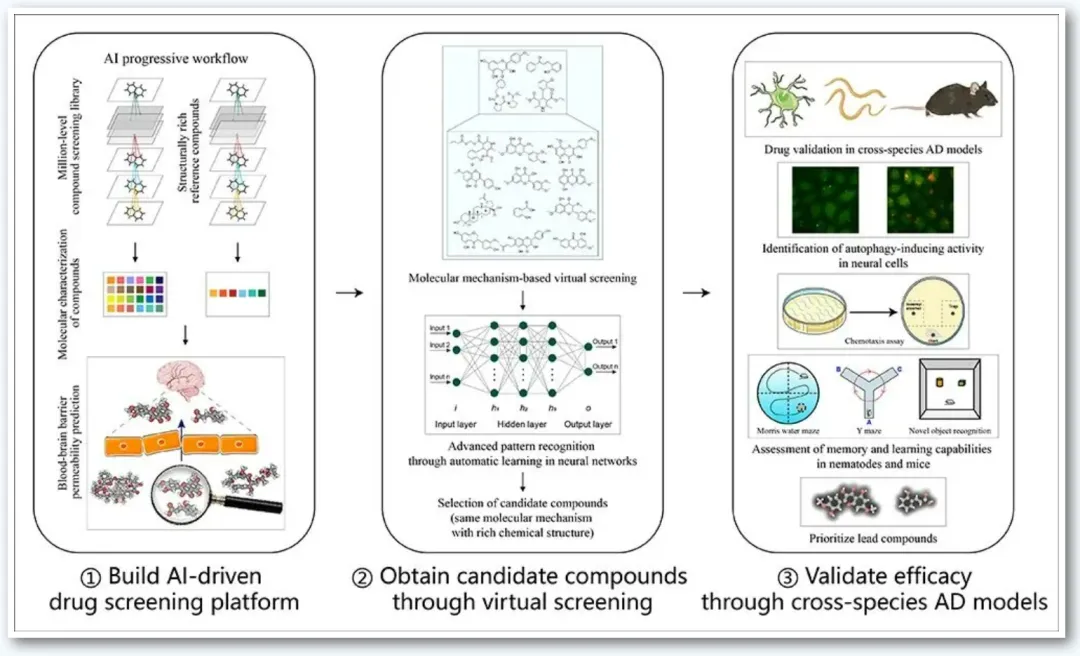
这一流程体现出AI平台在早期药物发现中的商业价值:它并非只提供计算预测,而是将机制筛选、成药性判断和实验验证前置整合,从而提高复杂疾病药物发现的效率和可验证性。
AI赋能:高效筛获潜在先导化合物
实验验证结果显示,筛选出的15个候选分子在细胞实验中均表现出促进自噬的能力。
随后,研究团队进一步结合N2a细胞中的自噬标志物变化,以及对mTOR及其下游信号的检测,筛选出7个能够在不明显影响mTOR通路的情况下增强自噬的候选分子。
这一结果具有重要意义。它说明候选分子并非简单通过传统mTOR通路发挥作用,而是可能提供一种更具差异化的自噬调节方式。
对于AD这类慢性中枢神经系统疾病而言,潜在安全性和机制差异化,是后续开发价值的重要基础。
根据作用机制的新颖性、神经保护活性以及化学结构多样性,研究团队从7个分子中进一步遴选出4个更具成药潜力的候选物进行深入研究。
在阿尔茨海默病相关细胞模型中,这4个分子均能促进异常蛋白清除。其中,Ombuin和2-Hydroxycinnamic acid表现最为突出,被确定为核心先导化合物。
随后,这2个先导化合物又在秀丽隐杆线虫和3×Tg-AD小鼠模型中完成体内验证,并进一步接受血脑屏障穿透能力评估,均显示出较好的神经保护潜力。
研究意义与商业展望
本研究不仅为阿尔茨海默病治疗提供了2个具备进一步开发潜力的候选分子,更重要的是,它验证了一条可复制、可扩展的AI驱动新药发现路径。
通过将机制导向筛选、成药性评估与跨物种实验验证高效整合,AI技术有望缩短早期发现周期、降低试错成本,并提高中枢神经系统等高难度疾病领域的研发效率。
从产业角度看,这项研究对德睿智药的意义并不局限于单个AD项目。
对于AI制药企业而言,真正的价值不是一次性发现某个候选分子,而是能否持续产出可验证、可优化、可推进的早期资产。DeepDrugDiscovery此次在阿尔茨海默病这一高壁垒场景中完成实验闭环,有助于增强其平台能力的外部可信度。
同时,该研究也为中药和天然产物资源的现代化开发提供了新路径。
中国拥有庞大的天然产物和中药化合物库,但长期面临机制解释不足、筛选效率偏低和临床转化不稳定等问题。
AI平台若能持续提升候选分子的识别效率和机制验证能力,将有机会把传统化合物资源转化为更具产业价值的创新药发现入口。
研究团队已将DeepDrugDiscovery平台开源,以期推动更多中药机制解析与创新药研发。
若未来该平台能够在更多复杂疾病场景中持续产出高质量候选分子,其商业价值将不只体现为单一管线进展,也可能体现为对外合作、资产授权和平台型研发能力的系统放大。
关于德睿智药
德睿智药MindRank是一家AI for drug discovery(人工智能药物发现)科技创新公司,致力于以机器学习、强化学习与第一性原理计算赋能新药研发。公司依托融合生物学、结构生物学、化学和医学的自研一站式AI平台,拓展新药研发的技术边界,推动更多疾病领域的创新药发现。
肿瘤指南幻灯资料库

点击加入:肿瘤指南幻灯资料库,学习肿瘤治疗知识















肿瘤指南幻灯资料库(万份)目录如下
 夜雨聆风
夜雨聆风