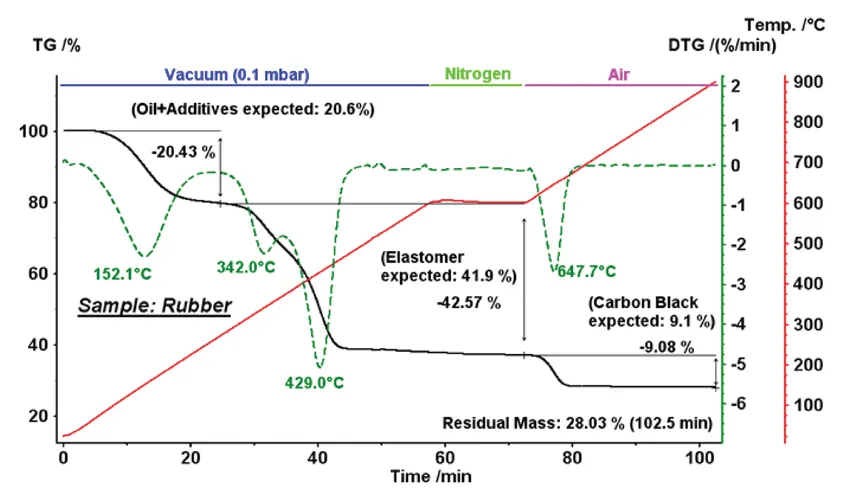
看懂这张图,高考化学最后一题10分轻松到手
翻开近几年的高考化学试卷,有一类题型的出现频率和难度都在稳步攀升——热重曲线分析题。这类题目将热重曲线图与化学计算相结合,考查学生从图像中获取信息、进行数据处理和综合分析的能力。从2025年各地的高考模拟题和复习资料来看,热重曲线已成为许多省份卷面的高频考点,尤其在工艺流程综合题中频繁出现。
今天,我们就用这一篇文章,把热重曲线的原理、分析步骤、计算方法和常见陷阱彻底讲透,让你面对任何热重图都能心中有数。
一、什么是热重曲线?一张图看懂
热重法是在程序控制温度的条件下,测量物质的质量与温度关系的方法。记录质量随温度变化的曲线,就是热重曲线(TG曲线)。
怎么读图?
横坐标:温度(或时间),自左向右升高。
纵坐标:样品的剩余质量或固体残留率(%)。
曲线中出现的每一段水平台阶表示在该温度范围内样品质量保持恒定;台阶之间的斜坡表示样品正在发生质量损失的热分解反应。
热重分析得到的TG曲线,还可以对温度求一阶导数得到DTG曲线(微分热重曲线),它反映失重速率与温度的关系——DTG曲线上的每个峰与TG曲线的一个失重台阶对应,峰顶点对应失重速率最快的温度点。
二、常见的失重过程:热重曲线考什么?
高考热重曲线试题常见于两类情境:
| 分解失重型 | ||
| 氧化还原型 |
结晶水合盐的典型热分解规律
加热结晶水合盐的反应通常遵循以下三步路径:
脱去部分结晶水 → 生成较低水合度的盐
生成羟基盐或含水盐 → 中间过渡产物
最终生成金属氧化物 → 热重曲线的终点
⚠️ 重点提示:如果热重实验在空气氛围中进行,低价态的金属元素还可能被空气中的氧气氧化,使反应变得更加复杂,考查的难度也随之提升。
也就是说,在空气中加热过渡金属的含氧酸盐,很可能是“先失水再氧化”的双重过程,在分析每步固体的化学式时要充分考虑这一层因素。
三、五步计算法:一张表格搞定所有热重题
热重曲线类试题大多基于结晶水合盐试样的热重实验图像命题。这类题的核心计算方法可以总结为清晰的“五步法”:
第1步:设晶体的物质的量为1 mol,计算其质量m。
第2步:按“先失水,再失非金属氧化物”的顺序判断失重步骤。
第3步:计算各温度段固体剩余的质量m余,固体残留率=m余/m×100%。
第4步:晶体中金属元素的质量在热分解过程中保持不变(仍在m余中)。
第5步:失重终点产物一般为金属氧化物。用质量守恒求氧元素的质量m氧,再由n(金属)∶n(氧)的比值确定最终产物的化学式。
这一套“设1 mol金属化合物为计算基准”的解题模式,等于为所有热重曲线题提供了一个万能的解题框架。不管题目怎么变,按这个流程走就不会乱。
四、三步读图法:把热重曲线变成“阶梯图”
面对热重曲线题目时,建议按“识图→析图→用图”三个步骤进行,既稳妥又可高效拿分:
步骤❶:识图(三看)
一看轴:横坐标是什么?纵坐标表示的是样品质量还是残留率?
二看点:找出每条曲线的拐点、平台、起始分解温度和终止温度。
三看线:观察曲线是否存在连续的多台阶失重现象,多段失重意味着以上失重原理推测的一环扣一环已经开始从平面图上发挥作用了。
步骤❷:析图:分析每一个失重台阶对应什么样的反应——是失去结晶水,还是分解产生了CO₂或SO₃,或是发生了氧化反应(增重变化)?
步骤❸:用图:将热重图上的关键数据代入物质的量计算的守恒思路中去,即可推演出每一步产物的化学式,写出化学方程式,完成所有填空问句。
五、高考真题示例
经典案例一:CaC₂O₄·H₂O在氮气中的热分解
一水草酸钙(CaC₂O₄·H₂O)在N₂氛围中的热重曲线是典型的 “三步分解” ,常作为高考例题的基础模型:
这类题的高分关键是:每个温度区间对应一个清楚明确的热分解半反应,利用总质量和相对分子质量逐一列方程解出各步计量关系,就能推出每个台阶产物的化学式。
⚠️ 如果热重实验的气氛改为空气(——比如经典的含氧气氛下分解),草酸钙的热分解路径会截然不同:空气中的O₂会参与反应,直接生成CaCO₃和CO₂:
2CaC₂O₄ + O₂ ——△→ 2CaCO₃ + 2CO₂↑
经典案例二:硫酸铁铵结晶水数的测定(2019·全国卷Ⅰ)
将硫酸铁铵晶体样品加热到150℃时失掉1.5个结晶水,失重5.6%。求该晶体的化学式。
解析:设化学式为NH₄Fe(SO₄)₂·xH₂O
失重5.6%对应的质量损失即为失去的1.5个H₂O的相对分子质量:
(1.5 × 18) / M晶体 = 5.6%
解出M晶体≈482,减去NH₄Fe(SO₄)₂(266)后得到x≈12。故化学式为NH₄Fe(SO₄)₂·12H₂O。
这类以残留率或失重百分比正向推导化学式的题目,考查的就是用数据的定量解读能力。
真题演练三:2024·新高考江苏卷
将8.84 mg Nd(OH)CO₃在N₂氛围中焙烧,剩余固体质量随温度变化的曲线如下。550~600℃时,所得固体产物可表示为NdₐO_b(CO₃)_c,通过实验数据确定该产物中n(Nd³⁺)∶n(CO₃²⁻)的比值。
解析:n[Nd(OH)CO₃]=8.84mg÷221g·mol⁻¹=4×10⁻⁵mol。550~600℃时,固体质量减少1.24mg。根据2OH⁻~H₂O,生成的H₂O为0.36mg(即2×10⁻⁵mol),则CO₂的质量为1.24-0.36=0.88mg,对应CO₂为2×10⁻⁵mol。反应掉的CO₃²⁻为2×10⁻⁵mol,剩余固体中CO₃²⁻为4×10⁻⁵-2×10⁻⁵=2×10⁻⁵mol。而Nd³⁺在焙烧过程中质量不变,仍为4×10⁻⁵mol。
因此,n(Nd³⁺)∶n(CO₃²⁻)=2∶1。
解题要点:原子守恒贯穿整个过程——Nd总量守恒、C总量守恒,逐一列式就能解出产物的组成比例。
六、解题避坑指南:四个常见失分点
❶ 忽略实验气氛的影响
在空气中加热和惰性气体中加热,热重曲线的样貌可能完全不同。拿到题目后,第一件事是看题干给出的实验气氛——N₂、Ar还是空气?直接决定了你的分析方向。
❷ 将终点产物的判断弄错
大多数金属盐在空气中充分灼烧的最终产物是其最高价氧化物(或金属氧化物)。但也有些过渡金属在高温下会形成碱性更强的氧化物(如Mn₃O₄),推导化学式时不要“想当然”用最高价代入。
❸ 分段计算时忽略中间产物的化学式变化
热重曲线的每一段台阶都代表一个相对稳定的中间产物,而各段之间的斜坡则是反应的发生区间。做题时切勿以“整体猜测”取代分步计算——多步分解的唯一可靠思路就是用数据一步步算,而不是“猜每个台阶对应什么东西”。
❹ 缺少物质的量的精准换算
热重分析本质是定量实验,因此晶体的物质的量和实际失重量是配方程式以及写化学式的关键依据。在复杂多金属系统中尤其要多加检查守恒数据,放慢节奏再核对一遍也能有效避免粗心出错。
七、2026高考命题趋势与备考建议
从最新一轮复习和模拟题的动向来看,热重曲线的两个考查重点非常明确。
趋势一:热重分析与工艺流程题深度融合——例如在废渣回收稀散金属(Co、Ni)中嵌入热重曲线分析,要求学生根据质量变化推演出多段焙烧产物并写出合理的热分解方程式。
趋势二:“物质组成判断→方程式书写→多步反应设计”这一考查链路,在高考中与守恒思想的捆绑日益紧密。利用原子守恒、电子守恒推中间产物的化学式,已经成为区分高分考生的关键增量。
备考策略:建议吃透“五步法”计算框架,刷透近3—5年真题中的热重曲线计算题。从一水草酸钙到硫酸铁铵晶体,从NiSO₄·6H₂O煅烧到MnSO₄·H₂O受热分解,这些经典案例反复演练后,考场上遇到陌生的热重曲线时自然能够调用既有模型,游刃有余地转化为必得分数。
八、考场实战指南
若在考试中遇到热重曲线题,可以遵循如下思路快速应对:
先确定实验气氛:是N₂、Ar还是空气?判断会不会发生氧化反应。
找出失重台阶与平台:到底经历了几步分解?分别对应多少质量损失?
计算残留率并在每一步列守恒方程:利用设1 mol晶体为基准的统一方式,精准算出每步产物的化学式。
金属元素总量永远是判断的“定海神针” ——几乎所有热重曲线题的突破点都在这里。
💡 核心记忆口诀
先看气氛看气氛,五步计算不绕路。
金属元素从不丢,代数求比得氧化物。
记忆口诀记一点:金属守恒、氧算比。
掌握好这篇的热重分析框架,不论高考将热重曲线放在哪一道大题中结合考查,你都能够从容应对,把属于你的分数稳稳拿到手!
 夜雨聆风
夜雨聆风