文档内容
2011年河南省初中学业水平暨高级中等学校招生考试
化 学
满分50分,考试时间50分钟。
可能用到的相对原子质量:H-1 C—12 O-16 A1-27 Ca-40 Fe-56
Cu-64 Ag-108
一、选择题(本题包括10个小题,每小题1分,共10分)
下列各题,每题只有一个选项符合题意,请将正确选项的标号填入题后括号内。
1.生活中发生的下列变化,属于化学变化的是 ( )
A.冰雪融化 B.食物腐烂 C.汽油挥发 D.石蜡熔化
2.燃煤排出的二氧化硫进入大气后,会引起的环境问题是 ( )
A.温室效应 B.白色污染 C.酸雨 D.臭氧层破坏
3.用氯化钠固体配制一定质量分数的氯化钠溶液,不需要用到的仪器是 ( )
A.烧杯 B.量筒 C.托盘天平 D.蒸发皿
4.某物质不含碳元素和氢元素,它不可能是①酸、②碱、③盐、④有机物中的 ( )
A.①②④ B.②③④ C.①②③ D.①③④
5.下图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是 ( )
A.甲的溶解度大于乙的溶解度
B.t℃时,甲、乙饱和溶液中溶质的质量分数相等
C.升高温度能使接近饱和的甲溶液变为饱和溶液
D.10℃时,分别用100 g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
6.“信阳毛尖”是一种绿茶,绿茶中含有的单宁酸(化学式为C H O )具有抑制血压上升、
76 52 46
清热解毒等功效。下列有关单宁酸的说法正确的是 ( )A.属于氧化物 B.由碳原子、氢分子和氧分子构成
C.氢元素的质量分数最小 D.碳、氧两种元素的质量比为76∶46
7.有元素化合价升降的反应是氧化还原反应。下列属于氧化还原反应的是 ( )
A.CaCO CaO + CO↑ B.HCl+ KOH = KCl+ H O
3 2 2
C.SO +2NaOH = NaSO +H O D.2Na +2H O = 2NaOH+ H↑
2 2 3 2 2 2
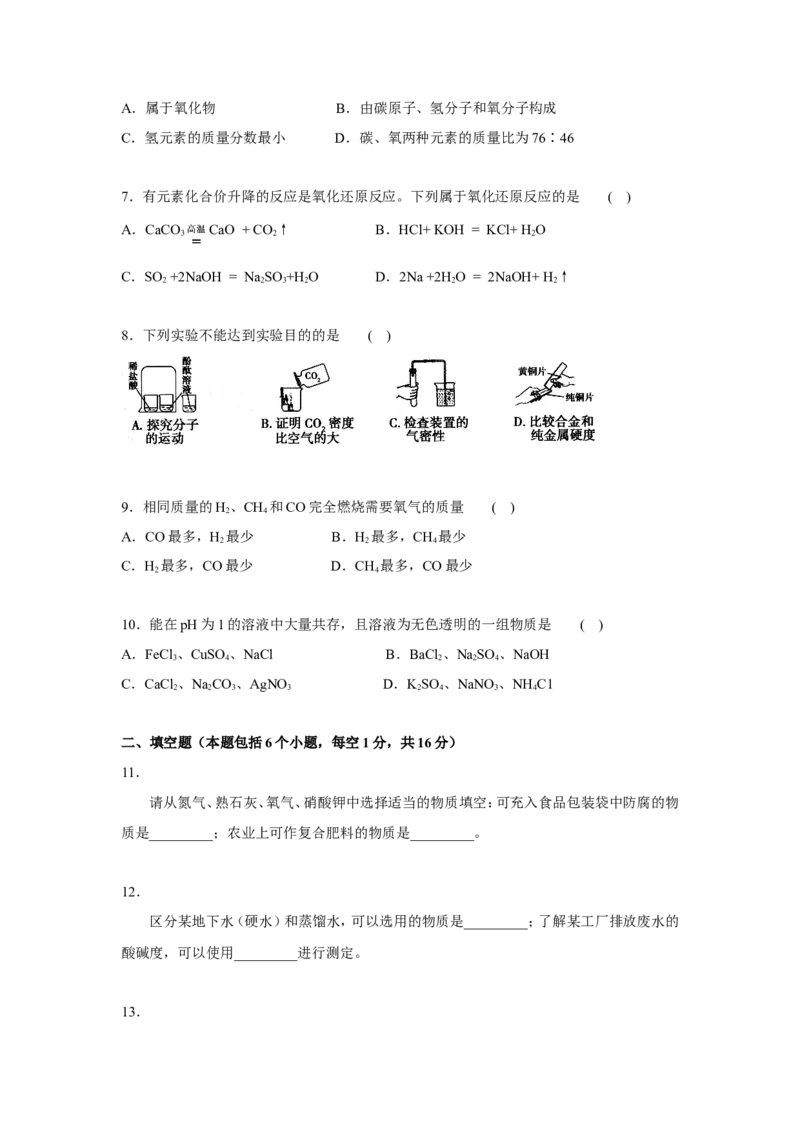
8.下列实验不能达到实验目的的是 ( )
9.相同质量的H、CH 和CO完全燃烧需要氧气的质量 ( )
2 4
A.CO最多,H 最少 B.H 最多,CH 最少
2 2 4
C.H 最多,CO最少 D.CH 最多,CO最少
2 4
10.能在pH为1的溶液中大量共存,且溶液为无色透明的一组物质是 ( )
A.FeCl、CuSO 、NaCl B.BaCl、NaSO 、NaOH
3 4 2 2 4
C.CaCl、NaCO、AgNO D.KSO 、NaNO 、NH C1
2 2 3 3 2 4 3 4
二、填空题(本题包括6个小题,每空1分,共16分)
11.
请从氮气、熟石灰、氧气、硝酸钾中选择适当的物质填空:可充入食品包装袋中防腐的物
质是_________;农业上可作复合肥料的物质是_________。
12.
区分某地下水(硬水)和蒸馏水,可以选用的物质是_________;了解某工厂排放废水的
酸碱度,可以使用_________进行测定。
13.“岩盐之都”河南叶县盛产食盐。食盐的主要成分NaCl由_________(填“分子”、“原
子”或“离子”)构成;除去食盐水中泥沙等不溶性杂质的方法是_________;电解食盐水可
制烧碱:2NaCl + 2HO 2NaOH + H↑+ X↑,则X的化学式为_________。
2 2
14.
2011年是“国际化学年”。化学与生活密切相关,合理选择饮食、正确使用药物等都离不
开化学。水果、蔬菜能为人体提供的主要营养素是_________;人体缺少必需微量元素会得病,
如缺_________会引起甲状腺肿大(俗称大脖子病);含小苏打的药物治疗胃酸过多症的化学
方程式为__________________。
15.
一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
物质 A B C D
反应前质量/g 1.7 2.2 7.9 0.9
反应后质量/g 待测 6.6 0 2.7
则反应后A的质量为_________;该反应所属的基本反应类型是_________;该反应中B
和D两种物质变化的质量比为_________。
16.
在Cu(NO )、Al( NO) 和AgNO 的混合溶液中加入一定量的铁粉,充分反应后过滤,向
3 2 3 3 3
滤出的固体上滴加稀硫酸时有气泡产生,则反应后所得溶液中含有的金属离子有_________;
反应后溶液的质量比原混合溶液的质量_________(填“大”或“小”);有关反应的化学方
程式为_________(写出一个即可)。
三、简答题(本题包括4个小题,共12分)
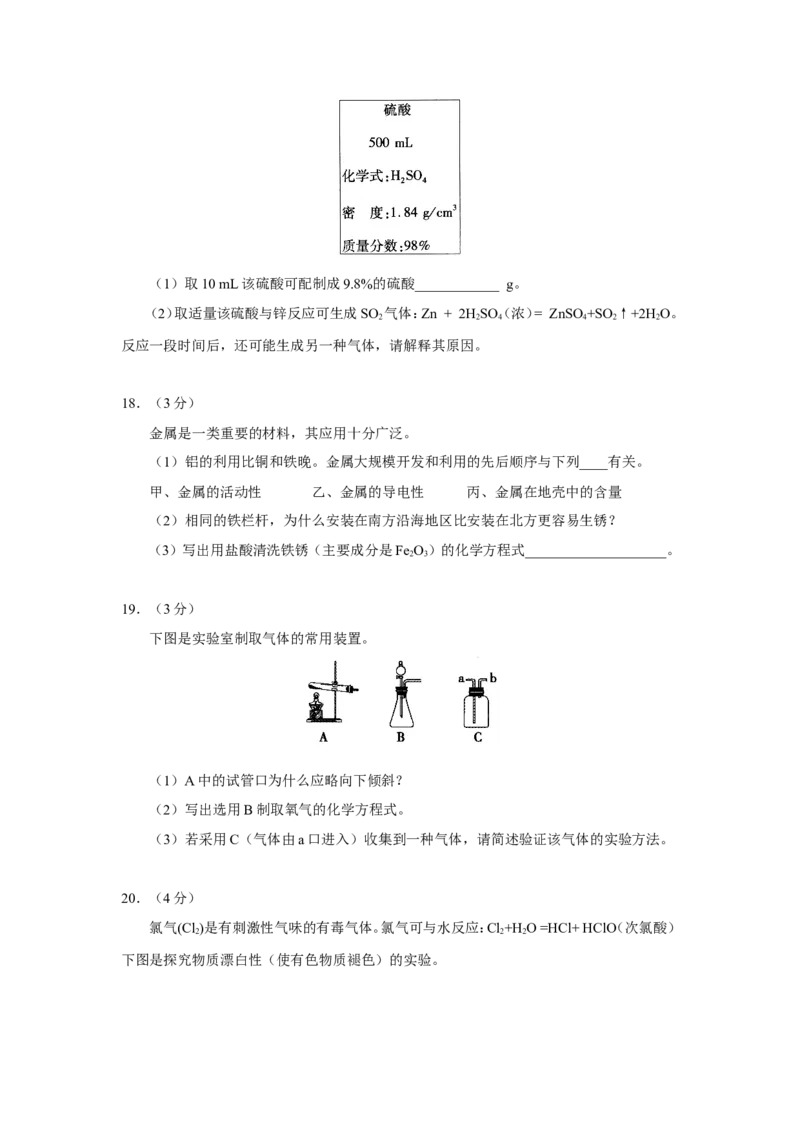
17.(2分)
下图是某硫酸试剂瓶标签上的部分文字说明。(1)取10 mL该硫酸可配制成9.8%的硫酸____________ g。
(2)取适量该硫酸与锌反应可生成SO 气体:Zn + 2HSO(浓)= ZnSO+SO↑+2H O。
2 2 4 4 2 2
反应一段时间后,还可能生成另一种气体,请解释其原因。
18.(3分)
金属是一类重要的材料,其应用十分广泛。
(1)铝的利用比铜和铁晚。金属大规模开发和利用的先后顺序与下列____有关。
甲、金属的活动性 乙、金属的导电性 丙、金属在地壳中的含量
(2)相同的铁栏杆,为什么安装在南方沿海地区比安装在北方更容易生锈?
(3)写出用盐酸清洗铁锈(主要成分是Fe O)的化学方程式____________________。
2 3
19.(3分)
下图是实验室制取气体的常用装置。
(1)A中的试管口为什么应略向下倾斜?
(2)写出选用B制取氧气的化学方程式。
(3)若采用C(气体由a口进入)收集到一种气体,请简述验证该气体的实验方法。
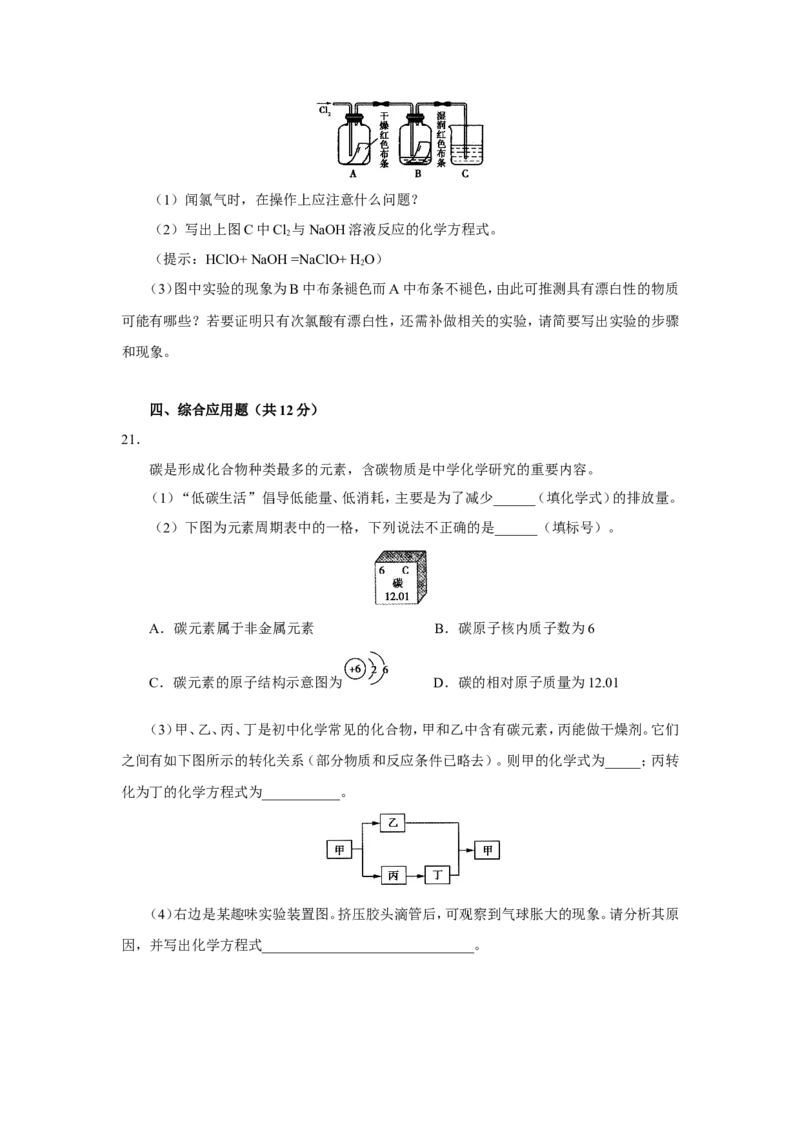
20.(4分)
氯气(Cl)是有刺激性气味的有毒气体。氯气可与水反应:Cl+H O =HCl+ HClO(次氯酸)
2 2 2
下图是探究物质漂白性(使有色物质褪色)的实验。(1)闻氯气时,在操作上应注意什么问题?
(2)写出上图C中Cl 与NaOH溶液反应的化学方程式。
2
(提示:HClO+ NaOH =NaClO+ H O)
2
(3)图中实验的现象为B中布条褪色而A中布条不褪色,由此可推测具有漂白性的物质
可能有哪些?若要证明只有次氯酸有漂白性,还需补做相关的实验,请简要写出实验的步骤
和现象。
四、综合应用题(共12分)
21.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容。
(1)“低碳生活”倡导低能量、低消耗,主要是为了减少______(填化学式)的排放量。
(2)下图为元素周期表中的一格,下列说法不正确的是______(填标号)。
A.碳元素属于非金属元素 B.碳原子核内质子数为6
C.碳元素的原子结构示意图为 D.碳的相对原子质量为12.01
(3)甲、乙、丙、丁是初中化学常见的化合物,甲和乙中含有碳元素,丙能做干燥剂。它们
之间有如下图所示的转化关系(部分物质和反应条件已略去)。则甲的化学式为_____;丙转
化为丁的化学方程式为___________。
(4)右边是某趣味实验装置图。挤压胶头滴管后,可观察到气球胀大的现象。请分析其原
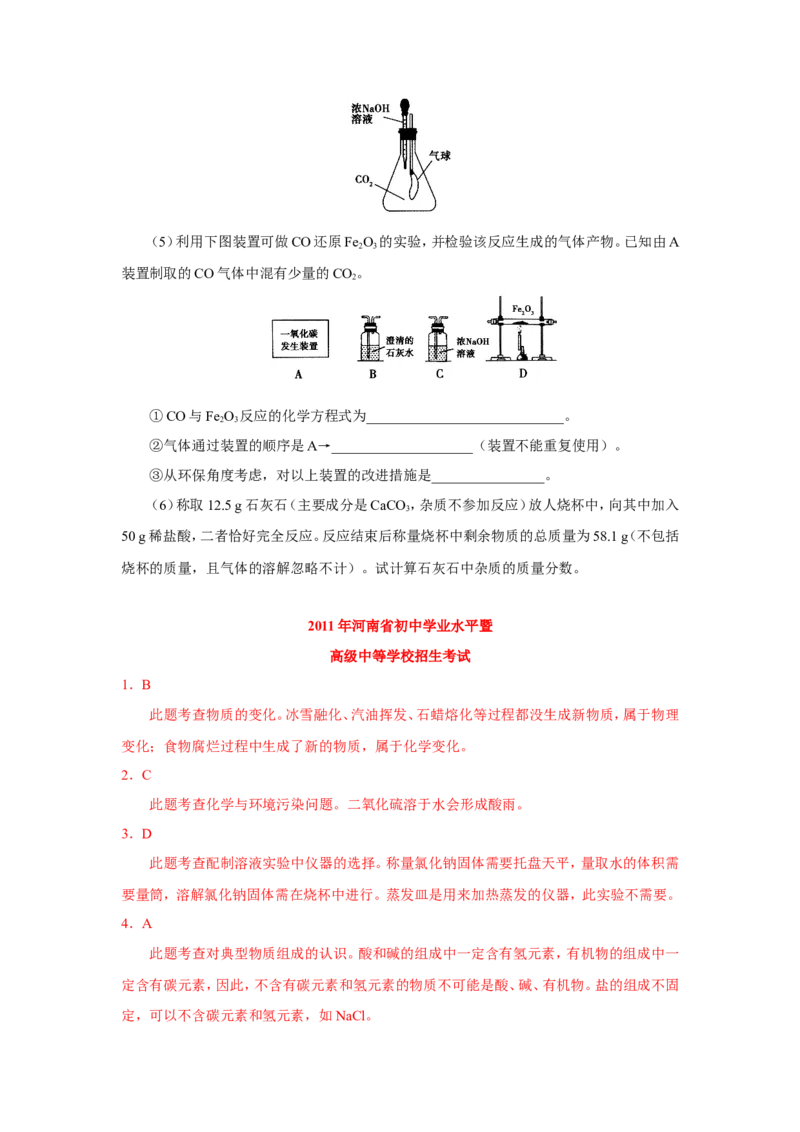
因,并写出化学方程式______________________________。(5)利用下图装置可做CO还原Fe O 的实验,并检验该反应生成的气体产物。已知由A
2 3
装置制取的CO气体中混有少量的CO。
2
①CO与Fe O 反应的化学方程式为____________________________。
2 3
②气体通过装置的顺序是A→____________________(装置不能重复使用)。
③从环保角度考虑,对以上装置的改进措施是________________。
(6)称取12.5 g石灰石(主要成分是CaCO ,杂质不参加反应)放人烧杯中,向其中加入
3
50 g稀盐酸,二者恰好完全反应。反应结束后称量烧杯中剩余物质的总质量为58.1 g(不包括
烧杯的质量,且气体的溶解忽略不计)。试计算石灰石中杂质的质量分数。
2011年河南省初中学业水平暨
高级中等学校招生考试
1.B
此题考查物质的变化。冰雪融化、汽油挥发、石蜡熔化等过程都没生成新物质,属于物理
变化;食物腐烂过程中生成了新的物质,属于化学变化。
2.C
此题考查化学与环境污染问题。二氧化硫溶于水会形成酸雨。
3.D
此题考查配制溶液实验中仪器的选择。称量氯化钠固体需要托盘天平,量取水的体积需
要量筒,溶解氯化钠固体需在烧杯中进行。蒸发皿是用来加热蒸发的仪器,此实验不需要。
4.A
此题考查对典型物质组成的认识。酸和碱的组成中一定含有氢元素,有机物的组成中一
定含有碳元素,因此,不含有碳元素和氢元素的物质不可能是酸、碱、有机物。盐的组成不固
定,可以不含碳元素和氢元素,如NaCl。5.B
此题考查溶解度曲线的意义及应用。甲、乙溶解度的大小关系随温度变化而变化,A错;
t℃时甲、乙溶解度相等,因此它们的饱和溶液中溶质质量分数相等,B正确;甲的溶解度随温
度升高而增大,因此,接近饱和的甲溶液升温后会变得更不饱和了,C错;10℃时甲的溶解度
小于乙的溶解度,因此,在100 g水中溶解的甲的质量小于乙的质量,D错。
6.C
此题考查化学式的意义及计算。根据单宁酸的化学式C H O 可以看出,单宁酸由三种
76 52 46
元素组成,不属于氧化物,A错;单宁酸由单宁酸分子构成,单宁酸分子由碳原子、氢原子、氧
原子构成,B错;单宁酸中C、H、O的相对质量分别为12×76 =912,1×52 =52,16×46= 736,显
然,氢元素质量最小,其质量分数也最小,C正确;碳、氧两种元素质量比为 912∶736
=57∶46,D错。
7.D
选项D的化学反应中Na的化合价由0升高到+1,H的化合价由+1降到0,此反应属于
氧化还原反应。A、B、C中元素的化合价在反应前后均没有变化,不属于氧化还原反应。
8.A
此题考查对实验设计的分析能力。由于稀盐酸不能使酚酞溶液变色,因此,A实验小烧
杯中的酚酞溶液颜色不变,此实验不能用来探究分子的运动;B中实验底层的蜡烛先熄灭,
证明CO 的密度比空气大;C中实验导管口出现气泡,证明装置严密;D中实验纯铜片上出现
2
划痕,证明黄铜片比纯铜片硬度大。
9.C
此题考查化学方程式的计算。设H、CO、CH 的质量均为1 g,完全燃烧消耗氧气的质量
2 4
分别为x、y、z。
2H + O HO 2CO + O 2CO CH + 2O CO +2H O
2 2 2 2 2 4 2 2 2
4 32 56 32 16 64
1 g x 1 g y l g z
x = 8 g y = 0.57 g z = 4 g
因此,消耗氧气的质量H 最多,CO最少。
2
10.D此题考查溶液中物质的共存问题,实质是考查酸、碱、盐之间的反应。pH为1的溶液显
酸性,CuSO 溶于水显蓝色且FeCl 溶于水显黄色,A错;B中BaCl 与NaSO 在溶液中能发
4 3 2 2 4
生反应生成BaSO 沉淀(此沉淀不能被酸溶解),二者不能共存,NaOH也不能在酸性条件下
4
存在;C中CaCl 与AgNO 能反应生成AgCl沉淀(此沉淀不能被酸溶解),二者不能共存,
2 3
NaCO 在酸性条件下也不能存在;D中三种物质的溶液均为无色,它们之间都不发生反应,
2 3
且与酸也不反应,符合要求。
11.
氮气(或N) 硝酸钾(或KNO)
2 3
12.
肥皂水 pH试纸
13.
离子 过滤 Cl
2
14.维生素 碘 NaHCO + HCl = NaCl+CO↑+H O
3 2 2
15.3.4 g 分解反应 22∶9
16.Al3+和Fe2+ 小 Fe +2AgNO = Fe(NO) +2Ag [或Fe+Cu(NO)=Fe(NO)+Cu或
3 3 2 3 2 3 2
Fe+H SO= FeSO+ H ↑]
2 4 4 2
17.(2分)
(1)184
(2)随着硫酸的消耗和水的生成,硫酸变稀,锌与稀硫酸反应能生成氢气。
18.
(1)甲
(2)铁在潮湿的空气中容易生锈,南方沿海地区的空气湿度较大且温度要高一些。
(3)Fe O+ 6HCl = 2FeCl+3H O
2 3 3 2
19.
(1)防止试管口的冷凝水回流到热的试管底部,炸裂试管。
(2)2HO 2HO +O↑
2 2 2 2
(3)将带火星的木条伸入集气瓶中,木条复燃,证明收集的气体是氧气。(或向集气瓶中
加入澄清的石灰水,石灰水变浑浊,证明收集的气体是二氧化碳。)
20.
(1)不要把鼻孔凑到容器口去闻氯气的气味。(或用手在容器口轻轻扇动,让极少量气体飘进鼻孔。)
(2)Cl+ 2NaOH = NaCl + NaClO + HO
2 2
(3)具有漂白性的物质可能有盐酸和次氯酸。取一红色布条,在上面滴加盐酸,布条不褪
色。
21.
(1)CO
2
(2)C
(3)CaCO CaO + HO = Ca(OH)
3 2 2
(4)CO 被浓NaOH溶液吸收,锥形瓶内的气压减小,外界大气压大于锥形瓶内的气压,
2
使气球胀大。 2NaOH+ CO= NaCO+ H O
2 2 3 2
(5)①Fe O +3CO 2Fe +3CO ②C→D→B ③将尾气点燃或进行收集等
2 3 2
(6)解:生成CO 的质量为:12.5 g + 50 g - 58.1 g = 4.4 g
2
设石灰石中CaCO 的质量为x。
3
CaCO +2HCl = CaCl+ CO↑+ H O
3 2 2 2
100 44
x 4.4 g
x =10 g
石灰石中杂质的质量分数为: × l00% = 20%
答:石灰石中杂质的质量分数为20%。