文档内容
常州市 2014 年中等学校招生考试
一、选择
1.氢气是21世纪的新能源。储氢材料C 是
60
A.金属单质 B.非金属单质 C无机化合物 D.有机化合物
2.海洋约占地球表面积的71%,海水中含量最高的元素是
A.Na B.Cl C.H D.O
3.人类.最先使用的金属是
A.镁 B.铝 C.铁 D.铜
4. 下列变化属于化学变化的是
[来源:学科网ZXXK]
A.海水晒盐 B.干冰升华 C.粮食酿酒 D.电灯发光
5.下列物质由原子直接构成的是
A.氧气 B.金刚石 C. 氯化钠 D.水
6.下列气体无色无味的是
A. NH B.HCI C.CO D. SO
3 2
7.下列物质富含淀粉的是
A.玉米 B.牛奶 C.豆油 D.青菜
8.下列化肥属于复合肥料的是
A.硝酸钾 B.氯化钾 C.氨水(NH .H 0) D.碳酸氢铵
3 2
9.实验室盛装浓硫酸的试剂瓶上贴有的标示为
10.下列实验操作正确的是
11.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,下列事实与形成PM2.5无关的是
A.水力发电 B.风扬尘土 C. 汽车尾气 D.煤炭燃烧12.过氧化氢消除矿业中氰化物的原理为:KCN+H O+H O=X+NH ↑,X是
2 2 2 3
A.KO B.KOH C.KCO D.KHCO
2 2 3 3
13.在一定条件下,下列物质的转化一步不能能实现的是
A.Fe-----Fe O B.Fe O——Fe C.S——SO D.NaOH——NaSO
3 4 2 3 2 2 4
14.T0C时,将一定量的生石灰放入饱和的石灰水中,搅拌,并冷却到原温度,得到的溶液
与原溶液相比,下列物理量前后不变化的是
①溶质质量 ②溶剂质量 ③溶液质量 ④溶质质量分数 ⑤溶解度
A.① ③ ⑤ B. ② ④ ⑤ C. ② ④ D. ④ ⑤
15.作为相对原子质量标准的1个碳原子的质量是1.993×10-26kg,一种氢原子1个原子的质
量为3.348×10-27kg,则该氢原子的相对原子质量为
A.1 B.2 C.3 D.4
16.X、Y、Z三种金属分别放入稀硫酸中,Y溶解并产生氢气,X、Z不溶解,X、Z放入硝酸
银溶液中,X的表面有银析出,Z的表面无变化,下列金属的活动顺序由强到弱的顺序是
A. X>(H)>Y>Z B. Y>(H)>Z >X C. Y>(H)> X >Z D. Z>X>(H)
>Y
17.下列实验操作或方法正确的是
A.将空气通过灼热的铜网可以除去氧气
B.用点燃的方法可以除去二氧化碳中的一氧化碳
C. pH试纸使用前,先用蒸馏水湿润,再测定未知浓液的pH
D.稀释浓硫酸时,向浓硫酸中缓缓加人蒸馏水,用玻璃棒搅拌
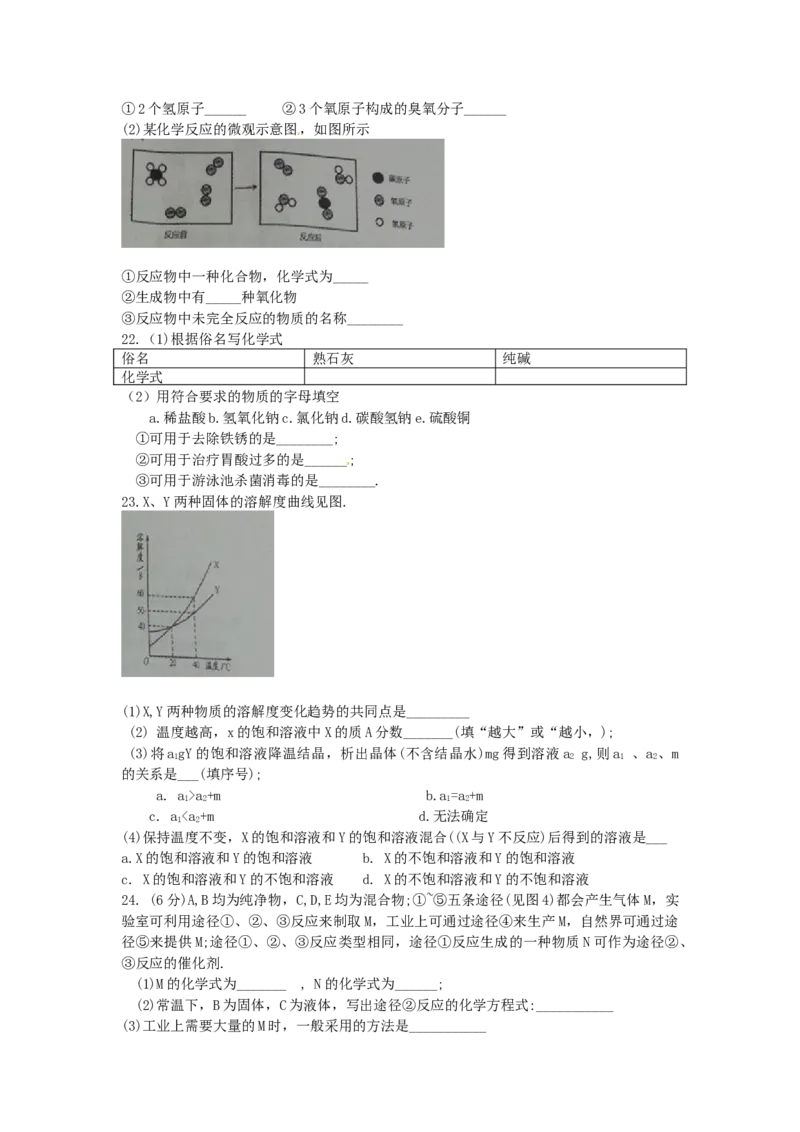
18.对下列一些事实的解释错误的是
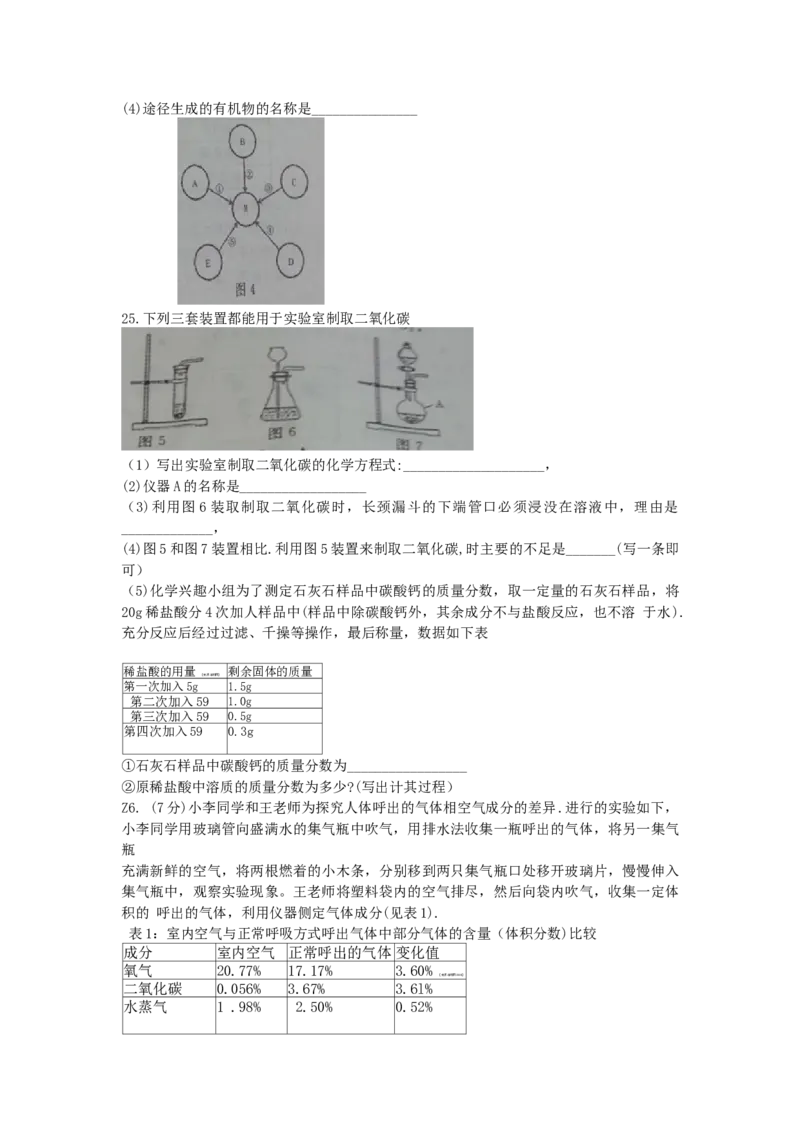
19.如留所示,将摘管甲中的液体挤出,气球明显鼓起,一段时间后恢复原状,再将滴管乙
中的液体挤出,气球又明显鼓起且不恢复原状.则滴管甲、乙和
烧杯①②中的物质可能是
A.甲:水,①:食盐; 乙:水, ②:蔗糖
B.甲:水①硝酸铵; 乙:稀盐胶, ②:铁
C.甲:水①氢氧化钠 ; 乙:稀硫酸 ②:锌
D.甲:水①生石灰; 乙:稀盐酸 ②:氢氧化钠
20.工业上用Mg(NO ) 作为浓缩HNO 的吸水剂,向m g溶质质量
3 2 3 1
分数为65%的硝酸溶液中加人mg溶质质量分数为72 %的Mg (NO,) 溶液,蒸馏,分别得到
2 2
97.5%硝酸溶液和60%硝酸镁溶液,若蒸馏过程中,硝酸、硝酸镁和水均无损耗,则投料质
量比m/m 为
1 2
A.0.3 B.0.4 C.0.5 D.0.6
二.
21.(1)用化学符号农示下列粒子①2个氢原子______ ②3个氧原子构成的臭氧分子______
(2)某化学反应的微观示意图,如图所示
①反应物中一种化合物,化学式为_____
②生成物中有_____种氧化物
③反应物中未完全反应的物质的名称________
22.(1)根据俗名写化学式
俗名 熟石灰 纯碱
化学式
(2)用符合要求的物质的字母填空
a.稀盐酸b.氢氧化钠c.氯化钠d.碳酸氢钠e.硫酸铜
①可用于去除铁锈的是________;
②可用于治疗胃酸过多的是______;
③可用于游泳池杀菌消毒的是________.
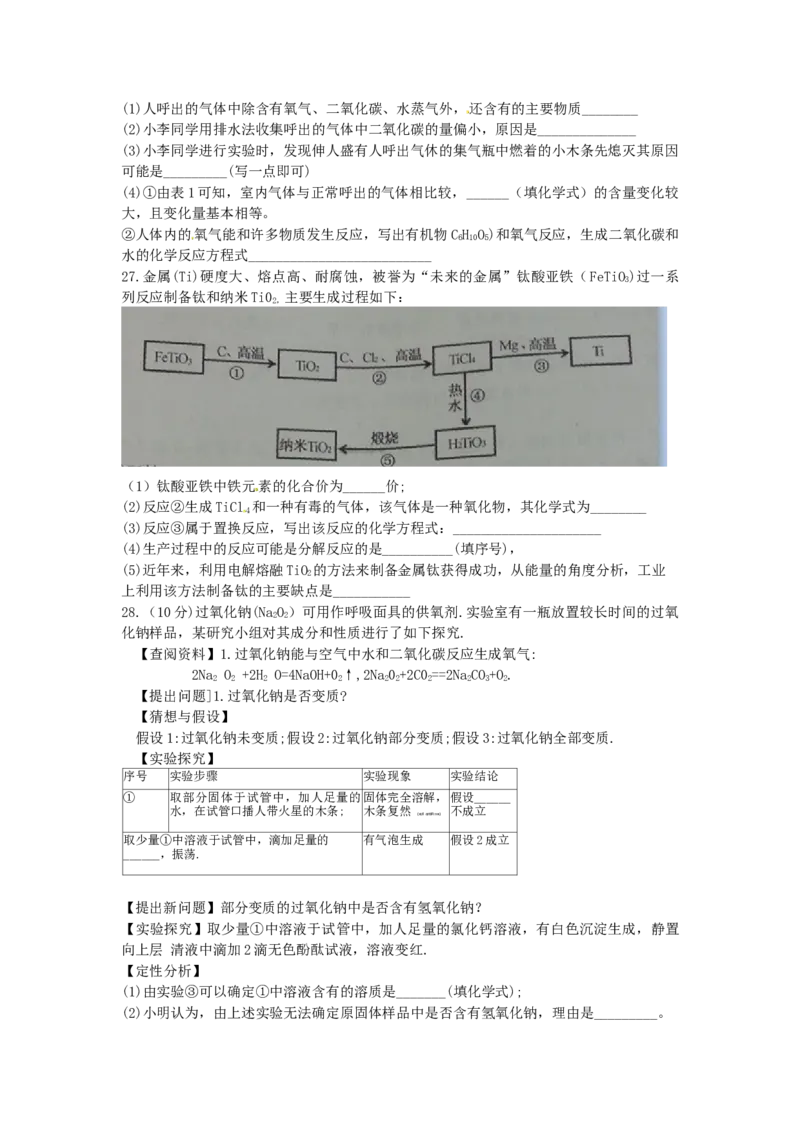
23.X、Y两种固体的溶解度曲线见图.
(1)X,Y两种物质的溶解度变化趋势的共同点是_________
(2) 温度越高,x的饱和溶液中X的质A分数_______(填“越大”或“越小,);
(3)将agY的饱和溶液降温结晶,析出晶体(不含结晶水)mg得到溶液a g,则a 、a 、m
1 2 1 2
的关系是___(填序号);
a. a>a+m b.a=a+m
1 2 1 2
c. aZ。
17.【答案】A
【解析】选项B中,二氧化碳是主体,因此无法点燃;选项C中, pH试纸使用前不能用水
湿润,否则相当于将溶液稀释,测得的结果不正确;选项D应该是将浓硫酸注入水中,否
则会造成液滴飞溅。
18.【答案】B
【解析】A正确,蛋白质变性后,病毒就失去了活性;B错误,氨气被压缩是因为分子之间
的间隔变小了;选项C正确,分子是保持物质的化学性质的最小粒子,分子构成不同,化
学性质不同;选项D正确,亚铁离子在溶液中呈浅绿色,铁离子为淡黄色。
19.【答案】C
【解析】将摘管甲中的液体挤出,气球明显鼓起,说明瓶内的压强变大,所以可能是温度
升高或者产生气体,一段时间后恢复原状,说明是温度又降低,因此甲和乙接触要放热,
因此排除了A、B;再将滴管乙中的液体挤出,气球又明显鼓起且不恢复原状,说明生成了
气体,因此选C。
20.【答案】D
【解析】解:设被转移的水的质量为%.65%的硝酸含水为35%, 72%的硝酸酸镁溶液含水为
28%. 97.5%的硝酸含水量为2.5%. 60%的硝酸镁溶液含水量为40%.则硝酸中水0. 35m-X=
1
(m-X) × 0. 025,则m= 3X硝酸镁中水:0. 28m+X= (m+X) x 0. 4
1 1 2 2
解得m=5X,故二者的比值为0.6.
2
二.
21.【答案】(1)①2H;②O; (2)①CH; ②2; ③氧气
3 4
【解析】(1)2个氢原子表示为2H,臭氧分子为O;
3
(2)据图可知,反应物是甲烷和氧气,其中氧气有剩余,生成物是水和二氧化碳,均为氧
化物。
考点14 碱和碱的化学性质
22.【答案】(1)
俗名 熟石灰 纯碱
化学式 Ca(OH) NaCO
2 2 3
(2)①a ②d ③e
【解析】氢氧化钙俗称熟石灰或消石灰;纯碱是碳酸钠的俗称;可用于去除铁锈的是稀酸
可用于治疗胃酸过多的是小苏打碳酸氢钠,可用于游泳池杀菌消毒的是硫酸铜。
23.
【答案】(1)溶解度都随温度的升高而增大;(2)越大;(3)b;(3)d
【解析】通过示意图可以看出,两种物质的溶解度都随温度的升高而增大;温度越高,相
同质量的水中溶解的溶质越多,所以质量分数越大;保持温度不变,两种饱和溶液混合,
各自的溶质没有改变,但是溶剂变多了,因此都成为了不饱和溶液。
24. 【答案】(1)O ;MnO;(2) ;(3)分离液态空气;(4)淀
2 2
粉或葡萄糖【解析】根据题意可知,物质M是氧气,再据题目信息可知,途径一是高锰酸钾分解,产
生的二氧化锰可做途径二氯酸钾分解和途径三过氧化氢分解的催化剂;途径四是利用分离
液态空气法制取氧气;途径五是光合作用产生氧气,同时产生淀粉或葡萄糖。
25.【答案】(1)CaCO +2HCl==CaCl +H O+CO↑ (2)烧瓶;(3)防止产生的气体从长
3 2 2 2
颈漏斗中逸出;(4)不能控制反应的发生和停止;(5)①85%
设第一次反应中消耗氯化氢的质量为x
CaCO +2HCl==CaCl +H O+CO↑
3 2 2 2
100 73
0.5g x
100/73=0.5g/x
X=0.365g
原稀盐酸中溶质的质量分数为:0.365g/5g×100%=7.3%
【解析】此题是一道实验探究和化学计算的综合题,通过图示可知,制取二氧化碳时,长
颈漏斗的下端管口必须浸没在溶液中,理由是防止产生的气体从长颈漏斗中逸出;图 5和
图7装置相比.利用图5装置来制取二氧化碳,时主要的不足是不能控制反应的发生和停止;
通过表格分析可知,5g的盐酸能反应掉碳酸钙0.5g,所以原来的石灰石是2g,杂质是
0.3g,所以碳酸钙的质量分数为:1.7g/2g×100%=85%,第一次反应消耗碳酸钙0.5g,据
此代入方程式计算即可。
Z6. 【答案】(1)氮气 (2)二氧化碳可溶于水 (3)呼出的气体中氧气的含量低
(4)①O 和CO ②C H O+6O === 6CO + 5H O
2 2 6 10 5 2 2 2
【解析】 通过题目提供的信息可知,呼吸中氮气没有参与,因此呼出的气体中还含有较
多的氮气;因为二氧化碳可溶于水小李同学用排水法收集呼出的气体中二氧化碳的量偏小;
小李同学进行实验时,发现伸人盛有人呼出气休的集气瓶中燃着的小木条先熄灭其原因可
能是呼出的气体中氧气的含量低;由表1可知,室内气体与正常呼出的气体相比较,O 和
2
CO 的含量变化较大,且变化量基本相等
2
27.【答案】(1)+4 (2)CO (3)TiCl+2Mg 高温 Ti+2MgCl (3)⑤ (4)消耗大量
4 2
的电能,浪费能源
【解析】 (1)根据化合物中,化合价的代数和为零,可设钛的化合价为 x,则(+2)+x+
(-2)×3=0 x=+4
(2)根据质量守恒定律可知,反应前后元素的种类不变,因此有毒的气体为CO
(3)据题意可知生成物为单质和化合物,可写。
(4)因为只有反应⑤ 的反应物是一种,所以只有此反应为分解反应。
(5)利用电解熔融TiO 的方法来制备金属钛获得成功,从能量的角度分析要消耗大量的
2
电能,浪费能源。
28.【答案】【实验探究】
序号 实验步骤 实验现象 实验结论
① 取部分固体于试管中,加人足量的固体完全溶解,假设3
水,在试管口播人带火星的木条; 木条复然 不成立
取少量①中溶液于试管中,滴加足量的稀盐有气泡生成 假设2成立
酸(稀硫酸),振荡.
【定性分析】(1)NaOH、NaCO
2 3
(2)过氧化钠和水反应也能生成氢氧化钠
【定量研究】(1)CO +Ca(OH) ==CaCO↓+ H 0;(2)0.8g
2 2 3 2
【反思与提高】NaCO
2 3【解析】此题难度较大,【实验探究】中,因为带火星的木条复燃所以有氧气生成,即过
氧化钠未完全变质,所以猜想3错误;为证明是否有碳酸根,可以加入稀酸。【定性分
析】因加人足量的氯化钙溶液,有白色沉淀生成,说明有碳酸钠,静置,向上层 清液中滴
加2滴无色酚酞试液,溶液变红说明有氢氧化钠。【定量研究】设混合物中的过氧化钠为
x,碳酸钠为y,则
2Na O +2H O=4NaOH+0↑
2 2 2 2
156 32
X 0.64g
156/x=32/0.64g
X=3.12g
Ca(OH) +Na CO==CaCO↓+2NaOH
2 2 3 3
106 100
Y 2.00g
106/100=y/2g
Y=2.12g
所以原混合物中,氢氧化钠的质量为:6.04g-(2.12g+3.12g)=0.8g
29.【答案】(1)2NH+NO ====3N+4HO (2)40% (3)b (4)c (5)化学
2 4 2 4 2 2
【解析】(1)根据反应物和生成物可以写出化学反应方程式;
(2)碳元素的质量分数为:24/(24+8+28)×100%=40%
(3)航天工业使用的一种碳纤维材料,是在碳化硅、陶瓷中嵌入碳纤维而制成,它是一种
复合而成的材料
(4)制成不锈钢是形成合金,增强耐腐蚀性;
[来源:学科网ZXXK]
(5)燃料电池是将化学能转化为电能。
30.【答案】(1)C H+ 5O 点燃 3 CO + 4H O(2)17.6 (3)c (4)b (5)氧气和水
3 8 2 2 2
蒸气
【解析】(1)根据反应物和生成物可以写出化学反应方程式;
(2)根据质量守恒定律可知,反应前后碳的质量相等,所以,生成二氧化碳的质量为:
5.8kg×48/58÷12/44=17.6kg;
(3)铝合金具有金属的特性,因此能导电;
(4)废纸和易拉罐都可以再回收利用;
(5)喷油漆可以防锈蚀的原因是避免钢材与氧气和水蒸气作用生锈。