文档内容
2014年湖南省株洲市中考化学试卷
一、选择题(本题共20小题,每小题2分,共40分.每小题只有一个选项符合题意)
1.(2分)下列物质不属于有机高分子材料的是( )
A.普通玻璃 B.合成纤维 C.天然橡胶 D.塑料薄膜
2.(2分)下列过程发生了化学变化的是( )
A.水的沸腾 B.胆矾研碎 C.过滤液体 D.酸碱中和
3.(2分)今年中国环境日(6月5日)的主题是“向污染宣战”.下列措施会引起环境
污染的是( )
A.合理推广使用新能源 B.大量燃烧含硫燃料
C.控制家用汽车的使用 D.分类回收处理垃圾
4.(2分)下列有关的图示和图标中正确的是( )
A. 浓硫酸的稀释 B. 实验室制取CO
2
C. 当心火灾 D. 禁止吸烟
5.(2分)下列说法正确的是( )
A.化石燃料主要包括煤、石油、天然气,属于可再生能源
B.可燃冰就是干冰,主要成分为CO
2
C.乙醇是一种很好的燃料,属于不可再生能源
D.点燃氢气前一定要检验其纯度
6.(2分)溶液是自然界中常见的物质。下列有关溶液的说法正确的是( )
A.溶液的上层浓度小,下层浓度大
B.溶液蒸干后,均能得到固体溶质
C.溶液中只有一种溶质时,溶液为纯净物
D.物质在溶解得到溶液的过程中,通常有放热或吸热的现象出现7.(2分)下列说法正确的是( )
A.糖类、油脂、蛋白质都是由C、H、O三种元素组成的高分子化合物
B.我们不需要从食物中摄取维生素,因为多数维生素能在人体内合成
C.由于缺碘会引起甲状腺肿大,所以我们要多食用加碘食盐
D.由于霉变食物中含有能损害人的肝脏、诱发肝癌等疾病的黄曲霉毒素,因此,我们
绝对不能食用霉变食物
8.(2分)在光照或点燃条件下,氢气和氯气发生反应生成氯化氢,其反应的微观示意图
如图所示。下列说法正确的是( )
A.所有化学反应在反应前后分子个数都不发生变化
B.此反应过程中只有物质变化,没有能量变化
C.在任何条件下,H 和Cl 均不能大量共存
2 2
D.由微观示意图可知:2gH 和71g Cl 发生反应可生成73g HCl
2 2
9.(2分)人类每时每刻都离不开空气,通过治理,株洲市的空气质量近年来有所好转。
下列有关空气的说法不正确的是( )
A.空气是由多种单质和化合物组成的混合物
B.空气中含量较多且化学性质活泼的是氮气
C.呼吸、燃烧、炼钢、化工生产等都要用到氧气
D.空气是一种宝贵的自然资源,要保护空气,防止污染空气
10.(2分)下列处理方法不正确的是( )
A.炒菜时油锅中的油不慎着火,可用锅盖盖灭
B.扑灭森林火灾有效方法之一是将大火蔓延路线前的 一片树木砍掉,形成隔离带
C.不慎碰倒酒精灯,酒精在桌面上燃烧起来,应立即用水浇灭
D.遇到火灾时,可用湿毛巾捂住口鼻,蹲下靠近地面或沿墙壁跑离着火区域
11.(2分)河水因含有杂质而需要净化.下列操作都是净化水的方法,其中一定需要加
热的是( )
A.过滤 B.吸附 C.蒸馏 D.沉淀
12.(2分)某物质W在空气中完全燃烧后的产物只有二氧化碳和水。根据以上信息,下
列关于物质W组成的说法中正确的是( )
A.含有C、H、O三种元素B.只含C、H元素
C.含有C、H元素,可能含有O元素
D.含有C元素,可能含有H、O元素
13.(2分)中国南车株洲时代集团生产的油电双动力公交车因省油、环保而在全国推广,
双动力公交车制造需要大量使用金属材料.下列有关金属材料的说法正确的是( )
A.金属材料中一定不含有非金属元素
B.多数合金的抗腐蚀性能比组成它们的纯金属更好
C.双动力公交车所有部件都是由金属材料制造的
D.地球上的金属资源是取之不尽、用之不竭的
14.(2分)地球上可利用的淡水不到总水量的1%,我们应爱护水资源.下列有关水的说
法正确的是( )
A.海水都是混合物,淡水都是纯净物
B.通过水的电解实验可以得到“水是由氢气和氧气组成”的结论
C.爱护水资源主要应从节约用水和防治水体污染两方面采取措施
D.硬水是含有可溶性钙、镁化合物的水,软水是不含可溶性钙、镁化合物的水
15.(2分)如图是X、Y、Z、W四种金属与稀盐酸反应状况的示意图,据此判断四种金
属中活动性最弱的是( )
A.X B.Y C.Z D.W
16.(2分)我市湘江风光带桥头广场上介绍侯德榜曾在株洲开办“永利化工厂”,利用
联合制碱法(侯氏制碱法)生产纯碱.下列有关联合制碱法的原料(氯化钠、二氧化碳、
氨气、水)与产品(碳酸钠、氯化铵)的说法不正确的是( )
A.碳酸钠广泛应用于玻璃、造纸、纺织和洗涤剂的生产
B.氯化钠在自然界中分布很广,海洋、盐湖、盐井、盐矿等都是氯化钠的来源
C.侯氏制碱法消耗了二氧化碳,极大地缓解了酸雨的形成
D.氯化铵与熟石灰粉末混合研磨,放出具有刺激性气味的氨气
17.(2分)下列反应中属于置换反应的是( )A.C+CO 2CO
2
B.3CO+Fe O 2Fe+3CO
2 3 2
C.2Na+2H O═2NaOH+H ↑
2 2
D.Cu+4HNO (浓)═Cu(NO ) +2NO ↑+2H O
3 3 2 2 2
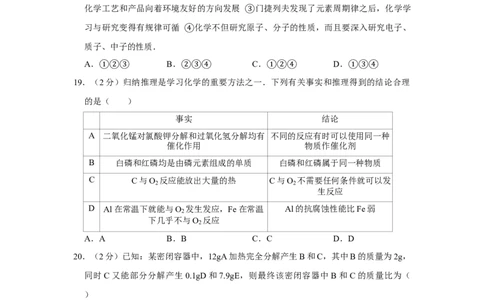
18.(2分)我们学化学、用化学、爱化学.下列有关化学的说法中合理的是( )
化学在保证人类生存与不断提高生活质量方面起着重要的作用 绿色化学使更多的
①化学工艺和产品向着环境友好的方向发展 门捷列夫发现了元素②周期律之后,化学学
习与研究变得有规律可循 化学不但研究③原子、分子的性质,而且要深入研究电子、
质子、中子的性质. ④
A. B. C. D.
19.(①2分②)③归纳推理是学习②化③学的④重要方法之一.①下②列④有关事实和推理①得到③的④结论合理
的是( )
事实 结论
A 二氧化锰对氯酸钾分解和过氧化氢分解均有 不同的反应有时可以使用同一种
催化作用 物质作催化剂
B 白磷和红磷均是由磷元素组成的单质 白磷和红磷属于同一种物质
C C与O 反应能放出大量的热 C与O 不需要任何条件就可以发
2 2
生反应
D Al在常温下就能与O 发生发应,Fe在常温 Al的抗腐蚀性能比Fe弱
2
下几乎不与O 反应
2
A.A B.B C.C D.D
20.(2分)已知:某密闭容器中,12gA加热完全分解产生B和C,其中B的质量为2g,
同时C又能部分分解产生0.1gD和7.9gE,则最终该密闭容器中B和C的质量比为(
)
A.1:1 B.1:2 C.1:4 D.1:5
二、填空题(本题共6小题,共22分)
21.(4分)请用化学用语填空:
(1)2个镁离子 ;
(2)生理盐水中的溶剂分子 ;
(3)硝酸铵的化学式 ;
(4)钻石的主要成分 .22.(4分)现有CO 、H O、CH 、NO (二氧化氮)、O 、SO 、NO(一氧化氮)等七
2 2 4 2 3 2
种物质.
(1)其中不属于氧化物的是 .
(2)二氧化硫与二氧化碳一样,都能与水发生化合反应.请写出二氧化硫与水反应的
生成物的化学式 .
(3)一氧化氮与氧气化合可生成二氧化氮,请写出反应的化学方程式 .
23.(3分)如图中A、B、C、D是四种粒子的结构示意图,请回答下列问题:
(1)以上四种结构示意图所表示的粒子中,属于非金属元素的是 (填字母代
号)。
(2)以上四种结构示意图所表示的粒子中,易失去电子的是 (填字母代号)。
(3)C中x= 。
24.(3分)混盐一般是由一种阳离子与两种酸根离子组成的盐,如:Ca(NO )Cl.漂白
3
粉中有一种混盐CaOCl (其中钙元素的化合价为+2,氧元素的化合价为﹣2).
2
(1)已知CaOCl 中的一种酸根离子是次氯酸根离子(ClO﹣),则另一种酸根离子对
2
应的酸的化学式为 .若将该混盐改写成如Ca(NO )Cl的形式,其化学式可表
3
示为 .
(2)在Ca(NO )Cl中氮元素的化合价为 .
3
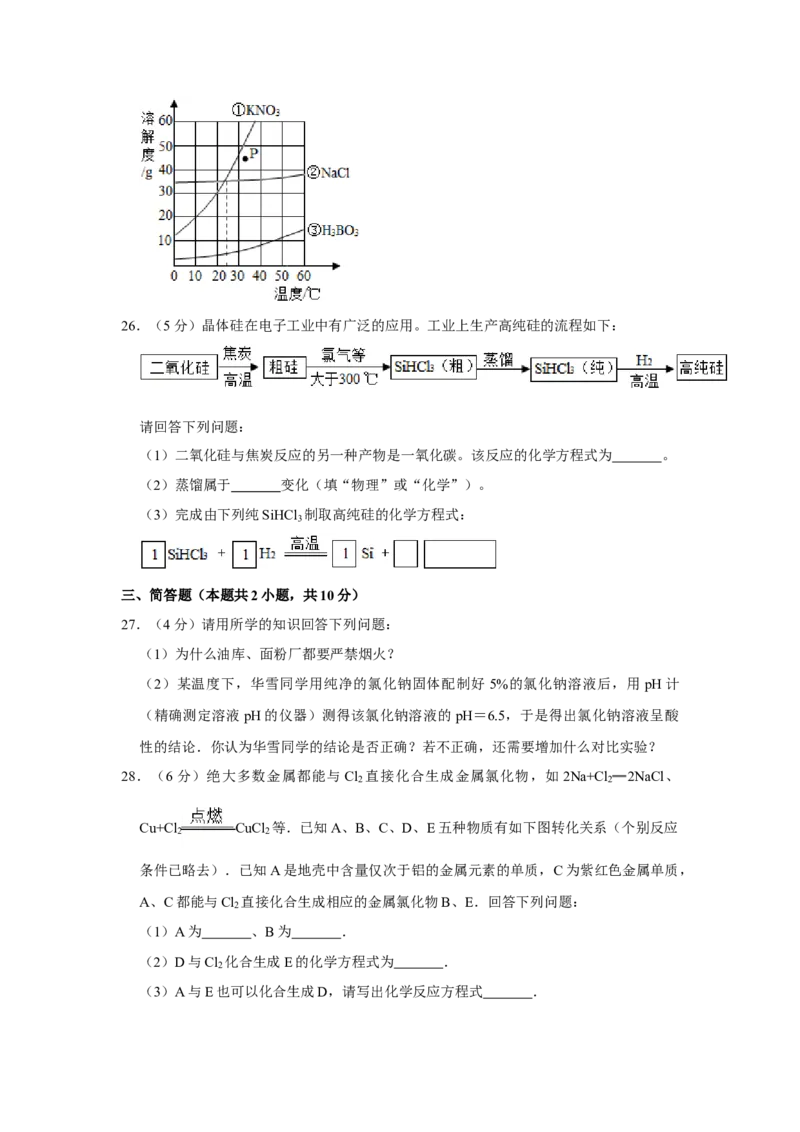
25.(3分)如图所示为 硝酸钾、 氯化钠、 硼酸(H BO )的溶解度曲线图。由图
3 3
可知: ① ② ③
(1)当温度为 25℃时,硝酸钾、氯化钠和硼酸三种物质的溶解度大小关系为
(请用序号作答)。
(2)图中P点表示硝酸钾的 (填“饱和”或“不饱和”)溶液。
(3)从图中可得到的有关硼酸溶解度的信息有:硼酸的溶解度随着温度的升高逐渐增
大、 (任写一条)等。26.(5分)晶体硅在电子工业中有广泛的应用。工业上生产高纯硅的流程如下:
请回答下列问题:
(1)二氧化硅与焦炭反应的另一种产物是一氧化碳。该反应的化学方程式为 。
(2)蒸馏属于 变化(填“物理”或“化学”)。
(3)完成由下列纯SiHCl 制取高纯硅的化学方程式:
3
三、简答题(本题共2小题,共10分)
27.(4分)请用所学的知识回答下列问题:
(1)为什么油库、面粉厂都要严禁烟火?
(2)某温度下,华雪同学用纯净的氯化钠固体配制好 5%的氯化钠溶液后,用pH计
(精确测定溶液pH的仪器)测得该氯化钠溶液的pH=6.5,于是得出氯化钠溶液呈酸
性的结论.你认为华雪同学的结论是否正确?若不正确,还需要增加什么对比实验?
28.(6分)绝大多数金属都能与Cl 直接化合生成金属氯化物,如2Na+Cl ═2NaCl、
2 2
Cu+Cl CuCl 等.已知A、B、C、D、E五种物质有如下图转化关系(个别反应
2 2
条件已略去).已知A是地壳中含量仅次于铝的金属元素的单质,C为紫红色金属单质,
A、C都能与Cl 直接化合生成相应的金属氯化物B、E.回答下列问题:
2
(1)A为 、B为 .
(2)D与Cl 化合生成E的化学方程式为 .
2
(3)A与E也可以化合生成D,请写出化学反应方程式 .四、实验与探究题(本题共2小题,共18分)
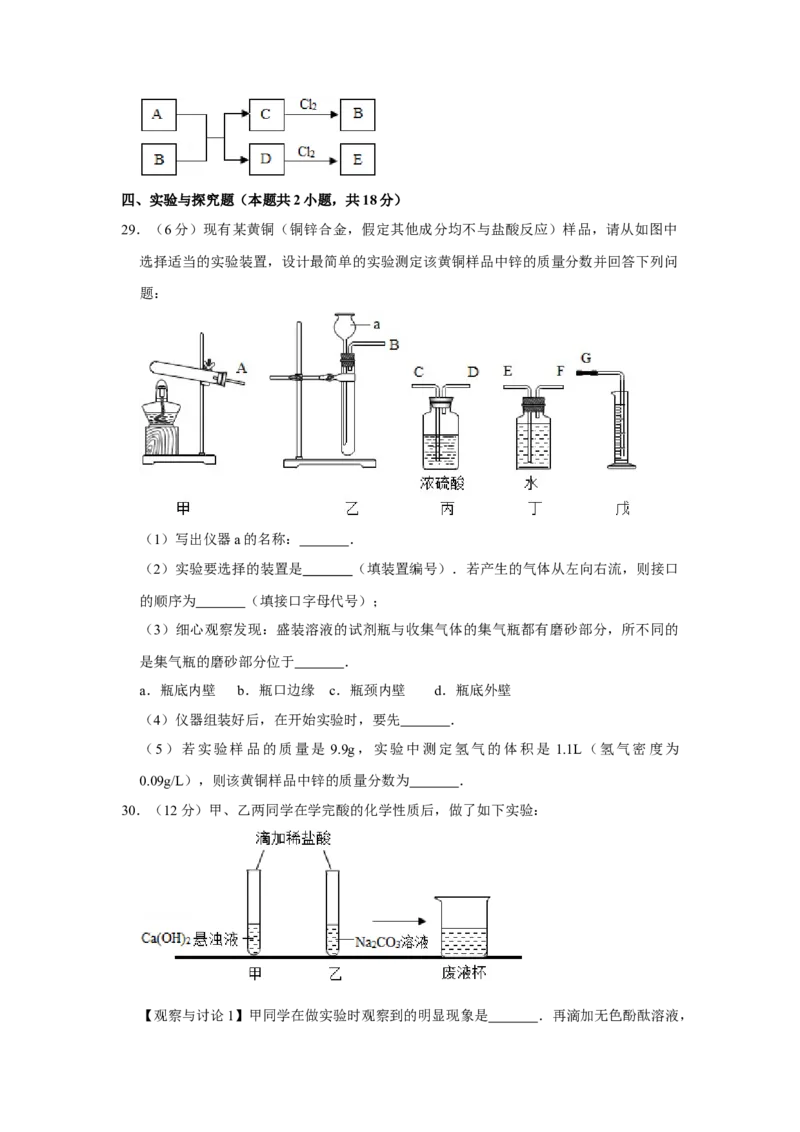
29.(6分)现有某黄铜(铜锌合金,假定其他成分均不与盐酸反应)样品,请从如图中
选择适当的实验装置,设计最简单的实验测定该黄铜样品中锌的质量分数并回答下列问
题:
(1)写出仪器a的名称: .
(2)实验要选择的装置是 (填装置编号).若产生的气体从左向右流,则接口
的顺序为 (填接口字母代号);
(3)细心观察发现:盛装溶液的试剂瓶与收集气体的集气瓶都有磨砂部分,所不同的
是集气瓶的磨砂部分位于 .
a.瓶底内壁 b.瓶口边缘 c.瓶颈内壁 d.瓶底外壁
(4)仪器组装好后,在开始实验时,要先 .
(5)若实验样品的质量是 9.9g,实验中测定氢气的体积是 1.1L(氢气密度为
0.09g/L),则该黄铜样品中锌的质量分数为 .
30.(12分)甲、乙两同学在学完酸的化学性质后,做了如下实验:
【观察与讨论1】甲同学在做实验时观察到的明显现象是 .再滴加无色酚酞溶液,无明显现象(已知CaCl 溶液呈中性).
2
【观察与讨论2】乙同学在做实验时开始没有观察到气泡产生,于是对碳酸钠能否与盐
酸反应表示怀疑.甲同学通过查阅资料得知:在碳酸钠溶液中滴加少量稀盐酸,先发生
反 应 Na CO +HCl═ NaCl+NaHCO , 继 续 滴 加 稀 盐 酸 , 再 发 生 反 应
2 3 3
NaHCO +HCl═NaCl+H O+CO ↑.所以甲同学认为,乙同学实验时还应 ,才能
3 2 2
观察到有气泡产生.
【观察与讨论3】甲同学先将废液缓慢倒入一洁净的废液杯中,乙同学在观察到气泡产
生后,也将实验废液缓慢倒入该废液杯中,没有观察到明显现象.经过讨论确定,甲同
学的试管中废液含有的溶质一定有 ,乙同学的试管中废液含有的溶质一定有
(均写化学式).
为了处理实验后产生的废液,甲、乙同学决定对废液杯中最终废液溶质的成分进行探究.
【提出问题】最终废液中含有什么溶质?
【猜想与假设】猜想1:废液中含有 (写化学式)两种溶质.
猜想2:废液中含有 (写化学式)三种溶质.
猜想3:废液中含有NaHCO 、CaCl 、NaCl三种溶质.
3 2
【活动与探究】甲、乙同学为了验证猜想,进行了如下实验:
甲同学实验:取少量废液于试管中,向其中滴加盐酸,无气泡产生.
乙同学实验:取少量废液于试管中,向其中滴加紫色石蕊试液,溶液变红色.
【结论与反思】(1)猜想 (填“1”或“2”或“3”)正确.
(2)要得到相同的结论,还可采用很多种方法.如加入氧化铁粉末,可观察到溶液呈
色,该反应的化学方程式为 .
【表达与交流】甲、乙同学确认了最终废液中溶质的成分,若直接排放,可能造成的危
害是 ,你认为处理该废液的方法是 .
五、计算题(本题共2小题,共10分)
31.(4分)人体胃酸过多会引起胃病.如图所示为某抗酸药包装标签上的部分文字,请
回答下列问题.
(1)Al(OH) 的相对分子质量为 .
3
(2)经测定,每片该抗酸药实含氢氧化铝234mg.计算一片该抗酸药可消耗7.3%的盐
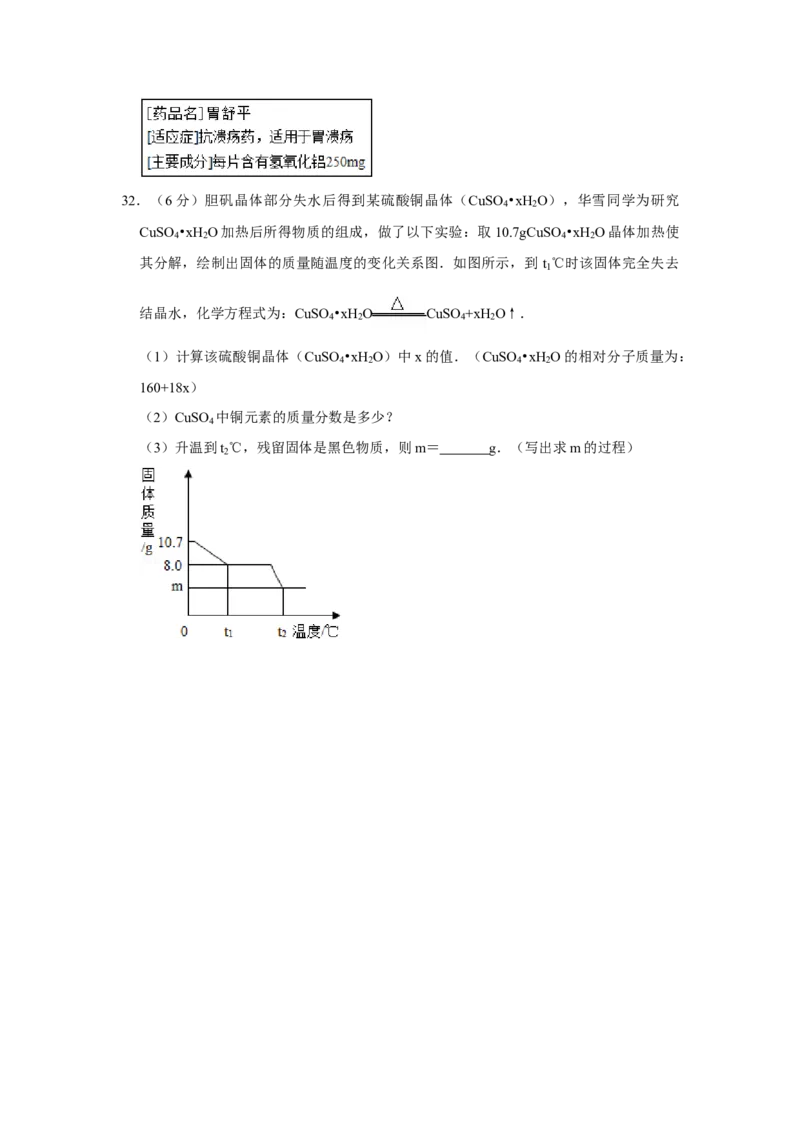
酸多少克(请写出计算过程)?32.(6分)胆矾晶体部分失水后得到某硫酸铜晶体(CuSO •xH O),华雪同学为研究
4 2
CuSO •xH O加热后所得物质的组成,做了以下实验:取10.7gCuSO •xH O晶体加热使
4 2 4 2
其分解,绘制出固体的质量随温度的变化关系图.如图所示,到 t ℃时该固体完全失去
1
结晶水,化学方程式为:CuSO •xH O CuSO +xH O↑.
4 2 4 2
(1)计算该硫酸铜晶体(CuSO •xH O)中x的值.(CuSO •xH O的相对分子质量为:
4 2 4 2
160+18x)
(2)CuSO 中铜元素的质量分数是多少?
4
(3)升温到t ℃,残留固体是黑色物质,则m= g.(写出求m的过程)
2