文档内容
曲靖一中 2026 届高三年级教学质量检测三
化 学 试 卷
注意事项:
1. 答卷前,考生务必用黑色字迹钢笔或签字笔将自己的姓名、考生号、考场号和座位号填
写在答题卡上。
2. 作答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目选项的答案信息点
涂黑;如需改动,用橡皮擦干净后,再选涂其他答案,答在试卷上无效。
3. 本试卷共 8 页,共 18 小题,满分 100 分。考试用时 75 分钟。
4. 本试卷可能用到的相对分子质量:H-1 O-16 Na-23 N-14
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.93阅兵中,打击范围覆盖全球的“DF—5C”液体洲际战略核导弹震撼亮相。下列关于
“DF—5C”涉及的化学知识说法错误的是
A.“DF—5C”采用二级液体燃料火箭发动机,其燃料偏二甲肼C H N 与N O 反应时,
2 8 2 2 4
偏二甲肼作还原剂
B.导弹的贮箱采用高强度铝铜合金,该合金的熔点比纯铝和纯铜低
C.导弹可携带多个分导核弹头,制造弹头的材料中涉及一些放射性元素,这些元素发
生的核反应属于化学变化
D.导弹中的部分耐高温部件使用了碳化硅陶瓷,是新型无机非金属材料,
2.劳动是“知行合一”有力的手段。下列劳动项目与所述化学知识存在关联的是
选项 劳动项目 化学知识
A 家务劳动:食醋清除水壶中的少量水垢 醋酸的酸性比碳酸强
B 农业生产:石膏改良盐碱土壤 硫酸钙显酸性
C 水厂帮工:用Na S除去废水中Cu2+和Hg2+ Na S具有还原性
2 2
D 船厂研学:轮船船体镶嵌镁合金 主要是镁有导电性
第1页,共10页
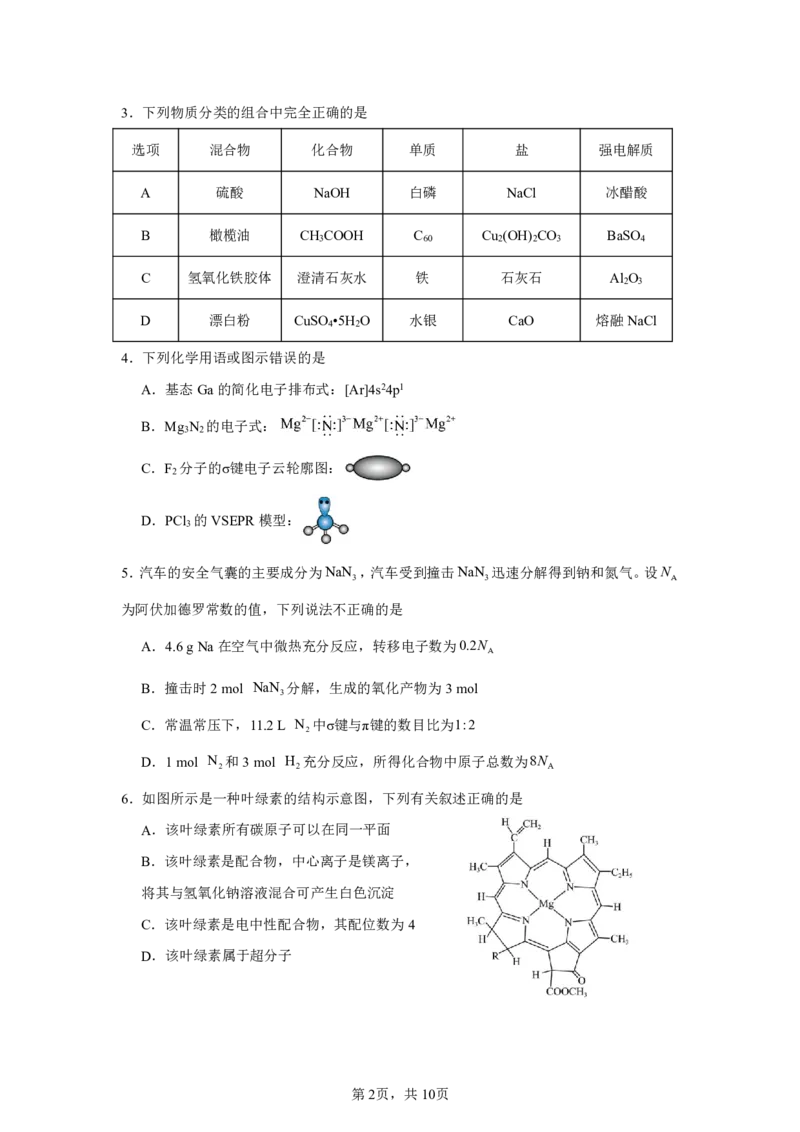
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}3.下列物质分类的组合中完全正确的是
选项 混合物 化合物 单质 盐 强电解质
A 硫酸 NaOH 白磷 NaCl 冰醋酸
B 橄榄油 CH COOH C Cu (OH) CO BaSO
3 60 2 2 3 4
C 氢氧化铁胶体 澄清石灰水 铁 石灰石 Al O
2 3
D 漂白粉 CuSO •5H O 水银 CaO 熔融NaCl
4 2
4.下列化学用语或图示错误的是
A.基态Ga的简化电子排布式:[Ar]4s24p1
B.Mg N 的电子式:
3 2
C.F 分子的σ键电子云轮廓图:
2
D.PCl 的VSEPR模型:
3
5.汽车的安全气囊的主要成分为NaN ,汽车受到撞击NaN 迅速分解得到钠和氮气。设N
3 3 A
为阿伏加德罗常数的值,下列说法不正确的是
A.4.6gNa在空气中微热充分反应,转移电子数为0.2N
A
B.撞击时2mol NaN 分解,生成的氧化产物为3mol
3
C.常温常压下,11.2L N 中σ键与π键的数目比为1:2
2
D.1mol N 和3mol H 充分反应,所得化合物中原子总数为8N
2 2 A
6.如图所示是一种叶绿素的结构示意图,下列有关叙述正确的是
A.该叶绿素所有碳原子可以在同一平面
B.该叶绿素是配合物,中心离子是镁离子,
将其与氢氧化钠溶液混合可产生白色沉淀
C.该叶绿素是电中性配合物,其配位数为4
D.该叶绿素属于超分子
第2页,共10页
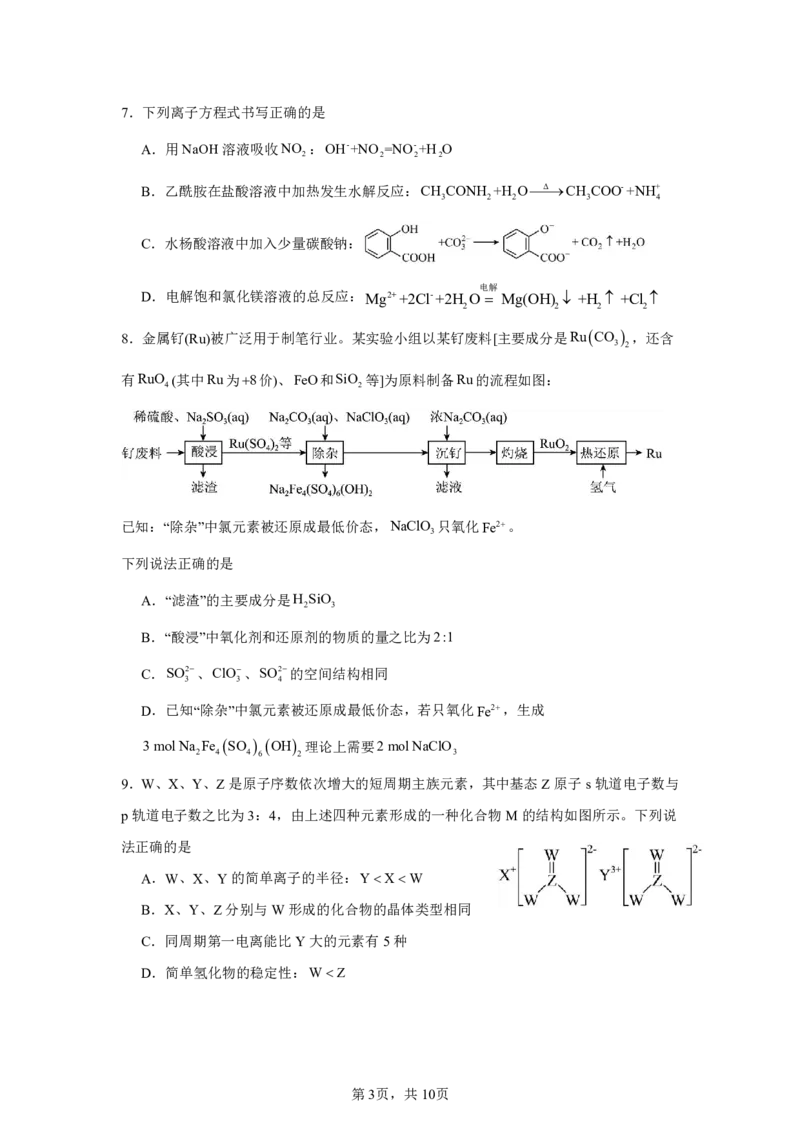
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}7.下列离子方程式书写正确的是
A.用NaOH溶液吸收NO :OH-+NO =NO-+H O
2 2 2 2
B.乙酰胺在盐酸溶液中加热发生水解反应:CH CONH +H OΔCH COO-+NH+
3 2 2 3 4
C.水杨酸溶液中加入少量碳酸钠:
电解
D.电解饱和氯化镁溶液的总反应: Mg2++2Cl-+2H O Mg(OH) +H +Cl
2 2 2 2
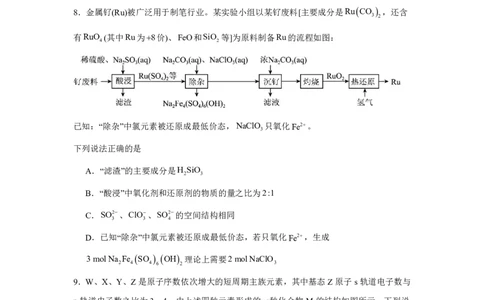
8.金属钌(Ru)被广泛用于制笔行业。某实验小组以某钌废料[主要成分是RuCO ,还含
3 2
有RuO (其中Ru为8价)、FeO和SiO 等]为原料制备Ru的流程如图:
4 2
已知:“除杂”中氯元素被还原成最低价态,NaClO 只氧化Fe2。
3
下列说法正确的是
A.“滤渣”的主要成分是H SiO
2 3
B.“酸浸”中氧化剂和还原剂的物质的量之比为2:1
C.SO2、ClO、SO2的空间结构相同
3 3 4
D.已知“除杂”中氯元素被还原成最低价态,若只氧化Fe2,生成
3 mol Na Fe SO OH 理论上需要2 mol NaClO
2 4 4 6 2 3
9.W、X、Y、Z是原子序数依次增大的短周期主族元素,其中基态Z原子s轨道电子数与
p轨道电子数之比为3:4,由上述四种元素形成的一种化合物M的结构如图所示。下列说
法正确的是
A.W、X、Y的简单离子的半径:YXW
B.X、Y、Z分别与W形成的化合物的晶体类型相同
C.同周期第一电离能比Y大的元素有5种
D.简单氢化物的稳定性:WZ
第3页,共10页
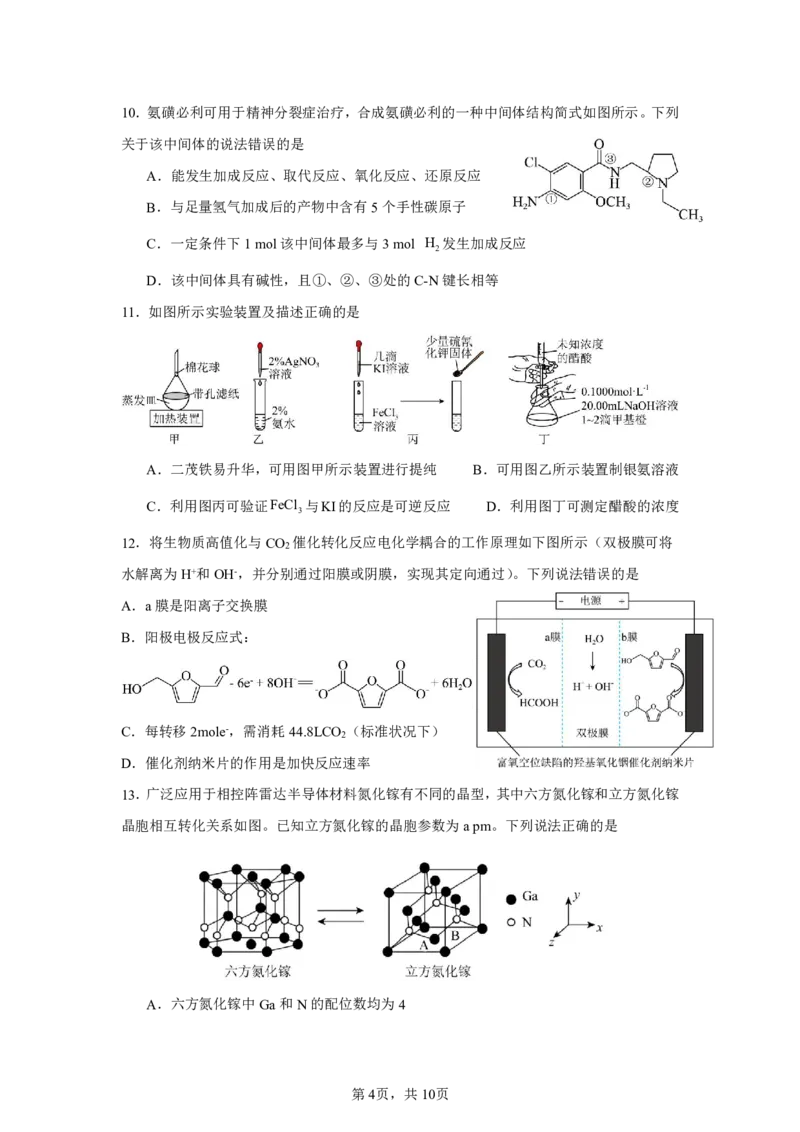
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}10.氨磺必利可用于精神分裂症治疗,合成氨磺必利的一种中间体结构简式如图所示。下列
关于该中间体的说法错误的是
A.能发生加成反应、取代反应、氧化反应、还原反应
B.与足量氢气加成后的产物中含有5个手性碳原子
C.一定条件下1mol该中间体最多与3mol H 发生加成反应
2
D.该中间体具有碱性,且①、②、③处的C-N键长相等
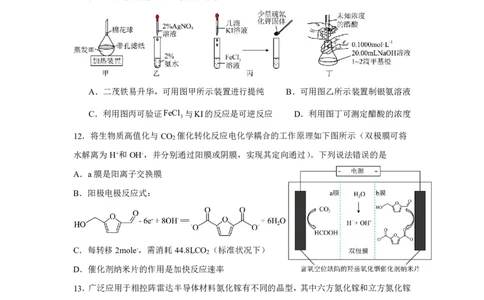
11.如图所示实验装置及描述正确的是
A.二茂铁易升华,可用图甲所示装置进行提纯 B.可用图乙所示装置制银氨溶液
C.利用图丙可验证FeCl 与KI的反应是可逆反应 D.利用图丁可测定醋酸的浓度
3
12.将生物质高值化与CO 催化转化反应电化学耦合的工作原理如下图所示(双极膜可将
2
水解离为H+和OH-,并分别通过阳膜或阴膜,实现其定向通过)。下列说法错误的是
A.a膜是阳离子交换膜
B.阳极电极反应式:
C.每转移2mole-,需消耗44.8LCO (标准状况下)
2
D.催化剂纳米片的作用是加快反应速率
13.广泛应用于相控阵雷达半导体材料氮化镓有不同的晶型,其中六方氮化镓和立方氮化镓
晶胞相互转化关系如图。已知立方氮化镓的晶胞参数为apm。下列说法正确的是
A.六方氮化镓中Ga和N的配位数均为4
第4页,共10页
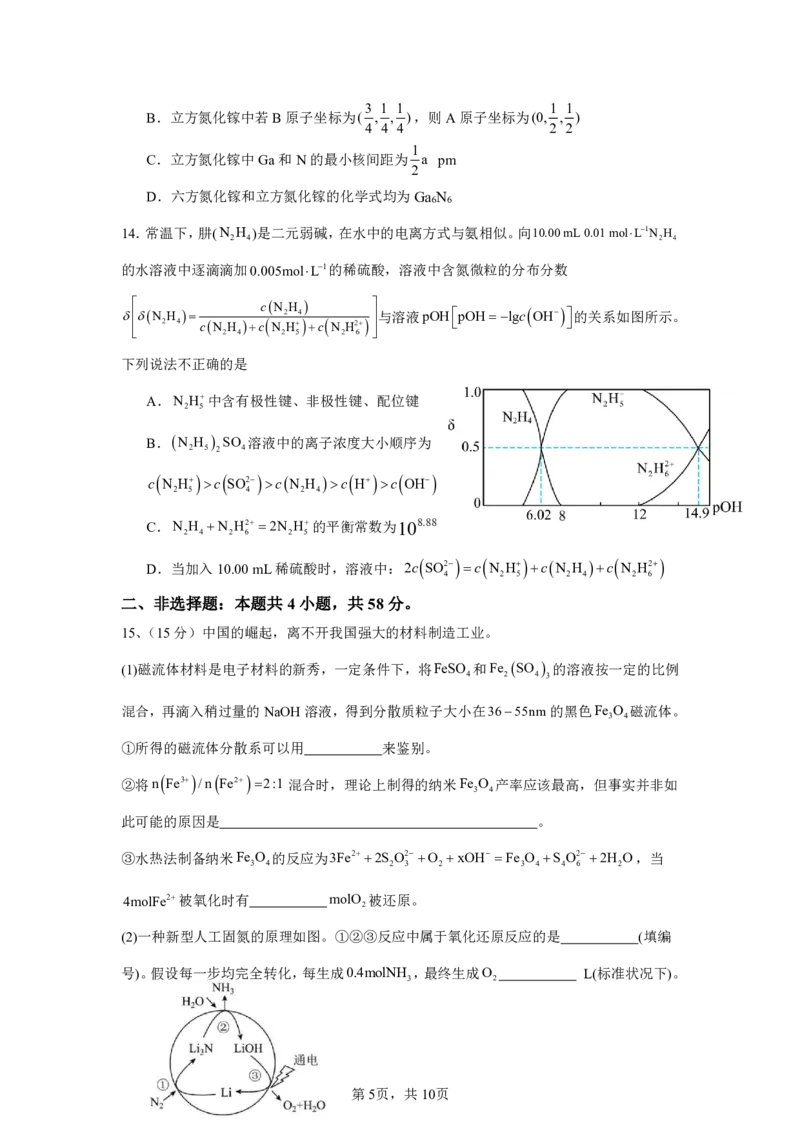
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}3 1 1 1 1
B.立方氮化镓中若B原子坐标为( , , ),则A原子坐标为(0, , )
4 4 4 2 2
1
C.立方氮化镓中Ga和N的最小核间距为 a pm
2
D.六方氮化镓和立方氮化镓的化学式均为Ga N
6 6
14.常温下,肼(N H )是二元弱碱,在水中的电离方式与氨相似。向10.00 mL 0.01 molL1N H
2 4 2 4
的水溶液中逐滴滴加0.005molL1的稀硫酸,溶液中含氮微粒的分布分数
N H cN 2 H 4 与溶液pOHpOHlgc OH的关系如图所示。
2 4 cN H c N H c N H2
2 4 2 5 2 6
下列说法不正确的是
A.N H中含有极性键、非极性键、配位键
2 5
B.N H SO 溶液中的离子浓度大小顺序为
2 5 2 4
c N H c SO2 cN H c H c OH
2 5 4 2 4
C.N H N H2 2N H的平衡常数为108.88
2 4 2 6 2 5
D.当加入10.00mL稀硫酸时,溶液中:2c SO2 c N H cN H c N H2
4 2 5 2 4 2 6
二、非选择题:本题共 4小题,共 58分。
15、(15分)中国的崛起,离不开我国强大的材料制造工业。
(1)磁流体材料是电子材料的新秀,一定条件下,将FeSO 和Fe SO 的溶液按一定的比例
4 2 4 3
混合,再滴入稍过量的NaOH溶液,得到分散质粒子大小在3655nm的黑色Fe O 磁流体。
3 4
①所得的磁流体分散系可以用 来鉴别。
②将n
Fe3
/n
Fe2
2:1混合时,理论上制得的纳米Fe O 产率应该最高,但事实并非如
3 4
此可能的原因是 。
③水热法制备纳米Fe O 的反应为3Fe2 2S O2O xOH Fe O S O22H O,当
3 4 2 3 2 3 4 4 6 2
4molFe2被氧化时有 molO 被还原。
2
(2)一种新型人工固氮的原理如图。①②③反应中属于氧化还原反应的是 (填编
号)。假设每一步均完全转化,每生成0.4molNH ,最终生成O L(标准状况下)。
3 2
第5页,共10页
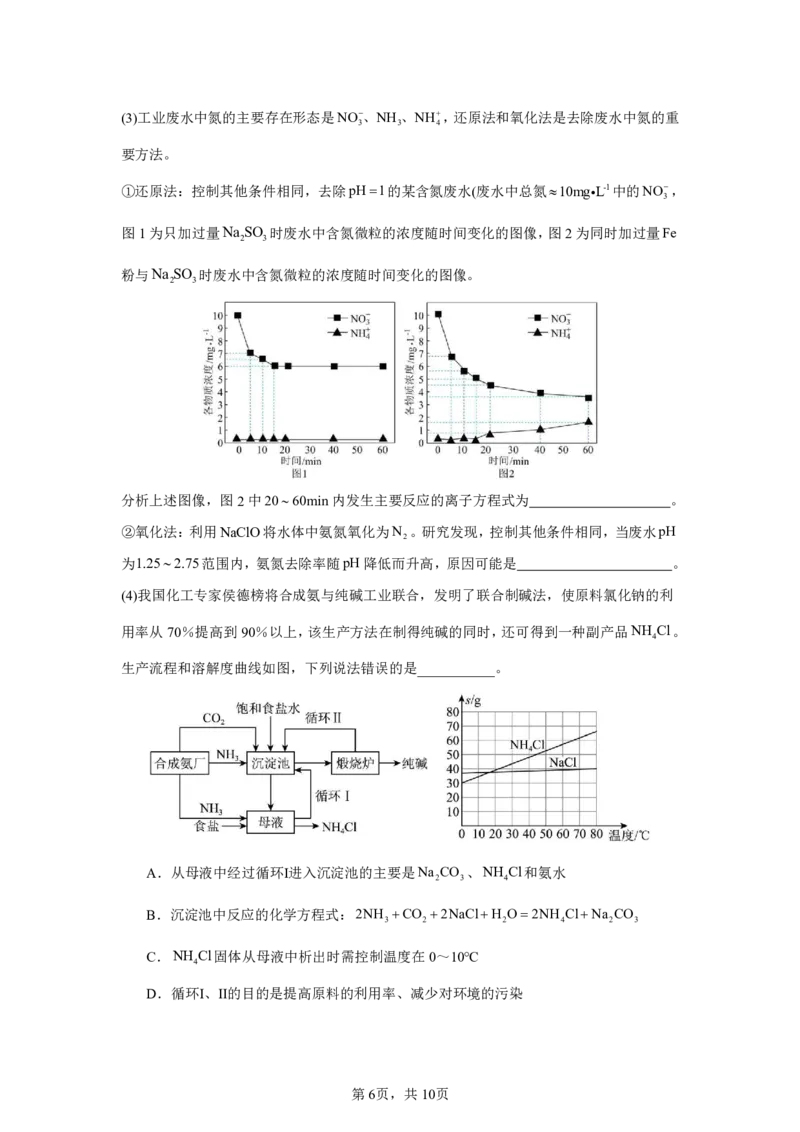
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}(3)工业废水中氮的主要存在形态是NO、NH、NH,还原法和氧化法是去除废水中氮的重
3 3 4
要方法。
①还原法:控制其他条件相同,去除pH1的某含氮废水(废水中总氮10mgL-1中的NO,
3
图1为只加过量Na SO 时废水中含氮微粒的浓度随时间变化的图像,图2为同时加过量Fe
2 3
粉与Na SO 时废水中含氮微粒的浓度随时间变化的图像。
2 3
分析上述图像,图2中2060min内发生主要反应的离子方程式为 。
②氧化法:利用NaClO将水体中氨氮氧化为N 。研究发现,控制其他条件相同,当废水pH
2
为1.252.75范围内,氨氮去除率随pH降低而升高,原因可能是 。
(4)我国化工专家侯德榜将合成氨与纯碱工业联合,发明了联合制碱法,使原料氯化钠的利
用率从70%提高到90%以上,该生产方法在制得纯碱的同时,还可得到一种副产品NH Cl。
4
生产流程和溶解度曲线如图,下列说法错误的是___________。
A.从母液中经过循环Ⅰ进入沉淀池的主要是Na CO 、NH Cl和氨水
2 3 4
B.沉淀池中反应的化学方程式:2NH CO 2NaClH O2NH ClNa CO
3 2 2 4 2 3
C.NH Cl固体从母液中析出时需控制温度在0~10℃
4
D.循环Ⅰ、Ⅱ的目的是提高原料的利用率、减少对环境的污染
第6页,共10页
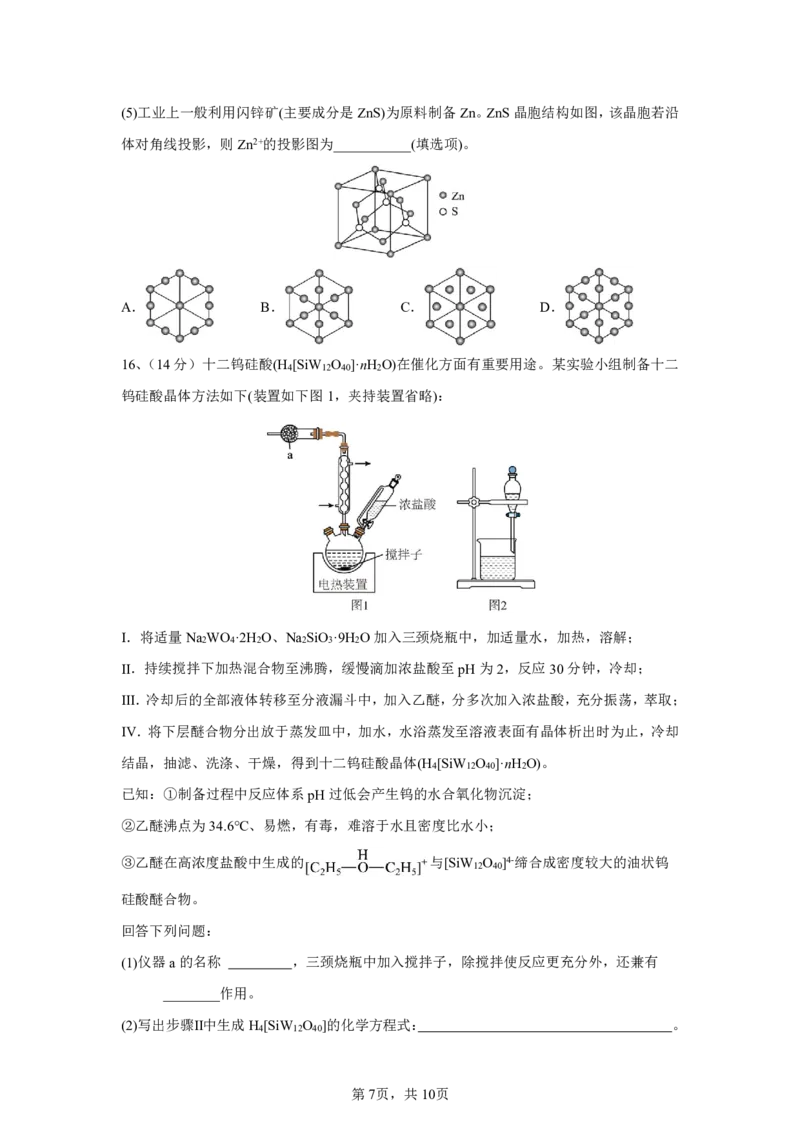
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}(5)工业上一般利用闪锌矿(主要成分是ZnS)为原料制备Zn。ZnS晶胞结构如图,该晶胞若沿
体对角线投影,则Zn2+的投影图为___________(填选项)。
A. B. C. D.
16、(14分)十二钨硅酸(H [SiW O ]·nH O)在催化方面有重要用途。某实验小组制备十二
4 12 40 2
钨硅酸晶体方法如下(装置如下图1,夹持装置省略):
Ⅰ.将适量Na WO ·2H O、Na SiO ·9H O加入三颈烧瓶中,加适量水,加热,溶解;
2 4 2 2 3 2
Ⅱ.持续搅拌下加热混合物至沸腾,缓慢滴加浓盐酸至pH为2,反应30分钟,冷却;
Ⅲ.冷却后的全部液体转移至分液漏斗中,加入乙醚,分多次加入浓盐酸,充分振荡,萃取;
Ⅳ.将下层醚合物分出放于蒸发皿中,加水,水浴蒸发至溶液表面有晶体析出时为止,冷却
结晶,抽滤、洗涤、干燥,得到十二钨硅酸晶体(H [SiW O ]·nH O)。
4 12 40 2
已知:①制备过程中反应体系pH过低会产生钨的水合氧化物沉淀;
②乙醚沸点为34.6℃、易燃,有毒,难溶于水且密度比水小;
③乙醚在高浓度盐酸中生成的 与[SiW O ]4-缔合成密度较大的油状钨
12 40
硅酸醚合物。
回答下列问题:
(1)仪器a的名称 ,三颈烧瓶中加入搅拌子,除搅拌使反应更充分外,还兼有
________作用。
(2)写出步骤Ⅱ中生成H [SiW O ]的化学方程式: 。
4 12 40
第7页,共10页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}(3)步骤Ⅲ不能用乙醇替代乙醚作萃取剂的主要原因是 ;该步骤应在下列
(填选项)条件下进行操作。
A. B. C.
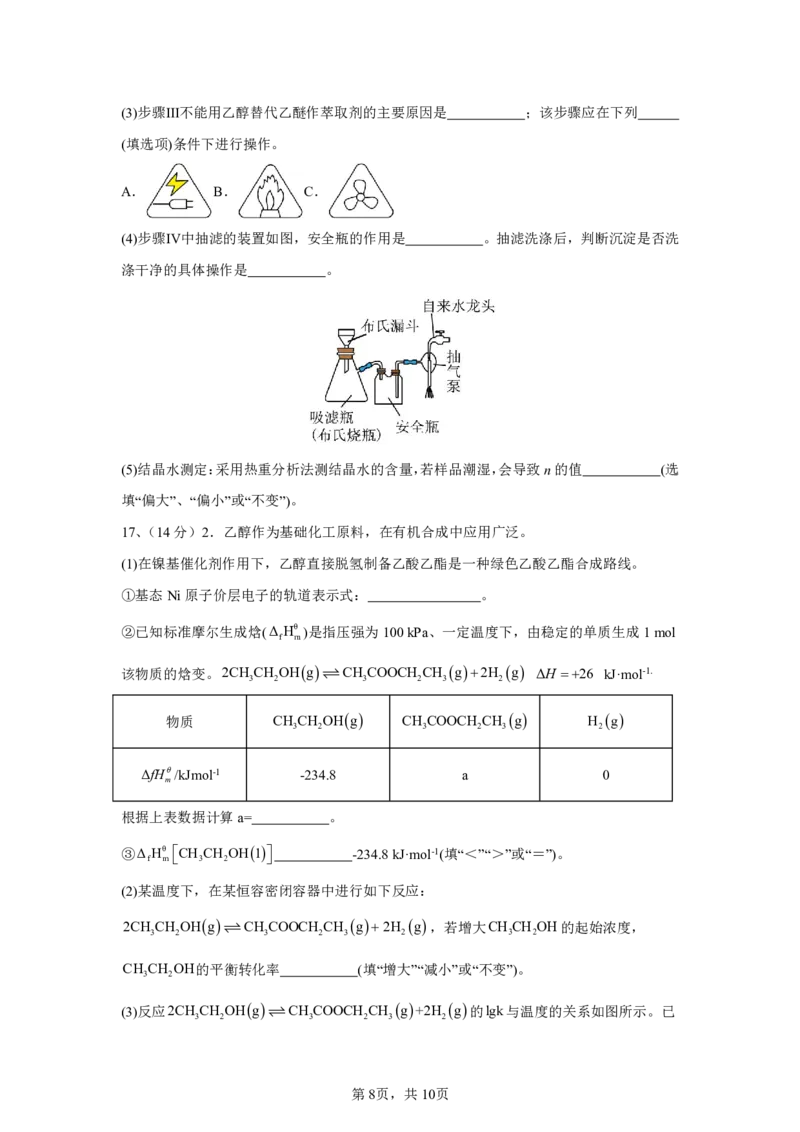
(4)步骤Ⅳ中抽滤的装置如图,安全瓶的作用是 。抽滤洗涤后,判断沉淀是否洗
涤干净的具体操作是 。
(5)结晶水测定:采用热重分析法测结晶水的含量,若样品潮湿,会导致n的值 (选
填“偏大”、“偏小”或“不变”)。
17、(14分)2.乙醇作为基础化工原料,在有机合成中应用广泛。
(1)在镍基催化剂作用下,乙醇直接脱氢制备乙酸乙酯是一种绿色乙酸乙酯合成路线。
①基态Ni原子价层电子的轨道表示式: 。
②已知标准摩尔生成焓(Δ Hθ )是指压强为100kPa、一定温度下,由稳定的单质生成1mol
f m
该物质的焓变。2CH CH OHg CH COOCH CH g2H g ΔH 26 kJ·mol-1.
3 2 3 2 3 2
物质 CH CH OHg CH COOCH CH g H g
3 2 3 2 3 2
ΔfH/kJmol-1 -234.8 a 0
m
根据上表数据计算a= 。
③Δ f Hθ m CH 3 CH 2 OH1 -234.8kJ·mol-1(填“<”“>”或“=”)。
(2)某温度下,在某恒容密闭容器中进行如下反应:
2CH CH OHg CH COOCH CH g 2H g,若增大CH CH OH的起始浓度,
3 2 3 2 3 2 3 2
CH CH OH的平衡转化率 (填“增大”“减小”或“不变”)。
3 2
(3)反应2CH CH OHg CH COOCH CH g+2H g的lgk与温度的关系如图所示。已
3 2 3 2 3 2
第8页,共10页
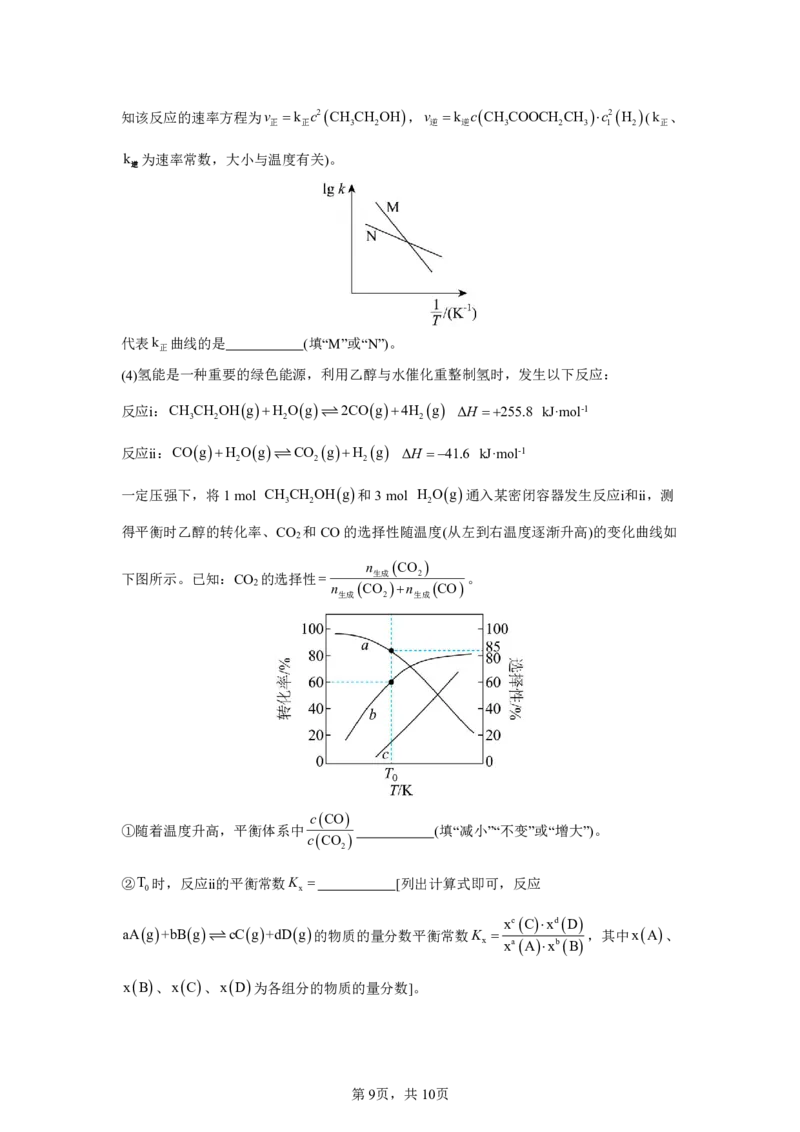
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}知该反应的速率方程为v k c2CH CH OH,v k cCH COOCH CH c2H (k 、
正 正 3 2 逆 逆 3 2 3 1 2 正
k 为速率常数,大小与温度有关)。
逆
代表k 曲线的是 (填“M”或“N”)。
正
(4)氢能是一种重要的绿色能源,利用乙醇与水催化重整制氢时,发生以下反应:
反应ⅰ:CH CH OHgH Og 2COg4H g ΔH 255.8 kJ·mol-1
3 2 2 2
反应ⅱ:COgH Og CO gH g ΔH 41.6 kJ·mol-1
2 2 2
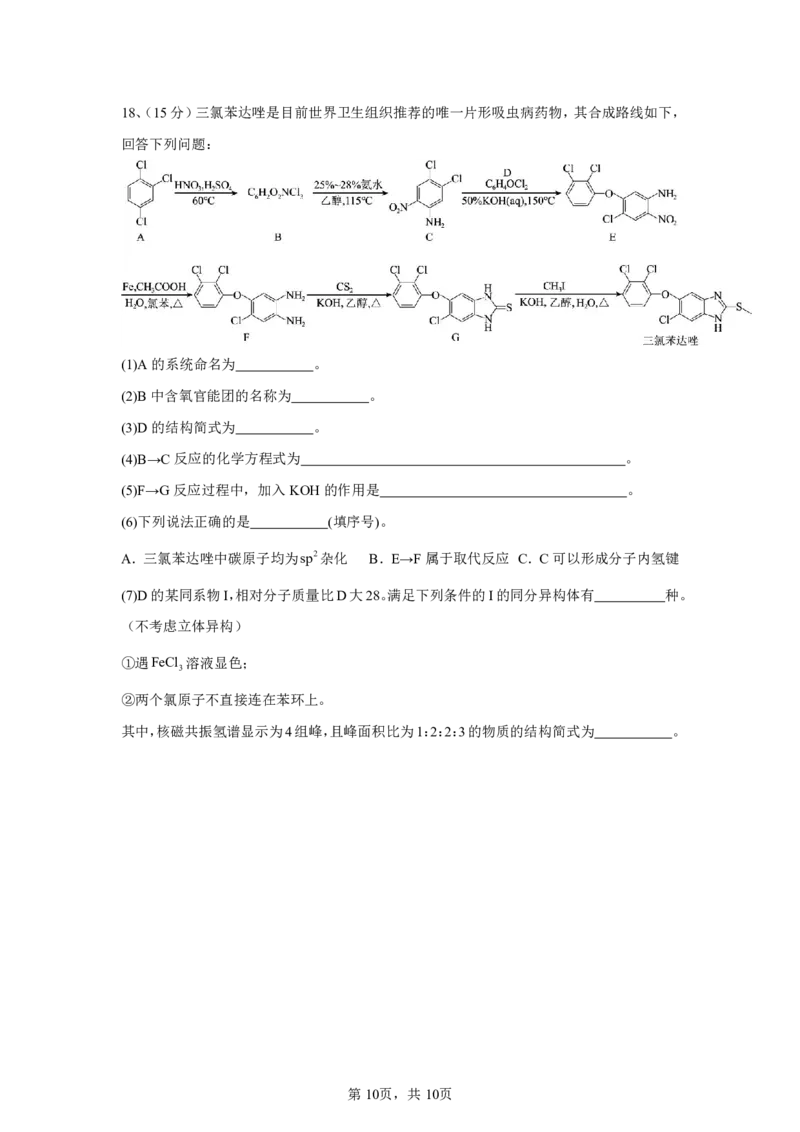
一定压强下,将1mol CH CH OHg和3mol H Og通入某密闭容器发生反应ⅰ和ⅱ,测
3 2 2
得平衡时乙醇的转化率、CO 和CO的选择性随温度(从左到右温度逐渐升高)的变化曲线如
2
n CO
下图所示。已知:CO 的选择性 生成 2 。
2 n CO n CO
生成 2 生成
cCO
①随着温度升高,平衡体系中 (填“减小”“不变”或“增大”)。
cCO
2
②T 时,反应ⅱ的平衡常数K [列出计算式即可,反应
0 x
xcCxdD
aAg+bBg cCg+dDg的物质的量分数平衡常数K ,其中xA、
x xaAxbB
xB、xC、xD为各组分的物质的量分数]。
第9页,共10页
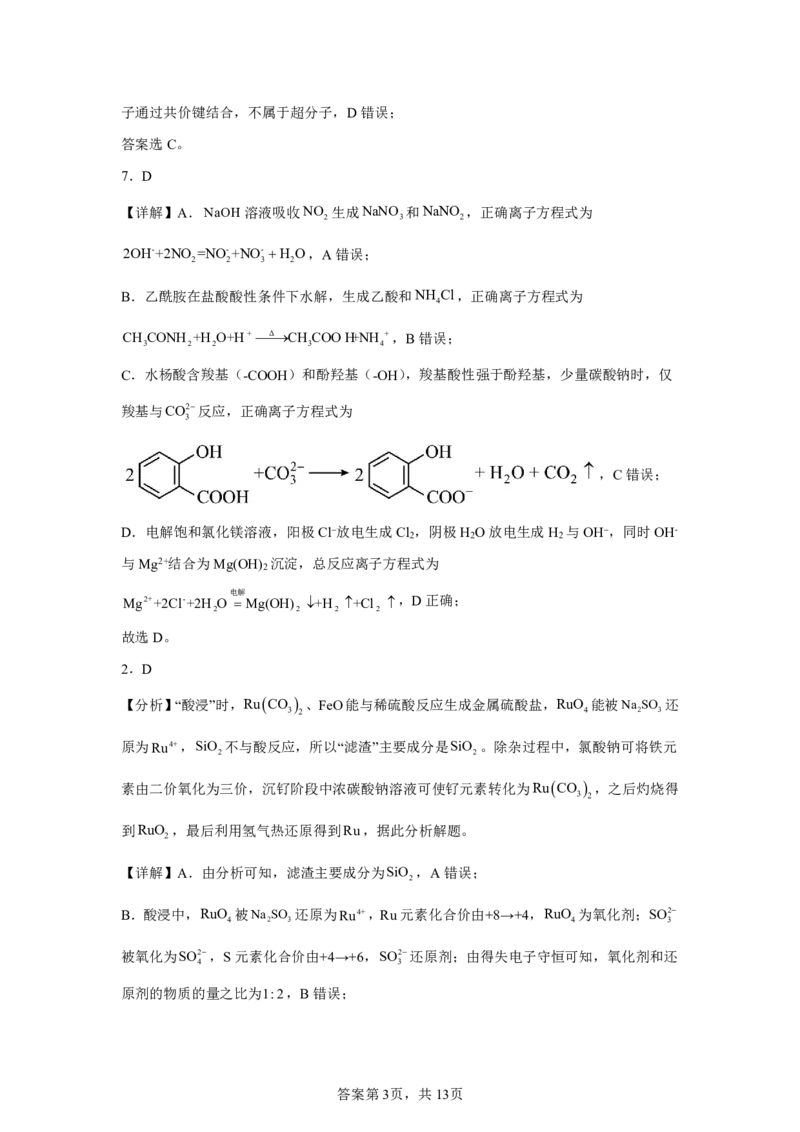
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}18、(15分)三氯苯达唑是目前世界卫生组织推荐的唯一片形吸虫病药物,其合成路线如下,
回答下列问题:
(1)A的系统命名为 。
(2)B中含氧官能团的名称为 。
(3)D的结构简式为 。
(4)B→C反应的化学方程式为 。
(5)F→G反应过程中,加入KOH的作用是 。
(6)下列说法正确的是 (填序号)。
A.三氯苯达唑中碳原子均为sp2杂化 B.E→F属于取代反应 C.C可以形成分子内氢键
(7)D的某同系物I,相对分子质量比D大28。满足下列条件的I的同分异构体有 种。
(不考虑立体异构)
①遇FeCl 溶液显色;
3
②两个氯原子不直接连在苯环上。
其中,核磁共振氢谱显示为4组峰,且峰面积比为1:2:2:3的物质的结构简式为 。
第10页,共10页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}《2025-2026学年度高中化学期中考试卷》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C A B A D C D D A D
题号 11 12 13 14
答案 A C A B
1.C
【详解】A.偏二甲肼在反应中被氧化,作为还原剂,A正确;
B.合金的熔点通常低于其成分金属,铝铜合金熔点比纯铝、铜低,B正确;
C.放射性元素的核反应涉及原子核变化,属于物理变化而非化学变化,C错误;
D.碳化硅陶瓷属于新型无机非金属材料,D正确;
故选C。
2.A
【详解】A.水壶中的水垢主要成分为CaCO 和MgOH ,同时醋酸的酸性大于碳酸的酸
3 2
性,醋酸和碳酸钙反应生成醋酸钙、二氧化碳、水,也能与MgOH 中和,所以食醋清除
2
水壶中的少量水垢,A正确;
B.石膏能改良盐碱土壤,是因为硫酸钙和碳酸钠反应生成碳酸钙沉淀和硫酸钠,而本身硫
酸钙显中性,不显酸性,B错误;
C.用NaS除去废水中Cu2和Hg2是因为发生反应Cu2 S2 CuS 和Hg2 S2 HgS ,
2
不是因为NaS的还原性,C错误;
2
D.轮船船体镶嵌镁合金是利用Mg比Fe活泼,发生腐蚀时先消耗Mg起到保护铁的作用,
属于电化学防金属腐蚀中的牺牲阳极法,不是镁有导电性,D错误;
故答案为:A。
3.B
【详解】A.硫酸是纯净物,不是混合物;冰醋酸是弱电解质,A错误;
B.橄榄油为混合物,CH COOH是化合物,C 是单质,Cu (OH) CO 是盐,BaSO 是强电
3 60 2 2 3 4
解质,B正确;
C.澄清石灰水是混合物,不是化合物,石灰石是混合物,C错误;
D.CaO是氧化物,不属于盐,D错误;
故选B。
答案第1页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}4.A
【详解】A.Ga为31号元素,基态电子排布式为[Ar]3d104s24p1,简化电子排布式需包含3d10,
A错误;
B.Mg N 为离子化合物,由Mg2+和N3-构成,N3-最外层8电子稳定结构,电子式为
3 2
,B正确;
C.F 分子中F原子通过p轨道“头碰头”重叠形成σ键,σ键电子云轮廓图呈轴对称,图示符
2
合σ键特征,C正确;
D.PCl 中P的价层电子对数为4(3个成键对+1个孤电子对),VSEPR模型为四面体,图
3
示为四面体结构,D正确;
故选A。
5.D
【详解】A.钠的摩尔质量为23g/mol,4.6gNa为0.2mol。无论生成Na O还是Na O ,
2 2 2
每个Na原子均失去1个电子,故转移电子数为0.2N ,A正确;
A
B.撞击时,NaN 分解生成N (氧化产物),2molNaN 可生成3molN ,B正确;
3 2 3 2
C.每个N 分子含1个σ键和2个π键,比例固定为1:2,与气体体积无关,C正确;
2
高温、高压
D.合成氨反应(3H +N 2NH )为可逆反应,无法完全转化,生成的NH 少于2mol,
2 2 3 3
催化剂
化合物中原子总数小于8N ,D错误;
A
故答案为:D。
6.C
【详解】A.叶绿素分子中存在多个sp3杂化的碳原子,sp3杂化碳为四面体结构,与其相连
的原子不可能共平面,因此所有碳原子不可能在同一平面,A错误;
B.叶绿素是配合物,中心离子为Mg2+,但Mg2+与卟啉环中的四个N原子形成稳定的配位
键,不易解离,与NaOH溶液混合时,Mg2+不会游离出来与OH⁻结合生成Mg(OH) 白色沉
2
淀,B错误;
C.叶绿素中中心离子Mg2+与4个N原子配位,配位数为4;分子中卟啉环为带两个负电荷
的配体,其他基团也呈电中性,整体为电中性配合物,C正确;
D.超分子是由多个分子通过分子间作用力形成的聚集体,而叶绿素是单一分子,其内部原
答案第2页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}子通过共价键结合,不属于超分子,D错误;
答案选C。
7.D
【详解】A.NaOH溶液吸收NO 生成NaNO 和NaNO ,正确离子方程式为
2 3 2
2OH-+2NO =NO-+NO- H O,A错误;
2 2 3 2
B.乙酰胺在盐酸酸性条件下水解,生成乙酸和NH Cl,正确离子方程式为
4
CH CONH +H O+H ΔCH COOH+NH ,B错误;
3 2 2 3 4
C.水杨酸含羧基(-COOH)和酚羟基(-OH),羧基酸性强于酚羟基,少量碳酸钠时,仅
羧基与CO2反应,正确离子方程式为
3
,C错误;
D.电解饱和氯化镁溶液,阳极Cl⁻放电生成Cl ,阴极H O放电生成H 与OH⁻,同时OH-
2 2 2
与Mg2+结合为Mg(OH) 沉淀,总反应离子方程式为
2
电解
Mg2++2Cl-+2H O Mg(OH) +H +Cl ,D正确;
2 2 2 2
故选D。
2.D
【分析】“酸浸”时,RuCO 、FeO能与稀硫酸反应生成金属硫酸盐,RuO 能被Na SO 还
3 2 4 2 3
原为Ru4+,SiO 不与酸反应,所以“滤渣”主要成分是SiO 。除杂过程中,氯酸钠可将铁元
2 2
素由二价氧化为三价,沉钌阶段中浓碳酸钠溶液可使钌元素转化为RuCO ,之后灼烧得
3 2
到RuO ,最后利用氢气热还原得到Ru,据此分析解题。
2
【详解】A.由分析可知,滤渣主要成分为SiO ,A错误;
2
B.酸浸中,RuO 被Na SO 还原为Ru4+,Ru元素化合价由+8→+4,RuO 为氧化剂;SO2
4 2 3 4 3
被氧化为SO2,S元素化合价由+4→+6,SO2还原剂;由得失电子守恒可知,氧化剂和还
4 3
原剂的物质的量之比为1:2,B错误;
答案第3页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}6232
C.SO2的中心原子S的价层电子对数为3 314,孤电子对数1,空间结构
3 2
7132
为三角锥形;ClO-的中心原子Cl的价层电子对数为3 314,孤电子对数1,
3 2
6242
空间结构为三角锥形;SO2的中心原子S的价层电子对数为4 404,孤电
4 2
子对数0,空间结构为正四面体,C错误;
D.除杂中Fe2+被氧化为Na Fe SO OH ,其中铁元素为+3价,生成3mol 该物质,
2 4 4 6 2
表明有12molFe2被氧化,共失去12mole⁻;ClO-(Cl为+5价)被还原为Cl-(Cl为-1价),
3
故需NaClO :12mol÷6=2mol,D正确;
3
故答案选D。
9.A
【分析】W、X、Y、Z是原子序数依次增大的短周期主族元素,其中基态Z原子s轨道电
子数与p轨道电子数之比为3∶4,结合化合物M的结构图中Z的成键特点,Z的核外电子
排布为1s22s22p63s23p2,Z为Si元素;W形成两条共价键,W为O元素;X为Na;Y为
Al。
【详解】A.W、X、Y的简单离子的电子层数相同,核电荷数越大离子半径越小,故简单
离子半径YZ,D错误;
故选A。
10.D
【详解】A.该中间体含苯环(可加成、取代)、氨基(可氧化、取代)、羰基(可还原)、
肽键(可取代)等,能发生加成、取代、氧化、还原反应,A正确;
B.与足量H 加成后,苯环变为环己烷环(含4个手性碳),五元环中与N相连的碳(若连
2
乙基等不同基团)也为手性碳,共5个手性碳,B正确;
C.苯环需3mol H 加成,酰胺羰基难加成,故1mol中间体最多与3mol H 加成,C正
2 2
答案第4页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}确;
D.含氨基和脂肪胺N(显碱性),但①(苯环C-N单键)、②(环C-N单键)为普通单键,
③(酰胺C-N键,因共轭具部分双键性)键长更短,三者键长不相等,D错误;
故答案选D。
11.A
【详解】A.二茂铁易升华,升华提纯需固体加热升华后气体凝华。图甲中蒸发皿加热,带
孔滤纸可作为凝华载体,棉花球防止杂质进入,简易装置可实现升华提纯,A正确;
B.制银氨溶液应在AgNO 溶液中逐滴加氨水至沉淀恰好溶解,图乙为氨水中滴加AgNO ,
3 3
试剂添加顺序错误,B错误;
C.验证可逆反应需证明反应物和生成物同时存在。图丙中FeCl 溶液滴加少量KI,Fe3过
3
量,加KSCN变红可能是过量Fe3导致,无法证明反应可逆,C错误;
D.醋酸滴定NaOH终点产物为CH COONa,水解显碱性,应选酚酞作指示剂,甲基橙在
3
酸性范围变色会导致误差,D错误;
故答案为:A。
12.C
【分析】
阴极 CO 变为 HCOOH,电极反应式为 CO +2e-+2H+=HCOOH,阳极的反应式为
2 2
,双极膜中的H+向阴
极移动,OH-向阳极移动;
【详解】A.双极膜解离出H⁺和OH⁻,H⁺向阴极移动,a膜允许H⁺(阳离子)通过,故a
膜为阳离子交换膜,A正确;
B.右侧电极为阳极,发生氧化反应,反应物为含羟基的呋喃衍生物,失电子后生成二羧酸
盐,电极反应式中电子、电荷及原子守恒,B正确;
C.阴极反应为CO +2e-+2H+=HCOOH,C元素由+4价降为+2价,每消耗1molCO 转移2mol
2 2
e⁻,则转移2mole⁻时消耗1molCO ,标准状况下体积为22.4L,并非44.8L,C错误;
2
D.催化剂纳米片可降低反应活化能,加快反应速率,D正确;
答案选C。
13.A
答案第5页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}【详解】A.由晶胞结构可知六方氮化镓中Ga在N围成的四面体空隙处,N在Ga围成的
四面体空隙处,故Ga和N的配位数均为4,A正确;
3 1 1
B.立方氮化镓中,若B原子坐标为( , , )(四面体空隙位置),A原子若为面心立方格
4 4 4
1 1
子中的Ga原子,其坐标应为( ,,0),B错误;
2 2
1 3
C.立方氮化镓中Ga和N的最小核间距为体对角线的 ,即 apm,C错误;
4 4
D.六方和立方氮化镓的晶胞中Ga与N原子数比均为1:1,化学式均为GaN,D错误;
故答案选A。
14.B
【分析】已知联氨(又称肼,N H 是无色液体)为二元弱碱,向联氨溶液中加入硫酸时,溶液
2 4
的碱性减弱,c(OH-)减小,则pOH增大,随着pOH增大,减小的为N H ,增大再减小的为
2 4
N H+,pOH大于12增大的为N H2+,据此分析;
2 5 2 6
【详解】A.N H中N-N为非极性键,N-H为极性键,N原子提供孤对电子与H+形成配位
2 5
键,含有三种键,A正确;
B.(N H ) SO 电离生成N H和SO2,N H水解:N H++H ON H +H+,溶液显酸性。水
2 5 2 4 2 5 4 2 5 2 5 2 2 4
解生成的N H 与H+物质的量相等,且H+还来自水电离,故c(H+)>c(N H ),正确顺序应为
2 4 2 4
c N H+ >c SO2- >c H+ >cN H >c OH- ,B错误;
2 5 4 2 4
c2
N
H+
C.反应平衡常数K= 2 5 ,由(N H)与 N H 的曲线交点在pOH6.02处,
cN H c N H2+ 2 5 2 4
2 4 2 6
c
N
H+
c
OH-
可知K = 2 5 =10-6.02,由(N H)与(N H2)的曲线交点在pOH14.9处,可
b1 cN H 2 5 2 6
2 4
c
N
H2+
c
OH-
K 10-6.02
知K = 2 6 =10-14.9,可得K= b1= =108.88,C正确;
b2 c N H+ K 10-14.9
2 5 b2
D.加入10mL硫酸时,n(N H )=0.0001mol(含氮微粒总量),n(SO2)=0.00005mol,溶液体
2 4 4
0.0001mol 0.00005mol
积20mL,含氮微粒总浓度= =0.005mol/L,2c(SO2)=2×( )=0.005mol/L,
0.02L 4 0.02L
故2c SO2- =c N H+ +cN H +c N H2+ ,D正确;
4 2 5 2 4 2 6
故选B。
答案第6页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}15.(1) 丁达尔效应 Fe2被氧化,使四氧化三铁的产率降低 2
(2) ①③ 6.72
(3) 4Fe+NO-+10H+=NH++4Fe2++3H O HClO氧化性比ClO-强,随着pH降低,溶
3 4 2
液中HClO浓度增大,氧化能力增强,导致氨氮去除率升高
(4)B
(5)B
【分析】由流程可知,合成氨厂提供氨气,与二氧化碳、饱和食盐水反应生成NH Cl、NaHCO ,
4 3
在沉淀池中过滤分离出碳酸氢钠,碳酸氢钠加热分解生成碳酸钠、水、二氧化碳,二氧化碳
可循环使用。母液中含溶质氯化铵,通入氨气,加入食盐可分离得到氯化铵,据此分析;
【详解】(1)①磁流体分散系的分散质粒子大小在36−55nm之间,属于胶体,胶体可以利
用丁达尔效应来鉴别;
②将n(Fe3+):n(Fe2+)=2:1混合时,理论上制得的纳米Fe O 产率应该最高,但是事实上,亚铁
3 4
离子会被空气中氧气等被氧化为三价铁离子,导致纳米Fe O 产率降低;
3 4
③根据离子方程式3Fe2++2S O2-+O +xOH-=Fe O +S O2-+2H O,利用电荷守恒可以得到
2 3 2 3 4 4 6 2
x4;硫元素、铁元素化合价升高被氧化,氧气中氧元素化合价降低被还原,当消耗1mol
氧气时,氧化2molFe2+,当4molFe2+被氧化时,消耗的氧气为2mol;
(2)转化过程反应①:N +6Li=2Li N,为氧化还原反应;反应②Li N+3H O=NH ↑+3LiOH
2 3 3 2 3
电解
为非氧化还原反应反应;③反应4LiOH 4Li+O ↑+2H O为氧化还原反应,所以转化过程
2 2
反应中为氧化还原反应的是①③;生成1molNH 转移3mol电子,生成1molO ,转移4mol
3 2
电子,所以4NH ~3O ,假设每一步均完全转化,每生成0.4molNH ,同时生成0.3molO ,
3 2 3 2
标准状况下体积为6.72L;
(3)
①图2中硝酸根离子浓度下降,铵根离子浓度上升,20 60min内发生主要反应的离子方程
式为:4Fe+NO-+10H+=NH++4Fe2++3H O;
3 4 2
②控制其他条件相同,当废水pH为1.252.75范围内,氨氮去除率随pH降低而升高,原
因是HClO氧化性比ClO-强,随着pH降低,溶液中HClO浓度增大,氧化能力增强,导致
氨氮去除率升高。
答案第7页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}(4)A.由联碱法生产流程示意图可以看出从母液中经过循环Ⅰ进入沉淀池的主要是Na CO 、
2 3
NH Cl和氨水,A正确;
4
B.沉淀池中反应的化学方程式:NH +CO +NaCl+H O=NH Cl+NaHCO ↓,B错误;
3 2 2 4 3
C.由溶解度曲线可以看出,NH Cl的溶解度随温度升高而增大,因此如果NH Cl固体从母
4 4
液中析出时需控制温度在0~10℃以下,C正确;
D.由流程可知,循环Ⅰ、Ⅱ的目的是提高原料的利用率、减少对环境的污染,D正确;
故选B。
(7)由图2可知,晶胞中,Zn位于顶点和面心,该晶胞若沿体对角线投影,则Zn2+投影图
为B。
16.(1) (球形)干燥管 防暴沸
(2)12Na WO +Na SiO +26HCl H [SiW O ]+26NaCl+11H O
2 4 2 3 4 12 40 2
(3) 乙醇与水互溶,不能用作该体系的萃取剂 C
(4) 防倒吸 取适量最后一次洗涤液于试管中,滴加硝酸酸化的AgNO 溶液,若溶
3
液出现白色沉淀,则未洗净,若没有出现白色沉淀,则洗净
(5)偏大
【分析】制取十二钨硅酸晶体(H SiW O ·nH O)时,先将适量Na WO 2H O、
4 12 40 2 2 4 2
Na SiO 9H O加入三颈烧瓶中,加适量水,加热,溶解;然后在持续搅拌下加热混合物至
2 3 2
近沸,缓慢滴加浓盐酸至pH为2,反应30分钟,冷却;将反应液转至萃取仪器中,加入乙
醚,再分批次加入浓盐酸,萃取;静置后液体分上、中、下三层,下层是油状钨硅酸醚合物;
将下层油状物转至蒸发皿中,加少量水,加热至混合液表面有晶膜形成,冷却结晶,抽滤,
干燥,得到十二钨硅酸晶体(H SiW O ·nH O)。
4 12 40 2
【详解】(1)由图可知,仪器a为(球形)干燥管,其作用应是防止外界水蒸气进入或吸收挥
发的杂质气体。在液体加热反应中,若局部温度过高,液体容易因过热而突然沸腾,发生暴
沸现象。搅拌子在搅拌使反应更充分的同时,能不断打破液体表面的过热区域,使液体温度
均匀分布,从而起到防止暴沸的作用;
(2)在第一步中,晶体均加热溶解,故反应物为Na WO 、Na SiO 和HCl,生成物为
2 4 2 3
H [SiW O ]和NaCl,则步骤Ⅱ中生成H [SiW O ]的化学方程式为:
4 12 40 4 12 40
答案第8页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}
12Na WO +Na SiO +26HCl H [SiW O ]+26NaCl+11H O;
2 4 2 3 4 12 40 2
(3)乙醚难溶于水,能与钨硅酸缔合成油状醚合物从而实现萃取;而乙醇与水可以任意比
例互溶,无法与水形成分层体系,不能将钨硅酸从水溶液中分离出来,故不能用乙醇替代乙
醚作萃取剂。已知乙醚易燃、有毒,操作时需满足两个关键条件;防明火、通风,故答案为:
乙醇与水互溶,不能用作该体系的萃取剂;C;
(4)抽滤(减压过滤)时,装置内压强会显著减小。安全瓶能有效阻断倒吸路径,起到防止
倒吸的作用。制备过程中使用了浓盐酸,产物表面可能残留Cl-(来自过量的HCl或生成的
NaCl),故可通过检验最后一次洗涤液中是否含Cl-来判断沉淀是否洗净,则答案为:防倒吸;
取适量最后一次洗涤液于试管中,滴加硝酸酸化的AgNO 溶液,若溶液出现白色沉淀,则
3
未洗净,若没有出现白色沉淀,则洗净;
(5)若样品潮湿,说明样品中除了结晶水外,还含有额外的游离水。加热时,游离水会与
结晶水一同挥发,导致测得的“质量减少量”偏大(包含了游离水的质量)。偏大会使计算出的
n值偏大。
2.(1) -443.6 <
(2)减小
(3)M
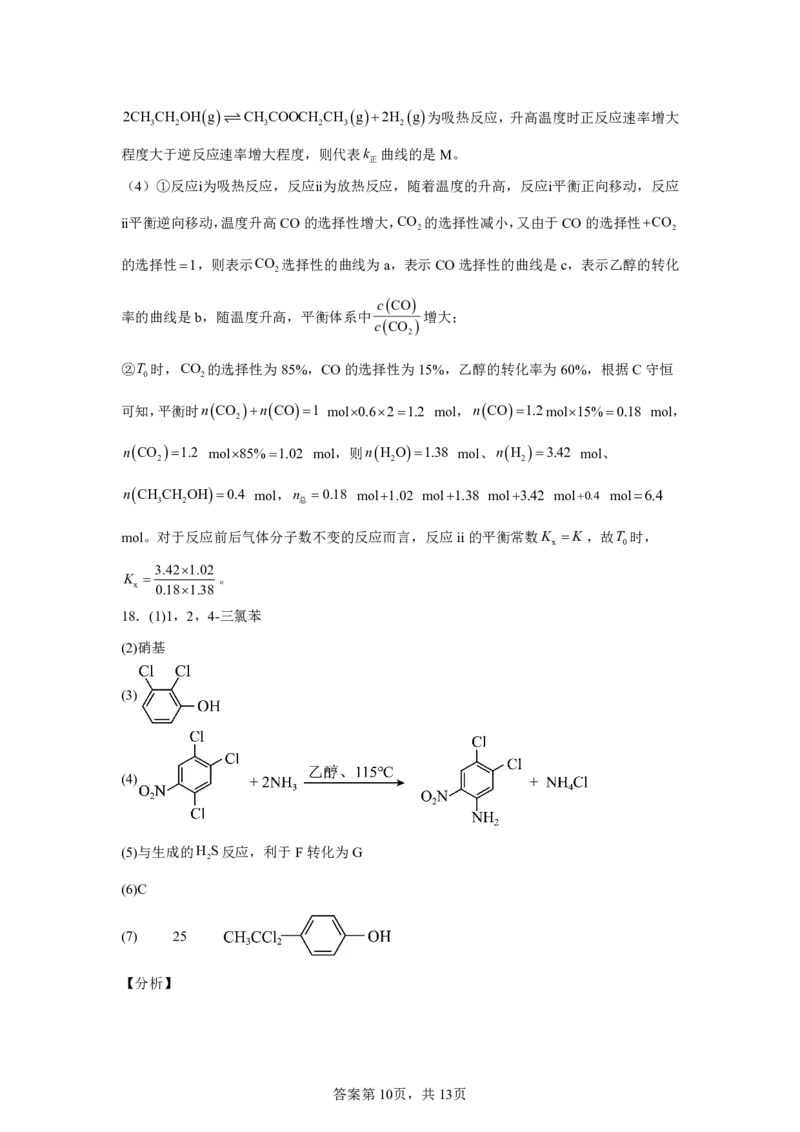
3.421.02
(4) 增大
0.181.38
【详解】(1)
①Ni是28号元素,基态Ni原子的价层电子排布式为3d84s2,故其价层电子轨道表示式为
;
②根据盖斯定律可得:ΔH 2Δ H (乙醇)Δ H (乙酸乙酯)26 kJ·mol-1,Δ H (乙
f m f m f m
酸乙酯)443.6 kJ·mol-1;
③CH 3 CH 2 OHg转化为CH 3 CH 2 OHl放出热量,故Δ f H m CH 3 CH 2 OH1 234.8
kJ·mol-1。
(2)对反应后气体分子数增大的反应而言,增大反应物的起始浓度,可视为增大压强,平
衡正向移动,反应物的平衡转化率减小。
1
(3)由图中信息可知,温度越高,则 越小,
T
答案第9页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}2CH CH OHg CH COOCH CH g2H g为吸热反应,升高温度时正反应速率增大
3 2 3 2 3 2
程度大于逆反应速率增大程度,则代表k 曲线的是M。
正
(4)①反应ⅰ为吸热反应,反应ⅱ为放热反应,随着温度的升高,反应ⅰ平衡正向移动,反应
ⅱ平衡逆向移动,温度升高CO的选择性增大,CO 的选择性减小,又由于CO的选择性CO
2 2
的选择性1,则表示CO 选择性的曲线为a,表示CO选择性的曲线是c,表示乙醇的转化
2
cCO
率的曲线是b,随温度升高,平衡体系中 增大;
cCO
2
②T 时,CO 的选择性为85%,CO的选择性为15%,乙醇的转化率为60%,根据C守恒
0 2
可知,平衡时nCO nCO1 mol0.621.2 mol,nCO1.2mol15%0.18 mol,
2
nCO 1.2 mol85%1.02 mol,则nH O1.38 mol、nH 3.42 mol、
2 2 2
nCH CH OH0.4 mol,n 0.18 mol1.02 mol1.38 mol3.42 mol0.4 mol6.4
3 2 总
mol。对于反应前后气体分子数不变的反应而言,反应ii的平衡常数K K,故T 时,
x 0
3.421.02
K 。
x 0.181.38
18.(1)1,2,4-三氯苯
(2)硝基
(3)
(4)
(5)与生成的H S反应,利于F转化为G
2
(6)C
(7) 25
【分析】
答案第10页,共13页
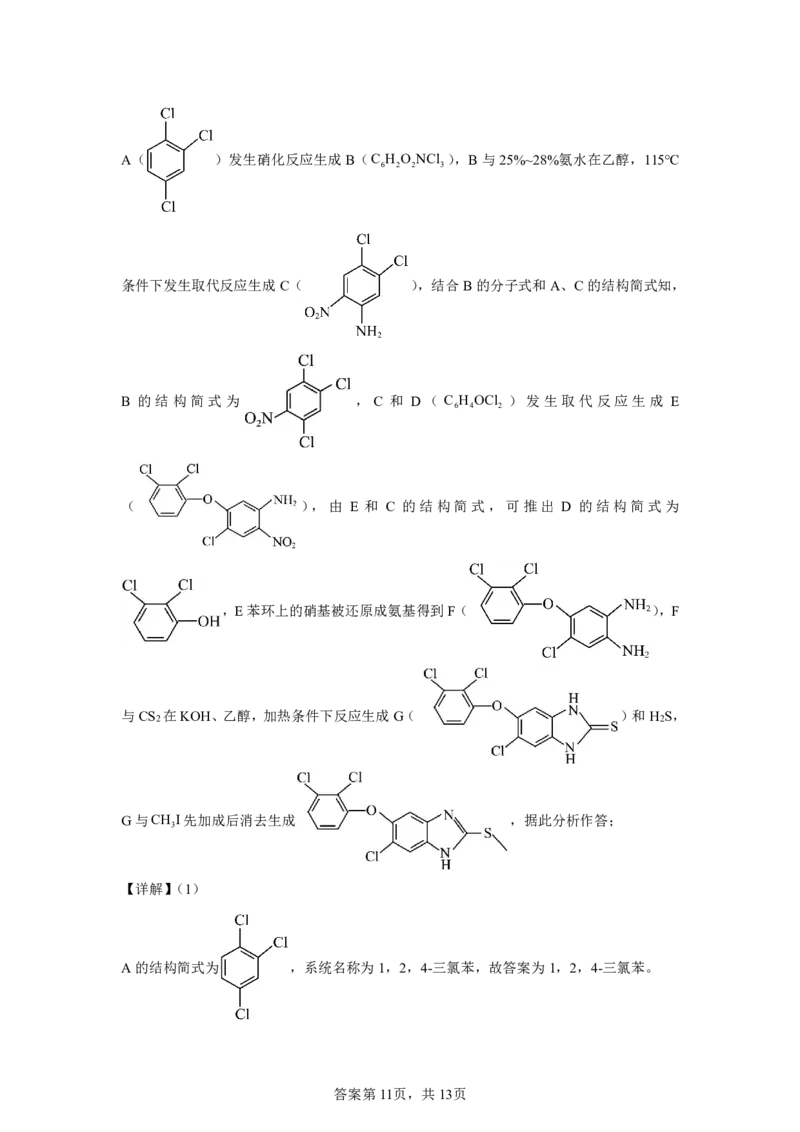
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}A( )发生硝化反应生成B(C H O NCl ),B与25%~28%氨水在乙醇,115℃
6 2 2 3
条件下发生取代反应生成C( ),结合B的分子式和A、C的结构简式知,
B 的结构简式为 ,C 和 D( C H OCl )发生取代反应生成 E
6 4 2
( ),由 E 和 C 的结构简式,可推出 D 的结构简式为
,E苯环上的硝基被还原成氨基得到F( ),F
与CS 在KOH、乙醇,加热条件下反应生成G( )和H S,
2 2
G与CH I先加成后消去生成 ,据此分析作答;
3
【详解】(1)
A的结构简式为 ,系统名称为1,2,4-三氯苯,故答案为1,2,4-三氯苯。
答案第11页,共13页
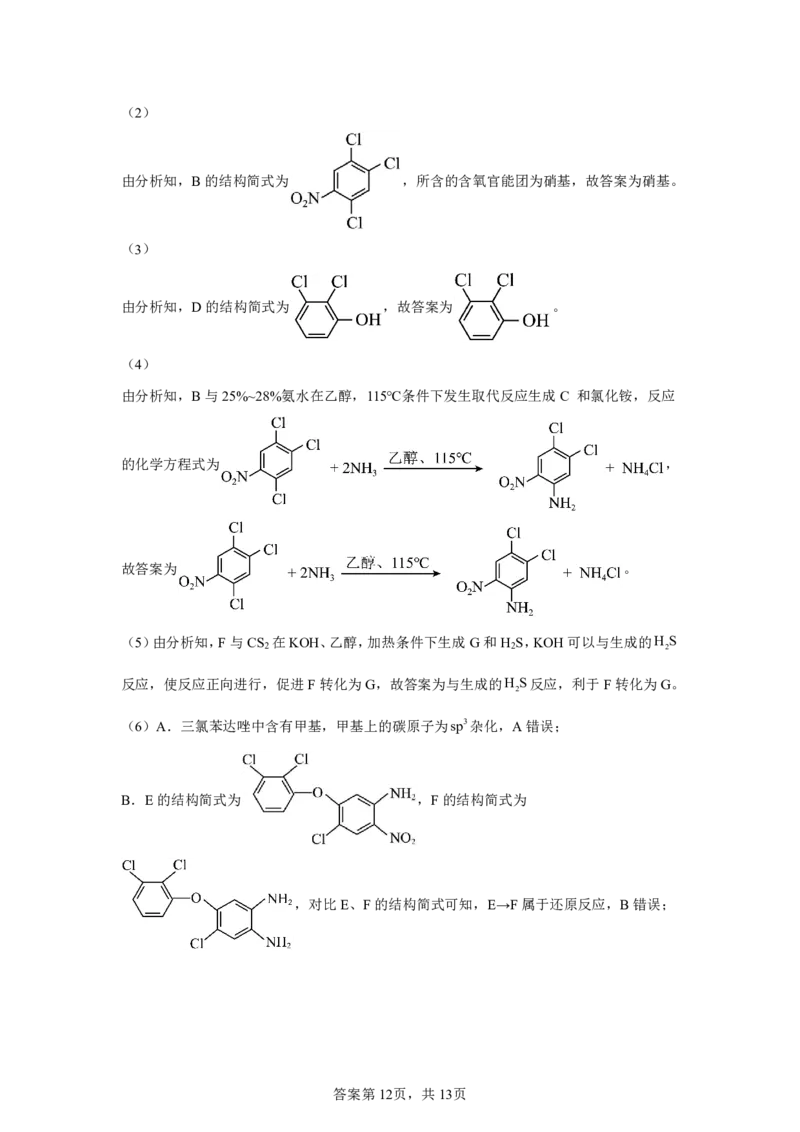
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}(2)
由分析知,B的结构简式为 ,所含的含氧官能团为硝基,故答案为硝基。
(3)
由分析知,D的结构简式为 ,故答案为 。
(4)
由分析知,B与25%~28%氨水在乙醇,115℃条件下发生取代反应生成C 和氯化铵,反应
的化学方程式为 ,
故答案为 。
(5)由分析知,F与CS 在KOH、乙醇,加热条件下生成G和H S,KOH可以与生成的H S
2 2 2
反应,使反应正向进行,促进F转化为G,故答案为与生成的H S反应,利于F转化为G。
2
(6)A.三氯苯达唑中含有甲基,甲基上的碳原子为sp3杂化,A错误;
B.E的结构简式为 ,F的结构简式为
,对比E、F的结构简式可知,E→F属于还原反应,B错误;
答案第12页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}C.C的结构简式为 ,含有硝基和氨基且处于邻位,可以形成分子内氢键,
故C正确;
故答案为C。
(7)
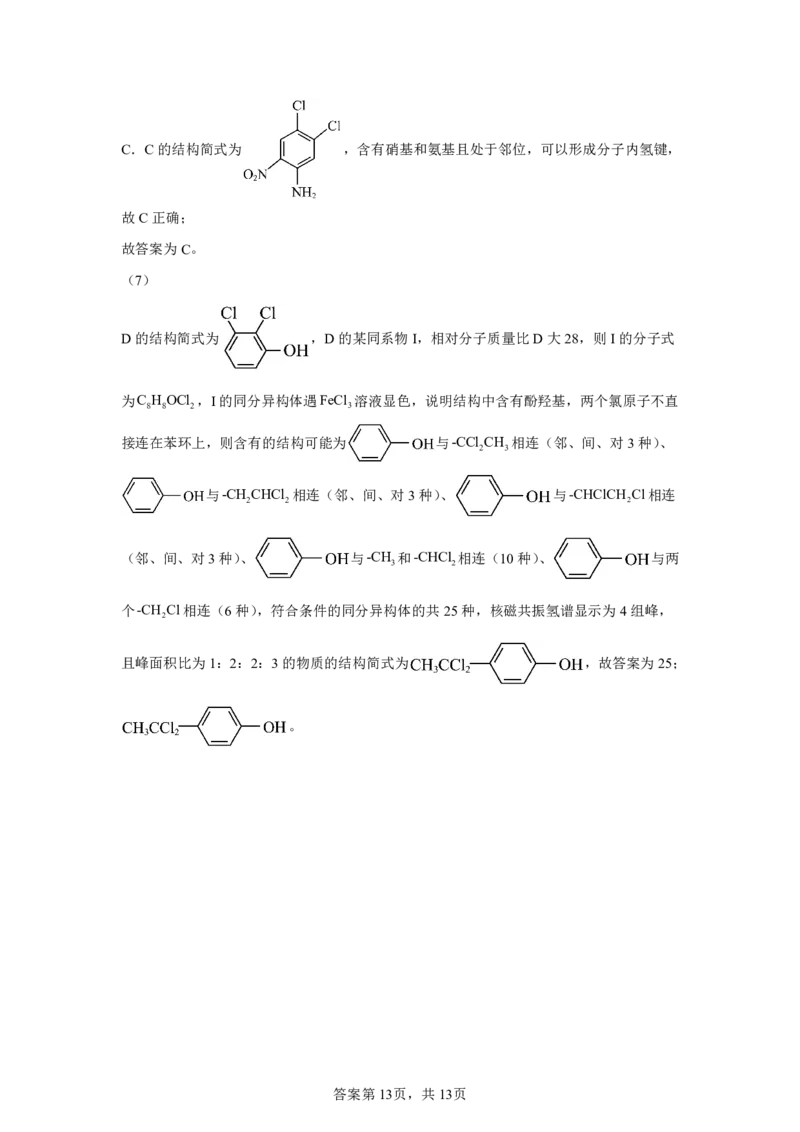
D的结构简式为 ,D的某同系物I,相对分子质量比D大28,则I的分子式
为C H OCl ,I的同分异构体遇FeCl 溶液显色,说明结构中含有酚羟基,两个氯原子不直
8 8 2 3
接连在苯环上,则含有的结构可能为 与-CCl CH 相连(邻、间、对3种)、
2 3
与-CH CHCl 相连(邻、间、对3种)、 与-CHClCH Cl相连
2 2 2
(邻、间、对3种)、 与-CH 和-CHCl 相连(10种)、 与两
3 2
个-CH Cl相连(6种),符合条件的同分异构体的共25种,核磁共振氢谱显示为4组峰,
2
且峰面积比为1:2:2:3的物质的结构简式为 ,故答案为25;
。
答案第13页,共13页
{#{QQABTQAUogiAQIJAAQgCQQkiCAMYkBCCCIgGABAQoAABgAFABAA=}#}