文档内容
高三化学期中考试
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 K 39 Fe 56
一、单选题(共14题,每题3分,共42分)
1. 2025年《政府工作报告》提出:“协同推进降碳减污扩绿增长,加快经济社会发展绿色转型。”下列有关说法正
确的是
A. 利用太阳能分解水制氢,实现“氢能源”循环
B. 为了粮食增产应大量使用化肥农药
C. 生活垃圾集中露天焚烧
D. 将废旧电池深埋处理,以减少重金属的污染
2. 下列化学用语或图示表达错误的是
A. 1-丁烯的实验式:
B. 的电子式:
C. 用电子式表示KCl形成过程:
D. 中子数为46的溴原子:
3. 河南美食天下闻名,每一道经典菜肴都承载着中原文明的烟火气。下列说法错误的是
美
食
洛阳牛肉汤 胡辣汤 黄河大鲤鱼 羊肉烩面
A. 洛阳牛肉汤——制作牛肉汤的调料简单,仅用食盐,NaCl属于离子化合物
B. 胡辣汤——制作胡辣汤要用到黄花菜,黄花菜富含纤维素,纤维素属于高分子
C. 黄河大鲤鱼——做大鲤鱼的佐料之一为料酒,料酒含有乙醇,乙醇属于饱和一元醇
D. 羊肉烩面——制作烩面片要用到食用碱,食用碱的主要成分为NaOH
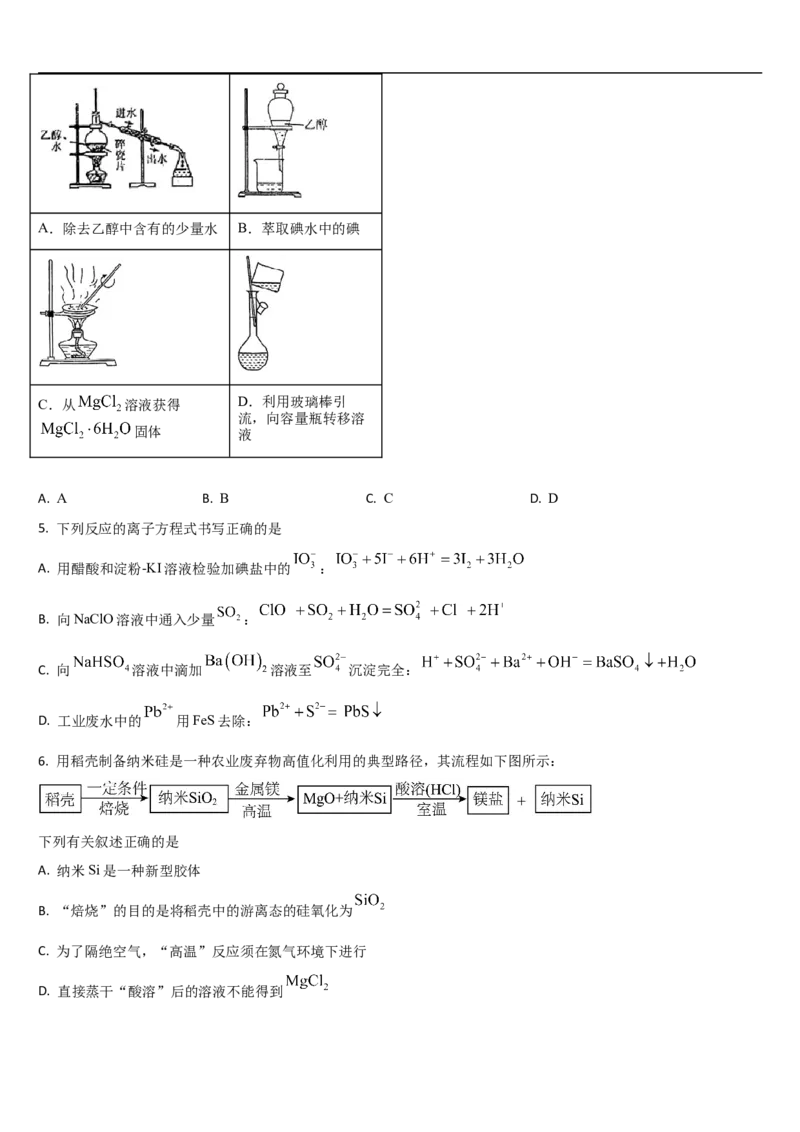
4. 下列实验的对应操作中,合理的是A.除去乙醇中含有的少量水 B.萃取碘水中的碘
C.从 溶液获得 D.利用玻璃棒引
流,向容量瓶转移溶
固体 液
A. A B. B C. C D. D
5. 下列反应的离子方程式书写正确的是
A. 用醋酸和淀粉-KI溶液检验加碘盐中的 :
B. 向NaClO溶液中通入少量 :
C. 向 溶液中滴加 溶液至 沉淀完全:
D. 工业废水中的 用FeS去除:
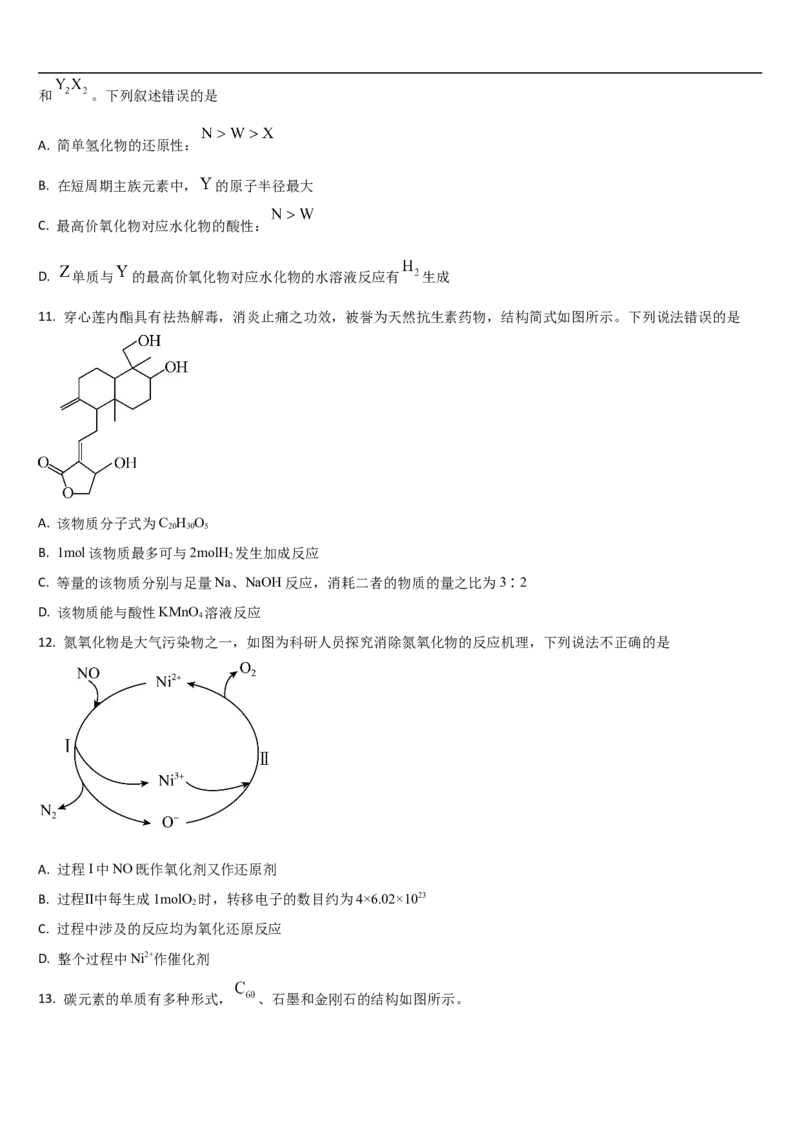
6. 用稻壳制备纳米硅是一种农业废弃物高值化利用的典型路径,其流程如下图所示:
下列有关叙述正确的是
A. 纳米Si是一种新型胶体
B. “焙烧”的目的是将稻壳中的游离态的硅氧化为
C. 为了隔绝空气,“高温”反应须在氮气环境下进行
D. 直接蒸干“酸溶”后的溶液不能得到7. 设 表示阿伏加德罗常数的值。下列叙述正确的是
A. 溶液中 的数目大于
B. 常温下, 分子中极性键的数目为
的
C. 标准状况下, 溶于水,转移电子 数目为
D. 与 蒸气置于密闭容器中,充分反应后生成 分子的数目为
8. 下列说法错误的是
A. 应远离热源、可燃物,并与还原性物质分开存放
B. 向饱和碳酸钠溶液中缓慢滴加稀盐酸,一开始未观察到有气泡产生
C. 将 和 按体积比 通入品红溶液,能观察到品红溶液快速褪色
D. 实验安全图标 提醒实验者实验中会用到明火,要正确使用火源
9. 下列根据实验操作和现象能得到相应结论的是
选
实验操作和现象 结论
项
NaHS 固体中含有
A 将NaHS固体溶于水,进行导电性实验,电流计指针偏转
B 向饱和 溶液中加入足量氯水,有无色气体产生 氯水中有HClO
常温下,将两块相同的未经打磨的铝片分别投入等体积等
作用下,铝片表
C 物质的量浓度的 溶液和 溶液中,前者无明显 面的氧化膜易被破
现象,后者迅速反应, 析出现象明显 坏
D 向某黄色溶液中加入淀粉-KI溶液,溶液呈蓝色 溶液中一定含
A. A B. B C. C D. D
10. 已知X、Y、Z、W、N为原子序数依次增大的五种短周期主族元素,X、W的原子序数之和等于 与 的原子序
数之和, 与 同主族, 是 的相邻元素,元素 与 能组成两种阴、阳离子个数比相同的常见化合物和 。下列叙述错误的是
A. 简单氢化物的还原性:
B. 在短周期主族元素中, 的原子半径最大
C. 最高价氧化物对应水化物的酸性:
D. 单质与 的最高价氧化物对应水化物的水溶液反应有 生成
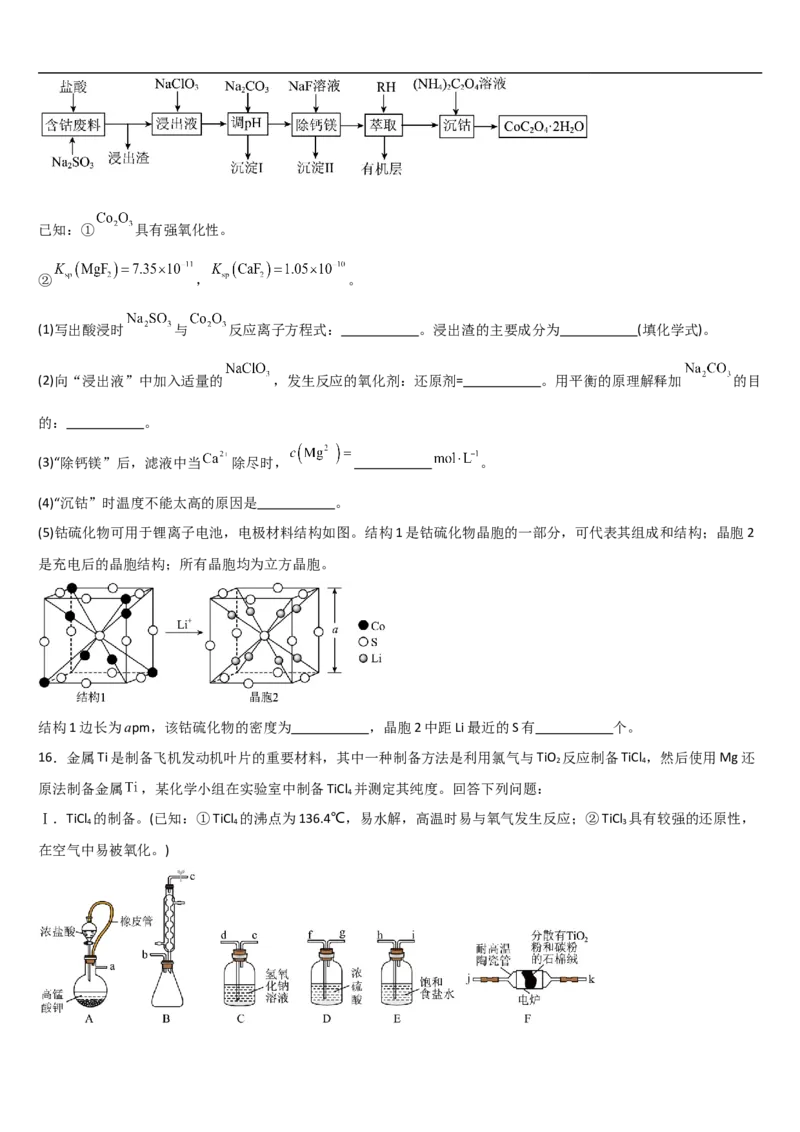
11. 穿心莲内酯具有祛热解毒,消炎止痛之功效,被誉为天然抗生素药物,结构简式如图所示。下列说法错误的是
A. 该物质分子式为C H O
20 30 5
B. 1mol该物质最多可与2molH 发生加成反应
2
C. 等量的该物质分别与足量Na、NaOH反应,消耗二者的物质的量之比为3∶2
D. 该物质能与酸性KMnO 溶液反应
4
12. 氮氧化物是大气污染物之一,如图为科研人员探究消除氮氧化物的反应机理,下列说法不正确的是
A. 过程I中NO既作氧化剂又作还原剂
B. 过程Ⅱ中每生成1molO 时,转移电子的数目约为4×6.02×1023
2
C. 过程中涉及的反应均为氧化还原反应
D. 整个过程中Ni2+作催化剂
13. 碳元素的单质有多种形式, 、石墨和金刚石的结构如图所示。下列说法错误的是
A. 、石墨互为同素异形体
B. 1个金刚石晶胞中含有8个C原子
C. 石墨晶体中含有 键的物质的量为
D. 加热熔融石墨晶体既破坏共价键,又要破坏分子间作用力
14. 三氯乙烯(C HCl )是某市地下水中有机污染物的主要成分,研究显示,在该地下水中加入HO 可将其中的三氯乙
2 3 2 2
烯除去,发生的反应如下: 。常温下,在某密闭容器中进行上述反应,
测得 随时间的变化如表所示:
时间/min 0 2 4 6 8 …
/(mol·L-1) 1.20 0.90 0.70 0.60 0.55 …
已知:在反应体系中加入Fe2+,可提高反应速率。下列说法错误的是
A. 为该反应的催化剂 B. 反应过程中可能产生
C. 与 的空间结构相同 D. 0~4 min内,
二、非选择题(共58分)
15.钴广泛应用于机械制造、电子电器、航空航天、电池制造等行业,是国家重要的战略资源。用含钴废料(主要成
分为 ,含少量 、 、 、 、 等)制备草酸钴晶体( )的工艺流程如图所示,试
回答下列问题:已知:① 具有强氧化性。
② , 。
(1)写出酸浸时 与 反应离子方程式: 。浸出渣的主要成分为 (填化学式)。
(2)向“浸出液”中加入适量的 ,发生反应的氧化剂:还原剂= 。用平衡的原理解释加 的目
的: 。
(3)“除钙镁”后,滤液中当 除尽时, 。
(4)“沉钴”时温度不能太高的原因是 。
(5)钴硫化物可用于锂离子电池,电极材料结构如图。结构1是钴硫化物晶胞的一部分,可代表其组成和结构;晶胞2
是充电后的晶胞结构;所有晶胞均为立方晶胞。
结构1边长为apm,该钴硫化物的密度为 ,晶胞2中距Li最近的S有 个。
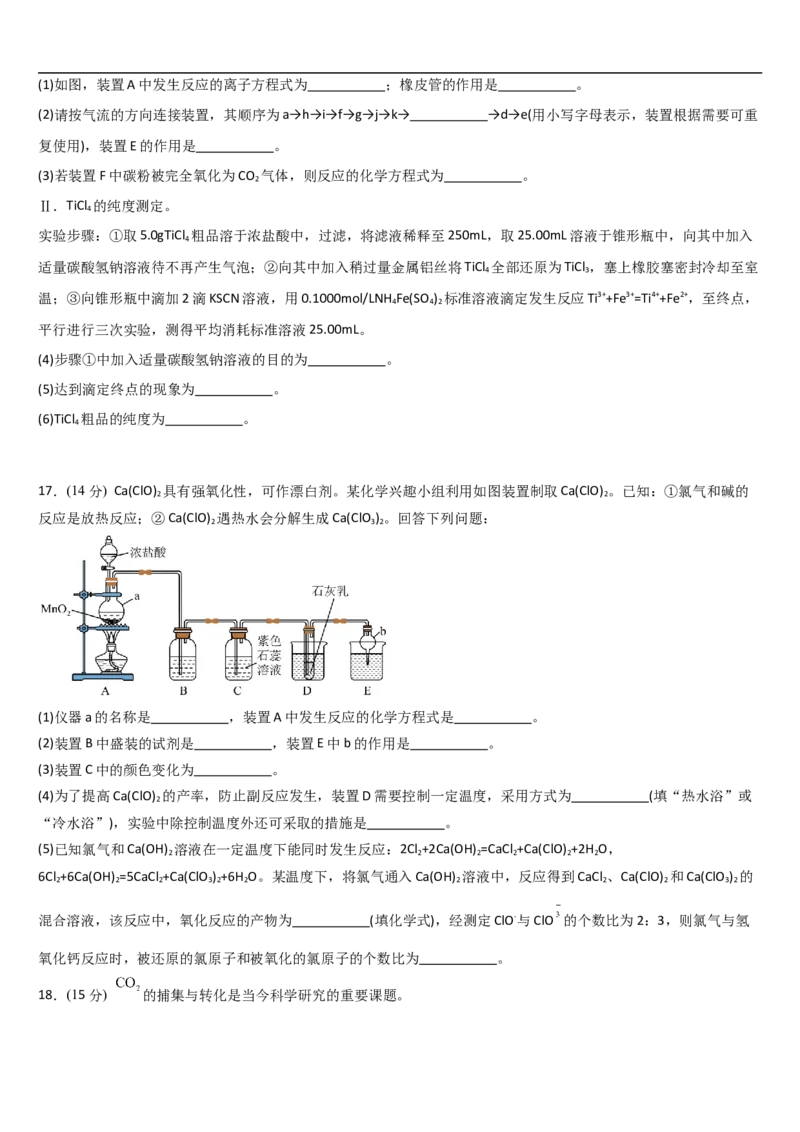
16.金属Ti是制备飞机发动机叶片的重要材料,其中一种制备方法是利用氯气与TiO 反应制备TiCl ,然后使用Mg还
2 4
原法制备金属 ,某化学小组在实验室中制备TiCl 并测定其纯度。回答下列问题:
4
Ⅰ.TiCl 的制备。(已知:①TiCl 的沸点为136.4℃,易水解,高温时易与氧气发生反应;②TiCl 具有较强的还原性,
4 4 3
在空气中易被氧化。)(1)如图,装置A中发生反应的离子方程式为 ;橡皮管的作用是 。
(2)请按气流的方向连接装置,其顺序为a→h→i→f→g→j→k→ →d→e(用小写字母表示,装置根据需要可重
复使用),装置E的作用是 。
(3)若装置F中碳粉被完全氧化为CO 气体,则反应的化学方程式为 。
2
Ⅱ.TiCl 的纯度测定。
4
实验步骤:①取5.0gTiCl 粗品溶于浓盐酸中,过滤,将滤液稀释至250mL,取25.00mL溶液于锥形瓶中,向其中加入
4
适量碳酸氢钠溶液待不再产生气泡;②向其中加入稍过量金属铝丝将TiCl 全部还原为TiCl ,塞上橡胶塞密封冷却至室
4 3
温;③向锥形瓶中滴加2滴KSCN溶液,用0.1000mol/LNH Fe(SO ) 标准溶液滴定发生反应Ti3++Fe3+=Ti4++Fe2+,至终点,
4 4 2
平行进行三次实验,测得平均消耗标准溶液25.00mL。
(4)步骤①中加入适量碳酸氢钠溶液的目的为 。
(5)达到滴定终点的现象为 。
(6)TiCl 粗品的纯度为 。
4
17.(14分) Ca(ClO) 具有强氧化性,可作漂白剂。某化学兴趣小组利用如图装置制取Ca(ClO) 。已知:①氯气和碱的
2 2
反应是放热反应;②Ca(ClO) 遇热水会分解生成Ca(ClO ) 。回答下列问题:
2 3 2
(1)仪器a的名称是 ,装置A中发生反应的化学方程式是 。
(2)装置B中盛装的试剂是 ,装置E中b的作用是 。
(3)装置C中的颜色变化为 。
(4)为了提高Ca(ClO) 的产率,防止副反应发生,装置D需要控制一定温度,采用方式为 (填“热水浴”或
2
“冷水浴”),实验中除控制温度外还可采取的措施是 。
(5)已知氯气和Ca(OH) 溶液在一定温度下能同时发生反应:2Cl +2Ca(OH) =CaCl +Ca(ClO) +2H O,
2 2 2 2 2 2
6Cl +6Ca(OH) =5CaCl +Ca(ClO ) +6H O。某温度下,将氯气通入Ca(OH) 溶液中,反应得到CaCl 、Ca(ClO) 和Ca(ClO ) 的
2 2 2 3 2 2 2 2 2 3 2
混合溶液,该反应中,氧化反应的产物为 (填化学式),经测定ClO-与ClO 的个数比为2:3,则氯气与氢
氧化钙反应时,被还原的氯原子和被氧化的氯原子的个数比为 。
18.(15分) 的捕集与转化是当今科学研究的重要课题。(1) 催化加氢合成二甲醚是一种 的转化方法,其过程中发生的反应如下:
反应①:
反应②:
催化加氢合成二甲醚的热化学方程式为 。
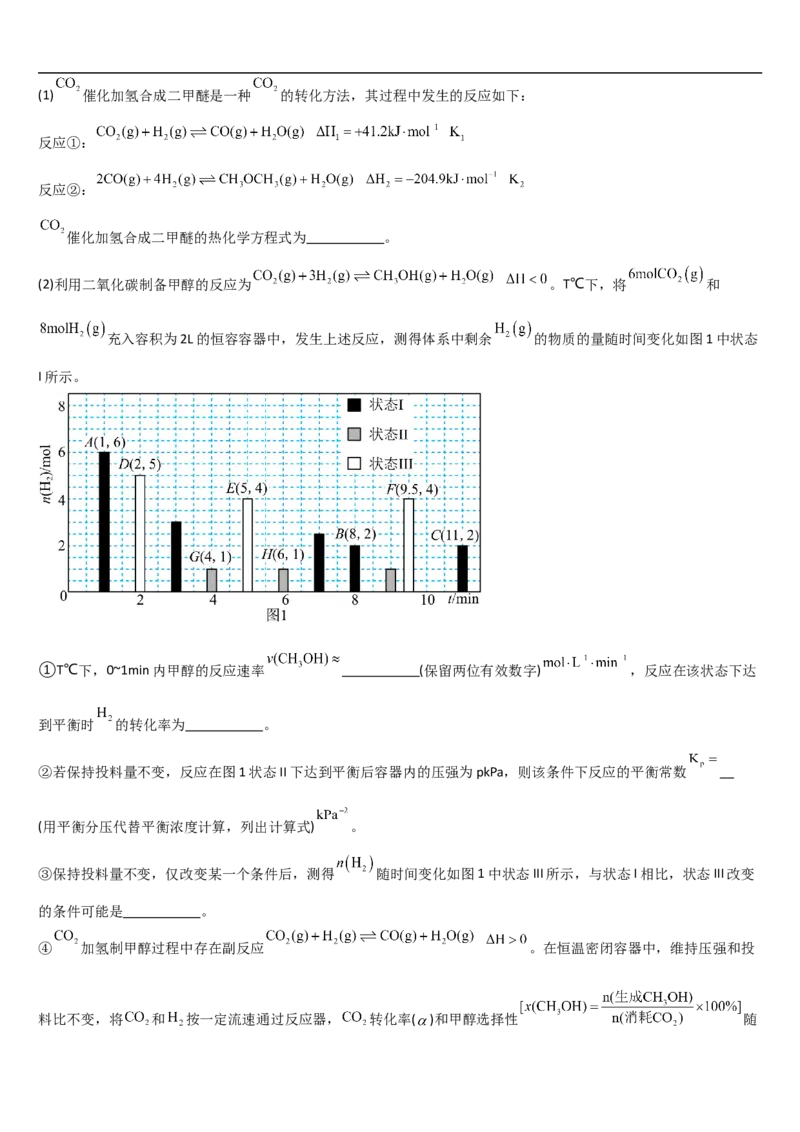
(2)利用二氧化碳制备甲醇的反应为 。T℃下,将 和
充入容积为2L的恒容容器中,发生上述反应,测得体系中剩余 的物质的量随时间变化如图1中状态
I所示。
①T℃下,0~1min内甲醇的反应速率 (保留两位有效数字) ,反应在该状态下达
到平衡时 的转化率为 。
②若保持投料量不变,反应在图1状态II下达到平衡后容器内的压强为pkPa,则该条件下反应的平衡常数
(用平衡分压代替平衡浓度计算,列出计算式) 。
③保持投料量不变,仅改变某一个条件后,测得 随时间变化如图1中状态III所示,与状态I相比,状态III改变
的条件可能是 。
④ 加氢制甲醇过程中存在副反应 。在恒温密闭容器中,维持压强和投
料比不变,将 和 按一定流速通过反应器, 转化率( )和甲醇选择性 随温度变化关系如图2所示:
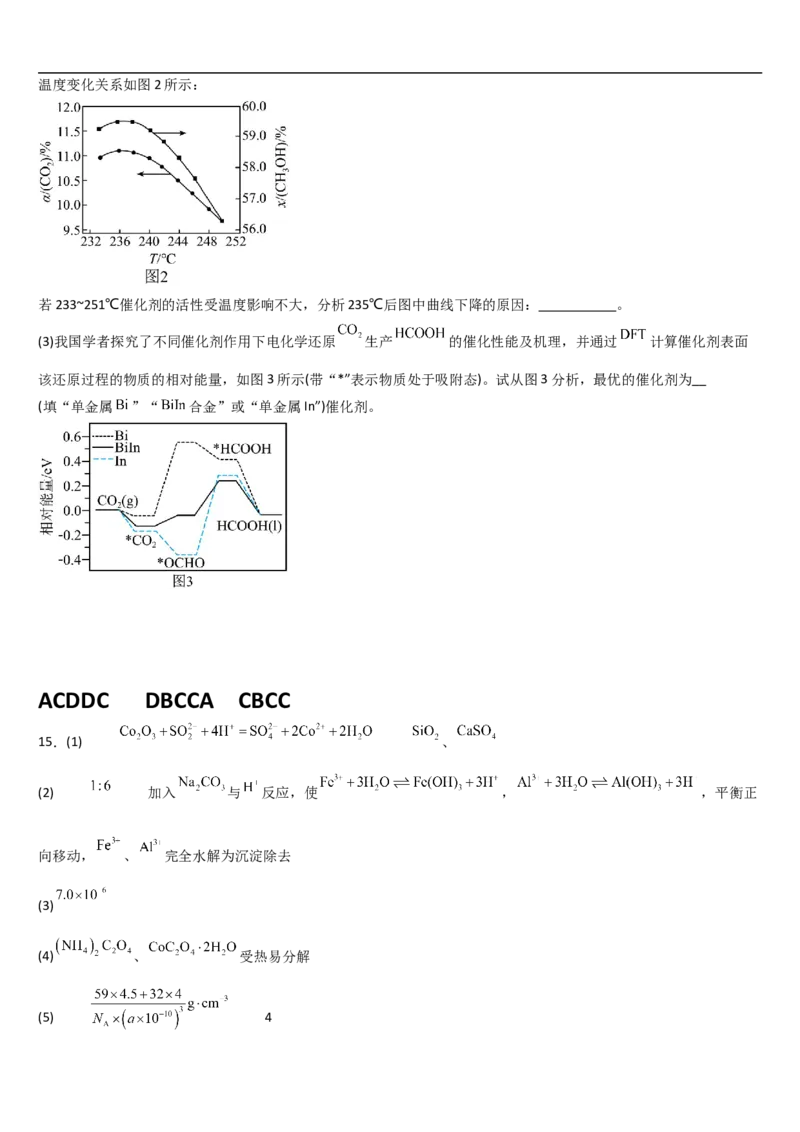
若233~251℃催化剂的活性受温度影响不大,分析235℃后图中曲线下降的原因: 。
(3)我国学者探究了不同催化剂作用下电化学还原 生产 的催化性能及机理,并通过 计算催化剂表面
该还原过程的物质的相对能量,如图3所示(带“*”表示物质处于吸附态)。试从图3分析,最优的催化剂为
(填“单金属 ”“ 合金”或“单金属In”)催化剂。
ACDDC DBCCA CBCC
15.(1) 、
(2) 加入 与 反应,使 , ,平衡正
向移动, 、 完全水解为沉淀除去
(3)
(4) 、 受热易分解
(5) 416.(1) 2 +10Cl-+16H+=2Mn2++5Cl ↑+8H O 平衡内外压强,使浓盐酸顺利流下
2 2
(2) b→c→f→g 除去Cl 中的HCl
2
(3)TiO +C+2Cl TiCl +CO
2 2 4 2
(4)利用反应生成的CO 排除装置内的空气,防止Ti3+被氧化
2
(5)当滴入最后半滴NH Fe(SO ) 标准溶液时,溶液恰好变成浅红色,且半分钟之内不褪色
4 4 2
(6)95.0%
17.(1) 圆底烧瓶(或烧瓶) (1分) MnO +4HCl MnCl +Cl ↑+2H O (2分)
2 2 2 2
(2) 饱和NaCl溶液 (1分) 防倒吸 (1分)
(3)紫色石蕊溶液先变红后褪色 (2分)
(4) 冷水浴 (1分) 控制浓盐酸的滴加速度 (2分)
(5) Ca(ClO) 、Ca(ClO ) (2分) 17:5 (2分)
2 3 2
18.(1) (2分)
(2) 0.33 (2分) 75% (2分) (2分) 升高温度 (2分) 主反应
放热,副反应吸热,升高温度使主反应平衡逆向移动程度大于副反应平衡正向移动程度,因而使 转化率和甲醇选
择性下降 (2分)
(3) 合金 (2分)