文档内容
2025—2026学年度上期高三年级半期考试
化学试卷
考试时间:75分钟 总分:100分
可能用到相对原子质量:H 1 B 11 C 12 O 16 Cl 35.5 Fe 56 Co 59 Cu 64
一、选择题:本题共15小题,每题3分,共45分。每小题只有一个选项符合题目要求。
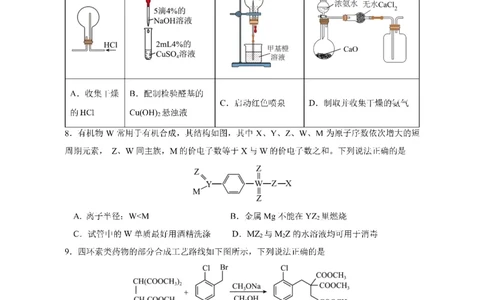
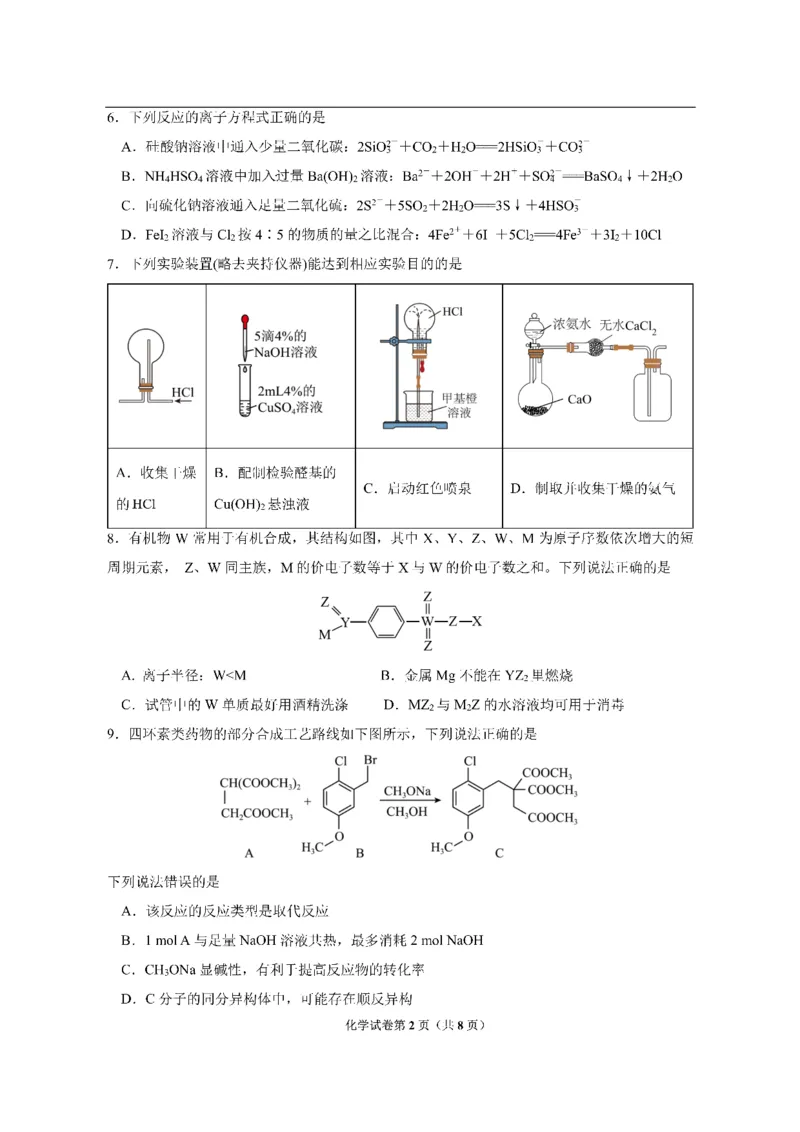
1.近年来我国科技在各个领域都有重大进展。下列说法错误的是
A.石墨烯固态电池具有超高的能量密度和高安全性,为新能源汽车带来新的动力电源,石墨
烯属于新型无机非金属材料
B.碳化硼可用作核反应堆的控制棒,碳化硼含极性共价键
C.量子通信材料螺旋碳纳米管与石墨烯互为同素异形体
D.制造阻燃或防火线缆的橡胶不能由加聚反应合成
2.下列有关叙述正确的是
A.葡萄糖和蔗糖互为同系物,淀粉和纤维素互为同分异构体
B.可以用热的浓NaOH溶液来区分植物油和矿物油
C.向溶液中滴加酸化的Ba(NO ) 溶液出现白色沉淀,证明该溶液中一定有SO2-
3 2 4
D.Cl 、SO 均能使品红溶液褪色,说明二者均有氧化性
2 2
3.下列化学用语或图示表达正确的是
A.1 mol CH CH Cl含极性键数目约为7×6.02×1023
3 2
B.SiO 的电子式:
2
C.HClO的结构式:H—Cl—O
D.顺-2-丁烯的球棍模型:
4.麻醉药布比卡因结构简式如右。下列关于布比卡因的说法错误的是
A. 布比卡因分子中存在手性碳原子
B. 一定条件下,布比卡因既能与盐酸反应,又能与NaOH溶液反应
C. 布比卡因分子中所有C原子可能共平面
D. 布比卡因分子中含有2种官能团
5.N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.0.1 L 1.0 mol·L-1的NH NO 溶液中含有氧原子的数目等于0.3N
4 3 A
B.标准状况下,4.48 L HF分子中含有电子的数目为0.2N
A
C.1 L 1 mol·L-1 CuCl 溶液中[Cu(H O) ] 2+离子数为N
2 2 4 A
D.56 g Fe和64 g Cu分别与1 mol Cl 充分反应,转移的电子数均为2N
2 A
化学试卷第1页(共8页)10.室温下,下列实验方案能得到相应的实验结论的是
实验方案设计 实验结论
将KMnO 加入到酸性FeCl 溶液中,溶液变成棕黄色,有黄
4 2
A 氧化性:MnO->Cl >Fe3+
4 2
绿色气体产生
分别向等体积AgCl和AgBr饱和溶液中加入足量同浓度的
B K :K (AgCl)> K (AgBr)
sp sp sp
AgNO 溶液,生成沉淀的物质的量前者更多
3
证明炭可与浓HNO 反应生
3
C 向浓HNO 中插入红热的炭,观察到有红棕色气体生成
3
成NO
2
将25°C 0.1 mol/LNa SO 溶液加热到40℃,用传感器监测溶液
2 3
D 说明水解过程放热
pH,溶液的pH逐渐减小
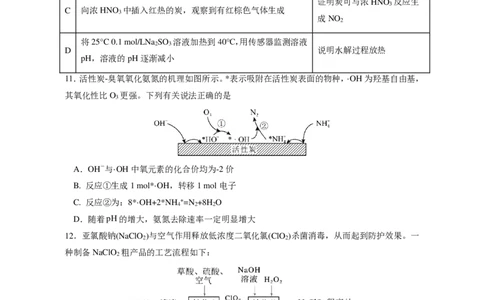
11.活性炭-臭氧氧化氨氮的机理如图所示。*表示吸附在活性炭表面的物种,·OH为羟基自由基,
其氧化性比O 更强。下列有关说法正确的是
3
A.OH-与·OH中氧元素的化合价均为-2价
B. 反应①生成1 mol*·OH,转移1 mol电子
C. 反应②为:8*·OH+2*NH +=N +8H O
4 2 2
D.随着pH的增大,氨氮去除速率一定明显增大
12.亚氯酸钠(NaClO )与空气作用释放低浓度二氧化氯(ClO )杀菌消毒,从而起到防护效果。一
2 2
种制备NaClO 粗产品的工艺流程如下:
2
注:纯ClO 易分解爆炸,一般用空气稀释到10%以下。下列说法错误的是
2
A.“转化Ⅰ”中氧化产物与还原产物物质的量之比为1:1
B.“转化Ⅰ”不能用稀盐酸代替稀硫酸
C.“转化Ⅱ”为加快反应速率,宜控制较高的反应温度
D.“转化Ⅱ”得到的NaClO 粗产品,可用重结晶的方法进一步提纯
2
化学试卷第3页(共8页)13.25°C时,H S的电离常数K (H S)=1.1×10-7,K (H S)=1.3×10-13,K (FeS)=6.3×10-18,
2 a1 2 a2 2 sp
K (CuS)=6.3×10-36。下列描述正确的是
sp
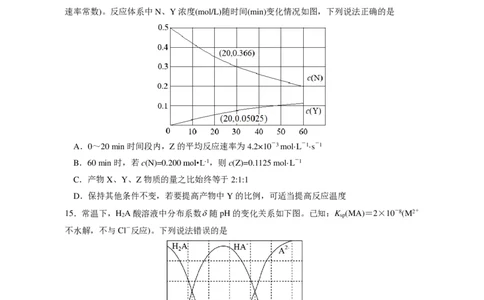
A.0.01 mol·L-1的Na S溶液中:c(H S) ”、“<”或“=”),反应在_______(填“高温”或“低温”)自发进行。
(2)图中X表示_____________,为提高该物质的产率,需要研发在___________(填“高温”或
“低温”)区的高效催化剂。
(3)随温度升高,CO 平衡转化率先减小后增大的原因是______________________________
2
_______________________________________________。
(4)一定条件下,向体积为V L的恒容密闭容器中通入充入1 mol CO (g)和3 mol(g)H ,经2 h
2 2
反应达平衡,CO(g)、CH OH(g)、CH OCH (g)的物质的量分别为a、b、c mol。
3 3 3
①则H 的平均消耗速率v=__________________________mol·L-1·h-1(用含a、b、c、V的代
2
数式表示,下同);
②反应Ⅱ的平衡常数K=__________________________ (mol·L-1)-2。
化学试卷第7页(共8页)19.(14分)富马酸依美斯汀(F)用于暂时缓解过敏性结膜炎的体征和症状,日本的科学家Ryuichi
Lemura合成富马酸依美斯汀路线如下(略去部分试剂和条件)。
回答下列问题:
(1)A的化学名称是________________。
(2)B中含氧官能团的名称是________________________。
(3)C的结构简式为___________________。
(4)E→F的反应类型为__________。
(5)D的同分异构体中,同时满足下列条件的共有_______种。
a.含有苯环结构,且苯环上连有3个取代基;
b.分子中含有2个酰胺基;
c.核磁共振氢谱为5组峰。
(6)中国科学家李艳芹设计的富马酸依美斯汀部分合成路线如下:
J含两个氨基,按照C→D的方法反应,生成物发生互变异构,生成含—OH的K。
K的结构简式为____________,第⑧步的化学反应方程式为_________________________。
化学试卷第8页(共8页)