文档内容
绝密★启用前 4.下列离子方程式书写正确的是
A.向酸性高锰酸钾溶液中滴加 HO 溶液:2MnO-+HO+6H+2Mn2++3O↑+4HO
2 2 4 2 2 2 2
江西省 2026届高三 11月一轮复习阶段检测
B.NaSO 溶液与稀硫酸反应:SO2-+2H+4S↓+2SO2-+HO
2 2 3 2 3 4 2
C.用稀硝酸清洗试管内壁上的银镜:3Ag+4H++NO-3Ag++NO↑+2HO
3 2
化 学 试 卷 D.NHAl(SO) 溶液与 Ba(OH) 溶液按物质的量之比为 12反应:Al3++2SO2-+2Ba2++4OH-
4 4 2 2 4
2BaSO↓+[Al(OH)]-
4 4
△
试卷共8页,18小题,满分100分。考试用时75分钟。 5.加热条件下可用液态肼与新制 Cu(OH) 制备纳米 CuO:4Cu(OH)+NH 2CuO+N↑+
2 2 2 2 4 2 2
注意事项: 6HO。设 N 为阿伏加德罗常数的值,下列说法错误的是
2 A
1.考查范围:化学物质及变化、化学计量在实验中的应用、元素及其化合物、物质结构与性质、 A.1molOH-中所含中子数为8N
A
化学反应与能量、化学反应速率与化学平衡。 B.22.4LNH 中所含原子数为6N
2 4 A
2.答卷前,考生务必将自己的姓名、准考证号等填写在答题卡指定位置上。 C.生成1molCuO,反应中转移的电子数为2N
2 A
3.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改 D.1molHO中最外层满足8电子稳定结构的原子数为 N
2 A
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷 6.下列装置或操作合理的是
上无效。
4.考生必须保持答题卡的整洁。考试结束后,请将答题卡交回。
!"
#
温度计
硬纸板 !"溶液
可能用到的相对原子质量:H—1 C—12 O—16 #$ 的&&’
稀硫酸 溶 % 液 ( 振荡
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目 碎纸屑
要求。
1.非物质文化遗产是人类文明的结晶,是文化多样性的体现。下列与江西非物质文化遗产有关的 A.吸收NH B.分离Fe(OH)胶体和FeCl溶液 C.测定中和反应反应热 D.比较Br和I氧化性强弱
3 3 3 2 2
物品中,其主要成分是金属的是
7.某有机化合物的化学式为 X Y ZW M,主要应用于涂料领域。Y、Z、X、W、M是原子序数依次增
12 28 4
大的短周期主族元素,其中 M的价层 p轨道中所含电子数与其电子层数相等,Z、X、W位于同一
周期,W是元素周期表中电负性最大的元素,ZW 分子呈平面正三角形。下列说法错误的是
3
A.原子半径:M>X>W B.氢化物沸点:M>W>X
C.NaZW 中含有配位键 D.XY 为非极性分子
4 4
8.由下列实验事实得出的结论正确的是
A.婺源歙砚 B.安福火腿 C.萍乡春锣 D.景德镇瓷器 选项 实验事实 结论
2.二氧化碳(CO)在电催化领域应用的最新趋势是与其他结构单元(如:N、HO、NH、NO-、SO2-) 将铜丝与浓硫酸反应产生的气体通入紫色石蕊溶液中,
2 2 2 3 3 3 A SO 没有漂白性
2
反应生成丰富的产物。下列说法错误的是 紫色石蕊溶液变红
A.NO-中的 N的价层电子对数为3 B.键的极性:H—O>H—N
3 将Ba(OH) 2 ·8H 2 O晶体与 NH 4 Cl晶体置于研钵中研 Ba(OH) 2 ·8H 2 O(s)与 NH 4 Cl(s)的反应是
B
C.键角:HO>NH D.键能:N帒帒N>NN
2 3 磨,研钵温度降低 吸热反应
3.下列符合实验安全要求的是
密闭容器中发生反应:H(g)+I(g)幑幐2HI(g),压缩容
2 2
A.未用完的钾可以放回原试剂瓶 C 压强增大,平衡逆向移动
器体积,气体颜色变深
B.被玻璃轻微划伤后立即用创可贴外敷
C.衣物大面积着火立即用湿抹布灭火
D 向FeCl溶液中加入适量铜粉,铜粉溶解,溶液变蓝 Fe比Cu活泼
3
D.浓盐酸沾到皮肤后先用大量水冲洗再涂上1%硼酸
高三化学 第1页(共8页) 高三化学 第2页(共8页)
书书书单质 氧化物 盐 碱
高三化学 第3页(共8页) 高三化学 第4页(共8页)
价合化
9.部分含铁物质的类别与相应化合价关系如图所示。下列说法错误的是 !" ’ ( )
A.b、e与硝酸反应只生成盐和水 !* $ % &
B.可存在 b→c→d→g→f的一步转化
C.e常用作油漆、涂料、油墨和橡胶的红色颜料 + #
D.常温下,可以用 a制作的容器来盛装浓硫酸
物质类别
HO
10.利用 CuSO、酒石酸钾钠(
4
HO
O
O
O- K+
)、甲醛(HCHO)和 NaOH进行化学镀铜的一种
O- Na+
工艺流程如图所示。已知:“还原”时发生反应:HCHO+[Cu(CHO)]2-+OH-→Cu+HCOO-+
4 4 6 2
H↑+HO+CHO2-(未配平)。下列说法错误的是
2 2 4 4 6
$
酒石酸钾钠 *$ &’$( )!*$
$
!"#$ +"
% 络合 $ 还原 !"
溶液 *$
$
$
$
$
$
$
$
*
*
,-
含 的溶液
$
#$
$
A. !"
$
#$
$
$
$
$
$
$
$
#
#
%&
中 Cu2+的配位数为4
B.“络合”可以增强 Cu2+的稳定性,防止其生成 Cu(OH)沉淀 2
C.常温下,酒石酸钾钠溶液 pH>7
D.“还原”时理论上消耗 HCHO和生成 Cu的物质的量之比为11
Cl Cl
師師 師師
11.一种以 帨帨 Cl为底物经电化学反应高效制备酰氯化合物 帨帨
師師 師師
N N Cl Cl
O
Cl,并在甲醇溶液
師師
中生成化合物 帨帨
師師
N
Cl
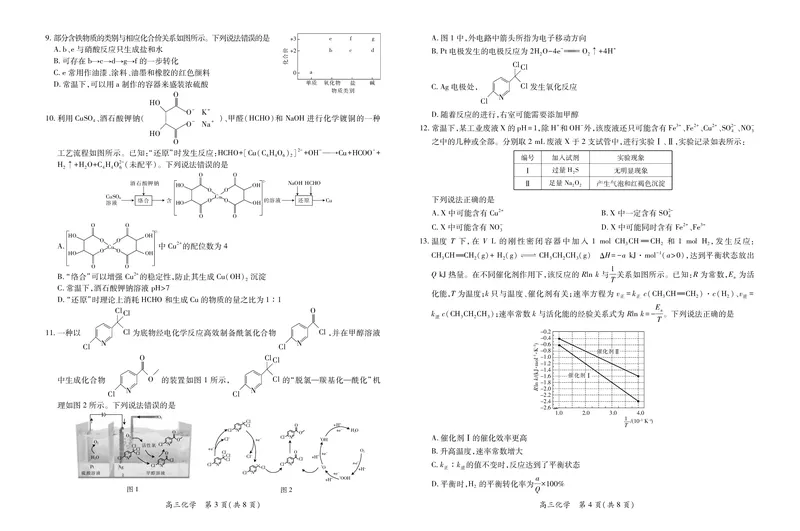
A.图1中,外电路中箭头所指为电子移动方向
B.Pt电极发生的电极反应为2HO-4e- O↑+4H+
2 2
Cl
Cl
師師
C.Ag电极处, 帨帨 Cl发生氧化反应
師師
N
Cl
D.随着反应的进行,右室可能需要添加甲醇
12.常温下,某工业废液X的pH=1,除H+和OH-外,该废液还只可能含有Fe3+、Fe2+、Cu2+、SO2-、NO-
4 3
之中的几种或全部。分别取2mL废液 X于2支试管中,进行实验Ⅰ、Ⅱ,实验记录如表所示:
编号 加入试剂 实验现象
Ⅰ 过量HS 无明显现象
2
Ⅱ 足量NaO 产生气泡和红褐色沉淀 2 2
下列说法正确的是
A.X中可能含有 Cu2+ B.X中一定含有 SO2-
4
C.X中可能含有 NO- D.X中可能同时含有 Fe2+、Fe3+
3
13.温度 T下,在 VL的刚性密闭容器中加入 1molCHCHCH 和 1molH,发生反应:
3 2 2
CHCHCH(g)+H(g)幑幐 CHCHCH(g) ΔH=-akJ·mol-1(a>0),达到平衡状态放出
3 2 2 3 2 3
1
QkJ热量。在不同催化剂作用下,该反应的 Rlnk与 关系如图所示。已知:R为常数,E 为活 T a
化能,T为温度;k只与温度、催化剂有关;速率方程为 v =k c(CHCHCH)·c(H)、v =
正 正 3 2 2 逆
E
a k c(CHCHCH);速率常数 k与活化能的经验关系式为 Rlnk=- 。下列说法正确的是
逆 3 2 3 T
!"#$
%"&’
%"&(
%"#)
O Cl %*&"
Cl
!*&$
師師 !*&’
!*&(
O 的装置如图 1所示, 帨帨 Cl的“脱氯—羰基化—酰化”机
師師 !*&)
N !$&"
Cl !$&$
!$&’
理如图2所示。下列说法错误的是
!$&(
*&" $&" +&" ’&"
% $ !%" * ,-*"%+.!*/
%" & (*( !
% %" $ & ()’ * + &
% $ % !"’ ()’ %" $ ,&*
%
$ () 活性氧 () *
( ( ) ) % ()’ !" & ()’ & +
# $ % () * () ! ! " " %"’ %" (*,
!" &’ () * !" # !! %" !" $ ,& ()’ (*(
硫酸溶液 甲醇溶液 !" $ ()’
(*, ,&&*
图1 图2
6*!.!*!054!32-,#10"
催化剂!
催化剂"
A.催化剂Ⅰ的催化效率更高
B.升高温度,速率常数增大
C.kk的值不变时,反应达到了平衡状态 正 逆
a
D.平衡时,H 的平衡转化率为 ×100%
2 Q14.金属间化合物 X用于半导体制造及恒温控制通讯领域。X的立方晶胞如图所示,晶胞边长为 ③根据上述实验得出结论:常温下,KClO 的氧化性比 NaClO弱。下列叙述正确且可以为该
3
1 3 1 结论提供支持的是 (填字母)。
qnm,a、b原子的分数坐标为(0,0,0)、( , , )。下列说法正确的是
4 4 4 A.基态 Cl原子的价层电子排布式为3s23p5,ClO-和 ClO-中 Cl的杂化方式相同
3
A.X中 M与 N的原子数之比为21 B.同一元素的高价含氧酸的氧化性强于低价含氧酸的氧化性
1 3 3 ’ C.ClO-和 ClO-被还原的过程中均存在 Cl—O键的断裂,Cl—O键越长,键能越小,断裂越
B.c原子的分数坐标为( , , ) 3
"
4 4 4
容易,氧化性越强
C.M原子周围距离最近且等距的 N原子数为4 !"! !"! ! & #
$ 16.(14分)红土镍矿资源丰富、采矿成本低,研究红土镍矿的开发具有重要的研究价值。某红土镍矿
# !"! %
(主要含有FeO、FeO、NiO、MgO、SiO)为原料制备黄钠铁矾和Ni(OH)的工艺流程如下:
2 3 2 2
D.该晶胞沿 z轴的投影为
-! !"#/’0 $%’( 12
& !
#$%& !" ’( )* +, 45*6
二、非选择题:本题共4小题,共58分。
15.(14分)次氯酸钠常用于污水净化、杀菌和染织等。某兴趣小组设计实验制备 NaClO溶液,并对其 ". ’( ,2 )3 )% $)*(+,
& &
氧化性进行探究。已知:ClO-中Cl—O键键长为0.170nm;ClO-中Cl—O键键长为0.157nm。回
3 $%- $%(+
答下列问题:
回答下列问题:
Ⅰ.利用如图所示装置制备 NaClO溶液
(1)基态镍原子的价层电子排布式为 。
浓盐酸 (2)下列措施可以提高“酸浸”速率的是 (填字母),“浸渣”的主要成分为 (填
! ( ) 化学式)。
温度计
% & % & !"#$%&’ a.使用浓硫酸 b.降低温度
溶液
"#$ % c.粉碎红土镍矿 d.适当增大搅拌速度
冰水浴
(3)“沉铁”时生成黄钠铁矾[NaFe(SO)(OH)]的离子方程式为 。
3 4 2 6
(4)图1是“沉铁”时黄钠铁钒形成的温度(t)与 pH之间的关系图,图中阴影部分是黄钠铁矾稳
!"#$溶液 饱和!"#$溶液 磁力搅拌器
定存在的区域。黄钠铁矾的形成较为复杂,可看成正盐和氢氧化物的中间产物,图 2是“沉
A B C D
铁”时溶液的 pH与沉铁率的关系图。根据图中信息,“沉铁”时选择 pH=2.5而不选择更高
(1)装置 A中,盛装浓盐酸的仪器名称为 ,圆底烧瓶中发生反应的离子方程式为
pH的原因是 。
。
#$$
(2)装置 C的作用是 。
%&$
(3)合理选择图中装置,按照气流方向,正确连接装置,连接顺序为 a→
%#$
(填小写字母)。
’$ (4)若装置 D中温度计的温度上升过快,可能导致产物中存在杂质,为避免此状况,针对装置 A
($
应进行的操作为 。
$
Ⅱ.比较 NaClO与 KClO 的氧化性
3
!"
(5)分别以等浓度的 NaClO溶液与 KClO 溶液为氧化剂,在同等的条件下与各还原剂溶液反应,
3
实验结果如表所示:
实验编号 还原剂 NaClO溶液与还原剂反应 KClO 溶液与还原剂反应
3
生成淡黄色沉淀,发生反应的化
1 饱和氢硫酸 无明显现象
学方程式为①
振荡有红褐色沉淀产生,加热现 常温无现象,加热有红褐色沉淀,测得溶液
2 FeSO 溶液
4
象明显 的pH为4,离子方程式为②
高三化学 第5页(共8页) 高三化学 第6页(共8页)
!)!
!""
#$
*+-
# /
#%
*+-!-" #&
#’
*+,-". / #"
# ( & ’ %$ %# %(
图1
)(#"!
!*" !*+ ’*" ’*+ ,*" ,*+ &*"
-.
图2
(5)“沉镁”的目的是生成 MgF沉淀除去 Mg2+。若溶液酸性过强,Mg2+沉淀不完全,从平衡移动
2
的角度解释原因: ;若溶液碱性过强,则容易形成氢氧化镁的悬
浊液:MgF(s)+2OH-(aq)幑幐Mg(OH)(s)+2F-(aq),K= 。(已知 25℃时,
2 2
K(MgF)=6.0×10-11,K [Mg(OH)]=6.0×10-12)
sp 2 sp 2
(6)Ni(OH) 是镍氢蓄电池的正极材料,在碱性电解质中,电池充电时,Ni(OH) 变为
2 2
NiO(OH),则电池放电时正极的电极反应式为 。17.(15分)绝对无水乙醇是纯度为 100%的乙醇,在常温常压下是一种易燃、易挥发的无色透明液 Ⅲ.2CO(g)+O(g)幑幐2CO(g) ΔH=ckJ·mol-1
2 2 3
体。由无水乙醇制备绝对无水乙醇的部分装置(夹持和加热装置略)和实验步骤如下: Ⅳ.2NO(g)+2CO(g)幑幐2CO(g)+N(g) ΔH<0
2 2 4
Ⅰ.向圆底烧瓶中加入10g无水乙醇和0.3g金属镁,连接好装置(图 1),将烧瓶中液体加热至 ΔH= (用含 a、b、c的代数式表示),反应Ⅳ在 (填“高温”“低温”或“任意温
4
微沸后停止加热。 度”)条件下能自发进行。
Ⅱ.向烧瓶中加入2粒碘,碘粒发生剧烈反应,溶液变成紫红色。 (2)温度为 TK,有催化剂存在时,向恒容密闭容器中加入1molCO(g)和1molNO(g),分别在
Ⅲ.将体系用小火加热回流,使碘反应完全。当溶液变成无色时停止加热。 恒温和绝热条件下,发生反应2NO(g)+2CO(g)幑幐2CO(g)+N(g),测得容器内压强与时
2 2
Ⅳ.向烧瓶中继续加入几粒沸石和20g无水乙醇。小火回流40分钟,回流速度为1~2滴/秒。 间关系如图1所示。
Ⅴ.回流结束后,待反应体系稍冷,将其改装成蒸馏装置(图 2),收集到 26.865g绝对无水乙醇,
并注意密封储存。
碱石灰
"
!
!#$ 甲 ! 碱石灰 乙 # "$$ "
" "%$
图1 图2
已知:①实验中使用的无水乙醇的质量分数为99.5%,25℃时,其密度约为0.785g·mL-1;
! !
" !
②乙醇镁溶于乙醇,是强亲水性物质,能与乙醇中残留的微量水反应生成不溶于乙醇的氢
氧化镁沉淀。
请回答下列问题:
(1)图1装置中,选用圆底烧瓶的规格应为 ;加入沸石的目的是 。
A.250mL B.150mL C.100mL D.25mL
(2)图1和图2装置中,冷凝管的进水口分别为 (填字母),将图 1中的冷凝管换成图 2
中的冷凝管可能导致的后果是 。
(3)图1和图2中干燥管在本实验中的主要作用是 。
(4)无水乙醇制备绝对无水乙醇的原理:
①步骤Ⅱ中,在碘的作用下,镁与少量乙醇反应生成乙醇镁[(CHO)Mg],发生反应的化
2 5 2
学方程式为 。
②步骤Ⅳ中,乙醇镁与残留水反应生成氢氧化镁沉淀,发生反应的化学方程式为 ,
通过反应,水被转化为固相沉淀物,实现彻底分离。
(5)检验绝对无水乙醇中是否含有 HO可以选择的试剂为 (填名称);本实验中绝对
2
无水乙醇的回收率为 %。
18.(15分)NO的减排和再利用是污染控制技术的重要研究方向。回答下列问题:
(1)用催化剂将 NO和 CO转化为 N 和 CO 是处理尾气的重要方式之一。相关反应如下:
2 2
Ⅰ.4N(g)+2O(g)幑幐4NO(g) ΔH=akJ·mol-1
2 2 2 1
Ⅱ.4NO(g)幑幐2NO(g)+O(g) ΔH=bkJ·mol-1
2 2 2
高三化学 第7页(共8页) 高三化学 第8页(共8页)
)(’&强压
!"#$$$%
#
!&*
图1
)(’&
+(*& ,)*& &(*&
-0 0-./ ,
-0/1.0/
-./ 0-.0/ -0/
-0/
-/
-./
43*2
5)*&
7*&
.6 !" 8777%
&*) 2*7 2*5
-.
&*&
92*)
9$*2
9$*)
94*2
94*)
<;:$#"!
-0/
4 -0/
,
,
-0/ 4
%&’(
图2
①曲线甲对应的反应条件是 (填“恒温”或“绝热”)。
②恒温 TK下,达到化学平衡状态时,CO的转化率为 ;该温度下反应的压强平衡常
数 K= kPa-1(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
p
③图中 CO的转化率:m n(填“>”“<”或“=”)。
(3)Os Pt 催化剂可使热催化 NO合成 NH 反应条件更温和且效率更高,相关反应历程(表
0.1 0.9 3
示吸附态)如图2所示。
①下列说法正确的是 (填字母)。
A.Os Pt(111)的催化效果更好
0.1 0.9
B.在两种催化剂作用下,总反应的平衡常数不同
C.NO与 H 反应生成 NH 的过程中不存在非极性键的断裂和生成
2 3
D.在 Pt(111)催化作用下,反应的决速步骤为 HNOHNH+OH
②已知:“mmol·g -1·h-1”是催化反应中描述催化剂活性的常用单位,其含义为每克金属
metal
催化剂在每小时内催化生成的目标物质的量。若在指定条件下,8gOs Pt 催化剂反应
0.1 0.9
24h产氨38.4mol,则 Os Pt 催化剂的产氨速率为 mmol·g -1·h-1。
0.1 0.9 metal