文档内容
2 0 2 5 上 教 师 资 格 · 化 学 学 科 笔 试
主讲老师 张世雄
粉笔教师教育 粉笔教师目
录
content
1 原子结构与性质
2 分子结构与性质
3 晶体结构与性质分子结构与性质P96
(二)范德华力及其对物质性质的影响
1.定义
物质的分子间存在的将分子聚集在一起的作用力称为分子间作用
力,也称范德华力。
范德华力很弱,约比化学键的键能小 1~2 个数量级。
2.影响
范德华力影响物质的熔点、沸点、溶解度等物理性质。
(1)相对分子质量越大,范德华力越大。
例如:卤素单质从 F 到 I ,熔、沸点越来越高。
2 2
(2)相对分子质量相同时,分子的极性越大,范德华力越大。P96
(三)氢键及其对物质性质的影响
1.定义
氢原子与电负性大的 X 原子以共价键结合,若与电负性大、半径
小的原子 Y(O、N、F等)接近,在 X 与 Y 之间以 H 为媒介,生成
X-H···Y 形式的一种特殊的分子间或分子内的相互作用,称为氢键。
形成氢键的分子可以是同一种分子,如水分子之间的氢键;也可
以是不同种分子,如一水合氨分子(NH ·H O)之间的氢键。
3 2
氢键不属于化学键,强度介于化学键与范德华力之间。
作用力强弱比较:化学键>氢键>分子间作用力P96
2.影响
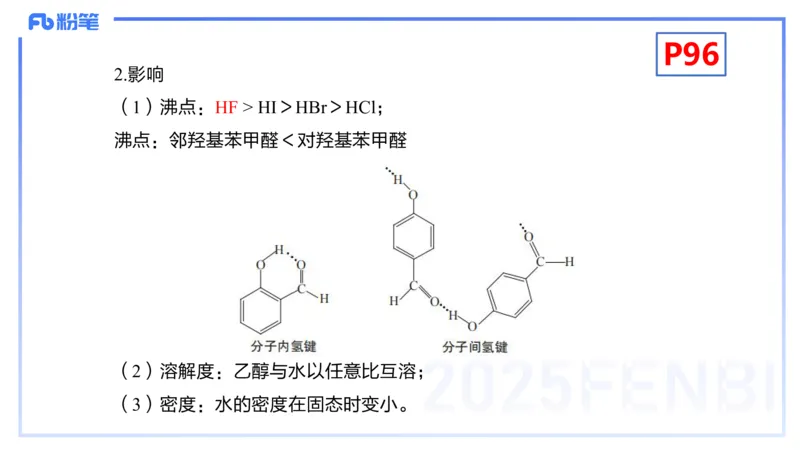
(1)沸点:HF > HI>HBr>HCl;
沸点:邻羟基苯甲醛<对羟基苯甲醛
(2)溶解度:乙醇与水以任意比互溶;
(3)密度:水的密度在固态时变小。P97
3.氢键和范德华力对比
项目 氢键 范德华力
某些物质的分子间(或分子内) 物质的分子间存在的
定义
氢核与非金属原子的静电吸引作用 将分子聚集在一起的作用力
范围 分子间或分子内 分子间
作用力强弱 化学键>氢键>分子间作用力
主要影响物质的物理性质 主要影响物质的物理性质
性质、影响
(如熔点、沸点、密度等) (如熔点、沸点等)P109
4. 可燃冰是一种新型能源,下列表述错误的是( )。
A. 可燃冰是一种化石能源
B. 可燃冰是一种高能清洁能源
C. 可燃冰是甲烷分子与水分子以氢键结合成的晶体
D. 如果开采不当可导致气体泄漏,会引发环境问题P97
(四)溶解性:相似相溶
相似相溶包括两种情况,一种是物质极性的相似,一种是物质结构的相似。
1.分子极性对溶解性的影响
极性溶质一般易溶解于极性溶剂中;非极性溶质一般易溶于非极性溶剂中。
溶质分子与溶剂分子间的范德华力大,则溶质分子的溶解度大。
例如,HCl 易溶于水,而 CH 不易溶于水;Br 和 I 易溶于苯,而水难溶于苯。
4 2 2P98
2.氢键对溶解性的影响
如果存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越
好,反之,不能形成氢键的溶质在有氢键的水中的溶解度就比较小。P98
此外,“相似相溶”还适用于分子结构的相似性。
例如,乙醇的化学式为 CH CH OH,其中的 —OH 与水分子的
3 2
OH- 相近,因而乙醇能与水互溶;
而戊醇 (CH CH CH CH CH OH) 中的烃基较大,其中的 —
3 2 2 2 2
OH 与水分子的 OH- 相似因素小得多,因而它在水中的溶解度就小得
多。P98
(五)手性和手性分子
1.手性碳原子
连有四个不同原子或基团的碳原子称为手性碳原子,常用*C表示。
如 ,R 、R 、R 、R 是互不相同的原子或基团。
1 2 3 4P98
2.手性分子
具有完全相同的组成和原子排列、互为镜像而不能重叠的一对分
子互称手性异构体。有手性异构体的分子叫作手性分子。
互为镜像的两个分子
【粉笔提示】
判断一种有机物是否具有手性异构体,就看其含有的碳原子是否
连有四个不同的原子或基团。(分子中只有一个手性碳原子)P98
3.手性合成
手性异构体药物分子中,往往是一种有毒副作用,而另一种能治
病,没有毒副作用,因此生产手性药物必须把手性异构体分离开。
按照获得2001年诺贝尔化学奖的三位科学家的合成方法,可以只
得到一种手性分子,不得到或者基本不得到它的手性异构分子,这种
独特的合成方法就称为手性合成。手性催化剂只催化或者主要催化一
种手性分子的合成。P99
(六)无机含氧酸分子的酸性
1.无机含氧酸分子的结构
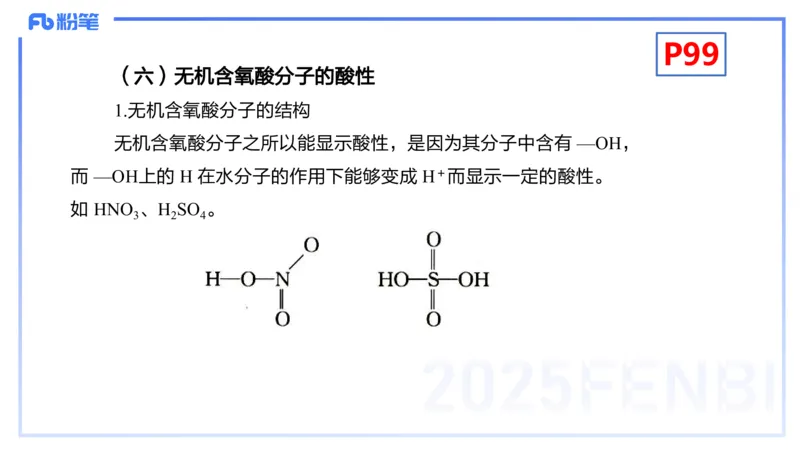
无机含氧酸分子之所以能显示酸性,是因为其分子中含有 —OH,
而 —OH上的 H 在水分子的作用下能够变成 H+而显示一定的酸性。
如 HNO 、H SO 。
3 2 4P99
2.无机含氧酸分子酸性强弱的比较
(1)对于同一种元素的含氧酸,该元素的化合价越高,其含氧酸的酸性越强。
例如 Cl:HClO >HClO >HClO >HClO 。
4 3 2
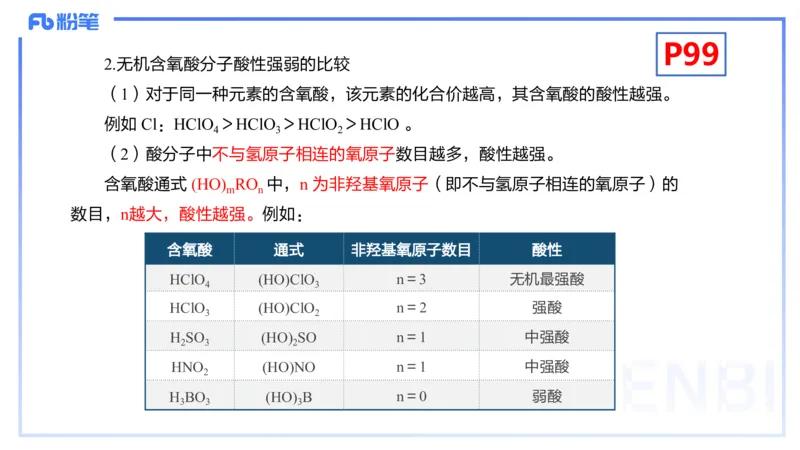
(2)酸分子中不与氢原子相连的氧原子数目越多,酸性越强。
含氧酸通式 (HO) RO 中,n 为非羟基氧原子(即不与氢原子相连的氧原子)的
m n
数目,n越大,酸性越强。例如:
含氧酸 通式 非羟基氧原子数目 酸性
HClO (HO)ClO n=3 无机最强酸
4 3
HClO (HO)ClO n=2 强酸
3 2
H SO (HO) SO n=1 中强酸
2 3 2
HNO (HO)NO n=1 中强酸
2
H BO (HO) B n=0 弱酸
3 3 3P99
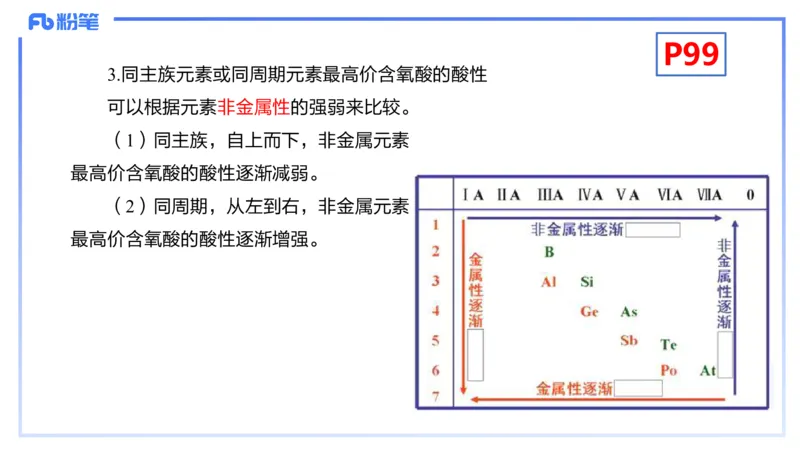
3.同主族元素或同周期元素最高价含氧酸的酸性
可以根据元素非金属性的强弱来比较。
(1)同主族,自上而下,非金属元素
最高价含氧酸的酸性逐渐减弱。
(2)同周期,从左到右,非金属元素
最高价含氧酸的酸性逐渐增强。P100
三、共价键
(一)共价键
1.本质和特征
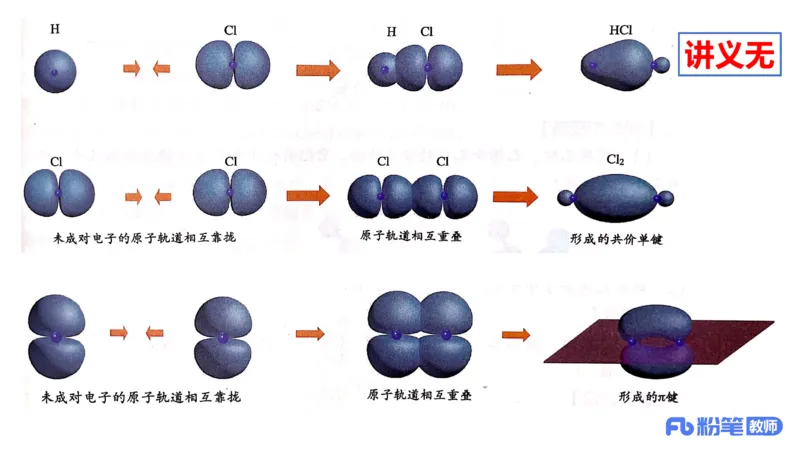
共价键的成键本质是成键原子相互靠近,自旋状态相反的两个电
子形成共用电子对(原子轨道相互重叠),电子出现在两核间的概率
增大,使体系总能量降低。
共价键具有饱和性和方向性。P100
饱和性:按共价键理论,一个原子有几个未成对电子,便可和几
个自旋状态相反的未成对电子配对成键,称为共价键的“饱和性”。
饱和性决定了各种原子形成分子时相互结合的数量关系。
例如,不可能有 H 、H Cl 和 Cl 分子,这表明共价键具有饱和
3 2 3
性。P100
方向性:指参与成键的原子轨道总是尽可能沿着电子出现概率最
大的方向重叠,而且原子轨道重叠越多,键越牢固,方向性决定了分
子的立体结构。
H 中的共价键是由球形的 s 轨道重叠而成的,无方向性。
2P100
2.共价键的类型
(1)按共用电子对是否偏移,分为极性键、非极性键。
(2)按成键原子间共用电子对的数目,分为单键、双键和三键。
(3)按原子轨道的重叠方式不同,分为 σ 键、π 键,前者的电子
云具有轴对称性,后者的电子云具有镜像对称性。P100
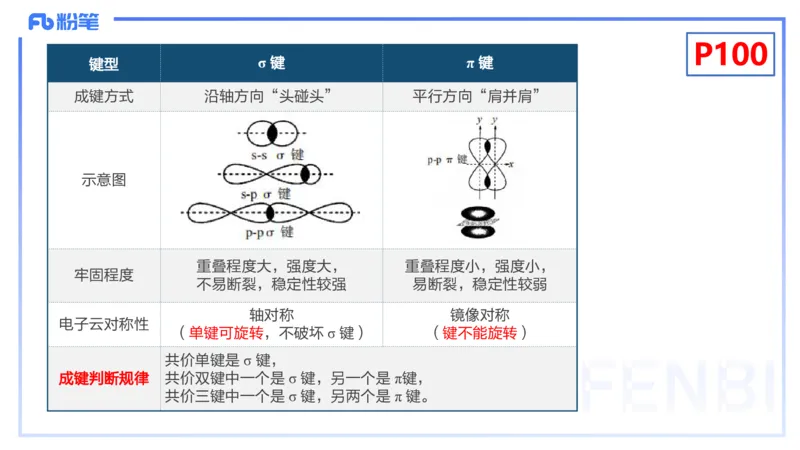
键型 σ 键 π 键
σ 键和 π 键的特征比较如下:
成键方式 沿轴方向“头碰头” 平行方向“肩并肩”
示意图
重叠程度大,强度大, 重叠程度小,强度小,
牢固程度
不易断裂,稳定性较强 易断裂,稳定性较弱
轴对称 镜像对称
电子云对称性
(单键可旋转,不破坏 σ 键) (键不能旋转)
共价单键是 σ 键,
成键判断规律 共价双键中一个是 σ 键,另一个是 π键,
共价三键中一个是 σ 键,另两个是 π 键。讲义无P101
【粉笔提示】
根据电子云的形状和成键时的重叠原则,两个原子之间形成共价
键时,有且只有 1 个 σ 键,其余均为 π 键。可以只形成 σ 键,但不能
只形成 π 键。P101
3.电子式的书写
(1)原子的电子式
用“•”或“×”来表示原子最外层电子。例如 H•、•Mg•、 。
(2)离子的电子式
简单阳离子:用离子符号表示,例如 Na+,Mg2+。
复杂阳离子、阴离子:不仅要画出各个原子的最外层电子,而且
还应用“[ ]”括起来,并在右上角标出所带电荷。P101
(3)离子化合物
由阴、阳离子的电子式构成,但相同的离子不得合并,且带同类电荷的
离子不得相邻(即每一个离子都与带相反电荷的离子直接相邻)。
如 Na O :
2 2P101
(4)共价化合物
共用电子对写在成键两原子中间(一般形成共价键后,成键原子达到
稳定结构),每个原子的最外层电子都要标出,相同的原子不能合并。
例如,CO 的电子式为 ,HCl 的电子式为 。
2P102
4.共价化合物的结构式
用一字线“—”表示共用电子对,例如,CH 的结构式为 。
4P108
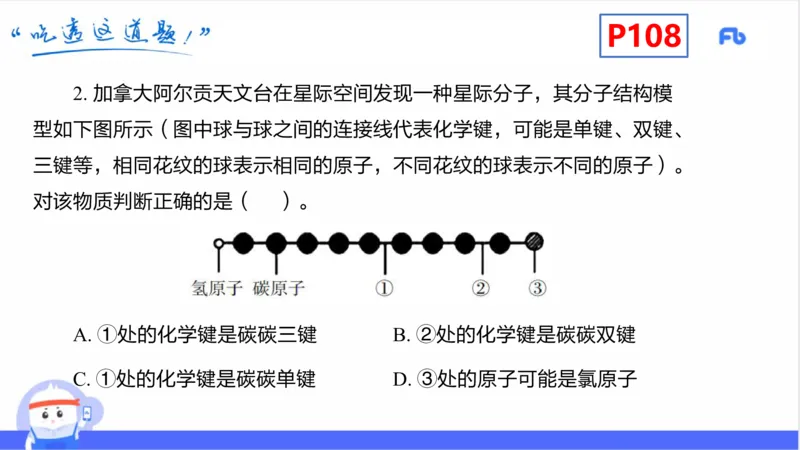
2. 加拿大阿尔贡天文台在星际空间发现一种星际分子,其分子结构模
型如下图所示(图中球与球之间的连接线代表化学键,可能是单键、双键、
三键等,相同花纹的球表示相同的原子,不同花纹的球表示不同的原子)。
对该物质判断正确的是( )。
A. ①处的化学键是碳碳三键 B. ②处的化学键是碳碳双键
C. ①处的化学键是碳碳单键 D. ③处的原子可能是氯原子P102
(二)键参数——键能、键长、键角
键参数 概念 意义
键能越大,化学键越强,越牢
键能 气态基态原子形成 1 mol 化学键释放的最低能量
固,形成的分子越稳定
形成共价键的两个原子之间的核间距
键长越短,化学键越强,
键长 (成键时原子轨道发生重叠,键长小于成键原子的半
形成的分子越稳定
径之和。)
键角 两个共价键之间的夹角 键角决定分子空间构型
键长、键能决定共价键的强弱和分子的稳定性:原子半径越小,
键长越短,键能越大,分子越稳定。P102
例如,HX(X=F、Cl、Br、I) 分子中:
X 原子半径:F < Cl < Br < I 。
H-X键的键长:H-F < H-Cl < H-Br < H-I 。
H-X键的键能:HF > HCl > HBr > HI 。
分子稳定性:HF > HCl > HBr > HI 。P102
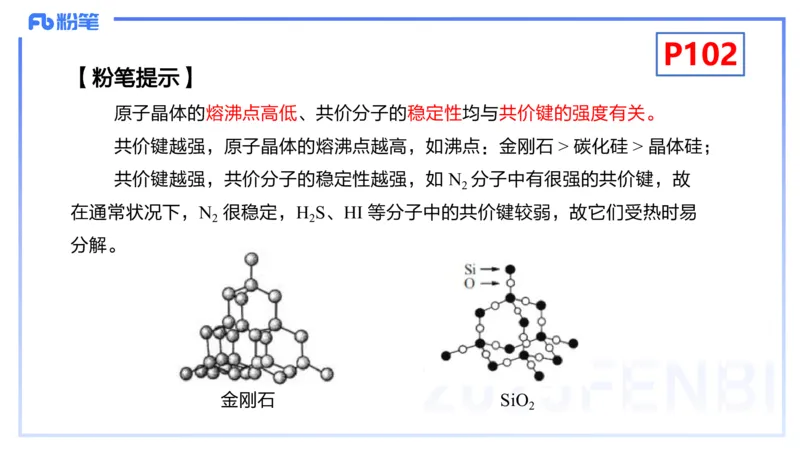
【粉笔提示】
原子晶体的熔沸点高低、共价分子的稳定性均与共价键的强度有关。
共价键越强,原子晶体的熔沸点越高,如沸点:金刚石 > 碳化硅 > 晶体硅;
共价键越强,共价分子的稳定性越强,如 N 分子中有很强的共价键,故
2
在通常状况下,N 很稳定,H S、HI 等分子中的共价键较弱,故它们受热时易
2 2
分解。
金刚石 SiO
2P102
【粉笔提示】
共价分子的熔沸点高低由分子间作用力的大小来决定,而与共价
键的键能无关,如 N 的沸点很低;沸点:F < Cl < Br < I 等。
2 2 2 2 2P103
四、分子的立体结构
(一)杂化轨道理论
1.杂化轨道理论的要点
杂化轨道理论认为,在同一原子中能量相近的不同能级的几条原
子轨道混杂起来,重新组成同等数目的、能量完全相同的杂化原子轨
道。
即有几个原子轨道参加杂化,杂化后就生成几个杂化轨道。
在原子形成分子的过程中,要经过激发、杂化、轨道重叠等过程,
这就是杂化轨道理论的基本要点。P103
2.杂化轨道的类型与分子构型
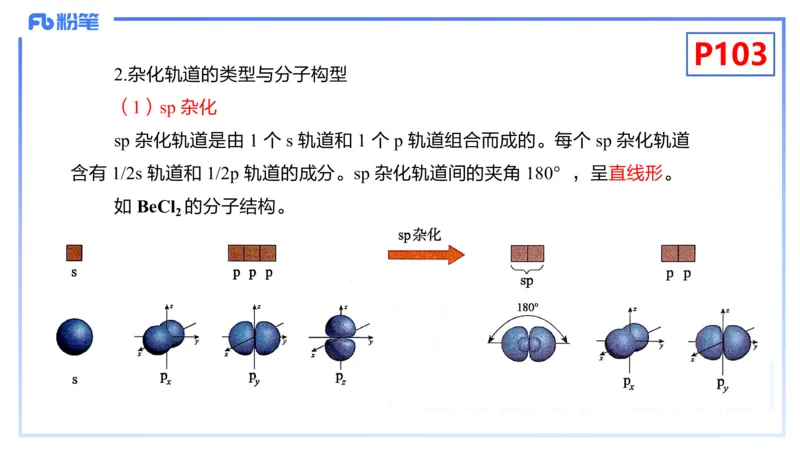
(1)sp 杂化
sp 杂化轨道是由 1 个 s 轨道和 1 个 p 轨道组合而成的。每个 sp 杂化轨道
含有 1/2s 轨道和 1/2p 轨道的成分。sp 杂化轨道间的夹角 180°,呈直线形。
如 BeCl 的分子结构。
2P103
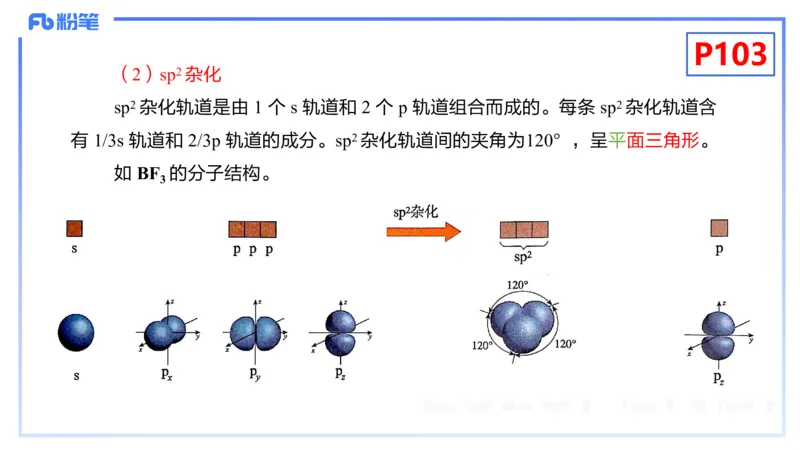
(2)sp2 杂化
sp2 杂化轨道是由 1 个 s 轨道和 2 个 p 轨道组合而成的。每条 sp2 杂化轨道含
有 1/3s 轨道和 2/3p 轨道的成分。sp2 杂化轨道间的夹角为120°,呈平面三角形。
如 BF 的分子结构。
3P103
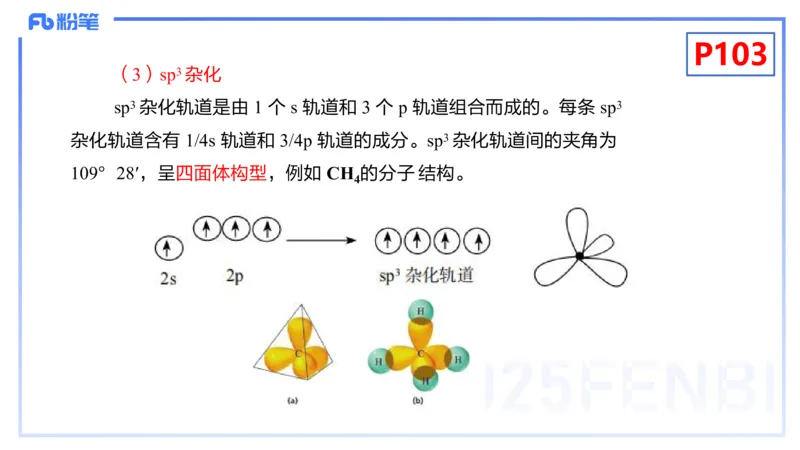
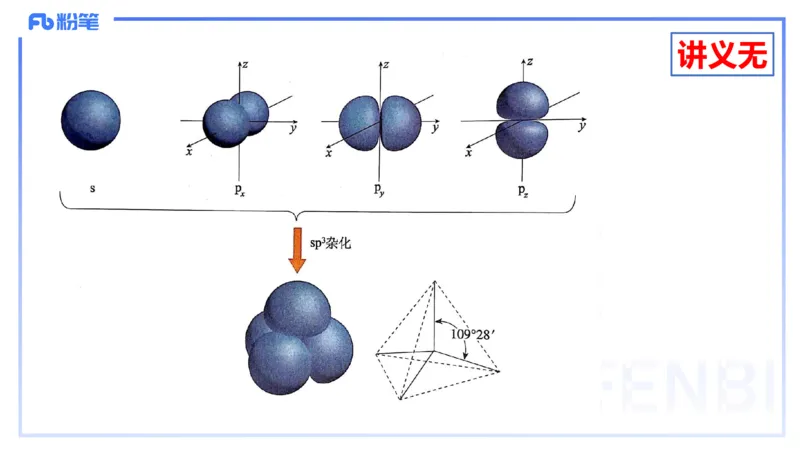
(3)sp3 杂化
sp3 杂化轨道是由 1 个 s 轨道和 3 个 p 轨道组合而成的。每条 sp3
杂化轨道含有 1/4s 轨道和 3/4p 轨道的成分。sp3 杂化轨道间的夹角为
109°28′,呈四面体构型,例如 CH 的分子 结构。
4讲义无P104
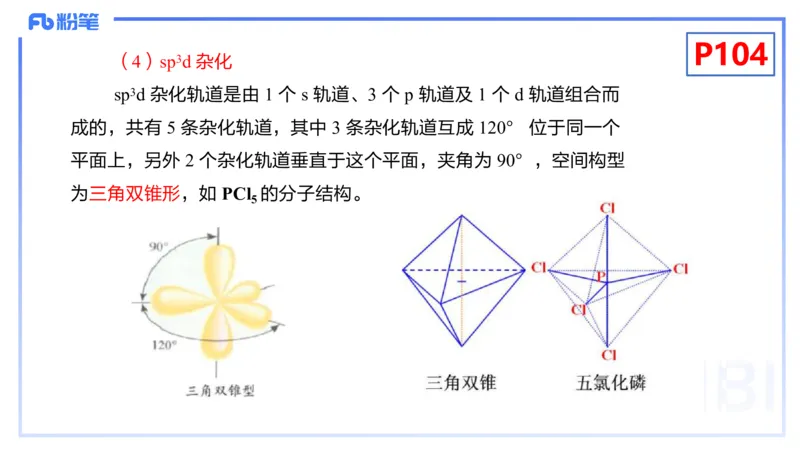
(4)sp3d 杂化
sp3d 杂化轨道是由 1 个 s 轨道、3 个 p 轨道及 1 个 d 轨道组合而
成的,共有 5 条杂化轨道,其中 3 条杂化轨道互成 120° 位于同一个
平面上,另外 2 个杂化轨道垂直于这个平面,夹角为 90°,空间构型
为三角双锥形,如 PCl 的分子结构。
5P104
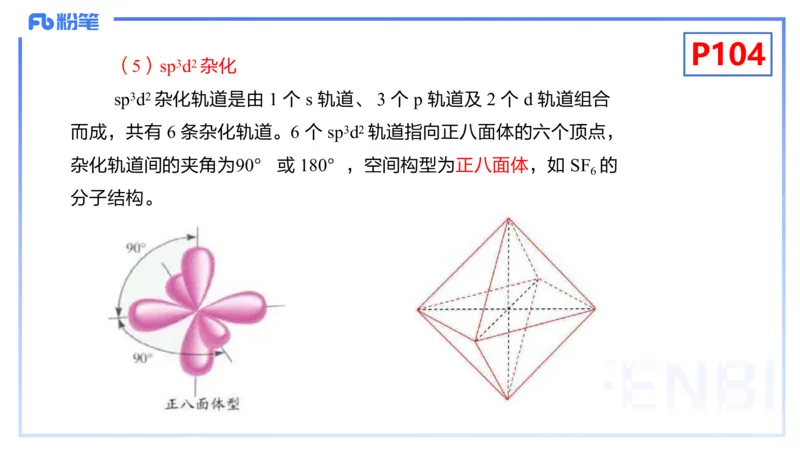
(5)sp3d2 杂化
sp3d2 杂化轨道是由 1 个 s 轨道、 3 个 p 轨道及 2 个 d 轨道组合
而成,共有 6 条杂化轨道。6 个 sp3d2 轨道指向正八面体的六个顶点,
杂化轨道间的夹角为90° 或 180°,空间构型为正八面体,如 SF 的
6
分子结构。P104
(二)价层电子对互斥理论
(确定VSEPR模型、预测分子立体模型)
1.价层电子对互斥理论的要点
(1)分子的立体构型取决于中心原子的价层电子对数。
价层电子对包括 σ 键电子对和中心原子上的孤电子对。P104
(2)价电子对之间存在斥力
斥力来源于两个方面,一是各电子对间的静电斥力,二是电子对中自旋
方向相同的电子间产生的斥力。为减小价层电子对间的排斥力,电子对间应尽
量相互远离。
若按能量最低原理设想中心原子的价电子排布在球面上,其分布方式为:
价层电子对数
2 3 4 5 6
电子对排布 直线形 平面三角形 正四面体 三角双锥 八面体P104
(3)成键电子对由于受两个原子核的吸引,电子云比较集中在键轴的位
置,而孤电子对不受这种限制,显得比较肥大。由于孤电子对肥大,故对相邻电
子对的排斥作用较大。不同价层电子对间的排斥作用顺序如下:
孤电子对—孤电子对 > 孤电子对—成键电子对 > 成键电子对—成键电子对
另外,电子对间的斥力还与其夹角有关,斥力大小顺序是90°>120°>180°。P109
5. 下列说法正确的是( )。
A. H O 中,H—O—H 的键角为 90°
2
B. NH + 中,H—N—H 的键角大于 109°28′,小于 120°
4
C. NH 中 N 以 sp2 杂化轨道与 H 成键,键角为 120°
3
D. NH + 中 N 以 sp3 杂化轨道与 H 成键,键角为 109°28′
4P104
(4)成键电子对只包括形成 σ 键的电子对,不包括形成 π 键的电子
对,即分子中的多重键皆按单键处理。π 键虽然不改变分子的基本构型,但
对键角有一定影响,一般是单键间的键角小,单一双键间及双一双键间键
角较大。P105
2.判断分子的立体构型
(1)分子的立体构型取决于中心原子的价电子对数。中心原子的价层电子对数
等于 σ 键电子对数和 中心原子上的孤电子对数之和。
σ 键电子对数即成键电子对数,而中心原子上的孤电子对数,从分子式中无法直
接得到,需通过计算得出,确定方法如下:
1
中心原子上的孤电子对数 = (a xb)
2
式中 a 为中心原子的价电子数,x 为与中心原子结合的原子数,b 为与中心原子
结合的原子最多能接受的电子数(H 为 1,其他原子为“8 减去该原子的价电子数”,如
O 和第ⅥA 族元素中的 S、Se 等均为 2,卤族元素的原子均为 1,等等)P105
(2)VSEPR模型
根据中心原子的价层电子对数,找出电子对间斥力最小的稳定的
立体构型,
称之为 VSEPR 模型,即理想构型。
价层电子对数 2 3 4 5 6
杂化类型 sp sp2 sp3 dsp2 sp3d sp3d2、d2sp3
VSEPR
直线形 平面三角形 四面体 平面正方形 三角双锥形 八面体
模型名称P105
(3)用 VSEPR 理论确定分子或离子的实际构型的步骤:
确定中心原子的价层电子对数 VSEPR模型 略去VSEPR
模型中中心原子上的孤电子对 分子或离子的实际空间构型P105
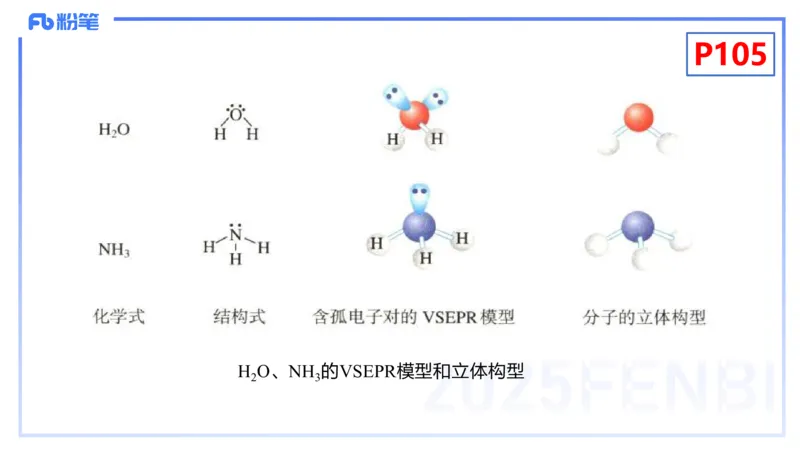
H O、NH 的VSEPR模型和立体构型
2 3P106
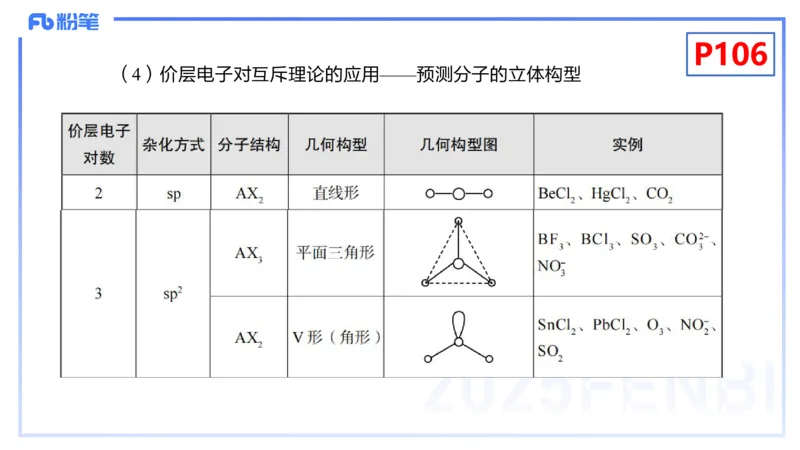
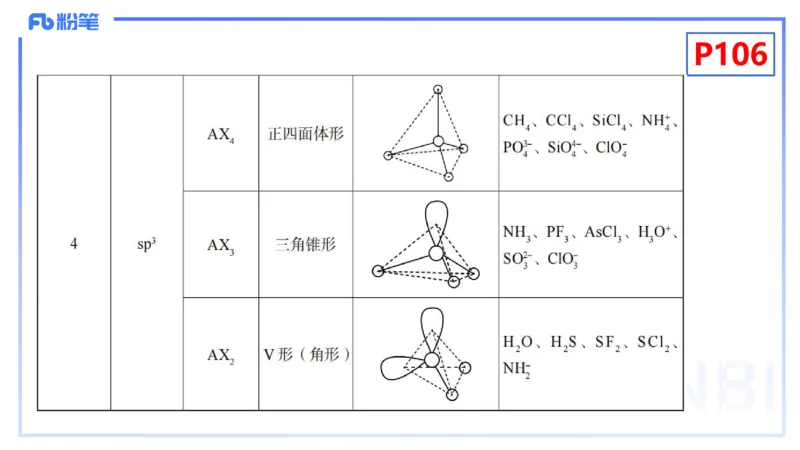
(4)价层电子对互斥理论的应用——预测分子的立体构型P106P108
2. 下列说法正确的是( )。
A. 在 NH 和 BF 中,中心原子均采用 sp2 杂化
3 3
B. 中心原子采取 sp3 杂化轨道成键的分子,其立体构型都是正四面体
C. CH 中的 sp3 杂化轨道是由 4 个 H 的 1s 轨道和 1 个 C 的 2p 轨道混
4
合形成的
D. sp3 杂化轨道是由同一个原子中能量相近的 1 个 s 轨道和 3 个 pP106
(三)等电子原理
1.等电子粒子
电子数相同的粒子(原子、分子、离子)称为等电子粒子。
2.等电子体
原子总数相同、价电子总数相同的粒子互称为等电子体。P106
3.等电子原理
等电子体具有相同的 VSEPR 通式—— AX ,有相似的化学键特
m
征,它们的结构相似,物理性质相似,此原理称为等电子原理。
这里说的“结构特征”的概念既包括分子的立体结构,又包括化
学键的类型,但键角并不一定相等,除非键角为 180° 或 90° 等特
定的角。
例如,CO 和 N 的熔沸点、溶解性、分子解离能等都非常相似。
2P107
【粉笔提示】
常见的等电子体
N 与 CO
2
CO 与 N O
2 2
SO 、O (及 NO -)
2 3 2
CO 2-、NO -与SO
3 3 3
SiO 4-、PO 3-、SO 2-与ClO -等。
4 4 4 4P107
(四)配合物理论简介
通常把金属离子(或原子)与某些分子或离子(称为配体或配位
体)以配位键结合形成的化合物称为配位化合物,简称配合物。
配位键的强度有大有小,因而有的配合物很稳定,有的不稳定。
许多过渡金属离子对多种配体具有很强的结合力,因而,过渡金属配
合物远比主族金属配合物多。P107
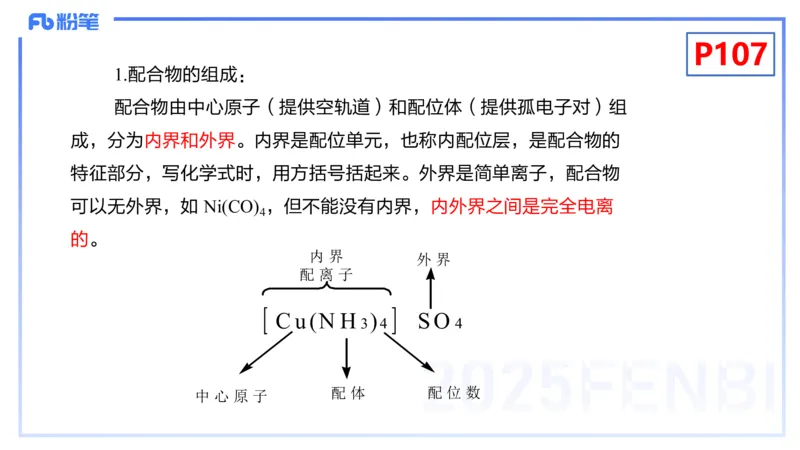
1.配合物的组成:
配合物由中心原子(提供空轨道)和配位体(提供孤电子对)组
成,分为内界和外界。内界是配位单元,也称内配位层,是配合物的
特征部分,写化学式时,用方括号括起来。外界是简单离子,配合物
可以无外界,如 Ni(CO) ,但不能没有内界,内外界之间是完全电离
4
的。
内 界
外 界
配 离 子
C u (N H ) S O
3 4 4
配 体 配 位 数
中 心 原 子P107
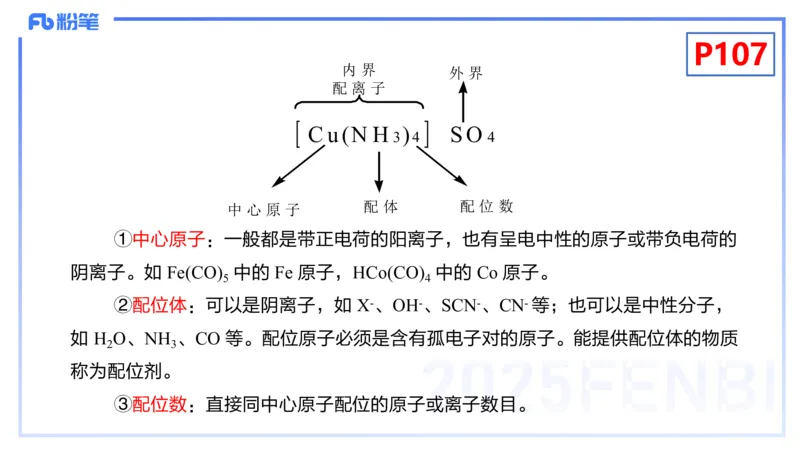
内 界
外 界
配 离 子
C u (N H ) S O
3 4 4
配 体 配 位 数
中 心 原 子
①中心原子:一般都是带正电荷的阳离子,也有呈电中性的原子或带负电荷的
阴离子。如 Fe(CO) 中的 Fe 原子,HCo(CO) 中的 Co 原子。
5 4
②配位体:可以是阴离子,如 X-、OH-、SCN-、CN- 等;也可以是中性分子,
如 H O、NH 、CO 等。配位原子必须是含有孤电子对的原子。能提供配位体的物质
2 3
称为配位剂。
③配位数:直接同中心原子配位的原子或离子数目。P108
2.配合物的异构现象
化学组成相同的配合物可以有不同的结构,这就是配合物的异构
现象。例如,Pt(NH ) Cl 有顺式和反式两种异构体,如下图所示:
3 2 2P108
顺式、反式 Pt(NH ) Cl 的性质差异如下表:
3 2 2
配合物 颜色 极性 在水中的溶解性 抗癌活性
顺式 Pt(NH ) Cl 棕黄色 极性 0.2577g/100gH O 有活性
3 2 2 2
反式 Pt(NH ) Cl 淡黄色 非极性 0.0366g/100gH O 无活性
3 2 2 2P108
3.配合物的应用
(1)Fe3+ 的检验:在含 Fe3+的溶液中滴加 KSCN 溶液,观察到
溶液变成血红色。
Fe3+ + 3SCN- Fe(SCN)
3
(2)银氨溶液的制备原理:往 AgNO 溶液中逐滴滴加稀氨水至
3
沉淀恰好溶解。
Ag+ + NH ·H O AgOH↓+ NH +
3 2 4
AgOH + 2NH ·H O [Ag(NH ) ]+ + OH- + 2H O
3 2 3 2 2粉笔教师教育 粉笔教师