文档内容
丰城九中 2023-2024 学年上学期高三化学第三次段考试卷
本试卷总分值为100分 考试时间75分钟
可能用到的相对原子质量:C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Cr-52 Cu-64 Se-79
Pd-106 Ba-137
一、单选题(每小题3分,共45分)
1.化学促进了科技进步和社会发展,同时也与生活密切相关.下列叙述正确的是( )
A.漂白粉与盐酸可混合使用以提高消毒效率
B.跨洲际往返塞尔维亚的“运-20”机身采用钨碳合金比纯金属钨具有更高的强度和韧性
C.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
D.T-碳(T-Carbon)是中科院预言的一种三维碳结构晶体,其与 互为同位素
2.下列化学用语表示正确的是( )
A.羟基的电子式:
B.基态氨原子的价层电子轨道表示式:
C. 的价层电子对互斥模型:
D. 的名称:3一溴丁烷
3.用下列装置进行实验,仪器选择正确且能达到实验目的的是( )
A B C D
对固体物质中的成分连 浓硫酸与萤石(主要成
除去 中的 快速制备少量
续萃取,节约溶剂且萃
分为 )加热制备
取效率高
HF
A.A B.B C.C D.D
4.向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明
学科网(北京)股份有限公司溶液;在深蓝色溶液中加入等体积的95%乙醇,深蓝色溶液变浑浊,静置后有深蓝色晶体析出.下列对此现
象说法正确的是( )
A. 的内界中含有 键
B. 的空间构型为平面正方形,中心离子 采用 杂化
C. 会与乙醇发生反应生成深蓝色晶体
D. 中所含的化学键有离子键、极性键、配位键、 键
5.物质的结构决定其性质.下列实例与解释不相符的是( )
选项 实例 解释
A He的电子构型稳定,不易得失电子
用He替代 填充探空气球更安全
B
与 形成配合物 中的B有空轨道接受 中N的孤电子对
C 碱金属中Li的熔点最高 碱金属中Li的价电子数最少,金属键最强
D 不存在稳定的 分子 N原子价层只有4个原子轨道,不能形成 5个
键
A.A B.B C.C D.D
6.工业上制一元弱酸——硼酸( )常采用硼镁矿(含 及少量
)
经 溶液溶浸后通过一系列反应制得.下列有关反应及离子方程式均正确的是( )
A.硼酸的解离反应方程式:
B.用KSCN溶液检验溶浸后溶液是否含有
C. 溶于 溶液:
D . 溶 于 溶 液 :
7.下列各实验的操作、现象及所得出的结论都正确的是( )
选项 实验操作 实验现象 结论
A 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐 后,试管里出 氯的非金属性比硅强
酸至红色褪去 现凝胶
学科网(北京)股份有限公司B 向2%稀氨水中滴加2%硝酸银溶液 产生白色沉淀,后消 现配现制银氨溶液
失
C 玻璃棒蘸取少量某溶液进行焰色试验 火焰呈黄色 肯定有钠元素
D 先产生白色沉淀,后 无法比较 ZnS、CuS
向试管中加入 溶液和 2
产生黑色沉淀
溶度积常数 大小
滴 溶液,再滴加2滴
溶液
A.A B.B C.C D.D
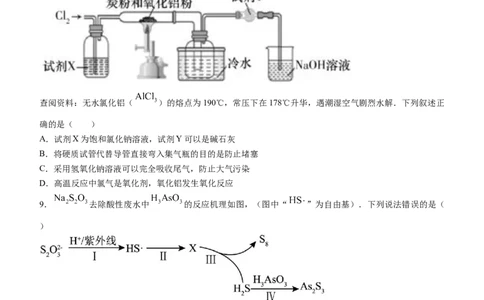
8.氯化铝在有机化学中有很广泛的应用.某兴趣小组设计实验制备少量纯净的无水氯化铝(装置如图,夹持
装置已省略).
查阅资料:无水氯化铝( )的熔点为190℃,常压下在178℃升华,遇潮湿空气剧烈水解.下列叙述正
确的是( )
A.试剂X为饱和氯化钠溶液,试剂Y可以是碱石灰
B.将硬质试管代替导管直接弯入集气瓶的目的是防止堵塞
C.采用氢氧化钠溶液可以完全吸收尾气,防止大气污染
D.高温反应中氯气是氧化剂,氧化铝发生氧化反应
9. 去除酸性废水中 的反应机理如图,(图中“ ”为自由基).下列说法错误的是(
)
A.X的化学式为
B. 反应活性较强,不能稳定存在
C.步骤III反应中氧化剂与还原剂的物质的量比为8:1
D.步骤IV除砷的方程式为
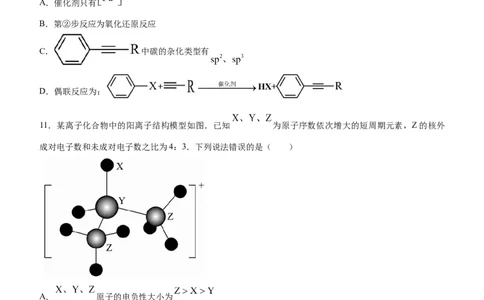
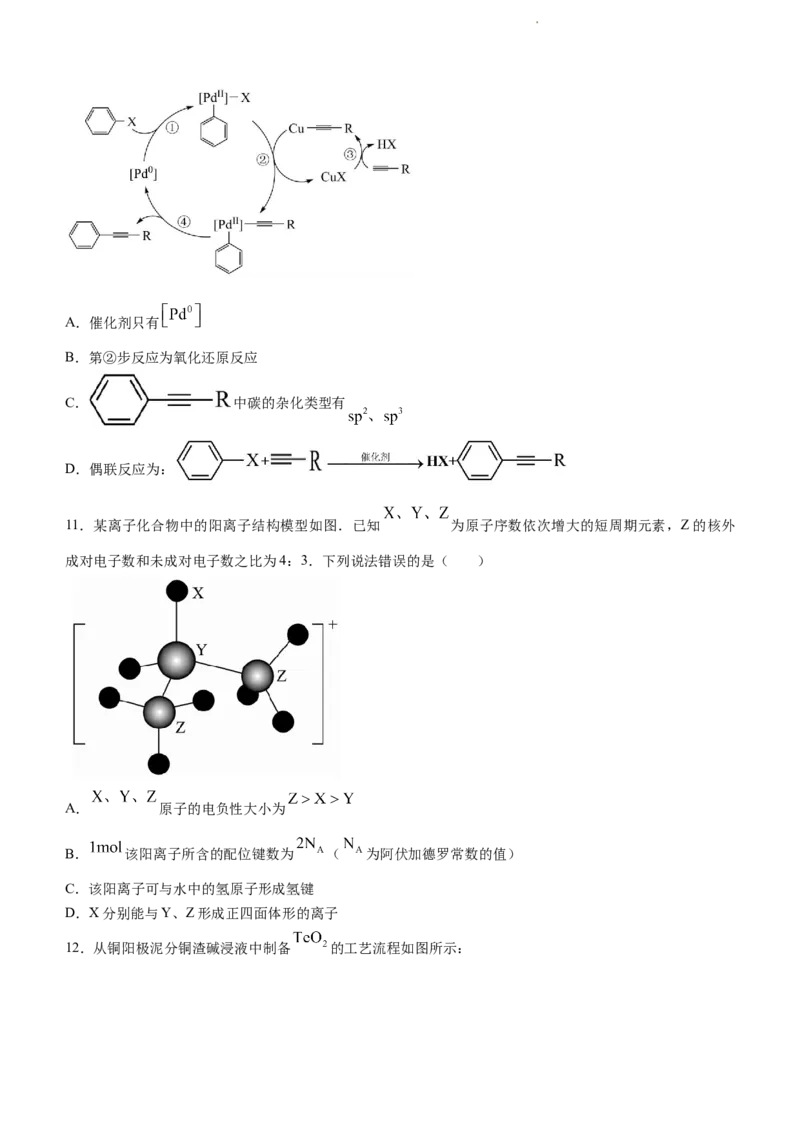
10.如图是催化偶联反应的机理,R—为烷烃基或氢原子.下列说法正确的是( )
学科网(北京)股份有限公司A.催化剂只有
B.第②步反应为氧化还原反应
C. 中碳的杂化类型有
D.偶联反应为:
11.某离子化合物中的阳离子结构模型如图.已知 为原子序数依次增大的短周期元素,Z的核外
成对电子数和未成对电子数之比为4:3.下列说法错误的是( )
A. 原子的电负性大小为
B. 该阳离子所含的配位键数为 ( 为阿伏加德罗常数的值)
C.该阳离子可与水中的氢原子形成氢键
D.X分别能与Y、Z形成正四面体形的离子
12.从铜阳极泥分铜渣碱浸液中制备 的工艺流程如图所示:
学科网(北京)股份有限公司已知:①碱浸液中碲以 的形式存在.
② 与氧化铝的性质具有一定的相似性.
下列说法错误的是( )
A. 中Te的化合价为+4
B.加入的 在反应中被氧化
C.根据上述反应可以推知,还原性:
D.为防止产品产率降低,加入硫酸的量不宜过多
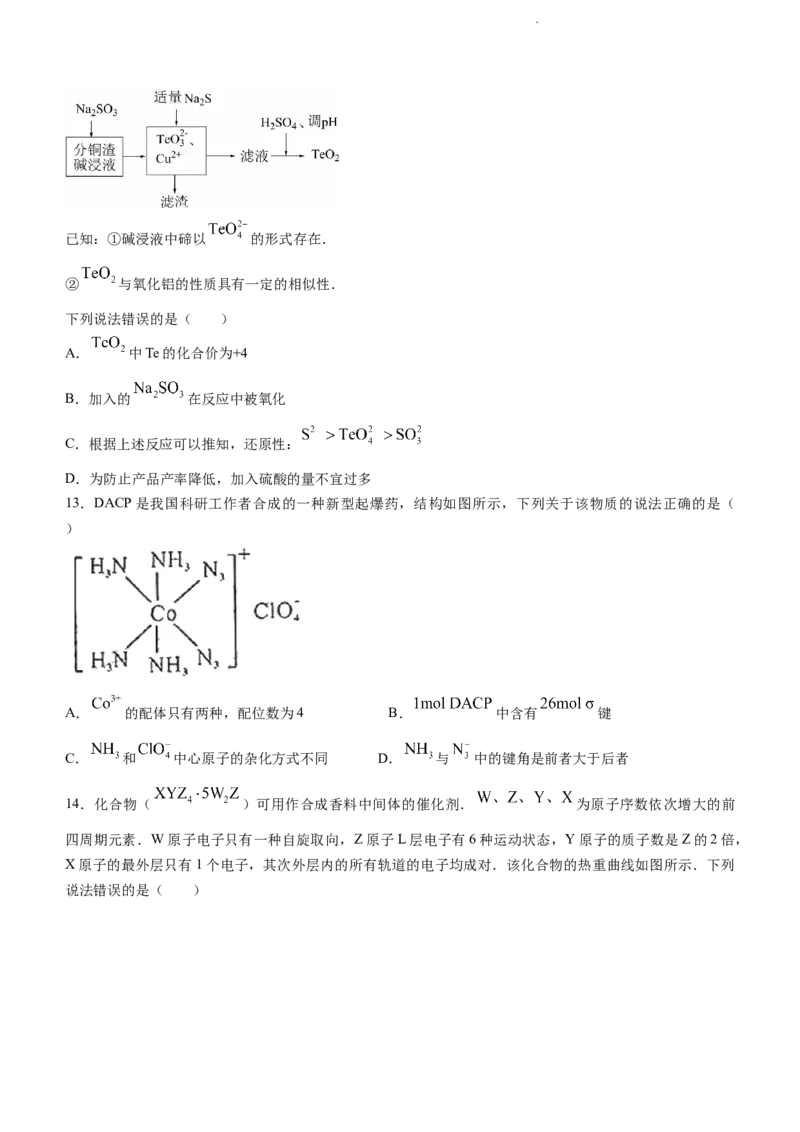
13.DACP是我国科研工作者合成的一种新型起爆药,结构如图所示,下列关于该物质的说法正确的是(
)
A. 的配体只有两种,配位数为4 B. 中含有 键
C. 和 中心原子的杂化方式不同 D. 与 中的键角是前者大于后者
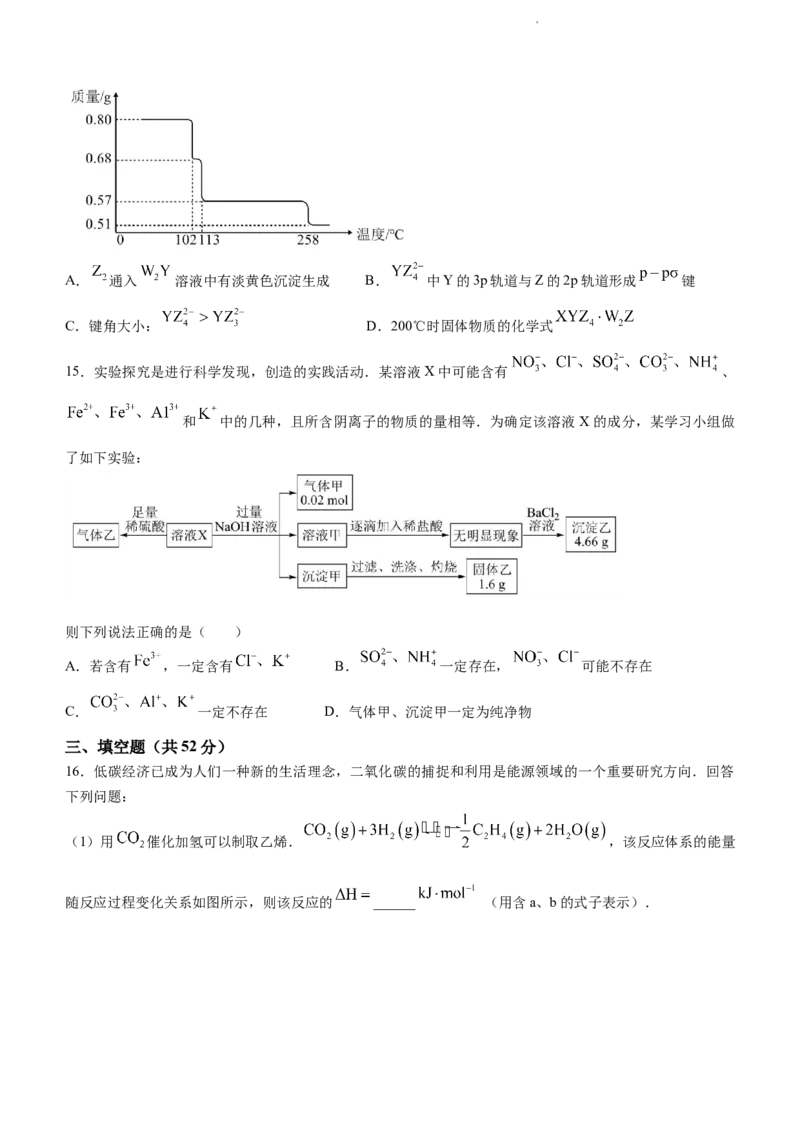
14.化合物( )可用作合成香料中间体的催化剂. 为原子序数依次增大的前
四周期元素.W原子电子只有一种自旋取向,Z原子L层电子有6种运动状态,Y原子的质子数是Z的2倍,
X原子的最外层只有1个电子,其次外层内的所有轨道的电子均成对.该化合物的热重曲线如图所示.下列
说法错误的是( )
学科网(北京)股份有限公司A. 通入 溶液中有淡黄色沉淀生成 B. 中Y的3p轨道与Z的2p轨道形成 键
C.键角大小: D.200℃时固体物质的化学式
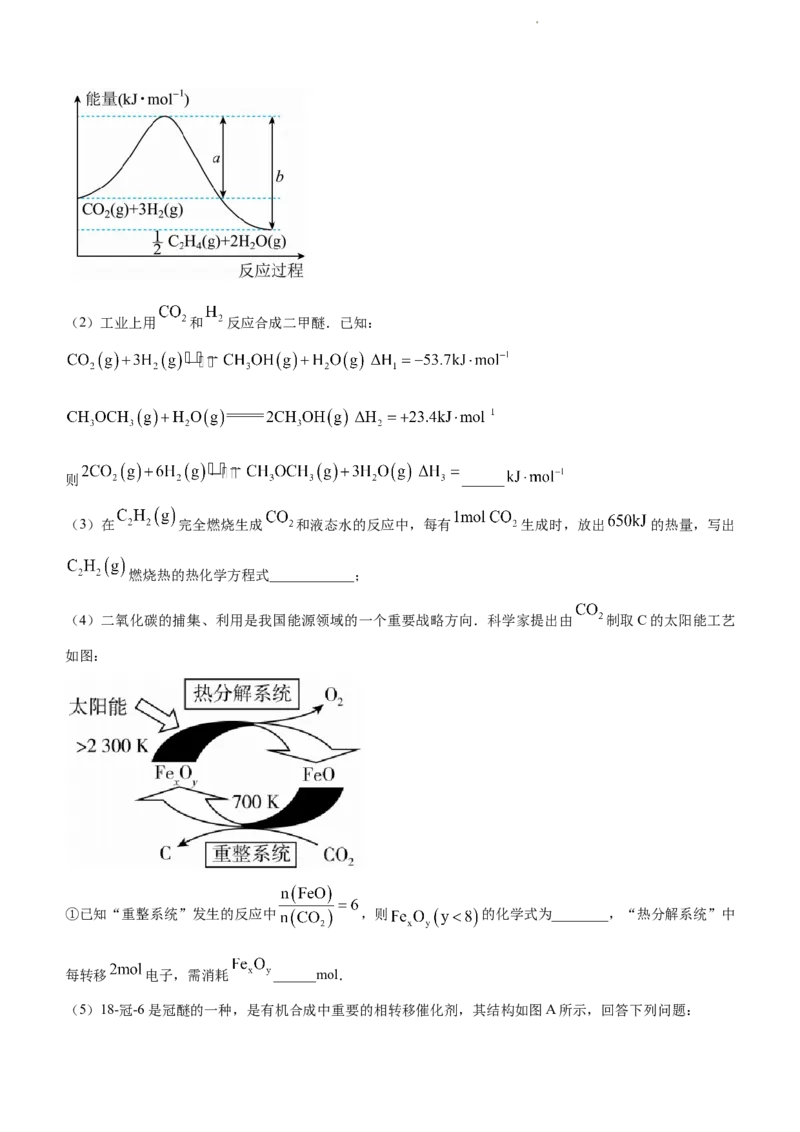
15.实验探究是进行科学发现,创造的实践活动.某溶液X中可能含有 、
和 中的几种,且所含阴离子的物质的量相等.为确定该溶液 X的成分,某学习小组做
了如下实验:
则下列说法正确的是( )
A.若含有 ,一定含有 B. 一定存在, 可能不存在
C. 一定不存在 D.气体甲、沉淀甲一定为纯净物
三、填空题(共52分)
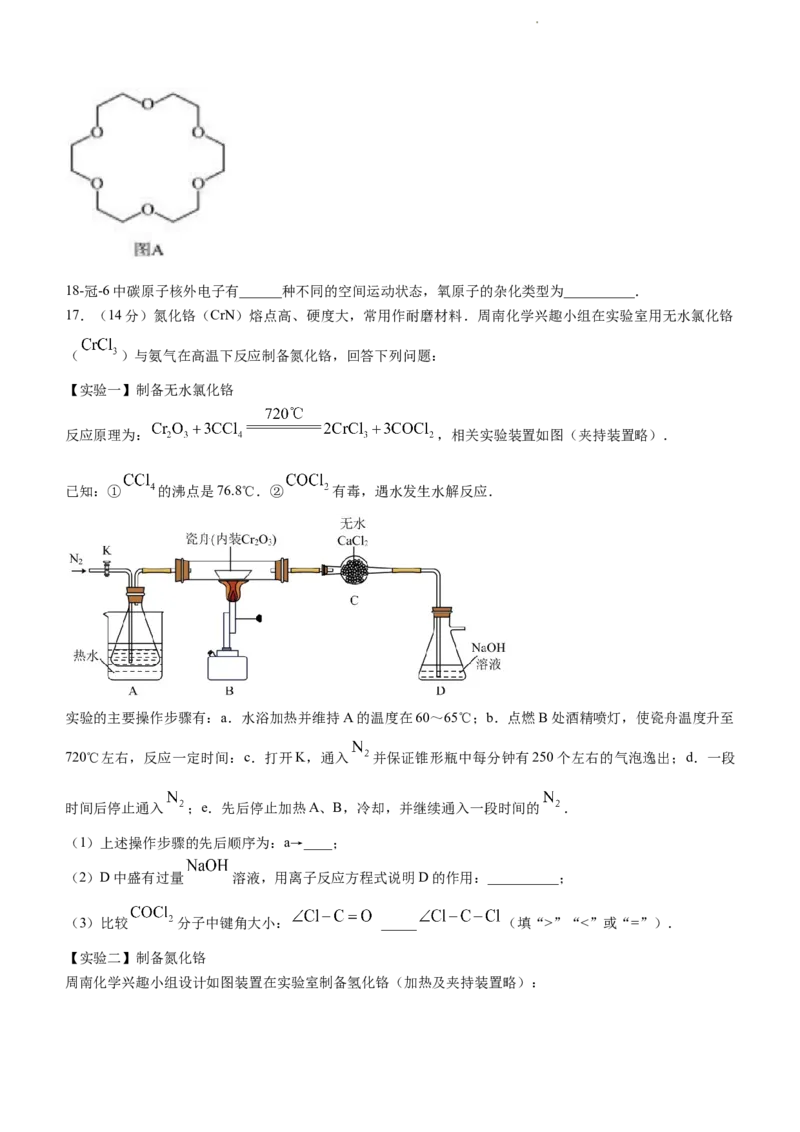
16.低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向.回答
下列问题:
(1)用 催化加氢可以制取乙烯. ,该反应体系的能量
随反应过程变化关系如图所示,则该反应的 ______ (用含a、b的式子表示).
学科网(北京)股份有限公司(2)工业上用 和 反应合成二甲醚.已知:
则 ______
(3)在 完全燃烧生成 和液态水的反应中,每有 生成时,放出 的热量,写出
燃烧热的热化学方程式____________;
(4)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向.科学家提出由 制取C的太阳能工艺
如图:
①已知“重整系统”发生的反应中 ,则 的化学式为________,“热分解系统”中
每转移 电子,需消耗 ______mol.
(5)18-冠-6是冠醚的一种,是有机合成中重要的相转移催化剂,其结构如图A所示,回答下列问题:
学科网(北京)股份有限公司18-冠-6中碳原子核外电子有______种不同的空间运动状态,氧原子的杂化类型为__________.
17.(14分)氮化铬(CrN)熔点高、硬度大,常用作耐磨材料.周南化学兴趣小组在实验室用无水氯化铬
( )与氨气在高温下反应制备氮化铬,回答下列问题:
【实验一】制备无水氯化铬
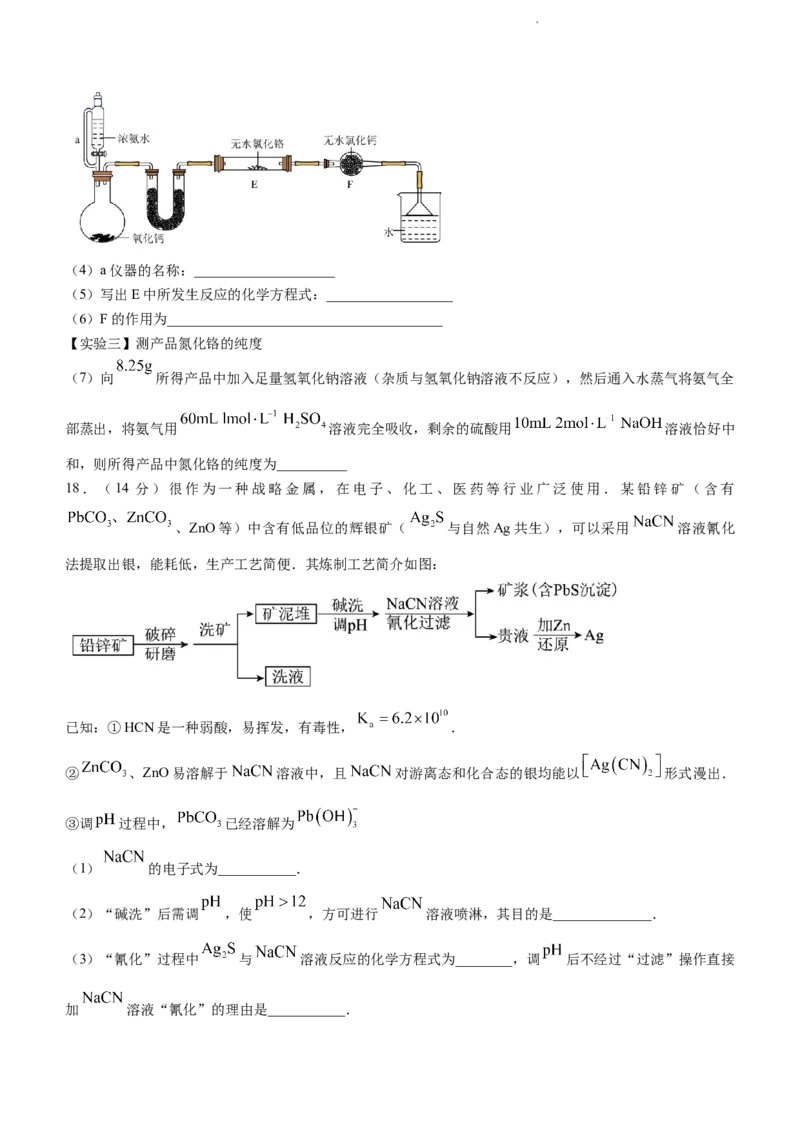
反应原理为: ,相关实验装置如图(夹持装置略).
已知:① 的沸点是76.8℃.② 有毒,遇水发生水解反应.
实验的主要操作步骤有:a.水浴加热并维持A的温度在60~65℃;b.点燃B处酒精喷灯,使瓷舟温度升至
720℃左右,反应一定时间:c.打开K,通入 并保证锥形瓶中每分钟有250个左右的气泡逸出;d.一段
时间后停止通入 ;e.先后停止加热A、B,冷却,并继续通入一段时间的 .
(1)上述操作步骤的先后顺序为:a→____;
(2)D中盛有过量 溶液,用离子反应方程式说明D的作用:__________;
(3)比较 分子中键角大小: _____ (填“>”“<”或“=”).
【实验二】制备氮化铬
周南化学兴趣小组设计如图装置在实验室制备氢化铬(加热及夹持装置略):
学科网(北京)股份有限公司(4)a仪器的名称:____________________
(5)写出E中所发生反应的化学方程式:__________________
(6)F的作用为_______________________________________
【实验三】测产品氮化铬的纯度
(7)向 所得产品中加入足量氢氧化钠溶液(杂质与氢氧化钠溶液不反应),然后通入水蒸气将氨气全
部蒸出,将氨气用 溶液完全吸收,剩余的硫酸用 溶液恰好中
和,则所得产品中氮化铬的纯度为__________
18.(14 分)很作为一种战略金属,在电子、化工、医药等行业广泛使用.某铅锌矿(含有
、ZnO等)中含有低品位的辉银矿( 与自然Ag共生),可以采用 溶液氰化
法提取出银,能耗低,生产工艺简便.其炼制工艺简介如图:
已知:①HCN是一种弱酸,易挥发,有毒性, .
② 、ZnO易溶解于 溶液中,且 对游离态和化合态的银均能以 形式漫出.
③调 过程中, 已经溶解为
(1) 的电子式为___________.
(2)“碱洗”后需调 ,使 ,方可进行 溶液喷淋,其目的是______________.
(3)“氰化”过程中 与 溶液反应的化学方程式为________,调 后不经过“过滤”操作直接
加 溶液“氰化”的理由是___________.
学科网(北京)股份有限公司(4)矿泥堆要有良好的渗透性和孔隙度,其原因是______________.
(5)“氰化法”中最终矿浆需要用 溶液消毒处理,发生的离子反应方程式为________,处理
含 的废水,实际至少需 ________g(实际用量应为理论值的4倍),才能使
含量低于 ,达到排放标准.
19 . 一 种 废 镍 催 化 剂 中 含 有 及 碳 粉 , 以 其 为 原 料 制 备 环 烷 酸 镍 [
,常温下为难溶于水的液体]的工艺流程如图所示:
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的 如表所示:
金属离子
开始沉淀的 1.9 7.0 6.4 5.4
完全沉淀的 3.2 9.0 8.4 6.7
回答下列问题:
(1)“灼烧”后Cr转化为 ,已知 与 性质相似,则滤液中阴离子有 、______.基态
Cr原子的价层电子排布式为______________.
(2)“酸溶”时,先加入一定量的水,然后分次加入浓硫酸,与直接用稀硫酸溶解相比,其优点是
___________.
(3)“调 ”时,溶液 的范围为______________.
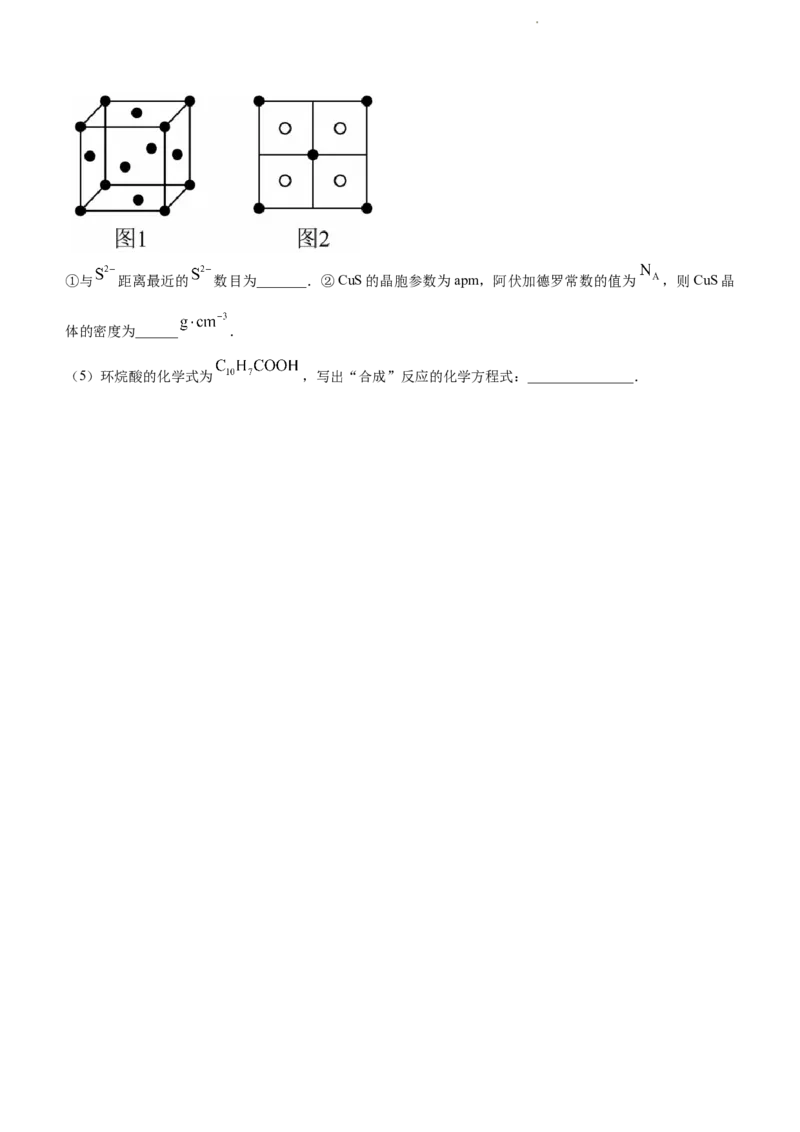
(4)常温下,CuS的 极小,用 可将 完全沉淀.CuS晶胞中 的位置如图1所示, 位于
所构成的四面体中心,晶胞侧视图如图2所示.
学科网(北京)股份有限公司①与 距离最近的 数目为_______.②CuS的晶胞参数为apm,阿伏加德罗常数的值为 ,则CuS晶
体的密度为______ .
(5)环烷酸的化学式为 ,写出“合成”反应的化学方程式:_______________.
学科网(北京)股份有限公司