文档内容
眉山市 2020 年初中学业水平暨高中阶段学校招生考试
化学试题
可能用到的相对原子质量H-1 C-12 N-14 O-16 Na-23 Mg-24 C1-35.5 Mn-55 Cu-64
Ag-108 Ba-137
第I卷(选择题1-26小题,共64分)
一、选择题:(本大题共26个小题,1-14每小题2分,15-26每小题3分;共计64分。在每
小题列出的四个选项中,只有一项符合题目要求)
1.物质世界在不断的变化,下列变化只发生了物理变化的是( )
A. 食物腐烂
B. 将矿石研磨成粉末
C. 熟石灰改良酸性土壤
D. 燃放烟花爆竹
【答案】B
【解析】
【详解】A、食物腐烂生成有害物质,属于化学变化,不符合题意;
B、将矿石研磨成粉末没有新物质生成,属于物理变化,符合题意;
C、熟石灰显碱性,熟石灰改良酸性土壤是熟石灰与酸反应,属于化学变化,不符合题意;
D、燃放烟花爆竹生成有害气体和烟尘,属于化学变化,不符合题意。故选B。
2.地球上资源日渐枯竭,我们应该节约资源、合理利用。下列资源属于纯净物的是( )
A. 石油
B. 空气
C. 赤铁矿
D. 冰水混合物
【答案】D
【解析】
【详解】A、石油中有汽油、煤油、柴油等,属于混合物,不符合题意;
B、空气中有氧气、氮气等,属于混合物,不符合题意;
C、赤铁矿中有氧化铁和杂质,属于混合物,不符合题意;
D、冰水混合物中只有水分子,属于纯净物,符合题意。故选D。
3.“绿水青山就是金山银山”,保护环境是每个公民应尽的义务。下列做法与此不相符的是( )
A. 农业上过量施用化肥、农药B. 废旧电池回收利用
C. 有计划、合理地开采矿物
D. 使用新型、可降解的塑料制品
【答案】A
【解析】
【详解】A、农业上过量施用化肥、农药,既浪费化肥和农药,又会造成土壤和水体污染,符合题意;
B、废旧电池回收利用既能节约金属资源、能源,又能保护环境,不符合题意;
C、有计划、合理地开采矿物有利于保护矿物资源,不符合题意;
D、使用新型、可降解的塑料制品可以有效防治白色污染,不符合题意。故选A。
4.我们知道物质的性质决定其用途。下列说法不正确的是( )
A. 干冰升华吸热,可用作制冷剂
B. 酸能与金属氧化物反应,可用盐酸除铁锈
C. 银是导电性最好的金属,电线一般用银制
D. 合金具有优良的性能,日常使用的金属材料大多数属于合金
【答案】C
【解析】
【详解】A、干冰是固体二氧化碳,升华吸热,可作制冷剂,故正确;
B、铁锈的主要成分是氧化铁,可以与酸反应生成氯化铁和水,故正确;
C、电线一般用铜制,这是由于性质很大程度上决定了物质的用途,但还有考虑价格,是否美观等因素,
故错误;
D、金属材料包括金属和合金,合金具有优良的性能,日常使用的金属材料大多数属于合金,故正确。
故选C
5.归类整理是生活中的一种常用方法,也是学习化学的一种重要方法。以下归类正确的是( )
A. 常见的碱:烧碱、纯碱、熟石灰
B. 常见的白色沉淀:CaCO 、BaSO、Cu(OH)
3 4 2
C. 常见的还原性物质:C、CO、H
2
D. 常见的合成材料:棉花、合成纤维、合成橡胶
【答案】C
【解析】
【详解】A、纯碱是碳酸钠的俗称,是由金属阳离子与酸根阴离子构成的化合物,属于盐,故选项错误;
B、氢氧化铜是一种蓝色沉淀,故选项错误;
C、C、CO、H 都具有还原性,故选项正确;
2
D、棉花属于天然材料,故选项错误。故选C。6.下列有关反应的化学方程式完全正确的是( )
A. 铁在氧气中燃烧:
B. 银放入稀盐酸中:
C. 碳酸钠投人稀盐酸中:
D. 氯酸钾分解制氧气:2KClO 2KCl+3O ↑
3 2
【答案】D
【解析】
【详解】A、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为 ,故选项错误;
B、在金属活动性顺序中,银的位置排在氢的后面,不能与稀盐酸反应,故选项错误;
C、该化学方程式没有配平,正确的化学方程式应为:Na CO +2HCl═2NaCl+CO ↑+H O,故选项错误;
2 3 2 2
D、该化学方程式书写完全正确,故选项正确。故选D。
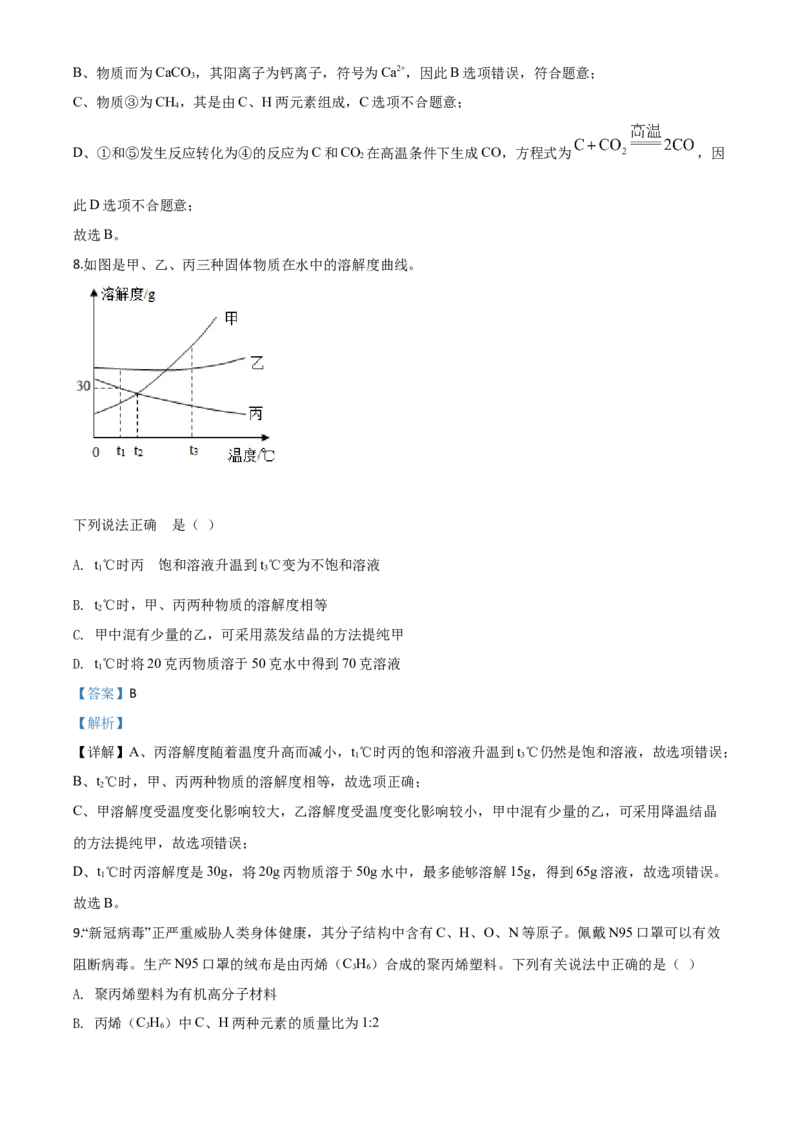
7.构建知识网络能提高学习的效率。下图为有关CO 的知识网络图,以下判断错误的是( )
2
A. 物质①中碳元素的化合价为+4价
B. 物质②中阳离子符号为Ca+2
C. 物质③由2种元素组成
D. 物质①和⑤发生反应转化为④的化学方程式为:
【答案】B
【解析】
【详解】A、物质①是CO,根据化学式代数和为0,其中氧为-2价,因此C为+4价,A选项不合题意;
2B、物质而为CaCO ,其阳离子为钙离子,符号为Ca2+,因此B选项错误,符合题意;
3
C、物质③为CH,其是由C、H两元素组成,C选项不合题意;
4
D、①和⑤发生反应转化为④的反应为C和CO 在高温条件下生成CO,方程式为 ,因
2
此D选项不合题意;
故选B。
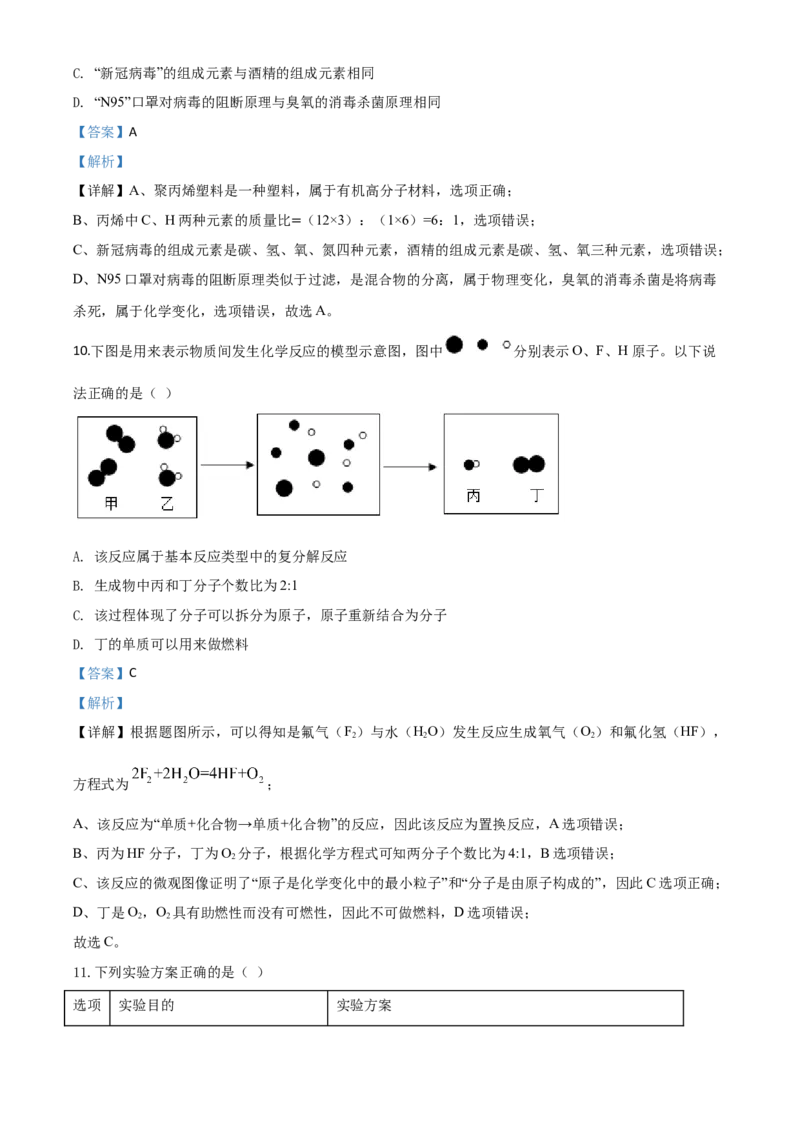
8.如图是甲、乙、丙三种固体物质在水中的溶解度曲线。
下列说法正确 的是( )
的
A. t℃时丙 饱和溶液升温到t℃变为不饱和溶液
1 3
B. t℃时,甲、丙两种物质的溶解度相等
2
C. 甲中混有少量的乙,可采用蒸发结晶的方法提纯甲
D. t℃时将20克丙物质溶于50克水中得到70克溶液
1
【答案】B
【解析】
【详解】A、丙溶解度随着温度升高而减小,t℃时丙的饱和溶液升温到t℃仍然是饱和溶液,故选项错误;
1 3
B、t℃时,甲、丙两种物质的溶解度相等,故选项正确;
2
C、甲溶解度受温度变化影响较大,乙溶解度受温度变化影响较小,甲中混有少量的乙,可采用降温结晶
的方法提纯甲,故选项错误;
D、t℃时丙溶解度是30g,将20g丙物质溶于50g水中,最多能够溶解15g,得到65g溶液,故选项错误。
1
故选B。
9.“新冠病毒”正严重威胁人类身体健康,其分子结构中含有C、H、O、N等原子。佩戴N95口罩可以有效
阻断病毒。生产N95口罩的绒布是由丙烯(C H)合成的聚丙烯塑料。下列有关说法中正确的是( )
3 6
A. 聚丙烯塑料为有机高分子材料
B. 丙烯(C H)中C、H两种元素的质量比为1:2
3 6C. “新冠病毒”的组成元素与酒精的组成元素相同
D. “N95”口罩对病毒的阻断原理与臭氧的消毒杀菌原理相同
【答案】A
【解析】
【详解】A、聚丙烯塑料是一种塑料,属于有机高分子材料,选项正确;
B、丙烯中C、H两种元素的质量比 (12×3):(1×6)=6:1,选项错误;
C、新冠病毒的组成元素是碳、氢、=氧、氮四种元素,酒精的组成元素是碳、氢、氧三种元素,选项错误;
D、N95口罩对病毒的阻断原理类似于过滤,是混合物的分离,属于物理变化,臭氧的消毒杀菌是将病毒
杀死,属于化学变化,选项错误,故选A。
10.下图是用来表示物质间发生化学反应的模型示意图,图中 分别表示O、F、H原子。以下说
法正确的是( )
A. 该反应属于基本反应类型中的复分解反应
B. 生成物中丙和丁分子个数比为2:1
C. 该过程体现了分子可以拆分为原子,原子重新结合为分子
D. 丁的单质可以用来做燃料
【答案】C
【解析】
【详解】根据题图所示,可以得知是氟气(F )与水(HO)发生反应生成氧气(O )和氟化氢(HF),
2 2 2
方程式为 ;
A、该反应为“单质+化合物→单质+化合物”的反应,因此该反应为置换反应,A选项错误;
B、丙为HF分子,丁为O 分子,根据化学方程式可知两分子个数比为4:1,B选项错误;
2
C、该反应的微观图像证明了“原子是化学变化中的最小粒子”和“分子是由原子构成的”,因此C选项正确;
D、丁是O,O 具有助燃性而没有可燃性,因此不可做燃料,D选项错误;
2 2
故选C。
11.下列实验方案正确的是( )
选项 实验目的 实验方案A 除去CO 中混有的HC1气体 将混合气体通过装有足量NaOH溶液的洗气瓶
2
B 鉴别NaCO 溶液和NaCl溶液 取少许样品于两支试管中,分别滴加无色酚酞试液
2 3
C 除去CaO中混有的CaCO 将混合物溶于水后过滤
3
D 除去MnO 中混有 的KCl 加水溶解、过滤、蒸发结晶
2
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、二氧化碳与氢氧化钠溶液会发生反应,相当于破坏了原物质,故不符合题意;
B、滴加无色酚酞试液,溶液变红则为碳酸钠溶液,无明显变化则为氯化钠溶液,故符合题意;
C、氧化钙和水反应生成氢氧化钙,破坏了原物质,故不符合题意;
D、欲想除去MnO 中混有的KCl,应加水溶解、过滤、洗涤干燥,故不符合题意。
2
故选B
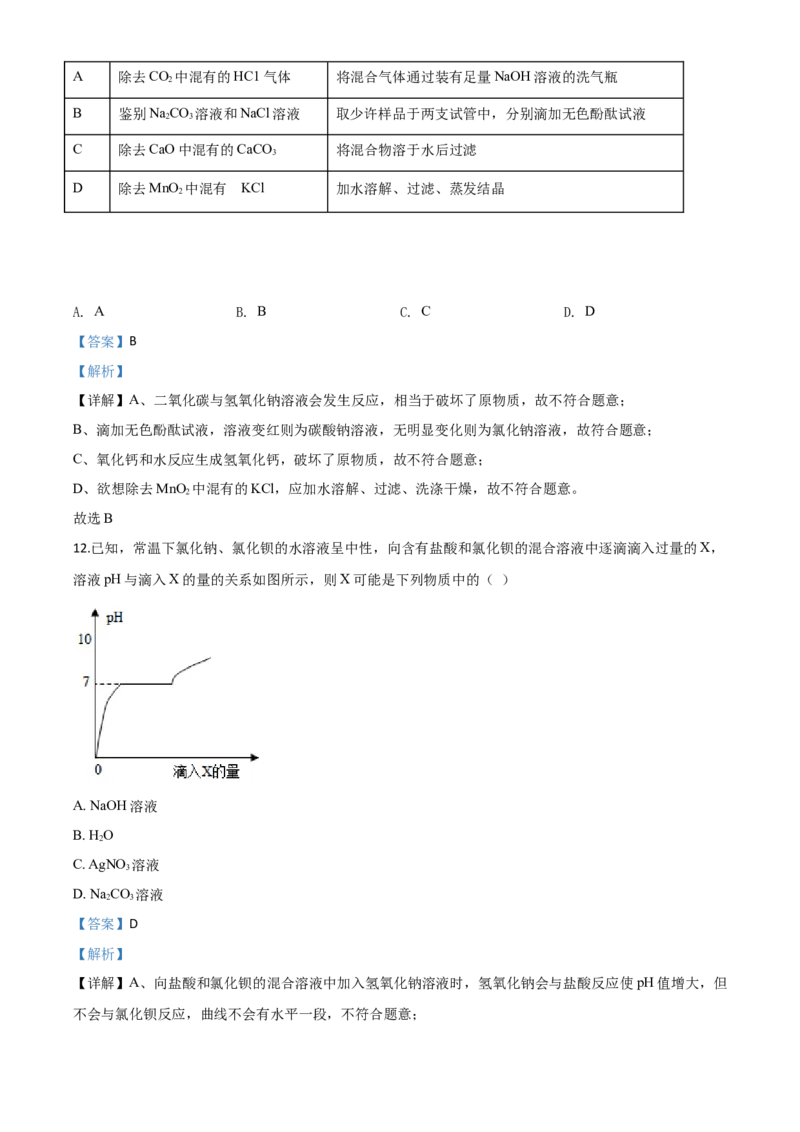
12.已知,常温下氯化钠、氯化钡的水溶液呈中性,向含有盐酸和氯化钡的混合溶液中逐滴滴入过量的X,
溶液pH与滴入X的量的关系如图所示,则X可能是下列物质中的( )
A. NaOH溶液
B. HO
2
C. AgNO 溶液
3
D. Na CO 溶液
2 3
【答案】D
【解析】
【详解】A、向盐酸和氯化钡的混合溶液中加入氢氧化钠溶液时,氢氧化钠会与盐酸反应使pH值增大,但
不会与氯化钡反应,曲线不会有水平一段,不符合题意;B、向盐酸和氯化钡的混合溶液中加入水时,溶液的酸性减弱,pH增大,但不可能等于7、大于7,不符
合题意;
C、向盐酸和氯化钡的混合溶液中加入AgNO 溶液时,盐酸能与硝酸银反应生成氯化银沉淀和硝酸,氯化
3
钡能与硝酸银反应生成氯化银沉淀和硝酸钡,反应后溶液仍显酸性,pH不可能等于7、大于7,不符合题
意;
的
D、向盐酸和氯化钡 混合溶液中加入纯碱溶液时,碳酸钠先和盐酸反应生成氯化钠和水,随着反应的进
行溶液的酸性减弱,pH升高,当恰好完全反应时溶液显中性;继续加入碳酸钠时,碳酸钠和氯化钡反应
生成碳酸钡沉淀和显中性的氯化钠,在碳酸钠和氯化钡反应的过程中溶液的pH不变,当氯化钡完全反应
后,再加入碳酸钠时,溶液的pH又升高,符合题意。故选D。
13.下列各组离子在pH=13的环境中能形成无色透明溶液的一组( )
A. H+、Na+、C1-、NO
B. Na+、Mg2+、C1-、NO
C. Cu2+、K+、SO 、Cl-
D. Ba2+、Na+、SO 、Cl-
【答案】A
【解析】
【分析】
pH为13的水溶液显碱性,水溶液中含有大量的OH-;溶液呈无色透明,不能含有明显有颜色的铜离子、
铁离子和亚铁离子等。
【详解】A、这四种离子在pH=13的环境中能形成无色透明溶液,符合题意;
B、Mg2+和溶液中的OH-结合生成氢氧化镁沉淀,不能形成无色透明的溶液,不符合题意;
C、Cu2+显蓝色且Cu2+和溶液中的OH-结合生成氢氧化铜沉淀,不能形成无色透明的溶液,不符合题意;
D、Ba2+和SO 2-结合生成白色沉淀,不能形成无色透明的溶液,不符合题意。故选A。
4
14.某NaCl样品中可能混有CuCl 、MgCl 、BaCl 中的一种或几种物质。取该样品11.7g溶于适量水中,得
2 2 2
到无色溶液,然后向其中加入足量的硝酸银溶液,得到30.7g白色沉淀,则该样品组成的下列推断中,正
确的是( )
A. 一定有MgCl ,可能有CuCl
2 2
B. 一定有MgCl ,没有BaCl
2 2
C. 一定有MgCl ,可能有BaCl
2 2D. 一定有MgCl 、BaC1
2 2
【答案】C
【解析】
【分析】
样品溶于水得无色溶液,证明氯化钙样品中一定不含CuCl ,因为氯化铜溶液为蓝色。
2
【详解】纯净的11.7g氯化钠与足量的硝酸银溶液反应生成的沉淀质量是x,
x=28.7g;
纯净的11.7g氯化镁与足量的硝酸银溶液反应生成的沉淀质量是y,
y=35.3g;
纯净的11.7g氯化钡与足量的硝酸银溶液反应生成的沉淀质量是z,
z=16.1g;
因为氯化钠生成的沉淀量小于30.7,所以另一种物质的生成的沉淀量要大于30.7,即该混合物中一定含有
氯化镁,可能含有氯化钡。
故选C。
二、填空題(本大題4个小题共20分,将正确答案直接填写在答题卡的相应位置上)
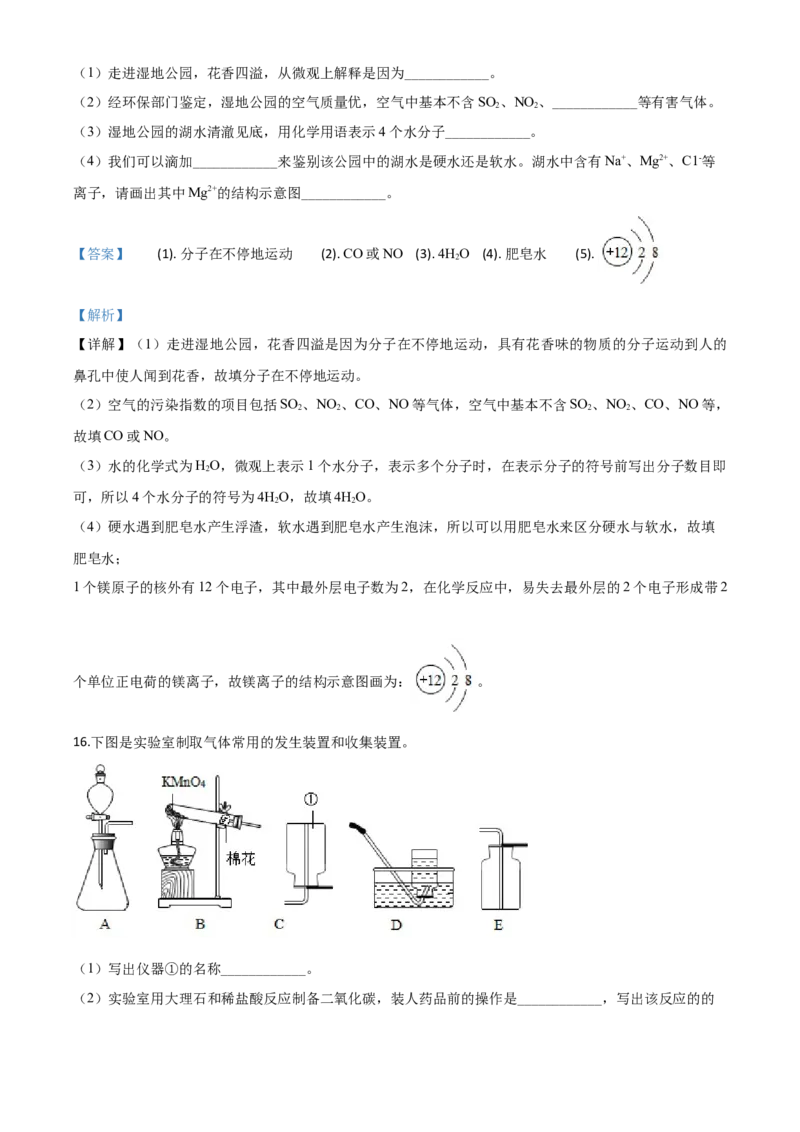
15.眉山市岷江河畔的东坡湿地公园,环境优美,是市民休闲的场所。请用所学的化学知识回答下列问题:(1)走进湿地公园,花香四溢,从微观上解释是因为____________。
(2)经环保部门鉴定,湿地公园的空气质量优,空气中基本不含SO 、NO 、____________等有害气体。
2 2
(3)湿地公园的湖水清澈见底,用化学用语表示4个水分子____________。
(4)我们可以滴加____________来鉴别该公园中的湖水是硬水还是软水。湖水中含有Na+、Mg2+、C1-等
离子,请画出其中Mg2+的结构示意图____________。
【答案】 (1). 分子在不停地运动 (2). CO或NO (3). 4HO (4). 肥皂水 (5).
2
【解析】
【详解】(1)走进湿地公园,花香四溢是因为分子在不停地运动,具有花香味的物质的分子运动到人的
鼻孔中使人闻到花香,故填分子在不停地运动。
(2)空气的污染指数的项目包括SO 、NO 、CO、NO等气体,空气中基本不含SO 、NO 、CO、NO等,
2 2 2 2
故填CO或NO。
(3)水的化学式为HO,微观上表示1个水分子,表示多个分子时,在表示分子的符号前写出分子数目即
2
可,所以4个水分子的符号为4HO,故填4HO。
2 2
(4)硬水遇到肥皂水产生浮渣,软水遇到肥皂水产生泡沫,所以可以用肥皂水来区分硬水与软水,故填
肥皂水;
1个镁原子的核外有12个电子,其中最外层电子数为2,在化学反应中,易失去最外层的2个电子形成带2
个单位正电荷的镁离子,故镁离子的结构示意图画为: 。
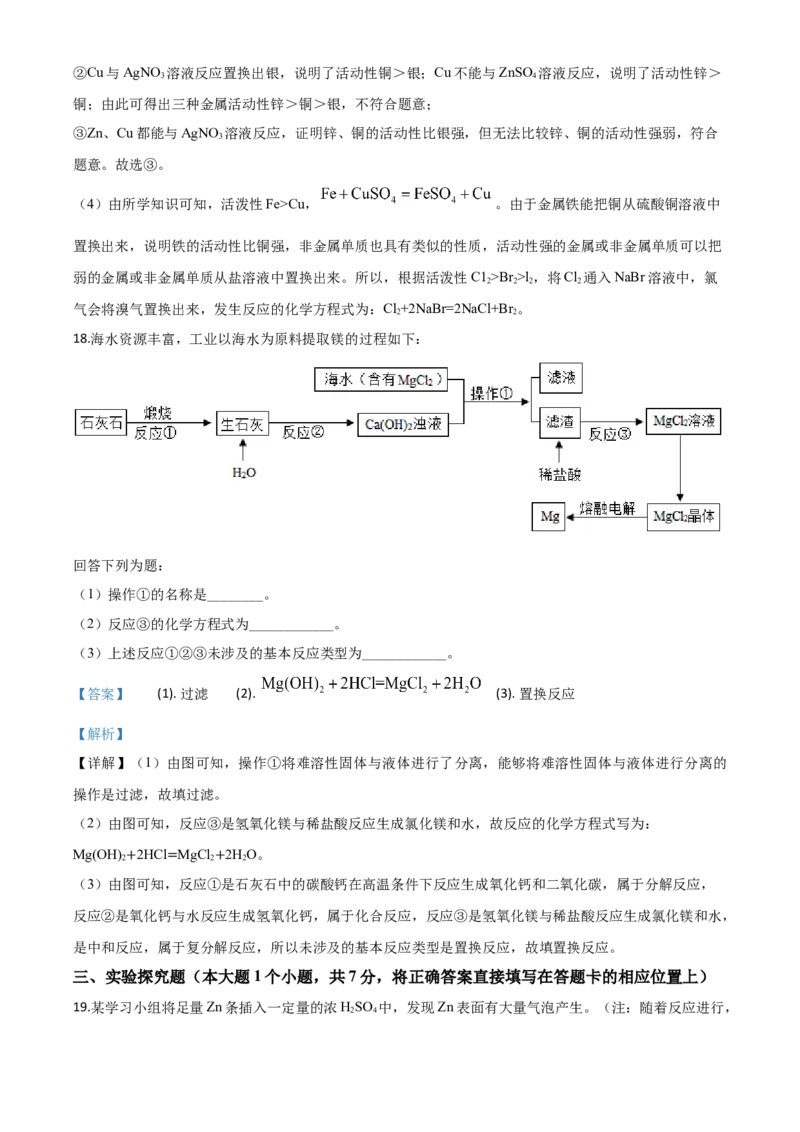
16.下图是实验室制取气体常用的发生装置和收集装置。
(1)写出仪器①的名称____________。
(2)实验室用大理石和稀盐酸反应制备二氧化碳,装人药品前的操作是____________,写出该反应的的化学方程式____________。
(3)B装置中棉花的作用____________。
(4)已知:实验室可用铜和硝酸的稀溶液反应制取一氧化氮(NO),NO气体难溶于水,在空气中容易
发生如下反应: ,请选用上述装置制取(发生并收集)NO___________。
【答案】 (1). 集气瓶 (2). 检查装置气密性 (3). (4).
防止高锰酸钾粉末阻塞导气管 (5). A、D
【解析】
【详解】(1)仪器①是集气瓶。
(2)实验室用大理石和稀盐酸反应制备二氧化碳,装入药品前要先检查装置的气密性,碳酸钙和盐酸反
应生成氯化钙、水和二氧化碳,该反应的的化学方程式为CaCO +2HCl═CaCl +H O+CO↑。
3 2 2 2
(3)B装置中棉花起到防止高锰酸钾的粉末堵塞导管的作用。
(4)实验室可用铜和硝酸的稀溶液反应制取一氧化氮(NO),是固液常温型反应,故发生装置为A,NO
气体难溶于水,在空气中容易和氧气反应,故只能采用排水法收集,故收集装置为D。
17.金属制品与我们的日常生活密不可分。
(1)有铝、锌、铜三种金属,其中不能与稀硫酸发生反应的是__________。
(2)铝的化学性质比较活泼,但铝制品具有很好的抗腐蚀性能,其原因是铝表面容易形成__________。
(3)为验证Zn、Cu、Ag三种金属的活动性强弱,某同学选用如下试剂组进行验证,其中不合理的一组是
__________(用序号①②③填空)
①Zn、CuSO 溶液、Ag ②ZnSO 溶液、Cu、AgNO 溶液 ③Zn、Cu、AgNO 溶液
4 4 3 3
(4)由所学知识可知,活泼性Fe>Cu, 。非金属与金属类似,活泼性
C1 >Br >l,请写出将Cl 通入NaBr溶液中发生反应的化学方程式____________。
2 2 2 2
【答案】 (1). Cu或铜 (2). 致密氧化膜 (3). ③ (4).
【解析】
【详解】(1)根据三种金属的活动性由强到弱为铝>锌>(氢)>铜可知,铜位于H之后不能与稀硫酸发生
置换反应。
(2)铝的化学性质比较活泼,但铝制品却具有很好的抗腐蚀性能,原因是铝在通常情况下能和空气中的
氧气反应生成致密氧化膜,对内部的铝起到保护作用;
(3)①Zn与CuSO 溶液反应置换出铜,说明了活动性锌>铜;Ag不能与硫酸铜溶液反应,说明了活动
4
性铜>银;由此可得出三种金属活动性锌>铜>银,不符合题意;②Cu与AgNO 溶液反应置换出银,说明了活动性铜>银;Cu不能与ZnSO 溶液反应,说明了活动性锌>
3 4
铜;由此可得出三种金属活动性锌>铜>银,不符合题意;
③Zn、Cu都能与AgNO 溶液反应,证明锌、铜的活动性比银强,但无法比较锌、铜的活动性强弱,符合
3
题意。故选③。
(4)由所学知识可知,活泼性Fe>Cu, 。由于金属铁能把铜从硫酸铜溶液中
置换出来,说明铁的活动性比铜强,非金属单质也具有类似的性质,活动性强的金属或非金属单质可以把
弱的金属或非金属单质从盐溶液中置换出来。所以,根据活泼性C1 >Br >l,将Cl 通入NaBr溶液中,氯
2 2 2 2
气会将溴气置换出来,发生反应的化学方程式为:Cl+2NaBr=2NaCl+Br 。
2 2
18.海水资源丰富,工业以海水为原料提取镁的过程如下:
回答下列为题:
(1)操作①的名称是________。
(2)反应③的化学方程式为____________。
(3)上述反应①②③未涉及的基本反应类型为____________。
【答案】 (1). 过滤 (2). (3). 置换反应
【解析】
【详解】(1)由图可知,操作①将难溶性固体与液体进行了分离,能够将难溶性固体与液体进行分离的
操作是过滤,故填过滤。
(2)由图可知,反应③是氢氧化镁与稀盐酸反应生成氯化镁和水,故反应的化学方程式写为:
Mg(OH) 2HCl MgCl 2HO。
2 2 2
(3)由图+可知,=反应①+是石灰石中的碳酸钙在高温条件下反应生成氧化钙和二氧化碳,属于分解反应,
反应②是氧化钙与水反应生成氢氧化钙,属于化合反应,反应③是氢氧化镁与稀盐酸反应生成氯化镁和水,
是中和反应,属于复分解反应,所以未涉及的基本反应类型是置换反应,故填置换反应。
三、实验探究题(本大题1个小题,共7分,将正确答案直接填写在答题卡的相应位置上)
19.某学习小组将足量Zn条插入一定量的浓HSO 中,发现Zn表面有大量气泡产生。(注:随着反应进行,
2 4硫酸浓度逐渐变小)
【提出问题】气体的成分是什么?
【猜想假设】猜想一:只有SO
2
猜想二:只有H
2
猜想三:____________。
【查阅资料】(Ⅰ)SO 可以使品红溶液褪色
2
(Ⅱ)SO 可以和碱性溶液反应
2
(Ⅲ)
【实验探究】用下图装置验证猜想(部分夹持仪器省略)
【方案设计】
主要实验步骤 主要现象 解释或结论
①打开止水夹,先通人一段时间N
2
B装置处品红溶液褪色
②关闭止水夹,将足量Zn条下放,
猜想三成立
浸入浓硫酸中,点燃E装置处酒精灯
E装置处_______
③结束实验
【表达交流】
(1)在步骤①中,通入N 的目的是:___________。
2
(2)请你设计一个实验,用化学方法证明E装置中CuO未完全反应。
实验步骤 实验现象 结论
_______ _______ CuO未完全反应
【反思拓展】
(1)请你根据上述实验探究,补充Zn与浓硫酸反应的化学方程式Zn+ 2HSO =ZnSO +SO↑+_______
2 4 4 2(2)已知A1与H 一样,在加热条件下能与CuO发生化学反应,请写出该反应的化学方程式_______。
2
【答案】 (1). 有SO ,也有H (2). 黑色固体变红,管口有水珠出现 (3). 排除装置中的空气,防止
2 2
爆炸 (4). 取E中少许固体于试管中,滴加稀盐酸(稀硫酸) (5). 溶液由无色变蓝色 (6). 2HO
2
(7).
【解析】
【详解】[猜想假设]根据猜想一:只有SO 和猜想二:只有H 可知,猜想三:SO 和H 都有;
2 2 2 2
[方案设计]氢气和氧化铜反应生成红色铜和水,所以E装置处得现象为:黑色固体变红,管口有水珠出现;
[表达交流](1)混有空气的氢气加热可能发生爆炸,所以在步骤①中,通入N 的目的是:排除装置中的
2
空气,防止爆炸;
(2)铜与硫酸不反应,而氧化铜和硫酸或盐酸反应生成蓝色硫酸铜溶液,实验方案如下:取E中少许固
体于试管中,滴加稀盐酸(稀硫酸),溶液由无色变蓝色,说明剩余固体中有氧化铜;
[反思拓展](1)根据上述实验探究可知,Zn与浓硫酸反应生成硫酸锌、二氧化硫和水,反应的化学方程
式为Zn+2H SO =ZnSO +SO↑+2H O;
2 4 4 2 2
(2)氢气和氧化铜反应生成红色铜和水,所以铝和氧化铜反应生成铜和氧化铝,反应的化学方程为:
。
四、计算题(本大題1个小題,共5分,将正确答案直接填写在答题卡的相应位置上)
20.实验室为了测定过氧化氢溶液的质量分数,称取85.00gHO 溶液和2.0gMnO 混合放入质量为50.00g的
2 2 2
烧杯中,用电子天平称得烧杯的总质量随时间变化如下表所示:
时间/S 15 30 45 60 75 90
烧杯总质量/g 136.50 136.10 135.70 135.50 135.40 135.40
(1)产生O 的质量为 g。
2
(2)过氧化氢溶液中溶质的质量分数为?(写出计算过程)
【答案】(1)16.0;(2)4%
【解析】
【详解】(1)过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应前后质量差即为反应生成氧气质
量,产生O 的质量为:85.00g+2.00g+50.00g-135.40g=1.60g;
2(2)设过氧化氢溶液中溶质的质量为 ,
解得 =3.40g,
过氧化氢溶液中溶质质量分数 为:
答:过氧化氢溶液中溶质质量分数为4%。本试卷的题干、答案和解析均由组卷网(http://zujuan.xkw.com)专业教师团队编校出品。
登录组卷网可对本试卷进行单题组卷、细目表分析、布置作业、举一反三等操作。
试卷地址:在组卷网浏览本卷
组卷网是学科网旗下的在线题库平台,覆盖小初高全学段全学科、超过900万精品解析试题。
关注组卷网服务号,可使用移动教学助手功能(布置作业、线上考试、加入错题本、错题训练)。
学科网长期征集全国最新统考试卷、名校试卷、原创题,赢取丰厚稿酬,欢迎合作。
钱老师 QQ:537008204 曹老师 QQ:713000635