文档内容
让更多的孩子得到更好的教育
中考总复习:混合物的去杂分离提纯物质制备解题技巧(提高)
撰稿:李伟 审稿:熊亚军
【考纲要求】
1.了解混合物提纯的基本原理,能根据物质的物理、化学性质确定分离方法。
2.掌握过滤、蒸发等方法对混合物进行分离;了解粗盐提纯等固体混合物分离的方法和过程。
3.了解气体混合物的净化、干燥、收集、尾气处理的流程。
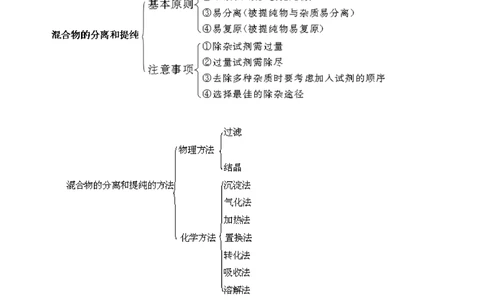
【知识网络】
【考点梳理】
考点一、物质分离和提纯的方法(高清课堂《物质的检验、分离和提纯》一)
1.物理方法:
方法 适用范围或原理 举例
①固体与液体混合物的分离 粗盐的提纯
过滤法
②可溶性固体与不溶性固体混合物的分离
物
理 ①分离溶质与溶剂 从含有 HCl 的 NaCl 溶液中
方 结 蒸发 ②除去易挥发的杂质 分离出固体NaCl
晶
法
法 降低温度 可溶性固体溶质溶解度受温度影响变化大 分离NaCl与KNO 3 的混合物
小不同
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共10页让更多的孩子得到更好的教育
(1)过滤:把不溶性的固体与液体分开的一种方法叫过滤。
①过滤器的准备(如图甲):取一张圆形滤纸,对折两次,然后打开,使滤纸成为圆锥形(一边是一层滤纸,
另一边是三层滤纸),放入漏斗内,使之紧帖漏斗壁,用少量水润湿滤纸使滤纸和漏斗壁之间不要留有气
泡。
甲 乙
②安装过滤器(如图乙):使漏斗的下端管口紧靠烧杯内壁。
③过滤操作:将浑浊的液体混合均匀后,沿玻璃棒慢慢倒入漏斗内进行过滤。
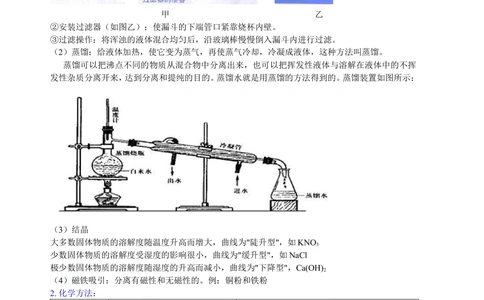
(2)蒸馏:给液体加热,使它变为蒸气,再使蒸气冷却,冷凝成液体,这种方法叫蒸馏。
蒸馏可以把沸点不同的物质从混合物中分离出来,也可以把挥发性液体与溶解在液体中的不挥
发性杂质分离开来,达到分离和提纯的目的。蒸馏水就是用蒸馏的方法得到的。蒸馏装置如图所示:
(3)结晶
大多数固体物质的溶解度随温度升高而增大,曲线为"陡升型",如KNO
3
少数固体物质的溶解度受湿度的影响很小,曲线为"缓升型",如NaCl
极少数固体物质的溶解度随湿度的升高而减小,曲线为"下降型",Ca(OH)
2
(4)磁铁吸引:分离有磁性和无磁性的。例:铜粉和铁粉
2. 化学方法:
方法 适用范围或原理 举例
除 NaSO 中 NaCO ,可加适量稀 HSO :
化气法 与杂质反应生成气体而除去 2 4 2 3 2 4
NaCO+ H SO =NaSO + CO↑+ H O
2 3 2 4 2 4 2 2
除去NaCl中的NaSO ,可加适量的 BaCl :
沉淀法 将杂质转化为沉淀过滤除去 2 4 2
NaSO + BaCl ==BaSO ↓+2NaCl
化 2 4 2 4
学 置换法 将杂质通过置换反应而除去 除FeSO 4 中的CuSO 4 ,可加过量的铁粉,再过
方 滤:CuSO +Fe==Cu+Fe SO
4 4
法 除C粉中的CuO粉,可加适量稀硫酸,再过滤:
溶解法 将杂质溶于某种试剂而除去
CuO+ H SO ==CuSO + H O
2 4 4 2
杂质受热易分解,通过加热将杂 除CaO中的CaCO 3 可加热:
加热法
质除去 CaCO CaO+ CO ↑
3 2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共10页让更多的孩子得到更好的教育
将杂质通过化学反应转化为主 除CO 2 中的CO,可将气体通过灼热的CuO:
转化法
要成分 CO+CuO Cu+CO
2
【要点诠释】
1. 过滤的操作要点是“一贴,二低,三靠”:
一贴:制作过滤器时,滤纸要紧贴漏斗内壁(中间不要留有气泡,否则会影响过滤速度)。
二低:(1)滤纸边缘低于漏斗边缘;(2)过滤器中液面低于滤纸边缘(否则,液体就会从滤纸和漏斗壁之间
流下,达不到过滤的目的)。
三靠:(1)盛待过滤液的烧杯口要紧靠玻璃棒,使液体沿玻璃棒流入过滤器;(2)玻璃棒下端轻轻斜靠在
三层滤纸的一边,以免弄破滤纸;(3)漏斗下端要紧靠在下面烧杯的内壁,使滤液沿烧杯壁流下(否则滤
液会向四周飞溅,而且影响过滤的速度)。
2.粗盐的提纯
(1)粗盐是含有较多杂质的氯化钠晶体。通过晾晒海水或煮盐井水、盐湖水而得到的粗盐中含有较多的可
溶性杂质(氯化镁、氯化钙、硫酸镁等)和不溶性杂质(泥沙等)。可以通过溶解、过滤、蒸发、结晶等步骤来
制取精盐。
(2)粗盐提纯的步骤:
①溶解:用托盘天平称取5.0g粗盐,用量筒量取10mL水,用药匙将粗盐逐渐加入盛有10mL水的烧杯里,
边加边用玻璃棒搅拌,加到不再溶解为止。
②过滤:过滤食盐水。
③蒸发:将澄清的滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多的固体时停止加热,利用
蒸发皿的余热使滤液蒸干。
④计算产率:用玻璃棒把氯化钠固体转移到纸上,称量,计算产率。
(3)粗盐提纯过程中玻璃棒的作用:
(1)溶解时:用玻璃棒搅拌,加快粗盐的溶解速率。
(2)过滤时;玻璃棒起引流作用,防止液体外洒。
(3)蒸发时:用玻璃棒搅拌液体,防止液体局部温度过高,造成液滴飞溅。
(4)转移时;玻璃棒起到了转移固体的作用。
考点二、气体的净化与干燥
1.气体净化的几种方法
(1)吸收法:用吸收剂将杂质气体吸收除去。如,除去CO中混有的少量CO,可先用浓NaOH溶液吸收
2
CO,再用浓硫酸等干燥剂除去水蒸气。
2
常见气体吸收剂见下表:
吸收剂 吸收的气体杂质 吸收剂 吸收的气体杂质
水 可溶性气体:HCl、NH 等 NaOH固体 CO、HCl、HO
3 2 2
无水CuSO HO 碱石灰 CO、HCl、HO
4 2 2 2
灼热的铜网 O NaOH溶液 CO、HCl
2 2
灼热的CuO H、CO 浓硫酸 HO
2 2
(2)转化法:通过化学反应,将杂质气体转化为所要得到的气体。如,除去CO 中的少量CO,可将混合气
2
体通过足量的灼热CuO,CO + CuO Cu + CO 。
2
2.气体的干燥
气体的干燥是通过干燥剂来实现的,选择干燥要根据气体的性质,一般原则是:酸性干燥剂不能用来
干燥碱性气体,碱性干燥剂不能用来干燥酸性气体,干燥装置由干燥剂状态决定。
(1)常见的干燥剂
干燥剂 干燥
可干燥气体 不可干燥气体
名称或化学式 酸碱性 状态 装置
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共10页让更多的孩子得到更好的教育
H、N、O、CO、
浓HSO 酸性 液态 2 2 2 2 NH A
2 4 HCl、CH、CO等 3
4
固体NaOH H、O、N、CH、
碱性 固态 2 2 2 4 CO、SO 、HCl B或C
生石灰 CO、NH 等 2 2
3
无水CaCl 中性 固态 除NH 外所有气体 NH B或C
2 3 3
(2)常用干燥装置如下:
【要点诠释】
1.选择吸收装置时,要注意进、出气体导管的连接方法,若用“洗气瓶”,要注意“长进短出”,若用干燥管
要注意“大进小出”。先除去气体中含有的其他杂质,干燥除去水蒸气的操作放在最后。
2.多功能瓶(装置A):集气瓶、双孔塞和两支导气管的组合装置因其可以实现洗气、储气、测量气体体积
等多种功能,而被称为“多功能瓶”。
常用于除去气体中的某些气体杂质,选用能与杂质气体反应并且不产生新气体杂质的液体试剂(或
者直接利用吸水性,如浓硫酸干燥某些气体;或能产生待保留气体的液体试剂)。
【典型例题】
类型一、考查物质的分离、除杂和提纯
1. 要除去下列四种物质中的少量杂质(括号内的物质为杂质)
甲:CaCO (NaCO)乙:NaOH(NaCO) 丙:KCl(KCO) 丁:炭粉(CuO)
3 2 3 2 3 2 3
可选用的试剂及操作方法有:①加适量盐酸,搅拌,过滤;②加适量水,搅拌,过滤;③加适量盐酸,蒸发;
④溶解,加适量石灰水,过滤,蒸发。下列组合正确的是( )
A.甲-②,乙-④ B.乙-③,丙-①
C.丙-①,丁-② D.丙-③,丁-①
【思路点拨】分析杂质和物质的性质,然后选择适当的试剂只与杂质反应,不与主要物质反应,不会生成新
的杂质。
【答案】 AD
【解析】甲:碳酸钙难溶于水,加水后过滤,可以将碳酸钙分离,选择②;乙:加水溶解后,加适量石灰水,会
将碳酸钠转化为氢氧化钠和碳酸钙沉淀,过滤后蒸发会得到氢氧化钠,选择④;丙:混合物中加盐酸反应
后只剩氯化钾,蒸发就可以得到氯化钾,选择③;丁:混合物中加入盐酸会将氧化铜溶解,过滤后就可以得
到炭粉,选择①。
【总结升华】解决除杂问题时,抓住除杂质的必需条件:加入的试剂只与杂质反应,反应后不能引入新的杂
质。
2. (2012岳阳)下表除去杂质的方法中,正确的是( )
选项 物质(括号内为杂质) 除去杂质的方法
A Cu(NO ) 溶液(AgNO) 加过量铜粉,过滤
3 2 3
B KCl溶液(CaCl ) 加适量NaCO 溶液,过滤
2 2 3
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共10页让更多的孩子得到更好的教育
C Fe(Zn) 加足量稀盐酸,过滤
D CO(CO) 通过灼热的氧化铜粉末
2
【思路点拨】除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后
不能引入新的难以分离的杂质。
【答案】 A
【解析】A中AgNO 能与过量铜粉的发生置换反应生成硝酸铜和银,再过滤除去不溶物,能除去杂质且没
3
有引入新的杂质,符合除杂原则;B中CaCl 能与适量NaCO 溶液反应生成碳酸钙沉淀和氯化钠,氯化钾
2 2 3
不与NaCO 溶液反应,能除去杂质但没有引入新的杂质氯化钠,不符合除杂原则;C中锌、铁均能与稀盐
2 3
酸反应,选用稀盐酸不但能把杂质除去,也会把原物质除去,不符合除杂原则; D中CO能与灼热的氧化
铜粉末反应生成铜和二氧化碳,二氧化碳不能与氧化铜反应,通过灼热的氧化铜粉末反而会把原物质除
去,不符合除杂原则。
【总结升华】记住常用的物质分离、除杂的方法,根据物质的性质选择合适的反应。
3. 要除去下列物质中混有的少量杂质(括号内为杂质),所用的试剂和操作都正确的是( )
A.CaCl 固体(CaCO )加足量稀硫酸、蒸发、结晶
2 3
B.NaCl固体(NaCO)加足量稀盐酸、蒸发、结晶
2 3
C.Fe粉(Cu)加足量稀盐酸、过滤、洗涤、干燥
D.MnO 固体(KCl)加足量水溶解、过滤、洗涤、干燥
2
【答案】 BD
【解析】A中碳酸钙与硫酸反应生成微溶的硫酸钙、水、二氧化碳,生成的硫酸钙是新杂质;B中碳酸钠与
盐酸反应生成氯化钠、水、二氧化碳,无新杂质产生,蒸发后可得纯净的氯化钠;C中铁和盐酸反应而被除
去,但杂质铜却和盐酸不反应,不能被除去;D中二氧化锰不溶于水,氯化钾能溶于水,加足量水溶解后过
滤,可得滤渣二氧化锰,再洗涤、干燥,可得纯净的二氧化锰。
【总结升华】除杂是基本的化学实验技能之一,其关键要求是:①要把杂质除去,②需保留的物质不能被破
坏,③不能添新的杂质。
4.下列除去杂质的方法正确的是( )
A.用足量的稀硫酸除去铁粉中少量的铜粉
B.用适量的KCO 溶液除去NaCl溶液中少量的CaCl
2 2 2
C.用足量的NaOH溶液除去CO气体中少量的CO
2
D.用适量的稀盐酸除去NaOH溶液中的少量的NaCO
2 3
【思路点拨】A根据金属活动性顺序进行分析; B根据碳酸钾会与氯化钙生成氯化钾进行分析;C根据酸
性气体会与碱性氧化物反应; D根据盐酸会与两者反应进行分析。
【答案】 C
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共10页让更多的孩子得到更好的教育
【解析】A中在混合物中加入硫酸,会与铁反应将铁除去,而不会与铜反应,故A错误;B中碳酸钾会与氯
化钙反应将氯化钙除去,但是生成的氯化钾对于氯化钠也是杂质,故B错误; C中混合气通过氢氧化钠
后,会与氢氧化钠反应而将二氧化碳除去,剩下一氧化碳,故C正确; D中盐酸既会与氢氧化钠反应,也
会与碳酸钠反应,除去杂质也会除去主要物质,故D错误。
【总结升华】把杂质除掉,原物质的质量不能减少,可以增加,不能带入新的杂质,操作越简便越好,把杂
质转化为和原物质状态不同的物质,便于分离。
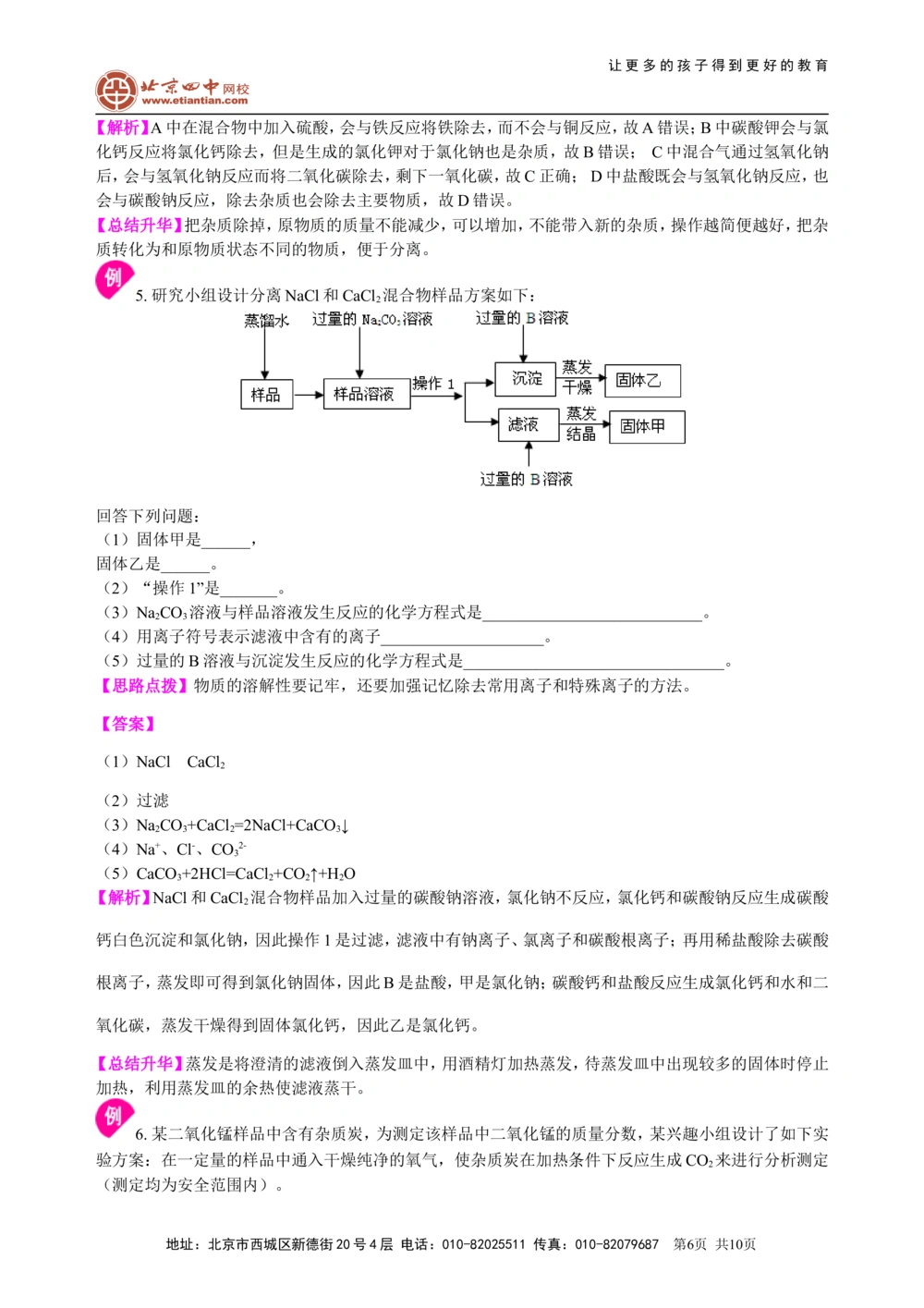
5. 研究小组设计分离NaCl和CaCl 混合物样品方案如下:
2
回答下列问题:
(1)固体甲是______,
固体乙是______。
(2)“操作1”是_______。
(3)NaCO 溶液与样品溶液发生反应的化学方程式是___________________________。
2 3
(4)用离子符号表示滤液中含有的离子____________________。
(5)过量的B溶液与沉淀发生反应的化学方程式是________________________________。
【思路点拨】物质的溶解性要记牢,还要加强记忆除去常用离子和特殊离子的方法。
【答案】
(1)NaCl CaCl
2
(2)过滤
(3)NaCO+CaCl =2NaCl+CaCO ↓
2 3 2 3
(4)Na+、Cl-、CO2-
3
(5)CaCO +2HCl=CaCl +CO ↑+H O
3 2 2 2
【解析】NaCl和CaCl 混合物样品加入过量的碳酸钠溶液,氯化钠不反应,氯化钙和碳酸钠反应生成碳酸
2
钙白色沉淀和氯化钠,因此操作1是过滤,滤液中有钠离子、氯离子和碳酸根离子;再用稀盐酸除去碳酸
根离子,蒸发即可得到氯化钠固体,因此B是盐酸,甲是氯化钠;碳酸钙和盐酸反应生成氯化钙和水和二
氧化碳,蒸发干燥得到固体氯化钙,因此乙是氯化钙。
【总结升华】蒸发是将澄清的滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多的固体时停止
加热,利用蒸发皿的余热使滤液蒸干。
6. 某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实
验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO 来进行分析测定
2
(测定均为安全范围内)。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共10页让更多的孩子得到更好的教育
(1)仪器①的名称是_________,如果该实验选择图(一)装置来制取氧气,则该装置中发生反应的方程式
为_________________________________。
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从___
(填“a”或“b”,下同)端通入;若在烧瓶内装入浓硫酸进行干燥气体,气体应从___
端通入。
(3)为验证图(三)中装置②己将CO 吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图
2
(四)装置中加入的试剂为____
(填字母)。
A.NaOH溶液 B.澄清石灰水 C.浓硫酸
(4)图(三)用干燥纯净的O 与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰(即氧化
2
钙和氢氧化钠固体混合物),其作用是___________________________________。
(5)称取5.0g二氧化锰样品进行实验,图㈢中装置②反应前后的质量差为1.1g,则样品中二氧化锰的质量
分数为__________。
(填计算结果)。
【思路点拨】(2)根据实验目的和气体的密度大小选择的选择;(3)根据实验目的,分析装置中应该盛放的
药品;(4)根据实验目的,分析装置中指定仪器的作用;(5)利用化学方程式,由生成气体的质量计算参加
反应的物质的质量。
【答案】 (1)长颈漏斗 2HO 2HO+O↑
2 2 2 2
(2)a b
(3)B
(4)防止空气中的二氧化碳进入氢氧化钠溶液,导致测定结果偏高
(5)94%
【解析】(1)仪器①长颈漏斗,图(一)装置可用于反应物是固体和液体反应,反应在常温下进行的反应,
故可用过氧化氢在二氧化锰催化作用下分解生成氧气;(2)用图(二)装置收集气体时,注意短导管进气,
长导管出水,干燥气体时要长导管进气,短导管出气;(3)验证二氧化碳气体可用澄清的石灰水;(4)图
(三)中碱石灰的作用是吸收空气中的二氧化碳和水蒸气,以防止空气中的氢氧化钠和碱石灰进入到空气
中使试验测量结果不准;
(5)解:根据题意反应后生成二氧化碳的质量为1.1g,设生成1.1gCO2需碳的质量为x。
C+O CO
2 2
12 44
x 1.1g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共10页让更多的孩子得到更好的教育
x=0.3g
则样品中二氧化锰的质量分数为: ×100%=94%
【总结升华】解答好这类题目,要熟记常见气体的检验与除杂方法及理论依据,还有氧气、二氧化碳等气体
的相关知识,有时还需弄清图示信息,以及有关的注意事项等。
举一反三:
【变式1】下列实验方案中,正确的是( )
A. 用稀盐酸除去CaO中的少量CaCO
3
B. 用Ba(OH) 溶液检验露置在空气中的NaOH溶液是否变质
2
C. 用水溶解后过滤分离CaCl 和KCO的混合物
2 2 3
D. 用稀HSO 和Cu制备氢气
2 4
【答案】 B
【解析】氢氧化钠溶液在空气中会与空气中的二氧化碳反应而变质,生成了碳酸钠,因此用Ba(OH) 溶液
2
检验时会生成白色的碳酸钡沉淀。盐酸会与CaO和CaCO 均发生反应;CaCl 和KCO 在溶液中会发生反
3 2 2 3
应,生成碳酸钙沉淀;铜在金属活动性顺序中排在氢后面,因此不能与稀硫酸反应。
【变式2】拟用实验方法除去下列(1)~(4)中各物质中的少量杂质,限从A~D提供的试剂及操作方法中
进行选择,并将其序号填在相应的短线上。
A.加适量的稀盐酸,搅拌、蒸发、结晶
B.加适量的稀盐酸,搅拌、过滤、洗涤、沉淀
C.加适量的水,溶解、过滤、洗涤、沉淀
D.加适量的水,溶解、过滤、蒸发、沉淀
(1)碳酸钙中混有少量杂质碳酸钠________
;
(2)铜粉中混有少量杂质锌粉________
;
(3)氯化钠中混有少量杂质碳酸钠________
;
(4)氯化钾中混有少量杂质二氧化锰________
。
【答案】(1)C (2)B (3)A (4)D
【解析】(1)碳酸钙是不溶于水的物质,碳酸钠易溶于水,所以可以根据这两种物质的溶解性采用加水的
方法把碳酸钠除掉,加水后碳酸钠溶解在水中,通过过滤可以将其除掉,然后将得到的沉淀进行洗涤就可
以得到纯净得碳酸钙;(2)根据金属活动性顺序,排在氢前的锌可以与酸发生置换反应,而排在氢后的铜
不能与酸发生置换反应,根据这两种物质是否与酸发生置换反应可以采用加酸的方法,使锌参加反应,经
过滤得到铜,再进行洗涤即可得到纯净的铜;(3)碳酸钠可以与盐酸反应生成氯化钠,要将得到的氯化钠
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第8页 共10页让更多的孩子得到更好的教育
从溶液中析出,需把水蒸发掉,使氯化钠结晶析出;(4)氯化钾易溶于水,而二氧化锰不溶于水,所以可以
根据这两种物质的溶解性采用加水的方法,使氯化钾溶于水,经过过滤除掉二氧化锰,要将得到的氯化钾
从溶液中析出,需把水蒸发掉,使氯化钾结晶析出。
【变式3】下表给出了在20℃和100℃时A、B两种化合物在不同溶剂中的溶解度数据,请分析有关数据,
判断利用重结晶法从A、B的混合物中提纯A时,使用那种溶剂的回收率最高(已知混合物含A70g,含B
15g)( )
20℃时的溶解度(g) 100℃时的溶解度(g)
溶剂序号 A B A B
甲 5 15 75 25
乙 20 5 90 30
丙 15 1 70 10
丁 10 12 80 20
A.甲 B.乙 C.丙 D.丁
【答案】 A
【解析】结晶原理是某物质的溶解度随温度的升高而显著增加,当冷却该物质的热饱和溶液,就会有较多
量晶体从溶液中析出。用结晶法从A、B的混合物种提纯A时,A物质的溶解度曲线应为陡升型,且低温
时的溶解度尽可能较小,这样当温度降低时,析出的晶体不仅多,而且留在母液中的溶质的质量少;而B
物质的溶解度曲线为缓升型或下降型,这样少量的B物质在降温后也不易形成饱和溶液,从溶液中析出,
从而保证降温后析出的晶体都是A物质。根据题中所给的信息,混合物中含有 A物质70g,含B物质
15g,将它们溶于100g甲的溶剂,由100℃降到20℃时,可析出65g的A,而B恰好达到饱和,这样使A的
回收率最高。
【变式4】为了测定某石灰矿样的纯度(其中所含杂质不与酸反应)。某同学按如下流程进行实验:用盐酸
溶解矿样→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重量计算矿样的纯度,实验过
程中所取矿样的质量为10.0g。实验装置如下图所示:
则根据上述装置进行实验,下列情况会使实验结果产生偏差的是( )
①实验开始前A、B装置及导气管内残留少量空气;
②进人C装置的气体中还混有少量HCl气体;
③气体通过速度过快,CO 来不及被NaOH溶液全部吸收;
2
④实验结束时,系统内还残留有少量CO 气体。
2
A. ①②③④ B. ①②③ C. ①②④ D. ②③④
【答案】 A
【解析】①由于空气中含有二氧化碳气体也会被氢氧化钠溶液吸收,而使装置C的质量增大;②中混有的
HCl会和氢氧化钠溶液反应,而使装置C的质量增大;③④都是二氧化碳气体未完全被氢氧化钠溶液吸
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第9页 共10页让更多的孩子得到更好的教育
收,而使装置C的质量减小。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第10页 共10页