文档内容
厦门市 2025 届高三年级第三次质量检测
化学参考答案
说明:化学方程式或离子方程式中,化学式写错的不给分;化学式对而未配平或重要条件错
误扣1分,气体或沉淀符号未标扣1分,以上扣分不累计。
一、选择题(每小题4分,共40分)
题号 1 2 3 4 5 6 7 8 9 10
答案 B C D C D D C A D B
二、填空题(本题包括4个小题,共60分)
11.(16分)
(1)Fe2++2HCO−===FeCO ↓+CO ↑+H O (2分)
3 3 2 2
(2)2FeCO +H O +2H O===2Fe(OH) +2CO ↑ (2分)
3 2 2 2 3 2
(3)①> (1分)
②生成大颗粒的FeCO 沉淀易于分离;Fe3+水解生成的阳离子易与水分子形成氢键,
3
生成絮状沉淀,难以洗脱 (2分)
(4)①1022.7 (2分)
H Y2- (1分)
2
②减小 (1分)
③溶液呈酸性,N原子易与H+配位且—COO-易与H+结合,降低配位能力 (2分)
(5)b (1分)
(6)沉铁 (2分)
12.(15分)
(1)①CH CSNH +H O CH CONH +H S↑ (2分)
3 2 2 3 2 2
CH CSNH 水解产生⥫⥬H S速率可控,可减少H S溢出,提升实验安全性 (2分)
3 2 2 2
②形成配合物缓慢释放Bi3+;产生H+抑制H S电离降低S2-浓度 (2分)
2
(2)a (1分)
(3)直形冷凝管、温度计 (2分)
(4)硝酸酸化的AgNO 溶液 (1分)
3
(5)d (1分)
(6)①pH过高,Bi3+会发生水解;pH过低,会影响Bi3+与H Y2-反应程度 (2分)
24.18b×10-2
② (2分)
a
13.(15分)
(1)羟基、酯基 (2分)
(2)乙基为推电子基,可增大N上的电子云密度,使其更容易与H+形成配位键 (2分)
Et N具有碱性,能与取代反应生成的酸结合,使平衡正向移动 (2分)
3
(3) (2分)
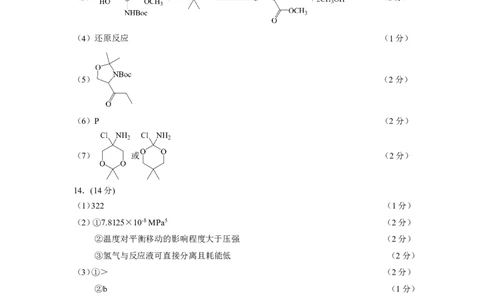
(4)还原反应 (1分)
(5) (2分)
(6)P (2分)
(7) 或 (2分)
14.(14分)
(1)322 (1分)
(2)①7.8125×10-8MPa5 (2分)
②温度对平衡移动的影响程度大于压强 (2分)
③氢气与反应液可直接分离且耗能低 (2分)
(3)①> (2分)
②b (1分)
生成C H1 →C H 活化能小于C H1 →C H ,但生成速率C H 远大于生成C H ,
10 8 10 12 10 8 10 8 10 8 10 12
说明C H 继续转化为C H (2分)
10 12 10 8
③34.7 (2分)