文档内容
海淀区 2024—2025 学年第一学期期末练习
高三化学
本试卷共8页,100分。考试时长90分钟。考生务必将答案答在答题纸上,在试卷上作答无
效。考试结束后,将本试卷和答题纸一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Ti 48 Mn 55 Fe 56 Au 197
第一部分
本部分共14题,每题3分,共42分。在下列各题的四个选项中,选出最符合题目要求的一项。
1. 40K是钾元素的一种较稳定的核素,其衰变后产生40Ar。40K的半衰期(放射性元素的原子核有
半数发生衰变所需的时间)长达13亿年,故常用于古老岩石的年代测定。下列说法不正确的是
4 4 4
A.40K的原子核内有21个中子 B.39K和40K均易失去一个电子
C.可通过质谱法区分39K和40K D.40K衰变为40Ar的过程属于化学变化
2.下列化学用语或图示表达正确的是
z
A.2p 的电子云图为 B.CO 的电子式为:O:C:O:
z y 2
x
高三年级(化学) 第1页(共8页)
:
:
:
:
:
:
2025. 01
C.乙炔的结构简式为HC=CH D.O2-的离子结构示意图为 +8 2 6
2 2
3.下列说法正确的是
A.淀粉能与银氨溶液发生银镜反应 B.两个氨基酸分子缩合最多生成一个水分子
C.脂肪酸可与甘油发生酯化反应 D.葡萄糖、蛋白质、油脂均可发生水解反应
4.下列物质性质不能由元素周期律推测的是
4 4
A.热稳定性:NH >PH B.沸点:HO>HF
3 3 2
C.氧化性:Br >I D.碱性:NaOH>Mg(OH)
2 2 2
5.下列实验中,不能达到实验目的的是
4 4
A.由FeCl·6HO D. 验证氨易溶于水且
3 2 B.实验室制氯气 C. 萃取碘水中的碘单质
制备无水FeCl 溶液呈碱性
3
NH (cid:8831)(cid:11260)(cid:18084) NH NH (cid:8831)(cid:11260)(cid:18084)(cid:8831)(cid:11260)(cid:18084) NH (cid:8831)(cid:11260)(cid:18084)
3 3 3 3
(cid:8544) (cid:8544) (cid:8544) (cid:8544)
CCl CCl CCl CCl
4 4 4 4
MnO MnOMnO MnO
2 2 2 2
(cid:9248)(cid:7221)(cid:18054)(cid:18058) (cid:9248)(cid:7221)(cid:18054)(cid:9248)(cid:18058)(cid:7221)(cid:18054)(cid:18058) (cid:9248)(cid:7221)(cid:18054)(cid:18058)
(cid:9186)(cid:8926)(cid:11184)(cid:8544) (cid:9186)(cid:8926)(cid:11184)(cid:9186)(cid:8544)(cid:8926)(cid:11184)(cid:8544) (cid:9186)(cid:8926)(cid:11184)(cid:8544)
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}6. 碱性锌锰干电池的结构示意图如右图。该电池放电时发生反应:
Zn + 2MnO + HO=ZnO + 2MnOOH。下列说法正确的是
2 2
A.Zn发生还原反应
B.正极发生反应MnO + H++ e- =MnOOH
2
C.电池工作时OH-向正极方向移动
D.理论上,每转移0.1 mol电子,有8.8 g MnOOH生成
7. 下列实验现象与HO的电离平衡无关的是
2
4 4
A.向NaCO 溶液中加入酚酞,溶液变红
2 3
B.向饱和HS溶液中通入少量SO 气体,生成淡黄色沉淀
2 2
C.加热CHCOONa溶液,pH减小
3
D.25 ℃时,将pH = 6的盐酸稀释10倍,溶液pH<7
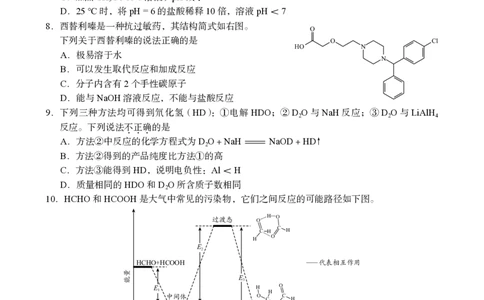
8. 西替利嗪是一种抗过敏药,其结构简式如右图。
下列关于西替利嗪的说法正确的是
A.极易溶于水
B.可以发生取代反应和加成反应
C.分子内含有2个手性碳原子
D.能与NaOH溶液反应,不能与盐酸反应
9. 下列三种方法均可得到氘化氢(HD):①电解HDO;②DO与NaH反应;③DO与LiAlH
2 2 4
反应。下列说法不正确的是
4 4 4
A. 方法②中反应的化学方程式为DO + NaH=NaOD + HD↑
2
B. 方法②得到的产品纯度比方法①的高
C. 方法③能得到HD,说明电负性:Al<H
D. 质量相同的HDO和DO所含质子数相同
2
10. HCHO和HCOOH是大气中常见的污染物,它们之间反应的可能路径如下图。
H O
O
C H C H
H O
H O H
(cid:857)(cid:19232)(cid:1151) O C C H
O
H
O H O
H C C H
H O
(cid:2297)(cid:5056)(cid:17671)(cid:12087)
高三年级(化学) 第2页(共8页)
(cid:18171)(cid:13865)
(cid:19000)(cid:12725)(cid:2488)
(cid:8526)(cid:8531)(cid:2114)(cid:18922)
(cid:952)(cid:8531)(cid:2114)(cid:19036)
(cid:2488)(cid:11551)(cid:3540)
O
O Cl
HO N
N
(cid:17651)(cid:9037)(cid:5421)
E(cid:19)
HCHO+HCOOH (cid:1039)(cid:15764)(cid:11300)(cid:958)(cid:1160)(cid:10836)
E(cid:20)
E(cid:18)
(cid:342) (cid:979)(cid:10133)
(cid:343)
O
下列说法正确的是
A. 总反应的速率主要由E 决定
2
B. 该路径中,HCHO与HCOOH发生取代反应
C. HCHO与HCOOH反应时,ΔH>0
D. 维持中间体的相互作用中,①和②均为氢键
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}11. 下列方程式与所给事实不相符的是
4 4 4
A.铜与稀硝酸反应:3Cu + 8HNO (稀)=3Cu(NO) + 2NO↑ + 4HO
3 3 2 2
B.用NaHCO 溶液检验邻羟基苯甲酸中的羧基:
3
OH O(cid:14)
COOH
(cid:12)(cid:1)2HCO 3 (cid:14)
COO(cid:14)
(cid:12)(cid:1)2H 2 O (cid:12)(cid:1)2CO 2 (cid:278)
C.用NaS作沉淀剂,处理废水中的Pb2+:S2- + Pb2+=PbS↓
2
D.向CuSO 溶液中滴加足量浓氨水:Cu2+ + 4NH·HO=[Cu(NH)]2+ + 4HO
4 3 2 3 4 2
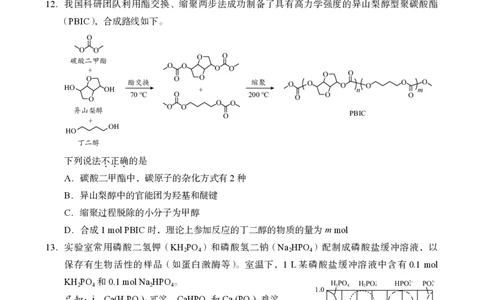
12. 我国科研团队利用酯交换、缩聚两步法成功制备了具有高力学强度的异山梨醇型聚碳酸酯
(PBIC),合成路线如下。
O
O O
(cid:11743)(cid:18084)(cid:952)(cid:10846)(cid:18075) O O
+ O O O O O O
HO O OH (cid:18075)(cid:976)(cid:6286) O + O (cid:13397)(cid:13702) O O O n O O m O
O 70 ℃ O 200 ℃ O O O
O O
(cid:5166)(cid:4509)(cid:7636)(cid:18099) O O
O PBIC
+
OH
HO
(cid:813)(cid:952)(cid:18099)
下列说法不正确的是
4 4 4
A.碳酸二甲酯中,碳原子的杂化方式有2种
B.异山梨醇中的官能团为羟基和醚键
C.缩聚过程脱除的小分子为甲醇
D.合成1 mol PBIC时,理论上参加反应的丁二醇的物质的量为m mol
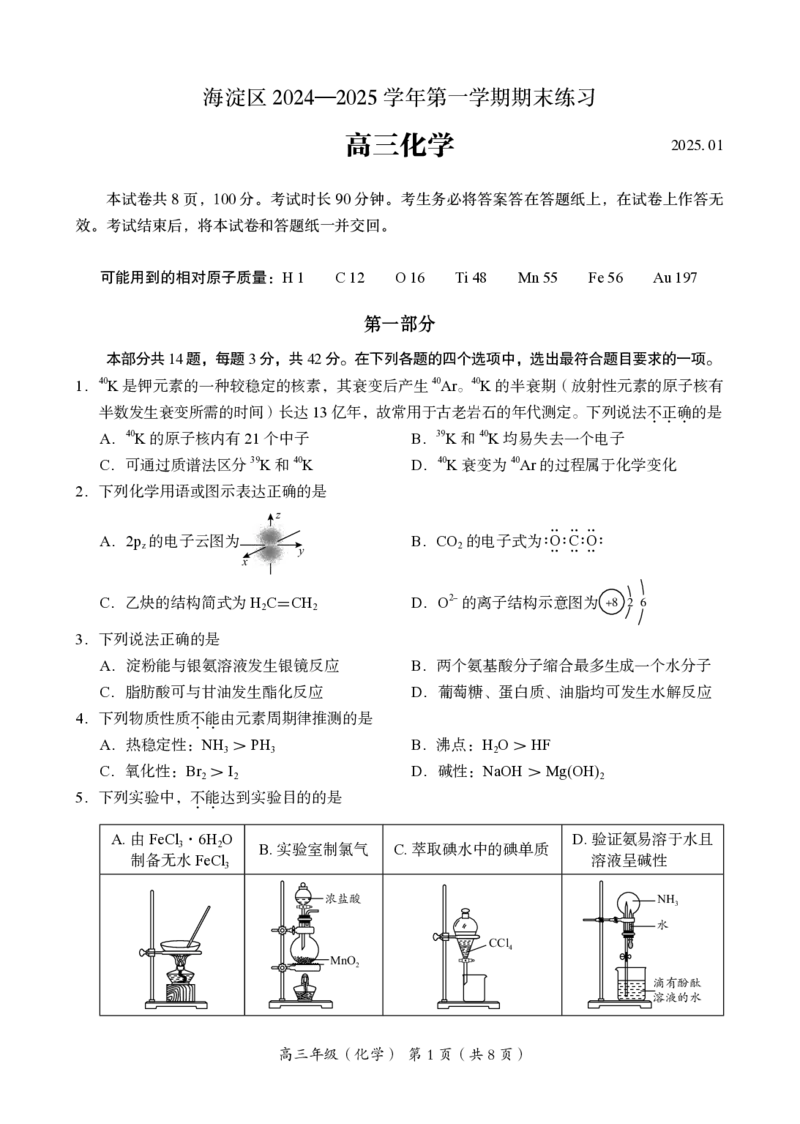
13. 实验室常用磷酸二氢钾(KHPO)和磷酸氢二钠(NaHPO)配制成磷酸盐缓冲溶液,以
2 4 2 4
保存有生物活性的样品(如蛋白激酶等)。室温下,1 L某磷酸盐缓冲溶液中含有0.1 mol
KH 2 PO 4 和0.1 mol Na 2 HPO 4 。 1.0 H 3 PO 4 H 2 PO(cid:14)4 HPO2 4(cid:14) PO(cid:20)4(cid:14)
已知:i.C a(HPO) 可溶,CaHPO 和Ca(PO) 难溶。
2 4 2 4 3 4 2 0.8
ii. 室温下,不同pH时,溶液中含磷微粒的物质
0.6
的量分数如右图。
0.4
下列关于该缓冲溶液的说法不正确的是 0.2
4 4 4
A.溶液pH约为7 0
0 2 4 6 8 10 12 14
B.c(HPO) + c(HPO- ) + c(HPO2- ) + c(PO3- )=0.2 mol·L-1 pH
3 4 2 4 4 4
C. 通入0.05 mol HCl气体后,溶液pH小于6
D.加入CaCl 激活蛋白激酶时,溶液pH可能降低
2
高三年级(化学) 第3页(共8页)
(cid:6812)(cid:1842)(cid:18171)(cid:11184)(cid:16980)(cid:10133)
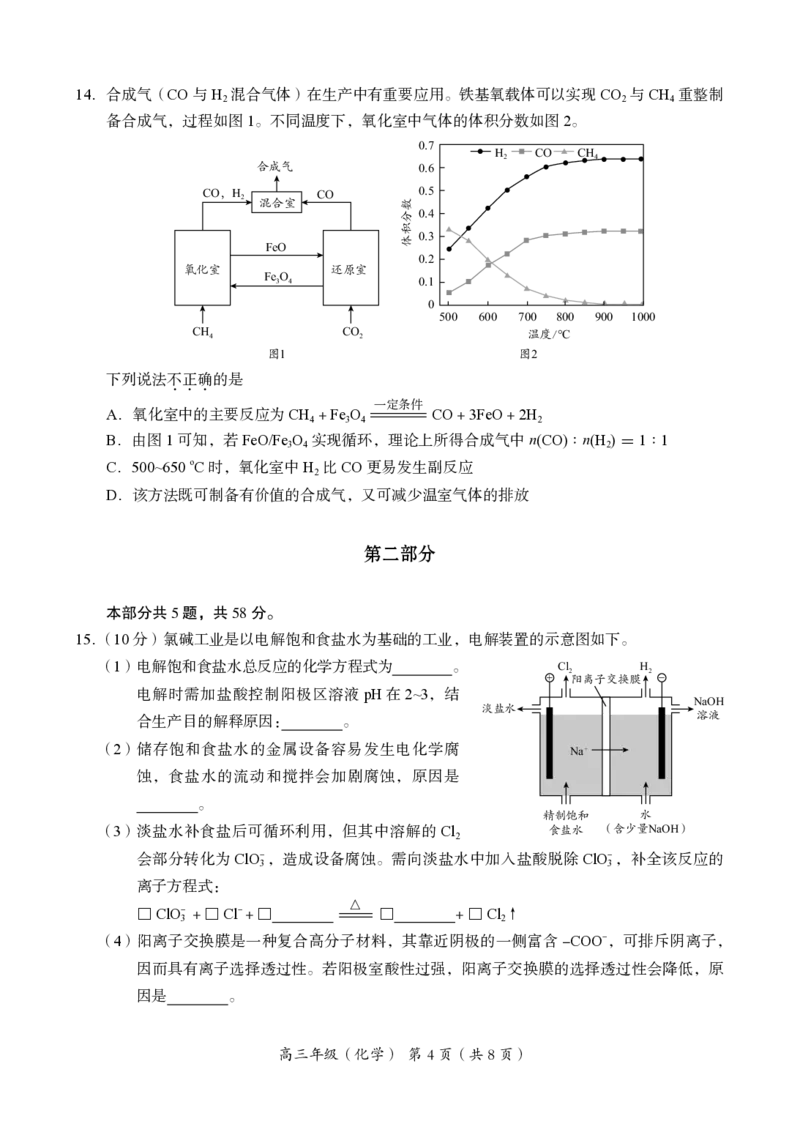
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}14. 合成气(CO与H 混合气体)在生产中有重要应用。铁基氧载体可以实现CO 与CH 重整制
2 2 4
备合成气,过程如图1。不同温度下,氧化室中气体的体积分数如图2。
H CO CH
2 4
(cid:2356)(cid:5948)(cid:8512)
CO,H CO
2
(cid:8995)(cid:2356)(cid:4304)
FeO
(cid:8531)(cid:2114)(cid:4304) FeO (cid:17668)(cid:2251)(cid:4304)
3 4
CH
4
CO
2
(cid:9045)(cid:5074)(cid:16)℃
(cid:3114)1 (cid:3114)2
高三年级(化学) 第4页(共8页)
(cid:6812)(cid:1842)(cid:12059)(cid:1151)
0.7
0.6
0.5
0.4
0.3
0.2
0.1
0
500 600 700 800 900 1000
下列说法不正确的是
4 4 4
一定条件
A.氧化室中的主要反应为CH + FeO=CO + 3FeO + 2H
4 3 4 2
B.由图1可知,若FeO/FeO 实现循环,理论上所得合成气中n(CO)∶n(H) = 1∶1
3 4 2
C.500~650 oC时,氧化室中H 比CO更易发生副反应
2
D.该方法既可制备有价值的合成气,又可减少温室气体的排放
第二部分
本部分共5题,共58分。
15.( 10分)氯碱工业是以电解饱和食盐水为基础的工业,电解装置的示意图如下。
(1) 电解饱和食盐水总反应的化学方程式为 。 Cl H
(cid:12) 2 (cid:19295)(cid:12007)(cid:4220)(cid:976)(cid:6286)(cid:14024) 2 (cid:14)
电解时需加盐酸控制阳极区溶液pH在2~3,结
NaOH
(cid:8973)(cid:11260)(cid:8544)
(cid:9186)(cid:8926)
合生产目的解释原因: 。
(2) 储存饱和食盐水的金属设备容易发生电化学腐 Na+
蚀,食盐水的流动和搅拌会加剧腐蚀,原因是
。
(cid:12778)(cid:1890)(cid:20125)(cid:2488) (cid:8544)
(3) 淡盐水补食盐后可循环利用,但其中溶解的Cl (cid:19979)(cid:11260)(cid:8544) (cid:21899)(cid:2391)(cid:4413)(cid:18171)NaOH(cid:21900)
2
会部分转化为ClO- ,造成设备腐蚀。需向淡盐水中加入盐酸脱除ClO- ,补全该反应的
3 3
离子方程式:
△
□ClO- + □Cl- + □ =□ + □Cl↑
3 2
(4) 阳离子交换膜是一种复合高分子材料,其靠近阴极的一侧富含-COO-,可排斥阴离子,
因而具有离子选择透过性。若阳极室酸性过强,阳离子交换膜的选择透过性会降低,原
因是 。
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}16.( 13分)Ti是一种密度小,强度大的金属。钛合金也有广泛应用。
(1)将Ti的基态原子价电子轨道表示式补充完整:
3d 4s
(2)Ti的三种四卤化物的熔点如下表。
四卤化物 TiCl TiBr TiI
4 4 4
熔点/℃ -24.1 38.3 155
TiCl、TiBr、TiI 的熔点依次升高的原因是 。
4 4 4
(3)TiCl 可用于制备金属Ti。工业上常以TiO 和Cl 为原料制备TiCl,反应时需加入焦炭。
4 2 2 4
已知:i.TiO(s) + 2Cl(g) TiCl(g) + O(g) ΔH =+172 kJ·mol-1 K =10-28.5
2 2 4 2 1 1
ii.2C(s) + O(g)=2CO(g) ΔH =-223 kJ·mol-1 K =1048.1
2 2 2
从平衡移动角度解释加入焦炭的作用: 。
(4)TiAu合金有良好的生物相容性,其晶体有α和β两种立方晶胞结构,如下图。
3
Au
Ti
(cid:30)-TiAu (cid:31)-TiAu
3 3
①α-TiAu中,Au周围最近且等距的Ti的个数为 。
3
② 若α-TiAu和β-TiAu两种晶胞棱长分别为a nm 和b nm,则两种晶体的密度之比
3 3
为 。
(5) 用滴定法测定TiAu合金中Ti含量:取a g合金,加入足量浓硫酸共热,得到紫色
3
Ti(SO) 溶液,并在酸性条件下定容至250 mL;取25 mL溶液于锥形瓶中,以KSCN
2 4 3
为指示剂,用c mol·L-1 Fe(SO) 溶液进行滴定,Ti(SO) 逐渐变为TiOSO(无色),
2 4 3 2 4 3 4
达到滴定终点时,消耗Fe(SO) 溶液V mL。
2 4 3
① 滴定过程Ti3+被氧化为TiO2+的离子方程式为 。
② 滴定终点的现象:滴入最后一滴Fe(SO) 溶液, 。
2 4 3
③ 合金中Ti的质量分数为 。
高三年级(化学) 第5页(共8页)
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}17.( 11分)钌(Ru)是贵金属,在医疗、催化等方面有重要应用。熔融-氧化-蒸馏法是工业
上回收废钌催化剂中Ru的一种方法,流程如下。
(cid:5067)(cid:18872)
(cid:1496)(cid:2114)(cid:1902)
6 (cid:9797) 50 (cid:9747) ℃ (cid:11741)(cid:9920)(cid:9039) Na (cid:1787) Cl (cid:2231) O(cid:543) (cid:14820) (cid:11671) (cid:20155) (cid:18084) R (cid:14820) u (cid:8512) O 4 (cid:8831)(cid:11260)(cid:18084) R (cid:9186) uC (cid:8926) l 3 (cid:6649)(cid:1160)A RuC (cid:7074) l 3 (cid:101) (cid:1151) 3H 2 O H 2 Ru
KOH
KNO
3
已知:i.RuO 易挥发,加热时容易分解成RuO 和O。
4 2 2
ii.随温度升高,RuCl 溶解度增大。
3
(1) 废钌催化剂中的钌单质和 RuO 经碱熔焙烧生成 K RuO ,其中 KNO 的作用是
2 2 4 3
。
(2) 如图1所示,蒸馏温度高于80 ℃时,RuO 蒸馏收率随着温度的升高而降低,可能的原
4
因是 。
(cid:10849)(cid:9148)
(cid:2391)RuO(cid:8878) (cid:2391)RuO(cid:8878)
2 2
(cid:4462)(cid:11184)(cid:5660)(cid:5459) (cid:4462)(cid:11184)(cid:5660)(cid:5459)
(cid:10849)(cid:7341)a (cid:10849)(cid:7341)b
(cid:9045)(cid:5074)(cid:16)(cid:269) H 2 SO 4 (cid:9186)(cid:8926)
(cid:3114)1 (cid:3114)2
高三年级(化学) 第6页(共8页)
%(cid:16)(cid:10419)(cid:6754)(cid:20155)(cid:14820)
100
80
60
40
20
0
60 70 80 90 100
(3)氧化-蒸馏时选用硫酸酸化而非盐酸,原因是 (用离子方程式表示)。
(4)获得RuCl·3HO晶体的操作A包括加热浓缩、 、 。
3 2
(5) 用交替电解法可剥落旧电极表面的RuO 催化涂层,再用熔融-氧化-蒸馏法回收Ru。
2
已知: i.电解时会生成Ru、RuO 和RuO,新生成的含钌物质在电极上的附着力弱。
2 4
ii.电解一段时间后,惰性阳极可能被部分氧化,导电能力降低。
① 交替电解装置如图2,每隔5~6分钟改变一次电流方向。电解时两电极上均有少量气
泡产生。刚通电时,阳极的电极反应式为 、 。
② 用交替电解法剥落RuO 涂层的效率较高,可能的原因有 (填序号)。
2
a.含钌物质可同时从a、b两电极上脱落
b.阴极上,全部电子均用于还原RuO
2
c.电流变向后,部分氧化的阳极被还原,电阻减小
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}18.( 12分)瓢虫分泌的生物碱可用于研发杀虫剂,瓢虫生物碱前体化合物L的合成路线如下。
O
O O
(cid:2114)(cid:2356)(cid:10133)P H DMF(aq) O O HO OH E
B O O
(cid:18099)(cid:18892) (cid:1496)(cid:2114)(cid:1902) CHO O H HCl(g) C 8 H 14 O 4
O C D
(cid:18099)(cid:18892)
O O O
A NH 2
DMF(aq)
(cid:2114)
(cid:18099)
(cid:2356)
(cid:18892)
(cid:10133)P
C 7 H
I
10 O 5
OHC
H
CHO (cid:263)
O O O O C 15 H
F
24 O 7
G
J DMF(aq) K N 2 H 4
N
pH=5.5(cid:13375)(cid:1758)(cid:8926) C 16 H 23 NO 5 C 12 H 19 NO (cid:812)(cid:4294)(cid:7309)(cid:1058)
L(C H N)
12 21
已知:
化
O O O O
(cid:18099)(cid:18892)
i. R 1 C OCH 3 + R 2 CH 2 C OR 3 R 1 C CH C OR 3 + CH 3 OH
R
2
R H O pH=5.5(cid:13375)(cid:1758)(cid:8926) R H O
N H + C O + R CH C R N C CH C R + HO
ii. 2 2 3 3 2
R R 1 R R 1 R 2
(1)P的结构简式是CHCOOCH。用乙酸和甲醇合成P的化学方程式为 。
3 3
(2)B → C的反应类型是 。
O O
(3) C中官能团的名称是 。用虚线标注出C→D时C的断键位置: O O
CHO
(4)E中不含醛基,含有一个五元环,E的结构简式为 。
(5) I的核磁共振氢谱有两组峰,峰面积之比为3∶2,A和P以物质的量之比1∶2合成I的
化学方程式为 。
(6)J中含有三个六元环,J的结构简式为 。
(7) K → L过程中NH 转变为N。理论上发生反应的K与NH 的物质的量之比为 。
2 4 2 2 4
高三年级(化学) 第7页(共8页)
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}19.( 12分)某小组同学用下图装置探究SO 与亚铁盐溶液的反应(夹持装置略)。
2
已知:稀溶液中Fe3+的水合离子几乎无色;Fe3++ 4Cl- [FeCl]-(黄色)。
4
(cid:12076)(cid:11671)(cid:18084) 70%(cid:11671)(cid:18084)
(cid:8807)(cid:3466)a
(cid:8807)(cid:3466)b
0.56 g(cid:18925)(cid:12725)(cid:857)
Na
2
CO
3
Na
2
SO
3 (cid:1996)(cid:1681)10 mL(cid:16641)(cid:1902)X
NaOH(cid:9186)(cid:8926)
A B C D
操作:向0.56 g铁粉中迅速加入10 mL试剂X,塞紧试管C上的胶塞,立即打开活塞a,待
C中铁粉完全溶解后,关闭活塞a,打开活塞b。C中现象如下表。
C中现象
序号 试剂X
打开活塞a后 打开活塞b后
有大量气泡产生,铁粉逐渐减少,无色 溶液逐渐变为浅黄色,
Ⅰ 6 mol·L-1盐酸
溶液迅速变黄,后逐渐变为浅绿色 产生极少量淡黄色沉淀
有大量气泡产生,铁粉逐渐减少,无色 溶液逐渐变为黄色,
Ⅱ 12 mol·L-1盐酸
溶液迅速变黄,后逐渐变为浅绿色 产生少量淡黄色沉淀
有大量气泡产生,铁粉逐渐减少,无色
Ⅲ 3 mol·L-1硫酸 无明显变化
溶液逐渐变为浅绿色
(1)打开活塞b后,B中反应的化学方程式为 。
(2)上述实验中,打开活塞a一段时间后关闭,再打开活塞b,目的是 。
(3)打开活塞a期间,实验Ⅰ~Ⅲ中的现象有相同也有不同。
① 实验Ⅰ、Ⅱ中,试管C内无色溶液均先变黄,再逐渐变为浅绿色。溶液由黄色变为浅
绿色的原因是 (用离子方程式表示)。
② 实验Ⅲ中,溶液始终未变黄,可能的原因是 。
(4) 经检验,实验Ⅰ、Ⅱ中的淡黄色沉淀为硫单质。甲同学猜想可能是 SO 自身发生歧化
2
反应,乙同学通过实验排除了这种可能性,其实验操作及现象为 。
(5)综合上述实验,可以得出的结论是 (结合化学用语说明)。
高三年级(化学) 第8页(共8页)
{#{QQABSYSEogigAgBAABgCAQmSCEKQkAEACSgGxBAcsAAASRFABAA=}#}