文档内容
箩 天星教育 泓馊 24年试卷品牌 ∞
|卡 ·TM
'△ ·
唇 目 录
百妆 CONTENTs 练100谰老题 ,不 如练1次新题
心受
主编 杜志建
2024江
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (一
西 ) 聚焦江西考情 · 就刷天星猜题卷
猜 题卷 新情境 两相无膜锌/吩噻嗪电池、萘生成1一 萘磺酸和2一 萘磺酸的机理
新考法 离子交换法测定PbC12的 Ksp
C圃mE目日》
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (二
◆ )
新情境 江西人文、钴单质催化剂的晶体结构
·依标命题,考教衔接
◆ ●
卷 (六 )T5
新考法 多平衡体系平衡后压强计算
匚 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (三
·重视教材实验
=彐 )
新情境 溴苯与CO反应的机理、新型固态电解质反应装置 卷 (一 )T16、 卷 (二 )T15
新考法 综合实验题渗透微观过程分析
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (四 蜘
练 100遍 老题 不如练1次 新题 ) 崛蹋圃晒心I蛳
新情境 提取金属铌的方法、铁酸钇晶胞结构
·实验题呈现形式多样
注意
△
高考考的全是新试题 新考法 物质转化途径的开放命题
! 卷 (三 )V
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (五
)
●元素推断题形式、角度、信息呈现丰富
新情境 溴介导的乙烯电氧化合成 E0、 过氧化氢法制备过氧乙酸
“ ”
多彩
参照 九省区联考 江西考试模式及新考向信息命制
新考法 结合物质结构与性质进行实验结果分析
卷 (五 )%
IRD 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (六
)
瑶
新情境 滕王阁、氟化钙的制备
付
李桥
裕龙
生
邱
刘
伟
宇
华
慧 赵
扶一
中 丁
不忪 一
汩
讼
进 杨
王
小
晓蕾
丹
李
陈
斯文
乐
刘
张
国顺
欢
谢
顶金
军敏
辉
郑
:长
丽
志
峰
:虽 V 新图像 电解水的阳极析氧反应机理图 瞵醉彝鼙鳓 吒匪夔盟豸心I婴鹬枷⒅婴婴杩
张毅强 谢英峰 杨志刚 齐平元 温江华 董中海 罗功举 彭传清 四 r 油 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (七
由 E日 鱼 土 」L 土 成昌华 黄 稳 黄爱华 韩 利 王字竞 杨立江 李子杰 ) ·工艺流程题综合性、创新性、开放性增强
乔 娜 杨志刚 戴艳霞 肖中荣 陈志坚 周慧智 吴新生 刘卫捐 新图像 氨基磺酸的制备装置、三甲基镓的制备装置
陈斯林 盛烨锋 章新阳 张 奇 杨 帆 周 冰 陈敏跚 汤俊艳 卷 (四 )T16、 卷 (八 )T15
熊 伟 钟天真 李志鹏 何祖莺 刘化毅 王 鹏 赵丽娜 廖 庄 新考法 与哲学观点结合、综合判断方程式和反应类型 ·反应原理综合题注重开放性
孙 宁 施艳华 赵明雪 王 静 吕清文 郎 晶 丛 莎 汲丛家 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (八
朱 松 王录飞 周 波 谢骏辉 谭 操 童建军 雷稳慧 张华良 ) 卷 (二 )T18
王
陈聪
福
敏
平
吴
董
艳欣
强
陈
张
日
国
红
彪
康
孙
红
康
红
荣
郭
唐
小
灵
双
生
周
喻
鑫
建
荣
军 李
陈
银
廷俊
秀
陈
王
志 明
豪 Ⅱ
新情境 可充电生物质电池、铁镁合金晶胞结构
●反应原理综合题注重思维容量
L
谭银光 袁俭良 孙功建 吴向东 张恒良 董志伟 郭慧芳 鞠秀芳 匚 删 新图像 二氧化碳淡化海水的循环图、温度一时间图 卷 (七 )T18
丁 怡 魏 恒 代国帅 刘天柱 王赤峰 王 波 张永冈 何清松
J
朱向阳 陈 熙 郑梓华 沈耀炫 苏国树 杨延光 戈益超 周 峰 躞 ·有机化学基础融合物质结构考查
李洪波 汤 伟 江已舒 苏振华 汤先金
卷 (七 )T16
(排名不分先后
) 讲题视频、答题卡
必 延边教育出版社箩 天星教育 泓馊 24年试卷品牌 ∞
|卡 ·TM
'△ ·
唇 目 录
百妆 CONTENTs 练100谰老题 ,不 如练1次新题
心受
主编 杜志建
2024江
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (一
西 ) 聚焦江西考情 · 就刷天星猜题卷
猜 题卷 新情境 两相无膜锌/吩噻嗪电池、萘生成1一 萘磺酸和2一 萘磺酸的机理
新考法 离子交换法测定PbC12的 Ksp
C圃mE目日》
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (二
◆ )
新情境 江西人文、钴单质催化剂的晶体结构
·依标命题,考教衔接
◆ ●
卷 (六 )T5
新考法 多平衡体系平衡后压强计算
匚 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (三
·重视教材实验
=彐 )
新情境 溴苯与CO反应的机理、新型固态电解质反应装置 卷 (一 )T16、 卷 (二 )T15
新考法 综合实验题渗透微观过程分析
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (四 蜘
练 100遍 老题 不如练1次 新题 ) 崛蹋圃晒心I蛳
新情境 提取金属铌的方法、铁酸钇晶胞结构
·实验题呈现形式多样
注意
△
高考考的全是新试题 新考法 物质转化途径的开放命题
! 卷 (三 )V
江西省2024年普通高中学业水平选择性考试 化学猜题卷 (五
)
●元素推断题形式、角度、信息呈现丰富
新情境 溴介导的乙烯电氧化合成 E0、 过氧化氢法制备过氧乙酸
“ ”
多彩
参照 九省区联考 江西考试模式及新考向信息命制
新考法 结合物质结构与性质进行实验结果分析
卷 (五 )%
IRD 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (六
)
瑶
新情境 滕王阁、氟化钙的制备
付
李桥
裕龙
生
邱
刘
伟
宇
华
慧 赵
扶一
中 丁
不忪 一
汩
讼
进 杨
王
小
晓蕾
丹
李
陈
斯文
乐
刘
张
国顺
欢
谢
顶金
军敏
辉
郑
:长
丽
志
峰
:虽 V 新图像 电解水的阳极析氧反应机理图 瞵醉彝鼙鳓 吒匪夔盟豸心I婴鹬枷⒅婴婴杩
张毅强 谢英峰 杨志刚 齐平元 温江华 董中海 罗功举 彭传清 四 r 油 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (七
由 E日 鱼 土 」L 土 成昌华 黄 稳 黄爱华 韩 利 王字竞 杨立江 李子杰 ) ·工艺流程题综合性、创新性、开放性增强
乔 娜 杨志刚 戴艳霞 肖中荣 陈志坚 周慧智 吴新生 刘卫捐 新图像 氨基磺酸的制备装置、三甲基镓的制备装置
陈斯林 盛烨锋 章新阳 张 奇 杨 帆 周 冰 陈敏跚 汤俊艳 卷 (四 )T16、 卷 (八 )T15
熊 伟 钟天真 李志鹏 何祖莺 刘化毅 王 鹏 赵丽娜 廖 庄 新考法 与哲学观点结合、综合判断方程式和反应类型 ·反应原理综合题注重开放性
孙 宁 施艳华 赵明雪 王 静 吕清文 郎 晶 丛 莎 汲丛家 江西省2024年普通高中学业水平选择性考试 化学猜题卷 (八
朱 松 王录飞 周 波 谢骏辉 谭 操 童建军 雷稳慧 张华良 ) 卷 (二 )T18
王
陈聪
福
敏
平
吴
董
艳欣
强
陈
张
日
国
红
彪
康
孙
红
康
红
荣
郭
唐
小
灵
双
生
周
喻
鑫
建
荣
军 李
陈
银
廷俊
秀
陈
王
志 明
豪 Ⅱ
新情境 可充电生物质电池、铁镁合金晶胞结构
●反应原理综合题注重思维容量
L
谭银光 袁俭良 孙功建 吴向东 张恒良 董志伟 郭慧芳 鞠秀芳 匚 删 新图像 二氧化碳淡化海水的循环图、温度一时间图 卷 (七 )T18
丁 怡 魏 恒 代国帅 刘天柱 王赤峰 王 波 张永冈 何清松
J
朱向阳 陈 熙 郑梓华 沈耀炫 苏国树 杨延光 戈益超 周 峰 躞 ·有机化学基础融合物质结构考查
李洪波 汤 伟 江已舒 苏振华 汤先金
卷 (七 )T16
(排名不分先后
) 讲题视频、答题卡
必 延边教育出版社绝密★启用前 4.下列关于仪器使用的说法正确的是
2024年 A。 仪器①、②可用于物质分离 厂只 田
江西省 普通高 中学业水平边择性考试
仪器②、③使用前需要检漏
`ll— 丿
rllllll
`丿
H
H
母
B。 吊
—
化学猜题卷 (一 C。 仪器④、⑤可用酒精灯直接加热 —
冫 ≡ 《≡≡≡,
)
D。 仪器③、⑥使用前需要烘干 u石 ② ③ ④ ⑤ ⑥
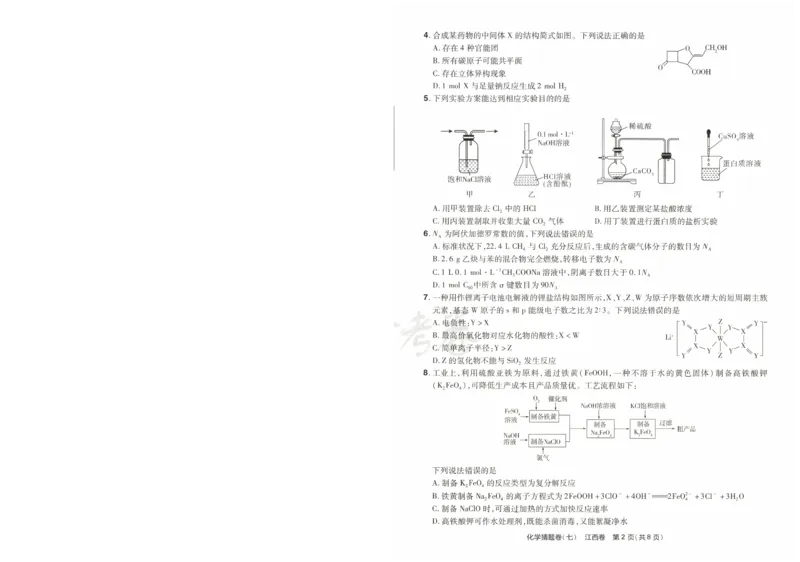
国 命题报告 5.中药丹参中存在丹参醇,具有抗心律失常作用,其合成路线中的部分反应如下。下列说法错误
■
舞 命题人思路:本套试卷以《高考评价体系》为指导,以《普通高中化学课程标准》为依据进行命制。试题将化学知 的是
识、思想、技能和方法融入真实情境,突 出考查考生的关键能力、学科素养和思维品质,注重考查考生对所学知识的融 A。 Ⅹ和 Y分 子中都存在手性碳原子
会贯通和灵活应用。
B。
Ⅹ与 Y都 能使溴的四氯化碳溶液褪色
枷 命题新风向:第 1题结合古诗文考查基础知识,能 弘扬中国传统文化,增 强文化自信;第 12题使用离子交换柱测定 C.Ⅹ 和 Y可 用金属钠进行鉴别 — CH3 MgBr ) — H2 → 0
“ ”
溶度积常数,需要考生根据题目信息进行分析,能有效避免死记硬背和 机械刷题 ;第 16题结合基础实验延伸考查 D。 Ⅹ→Y包 含加成、取代反应 0 0MgBr Y 0H
Ⅹ
含碘废液中余碘成分的探究与I^含量测定,优化情境创设,注重学用结合,试题的开放性、探究性和创新性高;第 17 6.下列实验操作、现象及结论均正确的是
唰 题结合氨气制化工产品的原理,考查可逆反应体系的平衡分析,涉及计算、原因分析、图像分析等,通过可视化、过程
选项 实验操作及现象 实验结论
化和规范化的训练来提高考生的思维品质。
巾
向蔗糖溶液中滴加稀硫酸,水浴加热,加入少量新制 的
划 搀 A 蔗糖未发生水解
舯 本试卷满分 100分。考试时间 75分 钟。 Cu(0H)2,无 砖红色沉淀生成
脚 可能用到的相对原子质量:H—
1 B-11 C—12 N-14 0-16 Ca-40 Fe-56 C0-59 B 向Ca(c10)2溶液中通入 SO2气体,有沉淀生成 沉淀为Caso4
Sn—119 Ta—
181
用铂丝蘸取少量某溶液进行焰色试验,透过蓝色钴玻璃观察
C 该溶液一定是钾盐溶液
K 逻 -、选择题 :本题共 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项是符合题 到火焰呈紫色
常温下,将铜片和铁片用导线连接插入浓硝酸中,铁片表面有
目要求的。 D 金属活动性:Cu)Fe
气泡产生
蝉
①滴定终点的实验现象是
柙 圾狠 碘成分
碉 干海带 」丝:室 )海 带灰 ≡垦·塑◆悬浊液 — )滤 液 」 L— 氧化液 萃取剂 ②待测滤液中I^的浓度是 mol· Lˉ 1。
———)晶
含碘有机层 体碘
化学猜题卷(一) 江西卷 第 5页(共8页 化学猜题卷(一) 江西卷 第 6页(共 8页
) )(1)下列仪器中,从于海带中提取碘的实验一定用不到的是 (填仪器名称
(一 )。
化学猜题卷 )选择题答题区
题号 2 4 5 6 得分
答案
题号 8 9 10 11 12 13 14
答案
■
二、非选择题:本题共 4小 题,共 58分。 (2)可 选用的萃取剂为 。(填标号
)
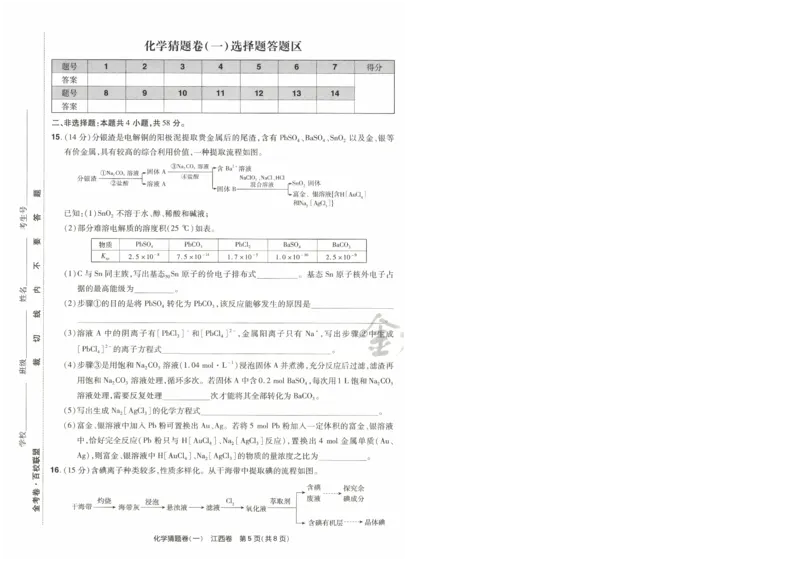
15.(14分 )分银渣是电解铜的阳极泥提取贵金属后的尾渣,含有 Pbs04、BaS04、Sn02以 及金、银等 A。 四氯化碳 B。 裂化汽油 C。 乙酸乙酯 D。 乙二醇 E。 植物油
有价金属,具有较高的综合利用价值,一种提取流程如图。 实验一 :某实验小组探究含碘废液中余碘成分。
A
③Na2C03溶液
Ba2十 溶液
(3)查 阅资料知:3I2+60Hˉ==5Iˉ +IOf+3H20、
5Iˉ
+IOf+6H+===3I2+3H20。
请选择必要
…~。 ①Na2 co3溶液 广固体
' 刀 z:·`Ji三 队IF1、】 ' 且 ‘ ②盐酸 L溶 液 A ④盐酸 NaC10 混 3、 合 N 溶 aCl 液 、HCl 02固体 的无机试剂以及实验操作,参考从甲到乙的图示,设计从含碘有机层中获取 I2的实验操作。
围 体 B 富金、银溶液 H[Auc1]
{含
试剂
和N%[AgC七 ]) 甲— → 乙 含碘有机层
巾 操作
已知:(1)Sn02不溶于水、醇、稀酸和碱液
划 如
絷 (2)部分难溶电解质的溶度积(25℃ )如表
;
。
(4)该小组继续查阅资料知
,在
酸性水溶液中,IOf能被SO:^还原成
I2。
①写出在酸性水溶液中,IOf氧化SO:^的离子方程式
脚
物质 Pbs04 PbC03 PbC12 BaS04 BaC03
②该小组测定含碘废液的pH=8.3,根 据资料准各了稀盐酸、淀粉溶液、Fec13溶液、Na2s03
Κ 2.5× 10ˉ: 7。 5× 10ˉ14 1.7× 10ˉ5 1。 0× 10ˉ1° 2.5× 10ˉ 9
K
逻
(1)C与 Sn同主族,写出基态 Sn原子的价电子排布式 。基态 Sn原子核外电子占
溶液,继续探究含碘废液中碘元素的存在形式,填写下表。
5。
蝉 据的最高能级为 实验操作及现象 实验结论或目的
恩
(2)步骤①的目的是将Pbs04转化为PbC03,该反应能够发生的原因是 取适量含碘废液,用萃取剂多次萃取、分液,最后一次分液
除掉废液中的I2
郴 量时,水层溶液滴加淀粉溶液不变蓝色
A试
(3)溶液 A中 的阴离子有[PbC13]^和 [PbC14]2ˉ ,金 属阳离子只有 Na+,写 出步骤②中生成 肛取水层溶液于 管中,加人稀盐酸酸化,滴加几滴淀粉
尽 [1]
i溽液,振荡,将溶液均分到 B和 C试 管中,溶液不变蓝色
[PbC14]2^的离子方程
淹 nw件 桶 (4)步骤③是用饱和Na2co3溶液(1.04 mol· Lˉ 1)浸 泡固体 A并 煮沸,充分反应后过滤,滤渣再
在B试管中[2]
废液中含有 Iˉ
碎
用饱和Na2co3溶液处理 ,循环多次。若固体 A中 含
0。
2m。l Bas04,每次用 1L饱 和Na2co3 在 C试 管中[3] 废液中不含 IOf
溶液处理,需要反复处理 次才能将其全部转化为Baco3。 实验二:该小组针对海带灼烧、浸泡、过滤所得的滤液,进行 I^含量的测定。
(5)写出生成Na2[AgC13]的化学方程式 (5)取待测滤液20.00 mL于锥形瓶中,加人20。 00 mLO。 010 0 mol· Lˉ 1 AgN03溶 液(过量),加
(6)富金、银溶液中加人Pb粉可置换出Au、Ag。 若将5m。l Pb粉加人一定体积的富金、银溶液 人 NH4Fe(S04)2作指示剂。用O.010 0 mo1· Lˉ 1 KSCN标 准溶液滴定剩余的Ag+至终点
,
中,恰好完全反应 (Pb粉 只与 H[Auc14]、 N%[AgC13]反应),置换出4m。l金属单质(Au、
重复上述操作两次。三次测定数据如下表
:
驯
Ag),则富金、银溶液中H[Auc14]、 N饧 [AgC13]的物质的量浓度之比为 ___
甾
实验序号 ^ 0
邱 (15分 Z D
16。 )含碘离子种类较多,性质多样化。从干海带中提取碘的流程如图。
肛 KSCN标 准溶液用量 /mL 10。 25 10。 02 9.98
究余
·
驷
室竺___>
①滴定终点的实验现象是
柙 圾狠 碘成分
碉 干海带 」丝:室 )海 带灰 ≡垦·塑◆悬浊液 — )滤 液 」 L— 氧化液 萃取剂 ②待测滤液中I^的浓度是 mol· Lˉ 1。
———)晶
含碘有机层 体碘
化学猜题卷(一) 江西卷 第 5页(共8页 化学猜题卷(一) 江西卷 第 6页(共 8页
) )(填 “ ”
17.(15分 )NH3在化学工业中是重要的原料,可以制各尿素、硝酸、丙烯腈等产品。 ③丙烯腈最高产率对应温度为460℃ 。低于460℃ 时,丙烯腈的产率 是 或
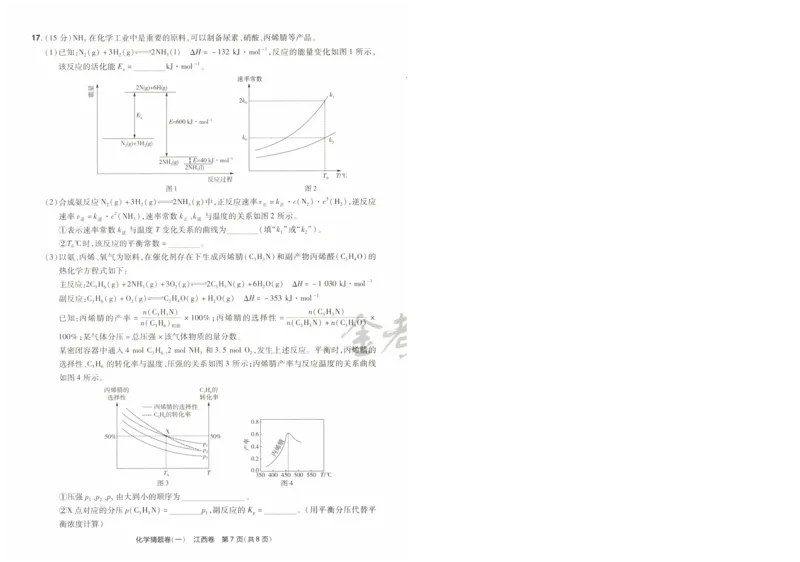
(1)已知:N2(g)+3H2(g)==圪 NH3(1) ΔⅡ=-132 kJ o mo1。 1,反 应的能量变化如图1所示 “ 不是 ” )对应温度下的平衡产率,判断理由是 ;高 于
,
该反应的活化能 Ea= kJ o molˉ1。 460℃ 时,丙烯腈产率降低的可能原因是 (写 2条 )。
W是
速率常数 18.(14分 )化合物 合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如图。
澜 2N(g)+6H(g)
驷 m
妲
,托 N02
人
0 0
人
NH2
^ z ,托 A Zn/HCl C o HOSO2Cl 0 H20/H+
‖
E C6H5F C6H6FN /\ NH3· H20
E〓600 kJ· mol^1 Ν N
B F H H
凡。
凡
D E
N2(g)+3H2(g) 2
0
Ⅹ Cl cl ||
2NH3(g) mol^1 F ①HCyH202 G C7H7Br \/′\ Cl I
飞 刀℃ C6H7FN2SO2 ②H20/催化剂 C6H5C1FN 一定条件 90℃ C15H12C12FNO
反应过程 Ν
1
图 图2 H
排
(2)合成氨反应 N2(g)+3H2(g)(=毛NH3(g)中 ,正反应速率v正 =尼正 ·c(N2)· c3(H2),逆反应 日
速率 v逆 =尼逆 ·c2(NH3),速率常数 凡 正 逆与温度的关系如图 2所 示。 Cl 出
`凡 (填“ “
①表示速率常数凡 逆与温度 r变化关系的曲线为
h”
或 凡
2” )。 160℃
AlC
~
1
1
3
70℃
②民℃时,该反应的平衡常数=
F
峪
(3)以 氨、丙烯、氧气为原料,在催化剂存在下生成丙烯腈 (C3H3N)和 副产物丙烯醛 (C3H40)的
W
△
热化学方程式如下 Η
:
圭三卢乏应:2C3H6(g)+2NH3(g)+302(g)乓==讫C3H3N(g)+6H20(g) ΔⅡ=-1 030 kJ o mol^1 NH2 Br N
一定条件 爿
鬲刂反 应 :C3H6(g)+02(g)了=主C3H40(g)+H20(g) ΔⅡ =-353 kJ o molˉ1
已知:(i)
+
已知:丙烯腈的产率 =萧 ∽r 过 r`I . 】 乱 瓦 IT、 惫 × 1° °%;丙 烯腈的选择性 = 几(C3H 尼 3 ( N C ) 3 + H n 3 ( N C ) 3 (ii) +R— Cl AlC13 R Ⅲ
160℃ ~170℃
100%;某气体分压=总压强 ×该气体物质的量分数。 啦
C的 官能团名称是
某密闭容器中通入4 mol c3H6、 2 mol NH3和 3.5m。102,发生上述反应。平衡时
,
选择性、C3H6的转化率与温度、压强的关系如图 3所 示;丙烯腈产率与反应温度的关系曲线
(2) 的反应类型是
渊
如图4所示。
(3)化合物 D中 碳原子的杂化方式为
(4)D→E和 F→G的
作用是
丙烯腈的 C3H6的
选择性 转化率 (5)写出I的结构简式
—
丙烯腈的选择性
……C3H6的转化率 (6)写出一种符合下列条件的 D的 同分异构体的结构简式
0000 Rυ
'6一 ①分子中除苯环外还有1个环
,苯
环上只有1个取代基
50% Ⅹ 50% 擀 烈 — 个 \ ② 1H-NMR谱 和IR谱检测表明:分子中共有6种不同化 ; 学环境的氢原子 ,有 N-0结 构。
怔 ∠ ·
^Z
熬、y—
— 0
/
— H
c1 ||
rx r ˉ \/\ H
400 450 500 550 T/℃ (7)设计由邻硝基甲苯和 cl制各 的合成路线(无机试剂任选 )。
图3 图 4
①压强 P3由大到小的顺序为
P1、P2、
②Ⅹ点对应的分压 P(C3H3N)=_R,副 反应的乌 = 。(用平衡分压代替平
衡浓度计算
)
化学猜题卷(一) 江西卷 第 7页(共8页 ) 化学猜题卷(一) 江西卷 第 8页(共 8页 )(填 “ ”
17.(15分 )NH3在化学工业中是重要的原料,可以制各尿素、硝酸、丙烯腈等产品。 ③丙烯腈最高产率对应温度为460℃ 。低于460℃ 时,丙烯腈的产率 是 或
(1)已知:N2(g)+3H2(g)==圪 NH3(1) ΔⅡ=-132 kJ o mo1。 1,反 应的能量变化如图1所示 “ 不是 ” )对应温度下的平衡产率,判断理由是 ;高 于
,
该反应的活化能 Ea= kJ o molˉ1。 460℃ 时,丙烯腈产率降低的可能原因是 (写 2条 )。
W是
速率常数 18.(14分 )化合物 合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如图。
澜 2N(g)+6H(g)
驷 m
妲
,托 N02
人
0 0
人
NH2
^ z ,托 A Zn/HCl C o HOSO2Cl 0 H20/H+
‖
E C6H5F C6H6FN /\ NH3· H20
E〓600 kJ· mol^1 Ν N
B F H H
凡。
凡
D E
N2(g)+3H2(g) 2
0
Ⅹ Cl cl ||
2NH3(g) mol^1 F ①HCyH202 G C7H7Br \/′\ Cl I
飞 刀℃ C6H7FN2SO2 ②H20/催化剂 C6H5C1FN 一定条件 90℃ C15H12C12FNO
反应过程 Ν
1
图 图2 H
排
(2)合成氨反应 N2(g)+3H2(g)(=毛NH3(g)中 ,正反应速率v正 =尼正 ·c(N2)· c3(H2),逆反应 日
速率 v逆 =尼逆 ·c2(NH3),速率常数 凡 正 逆与温度的关系如图 2所 示。 Cl 出
`凡 (填“ “
①表示速率常数凡 逆与温度 r变化关系的曲线为
h”
或 凡
2” )。 160℃
AlC
~
1
1
3
70℃
②民℃时,该反应的平衡常数=
F
峪
(3)以 氨、丙烯、氧气为原料,在催化剂存在下生成丙烯腈 (C3H3N)和 副产物丙烯醛 (C3H40)的
W
△
热化学方程式如下 Η
:
圭三卢乏应:2C3H6(g)+2NH3(g)+302(g)乓==讫C3H3N(g)+6H20(g) ΔⅡ=-1 030 kJ o mol^1 NH2 Br N
一定条件 爿
鬲刂反 应 :C3H6(g)+02(g)了=主C3H40(g)+H20(g) ΔⅡ =-353 kJ o molˉ1
已知:(i)
+
已知:丙烯腈的产率 =萧 ∽r 过 r`I . 】 乱 瓦 IT、 惫 × 1° °%;丙 烯腈的选择性 = 几(C3H 尼 3 ( N C ) 3 + H n 3 ( N C ) 3 (ii) +R— Cl AlC13 R Ⅲ
160℃ ~170℃
100%;某气体分压=总压强 ×该气体物质的量分数。 啦
C的 官能团名称是
某密闭容器中通入4 mol c3H6、 2 mol NH3和 3.5m。102,发生上述反应。平衡时
,
选择性、C3H6的转化率与温度、压强的关系如图 3所 示;丙烯腈产率与反应温度的关系曲线
(2) 的反应类型是
渊
如图4所示。
(3)化合物 D中 碳原子的杂化方式为
(4)D→E和 F→G的
作用是
丙烯腈的 C3H6的
选择性 转化率 (5)写出I的结构简式
—
丙烯腈的选择性
……C3H6的转化率 (6)写出一种符合下列条件的 D的 同分异构体的结构简式
0000 Rυ
'6一 ①分子中除苯环外还有1个环
,苯
环上只有1个取代基
50% Ⅹ 50% 擀 烈 — 个 \ ② 1H-NMR谱 和IR谱检测表明:分子中共有6种不同化 ; 学环境的氢原子 ,有 N-0结 构。
怔 ∠ ·
^Z
熬、y—
— 0
/
— H
c1 ||
rx r ˉ \/\ H
400 450 500 550 T/℃ (7)设计由邻硝基甲苯和 cl制各 的合成路线(无机试剂任选 )。
图3 图 4
①压强 P3由大到小的顺序为
P1、P2、
②Ⅹ点对应的分压 P(C3H3N)=_R,副 反应的乌 = 。(用平衡分压代替平
衡浓度计算
)
化学猜题卷(一) 江西卷 第 7页(共8页 ) 化学猜题卷(一) 江西卷 第 8页(共 8页 )绝密★启用前
2024年 干燥的 6H20
江西省 普通高 中学业水平选择性考试
I一K
一
△
~处尾气
) 理
(二
化学猜题卷
) z
r
v
目 命题报告
C.灼烧海带 D.制 各无水氯化镁
■ “ ”
本套试卷基于 三新 教育背景,结合对其他省份高考化学试卷的研究及江西省教学情况进行命制。本套试卷命 M的 M的
4.如 图是合成某种药物的中间体 结构简式。下列关于 叙述正确的有
题要达到的目的
: H00C H
①查漏补缺,促使对教材内容的挖掘,提升中低档题的得分率。选择题第 1~6题 属于常见考法,内 容较简单,第
8题、第10题 内容是教材内容拓展,第 15题也是教材实验的综合拓展,通过这些试题考查考生对相关知识的掌握和
应用情况。
②促进知识体系构建,多 维提升能力。第4题、第5题、第7题、第17题、第18题均涉及不同模块知识的综合考 H3C HC00 NH2
查,符合高考综合性的考查要求,有利于促进考生形成完整的知识体系。本套试卷图像较多且形式丰富,能促进考生
① M的 分子式为C17H1504N ② M含 有5种官能团 ③ M中 的碳原子杂化方式均为sp2
圊 运用多种思维方式进行探究,从而动态、全面地提升考生的能力和素养。
M的 M在
ˉ ④ 结构中不存在手性碳原子 ⑤ 一定条件下能发生取代、加成、消去、氧化、还原、加聚、
巾 本试卷满分 100分。考试时间 75分 钟。 lM最
划 如 缩聚反应 ⑥1m。 多可消耗3m。l Na0H
1 C—12 N-14 0-16 Na—23 A1-27 S-32 Cl—
舯 可能用到的相对原子质量:H— 35。 5
B。 C.① D。
Fe-56 Co—59 W-184 A。 ①②⑥ ③④⑤ ④⑥ ②③⑤
脚
-、选择题:本题共 14小题 ,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合题目 5.设 ⅣA为阿伏加德罗常数的值。下列叙述正确的是
K
要求。
A.0。
5 mol冰醋酸分子中含有的sp3杂化的原子数目为Ⅳ
A
1.江西省人文底蕴深厚、风景秀丽。下列说法错误的是
56 g Fe与 1m。l c12充分反应时转移的电子数为3Ⅳ
A。 江西萍乡的武功山冬季时的雾凇云海堪称绝美。雾凇是由水蒸气遇冷凝华而成的晶体,属于 B。 A
熙 蜃
慰 胶体 C。 2。 24 L CH2-CH2中 含共价键的数目为0.6Ⅳ A
— 郴 B。 江西抚州的资溪面包畅销国内外。面包 “ 疏松多孔的结构与发酵 ” 过程中产生大量的 C02有 关 。 D.0.01 mol· Lˉ 1 NaHC03溶 液中 HCOf的 数目小于0.01Ⅳ A
C。
江西九江的石钟山底部多洞穴,被称为 中国千古奇音第一山 。溶洞的形成是碳酸钙被溶蚀
下列能正确表示对应变化的离子方程式是
e∶
为碳酸氢钙的结果
尽 ˉ
D.瓦 罐汤是江西南昌的一大特色。煨汤用的瓦罐属于硅酸盐制品 A。
草酸与酸性KMno4溶液反应
:5C20】
+2MnOf+16H+===2Mn2++10C02↑ +8H20
ˉ
郦 韬 2.下列化学用语表示错误的是 B。 浓硝酸见光或受热易分解:4H++4NOf====4N0↑ +302↑ +2H20
秦 中子数为19的钙原子可表示为::Ca B.基态Cu原子的价层电子排布式为3d94s2
A。
C。 往 Nac1o溶 液 中通人少量 SO2:C10ˉ +SO2+H20==2H++Clˉ +SOlˉ
C。 NOf的 Ⅴ SEPR模 型为 D.NH3的 结构式为 H-I-H D。 向含有 NacN的 碱性溶液 中通入 C12进 行无毒处理 :5C12+2CNˉ +120Hˉ 〓==2CO:ˉ +N2+
H +6H20
10Clˉ
3.下列实验装置不能达到相应实验 目的的是 7.硫元素与氯元素可形成
SC12、
S2C12两种化合物,两种物质中各原子均满足最外层 8电子稳定结
Jf∶
舯 稀硫酸 构。其中S2C12是一种黄红色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发并产生酸
液
剁 mLO.1 mol·L-1●2 m 堡 LO.1 mo1· L-1
甾 F 04)溶 性悬浊液。下列说法正确的是
姆
肛 mL0.1 mo1·
l乡
A。
S2C12中 S的化合价为 一
1
· Na2Si03 溶液
抑 B。
S2C12无法使品红溶液褪色
N
柙
碉 A。 比较 S、C、 si的非金属性 B。 探究 Clˉ 、 SO1^对 Fe3+与 S20:^
C.S2C12与 水反应时,氧化产物与还原产物的物质的量之比为 1:2
SC12与 S2C12分子中共价键的类型不完全相同
反应速率的影响 D。
化学猜题卷(二 江西卷 第 1页(共 8页 化学猜题卷 (二 ) 江西卷 第2页(共8页
) ) )绝密★启用前
2024年 干燥的 6H20
江西省 普通高 中学业水平选择性考试
I一K
一
△
~处尾气
) 理
(二
化学猜题卷
) z
r
v
目 命题报告
C.灼烧海带 D.制 各无水氯化镁
■ “ ”
本套试卷基于 三新 教育背景,结合对其他省份高考化学试卷的研究及江西省教学情况进行命制。本套试卷命 M的 M的
4.如 图是合成某种药物的中间体 结构简式。下列关于 叙述正确的有
题要达到的目的
: H00C H
①查漏补缺,促使对教材内容的挖掘,提升中低档题的得分率。选择题第 1~6题 属于常见考法,内 容较简单,第
8题、第10题 内容是教材内容拓展,第 15题也是教材实验的综合拓展,通过这些试题考查考生对相关知识的掌握和
应用情况。
②促进知识体系构建,多 维提升能力。第4题、第5题、第7题、第17题、第18题均涉及不同模块知识的综合考 H3C HC00 NH2
查,符合高考综合性的考查要求,有利于促进考生形成完整的知识体系。本套试卷图像较多且形式丰富,能促进考生
① M的 分子式为C17H1504N ② M含 有5种官能团 ③ M中 的碳原子杂化方式均为sp2
圊 运用多种思维方式进行探究,从而动态、全面地提升考生的能力和素养。
M的 M在
ˉ ④ 结构中不存在手性碳原子 ⑤ 一定条件下能发生取代、加成、消去、氧化、还原、加聚、
巾 本试卷满分 100分。考试时间 75分 钟。 lM最
划 如 缩聚反应 ⑥1m。 多可消耗3m。l Na0H
1 C—12 N-14 0-16 Na—23 A1-27 S-32 Cl—
舯 可能用到的相对原子质量:H— 35。 5
B。 C.① D。
Fe-56 Co—59 W-184 A。 ①②⑥ ③④⑤ ④⑥ ②③⑤
脚
-、选择题:本题共 14小题 ,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合题目 5.设 ⅣA为阿伏加德罗常数的值。下列叙述正确的是
K
要求。
A.0。
5 mol冰醋酸分子中含有的sp3杂化的原子数目为Ⅳ
A
1.江西省人文底蕴深厚、风景秀丽。下列说法错误的是
56 g Fe与 1m。l c12充分反应时转移的电子数为3Ⅳ
A。 江西萍乡的武功山冬季时的雾凇云海堪称绝美。雾凇是由水蒸气遇冷凝华而成的晶体,属于 B。 A
熙 蜃
慰 胶体 C。 2。 24 L CH2-CH2中 含共价键的数目为0.6Ⅳ A
— 郴 B。 江西抚州的资溪面包畅销国内外。面包 “ 疏松多孔的结构与发酵 ” 过程中产生大量的 C02有 关 。 D.0.01 mol· Lˉ 1 NaHC03溶 液中 HCOf的 数目小于0.01Ⅳ A
C。
江西九江的石钟山底部多洞穴,被称为 中国千古奇音第一山 。溶洞的形成是碳酸钙被溶蚀
下列能正确表示对应变化的离子方程式是
e∶
为碳酸氢钙的结果
尽 ˉ
D.瓦 罐汤是江西南昌的一大特色。煨汤用的瓦罐属于硅酸盐制品 A。
草酸与酸性KMno4溶液反应
:5C20】
+2MnOf+16H+===2Mn2++10C02↑ +8H20
ˉ
郦 韬 2.下列化学用语表示错误的是 B。 浓硝酸见光或受热易分解:4H++4NOf====4N0↑ +302↑ +2H20
秦 中子数为19的钙原子可表示为::Ca B.基态Cu原子的价层电子排布式为3d94s2
A。
C。 往 Nac1o溶 液 中通人少量 SO2:C10ˉ +SO2+H20==2H++Clˉ +SOlˉ
C。 NOf的 Ⅴ SEPR模 型为 D.NH3的 结构式为 H-I-H D。 向含有 NacN的 碱性溶液 中通入 C12进 行无毒处理 :5C12+2CNˉ +120Hˉ 〓==2CO:ˉ +N2+
H +6H20
10Clˉ
3.下列实验装置不能达到相应实验 目的的是 7.硫元素与氯元素可形成
SC12、
S2C12两种化合物,两种物质中各原子均满足最外层 8电子稳定结
Jf∶
舯 稀硫酸 构。其中S2C12是一种黄红色液体,少量泄漏会产生窒息性气体,喷水雾可减慢其挥发并产生酸
液
剁 mLO.1 mol·L-1●2 m 堡 LO.1 mo1· L-1
甾 F 04)溶 性悬浊液。下列说法正确的是
姆
肛 mL0.1 mo1·
l乡
A。
S2C12中 S的化合价为 一
1
· Na2Si03 溶液
抑 B。
S2C12无法使品红溶液褪色
N
柙
碉 A。 比较 S、C、 si的非金属性 B。 探究 Clˉ 、 SO1^对 Fe3+与 S20:^
C.S2C12与 水反应时,氧化产物与还原产物的物质的量之比为 1:2
SC12与 S2C12分子中共价键的类型不完全相同
反应速率的影响 D。
化学猜题卷(二 江西卷 第 1页(共 8页 化学猜题卷 (二 ) 江西卷 第2页(共8页
) ) )“ ”
8.超分子化学的研究 日益深人。分离 C6。 和 C7。 就借助了超分子的 分子识别 特性,分离流程如图 12.北京理工大学某课题组用过渡金属碳化物(Co3ZnC)合成了钴单质催化剂(FPD-Co)。 FPD-Co
所示。下列有关说法错误的是 的晶体结构如图所示,其中8个 Co原子位于顶点,8个 Co原子位于棱上,4个 Co原子位于内部
,
+⑩
≤ D+≤D— ⑩ 其余位于面上。已知Co元素为元素周期表中的第 27号元素。设ⅣA为阿伏加德罗常数的值
,
超分子 下列说法错误的是
循环使用
甲苯、过滤 馥五勋
A。
基态Co原子的价层电子排布式为3d74s2
|
氯仿
8
“ ”
B.与 Co原子相邻且距离最近的Co原子个数为
墅蒿笤复了父踅弃
杯酚
邋瓦鼢 C。 若该晶体结构的棱长分别为2c pm、c pm、2c pm,则该晶体的密 z
^
→
A。 超分子是通过分子间相互作用形成的高分子 B。 氯仿的作用是溶解 “ 杯酚 ” F济 2。 36× 1032 gocm -3 跖 ∠ 彳 ^ 了 ' γ
店Dt
” D.Cω c3· Ⅳ A
C.“ 杯酚 是极性分子 和 C70互为同素异形体
FPD-Co晶
“ D。
胞中存在脱落价电子的钴离子与自由电子之间的相互作用
9。 某强还原性无机物的结构如图所示(图 中的 -” 可表示单键或双键),其中 W、Ⅹ、Y、 Z为 原子序
13.N0一 空气质子交换膜燃料电池实现了制硝酸、发电、环保一体化。某化学兴趣小组用该电池模
数依次增大的短周期主族元素,W和 Y为 同主族元素,Ⅹ 和 Z元 素原子的最外层电子数之和为
1,若 擀
拟工业处理废气和废水的过程,该过程装置如图所示。已知废水含Cl^的密度为7.1goLˉ
11。 下列叙述错误的是
)Y
处理一段时间后,测得丙池 M室 溶液质量减少 18g,忽略溶液体积变化,下列说法错误的是
A。 离子半径:Ⅹ …了 ~ 舀
)Z | |Γ | `I/ △ 交 交
简单气态氢化物的沸点
B。 :Ⅹ ~z_Ⅹ 换 换
C。 化合物 YW中 W显 负价 | | | Y十 | Ⅹ | NH3 浓 NH4 溶 )2 液 s04 膜 膜 b 燃
a
D。
W3ZⅩ2为三元酸 L 7v J N0+
H
H
N
2
0
0
3 H+
(增
+轧
湿
o
)
s° M室
浓
缩 N室 △
2 室
10。 学习小组利用如图所示的装置完成了制取并探究 SO2性质的实验。下列有关叙述正确的是
质子交换膜
(NH4)2S04稀溶液 稀硫酸稀溶液
丬
甲 乙 丙 ('雀rNi2+、 c1-)
稀硫酸
可上下移动的铜丝
Ⅲ
A。 交换膜 a为阳离子交换膜
4NO+302+2H20====4HN03
试管 1
酸性
试管2 试 Na 管 OH 3 卫 川 `'' 瓶 B。 甲池中总反应的化学方程式为 啦
的 酞 C.乙池增加 132g(NH4)2S04
Zns 溶
D.丙池 N室 处理废水量为 5L 曲
A。
硫酸的作用相同
14.二元有机酸 H2Ⅹ 的电离常数 凡1=1.67× 10ˉ :、K砣 =3.34× 10ˉ 17。 BaⅩ 难溶于水,常温下,将
试管 2和试管3中 SO2的作用相同
B。
BaⅩ 溶解在一定浓度的 HY溶 液中,直至不再溶解,测得混合液中c2(H+)与 c2(Ba2+)的关系如
C.试管 1中有气泡、酸雾产生,溶液中产生白色固体
图所示。下列说法错误的是
D.锥形瓶中红色变浅表明产生了NaHso3
11.相 2Ⅹ 同 (g 条 )+ 件 Y( 下 g) ,向 == 体 土 积 Z 均 (g 为 ) 1L Δ 的 Ⅱ《 甲 0, 乙 其 两 中 个 甲 恒 为 容 恒 密 温 闭 过 容 程 器 ,乙 中 为 分 绝 别 热 充 过 人 程 2 m , o 一 l 段 Ⅹ 时 和 间 1m 后 。 两 lY 反 ,发 应体 生反 系 应 均 0 三
已
.2 等
知
68 分
:
2
①
= 点 0
H
. 。 0
Y
7
是
22,
一
0.3
元
82
强
=0
酸
。
,B
1
a
4
Y
4
2
4
易
,拒
溶
△
于
1。
水
41
;
4
②
;③
0。
b点
192
为
=
线
0.
段
03
a
6
c
1
的
,
山
⌒
· ˇ + 凵
dˉ
` ⌒ ハ 日 0 0 . .0 4 3 4 61 ˉˉ-- a ●' b '° ` — c ● — — —
达到平衡状态。下列说法错误的是 ^的 ˇ 〓 —
A。 HⅩ 水解平衡常数约为6× 10ˉ 7 ` r
o
A。 容器甲中的压强不再改变说明反应已达平衡 B.无法确定 BaⅩ 的溶度积 c2(Ba2十)/(mo12· L-2)
B。
反应达到平衡状态时,平衡常数:K(甲 )>K(乙
)
C C
Ⅹ2ˉ
为定值
C。
反应达到平衡状态时,两容器中 X的 体积分数
:田
(甲 ))甲(乙
)
c(0H^)
D.再向甲容器中加入2 mol Ⅹ和 1m。lY,重新达到平衡时甲容器中 Y的 转化率变大 D.bJ点 :c(Ⅹ 2ˉ )+c(Yˉ )+c(0Hˉ )-c(H2Ⅹ)≈ 3.1m。 l· L^1
化学猜题卷(二 ) 江西卷 第3页(共8页 化学猜题卷(二 ) 江西卷 第4页(共8页
) )“ ”
8.超分子化学的研究 日益深人。分离 C6。 和 C7。 就借助了超分子的 分子识别 特性,分离流程如图 12.北京理工大学某课题组用过渡金属碳化物(Co3ZnC)合成了钴单质催化剂(FPD-Co)。 FPD-Co
所示。下列有关说法错误的是 的晶体结构如图所示,其中8个 Co原子位于顶点,8个 Co原子位于棱上,4个 Co原子位于内部
,
+⑩
≤ D+≤D— ⑩ 其余位于面上。已知Co元素为元素周期表中的第 27号元素。设ⅣA为阿伏加德罗常数的值
,
超分子 下列说法错误的是
循环使用
甲苯、过滤 馥五勋
A。
基态Co原子的价层电子排布式为3d74s2
|
氯仿
8
“ ”
B.与 Co原子相邻且距离最近的Co原子个数为
墅蒿笤复了父踅弃
杯酚
邋瓦鼢 C。 若该晶体结构的棱长分别为2c pm、c pm、2c pm,则该晶体的密 z
^
→
A。 超分子是通过分子间相互作用形成的高分子 B。 氯仿的作用是溶解 “ 杯酚 ” F济 2。 36× 1032 gocm -3 跖 ∠ 彳 ^ 了 ' γ
店Dt
” D.Cω c3· Ⅳ A
C.“ 杯酚 是极性分子 和 C70互为同素异形体
FPD-Co晶
“ D。
胞中存在脱落价电子的钴离子与自由电子之间的相互作用
9。 某强还原性无机物的结构如图所示(图 中的 -” 可表示单键或双键),其中 W、Ⅹ、Y、 Z为 原子序
13.N0一 空气质子交换膜燃料电池实现了制硝酸、发电、环保一体化。某化学兴趣小组用该电池模
数依次增大的短周期主族元素,W和 Y为 同主族元素,Ⅹ 和 Z元 素原子的最外层电子数之和为
1,若 擀
拟工业处理废气和废水的过程,该过程装置如图所示。已知废水含Cl^的密度为7.1goLˉ
11。 下列叙述错误的是
)Y
处理一段时间后,测得丙池 M室 溶液质量减少 18g,忽略溶液体积变化,下列说法错误的是
A。 离子半径:Ⅹ …了 ~ 舀
)Z | |Γ | `I/ △ 交 交
简单气态氢化物的沸点
B。 :Ⅹ ~z_Ⅹ 换 换
C。 化合物 YW中 W显 负价 | | | Y十 | Ⅹ | NH3 浓 NH4 溶 )2 液 s04 膜 膜 b 燃
a
D。
W3ZⅩ2为三元酸 L 7v J N0+
H
H
N
2
0
0
3 H+
(增
+轧
湿
o
)
s° M室
浓
缩 N室 △
2 室
10。 学习小组利用如图所示的装置完成了制取并探究 SO2性质的实验。下列有关叙述正确的是
质子交换膜
(NH4)2S04稀溶液 稀硫酸稀溶液
丬
甲 乙 丙 ('雀rNi2+、 c1-)
稀硫酸
可上下移动的铜丝
Ⅲ
A。 交换膜 a为阳离子交换膜
4NO+302+2H20====4HN03
试管 1
酸性
试管2 试 Na 管 OH 3 卫 川 `'' 瓶 B。 甲池中总反应的化学方程式为 啦
的 酞 C.乙池增加 132g(NH4)2S04
Zns 溶
D.丙池 N室 处理废水量为 5L 曲
A。
硫酸的作用相同
14.二元有机酸 H2Ⅹ 的电离常数 凡1=1.67× 10ˉ :、K砣 =3.34× 10ˉ 17。 BaⅩ 难溶于水,常温下,将
试管 2和试管3中 SO2的作用相同
B。
BaⅩ 溶解在一定浓度的 HY溶 液中,直至不再溶解,测得混合液中c2(H+)与 c2(Ba2+)的关系如
C.试管 1中有气泡、酸雾产生,溶液中产生白色固体
图所示。下列说法错误的是
D.锥形瓶中红色变浅表明产生了NaHso3
11.相 2Ⅹ 同 (g 条 )+ 件 Y( 下 g) ,向 == 体 土 积 Z 均 (g 为 ) 1L Δ 的 Ⅱ《 甲 0, 乙 其 两 中 个 甲 恒 为 容 恒 密 温 闭 过 容 程 器 ,乙 中 为 分 绝 别 热 充 过 人 程 2 m , o 一 l 段 Ⅹ 时 和 间 1m 后 。 两 lY 反 ,发 应体 生反 系 应 均 0 三
已
.2 等
知
68 分
:
2
①
= 点 0
H
. 。 0
Y
7
是
22,
一
0.3
元
82
强
=0
酸
。
,B
1
a
4
Y
4
2
4
易
,拒
溶
△
于
1。
水
41
;
4
②
;③
0。
b点
192
为
=
线
0.
段
03
a
6
c
1
的
,
山
⌒
· ˇ + 凵
dˉ
` ⌒ ハ 日 0 0 . .0 4 3 4 61 ˉˉ-- a ●' b '° ` — c ● — — —
达到平衡状态。下列说法错误的是 ^的 ˇ 〓 —
A。 HⅩ 水解平衡常数约为6× 10ˉ 7 ` r
o
A。 容器甲中的压强不再改变说明反应已达平衡 B.无法确定 BaⅩ 的溶度积 c2(Ba2十)/(mo12· L-2)
B。
反应达到平衡状态时,平衡常数:K(甲 )>K(乙
)
C C
Ⅹ2ˉ
为定值
C。
反应达到平衡状态时,两容器中 X的 体积分数
:田
(甲 ))甲(乙
)
c(0H^)
D.再向甲容器中加入2 mol Ⅹ和 1m。lY,重新达到平衡时甲容器中 Y的 转化率变大 D.bJ点 :c(Ⅹ 2ˉ )+c(Yˉ )+c(0Hˉ )-c(H2Ⅹ)≈ 3.1m。 l· L^1
化学猜题卷(二 ) 江西卷 第3页(共8页 化学猜题卷(二 ) 江西卷 第4页(共8页
) )(5)将得到的阴g苯 甲酸晶体配成 250 mL溶 液,取 25.00 mL于 锥形瓶中,用 O.54 mol· Lˉ1
化学猜题卷(二
)选择题答题区
Na0H溶 液滴定至终点,重复上述操作三次,平均消耗 NaoH溶 液 10.00 mL。
题号 ’ 一 3 4 0一 n 0 7 得分 ①滴定时选用的指示剂为 ,滴定终点的现象是
答案
题号 8 9 10 12 13 14
②苯甲酸的产率为
■ 答案
16.(15分 )苯二氮卓类药物氟马西尼(F)的 合成路线如图所示。
二、非选择题 :本大题包括 4小 题 ,共 58分 。
C00H NH2 C3H502Cl NHC00C2H5 c2H50H H Ν 0
/'
「
C00H ① C00H
②
15。 (14分 )苯甲酸( )是一种重要的化工用品,主要用于制各防腐剂与合成药物。某实验 A B (l
CH3 C00K C00H '` y H
巾 ˉ 唰 小组利用甲苯氧化法制各苯甲酸,其制各原理为 KMn04 — HCl ) ,制备 N ‘ I · 、 =△ ` 7 '1 △、 >' C00C C 2 N H C 5 H2C00C2H5 Cl POC13 `∈ H N 、 ″ 0 ˉ
)
划 洳
N
舯 装置如图所示(加热与夹持装置已省略 ⑤ F \CH3 ④
)。
F E D
跚
(1)按照系统命名法,A的名称为
K
汪 仪器a (2)B分 子中电负性最大的元素为
(3)反应①的化学方程式为
蝉
慰
(4)D在 NaoH溶
液中加热发生水解反应的化学方程式为
郴
(5 到L ,F中含氧官能团的名称为
'^丿
尽 CH3 Ⅹ
(6 是 F的 同分异构体,其中 — Ⅹ中含有一C00H,则 满足该条件的同分异构体有
滨 韬 步骤一:向三口烧瓶中依次加人 100 mL水 、6.0 mL甲 苯( ),加热至沸腾,然后加入过量
粼
件
中
高锰酸钾,继续加热至反应完全。
_种 (不考虑立体异构
)。
步骤二 :将反应混合液趁热过滤,酸化后得到苯甲酸粗品。
(7)已知氨基酸之间脱水能够形成含肽键的化合物,请设计 由甘氨酸 (H00CCH2NH2)和
mg苯
步骤三:经过一系列操作进行提纯,得到 甲酸晶体。
已知:①甲苯的密度为 92 go mLˉl。
0。
②苯甲酸在水中的溶解度:4℃ 时为 18g;25℃ 时为 34g;95℃ 时为6.8g。
NCCH2C00C2H5制
各
的合成路线(无机试剂任选
)。
0。 0。
羽
H5C200C /
淄 (1)仪器a的作用是 `
N
邱
肛 (2)制备苯甲酸的总化学方程式为
· ”
胂 (3)“ 趁热过滤 后应 ,目 的是提高苯甲酸的
柙
娟 收率。
(4)提纯苯甲酸的方法是
,用到的玻璃仪器有
化学猜题卷 (二 ) 江西卷 第5页(共 8页 化学猜题卷 (二 ) 江西卷 第6页(共 8页
) )(5)将得到的阴g苯 甲酸晶体配成 250 mL溶 液,取 25.00 mL于 锥形瓶中,用 O.54 mol· Lˉ1
化学猜题卷(二
)选择题答题区
Na0H溶 液滴定至终点,重复上述操作三次,平均消耗 NaoH溶 液 10.00 mL。
题号 ’ 一 3 4 0一 n 0 7 得分 ①滴定时选用的指示剂为 ,滴定终点的现象是
答案
题号 8 9 10 12 13 14
②苯甲酸的产率为
■ 答案
16.(15分 )苯二氮卓类药物氟马西尼(F)的 合成路线如图所示。
二、非选择题 :本大题包括 4小 题 ,共 58分 。
C00H NH2 C3H502Cl NHC00C2H5 c2H50H H Ν 0
/'
「
C00H ① C00H
②
15。 (14分 )苯甲酸( )是一种重要的化工用品,主要用于制各防腐剂与合成药物。某实验 A B (l
CH3 C00K C00H '` y H
巾 ˉ 唰 小组利用甲苯氧化法制各苯甲酸,其制各原理为 KMn04 — HCl ) ,制备 N ‘ I · 、 =△ ` 7 '1 △、 >' C00C C 2 N H C 5 H2C00C2H5 Cl POC13 `∈ H N 、 ″ 0 ˉ
)
划 洳
N
舯 装置如图所示(加热与夹持装置已省略 ⑤ F \CH3 ④
)。
F E D
跚
(1)按照系统命名法,A的名称为
K
汪 仪器a (2)B分 子中电负性最大的元素为
(3)反应①的化学方程式为
蝉
慰
(4)D在 NaoH溶
液中加热发生水解反应的化学方程式为
郴
(5 到L ,F中含氧官能团的名称为
'^丿
尽 CH3 Ⅹ
(6 是 F的 同分异构体,其中 — Ⅹ中含有一C00H,则 满足该条件的同分异构体有
滨 韬 步骤一:向三口烧瓶中依次加人 100 mL水 、6.0 mL甲 苯( ),加热至沸腾,然后加入过量
粼
件
中
高锰酸钾,继续加热至反应完全。
_种 (不考虑立体异构
)。
步骤二 :将反应混合液趁热过滤,酸化后得到苯甲酸粗品。
(7)已知氨基酸之间脱水能够形成含肽键的化合物,请设计 由甘氨酸 (H00CCH2NH2)和
mg苯
步骤三:经过一系列操作进行提纯,得到 甲酸晶体。
已知:①甲苯的密度为 92 go mLˉl。
0。
②苯甲酸在水中的溶解度:4℃ 时为 18g;25℃ 时为 34g;95℃ 时为6.8g。
NCCH2C00C2H5制
各
的合成路线(无机试剂任选
)。
0。 0。
羽
H5C200C /
淄 (1)仪器a的作用是 `
N
邱
肛 (2)制备苯甲酸的总化学方程式为
· ”
胂 (3)“ 趁热过滤 后应 ,目 的是提高苯甲酸的
柙
娟 收率。
(4)提纯苯甲酸的方法是
,用到的玻璃仪器有
化学猜题卷 (二 ) 江西卷 第5页(共 8页 化学猜题卷 (二 ) 江西卷 第6页(共 8页
) )“ ”
17.(14分 )江西赣州钨矿资源丰富,有 世界钨都 之称。由黑钨矿(主要成分为 Fewo4、 MnW04, 甲烷重整制氢工艺与太阳能资源相结合可有效降低碳排放。一种利用太阳能催化甲烷蒸气重
含有少量 si02)制 取碳酸锰 (Mnco3)和金属钨的流程如下 整制氢的反应 a的原理如图1所示。
:
H2C204 H2s04 lg气
太 4321012 I
MnO2 控温加热 Mns04(aq)
二EEIL)Mnc03 CH4
NiFe204 Co、H2 Ⅱ
稀盐酸 Δ
骂
800 900100011001200
过滤 蒸干、灼烧
A
H20 高能金属氧化物Nio、 FeO H2 一
滤液 固体 一
第Ⅱ步Δ 鸟 -3
水浸 NiFe204 -4
黑钨矿 粉碎、焙烧
过滤 反应 a分 步反应示意图 反应 a第
I、
Ⅱ步反应lg饩一r图像
滤渣Ⅱ
C02
调节pH
图 1
I 过滤 滤液Ⅱ 望 :坠 翌÷ Hw。 」生筮 ~w。 孳莛垂Lw 第 I步 :NiFe204(s)+CH4(g)==全 Nio(s)+2Feo(s)+Co(g)+2H2(g) ΔⅡ
1
已知:①钨酸 (H2W04)酸 性很弱,难溶于水,其钠盐易溶于水;②草酸(H2C204)为受热易分解的 第 Ⅱ步 :Nio(s)+2Feo(s)+H20(g)一 全NiFe2o4(s)+H2(g) ΔⅡ 2
还原性二元弱酸。 (3)对于第 I步反应 :Δ Ⅱ1 (选 填 “ >” “ (” 或 “ =” )0。 对于在恒容绝热密闭容器中发 排
(1)钨是74号元素,价层电子排布式为
生的第Ⅱ步反应,下列能够说明反应达到平衡状态的有
出
” (任 消耗 1m。l Nio(s)的 同时生成2m。l Feo(s)
(2)“ 焙烧 黑钨矿过程中除了将黑钨矿粉碎,还可以采取的措施有 写 A。
一种 焙烧
”
时 Mnwo4发 生反应的化学方程式为
B.H20(g)和 H2(g)的物质的量之比为1:1
燃
),“
” C.反应体系温度不变
(3)“ 控温加热 时发生反应的离子方程式为 。实际
△
D.反应体系压强不变
操作过程中发现,Mno2的溶解速率随着温度升高呈现出先增大后减小的递变规律,试分析
(Feo)=2v逆 (H2)
产生这一变化的原因为 E· v正
丬
(4)结合质子的能力 :sio:~_Wo:-(填 “ )” 或 “ (” ),滤 渣Ⅱ的化学式为 (4)在 1000℃ 时 ,反 应a的压强平衡常数民 的对数1g乌 =_。
(5)从 安全角度考虑,实验室采用热还原法将 W03还 原为 W的 过程中应选择 (选 填 (5)恒温恒压条件下,将 ~/ur·、 ` =%的混合气体通入盛有催化剂的反应器装置,测得 CH4的平 州
“ H2”或 “ Al” )作为还原剂,若生成 18.4gW,则 消耗还原剂的质量为 g。
百
|石
瓦斤
尼(H20) 啉
18.(15分 )氢能作为最有前途的能源之一 ,探究 H2的 高效制各途径备受关注。以C、 H20为 原料合 衡转化率与水碳比的关系如图2所示 =4时,CH4的转化率和混合气体流速的关
; 71(CH4)
成
H2涉及的主要反应如下。
系如图
3所示。已知:气体流速是指单位时间内通过任一截面的气体量。 渊
压L应 I:C(s)+H20(g)了 =土CO(g)+H2(g) ΔⅡ =+131 kJ o molˉ 1
术 98877 0 5 0 5 0
反 应 Ⅱ :CO(g)+H20(g)了 =土C02(g)+H2(g) Δ.H=-41 kJ o 1nolˉ 1 ` 擀 术 `
寒 擀
(1)反应 I高温下 (选 填 “ 能 ” 或 “ 不能 ” )自 发进行。 状 寒 P
翅 挥
(2)在一装有压强传感器的恒温恒容密闭容器中,加入足量的 C和一定量的H20(g),发生上述 半
寸 υ
〓 寸
〓
。
反应,测得压强变化如表所示 2 3 4
: 1 0.1
时间/min n U r D 10 15 ∞ 三 n( (H C 2° H4 ) ) 玛 ~ 卫 尼 - ( H C 2 H 二 4) =4时混合气体流速/(m3·s-1)
压强 /MPa 2。 34 3。 14 3.44 3.54 3.54 2
图 图 3
反丿立达到1甲:准轩后,p(CO)+P(C02)= MPa。 已知该温度下,反应 I的逆反应压强平 分析可知,图 3中的 P点 (选 填 “ 正向 ”“ 逆向 ” 或 “ 不 ” )移动,随
(I)= )= (保
衡常数民逆 ÷MPa^l,则 反应Ⅱ的压强平衡常数凡(Ⅱ 留两位有效 着混合气体流速的增大,CH4的转化率下降,主要原因是
Z r
数字
)。
化学猜题卷 (二 ) 江西卷 第7页(共 8页 化学猜题卷(二 ) 江西卷 第8页(共8页
) )“ ”
17.(14分 )江西赣州钨矿资源丰富,有 世界钨都 之称。由黑钨矿(主要成分为 Fewo4、 MnW04, 甲烷重整制氢工艺与太阳能资源相结合可有效降低碳排放。一种利用太阳能催化甲烷蒸气重
含有少量 si02)制 取碳酸锰 (Mnco3)和金属钨的流程如下 整制氢的反应 a的原理如图1所示。
:
H2C204 H2s04 lg气
太 4321012 I
MnO2 控温加热 Mns04(aq)
二EEIL)Mnc03 CH4
NiFe204 Co、H2 Ⅱ
稀盐酸 Δ
骂
800 900100011001200
过滤 蒸干、灼烧
A
H20 高能金属氧化物Nio、 FeO H2 一
滤液 固体 一
第Ⅱ步Δ 鸟 -3
水浸 NiFe204 -4
黑钨矿 粉碎、焙烧
过滤 反应 a分 步反应示意图 反应 a第
I、
Ⅱ步反应lg饩一r图像
滤渣Ⅱ
C02
调节pH
图 1
I 过滤 滤液Ⅱ 望 :坠 翌÷ Hw。 」生筮 ~w。 孳莛垂Lw 第 I步 :NiFe204(s)+CH4(g)==全 Nio(s)+2Feo(s)+Co(g)+2H2(g) ΔⅡ
1
已知:①钨酸 (H2W04)酸 性很弱,难溶于水,其钠盐易溶于水;②草酸(H2C204)为受热易分解的 第 Ⅱ步 :Nio(s)+2Feo(s)+H20(g)一 全NiFe2o4(s)+H2(g) ΔⅡ 2
还原性二元弱酸。 (3)对于第 I步反应 :Δ Ⅱ1 (选 填 “ >” “ (” 或 “ =” )0。 对于在恒容绝热密闭容器中发 排
(1)钨是74号元素,价层电子排布式为
生的第Ⅱ步反应,下列能够说明反应达到平衡状态的有
出
” (任 消耗 1m。l Nio(s)的 同时生成2m。l Feo(s)
(2)“ 焙烧 黑钨矿过程中除了将黑钨矿粉碎,还可以采取的措施有 写 A。
一种 焙烧
”
时 Mnwo4发 生反应的化学方程式为
B.H20(g)和 H2(g)的物质的量之比为1:1
燃
),“
” C.反应体系温度不变
(3)“ 控温加热 时发生反应的离子方程式为 。实际
△
D.反应体系压强不变
操作过程中发现,Mno2的溶解速率随着温度升高呈现出先增大后减小的递变规律,试分析
(Feo)=2v逆 (H2)
产生这一变化的原因为 E· v正
丬
(4)结合质子的能力 :sio:~_Wo:-(填 “ )” 或 “ (” ),滤 渣Ⅱ的化学式为 (4)在 1000℃ 时 ,反 应a的压强平衡常数民 的对数1g乌 =_。
(5)从 安全角度考虑,实验室采用热还原法将 W03还 原为 W的 过程中应选择 (选 填 (5)恒温恒压条件下,将 ~/ur·、 ` =%的混合气体通入盛有催化剂的反应器装置,测得 CH4的平 州
“ H2”或 “ Al” )作为还原剂,若生成 18.4gW,则 消耗还原剂的质量为 g。
百
|石
瓦斤
尼(H20) 啉
18.(15分 )氢能作为最有前途的能源之一 ,探究 H2的 高效制各途径备受关注。以C、 H20为 原料合 衡转化率与水碳比的关系如图2所示 =4时,CH4的转化率和混合气体流速的关
; 71(CH4)
成
H2涉及的主要反应如下。
系如图
3所示。已知:气体流速是指单位时间内通过任一截面的气体量。 渊
压L应 I:C(s)+H20(g)了 =土CO(g)+H2(g) ΔⅡ =+131 kJ o molˉ 1
术 98877 0 5 0 5 0
反 应 Ⅱ :CO(g)+H20(g)了 =土C02(g)+H2(g) Δ.H=-41 kJ o 1nolˉ 1 ` 擀 术 `
寒 擀
(1)反应 I高温下 (选 填 “ 能 ” 或 “ 不能 ” )自 发进行。 状 寒 P
翅 挥
(2)在一装有压强传感器的恒温恒容密闭容器中,加入足量的 C和一定量的H20(g),发生上述 半
寸 υ
〓 寸
〓
。
反应,测得压强变化如表所示 2 3 4
: 1 0.1
时间/min n U r D 10 15 ∞ 三 n( (H C 2° H4 ) ) 玛 ~ 卫 尼 - ( H C 2 H 二 4) =4时混合气体流速/(m3·s-1)
压强 /MPa 2。 34 3。 14 3.44 3.54 3.54 2
图 图 3
反丿立达到1甲:准轩后,p(CO)+P(C02)= MPa。 已知该温度下,反应 I的逆反应压强平 分析可知,图 3中的 P点 (选 填 “ 正向 ”“ 逆向 ” 或 “ 不 ” )移动,随
(I)= )= (保
衡常数民逆 ÷MPa^l,则 反应Ⅱ的压强平衡常数凡(Ⅱ 留两位有效 着混合气体流速的增大,CH4的转化率下降,主要原因是
Z r
数字
)。
化学猜题卷 (二 ) 江西卷 第7页(共 8页 化学猜题卷(二 ) 江西卷 第8页(共8页
) )绝密★启用前 4.ⅣA是阿伏加德罗常数的值。下列说法正确的是
A.1 mol[Ag(NH3)2]0H中 含有的σ键数为9Ⅳ
2024年 A
江西省 普通高中学业水平边择性考试
B.18g超
重水所含质子数为 10Ⅳ
A
C.标准状况下,22.4L新戊烷含有的共价键数为 16Ⅳ
化学猜题卷 (三 A
) D.C02气体通人含有 1m。l草酸氢钠的饱和溶液中生成草酸的分子数为Ⅳ
A
5.下列说法正确的是
□命题报告
■ A。 浓 H2s04可用于干燥酸性气体,因此浓 H2s04具有脱水性
本试卷依据高考评价体系和课程标准的要求,注重结合情境设置试题,创 新信息呈现方式,要求考生结合所学知识解
B.Fe可以从铜的盐溶液中置换出铜,因此可用 Fec13溶液腐蚀印刷电路板
决特定情境下的化学问题,体现学用结合。
C.so2具有漂白性,so2通人石蕊试液,使溶液先变红后褪色
"命题新素材:第 1题结合《天工开物》等考查传统文化中的化学知识;第 3题结合从栀子的干燥成熟果实中提取的
D.sio2能与 NaoH溶 液反应,保存 NaoH溶 液的试剂瓶不能用玻璃塞
栀子苷的结构简式考查有机物的结构与性质。 6.某强氧化性化合物的结构如图所示,其中W、X、Y、 z为 原子序数依次增大的短周期非金属元素
卜 命题新思维:第 8题考查溴苯与Co生成苯甲酸酯的机理分析,体现对考生思维方法的考查;第 13题结合新型固态 W的 最高正价和最低负价的代数和为零,Y与 z位 于同一主族。下列说法错误的是 ,
电解质反应装置考查电化学原理分析,素材较新,设题角度新颖。 瓦雳辈
巾
剥 本
可
试
能
卷
用
满
到
分
的相
10
对
0分
原子
。考
质
试
量
时
:H
间
-
7
1
5 分
C-
钟
1
。
2 N-14 0-16 Na—23 A1-27 Cl-35。 5
:
C.
霸
X和
,
z
晷
的最高
J
价
宣
氧
I
化
2价
物对
,
应
z显
水化
+7
物
价
均为 强 酸
[∶ I 〉 x 〈 l l
L
l
·
+II) ' z ′ JY Y ` `J ) z 《 |Jl
」
ˉ [I)x〈 lll+
划 舯 抑 Ca-40 Cr—52 C0—59 D.W、Ⅹ、 Y三 种元素形成的化合物可能是离子晶体
■ 脚
-、选择题:本题共14小题,每小题3分
,共
42分。在每小题给出的四个选项中,只有一项符合题目
7.根据下列实验操作和实验现象,得出的结论正确的是
选项 实验操作 实验现象 结论
要求。
K
将乙醇和浓硫酸的混合液加热,并将产生的气体直
1.传统文化中蕴含着许多化学知识。下列说法错误的是 A 溶液橙黄色褪去 产生的气体是乙烯
接通人溴水中
A。 《天工开物》中记载 :“ 凡煎卤未即凝结,将皂角椎碎,和粟米糠二味,卤沸之时投人其中搅和 向2一 溴丙烷和 NaoH溶 液反应后的溶液中加入
,
慰
岬 逻 盐即顷刻结成。 ” 其中涉及渗析 B AgN03溶 液 有沉淀生成 2一 溴丙烷中含有溴原子
■ 群 B。 《 “ 南村辍耕录》中 ” 记载 :“ 削松木为小片,其薄如纸,铬 (熔)硫黄涂木片顶分许,名 曰发烛 …… ” C 利用稀硫酸和镁条反应产生氢气的原理测气体摩尔 观察到装置漏气 测得气体摩尔体积的数值偏小
削松木为小片 有助于燃烧 体积
S
C。
《太平御览》中记载
:“
山公时一醉,遥造高阳池。日暮倒载归,酩酊无所知。 ” 酒精在人体内发 D 用 KSCN溶液检验铁发生电化学腐蚀后生成的离子 溶液变红 Fe被 腐蚀生成了Fe3十
生了化学变化 8 用下与 CO反 应,生成苯甲酸酯的机理如图所示,其中一Ph代 表一 C6H5。 下列
郦·攥 D。 《浣溪沙 · 徐州藏春阁园中》中有 :“ 惭愧今年二麦丰,千畦细浪舞晴空。 ” 小麦成熟过程中生成 说法 刀 曰 E
秦
ˉ 2.下列
了
化
多
学
糖
用语表述正确的是
0
H-F
P
d
|
P
-
h^
口
B 广
V
●
l
^
^
n
′ ∷Pd(PPh3)2
Br
OCH3
10)Ph3 HB+Br^
I
A.NaCl的形成过程 :Na/∶ )。i:_Na+[0:]^ B.SO:^的 Ⅴ SEPR模 型 PPh^
CH30H ˇ
|
ˉ Pd—Br
PPh~
斟 邱 C。 2一 甲基戊烷的键线式 :/ˇ| D。 羟基的电子式::0:H P | d - ˇ Br P|Ph3
`
剁 3.栀子苷 (M)是 从栀子的干燥成熟果实中提取的化合物,具有缓泻、镇痛、 0H P|Ph3 ΠⅡ
邯 Co
H
郅 抗炎等作用,其结构简式如图。关于该化合物,下列说法错误的是 C0
肛
KMno4溶
A。 该化合物可使酸性 液褪色 Ⅲ P| d—Br PPh3
·
抻 B.分子中含有 4种 官能团 PPh3 P|Ph3
柙
0H
碉 C。
分子中含有8个手性碳原子
M A。 反应Ⅲ生成物的分子式为 C43H35 0BrP2Pd B。 反应过程中 Pd形 成的化学键数不变
D。 1 mol M分别与足量 H2加成和与足量 Na反 应,最多消耗 n(H2):n(Na)=1:2 C.该反应的催化剂为 Pd(PPh3)2 D.反 应过程中没有非极性共价键的断裂
化学猜题卷(三) 江西卷 第1页(共8页 化学猜题卷(三) 江西卷 第2页(共8页
) )绝密★启用前 4.ⅣA是阿伏加德罗常数的值。下列说法正确的是
A.1 mol[Ag(NH3)2]0H中 含有的σ键数为9Ⅳ
2024年 A
江西省 普通高中学业水平边择性考试
B.18g超
重水所含质子数为 10Ⅳ
A
C.标准状况下,22.4L新戊烷含有的共价键数为 16Ⅳ
化学猜题卷 (三 A
) D.C02气体通人含有 1m。l草酸氢钠的饱和溶液中生成草酸的分子数为Ⅳ
A
5.下列说法正确的是
□命题报告
■ A。 浓 H2s04可用于干燥酸性气体,因此浓 H2s04具有脱水性
本试卷依据高考评价体系和课程标准的要求,注重结合情境设置试题,创 新信息呈现方式,要求考生结合所学知识解
B.Fe可以从铜的盐溶液中置换出铜,因此可用 Fec13溶液腐蚀印刷电路板
决特定情境下的化学问题,体现学用结合。
C.so2具有漂白性,so2通人石蕊试液,使溶液先变红后褪色
"命题新素材:第 1题结合《天工开物》等考查传统文化中的化学知识;第 3题结合从栀子的干燥成熟果实中提取的
D.sio2能与 NaoH溶 液反应,保存 NaoH溶 液的试剂瓶不能用玻璃塞
栀子苷的结构简式考查有机物的结构与性质。 6.某强氧化性化合物的结构如图所示,其中W、X、Y、 z为 原子序数依次增大的短周期非金属元素
卜 命题新思维:第 8题考查溴苯与Co生成苯甲酸酯的机理分析,体现对考生思维方法的考查;第 13题结合新型固态 W的 最高正价和最低负价的代数和为零,Y与 z位 于同一主族。下列说法错误的是 ,
电解质反应装置考查电化学原理分析,素材较新,设题角度新颖。 瓦雳辈
巾
剥 本
可
试
能
卷
用
满
到
分
的相
10
对
0分
原子
。考
质
试
量
时
:H
间
-
7
1
5 分
C-
钟
1
。
2 N-14 0-16 Na—23 A1-27 Cl-35。 5
:
C.
霸
X和
,
z
晷
的最高
J
价
宣
氧
I
化
2价
物对
,
应
z显
水化
+7
物
价
均为 强 酸
[∶ I 〉 x 〈 l l
L
l
·
+II) ' z ′ JY Y ` `J ) z 《 |Jl
」
ˉ [I)x〈 lll+
划 舯 抑 Ca-40 Cr—52 C0—59 D.W、Ⅹ、 Y三 种元素形成的化合物可能是离子晶体
■ 脚
-、选择题:本题共14小题,每小题3分
,共
42分。在每小题给出的四个选项中,只有一项符合题目
7.根据下列实验操作和实验现象,得出的结论正确的是
选项 实验操作 实验现象 结论
要求。
K
将乙醇和浓硫酸的混合液加热,并将产生的气体直
1.传统文化中蕴含着许多化学知识。下列说法错误的是 A 溶液橙黄色褪去 产生的气体是乙烯
接通人溴水中
A。 《天工开物》中记载 :“ 凡煎卤未即凝结,将皂角椎碎,和粟米糠二味,卤沸之时投人其中搅和 向2一 溴丙烷和 NaoH溶 液反应后的溶液中加入
,
慰
岬 逻 盐即顷刻结成。 ” 其中涉及渗析 B AgN03溶 液 有沉淀生成 2一 溴丙烷中含有溴原子
■ 群 B。 《 “ 南村辍耕录》中 ” 记载 :“ 削松木为小片,其薄如纸,铬 (熔)硫黄涂木片顶分许,名 曰发烛 …… ” C 利用稀硫酸和镁条反应产生氢气的原理测气体摩尔 观察到装置漏气 测得气体摩尔体积的数值偏小
削松木为小片 有助于燃烧 体积
S
C。
《太平御览》中记载
:“
山公时一醉,遥造高阳池。日暮倒载归,酩酊无所知。 ” 酒精在人体内发 D 用 KSCN溶液检验铁发生电化学腐蚀后生成的离子 溶液变红 Fe被 腐蚀生成了Fe3十
生了化学变化 8 用下与 CO反 应,生成苯甲酸酯的机理如图所示,其中一Ph代 表一 C6H5。 下列
郦·攥 D。 《浣溪沙 · 徐州藏春阁园中》中有 :“ 惭愧今年二麦丰,千畦细浪舞晴空。 ” 小麦成熟过程中生成 说法 刀 曰 E
秦
ˉ 2.下列
了
化
多
学
糖
用语表述正确的是
0
H-F
P
d
|
P
-
h^
口
B 广
V
●
l
^
^
n
′ ∷Pd(PPh3)2
Br
OCH3
10)Ph3 HB+Br^
I
A.NaCl的形成过程 :Na/∶ )。i:_Na+[0:]^ B.SO:^的 Ⅴ SEPR模 型 PPh^
CH30H ˇ
|
ˉ Pd—Br
PPh~
斟 邱 C。 2一 甲基戊烷的键线式 :/ˇ| D。 羟基的电子式::0:H P | d - ˇ Br P|Ph3
`
剁 3.栀子苷 (M)是 从栀子的干燥成熟果实中提取的化合物,具有缓泻、镇痛、 0H P|Ph3 ΠⅡ
邯 Co
H
郅 抗炎等作用,其结构简式如图。关于该化合物,下列说法错误的是 C0
肛
KMno4溶
A。 该化合物可使酸性 液褪色 Ⅲ P| d—Br PPh3
·
抻 B.分子中含有 4种 官能团 PPh3 P|Ph3
柙
0H
碉 C。
分子中含有8个手性碳原子
M A。 反应Ⅲ生成物的分子式为 C43H35 0BrP2Pd B。 反应过程中 Pd形 成的化学键数不变
D。 1 mol M分别与足量 H2加成和与足量 Na反 应,最多消耗 n(H2):n(Na)=1:2 C.该反应的催化剂为 Pd(PPh3)2 D.反 应过程中没有非极性共价键的断裂
化学猜题卷(三) 江西卷 第1页(共8页 化学猜题卷(三) 江西卷 第2页(共8页
) )9.某学科小组取少量新制 Feso4溶液进行如图实验。下列说法错误的是
0 7 542 0 5 045
足量H202溶液 P
现象Ⅲ
/
5滴 KSCN溶 液 少量 H202溶液
步骤Ⅲ
/
FeS04溶液 现象 I(不明显 现象Ⅱ
步骤 I ) 步骤Ⅱ KCl固体 a Q
现象Ⅳ
步骤Ⅳ 〃
〃
A。
步骤Ⅱ发生反应2Fe2++3H202+2H+===2Fe3++02↑ +4H20 ^
U 2025 40 60 80 J/Inin
B。
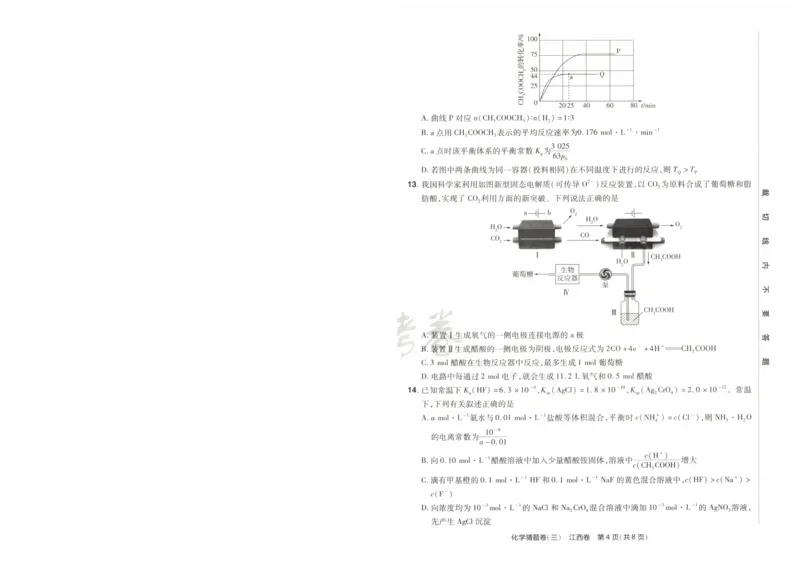
步骤Ⅲ中溶液红色褪去,可能的原因是H202将 SCN^氧化 A。 曲线PX寸应 n(cH3C00CH3):n(H2)=1:3
C。
步骤Ⅲ产生气泡的原因之一是Fe3+催化H202分解
B。
a点用CH3C00CH3表示的平均反应速率为0.176 mol· L^1 o minˉ 1
D。
步骤Ⅳ溶液红色变浅,可能的原因是发生反应Fe3++6Cl^丁=爿
FeC16]3ˉ C.a点时该平衡体系的平衡常数乌为
1商千
10.金属铬用途广泛,可形成配合物 M[Cr(0H)3(H20)(H2NCH2CH2NH2)],也 可组成复合材料。
复合材料氧铬酸钙可用于配制无机防锈颜料,氧铬酸钙的晶胞如图所示。已知A、 B的原子坐标 D。
若图中两条曲线为同一容器(投料相同)在不同温度下进行的反应,则 rQ>rP
13.我 国科学家利用如图新型固态电解质(可传导 02ˉ )反应装置,以 C02为原料合成了葡萄糖和脂
分别为(0,0,0)、 (1,1,0)。 下列说法错误的是 烨
A.基态原子的未成对电子数 :Cr)N>0>H
肪酸,实现了C02利用方面的新突破。下列说法正确的是
B C 。 .1 配 个 合 钙 物 原 M 子 的 与 中 1 心 2个 离 氧 子 原 的 子 配 等 位 距 数 离 为 且 5 最近 ▲ z~1 ● O O C C C 丶 ` r a H20— a叫 卜b /~H20 叫 0 舀
CO
C02~>
% B 燃
D.C的 原子坐标为(去,1,告 A
)
Ⅱ CH3C00H
H20
| △
11.亚硝酰硫酸 (NOS04H)主 要用于重氮化反应。在实验室中,将 二氧化硫通人到浓硫酸和浓硝酸
—
生物
葡萄糖
反应器
的混合液中,在低于20℃条件下发生氧化还原反应制各少量NOS04H(硝酸被还原,二氧化硫被
泵 丬
Ⅳ
氧化,夹持装置略
)。
已知:NOS04H遇水分解,溶于浓硫酸不分解。
CH3C00H
Ⅲ 删
a 搅拌器
A∶ 装置 I生成氧气的一侧电极连接电源的a极 啉
NaOH B。
装置Ⅱ生成醋酸的一侧电极为阴极,电极反应式为2CO+4eˉ +4H+===CH3C00H
冰
水 溶液
C。
3 mol醋酸在生物反应器中反应,最多生成 1m。l葡萄糖 渊
C (含
A 多孔球泡 B 酚酞 )
D。
电路中每通过2m。l电子,就会生成 11.2L氧 气和0.5m。l醋酸
下列说法错误的是 14.已知常温下凡 (HF)=6.3× 10^4,凡p(AgCl)=1.8× 10ˉ 10,Ksp(Ag2 Cro4)=2。 0× 10ˉ 12。 常温
A。 导管 a的 作用是平衡气压 ,保证液体顺利滴下 下,下列有关叙述正确的是
B.装置 B中 多孔球泡的作用为增大反应物接触面积 ,使反应更充分 A。 c mol· Lˉ 1氨 水与 0。 01 molo Lˉ 1盐 酸等体积混合,平衡时c(NH广 )=c(Clˉ ),则 NH3· H20
C。 装置 C主 要用于吸收挥发出的 SO2
的电离常数为
NOS04H的 「为 T
D。 该实验装置可能导致 产量偏高 T1。
12.一定温度下,在容积恒为 1L的 密闭容器中充人总物质的量为2m。l的 CH3C00CH3(g)和 H2(g), B。 向 0。 10 mol· L^1醋酸溶液中加入少量醋酸铵固体,溶液中 了击
:主
茺缶可 增大
CH3C00CH3(g)+2H2(g)(==空 CH30H(g)+C2H50H(g) 1 HF和 1 NaF的
起始体系总压强为PO,发生反应 C.滴有甲基橙的0.1m。 l· Lˉ 0。 1m。 l· Lˉ 黄色混合溶液中,c(HF))c(Na十 ))
ΔⅡ(0。 按 n(cH3C00CH3):尼 (H2)为 1:1、 1:3投料时 CH3C00CH3转 化率随反应时间的变化情 c(F^)
况如图。已知乌 为以平衡分压代替平衡浓度计算得到的平衡常数,分压 =总压 ×物质的量分 D。 向浓度均为 10ˉ 3 mol· Lˉ 1的 Nacl和 Na2 cr04混合溶液中滴加 10^3 mol· L^1的 AgN03溶液
,
数。下列说法错误的是 先产生AgCl沉淀
化学猜题卷(三) 江西卷 第 3页(共8页 化学猜题卷(三) 江西卷 第4页(共8页
) )9.某学科小组取少量新制 Feso4溶液进行如图实验。下列说法错误的是
0 7 542 0 5 045
足量H202溶液 P
现象Ⅲ
/
5滴 KSCN溶 液 少量 H202溶液
步骤Ⅲ
/
FeS04溶液 现象 I(不明显 现象Ⅱ
步骤 I ) 步骤Ⅱ KCl固体 a Q
现象Ⅳ
步骤Ⅳ 〃
〃
A。
步骤Ⅱ发生反应2Fe2++3H202+2H+===2Fe3++02↑ +4H20 ^
U 2025 40 60 80 J/Inin
B。
步骤Ⅲ中溶液红色褪去,可能的原因是H202将 SCN^氧化 A。 曲线PX寸应 n(cH3C00CH3):n(H2)=1:3
C。
步骤Ⅲ产生气泡的原因之一是Fe3+催化H202分解
B。
a点用CH3C00CH3表示的平均反应速率为0.176 mol· L^1 o minˉ 1
D。
步骤Ⅳ溶液红色变浅,可能的原因是发生反应Fe3++6Cl^丁=爿
FeC16]3ˉ C.a点时该平衡体系的平衡常数乌为
1商千
10.金属铬用途广泛,可形成配合物 M[Cr(0H)3(H20)(H2NCH2CH2NH2)],也 可组成复合材料。
复合材料氧铬酸钙可用于配制无机防锈颜料,氧铬酸钙的晶胞如图所示。已知A、 B的原子坐标 D。
若图中两条曲线为同一容器(投料相同)在不同温度下进行的反应,则 rQ>rP
13.我 国科学家利用如图新型固态电解质(可传导 02ˉ )反应装置,以 C02为原料合成了葡萄糖和脂
分别为(0,0,0)、 (1,1,0)。 下列说法错误的是 烨
A.基态原子的未成对电子数 :Cr)N>0>H
肪酸,实现了C02利用方面的新突破。下列说法正确的是
B C 。 .1 配 个 合 钙 物 原 M 子 的 与 中 1 心 2个 离 氧 子 原 的 子 配 等 位 距 数 离 为 且 5 最近 ▲ z~1 ● O O C C C 丶 ` r a H20— a叫 卜b /~H20 叫 0 舀
CO
C02~>
% B 燃
D.C的 原子坐标为(去,1,告 A
)
Ⅱ CH3C00H
H20
| △
11.亚硝酰硫酸 (NOS04H)主 要用于重氮化反应。在实验室中,将 二氧化硫通人到浓硫酸和浓硝酸
—
生物
葡萄糖
反应器
的混合液中,在低于20℃条件下发生氧化还原反应制各少量NOS04H(硝酸被还原,二氧化硫被
泵 丬
Ⅳ
氧化,夹持装置略
)。
已知:NOS04H遇水分解,溶于浓硫酸不分解。
CH3C00H
Ⅲ 删
a 搅拌器
A∶ 装置 I生成氧气的一侧电极连接电源的a极 啉
NaOH B。
装置Ⅱ生成醋酸的一侧电极为阴极,电极反应式为2CO+4eˉ +4H+===CH3C00H
冰
水 溶液
C。
3 mol醋酸在生物反应器中反应,最多生成 1m。l葡萄糖 渊
C (含
A 多孔球泡 B 酚酞 )
D。
电路中每通过2m。l电子,就会生成 11.2L氧 气和0.5m。l醋酸
下列说法错误的是 14.已知常温下凡 (HF)=6.3× 10^4,凡p(AgCl)=1.8× 10ˉ 10,Ksp(Ag2 Cro4)=2。 0× 10ˉ 12。 常温
A。 导管 a的 作用是平衡气压 ,保证液体顺利滴下 下,下列有关叙述正确的是
B.装置 B中 多孔球泡的作用为增大反应物接触面积 ,使反应更充分 A。 c mol· Lˉ 1氨 水与 0。 01 molo Lˉ 1盐 酸等体积混合,平衡时c(NH广 )=c(Clˉ ),则 NH3· H20
C。 装置 C主 要用于吸收挥发出的 SO2
的电离常数为
NOS04H的 「为 T
D。 该实验装置可能导致 产量偏高 T1。
12.一定温度下,在容积恒为 1L的 密闭容器中充人总物质的量为2m。l的 CH3C00CH3(g)和 H2(g), B。 向 0。 10 mol· L^1醋酸溶液中加入少量醋酸铵固体,溶液中 了击
:主
茺缶可 增大
CH3C00CH3(g)+2H2(g)(==空 CH30H(g)+C2H50H(g) 1 HF和 1 NaF的
起始体系总压强为PO,发生反应 C.滴有甲基橙的0.1m。 l· Lˉ 0。 1m。 l· Lˉ 黄色混合溶液中,c(HF))c(Na十 ))
ΔⅡ(0。 按 n(cH3C00CH3):尼 (H2)为 1:1、 1:3投料时 CH3C00CH3转 化率随反应时间的变化情 c(F^)
况如图。已知乌 为以平衡分压代替平衡浓度计算得到的平衡常数,分压 =总压 ×物质的量分 D。 向浓度均为 10ˉ 3 mol· Lˉ 1的 Nacl和 Na2 cr04混合溶液中滴加 10^3 mol· L^1的 AgN03溶液
,
数。下列说法错误的是 先产生AgCl沉淀
化学猜题卷(三) 江西卷 第 3页(共8页 化学猜题卷(三) 江西卷 第4页(共8页
) )(6)有效氯含量是指每克含氯消毒剂的氧化能力相当于多少克
C12的氧化能力,可用来衡量含氯
(三
化学猜题卷 )边择题答题区
消毒剂的消毒能力 ,C102、NaC102、NaC10作为消毒剂,还原产物均为 Cl^,则这三种消毒剂的
题号 1 2 n u 4 5 ^ 0 7 得分 有效氯含量由大到小的顺序为
答案 16。 (14分 )氧化亚钴 (Co0)常 用于电磁、颜料、半导体及镍氢、镍镉电池正极材料等工业。利用铜
题号 n ˇ 0 ˇ 10 11 12 13 14
铁钴合金渣制备的酸性电解造液(含大量 Co2+及少量的Fe2+、 Cu2+、Ca2+、Mg2+、Ni2+杂质)为原
答案
■
料制备 Co0的工艺流程如图
二、非选择题:本题共 4小 题,共 58分。 :
N N%C03N%S203 NaF NaC10
15.(15分 )C102是一种易溶于水而难溶于有机溶剂的气体,是 一种广谱消毒剂。某小组同学先制
酸性电
N%C03和NaoH
取干燥纯净的C12,再用 Nac1o2固体与C12反应,制取和收集较纯净的C102,装置如图所示(部分 解造液
夹持装置省略 Cu 草酸铵
)。
黄钠铁矾
盐酸
a Co0 04· 2H20 沉钴
同
浓盐酸
巾
N 已知:①酸性条件下 ,三价Co可将Cl^氧化为C12;黄钠铁矾化学式为Na2Fe6(S04)4(0H)12;
划 如 吸
铷
收装置 ②常温下 ,相关物质的凡p如 表所示。
D
脚 物质 Co(0H)3 Co(0H)2 Ni(0H)2 CaF2 MgF2
KMn0
K
A B C E / 1.6× 10^仍 6。 3× 10ˉ15 5。 5x10ˉ 16 5.3× 10ˉ 9 9.0× 10ˉ11
F G
回答下列问题
回答下列问题
:
:
● 、
J
nrHK 逻 (1)装置 A烧 瓶内发生反应的离子方程式为 (1)基态钴原子的价电子排布式为
罩
■ 郴
装置 B中试剂的作用是
(2)‘:除铁
”
时 ,加 入Nac1o3的 作用为
(2)NaC102固体与 C12反应制各 C102的微观过程如图所示(忽略半径大小 ”
)。 (3)∶:球铜 时 ,发 生反应的离子方程式为
不 ●
d∩ 犭 ●黪 (4)常温下-加人足量NaF可除去Ca2+和 Mg2+,当 两者完全沉淀时溶液中F^浓度至少为
惑t· ˉ 攥
“:+∞
犭 '` + ●黠 (离子浓度≤ 1。 0× 10ˉ 5 mol· Lˉ 1时 认为该离子沉淀完全 )。
苦H丶 ”
(5)“ 沉钴 前加人盐酸的目的为
黠表示原子的基态原子的电子排布式为
,●
表示原子的基态原子的
”
(6)“ 沉钴 时,不使用饱和草酸钠溶液的原因是
最外层电子的电子云伸展方向有 种。
(3)装置E中 的试剂可以是 (填 标号
(7)空气氛围下加热CoC204· 2H20固体样品时,其分解过程分3个阶段,对应温度范围和失重
)。
A。 苯 B。 CC14 C.Na0H溶 液 D。 NaCl溶 液 率(失重率 =2土 上匣」 量 ×100%)如表所示
号 ;;景:;;曹::言;:i;;言 餍营 0L匝 :
(4)装 置 F为 C102收集装置,可以选用的装置是 (填序号
)。
驯 热分解阶段 Ⅲ≡
甾
邱 热分解温度/℃ 150~210 290~320 890~920
肛
水
抑
· 失重率 /% 19.67 36.43
2。
91
① ② ③
柙
碉 (5)C102稳定性差,因此常将制得的C102通入 H202和 NaoH的 混合溶液中,使之转化成 Nac1o2, 第ii阶段生成一种固体氧化物和两种气体,该阶段反应的化学方程式为
以便于储存。上述过程发生反应的离子方程式是
化学猜题卷(三) 江西卷 第 5页(共 8页 ) 化学猜题卷(三) 江西卷 第 6页(共 8页 )(6)有效氯含量是指每克含氯消毒剂的氧化能力相当于多少克
C12的氧化能力,可用来衡量含氯
(三
化学猜题卷 )边择题答题区
消毒剂的消毒能力 ,C102、NaC102、NaC10作为消毒剂,还原产物均为 Cl^,则这三种消毒剂的
题号 1 2 n u 4 5 ^ 0 7 得分 有效氯含量由大到小的顺序为
答案 16。 (14分 )氧化亚钴 (Co0)常 用于电磁、颜料、半导体及镍氢、镍镉电池正极材料等工业。利用铜
题号 n ˇ 0 ˇ 10 11 12 13 14
铁钴合金渣制备的酸性电解造液(含大量 Co2+及少量的Fe2+、 Cu2+、Ca2+、Mg2+、Ni2+杂质)为原
答案
■
料制备 Co0的工艺流程如图
二、非选择题:本题共 4小 题,共 58分。 :
N N%C03N%S203 NaF NaC10
15.(15分 )C102是一种易溶于水而难溶于有机溶剂的气体,是 一种广谱消毒剂。某小组同学先制
酸性电
N%C03和NaoH
取干燥纯净的C12,再用 Nac1o2固体与C12反应,制取和收集较纯净的C102,装置如图所示(部分 解造液
夹持装置省略 Cu 草酸铵
)。
黄钠铁矾
盐酸
a Co0 04· 2H20 沉钴
同
浓盐酸
巾
N 已知:①酸性条件下 ,三价Co可将Cl^氧化为C12;黄钠铁矾化学式为Na2Fe6(S04)4(0H)12;
划 如 吸
铷
收装置 ②常温下 ,相关物质的凡p如 表所示。
D
脚 物质 Co(0H)3 Co(0H)2 Ni(0H)2 CaF2 MgF2
KMn0
K
A B C E / 1.6× 10^仍 6。 3× 10ˉ15 5。 5x10ˉ 16 5.3× 10ˉ 9 9.0× 10ˉ11
F G
回答下列问题
回答下列问题
:
:
● 、
J
nrHK 逻 (1)装置 A烧 瓶内发生反应的离子方程式为 (1)基态钴原子的价电子排布式为
罩
■ 郴
装置 B中试剂的作用是
(2)‘:除铁
”
时 ,加 入Nac1o3的 作用为
(2)NaC102固体与 C12反应制各 C102的微观过程如图所示(忽略半径大小 ”
)。 (3)∶:球铜 时 ,发 生反应的离子方程式为
不 ●
d∩ 犭 ●黪 (4)常温下-加人足量NaF可除去Ca2+和 Mg2+,当 两者完全沉淀时溶液中F^浓度至少为
惑t· ˉ 攥
“:+∞
犭 '` + ●黠 (离子浓度≤ 1。 0× 10ˉ 5 mol· Lˉ 1时 认为该离子沉淀完全 )。
苦H丶 ”
(5)“ 沉钴 前加人盐酸的目的为
黠表示原子的基态原子的电子排布式为
,●
表示原子的基态原子的
”
(6)“ 沉钴 时,不使用饱和草酸钠溶液的原因是
最外层电子的电子云伸展方向有 种。
(3)装置E中 的试剂可以是 (填 标号
(7)空气氛围下加热CoC204· 2H20固体样品时,其分解过程分3个阶段,对应温度范围和失重
)。
A。 苯 B。 CC14 C.Na0H溶 液 D。 NaCl溶 液 率(失重率 =2土 上匣」 量 ×100%)如表所示
号 ;;景:;;曹::言;:i;;言 餍营 0L匝 :
(4)装 置 F为 C102收集装置,可以选用的装置是 (填序号
)。
驯 热分解阶段 Ⅲ≡
甾
邱 热分解温度/℃ 150~210 290~320 890~920
肛
水
抑
· 失重率 /% 19.67 36.43
2。
91
① ② ③
柙
碉 (5)C102稳定性差,因此常将制得的C102通入 H202和 NaoH的 混合溶液中,使之转化成 Nac1o2, 第ii阶段生成一种固体氧化物和两种气体,该阶段反应的化学方程式为
以便于储存。上述过程发生反应的离子方程式是
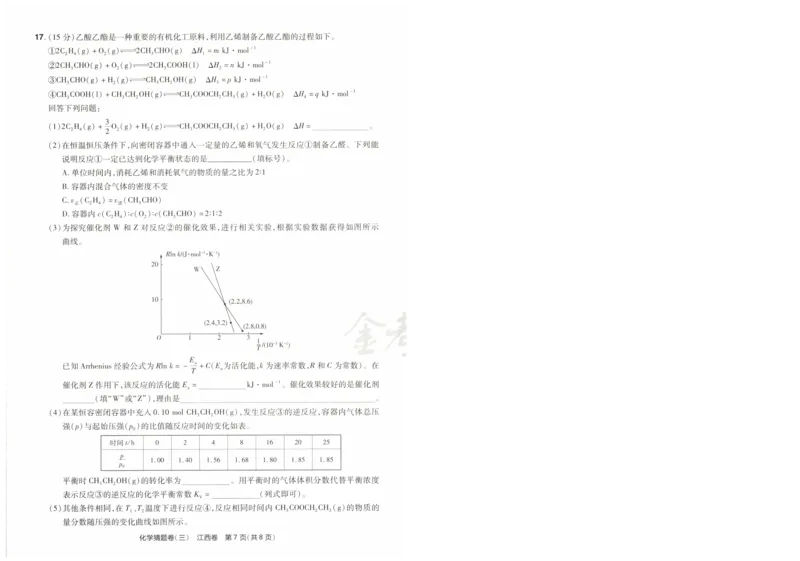
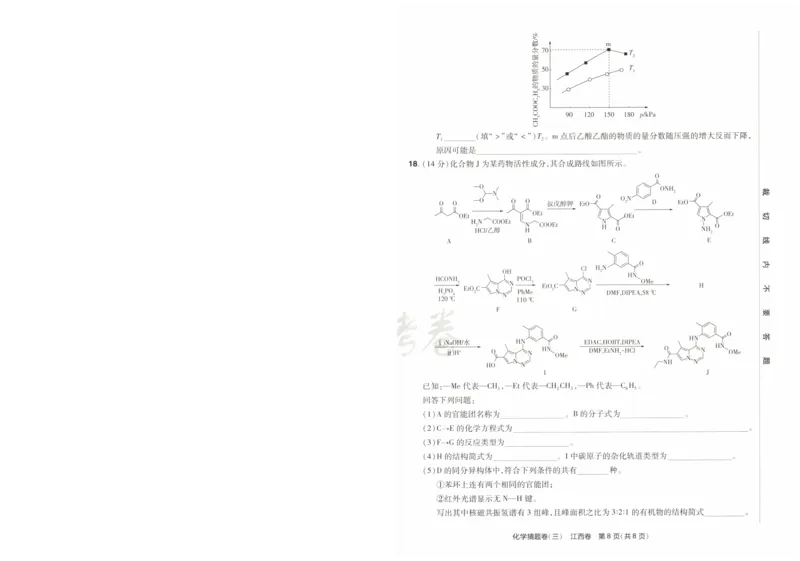
化学猜题卷(三) 江西卷 第 5页(共 8页 ) 化学猜题卷(三) 江西卷 第 6页(共 8页 )17.(15分 )乙酸乙酯是一种重要 的有机化工原料 ,利用 乙烯制备乙酸乙酯 的过程如下 。 s `
热
① 2C2H4(g)+02(g)==空 2CH3CH0(g) ΔⅡ1=阴 kJ o mol^1 心
酬
7` 'D nv nυ Πl %
② 2CH3CH0(g)+02(g)丁=空 2CH3C00H(l) ΔⅡ2=n kJ o molˉ 1 g 烬 T ˉ
③ CH3CH0(g)+H2(g)了=主 CH3CH20H(g) ΔⅡ3=p kJ o molˉ 1 彝 ^u
1
g
④ CH3C00H(1)+CH3CH20H(g)了=土 CH3C00CH2CH3(g)+H20(g) ΔⅡ4=g kJ· molˉ 1 ∽ ` 0 j一
o
o
υ
回答下列问题
: 90 120 150 180 P/kPa
m〓
(1)2C2H4(g)·+;02(g)+H2(g)丁
===主
CH3C00CH2CH3(g)+H20(g) Δ万= ハ
(2)在恒温恒压条件下
,向
密闭容器中通入一定量的乙烯和氧气发生反应①制备乙醛。下列能 甲工 1 (填 “ >”或 “ (” )r2。 m点 后乙酸乙酯的物质的量分数随压强的增大反而下降 ,
原因可能是
(填
说明反应①一定已达到化学平衡状态的是 标号
)。 18.(14分 )化合物J为某药物活性成分,其合成路线如图所示。
A。
单位时间内,消 耗乙烯和消耗氧气的物质的量之比为2:1
0
B.容器内混合气体的密度不变
/Ν ONH2 擀
(C2H4)=v逆 (CH3CH0) \ 0 02N
C· v正 0 O 叔戊醇钾 EtO D Eto
D.容 器 内 c(C2H4):c(02):c(CH3CH0)=2:1:2 Et 0Et 0Et 舀
H2N/\C00Et
(3)为探究催化剂 W和 Z对 反应②的催化效果,进行相关实验,根据实验数据获得如图所示 C00Et H NlH2
HC1/乙醇 Η
曲线。 A B C E 燃
Rln凡 /(J· mo1^1·K^1)
20 △
W Z Cl H2N
HCoNH2 POC13
EtO2C 丬
H3P04 tU2· PhMe DMF,DIPEA,58℃
10 120℃ 110℃
(⒉2,⒏6)
F G Ⅲ
(2.4,302)
8)
啉
0 0
÷ /(10-3K-) i)NaOH/7怅 EDAC,HOBT,DIPEA
DMF”EtNH。 ·HCl
ii)H+
已知 AⅡhenius经验公式为Rln凡 =一 丁 口 +C(Ea为 活化能 ,儿 为速率常数,R和 C为 常数 )。 在 HO / 厂 NH 渊
I J
催化剂 Z作 用下,该反应的活化能 Ea= kJ o molˉ1。 催化效果较好的是催化剂 已 知 :— Me代 表 一 CH3,一Et代 表 一 CH2CH3,— Ph代 表 一 C6H5。
“ “
~(填
W”或 z” ),理由是 回答下列问题
:
(4)在某恒容密闭容器中充入 0。 10 mol CH3CH20H(g),发 生反应③的逆反应,容器内气体总压 (1)A的 官能团名称为 。B的 分子式为
强(p)与起始压强(P。 )的 比值随反应时间的变化如表。 (2)C→E的化学方程式为
时间J/h 0 2 4 16 20 25 (3)F→G的 反应类型为
(4)H的 结构简式为 。I中碳原子的杂化轨道类型为
且 00 1.40 1.56 1.68 1.80 1.85 1.85
1。
Po
(5)D的 同分异构体中,符合下列条件的共有 种。
平衡时CH3CH20H(g)的转化率为 。用平衡时的气体体积分数代替平衡浓度
①苯环上连有两个相同的官能团
= (列 ;
表示反应③的逆反应的化学平衡常数ΚⅤ 式即可 N-H键
)。 ②红外光谱显示无 。
(5)其他条件相同,在
r1、
r2温度下进行反应④,反应相同时间内CH3C00CH2CH3(g)的 物质的
写出其中核磁共振氢谱有3组峰,且峰面积之比为3:2:1的有机物的结构简式
量分数随压强的变化曲线如图所示。
化学猜题卷(三) 江西卷 第 7页(共8页 ) 化学猜题卷(三) 江西卷 第 8页(共 8页 )17.(15分 )乙酸乙酯是一种重要 的有机化工原料 ,利用 乙烯制备乙酸乙酯 的过程如下 。 s `
热
① 2C2H4(g)+02(g)==空 2CH3CH0(g) ΔⅡ1=阴 kJ o mol^1 心
酬
7` 'D nv nυ Πl %
② 2CH3CH0(g)+02(g)丁=空 2CH3C00H(l) ΔⅡ2=n kJ o molˉ 1 g 烬 T ˉ
③ CH3CH0(g)+H2(g)了=主 CH3CH20H(g) ΔⅡ3=p kJ o molˉ 1 彝 ^u
1
g
④ CH3C00H(1)+CH3CH20H(g)了=土 CH3C00CH2CH3(g)+H20(g) ΔⅡ4=g kJ· molˉ 1 ∽ ` 0 j一
o
o
υ
回答下列问题
: 90 120 150 180 P/kPa
m〓
(1)2C2H4(g)·+;02(g)+H2(g)丁
===主
CH3C00CH2CH3(g)+H20(g) Δ万= ハ
(2)在恒温恒压条件下
,向
密闭容器中通入一定量的乙烯和氧气发生反应①制备乙醛。下列能 甲工 1 (填 “ >”或 “ (” )r2。 m点 后乙酸乙酯的物质的量分数随压强的增大反而下降 ,
原因可能是
(填
说明反应①一定已达到化学平衡状态的是 标号
)。 18.(14分 )化合物J为某药物活性成分,其合成路线如图所示。
A。
单位时间内,消 耗乙烯和消耗氧气的物质的量之比为2:1
0
B.容器内混合气体的密度不变
/Ν ONH2 擀
(C2H4)=v逆 (CH3CH0) \ 0 02N
C· v正 0 O 叔戊醇钾 EtO D Eto
D.容 器 内 c(C2H4):c(02):c(CH3CH0)=2:1:2 Et 0Et 0Et 舀
H2N/\C00Et
(3)为探究催化剂 W和 Z对 反应②的催化效果,进行相关实验,根据实验数据获得如图所示 C00Et H NlH2
HC1/乙醇 Η
曲线。 A B C E 燃
Rln凡 /(J· mo1^1·K^1)
20 △
W Z Cl H2N
HCoNH2 POC13
EtO2C 丬
H3P04 tU2· PhMe DMF,DIPEA,58℃
10 120℃ 110℃
(⒉2,⒏6)
F G Ⅲ
(2.4,302)
8)
啉
0 0
÷ /(10-3K-) i)NaOH/7怅 EDAC,HOBT,DIPEA
DMF”EtNH。 ·HCl
ii)H+
已知 AⅡhenius经验公式为Rln凡 =一 丁 口 +C(Ea为 活化能 ,儿 为速率常数,R和 C为 常数 )。 在 HO / 厂 NH 渊
I J
催化剂 Z作 用下,该反应的活化能 Ea= kJ o molˉ1。 催化效果较好的是催化剂 已 知 :— Me代 表 一 CH3,一Et代 表 一 CH2CH3,— Ph代 表 一 C6H5。
“ “
~(填
W”或 z” ),理由是 回答下列问题
:
(4)在某恒容密闭容器中充入 0。 10 mol CH3CH20H(g),发 生反应③的逆反应,容器内气体总压 (1)A的 官能团名称为 。B的 分子式为
强(p)与起始压强(P。 )的 比值随反应时间的变化如表。 (2)C→E的化学方程式为
时间J/h 0 2 4 16 20 25 (3)F→G的 反应类型为
(4)H的 结构简式为 。I中碳原子的杂化轨道类型为
且 00 1.40 1.56 1.68 1.80 1.85 1.85
1。
Po
(5)D的 同分异构体中,符合下列条件的共有 种。
平衡时CH3CH20H(g)的转化率为 。用平衡时的气体体积分数代替平衡浓度
①苯环上连有两个相同的官能团
= (列 ;
表示反应③的逆反应的化学平衡常数ΚⅤ 式即可 N-H键
)。 ②红外光谱显示无 。
(5)其他条件相同,在
r1、
r2温度下进行反应④,反应相同时间内CH3C00CH2CH3(g)的 物质的
写出其中核磁共振氢谱有3组峰,且峰面积之比为3:2:1的有机物的结构简式
量分数随压强的变化曲线如图所示。
化学猜题卷(三) 江西卷 第 7页(共8页 ) 化学猜题卷(三) 江西卷 第 8页(共 8页 )绝密★启用前 B.A1203是过渡晶体,可当作共价晶体处理
:0>C)Nb>Al
元素的电负性
2024年 C。
江西省 普通高 中学业水平选择性考试
D。
若消耗等质量的铝粉和焦炭,则方法 I中转移电子数更多
“ ”
化学猜题卷 (四 5.实验室模拟 侯氏制碱法 的过程主要包括:①粗盐(含有Ca2+、Mg2+、s0i^等杂质离子)提纯
) ;
②结晶沉淀 过滤洗涤 高温分解。下列说法错误的是
;③ ;④
目 命题报告
■ A。
粗盐提纯过程中,可以依次加入 Bac12溶液、 NaoH溶 液、Na2c03溶液及盐酸进行除杂
本套试卷整体符合江西省新高考化学试题结构,题 目新颖,原创度高,重 点考查考生在真实、复杂情境中解决问题的
B。
结晶沉淀时,应先向饱和食盐水中通人足量 C02,再通人 NH3
能力,强调学科理解在中学化学学习中的重要性。
|命 题新思维:第 5题 以我国化学史重要工艺发明 “ 侯氏制碱法 ” 为背景,渗透化学学科思想,考查对物质分离提纯的 C。 过滤洗涤时用到的玻璃仪器有漏斗、烧杯和玻璃棒
理解与应用,对考生的实验动手能力、理解分析能力要求较高。第10题 以微工艺流程题的形式,以 小见大,在真实复
D。
高温分解利用了NaHco3不稳定、受热易分解的性质
杂情境中考查考生快速提取分析框图及文本信息、整合有效信息以及应用已有知识的能力。
命题加强综合性:第 3题综合考查 “ 绿色化学 ” 、晶体类型、电负性,第 10题综合考查氧化还原反应、分子结构,第 16 6。
在碱性溶液中,Cu2+可与缩二脲形成紫色配离子,结构如图所示。下列说法错误的是
题综合考查流程分析和晶胞投影图,第 18题综合考查有机合成路线分析和杂化方式,均体现了高考题的综合性考查 A。 基态 Cu原子的价电子排布式为3d104s1 2-
Η
巾 ˉ 唰 i 要 命 求 题 ,有 新 利 形 于 式 促 :图 进考 文 生 并 全 茂 面 ,信 掌 息 握 呈 化 现 学 形 知 式 识 多 并 样 灵 。 活 本 应 套 用 试 。 卷图表较多,且形式各不相同,有 一定的开放性和灵活性,对考 B。 该配离子与水分子之间形成的氢键有 2种 0原 ΗN ` Ν 而 、 H \ G ′ 0 吕 ` / C H 曲 /u N — 《 NH
剁 洳 生的分析与推测能力、探究与创新能力要求较高。 C。 该配离子中铜离子提供的空轨道和N、 子提供的孤电子对形成 ∥ 一
o 0
舯 配位键
本试卷满分 100分。考试时间75分 钟。
C(H(0C)Nb>Al
元素的电负性
2024年 C。
江西省 普通高 中学业水平选择性考试
D。
若消耗等质量的铝粉和焦炭,则方法 I中转移电子数更多
“ ”
化学猜题卷 (四 5.实验室模拟 侯氏制碱法 的过程主要包括:①粗盐(含有Ca2+、Mg2+、s0i^等杂质离子)提纯
) ;
②结晶沉淀 过滤洗涤 高温分解。下列说法错误的是
;③ ;④
目 命题报告
■ A。
粗盐提纯过程中,可以依次加入 Bac12溶液、 NaoH溶 液、Na2c03溶液及盐酸进行除杂
本套试卷整体符合江西省新高考化学试题结构,题 目新颖,原创度高,重 点考查考生在真实、复杂情境中解决问题的
B。
结晶沉淀时,应先向饱和食盐水中通人足量 C02,再通人 NH3
能力,强调学科理解在中学化学学习中的重要性。
|命 题新思维:第 5题 以我国化学史重要工艺发明 “ 侯氏制碱法 ” 为背景,渗透化学学科思想,考查对物质分离提纯的 C。 过滤洗涤时用到的玻璃仪器有漏斗、烧杯和玻璃棒
理解与应用,对考生的实验动手能力、理解分析能力要求较高。第10题 以微工艺流程题的形式,以 小见大,在真实复
D。
高温分解利用了NaHco3不稳定、受热易分解的性质
杂情境中考查考生快速提取分析框图及文本信息、整合有效信息以及应用已有知识的能力。
命题加强综合性:第 3题综合考查 “ 绿色化学 ” 、晶体类型、电负性,第 10题综合考查氧化还原反应、分子结构,第 16 6。
在碱性溶液中,Cu2+可与缩二脲形成紫色配离子,结构如图所示。下列说法错误的是
题综合考查流程分析和晶胞投影图,第 18题综合考查有机合成路线分析和杂化方式,均体现了高考题的综合性考查 A。 基态 Cu原子的价电子排布式为3d104s1 2-
Η
巾 ˉ 唰 i 要 命 求 题 ,有 新 利 形 于 式 促 :图 进考 文 生 并 全 茂 面 ,信 掌 息 握 呈 化 现 学 形 知 式 识 多 并 样 灵 。 活 本 应 套 用 试 。 卷图表较多,且形式各不相同,有 一定的开放性和灵活性,对考 B。 该配离子与水分子之间形成的氢键有 2种 0原 ΗN ` Ν 而 、 H \ G ′ 0 吕 ` / C H 曲 /u N — 《 NH
剁 洳 生的分析与推测能力、探究与创新能力要求较高。 C。 该配离子中铜离子提供的空轨道和N、 子提供的孤电子对形成 ∥ 一
o 0
舯 配位键
本试卷满分 100分。考试时间75分 钟。
C(H(0”
“
<” 或
P2
P1
⌒ P。 压强
L ハ “ -。 ” ' 、 0 图2
E· ^。
● Z~t 46
由ˇ 1 ▲ ②压强超过P2,%(NH3)突然大幅度下降的原因是
41
古N2(g)1。 33 NH3(g)
. l
259
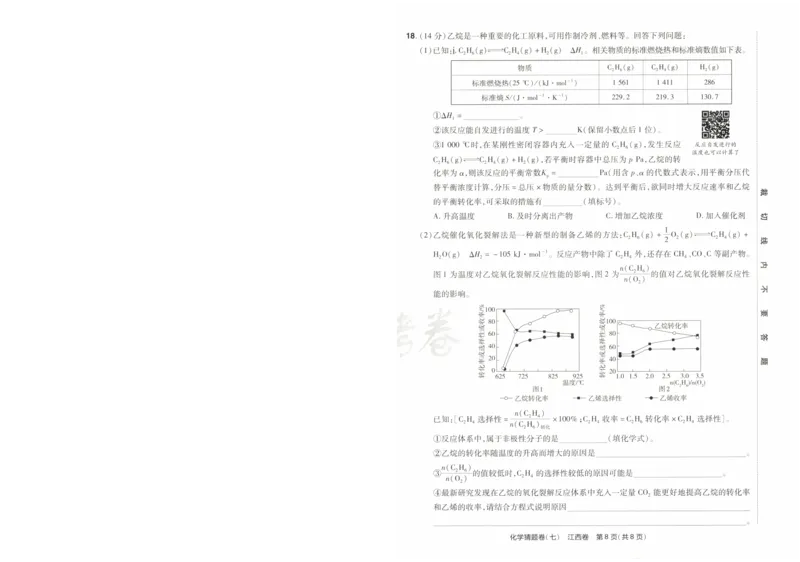
÷ ^Hˇ” (g)飞 + Νˉ扩 M . d⒈ 2+# |NH: 18.(15分 )维生素 B6(G)的一种合成路线如下。回答下列问题 :
和 2+ H
: r
N·+3H+
0
H3C 0
反应历程 H3C 00H C2H50H/HCl OC2H5 0HCNH2 P205/CHC13 H( 丿 C。 乙 \ ^
图1
NH2 NH2· HCl L.ρ 厂 擀
n3△ ^ .N′
写出上述反应条件下,生成 2m。l氨气的热化学方程式 A B `
D
舀
0
(2)科 研小组乙在催化剂作用下合成氨,反应速率 v〓 凡cc(N2)c3(H2)cm(NH3)(凡 为速率常数 /=\ 0H
, ( 9 CH。
I ~
只与温度有关。c、3、 m为 反应级数,可取正整数、负整数 、0,也可取分数 )。 为了测定反应级 0ˇ 0 H5C20 0 Ho H0 、ˇ ˇ cH2oH 燃
'八
H3C N H3C N H3C /^、 N冫'
数 ,在一定温度下进行实验 ,其结果如表(而 ≠0)。 E F G △
序号 c(N2)/(m。 l· Lˉ 1) c(H2)/(m。 l· Lˉ 1) c(NH3)/(m。 1· Lˉ 1) 反应速率 0 0
‖ 丬
‖
已知 : R1-C—NH2+R2—NH2· HCl—→ R2-NH—C—R1+NH4Cl。
`1
Ⅱ n 2尼
Ⅱ z Ⅲ
Ⅲ 4 8而 (1)A分 子中氧原子的杂化方式为 ,A发生缩聚反应生成的高分子化合物的
Ⅳ 4 Z∩ 4尼
啉
结构简式为
贝刂反应总级数 已+3+税 = 。
(2)B→C的 反应类型为 ,G的分子式为 渊
(3)科研小组丙、丁研究不同反应条件下的合成氨反应中平衡体系中氨气含量,所得数据如表。
(3)C→D的
化学方程式为
科研小组 压强/(105 Pa) 温度/℃ 平衡混合气体中 NH3所 占体积分数
(4)用 冰标出 E中 的手性碳原子
丙 100 600 C%
200 400 b% (5)F的 同分异构体中满足下列条件的有 种,其中核磁共振氢谱显示有 6组 峰,且峰面
丁
①实验数据表明G(3,从理论上解释 c<3的 原因 积之比为 1∶ 2:2:2:2:2的结构简式为
①能与Fec13溶液发生显色反应
②已知平衡时某气体分压与 100 kPa的 比值为该气体的相对平衡分压 ,用 各气体相对平衡 ;
分压表示的平衡常数即为相对分压平衡常数凡。若研究小组丁以物质的量之比为1:3通入
②碱性水解后酸化,产物中有α一氨基酸。
= (写
氮气和氢气,则 耳 出计算表达式),通过实验条件分析比
(T) “ “ “
较凡 耳 (丙)(填 )” (”或 =” )。
化学猜题卷(四 ) 江西卷 第7页(共 8页 化学猜题卷(四 ) 江西卷 第8页(共 8页
) )17.(14分 )氨是一种重要的化工原料,德国化学家
F。
Haber提出以氮气和氢气为原料合成氨,奠定 (4)科研小组戊用计算机模拟合成氨工艺,选择合适的催化 为(NH3)
了合成氨的理论基础,之后科学家们对合成氨反应进行了一系列的相关研究。 剂和温度,研究不同压强下从投料开始反应后相同时间
回答下列问题 内混合气体中氨气的体积分数%(NH3),得到图2。
:
(1)一定条件下,科研小组甲用计算机模拟出合成氨反应历程中的能量变化,如图 1所示。
①P0~P1过 程中 ,v正 v逆 (填
“
>”
“
<” 或
P2
P1
⌒ P。 压强
L ハ “ -。 ” ' 、 0 图2
E· ^。
● Z~t 46
由ˇ 1 ▲ ②压强超过P2,%(NH3)突然大幅度下降的原因是
41
古N2(g)1。 33 NH3(g)
. l
259
÷ ^Hˇ” (g)飞 + Νˉ扩 M . d⒈ 2+# |NH: 18.(15分 )维生素 B6(G)的一种合成路线如下。回答下列问题 :
和 2+ H
: r
N·+3H+
0
H3C 0
反应历程 H3C 00H C2H50H/HCl OC2H5 0HCNH2 P205/CHC13 H( 丿 C。 乙 \ ^
图1
NH2 NH2· HCl L.ρ 厂 擀
n3△ ^ .N′
写出上述反应条件下,生成 2m。l氨气的热化学方程式 A B `
D
舀
0
(2)科 研小组乙在催化剂作用下合成氨,反应速率 v〓 凡cc(N2)c3(H2)cm(NH3)(凡 为速率常数 /=\ 0H
, ( 9 CH。
I ~
只与温度有关。c、3、 m为 反应级数,可取正整数、负整数 、0,也可取分数 )。 为了测定反应级 0ˇ 0 H5C20 0 Ho H0 、ˇ ˇ cH2oH 燃
'八
H3C N H3C N H3C /^、 N冫'
数 ,在一定温度下进行实验 ,其结果如表(而 ≠0)。 E F G △
序号 c(N2)/(m。 l· Lˉ 1) c(H2)/(m。 l· Lˉ 1) c(NH3)/(m。 1· Lˉ 1) 反应速率 0 0
‖ 丬
‖
已知 : R1-C—NH2+R2—NH2· HCl—→ R2-NH—C—R1+NH4Cl。
`1
Ⅱ n 2尼
Ⅱ z Ⅲ
Ⅲ 4 8而 (1)A分 子中氧原子的杂化方式为 ,A发生缩聚反应生成的高分子化合物的
Ⅳ 4 Z∩ 4尼
啉
结构简式为
贝刂反应总级数 已+3+税 = 。
(2)B→C的 反应类型为 ,G的分子式为 渊
(3)科研小组丙、丁研究不同反应条件下的合成氨反应中平衡体系中氨气含量,所得数据如表。
(3)C→D的
化学方程式为
科研小组 压强/(105 Pa) 温度/℃ 平衡混合气体中 NH3所 占体积分数
(4)用 冰标出 E中 的手性碳原子
丙 100 600 C%
200 400 b% (5)F的 同分异构体中满足下列条件的有 种,其中核磁共振氢谱显示有 6组 峰,且峰面
丁
①实验数据表明G(3,从理论上解释 c<3的 原因 积之比为 1∶ 2:2:2:2:2的结构简式为
①能与Fec13溶液发生显色反应
②已知平衡时某气体分压与 100 kPa的 比值为该气体的相对平衡分压 ,用 各气体相对平衡 ;
分压表示的平衡常数即为相对分压平衡常数凡。若研究小组丁以物质的量之比为1:3通入
②碱性水解后酸化,产物中有α一氨基酸。
= (写
氮气和氢气,则 耳 出计算表达式),通过实验条件分析比
(T) “ “ “
较凡 耳 (丙)(填 )” (”或 =” )。
化学猜题卷(四 ) 江西卷 第7页(共 8页 化学猜题卷(四 ) 江西卷 第8页(共 8页
) )绝密★启用前
—
「 Η C
C \
/ H
B.反 一1,4一 聚异戊二烯的结构简式 — /C〓
\
江西省 2024年 普通高 中学业水平选择性考试 —
tΗ
尼
化学猜题卷 (五 C.Fe2+的结构示意图:(3)))少
)
D.中子数为10的氧原子
:1:0
目 命题报告
4.能正确表示下列反应的方程式是
命题人目标:本套试卷结合高考的创新性要求创设情境,结合文献论著命题,试题难度梯度明显,符合新高考命题方
A.向 NaOH溶液中逐滴加人Ca(Hc03)2溶液至沉淀完全:Ca2++HCOf+OH^==CaC03↓ +H20
向,引 导考生夯实基础,把握命题方向,提升基本技能,有利于培养考生的独立思考能力、灵活运用知识解决问题的能力。
· 命题新风向:第 3题是教材中相关概念的延伸,引 导考生回归教材,体现了考教衔接;第 10题是教材中乙酸乙酯的 B.向含有1m。1 FeB△ 和1m。l NaI的溶液中通入2 mo1氯气:2C12+2Br^+2Fe2++2I^===Br2+
制备实验的拓展,创 新性强;第 12题结合晶胞图像通过计算判断元素种类,命题角度与以往不同;第 13题电化学原理 2Fe3++I2+4Cl^
陌生、图像新颖,对考生的读图析图能力、信息提取能力要求较高;第 14题结合物质结构、计算考查离子平衡,综合性
C.用纯碱溶液浸泡锅炉水垢:Caso4(s)+Co:^(aq)==Caco3(s)+sol^(aq)
强;第 15题实验装置、探究过程新颖,有利于培养考生的探究能力、实验创新能力;第 16题融合考查ⅤsEPR模型,试
D.向红色Fe(scN)3溶 液中加人过量铁粉:2Fe3++Fe===3Fe2+
题综合性、应用性强。
唰 「 I ^ ·+ ^~~ I △ I F I △
巾
本试卷满分 100分。考试时间 75分 钟。 r
0
≥ 'GH】 是一种离子液体,可以用于锂离子电池的电解质。下列说法错误的是
划 搀 可能用到的相对原子质量 :H-1 C-12 N-14 0—16 S-32 Cl-35.5 Ⅴ-51 Cr-52 lH3C^哐 lAlC叫
舯
Mn—55 Fe—56 Sb-122 Cs—133
A.离子液体在常温下保持液态与其阴、阳离子体积较大有关
脚 -、选择题:本大题包括 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合
B.该离子液体中阴、阳离子中的化学键类型完全相同
C.该离子液体中 C的 杂化方式有2种
K 题 目要求。
该离子液体中阴离子的空间结构为正四面体
D。
1。
古诗词中蕴含着丰富的化学知识。下列说法错误的是
6. 三角锥形分子 M由 原子序数依次增大的短周期元素 A、 B组 成,其能与水反应生成两种酸 C和
“ ”
岬 逻 A。 白釉青花一火成,花从釉里透分明 ,釉里红创烧于元代景德镇,其呈红色是因为含有氧化亚铜 D,已知 B的 第一电离能高于同周期的相邻元素。下列说法正确的是
慰 “ ”
B。 驱愁知酒力,破睡见茶功 ,茶能提神是因为含有咖啡碱,咖啡碱可溶解在沸水中 A.C和 D都 能完全电离 B.A的 单质可以和水发生歧化反应
ˉ郴 0H 0H C.最高价氧化物对应水化物的酸性 :A)B D.M中 各原子最外层均达到8电子稳定结构
() OH 7. 4一 氯乙酰乙酸乙酯是一种治疗心脑血管疾病的高疗效药中间体。双乙烯酮 (M)法 合成4一 氯乙
” ” “ ” (0H0
尽 C.“ 终朝采绿,不盈一菊
,“
绿 通 慕 ,即荩草,其有效成分荩草素 0
酰乙酸乙酯 (N)的工艺涉及反应方程式如下(Cat.表示催化剂 下列说法错误的是
)。
ˉ — 0 Cl- — 0 C1— CH==C— 0
坐~ 0
郦 韬 | +cl^_£ +HCl +CH3CH20H—Cat. 卜 ‖
l ~
秦
—
是
“
天然高分子化合物
”
CH2
M
— C==0 CH2—
X
C==0 C
X
H2— C==o ClCH2-C-C
N
H2C00C2H5
D。
兰陵美酒郁金香,玉碗盛来琥珀光 ,美酒的香味与羟基、羧基、酯基等基团有关,利用红外光
A。
双乙烯酮中σ键与 π键数目之比为5:1
谱可以区分上述基团 X中 共平面的原子最多有8个
B。
2。 ⅣA为阿伏加德罗常数的值,下列说法正确的是 C.4一 氯乙酰乙酸乙酯能发生氧化、取代、加成、消去反应
督 ˉ A.0.1 mo1· Lˉ 1 NaC104溶 液中带电粒子的数目约为0.2Ⅳ A D。 等量的Ⅹ、4一 氯乙酰乙酸乙酯分别与足量 NaOH溶 液反应,消耗的 NaOH的 量相等
舯 8.下列类比合理的是
B.1 mol甲 醛、乙醛混合气体中含有的碳氢单键数可能为3Ⅳ
剁 A
督 s02中 S和 CS2中 C的 价层电子对数之比为 1:1 A。
NaC10溶液与 C02反应生成NaHco3和 HC10,贝刂Nac10溶液与SO2反应生成NaHso3和 HC10
C。
邱
B。
A1203与 NaoH和 盐酸均能反应,属于两性氧化物,则 Si02与 NaoH和 HF均 能反应,也属于两
肛
D。
电解精炼铜时,阳极质量减少64g,电路中通过0.2ⅣA个电子
性氧化物
·
驷 3.下列化学用语或图示表达正确的是
押 C。
CH4的沸点低于 SiH4的沸点,则 CC14的沸点也低于SiC14的沸点
钥 A。 甲烷的燃烧热为890 kJ o mol^1,则 其燃烧的热化学方程式为:CH4(g)+202(g)===C02(g)+ D.向 AlC13溶 液中加人过量氨水生成 Al(0H)3沉 淀,则 向 Cuc12溶 液中加入过量氨水生成
2H20(g) ΔⅡ=-890 kJ o mol^1 Cu(0H)2沉淀
化学猜题卷 (五 ) 江西卷 第1页(共 8页 化学猜题卷(五 ) 江西卷 第2页(共 8页
) )绝密★启用前
—
「 Η C
C \
/ H
B.反 一1,4一 聚异戊二烯的结构简式 — /C〓
\
江西省 2024年 普通高 中学业水平选择性考试 —
tΗ
尼
化学猜题卷 (五 C.Fe2+的结构示意图:(3)))少
)
D.中子数为10的氧原子
:1:0
目 命题报告
4.能正确表示下列反应的方程式是
命题人目标:本套试卷结合高考的创新性要求创设情境,结合文献论著命题,试题难度梯度明显,符合新高考命题方
A.向 NaOH溶液中逐滴加人Ca(Hc03)2溶液至沉淀完全:Ca2++HCOf+OH^==CaC03↓ +H20
向,引 导考生夯实基础,把握命题方向,提升基本技能,有利于培养考生的独立思考能力、灵活运用知识解决问题的能力。
· 命题新风向:第 3题是教材中相关概念的延伸,引 导考生回归教材,体现了考教衔接;第 10题是教材中乙酸乙酯的 B.向含有1m。1 FeB△ 和1m。l NaI的溶液中通入2 mo1氯气:2C12+2Br^+2Fe2++2I^===Br2+
制备实验的拓展,创 新性强;第 12题结合晶胞图像通过计算判断元素种类,命题角度与以往不同;第 13题电化学原理 2Fe3++I2+4Cl^
陌生、图像新颖,对考生的读图析图能力、信息提取能力要求较高;第 14题结合物质结构、计算考查离子平衡,综合性
C.用纯碱溶液浸泡锅炉水垢:Caso4(s)+Co:^(aq)==Caco3(s)+sol^(aq)
强;第 15题实验装置、探究过程新颖,有利于培养考生的探究能力、实验创新能力;第 16题融合考查ⅤsEPR模型,试
D.向红色Fe(scN)3溶 液中加人过量铁粉:2Fe3++Fe===3Fe2+
题综合性、应用性强。
唰 「 I ^ ·+ ^~~ I △ I F I △
巾
本试卷满分 100分。考试时间 75分 钟。 r
0
≥ 'GH】 是一种离子液体,可以用于锂离子电池的电解质。下列说法错误的是
划 搀 可能用到的相对原子质量 :H-1 C-12 N-14 0—16 S-32 Cl-35.5 Ⅴ-51 Cr-52 lH3C^哐 lAlC叫
舯
Mn—55 Fe—56 Sb-122 Cs—133
A.离子液体在常温下保持液态与其阴、阳离子体积较大有关
脚 -、选择题:本大题包括 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合
B.该离子液体中阴、阳离子中的化学键类型完全相同
C.该离子液体中 C的 杂化方式有2种
K 题 目要求。
该离子液体中阴离子的空间结构为正四面体
D。
1。
古诗词中蕴含着丰富的化学知识。下列说法错误的是
6. 三角锥形分子 M由 原子序数依次增大的短周期元素 A、 B组 成,其能与水反应生成两种酸 C和
“ ”
岬 逻 A。 白釉青花一火成,花从釉里透分明 ,釉里红创烧于元代景德镇,其呈红色是因为含有氧化亚铜 D,已知 B的 第一电离能高于同周期的相邻元素。下列说法正确的是
慰 “ ”
B。 驱愁知酒力,破睡见茶功 ,茶能提神是因为含有咖啡碱,咖啡碱可溶解在沸水中 A.C和 D都 能完全电离 B.A的 单质可以和水发生歧化反应
ˉ郴 0H 0H C.最高价氧化物对应水化物的酸性 :A)B D.M中 各原子最外层均达到8电子稳定结构
() OH 7. 4一 氯乙酰乙酸乙酯是一种治疗心脑血管疾病的高疗效药中间体。双乙烯酮 (M)法 合成4一 氯乙
” ” “ ” (0H0
尽 C.“ 终朝采绿,不盈一菊
,“
绿 通 慕 ,即荩草,其有效成分荩草素 0
酰乙酸乙酯 (N)的工艺涉及反应方程式如下(Cat.表示催化剂 下列说法错误的是
)。
ˉ — 0 Cl- — 0 C1— CH==C— 0
坐~ 0
郦 韬 | +cl^_£ +HCl +CH3CH20H—Cat. 卜 ‖
l ~
秦
—
是
“
天然高分子化合物
”
CH2
M
— C==0 CH2—
X
C==0 C
X
H2— C==o ClCH2-C-C
N
H2C00C2H5
D。
兰陵美酒郁金香,玉碗盛来琥珀光 ,美酒的香味与羟基、羧基、酯基等基团有关,利用红外光
A。
双乙烯酮中σ键与 π键数目之比为5:1
谱可以区分上述基团 X中 共平面的原子最多有8个
B。
2。 ⅣA为阿伏加德罗常数的值,下列说法正确的是 C.4一 氯乙酰乙酸乙酯能发生氧化、取代、加成、消去反应
督 ˉ A.0.1 mo1· Lˉ 1 NaC104溶 液中带电粒子的数目约为0.2Ⅳ A D。 等量的Ⅹ、4一 氯乙酰乙酸乙酯分别与足量 NaOH溶 液反应,消耗的 NaOH的 量相等
舯 8.下列类比合理的是
B.1 mol甲 醛、乙醛混合气体中含有的碳氢单键数可能为3Ⅳ
剁 A
督 s02中 S和 CS2中 C的 价层电子对数之比为 1:1 A。
NaC10溶液与 C02反应生成NaHco3和 HC10,贝刂Nac10溶液与SO2反应生成NaHso3和 HC10
C。
邱
B。
A1203与 NaoH和 盐酸均能反应,属于两性氧化物,则 Si02与 NaoH和 HF均 能反应,也属于两
肛
D。
电解精炼铜时,阳极质量减少64g,电路中通过0.2ⅣA个电子
性氧化物
·
驷 3.下列化学用语或图示表达正确的是
押 C。
CH4的沸点低于 SiH4的沸点,则 CC14的沸点也低于SiC14的沸点
钥 A。 甲烷的燃烧热为890 kJ o mol^1,则 其燃烧的热化学方程式为:CH4(g)+202(g)===C02(g)+ D.向 AlC13溶 液中加人过量氨水生成 Al(0H)3沉 淀,则 向 Cuc12溶 液中加入过量氨水生成
2H20(g) ΔⅡ=-890 kJ o mol^1 Cu(0H)2沉淀
化学猜题卷 (五 ) 江西卷 第1页(共 8页 化学猜题卷(五 ) 江西卷 第2页(共 8页
) )9.甲酸 (FA)是一种常温条件下稳定的液体,被认为是一种很有前途的储氢化合物。实验证明在一 12.如图为某元素 A形 成的氯化物的晶胞结构示意图,已知 α =120° 、卩=γ =90° ,晶胞体
定条件下,用 Ir配合物可实现高选择性催化甲酸 H2 积为 2。 146× 10ˉ 2:m3,晶 体密度为2.92 gocmˉ 3。 下列说法正确的是
1 HCOI
HC°
脱氢,过程如图所示。下列说法错误的是 I 下上 子 丫 A。 元素 A为 Fe
A。 反应过程中金属元素Ir的化合价未发生改变 HC02H 步骤3 Ir= 步骤1 B.该晶体中 A离 子的价层电子排布式为3d5
B。 图示 三个步骤 中只有一步涉及 了氧化还原 H20 H20 C.该晶胞中 A原 子的配位数为3
反应
C。
在高浓度甲酸中限速步可能为步骤 2,在低浓
[Ir
3
—H]+
步骤2
[Ir-
2
02CH]+ D.该晶体的熔点高、硬度大
13.环氧乙烷 (/0\,用 E0表 示)广泛应用于日用化学品、医药、建筑和农药等领 E0
度甲酸中限速步可能为步骤 3
C02
0
E0的
域。如图是溴介导的乙烯电氧化合成 四步反应机理示意图。下列说法错
‖
H-C-0H-→
C02+H2
总反应方程式是
D。
误的是
ˉ〓
10.为实现可视化、绿色化、高效制备乙酸乙酯,某小组采用以下方法进行实验
:
A。
电极 a为阳极,电极反应式为2Br— _2eˉ 〓==Br2
0'd〓 排
喊
步骤
I。
在圆底烧瓶中加人乙酸和乙醇,搅拌状态下加人适量硫酸氢钠以及数滴
口
B.KCl能增加b电极溶液的导电性 出
1%o的 甲基紫指示剂(以乙醇为溶剂配制),溶液由无色变为蓝色。
KCl KBr
麇 H20+CH2-CH2===E0+H2
该体系发生的总反应方程式为
步骤Ⅱ。在小孔冷凝柱(如图)中加人适量变色硅胶,然后依次将该装置和球形冷凝 C。 阳 燃
管安装在烧瓶上,加热回流,直至反应体系溶液由蓝色变为紫色。
D.体系中生成 1m。l H2时 ,经过阳离子交换膜的 H+为 2m。
l
0
△
步骤Ⅲ。稍冷后,缓慢向烧瓶中加人饱和碳酸钠水溶液,至不再有二氧化碳气体逸 14.甲 醛法测定氯化铵中的含氮量的原理是 4NH广 +6HCH0==(CH2)6N4H++3H++6H20,然 后
出,然后经过一系列操作得到纯化的乙酸乙酯溶液。
用 O.1m。 l· Lˉ
1NaOH标
准溶液滴定 :(CH2)6N4H++3H++40Hˉ ===(CH2)6N4+4H20,滴 定 丬
下列说法正确的是
I//`T~r`TI`
过程 溶液的 pH随 的变化如图所示。已知:常温下,NH3· H20的 电离常数 Kb= Ⅲ
A。
硫酸氢钠的作用与实验室制各乙酸乙酯中浓硫酸的作用一致 中 炭铸荐羼瑞打
B。 可以用酚酞替代甲基紫作指示剂 1.8火 1oTF。 下列说法错误的是 啦
可以用无水氯化钙固体代替变色硅胶
C。
溜
D。
步骤Ⅲ中的一系列操作包括分液、蒸馏
11.已知某密闭容器中发生可逆反应2A∶=土B+2C,起 始时投人适量物质 A,分别在不同温度、不同
压强下发生该反应,得到物质 B的 物质的量随时间的变化分别如图甲、图乙所示,下列说法错误
的是
A.r3)骂 》 r1、P3)p2)pl
B。 若在 1L恒 容密闭容器中发生该反应,30s内 生 而 : 飞 ri1: 0.20。40。60.8 1.0 1.2 1.4 1.6 1.8 《 《 样 N 品 a0 溶 H) 液
P2 )
成3m。lB,则 该反应的平均反应速率可表示为
r1 P1 A。 已知 (CH2)6N4的 四个 N等 效 ,则其二氯代物有 3种 (不考虑立体异构 )
v(B)=0.1m。 l· Lˉ 1· sˉ 1
i f B。 滴定过程中始终存在 c(Na+)+c(H+)+c[(CH2)6N4H+]=c(Clˉ )+c(0H^)
C。
其他条件相同,绝热条件下达到平衡时,A的物
甲 乙
质的量分数比恒温条件下大 C。 若已知滴定终点的 pH,则可以计算得到 (CH2)6N4H+的 篾
D。 r1、P1条件下,反应达到平衡后,再加入 1 mol B,重新达到平衡时,A的转化率不变 D。 等浓度的 NH3· H20、NH4Cl溶 液中:c(NH广 )+c(H+)=c(NH3· H20)+c(0Hˉ )
化学猜题卷(五 ) 江西卷 第3页(共8页 化学猜题卷 (五 ) 江西卷 第4页(共8页
) )9.甲酸 (FA)是一种常温条件下稳定的液体,被认为是一种很有前途的储氢化合物。实验证明在一 12.如图为某元素 A形 成的氯化物的晶胞结构示意图,已知 α =120° 、卩=γ =90° ,晶胞体
定条件下,用 Ir配合物可实现高选择性催化甲酸 H2 积为 2。 146× 10ˉ 2:m3,晶 体密度为2.92 gocmˉ 3。 下列说法正确的是
1 HCOI
HC°
脱氢,过程如图所示。下列说法错误的是 I 下上 子 丫 A。 元素 A为 Fe
A。 反应过程中金属元素Ir的化合价未发生改变 HC02H 步骤3 Ir= 步骤1 B.该晶体中 A离 子的价层电子排布式为3d5
B。 图示 三个步骤 中只有一步涉及 了氧化还原 H20 H20 C.该晶胞中 A原 子的配位数为3
反应
C。
在高浓度甲酸中限速步可能为步骤 2,在低浓
[Ir
3
—H]+
步骤2
[Ir-
2
02CH]+ D.该晶体的熔点高、硬度大
13.环氧乙烷 (/0\,用 E0表 示)广泛应用于日用化学品、医药、建筑和农药等领 E0
度甲酸中限速步可能为步骤 3
C02
0
E0的
域。如图是溴介导的乙烯电氧化合成 四步反应机理示意图。下列说法错
‖
H-C-0H-→
C02+H2
总反应方程式是
D。
误的是
ˉ〓
10.为实现可视化、绿色化、高效制备乙酸乙酯,某小组采用以下方法进行实验
:
A。
电极 a为阳极,电极反应式为2Br— _2eˉ 〓==Br2
0'd〓 排
喊
步骤
I。
在圆底烧瓶中加人乙酸和乙醇,搅拌状态下加人适量硫酸氢钠以及数滴
口
B.KCl能增加b电极溶液的导电性 出
1%o的 甲基紫指示剂(以乙醇为溶剂配制),溶液由无色变为蓝色。
KCl KBr
麇 H20+CH2-CH2===E0+H2
该体系发生的总反应方程式为
步骤Ⅱ。在小孔冷凝柱(如图)中加人适量变色硅胶,然后依次将该装置和球形冷凝 C。 阳 燃
管安装在烧瓶上,加热回流,直至反应体系溶液由蓝色变为紫色。
D.体系中生成 1m。l H2时 ,经过阳离子交换膜的 H+为 2m。
l
0
△
步骤Ⅲ。稍冷后,缓慢向烧瓶中加人饱和碳酸钠水溶液,至不再有二氧化碳气体逸 14.甲 醛法测定氯化铵中的含氮量的原理是 4NH广 +6HCH0==(CH2)6N4H++3H++6H20,然 后
出,然后经过一系列操作得到纯化的乙酸乙酯溶液。
用 O.1m。 l· Lˉ
1NaOH标
准溶液滴定 :(CH2)6N4H++3H++40Hˉ ===(CH2)6N4+4H20,滴 定 丬
下列说法正确的是
I//`T~r`TI`
过程 溶液的 pH随 的变化如图所示。已知:常温下,NH3· H20的 电离常数 Kb= Ⅲ
A。
硫酸氢钠的作用与实验室制各乙酸乙酯中浓硫酸的作用一致 中 炭铸荐羼瑞打
B。 可以用酚酞替代甲基紫作指示剂 1.8火 1oTF。 下列说法错误的是 啦
可以用无水氯化钙固体代替变色硅胶
C。
溜
D。
步骤Ⅲ中的一系列操作包括分液、蒸馏
11.已知某密闭容器中发生可逆反应2A∶=土B+2C,起 始时投人适量物质 A,分别在不同温度、不同
压强下发生该反应,得到物质 B的 物质的量随时间的变化分别如图甲、图乙所示,下列说法错误
的是
A.r3)骂 》 r1、P3)p2)pl
B。 若在 1L恒 容密闭容器中发生该反应,30s内 生 而 : 飞 ri1: 0.20。40。60.8 1.0 1.2 1.4 1.6 1.8 《 《 样 N 品 a0 溶 H) 液
P2 )
成3m。lB,则 该反应的平均反应速率可表示为
r1 P1 A。 已知 (CH2)6N4的 四个 N等 效 ,则其二氯代物有 3种 (不考虑立体异构 )
v(B)=0.1m。 l· Lˉ 1· sˉ 1
i f B。 滴定过程中始终存在 c(Na+)+c(H+)+c[(CH2)6N4H+]=c(Clˉ )+c(0H^)
C。
其他条件相同,绝热条件下达到平衡时,A的物
甲 乙
质的量分数比恒温条件下大 C。 若已知滴定终点的 pH,则可以计算得到 (CH2)6N4H+的 篾
D。 r1、P1条件下,反应达到平衡后,再加入 1 mol B,重新达到平衡时,A的转化率不变 D。 等浓度的 NH3· H20、NH4Cl溶 液中:c(NH广 )+c(H+)=c(NH3· H20)+c(0Hˉ )
化学猜题卷(五 ) 江西卷 第3页(共8页 化学猜题卷 (五 ) 江西卷 第4页(共8页
) )化学猜题卷 (五 )选择题答题区 时间
过氧乙酸含量
14天 28天
添加剂
题号 一 ’ 3 4 5 ^ 0 7 得分
空白样品
18。
02% 15.12%
答案
Cus04· 5H20 15.50% 12.70%
题号 8 Q 10 11 12 13 14
u
CoS04 1.66% 1.10%
答案
■
二、非选择题:本大题包括4小题,共 58分
。
8一 羟基喹啉 18.90% 18.70%
15.(15分 )过氧乙酸 (CH3C000H)是 一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解。 已知空白样品中过氧乙酸的含量为 19.25%,其 中各类金属离子的含量如下
:
已知过氧化氢法制各过氧乙酸的原理为 H202+CH3C00H===CH3C000H+H20 ΔⅡ(0。 金属离子 Zn2+ co2+ Ni2+ Fe3+ Mn2+ Cr3+ Cu2+ A13+
实验一:提纯过氧化氢溶液 含量/pp1n O。 23 0。 01 0。 10 0.54 0.11 0.09 0。 07 0。 14
据文献报道过氧乙酸合成需较高浓度的过氧化氢(含量 )30%),否 则其生成量很少。某实验小 (5)根据上述实验结果得出的结论是 可以促进过氧乙酸分解
: ,
唰
组利用如图甲装置提高过氧化氢(沸点:152℃ )浓度,使蛇形冷凝管连接恒温水槽,并使蛇形冷
ˉ
8一 羟基喹啉( )可以作为过氧乙酸的有效稳定剂,从物质结构角度分析原因
巾 凝管中的水维持在60℃ ,右边的接收器连接抽气装置,维持系统压强为0.1 MPa。 通过 a装置
划 加
舯
缓慢加入30%过
氧化氢溶液,最终可以获得高浓度溶液。
0H
“ “
甜 (1)a装置的名称是 ,最终在 (填 A”或 B” )中收集到高浓 早
度过氧化氢溶液。 16.(14分)Mo03是生产含钼催化剂的重要原料。以钼精矿(主要成分是 MoS2,还含有 Fes2、 Cus、
K
汪
实验二:制备过氧乙酸 Zns、CaC03和 Si02等杂质)为原料制各 Mo03的工艺流程如图所示。
实验中加人乙酸、过氧化氢、乙酸丁酯和固体催化剂发生反应,制备装置如图乙所示,已知恒温 02
氨水
HN03溶液
蝉 水浴温度为60℃ ,乙酸丁酯和水在90.7℃ 形成共沸物。
击爿
ˉn` 钼精矿 滤液1 除杂 酸沉 四钼 Mo03
郴
2
滤渣 滤液2
探究挖掘隐藏信息
,
不
秒解制各、探究综合 |3、Fe2(M004)3、 CuM004千 日ZnM004;
实验
(NH3)412+、 [Cu(NH3)4]2+和 NH矿
;
边
韬 ③Ksp(Cus)=6.0×
10ˉ
36;
粼
且爿 ^ 抽气泵
仟 `
■
Z 油
离
水
器 O ●
④ [Cu(NH3)4]2+(aq)丁 =主Cu2+(aq)+4NH3(aq) Κ=5.0× 10ˉ 14。
回答下列问题
:
恒
1 0△△
=△≡
△7℃二△ 缓 (1)C02和 SO2的 ⅤSEPR模型分别为 。
A B oc ` = ≡ ) 0 瓶 冲 (2)“ 焙烧 ” 时Mos2转化成 Mo03的化学方程式为
”
ˉ 图甲 图乙 (3)“焙烧 后产生so2气体,处理并利用该副产物的措施有 (写 一种
抬· )。
卡 蚁 孙 L r 3· (2)过 氧化氢应盛装在仪器 (填 “ 1” 或 “ 2” )中 ,原因是 (4)“滤渣 1” 的主要成分是 Sio2、 _、 _、 Fe2(M004)3。 已知 Fe2(Mo04)3能溶于氨水
甾 剁 (3)抽 气泵的作用是 但 “ 滤渣 1” 中仍存在 Fe2(Mo04)3的原因可能是 ,
邱 (4)为提高过氧乙酸的产率,实验过程中应进行的操作是 (5)“ 除杂 ” 时加人适量 (NH4)2S溶 液 的 目的是 __-
肛
· 判断制各反应结束的实验现象是 [Cu(NH3)4]2+(aq)+S2ˉ (aq)t=土Cus(s)+4NH3(aq)的 平衡常数 F= (计
抑
柙
实验三:探究各类添加剂对过氧乙酸稳定性的影响
算结果保留两位有效数字 )。
碉 相同条件下,向相同的过氧乙酸样品中分别加人等浓度的添加剂,放置一段时间后,得到如下实 (6)写出四钼酸铵[(NH4)2Mo4013· 2H20]发生 “ 焙解 ” 反应的化学方程式
验结果
:
化学猜题卷 (五 ) 江西卷 第5页(共 8页 化学猜题卷(五 ) 江西卷 第6页(共 8页
) )化学猜题卷 (五 )选择题答题区 时间
过氧乙酸含量
14天 28天
添加剂
题号 一 ’ 3 4 5 ^ 0 7 得分
空白样品
18。
02% 15.12%
答案
Cus04· 5H20 15.50% 12.70%
题号 8 Q 10 11 12 13 14
u
CoS04 1.66% 1.10%
答案
■
二、非选择题:本大题包括4小题,共 58分
。
8一 羟基喹啉 18.90% 18.70%
15.(15分 )过氧乙酸 (CH3C000H)是 一种常用的消毒剂,易溶于水、易挥发、见光或受热易分解。 已知空白样品中过氧乙酸的含量为 19.25%,其 中各类金属离子的含量如下
:
已知过氧化氢法制各过氧乙酸的原理为 H202+CH3C00H===CH3C000H+H20 ΔⅡ(0。 金属离子 Zn2+ co2+ Ni2+ Fe3+ Mn2+ Cr3+ Cu2+ A13+
实验一:提纯过氧化氢溶液 含量/pp1n O。 23 0。 01 0。 10 0.54 0.11 0.09 0。 07 0。 14
据文献报道过氧乙酸合成需较高浓度的过氧化氢(含量 )30%),否 则其生成量很少。某实验小 (5)根据上述实验结果得出的结论是 可以促进过氧乙酸分解
: ,
唰
组利用如图甲装置提高过氧化氢(沸点:152℃ )浓度,使蛇形冷凝管连接恒温水槽,并使蛇形冷
ˉ
8一 羟基喹啉( )可以作为过氧乙酸的有效稳定剂,从物质结构角度分析原因
巾 凝管中的水维持在60℃ ,右边的接收器连接抽气装置,维持系统压强为0.1 MPa。 通过 a装置
划 加
舯
缓慢加入30%过
氧化氢溶液,最终可以获得高浓度溶液。
0H
“ “
甜 (1)a装置的名称是 ,最终在 (填 A”或 B” )中收集到高浓 早
度过氧化氢溶液。 16.(14分)Mo03是生产含钼催化剂的重要原料。以钼精矿(主要成分是 MoS2,还含有 Fes2、 Cus、
K
汪
实验二:制备过氧乙酸 Zns、CaC03和 Si02等杂质)为原料制各 Mo03的工艺流程如图所示。
实验中加人乙酸、过氧化氢、乙酸丁酯和固体催化剂发生反应,制备装置如图乙所示,已知恒温 02
氨水
HN03溶液
蝉 水浴温度为60℃ ,乙酸丁酯和水在90.7℃ 形成共沸物。
击爿
ˉn` 钼精矿 滤液1 除杂 酸沉 四钼 Mo03
郴
2
滤渣 滤液2
探究挖掘隐藏信息
,
不
秒解制各、探究综合 |3、Fe2(M004)3、 CuM004千 日ZnM004;
实验
(NH3)412+、 [Cu(NH3)4]2+和 NH矿
;
边
韬 ③Ksp(Cus)=6.0×
10ˉ
36;
粼
且爿 ^ 抽气泵
仟 `
■
Z 油
离
水
器 O ●
④ [Cu(NH3)4]2+(aq)丁 =主Cu2+(aq)+4NH3(aq) Κ=5.0× 10ˉ 14。
回答下列问题
:
恒
1 0△△
=△≡
△7℃二△ 缓 (1)C02和 SO2的 ⅤSEPR模型分别为 。
A B oc ` = ≡ ) 0 瓶 冲 (2)“ 焙烧 ” 时Mos2转化成 Mo03的化学方程式为
”
ˉ 图甲 图乙 (3)“焙烧 后产生so2气体,处理并利用该副产物的措施有 (写 一种
抬· )。
卡 蚁 孙 L r 3· (2)过 氧化氢应盛装在仪器 (填 “ 1” 或 “ 2” )中 ,原因是 (4)“滤渣 1” 的主要成分是 Sio2、 _、 _、 Fe2(M004)3。 已知 Fe2(Mo04)3能溶于氨水
甾 剁 (3)抽 气泵的作用是 但 “ 滤渣 1” 中仍存在 Fe2(Mo04)3的原因可能是 ,
邱 (4)为提高过氧乙酸的产率,实验过程中应进行的操作是 (5)“ 除杂 ” 时加人适量 (NH4)2S溶 液 的 目的是 __-
肛
· 判断制各反应结束的实验现象是 [Cu(NH3)4]2+(aq)+S2ˉ (aq)t=土Cus(s)+4NH3(aq)的 平衡常数 F= (计
抑
柙
实验三:探究各类添加剂对过氧乙酸稳定性的影响
算结果保留两位有效数字 )。
碉 相同条件下,向相同的过氧乙酸样品中分别加人等浓度的添加剂,放置一段时间后,得到如下实 (6)写出四钼酸铵[(NH4)2Mo4013· 2H20]发生 “ 焙解 ” 反应的化学方程式
验结果
:
化学猜题卷 (五 ) 江西卷 第5页(共 8页 化学猜题卷(五 ) 江西卷 第6页(共 8页
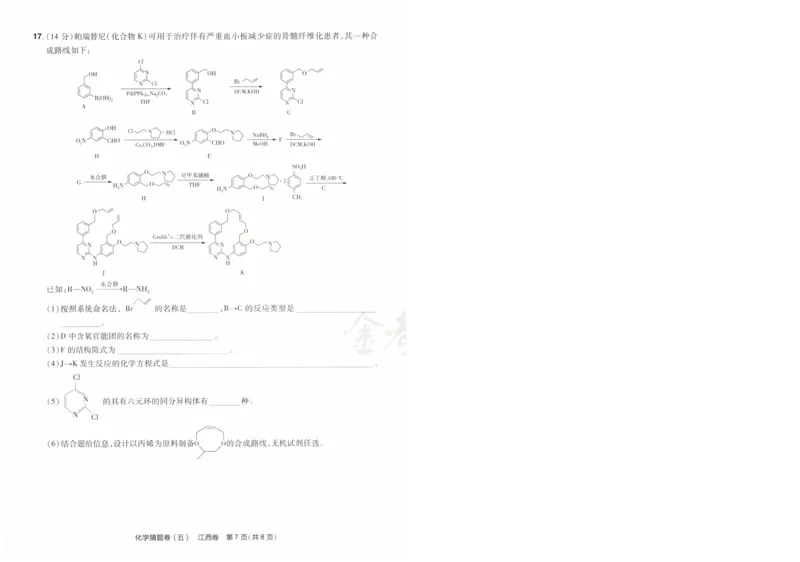
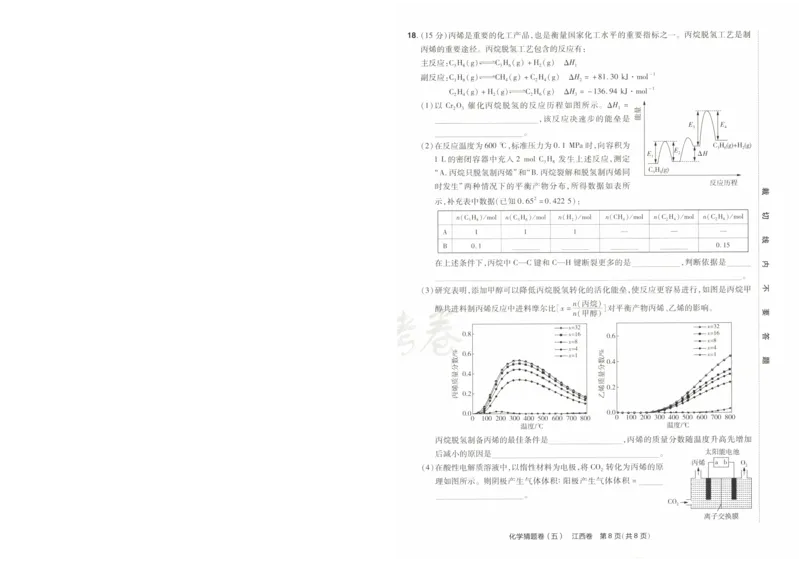
) )17。 (14分 )帕瑞替尼(化合物 K)可用于治疗伴有严重血小板减少症的骨髓纤维化患者,其一种合 18。 (15分 )丙烯是重要的化工产品,也是衡量国家化工水平的重要指标之一。丙烷脱氢工艺是制
成路线如下 丙烯的重要途径。丙烷脱氢工艺包含的反应有
: :
Cl 主反应 :C3H:(g)==乇3H6(g)+H2(g) ΔⅡ
/农 l 、N 0/′“夕 1
1宀 Br/ˇ 副 反 应 :C3H:(g)丁=空CH4(g)+C2H4(g) ΔⅡ2=+81.30 kJ o molˉ 1
Cl
Pd(PPh3)4,Na2co3 N DCM,KOH N C2H4(g)+H2(g)了 =主C2H6(g) ΔⅡ3=-136.94 kJ o molˉ 1
B(0H)2
A
THF Cl Cl (1)以 Cr2o3催化丙烷脱氢的反应历程如图所示。ΔⅡ1=到
酬
B C
,该反应决速步的能垒是 程
D州 · -F榀
E3 工`'4
02N 尖≡岛:苎 。 2NK× ∶「 黠 》
(2)在反应温度为600℃ ,标准压力为0.1 MPa时 ,向容积为 C3H6(g)+H2(g)
D E 1L的 密闭容器中充人 2m。l c3H:发生上述反应,测定 El ΔⅡ
S03H “ ” “
G—
水合肼
H2N
对甲
T
苯
HF
磺酸
H2N 0 ·2
/
Ψ
′、 ^ 正丁 了 醇,1∞ ^ ℃
时
A。
发
丙
生
烷
” 两
只
种
脱
情
氢制
况
丙
下
烯
的平
和
衡
B
产
。 丙
物
烷
分
裂
布
解
,所
和
得
脱
数
氢
据
制
如
丙
表
烯
所
同 C3H:(g)
反应历程 擀
H I CH3 示,补充表中数据(已知
0。
652=0.4225):
'\'
舀
n(C3H:)/m。 l 尼(C3H6)/m。 l 尼(H2)/m。 l 乃(CH4)/m。 l 而(C2H4)/m。 l n(C2H6)/m。 l
A 1 1 1
Gmbb’s二代催化剂 雌
‘′ ' ^` T'⊥′ I ) DcM N 、/′N L \ / B 0.1 0.15
△_y
H 在上述条件下,丙烷中C—C键 和 C-H键 断裂更多的是 ,判断依据是 △
K
J
已 知 :R-N02一兰 ik 型 Δ 阡 飞 I+ R_NH2 (3)研究表明,添加甲醇可以降低丙烷脱氢转化的活化能垒,使反应更容易进行,如图是丙烷甲 爿
(1)按照系统命名法,Br ^彡 的名称是 ,B→ C的 反应类型是 醇共进料制丙烯反应中进料摩尔比
[冗
=靛 /ˇ
诨
=「 才
璀
1贮
葑
r` ]对平衡产物丙烯、乙烯的影响。
Ⅲ
— ¨%=32 —0—冗=32
(2)D中 含氧官能团的名称为 00000 86420 _
-◆
_哨
一哨
=
=
1
8
6 0.6 -
-
ˉ
◆
—
一
以
哨
=
=
1
8
6 啉
(3)F的 结构简式为 球 —◆—写=4 术 —●—凭=4
` -“ =1 ` — 哨=1 渊
(4)J→K发 生反应的化学方程式是
恕
酬
懋
心
酬
懋 nˇ
^u
4
2
Cl
烬 烬
蟥 寒
挺 闷
/(` 的具有六元环的同分异构体有 种 。
`J丿 0
Cl 0 100 200 300 400 500 600 700 800 300 400 500 600 700 800
/石 ′\ 温度/℃ 温度/℃
(6)结合题给信息,设计以丙烯为原料制各 0\ /0 的合成路线,无机试剂任选。 丙烷脱氢制备丙烯的最佳条件是 ,丙烯的质量分数随温度升高先增加
/~ 后减小的原因是 。 太阳能电池
a b
(4)在酸性电解质溶液中,以惰性材料为电极,将 C02转化为丙烯的原 丙烯
|
理如图所示。则阴极产生气体体积:阳极产生气体体积 =
C02
离子交换膜
化学猜题卷(五 ) 江西卷 第7页(共 8页 化学猜题卷(五 ) 江西卷 第8页(共8页
) )17。 (14分 )帕瑞替尼(化合物 K)可用于治疗伴有严重血小板减少症的骨髓纤维化患者,其一种合 18。 (15分 )丙烯是重要的化工产品,也是衡量国家化工水平的重要指标之一。丙烷脱氢工艺是制
成路线如下 丙烯的重要途径。丙烷脱氢工艺包含的反应有
: :
Cl 主反应 :C3H:(g)==乇3H6(g)+H2(g) ΔⅡ
/农 l 、N 0/′“夕 1
1宀 Br/ˇ 副 反 应 :C3H:(g)丁=空CH4(g)+C2H4(g) ΔⅡ2=+81.30 kJ o molˉ 1
Cl
Pd(PPh3)4,Na2co3 N DCM,KOH N C2H4(g)+H2(g)了 =主C2H6(g) ΔⅡ3=-136.94 kJ o molˉ 1
B(0H)2
A
THF Cl Cl (1)以 Cr2o3催化丙烷脱氢的反应历程如图所示。ΔⅡ1=到
酬
B C
,该反应决速步的能垒是 程
D州 · -F榀
E3 工`'4
02N 尖≡岛:苎 。 2NK× ∶「 黠 》
(2)在反应温度为600℃ ,标准压力为0.1 MPa时 ,向容积为 C3H6(g)+H2(g)
D E 1L的 密闭容器中充人 2m。l c3H:发生上述反应,测定 El ΔⅡ
S03H “ ” “
G—
水合肼
H2N
对甲
T
苯
HF
磺酸
H2N 0 ·2
/
Ψ
′、 ^ 正丁 了 醇,1∞ ^ ℃
时
A。
发
丙
生
烷
” 两
只
种
脱
情
氢制
况
丙
下
烯
的平
和
衡
B
产
。 丙
物
烷
分
裂
布
解
,所
和
得
脱
数
氢
据
制
如
丙
表
烯
所
同 C3H:(g)
反应历程 擀
H I CH3 示,补充表中数据(已知
0。
652=0.4225):
'\'
舀
n(C3H:)/m。 l 尼(C3H6)/m。 l 尼(H2)/m。 l 乃(CH4)/m。 l 而(C2H4)/m。 l n(C2H6)/m。 l
A 1 1 1
Gmbb’s二代催化剂 雌
‘′ ' ^` T'⊥′ I ) DcM N 、/′N L \ / B 0.1 0.15
△_y
H 在上述条件下,丙烷中C—C键 和 C-H键 断裂更多的是 ,判断依据是 △
K
J
已 知 :R-N02一兰 ik 型 Δ 阡 飞 I+ R_NH2 (3)研究表明,添加甲醇可以降低丙烷脱氢转化的活化能垒,使反应更容易进行,如图是丙烷甲 爿
(1)按照系统命名法,Br ^彡 的名称是 ,B→ C的 反应类型是 醇共进料制丙烯反应中进料摩尔比
[冗
=靛 /ˇ
诨
=「 才
璀
1贮
葑
r` ]对平衡产物丙烯、乙烯的影响。
Ⅲ
— ¨%=32 —0—冗=32
(2)D中 含氧官能团的名称为 00000 86420 _
-◆
_哨
一哨
=
=
1
8
6 0.6 -
-
ˉ
◆
—
一
以
哨
=
=
1
8
6 啉
(3)F的 结构简式为 球 —◆—写=4 术 —●—凭=4
` -“ =1 ` — 哨=1 渊
(4)J→K发 生反应的化学方程式是
恕
酬
懋
心
酬
懋 nˇ
^u
4
2
Cl
烬 烬
蟥 寒
挺 闷
/(` 的具有六元环的同分异构体有 种 。
`J丿 0
Cl 0 100 200 300 400 500 600 700 800 300 400 500 600 700 800
/石 ′\ 温度/℃ 温度/℃
(6)结合题给信息,设计以丙烯为原料制各 0\ /0 的合成路线,无机试剂任选。 丙烷脱氢制备丙烯的最佳条件是 ,丙烯的质量分数随温度升高先增加
/~ 后减小的原因是 。 太阳能电池
a b
(4)在酸性电解质溶液中,以惰性材料为电极,将 C02转化为丙烯的原 丙烯
|
理如图所示。则阴极产生气体体积:阳极产生气体体积 =
C02
离子交换膜
化学猜题卷(五 ) 江西卷 第7页(共 8页 化学猜题卷(五 ) 江西卷 第8页(共8页
) )绝密★启用前 3.设 ⅣA为阿伏加德罗常数的值。下列说法正确的是
2024年
A.1 mol冰醋酸与足量 CH3CH20H充 分反应,生成的 CH3C00CH2CH3分 子数目为Ⅳ
A
江西省 普通高 中学业水平选择性考试
B。
熔融状态下 1m。l AlC13中含有 A13+的数目为Ⅳ
A
化学猜题卷
(六 C.6.4g铜 与足量硫粉共热,反应中转移的电子数为0.1Ⅳ
A
4L苯
) D。 标准状况下 ,22。 中含有碳碳双键的数目为3Ⅳ A
4.下列实验装置和实验目的均正确的是
目 命题报告
■
本套试卷依据《高考评价体系》指导要求命题,通过对《课程标准》和新教材的学习与研究精心编制而成,试卷的结构 选项 A B C D
与知识点分布力求符合江西本地教学实际。 0.1 mol· L-1
命题总特点:①立足教材,注重考教衔接。如第2题考查化学用语,第 5题考查元素周期律、价层电子对互斥模型、 一 N) 一 N%s04
2 溶液
杂化轨道理论,第 7题考查离子液体性质,有利于引导学生重视并落实基础,体现测试的基础性要求。
实验装置
②情境多样,凸显学科价值。如第1题滕王阁、第8题静脉麻醉药、第13题 串联电池、第16题高钛渣的利用等均基于
真实情境设计具体问题任务,既能考查必备知识、关键能力,又能彰显化学学科的社会应用价值,体现试题的应用性
Na0H溶液
和创新性要求。
围
ˉ ③注重迁移,适度体现创新。如第9题考查实验用品、试剂的选择,命题角度创新,第 12题反应机理图像新颖,第 13 实验 目的 收集 N02气体 制取氯气 制取 Na2so4· 10H20 检查装置的气密性
眇 题电池工作原理陌生,这些试题能很好地测评学生是基于题给信息的理解还是基于平时学习的简单记忆,体现试题
划 洳
5.下列说法错误的是
舯 的综合性及适度的创新性要求。
A。 随原子序数的递增,元素原子的核外电子排布、原子半径和化合价都呈现周期性变化
脚 本试卷满分 100分 ,考试时间 75分 钟。
可能用到的相对原子质量 :F-19 Ca-40 Cu—64 Nb-93 B。
卤族元素对应的氢化物的稳定性随核电荷数的增加而增强
“ ”
C.价层电子对互斥模型认为分子的空间结构是中心原子周围的 价层电子对 相互排斥的结果
阡 -、选择题 :本大题包括 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合 D.杂化轨道用于形成 σ键或用于容纳未参与成键的孤电子对
题目要求。
6.某无机盐药物中含有前四周期元素 Ⅹ、Y、Z、 W,已 知四种元素原子序数依次增大,X的基态原子
蝉 江 1.滕王阁被誉为 “ 江南三大名楼 ” 之一,下列说法错误的是 的2p能级上有三个未成对电子,含 Y的 物质灼烧时火焰呈黄色,Z的 电负性在同周期中最大,W
慰 “ ”
A。 滕王阁正东人口处的 八怪 宝鼎由青铜铸成。青铜是铜锡合金 、山0“J 原子的最外层只有一个电子,其余能层均充满。下列说法正确的是
郴
B。 一楼正 中的石碑外 围以玛瑙红大理石镶边。玛瑙红大理石 的主要成分 A。 Ⅹ的简单氢化物的中心原子的杂化方式为sp2
B.Y的
灭
=CaC03
单质与乙醇反应的剧烈程度强于水
尽
“ ”
C。 三楼有丙烯壁画《临川梦》。丙烯颜料沾到衣物上可以利用 相似相溶 原 C。 Z的一种氧化物可用于自来水消毒
W原
韬 理用酒精清洗 D。 同周期中与 子的未成对电子数相同的元素有3种
泛
弋
T
H
军
丬 qˉ
、 D。 瓦件采用碧色琉璃瓦。琉璃瓦呈碧色是由于含有Fe2o3
7.磺酸盐型离子液体通常由一种带有磺酸基团的阳离子和一种无机阴离子组成(如 图所示),其在
电池、电容器等领域有着广泛应用。下列说法错误的是
下列化学用语表示正确的是
2。
3p
A。 基态 0原 子中电子占据最高能级的电子云轮廓图为哑铃形 /人 厂 一\ \
' ^
A。 基态 Cl原子的价电子轨道表示式
:
— 个
l
个 ˉ— l v ▲T—
C
B
。
。
该
阳离
离
子
子液
中
体
而
结
值
构
越大
中存
,该
在
离
非
子
极
液
性
体
共
的
价
熔
键
点越高 o '
R
` '议
卜片丶
`
/
n
s0
Ⅹ
3H
D。 该离子液体具有强酸性,在催化反应中具有重要的应用价值
堆 甲烷的空间填充模型
B。
群 : 8.环泊酚是中国首个自主化合物创新静脉麻醉药,其在丙泊酚化学结构的基础上引人了环丙基,已
羽
督 知丙泊酚和环泊酚的结构如图所示。下列说法正确的是
姆 A.1 mol丙 泊酚与足量 的浓溴水 反应最多消耗 0H 0H =
肛 C.邻羟基苯甲醛形成的分子内氢键 H
: 3 mol Br2
·
驷
B。 丙泊酚和环泊酚均具有手性
柙
碉 辶⌒ C。 环泊酚中共平面的碳原子最多有 11个 丙泊酚 环泊酚
SO2分 SEPR模 ~''1豳
D。 子 的 Ⅴ 型 ④ D。 环泊酚的分子式是 C14H160
化学猜题卷(六) 江西卷 第 1页(共 8页 ) 化学猜题卷(六) 江西卷 第 2页(共 8页 )绝密★启用前 3.设 ⅣA为阿伏加德罗常数的值。下列说法正确的是
2024年
A.1 mol冰醋酸与足量 CH3CH20H充 分反应,生成的 CH3C00CH2CH3分 子数目为Ⅳ
A
江西省 普通高 中学业水平选择性考试
B。
熔融状态下 1m。l AlC13中含有 A13+的数目为Ⅳ
A
化学猜题卷
(六 C.6.4g铜 与足量硫粉共热,反应中转移的电子数为0.1Ⅳ
A
4L苯
) D。 标准状况下 ,22。 中含有碳碳双键的数目为3Ⅳ A
4.下列实验装置和实验目的均正确的是
目 命题报告
■
本套试卷依据《高考评价体系》指导要求命题,通过对《课程标准》和新教材的学习与研究精心编制而成,试卷的结构 选项 A B C D
与知识点分布力求符合江西本地教学实际。 0.1 mol· L-1
命题总特点:①立足教材,注重考教衔接。如第2题考查化学用语,第 5题考查元素周期律、价层电子对互斥模型、 一 N) 一 N%s04
2 溶液
杂化轨道理论,第 7题考查离子液体性质,有利于引导学生重视并落实基础,体现测试的基础性要求。
实验装置
②情境多样,凸显学科价值。如第1题滕王阁、第8题静脉麻醉药、第13题 串联电池、第16题高钛渣的利用等均基于
真实情境设计具体问题任务,既能考查必备知识、关键能力,又能彰显化学学科的社会应用价值,体现试题的应用性
Na0H溶液
和创新性要求。
围
ˉ ③注重迁移,适度体现创新。如第9题考查实验用品、试剂的选择,命题角度创新,第 12题反应机理图像新颖,第 13 实验 目的 收集 N02气体 制取氯气 制取 Na2so4· 10H20 检查装置的气密性
眇 题电池工作原理陌生,这些试题能很好地测评学生是基于题给信息的理解还是基于平时学习的简单记忆,体现试题
划 洳
5.下列说法错误的是
舯 的综合性及适度的创新性要求。
A。 随原子序数的递增,元素原子的核外电子排布、原子半径和化合价都呈现周期性变化
脚 本试卷满分 100分 ,考试时间 75分 钟。
可能用到的相对原子质量 :F-19 Ca-40 Cu—64 Nb-93 B。
卤族元素对应的氢化物的稳定性随核电荷数的增加而增强
“ ”
C.价层电子对互斥模型认为分子的空间结构是中心原子周围的 价层电子对 相互排斥的结果
阡 -、选择题 :本大题包括 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项符合 D.杂化轨道用于形成 σ键或用于容纳未参与成键的孤电子对
题目要求。
6.某无机盐药物中含有前四周期元素 Ⅹ、Y、Z、 W,已 知四种元素原子序数依次增大,X的基态原子
蝉 江 1.滕王阁被誉为 “ 江南三大名楼 ” 之一,下列说法错误的是 的2p能级上有三个未成对电子,含 Y的 物质灼烧时火焰呈黄色,Z的 电负性在同周期中最大,W
慰 “ ”
A。 滕王阁正东人口处的 八怪 宝鼎由青铜铸成。青铜是铜锡合金 、山0“J 原子的最外层只有一个电子,其余能层均充满。下列说法正确的是
郴
B。 一楼正 中的石碑外 围以玛瑙红大理石镶边。玛瑙红大理石 的主要成分 A。 Ⅹ的简单氢化物的中心原子的杂化方式为sp2
B.Y的
灭
=CaC03
单质与乙醇反应的剧烈程度强于水
尽
“ ”
C。 三楼有丙烯壁画《临川梦》。丙烯颜料沾到衣物上可以利用 相似相溶 原 C。 Z的一种氧化物可用于自来水消毒
W原
韬 理用酒精清洗 D。 同周期中与 子的未成对电子数相同的元素有3种
泛
弋
T
H
军
丬 qˉ
、 D。 瓦件采用碧色琉璃瓦。琉璃瓦呈碧色是由于含有Fe2o3
7.磺酸盐型离子液体通常由一种带有磺酸基团的阳离子和一种无机阴离子组成(如 图所示),其在
电池、电容器等领域有着广泛应用。下列说法错误的是
下列化学用语表示正确的是
2。
3p
A。 基态 0原 子中电子占据最高能级的电子云轮廓图为哑铃形 /人 厂 一\ \
' ^
A。 基态 Cl原子的价电子轨道表示式
:
— 个
l
个 ˉ— l v ▲T—
C
B
。
。
该
阳离
离
子
子液
中
体
而
结
值
构
越大
中存
,该
在
离
非
子
极
液
性
体
共
的
价
熔
键
点越高 o '
R
` '议
卜片丶
`
/
n
s0
Ⅹ
3H
D。 该离子液体具有强酸性,在催化反应中具有重要的应用价值
堆 甲烷的空间填充模型
B。
群 : 8.环泊酚是中国首个自主化合物创新静脉麻醉药,其在丙泊酚化学结构的基础上引人了环丙基,已
羽
督 知丙泊酚和环泊酚的结构如图所示。下列说法正确的是
姆 A.1 mol丙 泊酚与足量 的浓溴水 反应最多消耗 0H 0H =
肛 C.邻羟基苯甲醛形成的分子内氢键 H
: 3 mol Br2
·
驷
B。 丙泊酚和环泊酚均具有手性
柙
碉 辶⌒ C。 环泊酚中共平面的碳原子最多有 11个 丙泊酚 环泊酚
SO2分 SEPR模 ~''1豳
D。 子 的 Ⅴ 型 ④ D。 环泊酚的分子式是 C14H160
化学猜题卷(六) 江西卷 第 1页(共 8页 ) 化学猜题卷(六) 江西卷 第 2页(共 8页 )9.利用下列实验用品、试剂,不能达到实验目的的是 A。 该过程中存在极性键、非极性键的断裂和形成
Ni2B(001)降低了阳极析氧反应的活化能和焓变
选项 实验目的 实验用品、试剂 B。
第二步发生反应:20H~—→ 米0+H20+eˉ
A 比较水和四氯化碳分子的极性 H20、CC14、橡胶棒、毛皮 C。
B 验证蛋白质的盐析是可逆过程
鸡蛋清溶液、Pb(CH3C00)2溶液 D。
该过程总反应是40H~—
4eˉ
===02+2H20
13.华中科技大学团队开发了一种溴介导的双重增强策略,以促进 C2H4电环氧化为环氧乙烷 (EO)
C 证明Na2so3、Na2C03水解程度大小 pH计 、0.1 1nol· Lˉ 1 Na2S03、 0.1 mol· Lˉ 1 Na2C03 和C02电还原为 C2H4,从而提高了C02转化为 E0的 总效率。已知 C02串联电合成 E0的工作
D 证明牺牲阳极法保护铁 Fe、Zn、酸化的食盐水、K3[Fe(CN)6]溶 液 原理如图所示。
10.四
法
MnC
正
氧
03
化
确
、
三
的
Mn
锰
是
20
(
3
N
、
M
H
n
4H
M
3
S
o
n
0
4
4
0
、
)
0
广
H
H
及
泛
20
应
2
少
用
量
于
F
M
e
n
电
2
(
o
0
3
子
、
H)
工
A
2
1
业
2 03
N
,
、
H
是
3
s
·
i
生
02
H
产
)
2
为
0
软
原
磁
料
铁
生
氧
产
体
M
的
n 3
原
o
料
o
4
2
的
。
工
一
艺
种
流
以
程
低
如
品
下
位
。
锰
下
矿
列
(含
说
9
h`·
〓 严
≡、
田
\ \
丶
—
「
hml0㈧
一 叫
ˉ
ˉ
ˉ
∽
/Na4[Fe(cN)61
一 |
爿
卜 邕
U 留
气体
|
X
一 υμd
γ m
`
“"
Br^
锰矿粉 溶浸 调pH=5 沉锰 M Mn n 2 ( ( 0 0 H H ) ) 2 2s04 Mn304 / ˉ J ∵ iˉ υ ● ˉ ˉ `Na3[Fe(cN)61 ·
烨
滤渣 1 滤渣 2 母液 宀吧也 川 刀 午 氍 电解槽2
“ ”
H202作
A。 溶浸 过程中 氧化剂 下列说法错误的是 出
B.键角 :NH广 )SOlˉ 电解槽 1中阴极的电极反应式为 2C02+12H++12eˉ ===C2H4+4H20
“ ” A。
C。 “ 母液 ” 可以直接循环利用于溶浸过程 6Mn(oH)2+02===2Mn304+6H20、3Mn2(0H)2S04+ B。 电解槽2中 阳极附近溶液 pH变 小 擗
D。
02
氧
=
化
==2
时
Mn
发
30
生
4
反
+3
应
H2
的
S
化
04
学方程式为
C。
当电路中通过4m。l电子时,理论上可获得 88 g C2H40
(
2C02+2H20===C2H40+;02 △
11.二氧化钛被认为是现今世界上性能最好的一 b D。 电解总反应为
种白色颜料,同时被广泛应用于涂料、造纸、化
14.利用平衡移动原理 ,分析常温下 Ni2+在不同.pH的 Na2co3体系中的可能产物。
丬
纤、橡胶等工业,是一种环境安全的清洁剂。 已知:图 1中 曲线表示 Na2co3体系中各含碳粒子的物质的量分数与 pH的 关系;图 2中 曲线I的离
二氧化钛晶体也称金红石晶体,晶胞结构如图 ○ 锱 O 子浓度关系符合c(Ni2+)· c(CO:ˉ )=凡p(NiC03);曲 线Ⅱ的离子浓度关系符合c(Ni2+) ·
Ⅲ
甲所示。下列说法错误的是 1c2(0H^)=凡 c(CO:^)+c(HCOf)+c(H2C03)=
p[Ni(0H)2][注 :起 始Na2 co3体 系中
A.Ti的配位数是 6,0的配位数是3
B.基态 Ti核外电子共有22种空间运动状态 图甲 图乙 0.1 mo1· Lˉ 1;不 同pH下 c(CO:^)由 图1得到 ]。 聃
(;,;,;) \
C。
以晶胞参数为单位长度建立坐标系,体心原子的原子分数坐标为
\
D。 沿晶胞面对角线 a到 b方向的投影图如图乙 热 ^ U o o ΗC
\
rt\ 丶 3
一 2 47 6 58 0 ′
`、
\
`` 、II I :Nir‘
渊
12.电解水是产生清洁能源最有效的方法之一,科学家研究利用 Ni2B(001)表 面催化电解水的阳极
酬
心 3 z 一 ⒋ 一 上\ `
\
`、
析氧反应机理如图所示。下列说法正确的是 扭 ^ ho 一 \
0Hˉ
烬
彝
U
⑴
\\卜
\`ˉ
h
q 0 d
一
.
⒎
1
一
|8~9
` :
|
Ⅱ \
10
∶叮
25
irn
`匚~' = ' ◇ 0( 4 0厂 8 10 12 · ' 0 7 ` 8 9 10 11 12
pH pH
手把手教你分
第一步
H。 ‘0+ 0。
0
乙+
H
e
^
^
` '
价
H凵
酞
热
目
戢
H
酞
冂
H
◇
'rl`
Η
0 r
2 o
+
●
○
OH 0
B
析新型图像
A
下
.
列
Ni
说
(0
法
H)
错
2(
误
s)
的
+C
是
O:ˉ (a
图
q)了
1
=羽iC03(s)+20Hˉ (aq)的 平衡常数 K
图
为
2
2× 10ˉ ⒐ 3
ONi
B.M点时 液中存在c(CO:^)=c(0H^)
第三步 ,溶
仁 彐 C。 初始状 态 pH=9、 lg c(Ni2+)=-4,平 衡 后 存 在 c(CO:^)+c(HCOf)+c(H2C03)(
f `
e o ˉ 一△ 0.1 mol· Lˉ1
D。
向0.1m。
l·
L^1 Na2C03溶液中滴加NiC12溶液优先出现 Ni(0H)2沉淀
化学猜题卷(六) 江西卷 第 3页(共8页 ) 化学猜题卷(六) 江西卷 第 4页(共 8页 )9.利用下列实验用品、试剂,不能达到实验目的的是 A。 该过程中存在极性键、非极性键的断裂和形成
Ni2B(001)降低了阳极析氧反应的活化能和焓变
选项 实验目的 实验用品、试剂 B。
第二步发生反应:20H~—→ 米0+H20+eˉ
A 比较水和四氯化碳分子的极性 H20、CC14、橡胶棒、毛皮 C。
B 验证蛋白质的盐析是可逆过程
鸡蛋清溶液、Pb(CH3C00)2溶液 D。
该过程总反应是40H~—
4eˉ
===02+2H20
13.华中科技大学团队开发了一种溴介导的双重增强策略,以促进 C2H4电环氧化为环氧乙烷 (EO)
C 证明Na2so3、Na2C03水解程度大小 pH计 、0.1 1nol· Lˉ 1 Na2S03、 0.1 mol· Lˉ 1 Na2C03 和C02电还原为 C2H4,从而提高了C02转化为 E0的 总效率。已知 C02串联电合成 E0的工作
D 证明牺牲阳极法保护铁 Fe、Zn、酸化的食盐水、K3[Fe(CN)6]溶 液 原理如图所示。
10.四
法
MnC
正
氧
03
化
确
、
三
的
Mn
锰
是
20
(
3
N
、
M
H
n
4H
M
3
S
o
n
0
4
4
0
、
)
0
广
H
H
及
泛
20
应
2
少
用
量
于
F
M
e
n
电
2
(
o
0
3
子
、
H)
工
A
2
1
业
2 03
N
,
、
H
是
3
s
·
i
生
02
H
产
)
2
为
0
软
原
磁
料
铁
生
氧
产
体
M
的
n 3
原
o
料
o
4
2
的
。
工
一
艺
种
流
以
程
低
如
品
下
位
。
锰
下
矿
列
(含
说
9
h`·
〓 严
≡、
田
\ \
丶
—
「
hml0㈧
一 叫
ˉ
ˉ
ˉ
∽
/Na4[Fe(cN)61
一 |
爿
卜 邕
U 留
气体
|
X
一 υμd
γ m
`
“"
Br^
锰矿粉 溶浸 调pH=5 沉锰 M Mn n 2 ( ( 0 0 H H ) ) 2 2s04 Mn304 / ˉ J ∵ iˉ υ ● ˉ ˉ `Na3[Fe(cN)61 ·
烨
滤渣 1 滤渣 2 母液 宀吧也 川 刀 午 氍 电解槽2
“ ”
H202作
A。 溶浸 过程中 氧化剂 下列说法错误的是 出
B.键角 :NH广 )SOlˉ 电解槽 1中阴极的电极反应式为 2C02+12H++12eˉ ===C2H4+4H20
“ ” A。
C。 “ 母液 ” 可以直接循环利用于溶浸过程 6Mn(oH)2+02===2Mn304+6H20、3Mn2(0H)2S04+ B。 电解槽2中 阳极附近溶液 pH变 小 擗
D。
02
氧
=
化
==2
时
Mn
发
30
生
4
反
+3
应
H2
的
S
化
04
学方程式为
C。
当电路中通过4m。l电子时,理论上可获得 88 g C2H40
(
2C02+2H20===C2H40+;02 △
11.二氧化钛被认为是现今世界上性能最好的一 b D。 电解总反应为
种白色颜料,同时被广泛应用于涂料、造纸、化
14.利用平衡移动原理 ,分析常温下 Ni2+在不同.pH的 Na2co3体系中的可能产物。
丬
纤、橡胶等工业,是一种环境安全的清洁剂。 已知:图 1中 曲线表示 Na2co3体系中各含碳粒子的物质的量分数与 pH的 关系;图 2中 曲线I的离
二氧化钛晶体也称金红石晶体,晶胞结构如图 ○ 锱 O 子浓度关系符合c(Ni2+)· c(CO:ˉ )=凡p(NiC03);曲 线Ⅱ的离子浓度关系符合c(Ni2+) ·
Ⅲ
甲所示。下列说法错误的是 1c2(0H^)=凡 c(CO:^)+c(HCOf)+c(H2C03)=
p[Ni(0H)2][注 :起 始Na2 co3体 系中
A.Ti的配位数是 6,0的配位数是3
B.基态 Ti核外电子共有22种空间运动状态 图甲 图乙 0.1 mo1· Lˉ 1;不 同pH下 c(CO:^)由 图1得到 ]。 聃
(;,;,;) \
C。
以晶胞参数为单位长度建立坐标系,体心原子的原子分数坐标为
\
D。 沿晶胞面对角线 a到 b方向的投影图如图乙 热 ^ U o o ΗC
\
rt\ 丶 3
一 2 47 6 58 0 ′
`、
\
`` 、II I :Nir‘
渊
12.电解水是产生清洁能源最有效的方法之一,科学家研究利用 Ni2B(001)表 面催化电解水的阳极
酬
心 3 z 一 ⒋ 一 上\ `
\
`、
析氧反应机理如图所示。下列说法正确的是 扭 ^ ho 一 \
0Hˉ
烬
彝
U
⑴
\\卜
\`ˉ
h
q 0 d
一
.
⒎
1
一
|8~9
` :
|
Ⅱ \
10
∶叮
25
irn
`匚~' = ' ◇ 0( 4 0厂 8 10 12 · ' 0 7 ` 8 9 10 11 12
pH pH
手把手教你分
第一步
H。 ‘0+ 0。
0
乙+
H
e
^
^
` '
价
H凵
酞
热
目
戢
H
酞
冂
H
◇
'rl`
Η
0 r
2 o
+
●
○
OH 0
B
析新型图像
A
下
.
列
Ni
说
(0
法
H)
错
2(
误
s)
的
+C
是
O:ˉ (a
图
q)了
1
=羽iC03(s)+20Hˉ (aq)的 平衡常数 K
图
为
2
2× 10ˉ ⒐ 3
ONi
B.M点时 液中存在c(CO:^)=c(0H^)
第三步 ,溶
仁 彐 C。 初始状 态 pH=9、 lg c(Ni2+)=-4,平 衡 后 存 在 c(CO:^)+c(HCOf)+c(H2C03)(
f `
e o ˉ 一△ 0.1 mol· Lˉ1
D。
向0.1m。
l·
L^1 Na2C03溶液中滴加NiC12溶液优先出现 Ni(0H)2沉淀
化学猜题卷(六) 江西卷 第 3页(共8页 ) 化学猜题卷(六) 江西卷 第 4页(共 8页 )②一系列操作过程中使用的仪器有 (填标号
(六 )。
化学猜题卷 )选择题答题区
「了
Ⅱ
兰Ⅱ
题号 2 3 4 r ● ^ ● 7 得分 巨 巨 Ⅱ Ⅱ Ⅱ Ⅱ
且"丛
答案
A B C D E
题号 n u 9 10 1|1 12 13 14
(3)产品纯度测定
答案
■
二、非选择题:本题共 4小 题,共 58分。 利用 Cao溶于醋酸,而 CaF2不溶于醋酸的性质提取 mg产 品中的CaF2,并用适当的溶剂将
15.(15分 )氟硅酸(H2siF6)是磷矿生产工艺中的副产物,工业上利用其与氨气反应经多次处理后 其配制成250 mL溶液,移取25.00 mL于锥形瓶中,用 Gm。loLˉ 1的 EDTA标 准溶液滴定至
制备CaF2,能提高磷矿伴生资源的有效利用,减少资源浪费。实验室模拟该制备过程制备CaF2。 终点,消耗 EDTA标 准溶液的体积为 ⒕ mL,做空白实验,消耗 EDTA标 准溶液的体积为
(1)制备 NH4F溶 液 %mL(已 知 :EDTA+Ca2+===[Ca(EDTA)]2+)。 产 品中 CaF2的 质量分数 为 %。
同
连接好装置(如图),经检查装置气密性良好,装入药品。点燃 A处 酒精灯,一段时间后,当 16.(15分 )铌是一种战略性关键金属,在航空航天、电子信息、新能源等领域有着广泛的应用。以
眇
观察到C中 溶液 pH为 13左右时,用塑料注射器缓慢滴加 20%氟 硅酸溶液。 高钛渣(含 Nb205、Ta205、Ti02、Ca0、 Mg0)为原料制取单质铌的流程如图所示
:
划 如 HF HCl MIBK H2S04、 提钽有机液 NH3
柙
pH传感器
Nb205
钽铌液
脚 高钛渣 沉铌 烘干 Nb
蒸馏水
CS2
H2TaF7
K
滤渣1
忸
已知:① MBK为 甲基异丁基酮;②钽铌液中含有 H2TaF7、 H2NbF7;③ Nb(0H)5难 溶于水
;
砰 |H A CS2 C D ④凡p(CaF2)=2.5× 10ˉ 11,Ksp(MgF2)=6.4× 10ˉ 9。
B
吓双
郴 已知:①氟硅酸是二元强酸
,易
分解为四氟化硅和氟化氢;② NH3不溶于CS2;③CS2的密度
(1)为提高高钛渣的酸溶速率,可 以采取的措施有
(翼少回答两种
比水大。 )。
尽 ;酸
①装置A中发生反应的化学方程式为
(2)潜澄 △的成分是 溶时若溶液酸度过高
,则
会导致沉淀不完全
,其
∶
翎 泛 韬 ②装置B和 C中 CS2的作用是否相同 ? (填 “ 是 ” 或 “ 否 ” );两装置中CS2的作用是
絮i因是
Ca2+~(填 “ ” “ ”
再"丬、 若溶液中c(Mg2+)=1× 10^2 mo1· L^1,则 是 或 否 )沉淀完全。
(3)沉铌时发生反应的化学方程式为
③三颈烧瓶中除生成NH4F,还会生成一种难溶于水的酸性氧化物,该反应的离子方程式是
(4)金属 Nb为 体心立方晶胞,晶体密度为8.58g· cm^3,则 Nb的原子半径为 ~pm(已 知
④三颈烧瓶内部表层需要涂一层石蜡,原 因是
托百
=3.3,福 =1.73)。
群
4f∶ (5)以 Nb205为 电极电解制备 Nb时 ,Nb205作 电解池的 _极 。某些研究人员在电解时选
驯
甾
(2)制备CaF2
择熔融的K2NbF7为电解质,以铁和石墨为电极材料,通过不断补充Nb205来制备Nb。
研究
姆
肛 发现,加人的Nb205会与 K2NbF7彼此作用生成氟氧铌酸钾(K3Nbo2F4),光 谱分析的结果显
将上述三颈烧瓶中的混合物倒出,过滤,取滤液于烧杯中,加人适量石灰乳,充
·
抑 示在电解的过程中还存在 Nb可 。
柙
分反应后,经过一系列操作得到含有少量Cao的 CaF2粗品。
碉 ①电解时的阳极材料为
①指出如图所示过滤操作中不规范之处
:
②电解时 极反应式为
,阳
化学猜题卷(六) 江西卷 第 5页(共8页 ) 化学猜题卷(六) 江西卷 第 6页(共8页 )②一系列操作过程中使用的仪器有 (填标号
(六 )。
化学猜题卷 )选择题答题区
「了
Ⅱ
兰Ⅱ
题号 2 3 4 r ● ^ ● 7 得分 巨 巨 Ⅱ Ⅱ Ⅱ Ⅱ
且"丛
答案
A B C D E
题号 n u 9 10 1|1 12 13 14
(3)产品纯度测定
答案
■
二、非选择题:本题共 4小 题,共 58分。 利用 Cao溶于醋酸,而 CaF2不溶于醋酸的性质提取 mg产 品中的CaF2,并用适当的溶剂将
15.(15分 )氟硅酸(H2siF6)是磷矿生产工艺中的副产物,工业上利用其与氨气反应经多次处理后 其配制成250 mL溶液,移取25.00 mL于锥形瓶中,用 Gm。loLˉ 1的 EDTA标 准溶液滴定至
制备CaF2,能提高磷矿伴生资源的有效利用,减少资源浪费。实验室模拟该制备过程制备CaF2。 终点,消耗 EDTA标 准溶液的体积为 ⒕ mL,做空白实验,消耗 EDTA标 准溶液的体积为
(1)制备 NH4F溶 液 %mL(已 知 :EDTA+Ca2+===[Ca(EDTA)]2+)。 产 品中 CaF2的 质量分数 为 %。
同
连接好装置(如图),经检查装置气密性良好,装入药品。点燃 A处 酒精灯,一段时间后,当 16.(15分 )铌是一种战略性关键金属,在航空航天、电子信息、新能源等领域有着广泛的应用。以
眇
观察到C中 溶液 pH为 13左右时,用塑料注射器缓慢滴加 20%氟 硅酸溶液。 高钛渣(含 Nb205、Ta205、Ti02、Ca0、 Mg0)为原料制取单质铌的流程如图所示
:
划 如 HF HCl MIBK H2S04、 提钽有机液 NH3
柙
pH传感器
Nb205
钽铌液
脚 高钛渣 沉铌 烘干 Nb
蒸馏水
CS2
H2TaF7
K
滤渣1
忸
已知:① MBK为 甲基异丁基酮;②钽铌液中含有 H2TaF7、 H2NbF7;③ Nb(0H)5难 溶于水
;
砰 |H A CS2 C D ④凡p(CaF2)=2.5× 10ˉ 11,Ksp(MgF2)=6.4× 10ˉ 9。
B
吓双
郴 已知:①氟硅酸是二元强酸
,易
分解为四氟化硅和氟化氢;② NH3不溶于CS2;③CS2的密度
(1)为提高高钛渣的酸溶速率,可 以采取的措施有
(翼少回答两种
比水大。 )。
尽 ;酸
①装置A中发生反应的化学方程式为
(2)潜澄 △的成分是 溶时若溶液酸度过高
,则
会导致沉淀不完全
,其
∶
翎 泛 韬 ②装置B和 C中 CS2的作用是否相同 ? (填 “ 是 ” 或 “ 否 ” );两装置中CS2的作用是
絮i因是
Ca2+~(填 “ ” “ ”
再"丬、 若溶液中c(Mg2+)=1× 10^2 mo1· L^1,则 是 或 否 )沉淀完全。
(3)沉铌时发生反应的化学方程式为
③三颈烧瓶中除生成NH4F,还会生成一种难溶于水的酸性氧化物,该反应的离子方程式是
(4)金属 Nb为 体心立方晶胞,晶体密度为8.58g· cm^3,则 Nb的原子半径为 ~pm(已 知
④三颈烧瓶内部表层需要涂一层石蜡,原 因是
托百
=3.3,福 =1.73)。
群
4f∶ (5)以 Nb205为 电极电解制备 Nb时 ,Nb205作 电解池的 _极 。某些研究人员在电解时选
驯
甾
(2)制备CaF2
择熔融的K2NbF7为电解质,以铁和石墨为电极材料,通过不断补充Nb205来制备Nb。
研究
姆
肛 发现,加人的Nb205会与 K2NbF7彼此作用生成氟氧铌酸钾(K3Nbo2F4),光 谱分析的结果显
将上述三颈烧瓶中的混合物倒出,过滤,取滤液于烧杯中,加人适量石灰乳,充
·
抑 示在电解的过程中还存在 Nb可 。
柙
分反应后,经过一系列操作得到含有少量Cao的 CaF2粗品。
碉 ①电解时的阳极材料为
①指出如图所示过滤操作中不规范之处
:
②电解时 极反应式为
,阳
化学猜题卷(六) 江西卷 第 5页(共8页 ) 化学猜题卷(六) 江西卷 第 6页(共8页 )17.(14分 )头孢呋辛酯 (H)是一种第二代口服头孢菌素抗生素,其合成路线如下 : p(C2H2)/MPa p(H2)/MPa v逆 /(MPa· min-1)
H勺~N 、| ~|/ S `| 0.05 P1 4
0 r1、丿 0^ 垆
^ N、
| 彡
人\
CH20H p2 2.4
k·
0 NOCH。 C00H
` `〃一 0Α ) ` 少 CH2C 0 12 厂 ′ B 0 辶 / ~C ‖ — C00H N≡兰 lfIL二 三望工 《 C I、 ~世 — C00H22|£ L>D (2) E CSI 表中P2= ` , 2 该温度下凡 逆= p1 MPaˉ 16 J^ o m^1 n- 1 。
②反应 I达平衡后 ,温度由r1降到r2,再达平衡
,凡
正
1`凡
正2和 凡 逆
1`凡
逆2分别代表r1、r2时的正、
NOCH2 NOCH”
^` || ˇ
《 厂
。
》 -C-COHN s 《 。 》-C—COHN`「 .'δ、 逆反应速率常数
,
儿
凡
正2 (填 “ >” “ (”或 “ =” )。
N (1)DMF/KHC03
逆2
C00H ro、
O Br 0ˇ
0 ==
|
C
' CH20CONH2 (3)200℃ 时,向 2L恒 容密闭容器中充入 C2H2(分压为
6。
0 kPa)、H2(分压为4.8 kPa)和一定
F
`乙` / I人I 。
G
八I \
人
0 量 He,只发生反应Ⅱ,体系的总压强随反应时间的变化如图所示。
H 0
排
已知 :R-C00H+SOC12-→ R-COCl+s02+HCl 12
曰
(1)B的 分子式为 ,G中 官能团的名称为 《 山 11 舀
田 10
舶 9
(2)D的
结构简式为
峪
(3)F生 成 H的 反应类型为 ,KHC03的 作用为 0 1000 2000
反应时间/s
)=
2A(g)Fe:(g) △
①200℃ 时,反应Ⅱ的标准压强平衡常数 硝 。[已知反应
(4)E在 酸性条件下能形成内酯,反应的化学方程式为 r 'i、 、 ' 旧)△
的标准压强平衡常数
K.吕
=岂
?于劳钅 ‰十
,其中
P°
为标准压强(100 kPa),P(A)和 P(B)为平 丬
衡分压(某成分的物质的量分数×总压)]
删
(5)满足下列条件的 C的 同分异构体有 种。
②若将容器改为绝热容器
,初
始温度为200℃
,其
他条件不变
,达
到新平衡时
,乙
烯产率将
①属于芳香族化合物,且 苯环上有两种环境的氢原子
啉
“ ”“ ” “ ”
————||— (填 增大 减小 或 不变
②与Fec13溶液会发生显色反应 .i|i|— )。
③含有一 NH2、不含有过氧键 (-0—0-),一 定条件下会发生水解反应,但 不会发生银镜
(4)在恒温恒容条件下发生反应Ⅲ,下列说法正确的是 渊
A.使用高效催化剂能提高乙烯的平衡产率
反应
B.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
(任
其中核磁共振氢谱图中峰面积之比为2:2:2:1的 是 写一种
)。
C.压强不再变化,说明反应达到平衡状态
18.(14分 )以 甲烷为原料可制得工业生产的重要化工原料乙烯、乙炔。主要反应如下
:
D.其他条件不变,增大压强,平衡常数减小
反应 I:2CH4(g)==£2H2(g)+3H2(g) ΔⅡ
1 (5)C2H2和 02构成的燃料电池的结构示意图如图,M极的电极反应式为
压L应 Ⅱ:C2H2(g)+H2(g)了 =土C2H4(g) ΔⅡ2=-174.4 kJ o molˉ 1
反:应 Ⅲ :2CH4(g)==主 C2H4(g)+2H2(g) ΔⅡ3=+202.0 kJ o molˉ 1 M
(1)ΔⅡ1=
kJ·
molˉ1。
H+ -b
a—
(2)①r1温度下 ,反应 I的 v正 =凡正 · P2(CH4),v逆 =佬逆 °p(C2H2)· P3(H2),凡正 逆分别为正、逆
`凡
反应速率常数 ,部分数据如表所示 。 质子交换膜
化学猜题卷(六) 江西卷 第7页(共 8页
)
化学猜题卷(六) 江西卷 第 8页(共 8页
)17.(14分 )头孢呋辛酯 (H)是一种第二代口服头孢菌素抗生素,其合成路线如下 : p(C2H2)/MPa p(H2)/MPa v逆 /(MPa· min-1)
H勺~N 、| ~|/ S `| 0.05 P1 4
0 r1、丿 0^ 垆
^ N、
| 彡
人\
CH20H p2 2.4
k·
0 NOCH。 C00H
` `〃一 0Α ) ` 少 CH2C 0 12 厂 ′ B 0 辶 / ~C ‖ — C00H N≡兰 lfIL二 三望工 《 C I、 ~世 — C00H22|£ L>D (2) E CSI 表中P2= ` , 2 该温度下凡 逆= p1 MPaˉ 16 J^ o m^1 n- 1 。
②反应 I达平衡后 ,温度由r1降到r2,再达平衡
,凡
正
1`凡
正2和 凡 逆
1`凡
逆2分别代表r1、r2时的正、
NOCH2 NOCH”
^` || ˇ
《 厂
。
》 -C-COHN s 《 。 》-C—COHN`「 .'δ、 逆反应速率常数
,
儿
凡
正2 (填 “ >” “ (”或 “ =” )。
N (1)DMF/KHC03
逆2
C00H ro、
O Br 0ˇ
0 ==
|
C
' CH20CONH2 (3)200℃ 时,向 2L恒 容密闭容器中充入 C2H2(分压为
6。
0 kPa)、H2(分压为4.8 kPa)和一定
F
`乙` / I人I 。
G
八I \
人
0 量 He,只发生反应Ⅱ,体系的总压强随反应时间的变化如图所示。
H 0
排
已知 :R-C00H+SOC12-→ R-COCl+s02+HCl 12
曰
(1)B的 分子式为 ,G中 官能团的名称为 《 山 11 舀
田 10
舶 9
(2)D的
结构简式为
峪
(3)F生 成 H的 反应类型为 ,KHC03的 作用为 0 1000 2000
反应时间/s
)=
2A(g)Fe:(g) △
①200℃ 时,反应Ⅱ的标准压强平衡常数 硝 。[已知反应
(4)E在 酸性条件下能形成内酯,反应的化学方程式为 r 'i、 、 ' 旧)△
的标准压强平衡常数
K.吕
=岂
?于劳钅 ‰十
,其中
P°
为标准压强(100 kPa),P(A)和 P(B)为平 丬
衡分压(某成分的物质的量分数×总压)]
删
(5)满足下列条件的 C的 同分异构体有 种。
②若将容器改为绝热容器
,初
始温度为200℃
,其
他条件不变
,达
到新平衡时
,乙
烯产率将
①属于芳香族化合物,且 苯环上有两种环境的氢原子
啉
“ ”“ ” “ ”
————||— (填 增大 减小 或 不变
②与Fec13溶液会发生显色反应 .i|i|— )。
③含有一 NH2、不含有过氧键 (-0—0-),一 定条件下会发生水解反应,但 不会发生银镜
(4)在恒温恒容条件下发生反应Ⅲ,下列说法正确的是 渊
A.使用高效催化剂能提高乙烯的平衡产率
反应
B.升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
(任
其中核磁共振氢谱图中峰面积之比为2:2:2:1的 是 写一种
)。
C.压强不再变化,说明反应达到平衡状态
18.(14分 )以 甲烷为原料可制得工业生产的重要化工原料乙烯、乙炔。主要反应如下
:
D.其他条件不变,增大压强,平衡常数减小
反应 I:2CH4(g)==£2H2(g)+3H2(g) ΔⅡ
1 (5)C2H2和 02构成的燃料电池的结构示意图如图,M极的电极反应式为
压L应 Ⅱ:C2H2(g)+H2(g)了 =土C2H4(g) ΔⅡ2=-174.4 kJ o molˉ 1
反:应 Ⅲ :2CH4(g)==主 C2H4(g)+2H2(g) ΔⅡ3=+202.0 kJ o molˉ 1 M
(1)ΔⅡ1=
kJ·
molˉ1。
H+ -b
a—
(2)①r1温度下 ,反应 I的 v正 =凡正 · P2(CH4),v逆 =佬逆 °p(C2H2)· P3(H2),凡正 逆分别为正、逆
`凡
反应速率常数 ,部分数据如表所示 。 质子交换膜
化学猜题卷(六) 江西卷 第7页(共 8页
)
化学猜题卷(六) 江西卷 第 8页(共 8页
)绝密★启用前 4.合成某药物的中间体Ⅹ的结构简式如图。下列说法正确的是
2024年 A。 存在 4种 官能团 0H
江西省 普通高中学业水平边择性考试
B.所有碳原子可能共平面
化学猜题卷 (七
C.存在立体异构现象 H
) D。 1 mol Ⅹ与足量钠反应生成2m。l H2
5.下列实验方案能达到相应实验目的的是
国命题报告
■
艹 '命题人猜想:本试卷的命制遵循《高考评价体系》指导思想,试题素材关注社会发展热点,符合新课标下高考命题方
稀硫酸
向,充分反映了新高考化学的命题趋势,引 导考生关注社会发展,夯实基础,把握命题方向,提升基本技能,培养考生
— ) — )
0.1 mol· L-1 us04溶液
的独立思考和解决问题的能力,提高考生灵活运用知识的能力。 Na0H溶
液
命题新思维:第 5题考查实验基本操作,考查考生的实验操作能力;第 8题打破考生思维,加热可加快反应速率,但
要考虑副反应的影响;第 10题引入防倒吸新装置,要求考生调动所学知识进行辨证分析。
aCO
蛋白质溶液
本试卷满分 100分。考试时间75分 钟。
饱和Nacl溶液
/Δ
C
酚
l溶
酞
液 3
)
唰
可能用到的相对原子质量:H-1 C—12 N-14 0-16 S-32 Cl-35.5 Fe-56 Co-59 甲 乙 `肖 丙 丁
HC1 B。
巾 Ni—59 Cu—64 Ga-70 La-139 A。 用甲装置除去 C12中 的 用乙装置测定某盐酸浓度
划 铷
铷 -、选择题:本题共14小题,每小题3分
,共
42分。在每小题给出的四个选项中,只有一项符合题目 C.用丙装置制取并收集大量 C02气体 D。 用丁装置进行蛋白质的盐析实验
6.ⅣA为阿伏加德罗常数的值,下列说法错误的是
钳 要求。
1.中华文化中蕴含许多化学知识,下列说法正确的是 A。 标准状况下,22.4 L CH4与 C12充分反应后,生成的含碳气体分子的数目为Ⅳ A
阡 “ ”
B.2.6g乙 炔与苯的混合物完全燃烧,转移电子数为Ⅳ
A
A。 火树银花不夜天 指的是某些金属元素的焰色试验,属于化学变化 1CH3C00Na溶
“ ” “ ” C。 1LO.1 mol· Lˉ 液中,阴离子数目大于 0。 1Ⅳ A
岬 逻 B。
杨花榆荚无才思 中 榆荚 的主要成分纤维素的最终水解产物为葡萄糖
D。 1 mol C60中 所含σ键数目为90Ⅳ A
甘 吓× 爿 C。 “ (汞)得火即飞,不见垢尘。 …… 将欲制之,黄芽为根 ” ,可知汞溶于硫 7.一种用作锂离子电池电解液的锂盐结构如图所示 ,Ⅹ 、Y、Z、 W为 原子序数依次增大的短周期主族
郴 D。 “ 冬灰,乃冬月灶中所烧薪柴之灰也。 …… 今人以灰淋汁,取硷(碱 )浣衣 ” ,可知薪柴之灰中含 元素,基态 W原 子的s和 p能级电子数之比为2:3。 下列说法错误的是
不 2.下列
大
化
量
学
K
事
OH
实不符合 “ 量变引起质变 ” 哲学观点的是
A
B C 。
。
.简 最
电
学 高
负
价 胃
性
子 氧
:Y
化 半
)Ⅹ
径 物对 :Y 应 ) 水 Z 化 物 的 酸 性 : Ⅹ ( W [ Ti+|
「Y
Y
`
' — Ⅹ Ⅹ / `
Y
Y \ / — —
Z —
l哂 \ / 厂
孓
丫 ` / Ⅹ Ⅹ —
'
`
Y
Y
啦 帮 A。 加热条件下,Fe与浓硝酸反应先生成 N02气 体,后有 N0气 体生成 D.Z的 氢化物不能与Si02发生反应 Z
〓粼
μ
一啐 B。 向Cuso4溶液中滴入氨水,先产生蓝色沉淀后沉淀消失 8.工业上,利用硫酸亚铁为原料,通过铁黄 (FeooH,一 种不溶于水的黄色固体)制 各高铁酸钾
C。
葡萄糖(单糖)能发生银镜反应,但纤维素(多糖)不能发生银镜反应 (K2Fe04),可 降低生产成本且产品质量优。工艺流程如下
:
D。
向含淀粉的KI溶液中通人 C12,溶液先变蓝,后褪色 催化剂
NaoH浓溶液 KCl饱和溶液
FeS04
3.很多物质在空气中都会发生化学变化,下列有关反应方程式和反应类型均正确的是 各铁黄
溶液
制各 制备 过滤
粗产品
邱
选项 化学变化 反应方程式 反应类型 NaOH N|
鸟Fe04
舯 溶液 带刂备Naclo
驯 2C10^+C02+H20===2HC10+CO:^ 水解反应
甾 A 漂白液失效 气
邱 2HC10兰 平兰昭≡2H++2Cl^+02↑ 分解反应
下列说法错误的是
肛
· B 白磷自燃 P4+502≡ J狱 ≡ J ≡ 降 =2P2o5 氧化还原反应 A。 制各 K2Feo4的反应类型为复分解反应
抑
押 C 硫酸型酸雨的 pH变 小 2SO:^+02====2SOlˉ 化合反应 B。 铁黄制备Na2Fe04的离子方程式为2FeooH+3C10ˉ +40Hˉ ===2FeOl^+3Clˉ +3H20
碉 Nac1o时
D 苯酚逐渐变成粉红色 2 H+02— → 氧化反应 C。 制备 ,可通过加热的方式加快反应速率
D.高 铁酸钾可作水处理剂 ,既能杀菌消毒,又能絮凝净水
化学猜题卷(七) 江西卷 第 1页(共8页 化学猜题卷(七) 江西卷 第2页(共8页
) )绝密★启用前 4.合成某药物的中间体Ⅹ的结构简式如图。下列说法正确的是
2024年 A。 存在 4种 官能团 0H
江西省 普通高中学业水平边择性考试
B.所有碳原子可能共平面
化学猜题卷 (七
C.存在立体异构现象 H
) D。 1 mol Ⅹ与足量钠反应生成2m。l H2
5.下列实验方案能达到相应实验目的的是
国命题报告
■
艹 '命题人猜想:本试卷的命制遵循《高考评价体系》指导思想,试题素材关注社会发展热点,符合新课标下高考命题方
稀硫酸
向,充分反映了新高考化学的命题趋势,引 导考生关注社会发展,夯实基础,把握命题方向,提升基本技能,培养考生
— ) — )
0.1 mol· L-1 us04溶液
的独立思考和解决问题的能力,提高考生灵活运用知识的能力。 Na0H溶
液
命题新思维:第 5题考查实验基本操作,考查考生的实验操作能力;第 8题打破考生思维,加热可加快反应速率,但
要考虑副反应的影响;第 10题引入防倒吸新装置,要求考生调动所学知识进行辨证分析。
aCO
蛋白质溶液
本试卷满分 100分。考试时间75分 钟。
饱和Nacl溶液
/Δ
C
酚
l溶
酞
液 3
)
唰
可能用到的相对原子质量:H-1 C—12 N-14 0-16 S-32 Cl-35.5 Fe-56 Co-59 甲 乙 `肖 丙 丁
HC1 B。
巾 Ni—59 Cu—64 Ga-70 La-139 A。 用甲装置除去 C12中 的 用乙装置测定某盐酸浓度
划 铷
铷 -、选择题:本题共14小题,每小题3分
,共
42分。在每小题给出的四个选项中,只有一项符合题目 C.用丙装置制取并收集大量 C02气体 D。 用丁装置进行蛋白质的盐析实验
6.ⅣA为阿伏加德罗常数的值,下列说法错误的是
钳 要求。
1.中华文化中蕴含许多化学知识,下列说法正确的是 A。 标准状况下,22.4 L CH4与 C12充分反应后,生成的含碳气体分子的数目为Ⅳ A
阡 “ ”
B.2.6g乙 炔与苯的混合物完全燃烧,转移电子数为Ⅳ
A
A。 火树银花不夜天 指的是某些金属元素的焰色试验,属于化学变化 1CH3C00Na溶
“ ” “ ” C。 1LO.1 mol· Lˉ 液中,阴离子数目大于 0。 1Ⅳ A
岬 逻 B。
杨花榆荚无才思 中 榆荚 的主要成分纤维素的最终水解产物为葡萄糖
D。 1 mol C60中 所含σ键数目为90Ⅳ A
甘 吓× 爿 C。 “ (汞)得火即飞,不见垢尘。 …… 将欲制之,黄芽为根 ” ,可知汞溶于硫 7.一种用作锂离子电池电解液的锂盐结构如图所示 ,Ⅹ 、Y、Z、 W为 原子序数依次增大的短周期主族
郴 D。 “ 冬灰,乃冬月灶中所烧薪柴之灰也。 …… 今人以灰淋汁,取硷(碱 )浣衣 ” ,可知薪柴之灰中含 元素,基态 W原 子的s和 p能级电子数之比为2:3。 下列说法错误的是
不 2.下列
大
化
量
学
K
事
OH
实不符合 “ 量变引起质变 ” 哲学观点的是
A
B C 。
。
.简 最
电
学 高
负
价 胃
性
子 氧
:Y
化 半
)Ⅹ
径 物对 :Y 应 ) 水 Z 化 物 的 酸 性 : Ⅹ ( W [ Ti+|
「Y
Y
`
' — Ⅹ Ⅹ / `
Y
Y \ / — —
Z —
l哂 \ / 厂
孓
丫 ` / Ⅹ Ⅹ —
'
`
Y
Y
啦 帮 A。 加热条件下,Fe与浓硝酸反应先生成 N02气 体,后有 N0气 体生成 D.Z的 氢化物不能与Si02发生反应 Z
〓粼
μ
一啐 B。 向Cuso4溶液中滴入氨水,先产生蓝色沉淀后沉淀消失 8.工业上,利用硫酸亚铁为原料,通过铁黄 (FeooH,一 种不溶于水的黄色固体)制 各高铁酸钾
C。
葡萄糖(单糖)能发生银镜反应,但纤维素(多糖)不能发生银镜反应 (K2Fe04),可 降低生产成本且产品质量优。工艺流程如下
:
D。
向含淀粉的KI溶液中通人 C12,溶液先变蓝,后褪色 催化剂
NaoH浓溶液 KCl饱和溶液
FeS04
3.很多物质在空气中都会发生化学变化,下列有关反应方程式和反应类型均正确的是 各铁黄
溶液
制各 制备 过滤
粗产品
邱
选项 化学变化 反应方程式 反应类型 NaOH N|
鸟Fe04
舯 溶液 带刂备Naclo
驯 2C10^+C02+H20===2HC10+CO:^ 水解反应
甾 A 漂白液失效 气
邱 2HC10兰 平兰昭≡2H++2Cl^+02↑ 分解反应
下列说法错误的是
肛
· B 白磷自燃 P4+502≡ J狱 ≡ J ≡ 降 =2P2o5 氧化还原反应 A。 制各 K2Feo4的反应类型为复分解反应
抑
押 C 硫酸型酸雨的 pH变 小 2SO:^+02====2SOlˉ 化合反应 B。 铁黄制备Na2Fe04的离子方程式为2FeooH+3C10ˉ +40Hˉ ===2FeOl^+3Clˉ +3H20
碉 Nac1o时
D 苯酚逐渐变成粉红色 2 H+02— → 氧化反应 C。 制备 ,可通过加热的方式加快反应速率
D.高 铁酸钾可作水处理剂 ,既能杀菌消毒,又能絮凝净水
化学猜题卷(七) 江西卷 第 1页(共8页 化学猜题卷(七) 江西卷 第2页(共8页
) )9.我 国科学家发明了一种Zn~Pb02电池,电解质为 K2S04、H2S04和 KOH,由 a和 b两种离子交换 为探究I^在 SO2歧化反应中的作用及
i、
ii反应速率与SO2歧化反应速率的关系,实验如下:分
膜隔开,形成A、B、 C三 个电解质溶液区域。已知:E为电池电动势[电池电动势即电池的理论电 别将 18 mL sO2饱和溶液加入到2 mL下列溶液中,密闭放置,观察到的现象如表所示。
压,是两个电极电位之差,E=E(十
)ˉ
E(一)],金 属的活
实验序号 溶液组成 实验现象
泼性越强,电极电位越低。下列说法错误的是
I KI
① 0.4 mol· Lˉ 溶液变黄,一段时间后出现浑浊
A B 。 .正 Zn 极 电 的 极 电 为 极 电 反 池 应 的 为 负极 Pb02+2eˉ +SOlˉ +4H+=== [‰(0H)4]| / ` 彳 逆 F 乡 F丿` 0。 4 mo1· Lˉ 1 KI,0.2 mol· Lˉ 1H2S04 溶液变黄 ,出 现浑浊较①快
A B (l ③ 0。 2 mol· L^1H2S04 无明显现象
Pbs04+2H20
1 KI,0。
pH减 ④ 0。 4 mol· Lˉ 000 2 mol I2 溶液由棕褐色快速变成黄色,出 现浑浊较①快
电池工作一段时间后 ,A区溶液 小,C区溶液
C。
pH增 下列说法错误的是
大
D.该电池与传统铅酸蓄电池相比较
,Ezn~Pb。2 中的单向阀 △
B D ○ O ·
.○
○
丬
N%s03
粉末 E Ⅲ
A
A。 实验时,应先打开装置
A中
分液漏斗的活塞 A·
H,被吸收时首先要在合金表面解离变成氢原子,同时吸收热量
呐
B。 “ 单向阀 ” 能用图 E装 置代替 B.该合金储氢后,含 1m。l La的合金吸收 H原 子的数目为2Ⅳ A
C应
C。 装置 采用冰水浴来控制温度 C.该合金吸收 H2后所得晶体的密度 876× 1021 gocm -3 渊
H2NS03H中 NH4Hs04杂 c3cⅣ
D。 用该装置制得的 可能含有 质 A
11.下列性质差异与结构因素匹配错误的是
钐
拗
钐
跣
叨
彻作
D.若选取飨瘛 为结构单元的底面,则其中间的截面为
选项 性质差异 结构因素
1H2R溶 ⒉
A Br2在 CC14中 的溶解度大于在 H20中 的 分子极性 14.25℃ 时,向 0.1m。loLˉ 液中滴加 KOH溶 液 ⒛
,
“
B si原子间难形成双键而 C原 子间可以 原子半径大小 混合溶液中离子浓度与 pH的 变化关系如图所示(已知 艹⒓
柴
m m ~~~「I ^ˉ△| l △l
C NC13(70℃ )沸点高于 NF3(-207℃ ) 键能大小 lg 2=0。 3)。 下列说法错误的是 o 驯
⑾
~L0ˉ」__ ˉ-ˉ|~ˉ~上~~上 __
D CH2(C00H)2中 α -H的 活性比 CH3C00H中 的高 吸电子基团多少 A。 a表示 1g C c( H H R 2 ˉ R) 随 pH变 化的曲线 冖 杯 骀 剞
12.理论上 SO2能发生歧化反应,但 SO2通人水中密封很久没有明显现象。资料显示I^可以催化 · ˉ2 弱 ˉˉ~I___上 ~
B.K砣 (H2R)=4× 10ˉ 11 剖
s02
S
发
O2
生
+4
歧
Iˉ
化反
+4
应
H+
,
=
歧
==
化
S↓
反应
+
分
2I
为
2
两
+2
步
H2
:
0
C.当溶液的 pH=7时 ,溶液中c(K+))3c(HRˉ
)
〓 H 剁
i。 4.4 54 6.474 84 9.410。4114
I2+2H20+SO2:===SOl^+4H++2I^ D。
当溶液的pH=8· 4时
,c(R2ˉ
)=c(H2R) pH
Ⅱ。
化学猜题卷(七) 江西卷 第 3页(共 8页 化学猜题卷(七) 江西卷 第 4页(共8页
) )9.我 国科学家发明了一种Zn~Pb02电池,电解质为 K2S04、H2S04和 KOH,由 a和 b两种离子交换 为探究I^在 SO2歧化反应中的作用及
i、
ii反应速率与SO2歧化反应速率的关系,实验如下:分
膜隔开,形成A、B、 C三 个电解质溶液区域。已知:E为电池电动势[电池电动势即电池的理论电 别将 18 mL sO2饱和溶液加入到2 mL下列溶液中,密闭放置,观察到的现象如表所示。
压,是两个电极电位之差,E=E(十
)ˉ
E(一)],金 属的活
实验序号 溶液组成 实验现象
泼性越强,电极电位越低。下列说法错误的是
I KI
① 0.4 mol· Lˉ 溶液变黄,一段时间后出现浑浊
A B 。 .正 Zn 极 电 的 极 电 为 极 电 反 池 应 的 为 负极 Pb02+2eˉ +SOlˉ +4H+=== [‰(0H)4]| / ` 彳 逆 F 乡 F丿` 0。 4 mo1· Lˉ 1 KI,0.2 mol· Lˉ 1H2S04 溶液变黄 ,出 现浑浊较①快
A B (l ③ 0。 2 mol· L^1H2S04 无明显现象
Pbs04+2H20
1 KI,0。
pH减 ④ 0。 4 mol· Lˉ 000 2 mol I2 溶液由棕褐色快速变成黄色,出 现浑浊较①快
电池工作一段时间后 ,A区溶液 小,C区溶液
C。
pH增 下列说法错误的是
大
D.该电池与传统铅酸蓄电池相比较
,Ezn~Pb。2 中的单向阀 △
B D ○ O ·
.○
○
丬
N%s03
粉末 E Ⅲ
A
A。 实验时,应先打开装置
A中
分液漏斗的活塞 A·
H,被吸收时首先要在合金表面解离变成氢原子,同时吸收热量
呐
B。 “ 单向阀 ” 能用图 E装 置代替 B.该合金储氢后,含 1m。l La的合金吸收 H原 子的数目为2Ⅳ A
C应
C。 装置 采用冰水浴来控制温度 C.该合金吸收 H2后所得晶体的密度 876× 1021 gocm -3 渊
H2NS03H中 NH4Hs04杂 c3cⅣ
D。 用该装置制得的 可能含有 质 A
11.下列性质差异与结构因素匹配错误的是
钐
拗
钐
跣
叨
彻作
D.若选取飨瘛 为结构单元的底面,则其中间的截面为
选项 性质差异 结构因素
1H2R溶 ⒉
A Br2在 CC14中 的溶解度大于在 H20中 的 分子极性 14.25℃ 时,向 0.1m。loLˉ 液中滴加 KOH溶 液 ⒛
,
“
B si原子间难形成双键而 C原 子间可以 原子半径大小 混合溶液中离子浓度与 pH的 变化关系如图所示(已知 艹⒓
柴
m m ~~~「I ^ˉ△| l △l
C NC13(70℃ )沸点高于 NF3(-207℃ ) 键能大小 lg 2=0。 3)。 下列说法错误的是 o 驯
⑾
~L0ˉ」__ ˉ-ˉ|~ˉ~上~~上 __
D CH2(C00H)2中 α -H的 活性比 CH3C00H中 的高 吸电子基团多少 A。 a表示 1g C c( H H R 2 ˉ R) 随 pH变 化的曲线 冖 杯 骀 剞
12.理论上 SO2能发生歧化反应,但 SO2通人水中密封很久没有明显现象。资料显示I^可以催化 · ˉ2 弱 ˉˉ~I___上 ~
B.K砣 (H2R)=4× 10ˉ 11 剖
s02
S
发
O2
生
+4
歧
Iˉ
化反
+4
应
H+
,
=
歧
==
化
S↓
反应
+
分
2I
为
2
两
+2
步
H2
:
0
C.当溶液的 pH=7时 ,溶液中c(K+))3c(HRˉ
)
〓 H 剁
i。 4.4 54 6.474 84 9.410。4114
I2+2H20+SO2:===SOl^+4H++2I^ D。
当溶液的pH=8· 4时
,c(R2ˉ
)=c(H2R) pH
Ⅱ。
化学猜题卷(七) 江西卷 第 3页(共 8页 化学猜题卷(七) 江西卷 第 4页(共8页
) )“ ”
①该流程在 反萃取 中,加 人氨水、水的目的是 。图 4流 程
化学猜题卷(七 )选择题答题区
中可回收利用的无机物是 (填化学式
)。
题号 2 n ˇ 4 5 ^ 0 7 得分 ②已知高铼酸铵是白色片状晶体,微溶于冷水,易溶于热水。若要得到纯度较高的高铼酸铵
答案 晶体,可通过在水中 的方法提纯。
题号 n u 0 ˇ 10 11 12 13 14 16.(15分 )化合物 M是 合成一种解热、镇咳药物的中间体,实验室合成 M的 一种路线如下
:
答案
■
二、非选择题:本题共4小题,共 58分。
15.(15分
)铼
(Re)是广泛应用于航空航天领域的重要金属,工业上可用高铼废料(含
Re、Res2、Fe、
Al叽
Ni0、Si02等 )来提取铼,工艺流程如图1:
气 稀 D 96 试剂Ⅹ
细叱
~
HCy
高铼废 热还原
M
同 水相 有机相
ˉ
图 1
巾
划 铷 已知:浸液中Fe元素以Fe3+形式存在,含有的 HRe%为 强酸 离子交换 ” 发生的反应可表示为QCl+ 回答下列问题
,“ :
舯 Reof=≡
QReo4+C1^。 (1)A→B的 目的是
甜 回答下列问题 CN
K (1)Fe在 元素周
:
期表中位于 (填 “ p” “ d”或 “ ds” )区。 (2)Cl /\ / 中σ键和π键个数比为
”
(2)“ 焙烧 时,Res2(S为 一1价 )发生反应的化学方程式为
”
(3)B→C的
化学方程式为
(3)“ 酸浸 所得浸渣的主要成分是
岬 逻 (4)其他条件相同时 离子交换 ” 过程中料液和 D296体 积比与铼交换率、铼交换量的关系如图 (4)M中 所含官能团的名称为 。 G为 链状分子,G→ H
慰 ,“
2所示;混合液的 pH与 ReOf提 取率的关系如图 3所 示。 的反应类型为
■ 郴
(5)有机物 A与 SO2(0CH3)2反应生成 B,相对分子质量更大的有机物B与 A相 比熔点反而下
180 '个 察
百
尽 术97.8 160 (=) ` 觯 98 降:请说明原因
睽
1 涨 0〔 卜
1
1
2
硐
0
Ⅱ
日
骒
ε
97 (6)W为 E的 同分异构体,同时满足下列条件的 W的 结构有 (写 出结构简式
,
郦 粼 攥 米 1巛 97.2 铼交换率 1 8 0 0 0 蟋 滴 滥 95 不考虑立体异构 )。
铼交换量 %
97 ω 米 i“ ①含有苯环,核磁共振氢谱有5组吸收峰;② 1m。 lW最 多能与2m。l NaHC03反应。
6:1 料 8: 液 1 和 10 D :1 2 % 体 12:1 积 比 14∶ 1 0.00.5 1.0 1. p 5 H 2.02.5
图2 图3
”
①由图推断 离子交换 选择的适宜条件为
,“ (7)请 补充完成以苯、乙醛和乙炔为原料合成CH呷 H H2的 路线(无机试剂任选
②其他条件相同,混合液的pH)1。 5时,ReOf的提取率降低的主要原因为 )。
督 0H
舯
”
剁 甾 (5)“ 反萃取 时加人的试剂 Ⅹ宜为 (填化学式 )。 (合成路线常用的表示方式为 A 反 反应 应 试 条 剂 件 B· ···· 反 反应 应 试 条件 剂 目标产物 )
邱
(6)另一种途径从炼铜的废液中提取铼,其简易工艺流程如图4(部分副产物省略,铼在废液中
肛
以ReOf形
式存在):
胂
·
萃 氨水、水
CH3CHO
CH≡≡CH
'
`
丿
`Ⅱ
HC==CH2
碉 柙 含铼 → 匠塑 | 囝 → 医正彐 →含铼 NH4Re04→Re207- H Re 一定条件 AlC13 II呷
有机相 溶液 0H
图4
化学猜题卷(七) 江西卷 第 5页(共8页 化学猜题卷(七) 江西卷 第 6页(共 8页
) )“ ”
①该流程在 反萃取 中,加 人氨水、水的目的是 。图 4流 程
化学猜题卷(七 )选择题答题区
中可回收利用的无机物是 (填化学式
)。
题号 2 n ˇ 4 5 ^ 0 7 得分 ②已知高铼酸铵是白色片状晶体,微溶于冷水,易溶于热水。若要得到纯度较高的高铼酸铵
答案 晶体,可通过在水中 的方法提纯。
题号 n u 0 ˇ 10 11 12 13 14 16.(15分 )化合物 M是 合成一种解热、镇咳药物的中间体,实验室合成 M的 一种路线如下
:
答案
■
二、非选择题:本题共4小题,共 58分。
15.(15分
)铼
(Re)是广泛应用于航空航天领域的重要金属,工业上可用高铼废料(含
Re、Res2、Fe、
Al叽
Ni0、Si02等 )来提取铼,工艺流程如图1:
气 稀 D 96 试剂Ⅹ
细叱
~
HCy
高铼废 热还原
M
同 水相 有机相
ˉ
图 1
巾
划 铷 已知:浸液中Fe元素以Fe3+形式存在,含有的 HRe%为 强酸 离子交换 ” 发生的反应可表示为QCl+ 回答下列问题
,“ :
舯 Reof=≡
QReo4+C1^。 (1)A→B的 目的是
甜 回答下列问题 CN
K (1)Fe在 元素周
:
期表中位于 (填 “ p” “ d”或 “ ds” )区。 (2)Cl /\ / 中σ键和π键个数比为
”
(2)“ 焙烧 时,Res2(S为 一1价 )发生反应的化学方程式为
”
(3)B→C的
化学方程式为
(3)“ 酸浸 所得浸渣的主要成分是
岬 逻 (4)其他条件相同时 离子交换 ” 过程中料液和 D296体 积比与铼交换率、铼交换量的关系如图 (4)M中 所含官能团的名称为 。 G为 链状分子,G→ H
慰 ,“
2所示;混合液的 pH与 ReOf提 取率的关系如图 3所 示。 的反应类型为
■ 郴
(5)有机物 A与 SO2(0CH3)2反应生成 B,相对分子质量更大的有机物B与 A相 比熔点反而下
180 '个 察
百
尽 术97.8 160 (=) ` 觯 98 降:请说明原因
睽
1 涨 0〔 卜
1
1
2
硐
0
Ⅱ
日
骒
ε
97 (6)W为 E的 同分异构体,同时满足下列条件的 W的 结构有 (写 出结构简式
,
郦 粼 攥 米 1巛 97.2 铼交换率 1 8 0 0 0 蟋 滴 滥 95 不考虑立体异构 )。
铼交换量 %
97 ω 米 i“ ①含有苯环,核磁共振氢谱有5组吸收峰;② 1m。 lW最 多能与2m。l NaHC03反应。
6:1 料 8: 液 1 和 10 D :1 2 % 体 12:1 积 比 14∶ 1 0.00.5 1.0 1. p 5 H 2.02.5
图2 图3
”
①由图推断 离子交换 选择的适宜条件为
,“ (7)请 补充完成以苯、乙醛和乙炔为原料合成CH呷 H H2的 路线(无机试剂任选
②其他条件相同,混合液的pH)1。 5时,ReOf的提取率降低的主要原因为 )。
督 0H
舯
”
剁 甾 (5)“ 反萃取 时加人的试剂 Ⅹ宜为 (填化学式 )。 (合成路线常用的表示方式为 A 反 反应 应 试 条 剂 件 B· ···· 反 反应 应 试 条件 剂 目标产物 )
邱
(6)另一种途径从炼铜的废液中提取铼,其简易工艺流程如图4(部分副产物省略,铼在废液中
肛
以ReOf形
式存在):
胂
·
萃 氨水、水
CH3CHO
CH≡≡CH
'
`
丿
`Ⅱ
HC==CH2
碉 柙 含铼 → 匠塑 | 囝 → 医正彐 →含铼 NH4Re04→Re207- H Re 一定条件 AlC13 II呷
有机相 溶液 0H
图4
化学猜题卷(七) 江西卷 第 5页(共8页 化学猜题卷(七) 江西卷 第 6页(共 8页
) )17.(14分 )三甲基镓[Ga(cH3)3]是 一种重要的半导体材料 GaN的 前驱体。实验室以镓镁合金 18.(14分 )乙烷是一种重要的化工原料,可用作制冷剂、燃料等。回答下列问题
:
(Ga2Mg5)、碘甲烷(CH3I)为原料制各Ga(cH3)3,实验步骤及装置(夹持及加热装置省去)如下 (1)已知 C2H6(g)==£2H4(g)+H2(g) ΔⅡ 相关物质的标准燃烧热和标准熵数值如下表。
: :i。 1。
C2H6(g) C2H4(g) H2(g)
物质
标准燃烧热(25℃
)/(kJ o mol^1)
1561 1411 286
标准熵 S/(J· mori -·1 了人'- 1 `丿 229.2 219.3 130.7
A
①ΔⅡ1=
②该反应能自发进行的温度 r> K(保留小数点后 1位
翻口 )。
J隋J性 ③1000℃ 时,在某刚性密闭容器内充入一定量的C2H6(g),发 生反应 反应自发进行的
气体 温度也可以计算了
C2H6(g)了土C2H4(g)+H2(g),若平衡时容器中总压为P
Pa,乙 烷的转
化率为α
,则
该反应的平衡常数凡= Pa(用含p、 α的代数式表示,用平衡分压代
向三颈烧瓶中加人 Ga2Mg5、CH3I和乙醚(Et20),加 热(55℃ )并搅拌30 min。 蒸出低沸点有机 替平衡浓度计算,分压=总压 ×物质的量分数 达到平衡后,欲同时增大反应速率和乙烷
)。 斟
物后减压蒸馏,收集 Ga(cH3)3· Et20。 向Ga(cH3)3· Et20中逐滴滴加三正辛胺(NR3),室温 的平衡转化率,可采取的措施有 (填 标号 )。
下搅拌 2~3h,并 用真空泵不断抽出Et20蒸气,制得Ga(cH3)3· NR3。 将 Ga(cH3)3· NR3置 A。 升高温度 B。 及时分离出产物 C.增 加乙烷浓度 D.加 人催化剂 舀
于真空中加热,蒸出Ga(cH3)3。 (2)乙烷催化氧化裂解法是一种新型的制备乙烯的方法:C2H6(g)+玄°2(g)=≡C2H4(g)+
燃
已知:①金属Ga的化学性质和Al相似,Ga的熔点为
29。
8℃
; H20(g) Δ 2=-105 kJ· mol^1。 反应产物中除了C2H4外 ,还存在 CH4、Co、 C等 副产物。
I叮
②常温下,Ga(cH3)3为无色透明的液体,易水解,在空气中易自燃 △
;
图1为温度对乙烷氧化裂解反应性能的影响,图 2为 的值对乙烷氧化裂解反应性
③相关物质的沸点信息如下。 讠京寸千
丬
能的影响。
物质 Ga(CH3)3 CH3I Et2 0 NR3
球
沸点/℃ 55。 7 42.4 34.6 365.8 100 ` 腓 Ⅲ
80 督 郴 08642 0 0 0 0 0 乙烷转化率
回答下列问题
60 型
: 聃
`
鞲
(1)仪器 A的 名称是 ,与分液漏斗相比,优点是 40 唰
杯
(2)上述实验需要在无水无氧的条件下进行,原因是 20 槲 醐
寒
0
撰
(3)三颈烧瓶中除生成 Ga(cH3)3· Et20外 ,还有 MgI2和 CH3 MgI生 成,该反应的化学方程式为 625 725 825 925 1.0 1.5 2.0 2.5 3.0 3.5
温度/℃ C2H6)/n(02)
图
1
图2以
<>乙
烷转化率 -乙 烯选择性 — 乙烯收率
(4)用真空泵不断抽出Et20蒸气,有利于Ga(cH3)3· NR3生成的理由是
~/r` IT `
已知:[C2H4选择性=页 ×100%;C2H4收率=C2H6转化率×C2H4选择性
(用平衡移动原理解释);与直接分解 Ga(cH3)3· Et20制备 Ga(cH3)3 瓦面 :丁赢 ]。
“ ” (填
相比,采用 NR3配 体交换 王艺制各的产品纯度更高的原因是 ①反应体系中,属于非极性分子的是 化学式
)。
(5)测定 Ga(cH3)3产品的纯度。取 而g Ga(CH3)3样 品于锥形瓶中,加入 y mLc m。 l。 L-1盐 ②乙烷的转化率随温度的升高而增大的原因是
酸,至不再产生气泡,加 入2滴 酚酞,用 c1m。l· Lˉ 1Na0H溶 液滴定剩余盐酸,消耗 NaoH溶 ③ 坠 。.rp △ IJ ≠ · 华 、 的值较低时,C2 H4的选择性较低的原因可能是
ˉ ·
而k U2丿
液的体积为 71 mL,则 Ga(cH3)3的质量分数为 (用含 m、y、 yl、 c、 cl的代数 ④最新研究发现在乙烷的氧化裂解反应体系中充人一定量C02能更好地提高乙烷的转化率
式表示);若滴定前滴定管尖嘴处没有气泡 ,滴定达终点时发现滴定管尖嘴内有气泡生成,则
和乙烯的收率,请结合方程式说明原因
“ ”“ ” “ ”
(填
测定结果 偏高 偏低 或 无影响
)。
化学猜题卷(七) 江西卷 第7页(共 8页 化学猜题卷(七) 江西卷 第 8页(共8页
) )17.(14分 )三甲基镓[Ga(cH3)3]是 一种重要的半导体材料 GaN的 前驱体。实验室以镓镁合金 18.(14分 )乙烷是一种重要的化工原料,可用作制冷剂、燃料等。回答下列问题
:
(Ga2Mg5)、碘甲烷(CH3I)为原料制各Ga(cH3)3,实验步骤及装置(夹持及加热装置省去)如下 (1)已知 C2H6(g)==£2H4(g)+H2(g) ΔⅡ 相关物质的标准燃烧热和标准熵数值如下表。
: :i。 1。
C2H6(g) C2H4(g) H2(g)
物质
标准燃烧热(25℃
)/(kJ o mol^1)
1561 1411 286
标准熵 S/(J· mori -·1 了人'- 1 `丿 229.2 219.3 130.7
A
①ΔⅡ1=
②该反应能自发进行的温度 r> K(保留小数点后 1位
翻口 )。
J隋J性 ③1000℃ 时,在某刚性密闭容器内充入一定量的C2H6(g),发 生反应 反应自发进行的
气体 温度也可以计算了
C2H6(g)了土C2H4(g)+H2(g),若平衡时容器中总压为P
Pa,乙 烷的转
化率为α
,则
该反应的平衡常数凡= Pa(用含p、 α的代数式表示,用平衡分压代
向三颈烧瓶中加人 Ga2Mg5、CH3I和乙醚(Et20),加 热(55℃ )并搅拌30 min。 蒸出低沸点有机 替平衡浓度计算,分压=总压 ×物质的量分数 达到平衡后,欲同时增大反应速率和乙烷
)。 斟
物后减压蒸馏,收集 Ga(cH3)3· Et20。 向Ga(cH3)3· Et20中逐滴滴加三正辛胺(NR3),室温 的平衡转化率,可采取的措施有 (填 标号 )。
下搅拌 2~3h,并 用真空泵不断抽出Et20蒸气,制得Ga(cH3)3· NR3。 将 Ga(cH3)3· NR3置 A。 升高温度 B。 及时分离出产物 C.增 加乙烷浓度 D.加 人催化剂 舀
于真空中加热,蒸出Ga(cH3)3。 (2)乙烷催化氧化裂解法是一种新型的制备乙烯的方法:C2H6(g)+玄°2(g)=≡C2H4(g)+
燃
已知:①金属Ga的化学性质和Al相似,Ga的熔点为
29。
8℃
; H20(g) Δ 2=-105 kJ· mol^1。 反应产物中除了C2H4外 ,还存在 CH4、Co、 C等 副产物。
I叮
②常温下,Ga(cH3)3为无色透明的液体,易水解,在空气中易自燃 △
;
图1为温度对乙烷氧化裂解反应性能的影响,图 2为 的值对乙烷氧化裂解反应性
③相关物质的沸点信息如下。 讠京寸千
丬
能的影响。
物质 Ga(CH3)3 CH3I Et2 0 NR3
球
沸点/℃ 55。 7 42.4 34.6 365.8 100 ` 腓 Ⅲ
80 督 郴 08642 0 0 0 0 0 乙烷转化率
回答下列问题
60 型
: 聃
`
鞲
(1)仪器 A的 名称是 ,与分液漏斗相比,优点是 40 唰
杯
(2)上述实验需要在无水无氧的条件下进行,原因是 20 槲 醐
寒
0
撰
(3)三颈烧瓶中除生成 Ga(cH3)3· Et20外 ,还有 MgI2和 CH3 MgI生 成,该反应的化学方程式为 625 725 825 925 1.0 1.5 2.0 2.5 3.0 3.5
温度/℃ C2H6)/n(02)
图
1
图2以
<>乙
烷转化率 -乙 烯选择性 — 乙烯收率
(4)用真空泵不断抽出Et20蒸气,有利于Ga(cH3)3· NR3生成的理由是
~/r` IT `
已知:[C2H4选择性=页 ×100%;C2H4收率=C2H6转化率×C2H4选择性
(用平衡移动原理解释);与直接分解 Ga(cH3)3· Et20制备 Ga(cH3)3 瓦面 :丁赢 ]。
“ ” (填
相比,采用 NR3配 体交换 王艺制各的产品纯度更高的原因是 ①反应体系中,属于非极性分子的是 化学式
)。
(5)测定 Ga(cH3)3产品的纯度。取 而g Ga(CH3)3样 品于锥形瓶中,加入 y mLc m。 l。 L-1盐 ②乙烷的转化率随温度的升高而增大的原因是
酸,至不再产生气泡,加 入2滴 酚酞,用 c1m。l· Lˉ 1Na0H溶 液滴定剩余盐酸,消耗 NaoH溶 ③ 坠 。.rp △ IJ ≠ · 华 、 的值较低时,C2 H4的选择性较低的原因可能是
ˉ ·
而k U2丿
液的体积为 71 mL,则 Ga(cH3)3的质量分数为 (用含 m、y、 yl、 c、 cl的代数 ④最新研究发现在乙烷的氧化裂解反应体系中充人一定量C02能更好地提高乙烷的转化率
式表示);若滴定前滴定管尖嘴处没有气泡 ,滴定达终点时发现滴定管尖嘴内有气泡生成,则
和乙烯的收率,请结合方程式说明原因
“ ”“ ” “ ”
(填
测定结果 偏高 偏低 或 无影响
)。
化学猜题卷(七) 江西卷 第7页(共 8页 化学猜题卷(七) 江西卷 第 8页(共8页
) )绝密★启用前 C.1 mol该物质最多消耗 2m。l Na0H
3个
2024年 D。 与足量氢气加成所得产物中,连有氧原子的碳原子中有 手性碳原子
江西省 普通高 中学业水平边择性考试
4。
下列不能正确描述其反应的离子方程式是
(八
化学猜题卷 A。 用 Fec13溶液清洗银镜 :Fe3++Ag+Cl^====Fe2++AgCl
)
B。
氢氧化亚铁露置在空气中变为红褐色 :4Fe(0H)2+02+2H20==-4Fe(0H)3
目 命题报告
■ “ 命题人猜想:本试卷以《高考评价体系》、课程标准、新教材等为依据,按照规定的知识和能力要求精心命制。试题 C。 向苯酚钠溶液中通入 C02,溶液变浑浊:2 ˉ +C02+H20— →2 H · +CO:ˉ
紧扣学科特点,考查化学用语,体现基础性,如第2题 ;试卷围绕化学学科素养,着力对综合能力进行考查,体现综合 D。 向K2Cr207溶液中滴加少量硫酸 ,溶 液橙色加深 :Cr2o;ˉ (橙色)+H20 Fe2crolˉ (黄色)+2H+
性和创新性,如第14题 ;降低数学计算要求,体现稳定性,如第17题考查平衡常数的计算表达式。 5.实验室几种常见仪器如图,下列仪器在相应实验中选用不合理的是
命题新角度:第 3题有附加条件的手性碳原子的判断;第 8题让考生结合图像分析各元素原子序数和原子半径大小
A。
粗盐提纯实验:③④⑤
关系,并根据判断的结果得出相应的结论;第 11题考查蒸发焓,角度新颖。 晷
B。
除杂、干燥、收集气体:②
命题新素材:第 12题通过最新研发的可充电生物质电池,考查电化学原理;第 15题以黏土钒矿为原料提取金属钒
唰 ,
C。
分离Mno2和 KCl的混合物:③④
考查自然资源的合理利用。
5%的 w v ③ ④ ⑤
巾 D。 配制 氯化钠溶液:①③
划 扣 本试卷满分 100分。考试时间 75分 钟。
舯
6.设 Ⅳ A为阿伏加德罗常数的值。下列说法正确的是
■ 路
可能用到的相对原子质量
:H-1 C-12 N— 14 0—16 Na—23 Mg—24 S-32 K—
39
A。
0.5 mol AsC13中 As原子价层电子对数为2Ⅳ
A
Ti—
48 Fe—56
K B.常温下,将 80 g s03与足量水充分反应,所得溶液中有 Ⅳ A个 H2S04分子
-、选择题 :本题共 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项是符合题 1 NaC10溶
C.0。 1 mol· Lˉ 液中C10^的数目一定小于0.1Ⅳ A
目要求的。
D。
1 mol CH4与 1m。l c12在光照下充分反应生成 CH3C1的分子数为Ⅳ
A
岬 逻 1.化学与生活、社会发展息息相关 ,下列有关说法错误的是
慰 根据下列实验操作及现象得出的结论错误的是
7。
A。 车辆使用的氢氧燃料电池将化学能直接转化为电能
■郴
选项 实验操作及现象 结论
B。 牙膏中添加氟化物用于预防龋齿
^
C.国产大飞机 C919用 到了铝锂合金,因为铝锂合金密度小、强度大、耐腐蚀 A
常温下,将铝片和镁片分别插人相同浓度的 NaoH溶 液中,前者
A1的金属性比 Mg强
产生无色气体,后者无明显现象
5G手
D。 我国某公司自主研发的 机芯片的主要成分是二氧化硅
ˉ 向盛有2 mL氯化铁溶液的试管中滴加浓的维生素 C溶 液,黄
郦 韬 2.下列化学用语的表达错误的是 B 维生素 C具 有还原性
秦
■ ~主 ·- α o | ~ ^ 0 C 将
色变
充有
为浅
N0
绿
2的
色
密闭烧瓶浸泡在热水中,烧瓶内气体颜色变深 N02生 成N204的反应为放热反应
A.2pz电子云轮廓图 亻 B.2一 甲基丁烷的球棍模型:飞
: 1卩 y
《
o阝
D
向浓度均为0。 1m。 1· L^1的 MgC12、 CuC12混合溶液中逐滴加人
Ksp[Mg(0H)2]>Ksp[Cu(0H)2]
NaOH溶
液,先出现蓝色沉淀
恻
邱
ˉ
督
照 8.已知前 18号元素 W、 Ⅹ、Y、 Z,在常温下,它们的最高价氧化物对应的水化物溶液(浓度均为
舯 C。 CaC12的电子式 :[CllˉCa2+[Cllˉ D。 乙醇的核磁共振氢谱 : 累 0。 01 mol· Lˉ 1)的 pH和 原子半径、原子序数的关系如图所示。下列说法 1
剁
^
U
甾
正确的是
邱 3.甲 氧沙林为皮肤抗感染药,临床上主要用于治疗白癜风、牛皮癣(银屑病),其结构简式如图所示。
W的
肛 A。 含氧酸均为强酸
· 下列有关该物质的说法错误的是 原 半径
:Y)Z
驷 B。 单质氧化性
柙
A。
分子式为 C12H:04
Y形
碉 C。 Ⅹ、 成的共价化合物中可能存在非极性键
不能使溴水褪色
B。 0 D。 Y2Z2分子中所有原子最外层均满足 8电 子稳定结构
化学猜题卷(八) 江西卷 第 1页(共 8页 化学猜题卷(八) 江西卷 第2页(共8页
) )绝密★启用前 C.1 mol该物质最多消耗 2m。l Na0H
3个
2024年 D。 与足量氢气加成所得产物中,连有氧原子的碳原子中有 手性碳原子
江西省 普通高 中学业水平边择性考试
4。
下列不能正确描述其反应的离子方程式是
(八
化学猜题卷 A。 用 Fec13溶液清洗银镜 :Fe3++Ag+Cl^====Fe2++AgCl
)
B。
氢氧化亚铁露置在空气中变为红褐色 :4Fe(0H)2+02+2H20==-4Fe(0H)3
目 命题报告
■ “ 命题人猜想:本试卷以《高考评价体系》、课程标准、新教材等为依据,按照规定的知识和能力要求精心命制。试题 C。 向苯酚钠溶液中通入 C02,溶液变浑浊:2 ˉ +C02+H20— →2 H · +CO:ˉ
紧扣学科特点,考查化学用语,体现基础性,如第2题 ;试卷围绕化学学科素养,着力对综合能力进行考查,体现综合 D。 向K2Cr207溶液中滴加少量硫酸 ,溶 液橙色加深 :Cr2o;ˉ (橙色)+H20 Fe2crolˉ (黄色)+2H+
性和创新性,如第14题 ;降低数学计算要求,体现稳定性,如第17题考查平衡常数的计算表达式。 5.实验室几种常见仪器如图,下列仪器在相应实验中选用不合理的是
命题新角度:第 3题有附加条件的手性碳原子的判断;第 8题让考生结合图像分析各元素原子序数和原子半径大小
A。
粗盐提纯实验:③④⑤
关系,并根据判断的结果得出相应的结论;第 11题考查蒸发焓,角度新颖。 晷
B。
除杂、干燥、收集气体:②
命题新素材:第 12题通过最新研发的可充电生物质电池,考查电化学原理;第 15题以黏土钒矿为原料提取金属钒
唰 ,
C。
分离Mno2和 KCl的混合物:③④
考查自然资源的合理利用。
5%的 w v ③ ④ ⑤
巾 D。 配制 氯化钠溶液:①③
划 扣 本试卷满分 100分。考试时间 75分 钟。
舯
6.设 Ⅳ A为阿伏加德罗常数的值。下列说法正确的是
■ 路
可能用到的相对原子质量
:H-1 C-12 N— 14 0—16 Na—23 Mg—24 S-32 K—
39
A。
0.5 mol AsC13中 As原子价层电子对数为2Ⅳ
A
Ti—
48 Fe—56
K B.常温下,将 80 g s03与足量水充分反应,所得溶液中有 Ⅳ A个 H2S04分子
-、选择题 :本题共 14小题,每小题 3分 ,共 42分 。在每小题给出的四个选项中,只有一项是符合题 1 NaC10溶
C.0。 1 mol· Lˉ 液中C10^的数目一定小于0.1Ⅳ A
目要求的。
D。
1 mol CH4与 1m。l c12在光照下充分反应生成 CH3C1的分子数为Ⅳ
A
岬 逻 1.化学与生活、社会发展息息相关 ,下列有关说法错误的是
慰 根据下列实验操作及现象得出的结论错误的是
7。
A。 车辆使用的氢氧燃料电池将化学能直接转化为电能
■郴
选项 实验操作及现象 结论
B。 牙膏中添加氟化物用于预防龋齿
^
C.国产大飞机 C919用 到了铝锂合金,因为铝锂合金密度小、强度大、耐腐蚀 A
常温下,将铝片和镁片分别插人相同浓度的 NaoH溶 液中,前者
A1的金属性比 Mg强
产生无色气体,后者无明显现象
5G手
D。 我国某公司自主研发的 机芯片的主要成分是二氧化硅
ˉ 向盛有2 mL氯化铁溶液的试管中滴加浓的维生素 C溶 液,黄
郦 韬 2.下列化学用语的表达错误的是 B 维生素 C具 有还原性
秦
■ ~主 ·- α o | ~ ^ 0 C 将
色变
充有
为浅
N0
绿
2的
色
密闭烧瓶浸泡在热水中,烧瓶内气体颜色变深 N02生 成N204的反应为放热反应
A.2pz电子云轮廓图 亻 B.2一 甲基丁烷的球棍模型:飞
: 1卩 y
《
o阝
D
向浓度均为0。 1m。 1· L^1的 MgC12、 CuC12混合溶液中逐滴加人
Ksp[Mg(0H)2]>Ksp[Cu(0H)2]
NaOH溶
液,先出现蓝色沉淀
恻
邱
ˉ
督
照 8.已知前 18号元素 W、 Ⅹ、Y、 Z,在常温下,它们的最高价氧化物对应的水化物溶液(浓度均为
舯 C。 CaC12的电子式 :[CllˉCa2+[Cllˉ D。 乙醇的核磁共振氢谱 : 累 0。 01 mol· Lˉ 1)的 pH和 原子半径、原子序数的关系如图所示。下列说法 1
剁
^
U
甾
正确的是
邱 3.甲 氧沙林为皮肤抗感染药,临床上主要用于治疗白癜风、牛皮癣(银屑病),其结构简式如图所示。
W的
肛 A。 含氧酸均为强酸
· 下列有关该物质的说法错误的是 原 半径
:Y)Z
驷 B。 单质氧化性
柙
A。
分子式为 C12H:04
Y形
碉 C。 Ⅹ、 成的共价化合物中可能存在非极性键
不能使溴水褪色
B。 0 D。 Y2Z2分子中所有原子最外层均满足 8电 子稳定结构
化学猜题卷(八) 江西卷 第 1页(共 8页 化学猜题卷(八) 江西卷 第2页(共8页
) )9.下列结构与性质或性质与用途具有对应关系的是 12.清华大学某科研团队利用糠醛创造了一种用于储电/发电,同时生产有价值化学品糠醇和糠酸
N=N键
A。
N2分子内含有 ,N2具有氧化性 (生成糠酸的反应为自发过程)的可充电生物质电池,其 工作原理如图所示。下列说法错误的是
B.snC14和 GaAs均由共价键构成,固态 Snc14和 GaAs都是分子晶体 ˉˉˉˉˉˉˉ
r∴rδ gˉ
I「 =ˉ
C.se是非金属元素,se单质可以用于制作半导体材料
D。
H20分 子中 0原 子含有孤电子对,可与 H+形成配位键
糠酸根 C0。 .2Ni。.:(0H)2
/
10.科学家开发了一种用二氧化碳淡化海水的技术,其循环图如图所示。下列有关叙述错误的是
r`桷 Q 疒
I
\
鹇
、@
`r)
海水
铮
Co。.2NiO.:00H
NaCl(aq)
KOH溶
RNH2 液
-HCl A。 该装置在生成糠酸时将化学能转化为电能
NaHC03 放电时,N极附近电解质溶液 pH减 小 排
B。
1o封
存或
+H+,-Na+ 循环 C.充电时,若外电路通过 1m。l电子,理论上阳极减轻 1g
出
A。
RNH2中 N原 子的杂化方式为sp3
B.“离子交换 ” 的原理为 RNH3HC03+NaCl===NaHC03+RNH3Cl↓ D.充电时,阴极电极反应为 +2eˉ +2H20==== +2C)Hˉ
雌
C.加热 RNH3Cl并用水吸收HCl可制盐酸 13.铁镁合金是目前已发现的储氢密度最高的储氢材料之一 ,其晶胞结构如图所示。该合金储氢后晶
D.上述转化中既有氧化还原反应,又有非氧化还原反应 体的化学式为FeMg2H2,储氢时,H2分子在晶胞的体心和棱的中心位置 ,ⅣA表示阿伏加德罗常数 △
11.探究不同结构 C4H90H中 存在分子间作用力的差异。室温下,三个温度传感器同时蘸取等体积 的值。下列说法错误的是
丬
样品,形成液膜,测得挥发时的温度 一时间曲线如下。
A。
上述晶体涉及的元素位于周期表 2个区
Ⅲ
2 2 6 6 . . 2 0 a.CH3CH2CH2CH20H B。 宙 表示 Fe原子 ,。 表示 Mg原 子
22222 55555 86420 CH^CH^CH0H
p
b. D‘
C。
1个 FeMg2H2晶胞的质量为群.里 g 聃
` a C|H3 i - 】VA
恻
照 C
|
H ^ °
D。
该合金中,与 Mg原 子等距离且最近的Fe原子有 4个 渊
24.8 c.H^C-C-0H
D |
2 2 4 4 . . 6 4 CH3 14.柠 檬酸 (H3Cit)是 一种重要 的三元有机 中强 酸。常温下,一定 pH范 围 内,存在 以下平衡 :
0 20 40 60 80 100120
时间/s H3Cit(s)(=尘H3Cit(aq);H3Cit(aq)t=土 H2Citˉ (aq)+H+(aq);H2Citˉ (aq)页=土 HCit2ˉ (aq)+
已知 :25℃ ,101 kPa时 ,C4H90H(l)====C4H90H(g)的 ΔⅡ 蒸发如表 。 H+(aq);HCit2ˉ (aq)了土 Cit3ˉ (aq)+H+(aq)。 平衡常数依次为 '` 三 Μ
C4H90H a 1 D C K。 J1=10ˉ 3· 13、K2=10ˉ ⒋ 76、 K3=10ˉ ⒍ 4° 。已知 lg c(x)[c(x)= ` 叫 0 ∞ Ν
ΔⅡ 蒸发/(kJ° mol^1) +52.3 +49.7 +46.7
pH变
。
c(H2Citˉ c(HCit2ˉ )或 c(Cit3ˉ )]随 化关系如图所示。下列 p
)、
1 。 L
下列说法正确的是
说法错误的是 回 剧回
.出
△曰闸型Ⅱ ·
A.c分子中 4个碳原子和 1个 0原 子构成平面四边形结构
A。 直线
L表
示 1g c(Cit3ˉ )随
pH的
变化 理理苕迸
B.a、b、 c在 Cu/o2催化条件下得到的产物种类相同 B。 一定 pH范 围内,随 pH增 大月3Cit(aq)的浓度不变 含溶孱军甚 | - 20
P点 pH为 3.72 沽 占 钮|陪涂
C.20~40s,Δ Ⅱ 蒸发越小的物质,单位时间内从环境中吸收的热量越少 C。 溶液 展舀裰骞磊
D。
该实验中,c的温度变化最大,其主要原因是 c挥发最快 D.4.76(pH(5。 58日寸,c(HCit2ˉ )>c(H2Citˉ ))c(Cit3ˉ )
化学猜题卷(八) 江西卷 第3页(共 8页 化学猜题卷(八) 江西卷 第 4页(共 8页
) )9.下列结构与性质或性质与用途具有对应关系的是 12.清华大学某科研团队利用糠醛创造了一种用于储电/发电,同时生产有价值化学品糠醇和糠酸
N=N键
A。
N2分子内含有 ,N2具有氧化性 (生成糠酸的反应为自发过程)的可充电生物质电池,其 工作原理如图所示。下列说法错误的是
B.snC14和 GaAs均由共价键构成,固态 Snc14和 GaAs都是分子晶体 ˉˉˉˉˉˉˉ
r∴rδ gˉ
I「 =ˉ
C.se是非金属元素,se单质可以用于制作半导体材料
D。
H20分 子中 0原 子含有孤电子对,可与 H+形成配位键
糠酸根 C0。 .2Ni。.:(0H)2
/
10.科学家开发了一种用二氧化碳淡化海水的技术,其循环图如图所示。下列有关叙述错误的是
r`桷 Q 疒
I
\
鹇
、@
`r)
海水
铮
Co。.2NiO.:00H
NaCl(aq)
KOH溶
RNH2 液
-HCl A。 该装置在生成糠酸时将化学能转化为电能
NaHC03 放电时,N极附近电解质溶液 pH减 小 排
B。
1o封
存或
+H+,-Na+ 循环 C.充电时,若外电路通过 1m。l电子,理论上阳极减轻 1g
出
A。
RNH2中 N原 子的杂化方式为sp3
B.“离子交换 ” 的原理为 RNH3HC03+NaCl===NaHC03+RNH3Cl↓ D.充电时,阴极电极反应为 +2eˉ +2H20==== +2C)Hˉ
雌
C.加热 RNH3Cl并用水吸收HCl可制盐酸 13.铁镁合金是目前已发现的储氢密度最高的储氢材料之一 ,其晶胞结构如图所示。该合金储氢后晶
D.上述转化中既有氧化还原反应,又有非氧化还原反应 体的化学式为FeMg2H2,储氢时,H2分子在晶胞的体心和棱的中心位置 ,ⅣA表示阿伏加德罗常数 △
11.探究不同结构 C4H90H中 存在分子间作用力的差异。室温下,三个温度传感器同时蘸取等体积 的值。下列说法错误的是
丬
样品,形成液膜,测得挥发时的温度 一时间曲线如下。
A。
上述晶体涉及的元素位于周期表 2个区
Ⅲ
2 2 6 6 . . 2 0 a.CH3CH2CH2CH20H B。 宙 表示 Fe原子 ,。 表示 Mg原 子
22222 55555 86420 CH^CH^CH0H
p
b. D‘
C。
1个 FeMg2H2晶胞的质量为群.里 g 聃
` a C|H3 i - 】VA
恻
照 C
|
H ^ °
D。
该合金中,与 Mg原 子等距离且最近的Fe原子有 4个 渊
24.8 c.H^C-C-0H
D |
2 2 4 4 . . 6 4 CH3 14.柠 檬酸 (H3Cit)是 一种重要 的三元有机 中强 酸。常温下,一定 pH范 围 内,存在 以下平衡 :
0 20 40 60 80 100120
时间/s H3Cit(s)(=尘H3Cit(aq);H3Cit(aq)t=土 H2Citˉ (aq)+H+(aq);H2Citˉ (aq)页=土 HCit2ˉ (aq)+
已知 :25℃ ,101 kPa时 ,C4H90H(l)====C4H90H(g)的 ΔⅡ 蒸发如表 。 H+(aq);HCit2ˉ (aq)了土 Cit3ˉ (aq)+H+(aq)。 平衡常数依次为 '` 三 Μ
C4H90H a 1 D C K。 J1=10ˉ 3· 13、K2=10ˉ ⒋ 76、 K3=10ˉ ⒍ 4° 。已知 lg c(x)[c(x)= ` 叫 0 ∞ Ν
ΔⅡ 蒸发/(kJ° mol^1) +52.3 +49.7 +46.7
pH变
。
c(H2Citˉ c(HCit2ˉ )或 c(Cit3ˉ )]随 化关系如图所示。下列 p
)、
1 。 L
下列说法正确的是
说法错误的是 回 剧回
.出
△曰闸型Ⅱ ·
A.c分子中 4个碳原子和 1个 0原 子构成平面四边形结构
A。 直线
L表
示 1g c(Cit3ˉ )随
pH的
变化 理理苕迸
B.a、b、 c在 Cu/o2催化条件下得到的产物种类相同 B。 一定 pH范 围内,随 pH增 大月3Cit(aq)的浓度不变 含溶孱军甚 | - 20
P点 pH为 3.72 沽 占 钮|陪涂
C.20~40s,Δ Ⅱ 蒸发越小的物质,单位时间内从环境中吸收的热量越少 C。 溶液 展舀裰骞磊
D。
该实验中,c的温度变化最大,其主要原因是 c挥发最快 D.4.76(pH(5。 58日寸,c(HCit2ˉ )>c(H2Citˉ ))c(Cit3ˉ )
化学猜题卷(八) 江西卷 第3页(共 8页 化学猜题卷(八) 江西卷 第 4页(共 8页
) )③相关物质的部分物理性质如表所示。
化学猜题卷(八 )选择题答题区
熔点/℃ 沸点/℃ 溶解性
题号 1 9 一 3 4 5 n 0 7 得分
TiC14 -23.2 136.4 极易水解生成白色沉淀,能溶于CC14等有机溶剂
答案
题号 8 9 10 11 12 13 14 FeC13 304 316 易水解生成红褐色沉淀
答案
■ CC14 -23 76.8 难溶于水
二、非选择题:本题共 4小 题,共 58分。
15。 (14分 )金属钒主要用于冶炼特种钢,被誉为
“
合金的维生素
”
。以黏土钒矿[主要成分为钒的+3、
回答下列问题
:
+4、 +5价 氧化物,Fe2o3及铝硅酸盐(A1203 0 Si02)等]为原料提取金属钒的工艺流程如下 (1)实验操作:①检查装置气密性;②将盛有 FeTio3和碳粉的瓷舟置于管式炉中;③依次通人
:
NaOH
KC103 Na2C03 溶液 HCl (NHD2s04 硅铁合金 cao
(填气体化学式),一段时间后接通冷凝管,加热开始反应,当观察到 (填
A中
实验现象)时 ,说明反应结束,停止加热管式炉。洗气瓶 的试剂为 。图示装置
唰 黏土钒矿 高温氧化 焙烧 浸取 调pH 沉钒 热解 Ⅴ|05 高温还原 钒
ˉ 中存在的缺陷是
巾 气体Ⅹ 滤渣 1 滤渣2 气体 Y 炉渣
删 洳 (1)Ⅴ 位于元素周期表第 周期 族。 (2)管式炉加热至900℃ ,瓷舟中发生的主要反应的化学方程式为
舯
“ ”
(2)写出 高温氧化 过程中Ⅴ203发生反应的化学方程式 (3)反应结束后的具体操作是停止加热管式炉、 ,停 止通冷凝水。
■ 脚
(3)“ 调 pH” 时生成的滤渣2的主要成分是 ___ (填 化学式
)。 Ⅱ。制备纳米Ti02
”
pH=8,pH不
(4)“沉钒 过程中,工业上调节溶液 宜过高的原因可能是
K
屐 ”
(4)①将锥形瓶中的液体混合物蒸馏后得到较为纯净的四氯化钛,将四氯化钛加人热水中得到
(5)“ 高温还原 时,硅参与反应的化学方程式为
蝉 ˉ (6)近年来,研究人员发现含钒的锑化物 M在 超导方面表现 卩=60° Ti02· 用20(不溶于水和稀酸),接下来进行如下操作:i。 过滤 ,ii。 (填 操作名
慰 出潜在的应用前景。 M晶 胞的结构如图所示。已知阿伏 称),Ⅱ 。干燥
,iv。
称重。得到固体氧化物mg。 操作 ii应在 (填标号)中进行。
● C
— 槲 加德罗常数的值为Ⅳ s
Ⅴ
A。 ●
ynm
1
尽
①
充在
晶胞
Sb
中
原
有
子
4
构
个
成
面
的
的面心由Ⅴ原
(
子
填
占
“
据
四
,
面
这
体
些
”
Ⅴ
或
原
“
八
子填
面
⑧ s b 一 一 b
郦 秦 ˉ 韬 ② 体 M ” 晶 )空 体 隙 的 中 密 。 度为 gocm -3 “nm 吵 个¢ ② Ti4 丶I亻 + 宀 午 还 乃 石 " 匚 原 得 为 mg固 Ti3+ 体 后 氧 过 化 滤 物 , 溶 加 于 人 足 几 量 滴 热的 KS 浓 C 硫 N溶 酸, 液 在 作 隔绝 指 空 示 气 剂 的 ,用 条件 O. 下 10 加 0 入 0 过 mo 量 l· 的铝 Lˉ 粉 1的 将
。
NH4Fe(S04)2标准溶液滴定至终点(将 Ti3+氧化为Ti4+),消耗NH4Fe(S04)2标 准溶液的体积为
16.(15分 )某小组在实验室中制备纳米Ti02。
I。
制备并收集TiC14(装置如图所示,夹持装置略去
)
y mL。 试样中所含Ti02的质量分数表达式为 ,下列关于测定结果的分析
,
说法正确的是 (填标号
)。
碱石灰
a。
若固体氧化物中含有少量铁元素,将导致测定结果偏低
N2
驯 b.若滴定速度过慢,将导致测定结果偏低
甾 k2
邱
c。
若滴定前仰视读数,滴定后俯视读数,将导致测定结果偏高
肛
A
· 管式炉 瓷舟
抑
柙 已知:①TiC14高温时能与02反应 ,遇水极易水解
碉 ;
②瓷舟中物质反应后除生成TiC14、FeC13外 ,还 生成一种不成盐氧化物和少量副产物 CC14;
化学猜题卷(八) 江西卷 第 5页(共 8页 化学猜题卷(八) 江西卷 第 6页(共 8页
) )③相关物质的部分物理性质如表所示。
化学猜题卷(八 )选择题答题区
熔点/℃ 沸点/℃ 溶解性
题号 1 9 一 3 4 5 n 0 7 得分
TiC14 -23.2 136.4 极易水解生成白色沉淀,能溶于CC14等有机溶剂
答案
题号 8 9 10 11 12 13 14 FeC13 304 316 易水解生成红褐色沉淀
答案
■ CC14 -23 76.8 难溶于水
二、非选择题:本题共 4小 题,共 58分。
15。 (14分 )金属钒主要用于冶炼特种钢,被誉为
“
合金的维生素
”
。以黏土钒矿[主要成分为钒的+3、
回答下列问题
:
+4、 +5价 氧化物,Fe2o3及铝硅酸盐(A1203 0 Si02)等]为原料提取金属钒的工艺流程如下 (1)实验操作:①检查装置气密性;②将盛有 FeTio3和碳粉的瓷舟置于管式炉中;③依次通人
:
NaOH
KC103 Na2C03 溶液 HCl (NHD2s04 硅铁合金 cao
(填气体化学式),一段时间后接通冷凝管,加热开始反应,当观察到 (填
A中
实验现象)时 ,说明反应结束,停止加热管式炉。洗气瓶 的试剂为 。图示装置
唰 黏土钒矿 高温氧化 焙烧 浸取 调pH 沉钒 热解 Ⅴ|05 高温还原 钒
ˉ 中存在的缺陷是
巾 气体Ⅹ 滤渣 1 滤渣2 气体 Y 炉渣
删 洳 (1)Ⅴ 位于元素周期表第 周期 族。 (2)管式炉加热至900℃ ,瓷舟中发生的主要反应的化学方程式为
舯
“ ”
(2)写出 高温氧化 过程中Ⅴ203发生反应的化学方程式 (3)反应结束后的具体操作是停止加热管式炉、 ,停 止通冷凝水。
■ 脚
(3)“ 调 pH” 时生成的滤渣2的主要成分是 ___ (填 化学式
)。 Ⅱ。制备纳米Ti02
”
pH=8,pH不
(4)“沉钒 过程中,工业上调节溶液 宜过高的原因可能是
K
屐 ”
(4)①将锥形瓶中的液体混合物蒸馏后得到较为纯净的四氯化钛,将四氯化钛加人热水中得到
(5)“ 高温还原 时,硅参与反应的化学方程式为
蝉 ˉ (6)近年来,研究人员发现含钒的锑化物 M在 超导方面表现 卩=60° Ti02· 用20(不溶于水和稀酸),接下来进行如下操作:i。 过滤 ,ii。 (填 操作名
慰 出潜在的应用前景。 M晶 胞的结构如图所示。已知阿伏 称),Ⅱ 。干燥
,iv。
称重。得到固体氧化物mg。 操作 ii应在 (填标号)中进行。
● C
— 槲 加德罗常数的值为Ⅳ s
Ⅴ
A。 ●
ynm
1
尽
①
充在
晶胞
Sb
中
原
有
子
4
构
个
成
面
的
的面心由Ⅴ原
(
子
填
占
“
据
四
,
面
这
体
些
”
Ⅴ
或
原
“
八
子填
面
⑧ s b 一 一 b
郦 秦 ˉ 韬 ② 体 M ” 晶 )空 体 隙 的 中 密 。 度为 gocm -3 “nm 吵 个¢ ② Ti4 丶I亻 + 宀 午 还 乃 石 " 匚 原 得 为 mg固 Ti3+ 体 后 氧 过 化 滤 物 , 溶 加 于 人 足 几 量 滴 热的 KS 浓 C 硫 N溶 酸, 液 在 作 隔绝 指 空 示 气 剂 的 ,用 条件 O. 下 10 加 0 入 0 过 mo 量 l· 的铝 Lˉ 粉 1的 将
。
NH4Fe(S04)2标准溶液滴定至终点(将 Ti3+氧化为Ti4+),消耗NH4Fe(S04)2标 准溶液的体积为
16.(15分 )某小组在实验室中制备纳米Ti02。
I。
制备并收集TiC14(装置如图所示,夹持装置略去
)
y mL。 试样中所含Ti02的质量分数表达式为 ,下列关于测定结果的分析
,
说法正确的是 (填标号
)。
碱石灰
a。
若固体氧化物中含有少量铁元素,将导致测定结果偏低
N2
驯 b.若滴定速度过慢,将导致测定结果偏低
甾 k2
邱
c。
若滴定前仰视读数,滴定后俯视读数,将导致测定结果偏高
肛
A
· 管式炉 瓷舟
抑
柙 已知:①TiC14高温时能与02反应 ,遇水极易水解
碉 ;
②瓷舟中物质反应后除生成TiC14、FeC13外 ,还 生成一种不成盐氧化物和少量副产物 CC14;
化学猜题卷(八) 江西卷 第 5页(共 8页 化学猜题卷(八) 江西卷 第 6页(共 8页
) )17。 (15分 )将各种易得的、廉价的资源进行催化重整,可 以实现资源的综合利用,对环境保护和实
⌒
τ
现双碳目标具有十分重要的意义。C02制甲醇的过程如下 0.24 M ·
:
1 D 冖山
ハ
r′孑兰`歹
日
i。
催化剂活化:In2o3(无活性)+%H2层
矿
In2°
3-·
(有活性)+%H20 a ·
辶 ③
ii。
C02与 H2在活化后的催化剂表面发生可逆反应①,其反应历程如图 1,同时伴随反应②
:
0
1 1.5 2 以H2) 叫
I.g冖
^ U 1 /(10^3K^1)
C02(g)+H2(g):===CO(g)+H20(g) ΔⅡ=+41。 2 kJ o molˉ 1。 图3 n(C02) 图 4 Ti厂
⑻
①c点时H2的转化率α(H2)=
%。
。 飞 6 — C⒒0H选择性
%℃ 。 — C02转化率 ②鸟 (b)= (写 计算表达式)kPa-2。
— △
、 ③c点时,再加人 C02和 H20(g),使 两者分压均增大0.05 kPa,H2的转化率
`
“ ”“ ” “ ”
鼬 (填 增大 不变 或 减小
)。
觏
H20(g) 擀 (5)已知AⅡhenius经验公式:Rln凡 =一 +C(Ea为 活化能 为速率常数,R和 C为常数 反 烨
H2(g) 加 丁 ,凡 )。
H2(g) /H
)
0 应①可通过反应②和反应③两步完成,反应②和反应③的有关数据如图 4所 示,Ea:反应 舀
ˉ “ “
② 反应③(填 >”或 (” );研究表明,加 人某极性介质有助于加快整个反应的
4000 6000 8000 10000 12000
燃
CH30H(g)
气体流速/(mL· h^1)
速率,原因可能是
图1 图2 18.(14分 )有机物G(C9H:04)是 生产某洗面奶的中间体,以 甲苯为原料合成有机物 G的 路线如下
: △
回答下列问题
: B
(1)已 知:反应①每生成 1m。l cH30H(g)放 热 49.0 kJ。 则反应③ CO(g)+2H2(g)了土 甲苯 A 一定条件 Nao r ` · ' · 上 1 2 C D E 丬
C7H6C12
光照
Nao CH3
CH3CH0
CH30H(g) ΔⅡ
=
稀NaoH溶液 旧
△
(2)C02和 H2的混合气体以不同的流速通过反应器,相同时间内C02转化率、 CH30H选 择性与气
G ①新帝刂Cu(oH)2 F 聃
体流速的关系如图2所示。
C9H:04 C9H603Na2
②H+
渊
已知:CH30H选择性 =L-」 三 :】 ∠空 .{:曩 2)× 1。 。%.。 已知:① C是 B的一氯代物 ;
甥品吴:晨
:∶ |;sl C° NaoH溶
②
RCHO+R1CH2CH0 稀 液 RCH==C(R1)CH0 +H20(R、R1为
烃基或氢原子 )。
气体流速加快,CH30H选择性增大,可能的原因是 △
回答下列问题
(从催化剂方面回答 :
)。 (1)甲苯分子中共平面的碳原子最多有 个,B→ C的 反应类型为
(3)对 于以上 C02制 甲醇的过程 ,下列说法错误的是 (填标号 )。 (2)物质 G中 存在的作用力有 σ键、π键、 和
A。 反应①为熵增过程 B.催 化剂改变了C02中 0-C—0键角 (3)D的 结构简式为
加压可以提高C02的平衡转化率 D。 升高温度可以提高平衡时甲醇的选择性 (4)由 E生成 F的 化学方程式为
C。
(5)G长
期暴露在空气中容易变质的主要原因是
(4)r℃ ,在容积为 2L的 恒容密闭容器中充入 1 mol c02和 一定量H2,只发生可逆反应①。若
(6)Ⅹ 是 E酸 化后的产物,T是 Ⅹ的芳香族同分异构体,1m。 lT最多能消耗2m。l Na0H,则符合
起始时容器内气体压强为 1.2 kPa,达到平衡时,CH30H(g)的分压与起始投料比 [】 (H2)/ 条件的 T的 结构有 种(不包括立体异构),请写出其中一种核磁共振氢谱有 4组
尼(C02)]的 关系如图3所示。 峰的T的结构简
化学猜题卷(八) 江西卷 第 7页(共 8页 ) 化学猜题卷(八) 江西卷 第 8页(共8页 )17。 (15分 )将各种易得的、廉价的资源进行催化重整,可 以实现资源的综合利用,对环境保护和实
⌒
τ
现双碳目标具有十分重要的意义。C02制甲醇的过程如下 0.24 M ·
:
1 D 冖山
ハ
r′孑兰`歹
日
i。
催化剂活化:In2o3(无活性)+%H2层
矿
In2°
3-·
(有活性)+%H20 a ·
辶 ③
ii。
C02与 H2在活化后的催化剂表面发生可逆反应①,其反应历程如图 1,同时伴随反应②
:
0
1 1.5 2 以H2) 叫
I.g冖
^ U 1 /(10^3K^1)
C02(g)+H2(g):===CO(g)+H20(g) ΔⅡ=+41。 2 kJ o molˉ 1。 图3 n(C02) 图 4 Ti厂
⑻
①c点时H2的转化率α(H2)=
%。
。 飞 6 — C⒒0H选择性
%℃ 。 — C02转化率 ②鸟 (b)= (写 计算表达式)kPa-2。
— △
、 ③c点时,再加人 C02和 H20(g),使 两者分压均增大0.05 kPa,H2的转化率
`
“ ”“ ” “ ”
鼬 (填 增大 不变 或 减小
)。
觏
H20(g) 擀 (5)已知AⅡhenius经验公式:Rln凡 =一 +C(Ea为 活化能 为速率常数,R和 C为常数 反 烨
H2(g) 加 丁 ,凡 )。
H2(g) /H
)
0 应①可通过反应②和反应③两步完成,反应②和反应③的有关数据如图 4所 示,Ea:反应 舀
ˉ “ “
② 反应③(填 >”或 (” );研究表明,加 人某极性介质有助于加快整个反应的
4000 6000 8000 10000 12000
燃
CH30H(g)
气体流速/(mL· h^1)
速率,原因可能是
图1 图2 18.(14分 )有机物G(C9H:04)是 生产某洗面奶的中间体,以 甲苯为原料合成有机物 G的 路线如下
: △
回答下列问题
: B
(1)已 知:反应①每生成 1m。l cH30H(g)放 热 49.0 kJ。 则反应③ CO(g)+2H2(g)了土 甲苯 A 一定条件 Nao r ` · ' · 上 1 2 C D E 丬
C7H6C12
光照
Nao CH3
CH3CH0
CH30H(g) ΔⅡ
=
稀NaoH溶液 旧
△
(2)C02和 H2的混合气体以不同的流速通过反应器,相同时间内C02转化率、 CH30H选 择性与气
G ①新帝刂Cu(oH)2 F 聃
体流速的关系如图2所示。
C9H:04 C9H603Na2
②H+
渊
已知:CH30H选择性 =L-」 三 :】 ∠空 .{:曩 2)× 1。 。%.。 已知:① C是 B的一氯代物 ;
甥品吴:晨
:∶ |;sl C° NaoH溶
②
RCHO+R1CH2CH0 稀 液 RCH==C(R1)CH0 +H20(R、R1为
烃基或氢原子 )。
气体流速加快,CH30H选择性增大,可能的原因是 △
回答下列问题
(从催化剂方面回答 :
)。 (1)甲苯分子中共平面的碳原子最多有 个,B→ C的 反应类型为
(3)对 于以上 C02制 甲醇的过程 ,下列说法错误的是 (填标号 )。 (2)物质 G中 存在的作用力有 σ键、π键、 和
A。 反应①为熵增过程 B.催 化剂改变了C02中 0-C—0键角 (3)D的 结构简式为
加压可以提高C02的平衡转化率 D。 升高温度可以提高平衡时甲醇的选择性 (4)由 E生成 F的 化学方程式为
C。
(5)G长
期暴露在空气中容易变质的主要原因是
(4)r℃ ,在容积为 2L的 恒容密闭容器中充入 1 mol c02和 一定量H2,只发生可逆反应①。若
(6)Ⅹ 是 E酸 化后的产物,T是 Ⅹ的芳香族同分异构体,1m。 lT最多能消耗2m。l Na0H,则符合
起始时容器内气体压强为 1.2 kPa,达到平衡时,CH30H(g)的分压与起始投料比 [】 (H2)/ 条件的 T的 结构有 种(不包括立体异构),请写出其中一种核磁共振氢谱有 4组
尼(C02)]的 关系如图3所示。 峰的T的结构简
化学猜题卷(八) 江西卷 第 7页(共 8页 ) 化学猜题卷(八) 江西卷 第 8页(共8页 )