文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证
号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修1第1章-第2章第二节(人教版2019)。
5.难度系数:0.60
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16
第Ⅰ卷(选择题 共 45 分)
一、选择题:本题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列日常生活情境与化学反应速率无关的是
A.用较浓的白醋清洗水壶垢 B.糖果制作过程中添加着色剂
C.夏天将食物放在冰箱中冷藏 D.面团加酵母粉放在温热处发酵
2.下列说法正确的是
A.吸热反应一定需要加热才能发生
B.高温煅烧石灰石既属于氧化还原反应,又属于吸热反应
C.由 可知:金刚石比石墨更稳定
D.已知 , ,则
3.对于可逆反应3X(s) + Y(g) 2Z(g) + 2Q(g) ,在不同条件下的化学反应速率如下,其中表示的反应速
率最快的是
A.v(X)=0.4 mol·L-1·s-1 B.v(Y)=5 mol·L-1·min-1
C.v(Z)=0.2 mol·L-1·s-1 D.v(Q)=6 mol·L-1·min-1
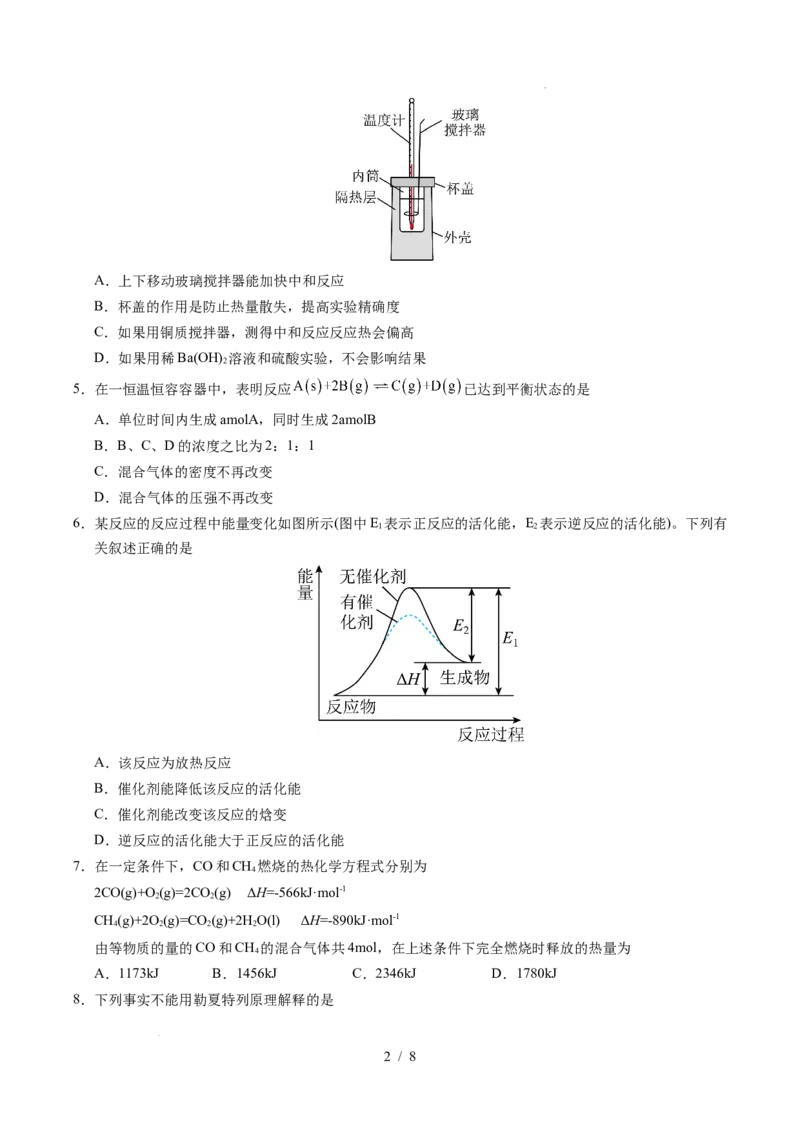
4.某小组利用如图装置测定稀盐酸和稀NaOH溶液中和反应反应热。下列叙述错误的是
1 / 8
学科网(北京)股份有限公司A.上下移动玻璃搅拌器能加快中和反应
B.杯盖的作用是防止热量散失,提高实验精确度
C.如果用铜质搅拌器,测得中和反应反应热会偏高
D.如果用稀Ba(OH) 溶液和硫酸实验,不会影响结果
2
5.在一恒温恒容容器中,表明反应 已达到平衡状态的是
A.单位时间内生成amolA,同时生成2amolB
B.B、C、D的浓度之比为2:1:1
C.混合气体的密度不再改变
D.混合气体的压强不再改变
6.某反应的反应过程中能量变化如图所示(图中E 表示正反应的活化能,E 表示逆反应的活化能)。下列有
1 2
关叙述正确的是
A.该反应为放热反应
B.催化剂能降低该反应的活化能
C.催化剂能改变该反应的焓变
D.逆反应的活化能大于正反应的活化能
7.在一定条件下,CO和CH 燃烧的热化学方程式分别为
4
2CO(g)+O(g)=2CO (g) ΔH=-566kJ·mol-1
2 2
CH(g)+2O(g)=CO (g)+2HO(l) ΔH=-890kJ·mol-1
4 2 2 2
由等物质的量的CO和CH 的混合气体共4mol,在上述条件下完全燃烧时释放的热量为
4
A.1173kJ B.1456kJ C.2346kJ D.1780kJ
8.下列事实不能用勒夏特列原理解释的是
2 / 8
学科网(北京)股份有限公司A.对于反应体系 ,给平衡体系增大压强可使颜色变深
B.在 溶液中存在如下平衡, ,若向 溶液中滴入5-15滴浓
硫酸,溶液颜色橙色加深
C.氯水中存在的平衡: ,当加入适当的 后,溶液颜色变浅
D.工业上生产硫酸的过程中使用过量的空气以提高 的利用率
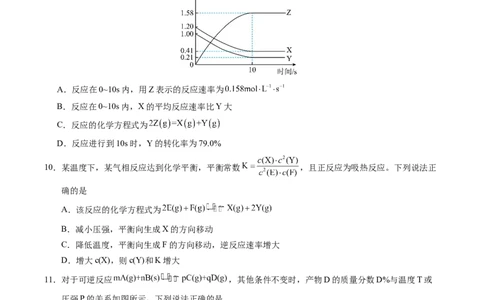
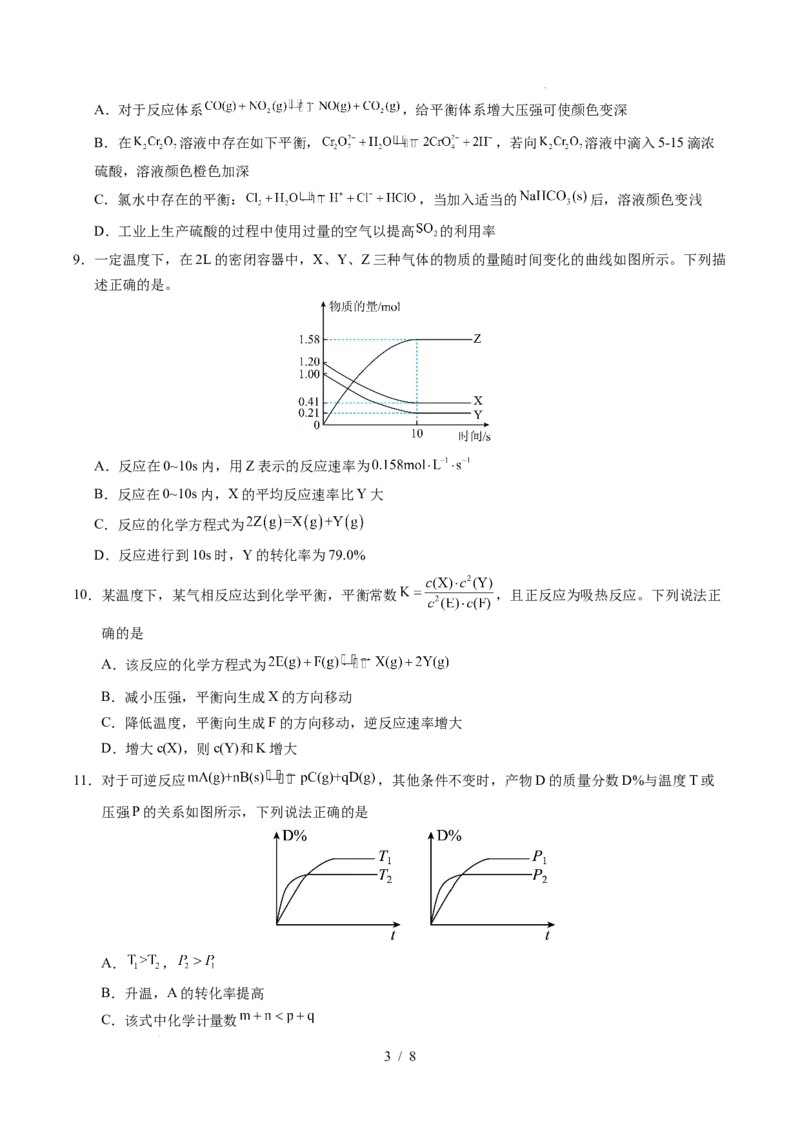
9.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。下列描
述正确的是。
A.反应在0~10s内,用Z表示的反应速率为
B.反应在0~10s内,X的平均反应速率比Y大
C.反应的化学方程式为
D.反应进行到10s时,Y的转化率为79.0%
10.某温度下,某气相反应达到化学平衡,平衡常数 ,且正反应为吸热反应。下列说法正
确的是
A.该反应的化学方程式为
B.减小压强,平衡向生成X的方向移动
C.降低温度,平衡向生成F的方向移动,逆反应速率增大
D.增大c(X),则c(Y)和K增大
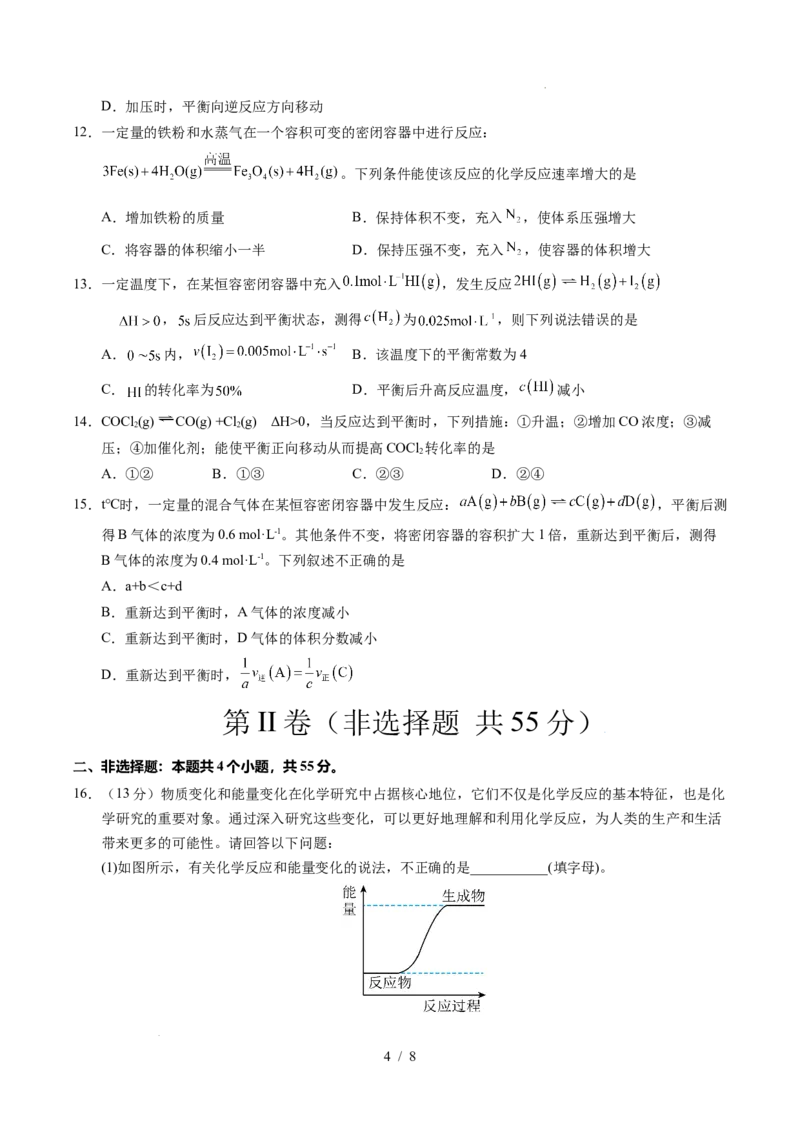
11.对于可逆反应 ,其他条件不变时,产物D的质量分数D%与温度T或
压强P的关系如图所示,下列说法正确的是
A. ,
B.升温,A的转化率提高
C.该式中化学计量数
3 / 8
学科网(北京)股份有限公司D.加压时,平衡向逆反应方向移动
12.一定量的铁粉和水蒸气在一个容积可变的密闭容器中进行反应:
。下列条件能使该反应的化学反应速率增大的是
A.增加铁粉的质量 B.保持体积不变,充入 ,使体系压强增大
C.将容器的体积缩小一半 D.保持压强不变,充入 ,使容器的体积增大
13.一定温度下,在某恒容密闭容器中充入 ,发生反应
, 后反应达到平衡状态,测得 为 ,则下列说法错误的是
A. 内, B.该温度下的平衡常数为4
C. 的转化率为 D.平衡后升高反应温度, 减小
14.COCl (g) CO(g) +Cl (g) ΔH>0,当反应达到平衡时,下列措施:①升温;②增加CO浓度;③减
2 2
压;④加催化剂;能使平衡正向移动从而提高COCl 转化率的是
2
A.①② B.①③ C.②③ D.②④
15.t℃时,一定量的混合气体在某恒容密闭容器中发生反应: ,平衡后测
得B气体的浓度为0.6 mol·L-1。其他条件不变,将密闭容器的容积扩大1倍,重新达到平衡后,测得
B气体的浓度为0.4 mol·L-1。下列叙述不正确的是
A.a+b<c+d
B.重新达到平衡时,A气体的浓度减小
C.重新达到平衡时,D气体的体积分数减小
D.重新达到平衡时,
第 II 卷(非选择题 共 55 分)
二、非选择题:本题共4个小题,共55分。
16.(13分)物质变化和能量变化在化学研究中占据核心地位,它们不仅是化学反应的基本特征,也是化
学研究的重要对象。通过深入研究这些变化,可以更好地理解和利用化学反应,为人类的生产和生活
带来更多的可能性。请回答以下问题:
(1)如图所示,有关化学反应和能量变化的说法,不正确的是___________(填字母)。
4 / 8
学科网(北京)股份有限公司A.反应物比生成物稳定
B.该反应一定需要加热才能发生
C.表示的是吸热反应的能量变化
D.不可以表示强酸与强碱发生中和反应的能量变化
(2)化学反应的焓变与反应物和生成物的键能有关。
已知:
共价键
键能 436 247
则 键的键能为 。
(3)如图是 与 反应生成 和 的过程中能量变化示意图。
①请写出该反应的热化学方程式: 。
②若在该反应体系中加入催化剂,则对反应热 (填“有”或“无”)影响。
(4)金属钛( )在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之一是将金红石
转化为 ,再进一步还原得到钛。 转化为 有直接氯化法和碳氯化法。在1000℃
时反应的热化学方程式如下:
i.直接氯化:
ii.碳氯化:
则反应 的 。
(5)“氧弹量热仪”可以测定蔗糖的燃烧热,“氧弹”是一个耐高温高压可通电点火的金属罐,将蔗糖
和足量氧气充入“氧弹”中点燃,产生的热量被“氧弹”外的水吸收,通过测定水温的变化从而计算
出蔗糖的燃烧热。已知:蔗糖 的质量为 ;量热计中水的质量为 ,水的比热容
为 ;忽略金属“氧弹”吸收的热量。反应前后所测水温如下表。
序 点火前温 燃烧后测得的最高温
号 度/℃ 度/℃
1 20.73 22.63
5 / 8
学科网(北京)股份有限公司2 20.76 21.25
3 20.72 22.82
①上述蔗糖燃烧放出的热量Q= J。
②请写出蔗糖燃烧的热化学方程式: 。
17.(14分)甲、乙、丙三个实验小组欲探究影响化学反应速率的因素,设计实验方案如下。
I.甲组:利用KMnO 与HC O(草酸)在酸性溶液中发生氧化还原反应生成CO 气体的体积来探究化
4 2 2 4 2
学反应速率的影响因素(实验中所用KMnO 溶液已加入稀硫酸酸化)。
4
(1)用离子方程式表示该反应原理: 。
实验装置如图所示,实验时装置中A溶液一次性加入,A、B溶液成分见下表。
实验 A溶液 B溶液
①
②
(2)盛装A溶液的仪器名称是 。
(3)该实验探究的是 对化学反应速率的影响。
Ⅱ.乙组:通过测定KMnO 与HC O(草酸)在酸性溶液中发生反应,KMnO 溶液褪色所需时间的长
4 2 2 4 4
短,探究浓度对化学反应速率的影响。该实验小组配制了以下3组溶液。
实验 1 2 3
水/mL 10 5 X
5 10 4
5 5 5
时间/s 40 20 -
(4)实验3中X= 。
(5)实验2反应中,HC O 的反应速率为 。
2 2 4
Ⅲ.丙组:通过硫代硫酸钠(Na SO)与硫酸反应有关实验,探究影响化学反应速率的因素,实验过程
2 2 3
的数据记录如下。已知:
加入物质
反应温度
实验
(℃)
NaSO HSO HO
2 2 3 2 4 2
6 / 8
学科网(北京)股份有限公司V/mL V/mL V/mL
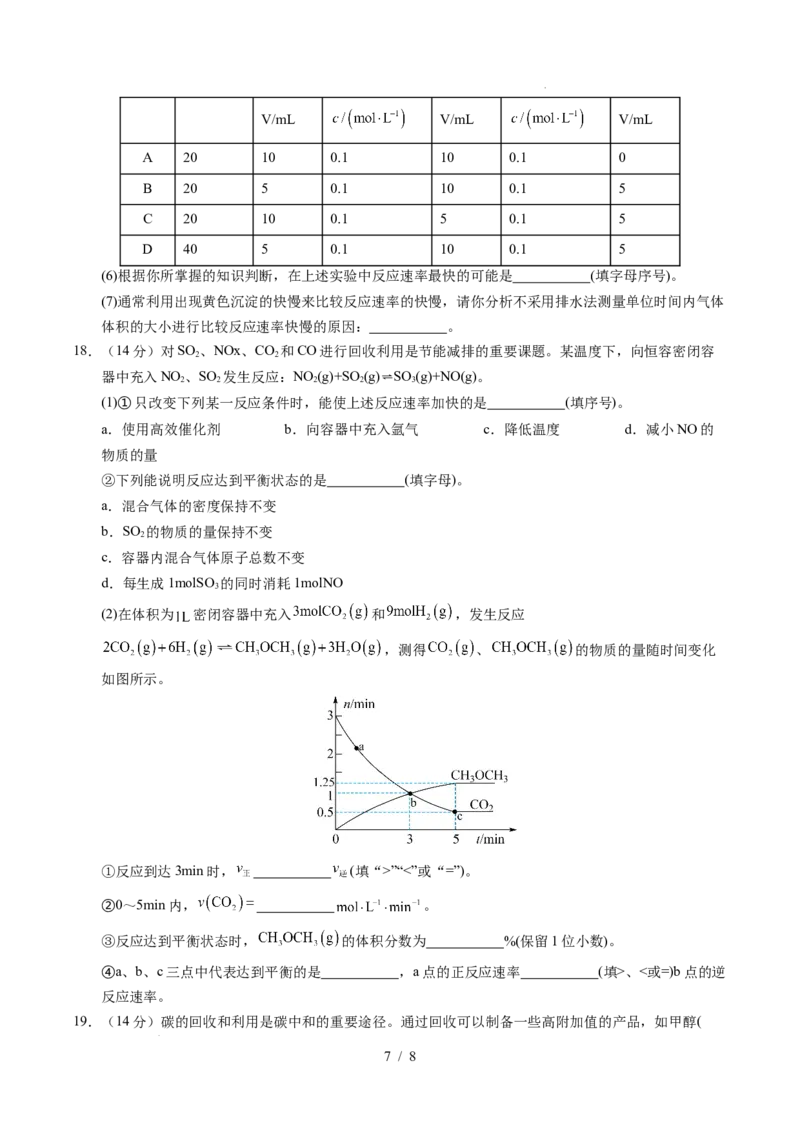
A 20 10 0.1 10 0.1 0
B 20 5 0.1 10 0.1 5
C 20 10 0.1 5 0.1 5
D 40 5 0.1 10 0.1 5
(6)根据你所掌握的知识判断,在上述实验中反应速率最快的可能是 (填字母序号)。
(7)通常利用出现黄色沉淀的快慢来比较反应速率的快慢,请你分析不采用排水法测量单位时间内气体
体积的大小进行比较反应速率快慢的原因: 。
18.(14分)对SO 、NOx、CO 和CO进行回收利用是节能减排的重要课题。某温度下,向恒容密闭容
2 2
器中充入NO
2
、SO
2
发生反应:NO
2
(g)+SO
2
(g)⇌SO
3
(g)+NO(g)。
(1)①只改变下列某一反应条件时,能使上述反应速率加快的是 (填序号)。
a.使用高效催化剂 b.向容器中充入氩气 c.降低温度 d.减小NO的
物质的量
②下列能说明反应达到平衡状态的是 (填字母)。
a.混合气体的密度保持不变
b.SO 的物质的量保持不变
2
c.容器内混合气体原子总数不变
d.每生成1molSO 的同时消耗1molNO
3
(2)在体积为 密闭容器中充入 和 ,发生反应
,测得 、 的物质的量随时间变化
如图所示。
①反应到达3min时, (填“>”“<”或“=”)。
②0~5min内, 。
③反应达到平衡状态时, 的体积分数为 %(保留1位小数)。
④a、b、c三点中代表达到平衡的是 ,a点的正反应速率 (填>、<或=)b点的逆
反应速率。
19.(14分)碳的回收和利用是碳中和的重要途径。通过回收可以制备一些高附加值的产品,如甲醇(
7 / 8
学科网(北京)股份有限公司)、甲酸( )、甲醛( )等。
(1)已知:① ;
② ;
③ ;
④ 。
化学键
键能 343 506 413 436 465 1076
根据上述数据计算 。表示 燃烧热的热化学方程式:
。
(2)科学研究表明,用 作催化剂, 和 反应合成 需经历三步:
第一步: ;
第二步: ;
第三步: 。
从能量角度分析,催化剂作用是 。
(3)用 和 为原料合成 的机理如图所示。总反应的正反应 (填“>”“<”
或“=”)0,总反应含 个基元反应,其中决定总反应速率的反应方程式为 。
8 / 8
学科网(北京)股份有限公司