文档内容
安徽省合肥市2025年高三第一次教学质量检测化学试题
(考试时间:75 分钟 满分:100分)
注意事项:
1.答卷前,务必将自己的姓名和座位号填写在答题卡和试卷上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,务必
擦净后再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量: O16 Zr 91
一、选择题:本题共14小题,每小题3分.共42分。在每小题给出的四个选项中,只有一项是符合题目要
求的。
1.下列安徽省出土的文物中,其主要成分属于有机物的是
A.木俑首 B.蚕形玉饰 C.金边玛瑙碗 D.青铜立鸟壶
2.谱图分析是化学中常用的研究方法,下列谱图所对应的作用错误的是
A.原子光谱:确定元素组成
B.质谱:分析有机物的碳骨架结构
C.红外光谱:可分析出分子中的化学键或官能团信息
D.核磁共振氢谱:确定有机物中不同化学环境氢原子的相对数目
3.生活中蕴含着丰富的化学知识,下列相关解释正确的是
A.盐卤用来制豆腐,因其可使蛋白质变性
B.洗涤剂清洗餐具,因其与油污发生中和反应
C.酿酒时蒸馏提高酒精度,利用酒和水的密度不同
D.活性炭用于除去冰箱中的异味,利用其吸附性
4.常温下,下表中各物质不能按照如图所示的转化关系一步实现的是
选项 甲 乙 丙
A NO NO₂ HNO₃
B HCl Cl₂ Ca(ClO)₂
C Fe Fe₂O₃ Fe(OH)₃
D Na₂O₂ Na₂CO₃ NaHCO₃
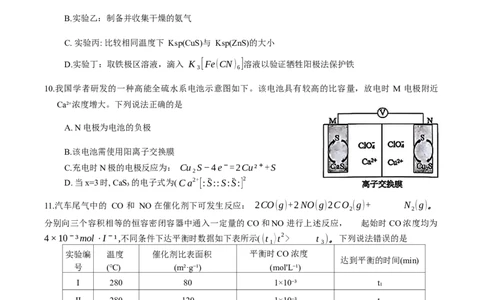
5.硅烷偶联剂X的水解产物Y 能融合无机界面和有机界面,可在无机材料和有机材料之间形成一座“分子
桥”。X水解反应如下图所示,下列说法错误的是A. X中 Si和O的杂化方式相同 B. Y中σ键和π键的个数比为5∶1
C. X水解为Y 时还生成了 CH₃OH D. Y能发生聚合反应
阅读下列材料,回答第6-7题
研究沉积物中硫循环对控制与治理水污染具有重要意义,沉积物中的硫通过微生物趋动的氧化或还原
过 程 可 转 化 为 不 同 价 态 的 含 硫 物 质 。 已 知 25℃ 时 , Kₐ₁(H₂SO₃)=1.4×10⁻²,
Kₐ₂(H₂SO₃)=6.0×10⁻⁸,Kₐ₁(H₂S)=1.1×10⁻⁷,Kₐ₂(H₂S)=1.3×10⁻¹³。
6.设NA为阿伏加德罗常数的值。下列说法正确的是
A. 1m ol H₂S中所含质子总数为18NA
B. 标准状况下, 22.4LSO₂和SO₃混合物中所含S原子数为. N
A
C. 1L0.1mol⋅L⁻¹的 Na₂S溶液中含HS⁻和S²⁻总数为0.1 NA
D. 1molS O2−完全转化为 S O2−,转移的电子数为2NA
2 3 4 6
7.下列有关物质结构或性质的说法错误的是
A. 键角: H₂SNaHS
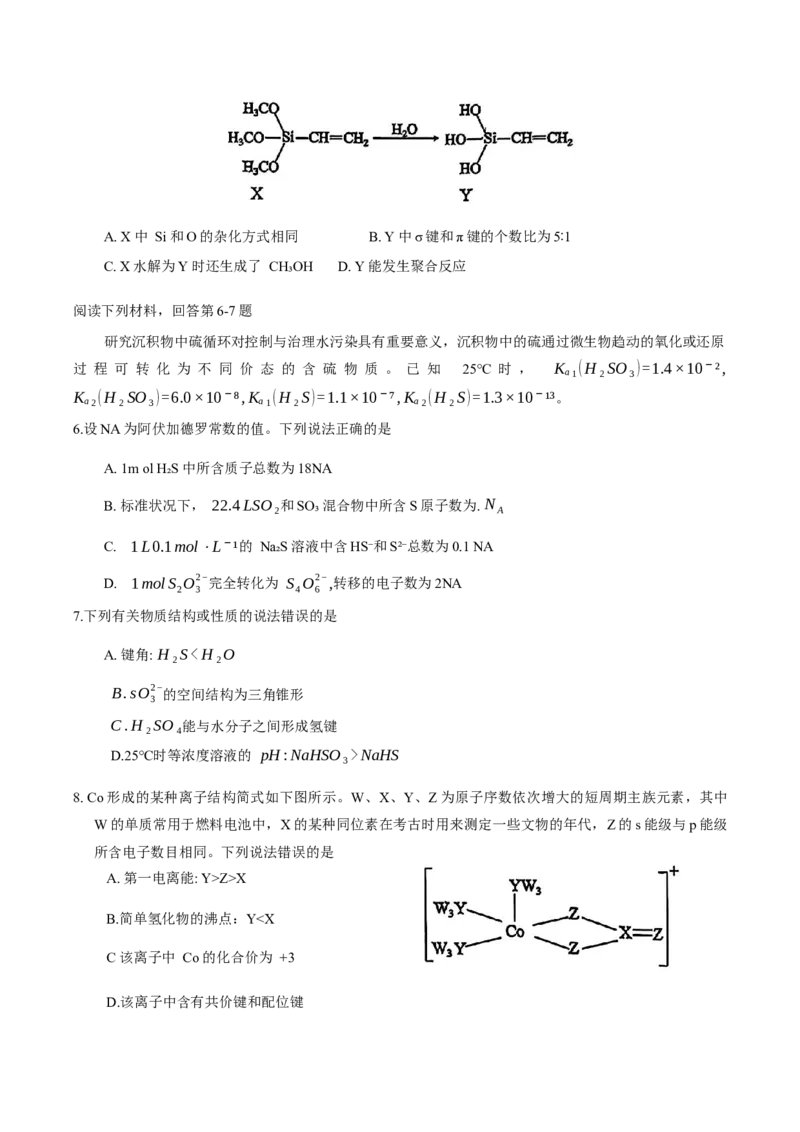
8. Co形成的某种离子结构简式如下图所示。W、X、Y、Z为原子序数依次增大的短周期主族元素,其中
W的单质常用于燃料电池中,X的某种同位素在考古时用来测定一些文物的年代,Z的s能级与p能级
所含电子数目相同。下列说法错误的是
A. 第一电离能: Y>Z>X
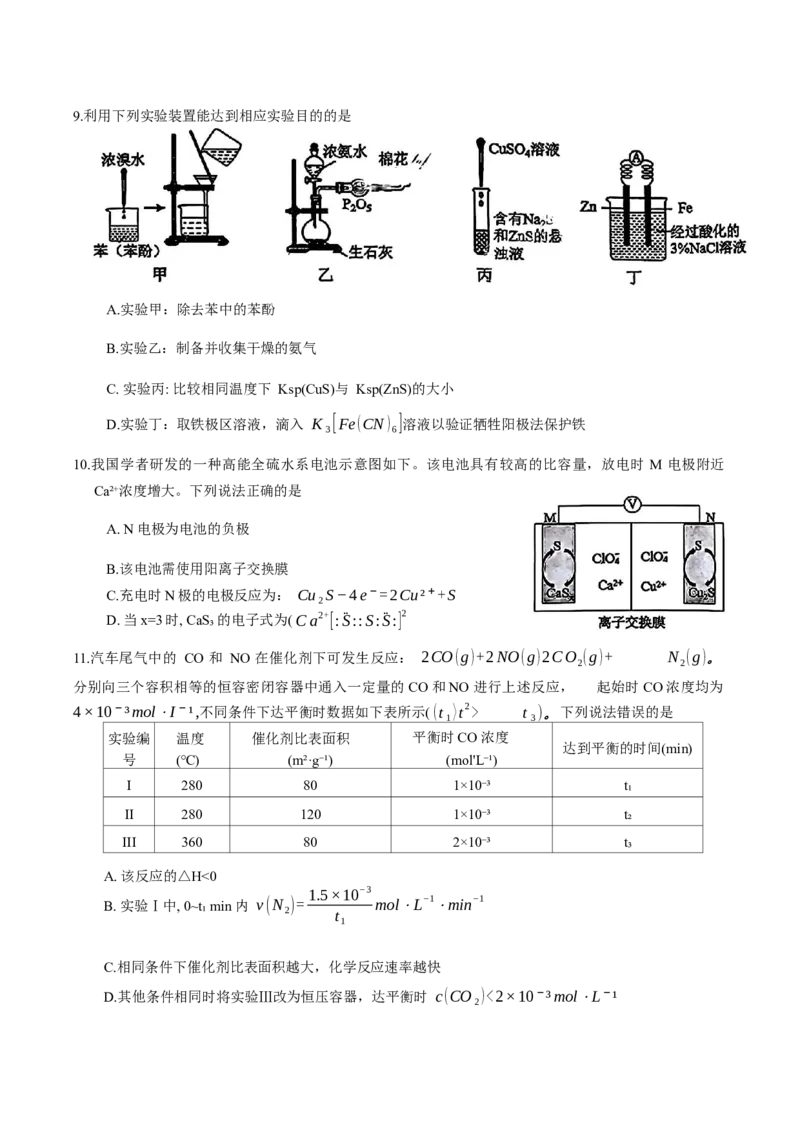
B.简单氢化物的沸点:Y t₃)。下列说法错误的是
实验编 温度 催化剂比表面积 平衡时CO 浓度
达到平衡的时间(min)
号 (℃) (m²·g⁻¹) (mol'L⁻¹)
I 280 80 1×10⁻³ t₁
II 280 120 1×10⁻³ t₂
III 360 80 2×10⁻³ t₃
A. 该反应的△H<0
1.5×10−3
B. 实验Ⅰ中, 0~t₁ min内 v(N )= mol⋅L−1 ⋅min−1
2 t
1
C.相同条件下催化剂比表面积越大,化学反应速率越快
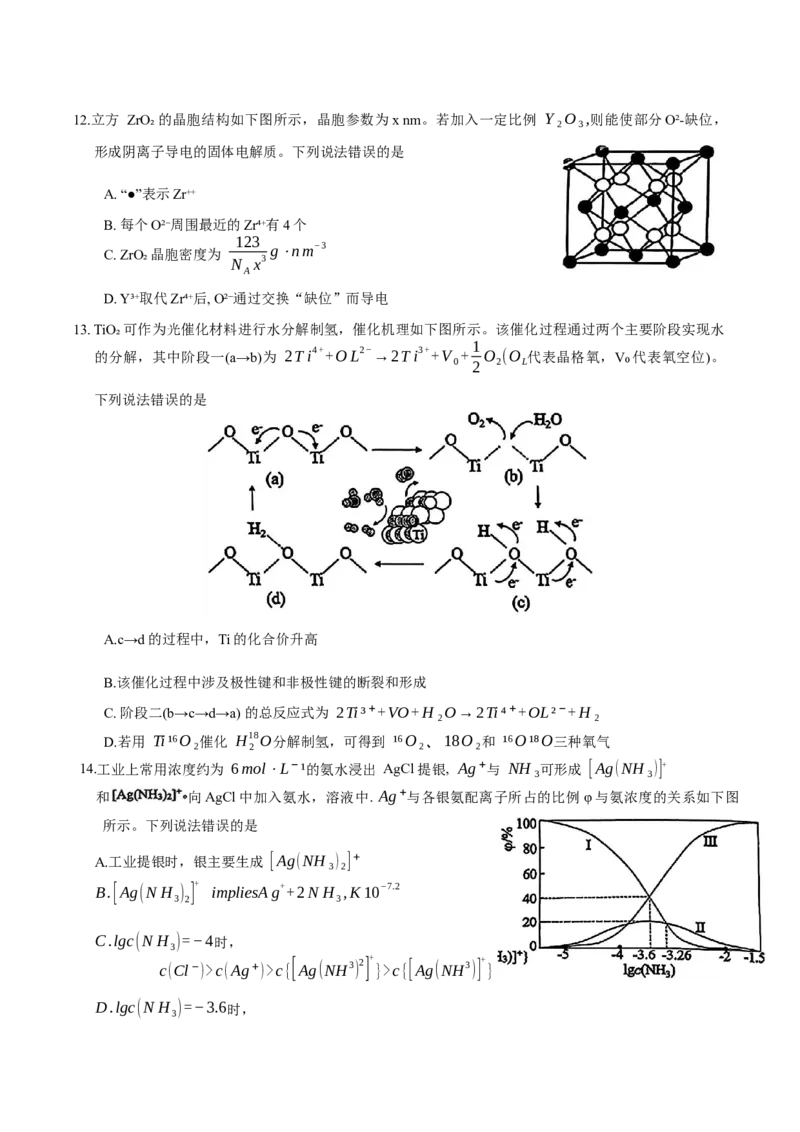
D.其他条件相同时将实验Ⅲ改为恒压容器,达平衡时 c(CO₂)<2×10⁻³mol⋅L⁻¹12.立方 ZrO₂的晶胞结构如下图所示,晶胞参数为x nm。若加入一定比例 Y₂O₃,则能使部分O²-缺位,
形成阴离子导电的固体电解质。下列说法错误的是
A. “●”表示Zr⁺⁺
B. 每个O²⁻周围最近的Zr⁴⁺有4个
123
C. ZrO₂晶胞密度为
g⋅nm−3
N x3
A
D. Y³⁺取代Zr⁴⁺后, O²⁻通过交换“缺位”而导电
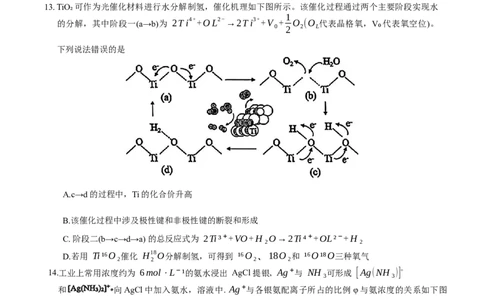
13. TiO₂可作为光催化材料进行水分解制氢,催化机理如下图所示。该催化过程通过两个主要阶段实现水
1
的分解,其中阶段一(a→b)为 2Ti4++OL2−→2Ti3++V + O (O 代表晶格氧,V₀代表氧空位)。
0 2 2 L
下列说法错误的是
A.c→d的过程中,Ti的化合价升高
B.该催化过程中涉及极性键和非极性键的断裂和形成
C. 阶段二(b→c→d→a) 的总反应式为 2Ti³⁺+VO+H₂O→2Ti⁴⁺+OL²⁻+H₂
D.若用 Ti¹⁶O₂催化 H18O分解制氢,可得到 ¹⁶O₂、18O₂和 ¹⁶O¹⁸O三种氧气
2
14.工业上常用浓度约为 6mol⋅L⁻¹的氨水浸出 AgCl 提银, Ag⁺与 NH₃可形成 [Ag(NH₃)]+
和 向AgCl中加入氨水,溶液中. Ag⁺与各银氨配离子所占的比例φ与氨浓度的关系如下图
所示。下列说法错误的是
A.工业提银时,银主要生成 [Ag(NH₃)₂]⁺
B.[Ag(N H ) ] + impliesAg++2N H ,K10−7.2
3 2 3
C.lgc(N H )=−4时,
3
c(Cl⁻)>c(Ag⁺)>c{ [ Ag(NH3) 2] + }>c{ [Ag(NH3)] + }
D.lgc(N H )=−3.6时,
3c(Cl⁻)+c(OH⁻)=5c[Ag(NH₃)]⁺+c(NH₄)+c(H⁺)
二、非选择题:本题共4 小题,共58分。
15.(14分) 五氧化二钒( (V ₂O₅)被广泛应用于钒电池、激光晶体等行业。一种由钒渣(主要化学成分包括:
等)制备 V ₂Os的流程如下:
已知: Ca(VO₃)₂难溶于水; Fe₂O;只能溶于 c(H⁺)>1mol⋅L⁻¹的溶液, Al₂O₃可溶于
pH<3.29的溶液。
回答下列问题:
(1)钒的原子序数为 23,其在周期表中位于第四周期第 族,基态钒原子价层电子排布式为
。
(2) “焙烧”时, FeO⋅V ₂O₃转化为 Fe₂O₃和 Ca(VO₃)₂,该反应中还原剂与氧化剂的物质的量之比为
。
(3) “酸浸”时, Ca(VO₃)₂与稀 H₂SO₄生成 vo+ 进入溶液中,写出该反应的离子方程式
2
。该过程硫酸浓度太高会导致钒的浸出率降低,可能的原因是 。
(4) “过滤”时所得滤渣的主要成分有( CaSO₄、硅酸和 (填化学式)。
(5) “沉钒”后所得滤液可返回“ ”步骤进行循环; “煅烧”后得到无污染的气体并生成
V ₂Oₛ ,写出该反应的化学方程式 。
16. (15分) 硫酸铜晶体 (CuSO₄⋅5H₂O)中因含有 Fe³⁺和 Fe²⁺等杂质对其品质的影响较大,其纯
度分析如下:
Ⅰ.测定铁含量:
取一定量硫酸铜晶体加水溶解,再加入少量稀 H₂SO₄和 H₂O₂,加热。冷却后,边搅拌边滴加
6mol⋅L⁻¹NH₃⋅H₂O,至沉淀不再溶解,溶液呈深蓝色为止。过滤,洗涤沉淀,洗涤后的沉淀中加入
盐酸,用分光光度法测定铁含量。
(1)加入 H₂O₂的目的是 ;沉淀溶解得到深蓝色溶液的离子方程式为 。
(2)洗涤沉淀时,下列洗涤剂中最佳的是 (填标号)。
A.蒸馏水 B.6mol⋅L⁻¹NH₃⋅H₂O C.过滤后的母液
Ⅱ.测定铜含量:
准确称取10.0g硫酸铜晶体加水溶解,加入过量KI溶液,发生反应 2Cu²⁺+4 I−2CuI↓+I₂(已
2−
掩蔽 Fe元素排除其干扰),用 0.1000mol⋅L⁻¹Na₂S₂O₃溶液滴定,发生反应 I +2S O2 2I-+S4O
2 2 3 6
加入淀粉溶液,滴至溶液呈浅蓝色,再加入KSCN溶液,摇匀,慢慢滴定到蓝色消失为止。4. K (CuI)=1.1×10⁻¹², K (CuSCN)=4.8×10⁻¹⁵
已知: CuI 易吸附I₂ SP SP
回答下列问题:
(3)测定铜含量实验中用到的仪器有 (填标号)。
(4)若滴定终点时滴定管尖嘴部分有气泡,会导致测定结果 (填“偏高”或“偏低”)。
(5)结合离子方程式解释加入KSCN溶液的作用 。
(6)滴定后最终消耗 VmLNa₂S₂O₃溶液,以此数据计算该硫酸铜晶体的纯度为 (用含V的
代数式表示,已知 M(CuSO₄⋅5H₂O)=250g⋅mol⁻¹)。
(7)CuSO₄⋅5H₂O在不同温度下会逐步脱水变成无水( CuSO₄,脱水时样品重量占比随温度变化的曲
线如图 1 所示,X 射线衍射法测得( CuSO₄⋅5H₂O的晶体结构如图 2 所示。由图可知,
CuSO₄⋅5H₂O受热至温度在 120−150°C之间破坏的作用力为 。
17. (15 分) 1, 3 - 丁二烯( (C₄H₆)是一种重要的石油化工基础原料,主要用于合成聚丁二烯橡胶、丁苯橡
胶、丁腈橡胶等多种产品,工业上可由1-丁烯( (C₄H₈)制备1,3-丁二烯。回答下列问题:
Ⅰ 催化直接脱氢: C H (g)C H (g)+H (g)H
4 8 4 6 2
(1)相关共价键的键能如下表,则
共价键 H-H C-H C-C
键能/(kJ· mol-¹) 436 413 348 615
(2)一定温度下,向恒容密闭反应器中通入一定量的( C₄H₈发生直接脱氢反应,下列选项能说明该反…
一定处于平衡状态的是 (填标号)。
A.v (C H )=vΩ(C H ) B. H₂的体积分数不变
2E 4 8 4 6
C.容器内气体的平均相对分子质量不变 D.容器内混合气体的密度不变
(3)向反应体系中通入一定量的高温水蒸气和( C₄H₈发生直接脱氢反应。n(H O)
2
①在相同温度、不同压强下,1-丁烯的平衡转化率随 的变化如图所示。
n(C H )
4 8
压强p₁、p₂、p₃的大小顺序为 。
② 恒压条件下,向反应体系通入高温水蒸气可提高反应物转化率,原因是 。
Ⅱ. O₂氧化脱氢:
1
主反应: C H (g)+ O (g) LC H (g)+H O(g)
4 8 2 2 4 6 2
副反应: C H (g)+5O (g)2CO (g)+2CO(g)+4H O(g)
4 8 2 2 2
(4)已知反应空速是指单位时间内通过单位体积催化剂的原料
气体流量。一定条件下,不同空速对 1-丁烯氧化脱氢反应性能
的影响如图所示。其中较适宜的空速为 h-¹ (填标号) 。
A.325左右 B.400左右 C.550左右
空速过小或过大时,1,3-丁二烯选择性较低的原因是
。
(5)在一定温度和压强下,按照 n(O₂):n(C₄H₈)=3:5的投料比进行反应,达到平衡时,( C₄H₈的转化
率为80%,C₄H₆的选择性为 95%[C₄H₆的选择性= ×100%] ,主反应的 Kₓ=___________(列出
计算式, Kₓ是以平衡物质的量分数代替平衡浓度计算的平衡常数)。
Ⅲ. CO₂氧化脱氢:
C H (g)+CO (g)C H (g)+CO(g)+H O(g))
4 8 2 4 6 2
(6)已知 CO₂可与 H₂发生反应: CO (g)+H (g)CO(g)+H O(g),与催化直接脱氢相比, CO₂
2 2 2
氧化脱氢的优点是 (写出一点即可)。
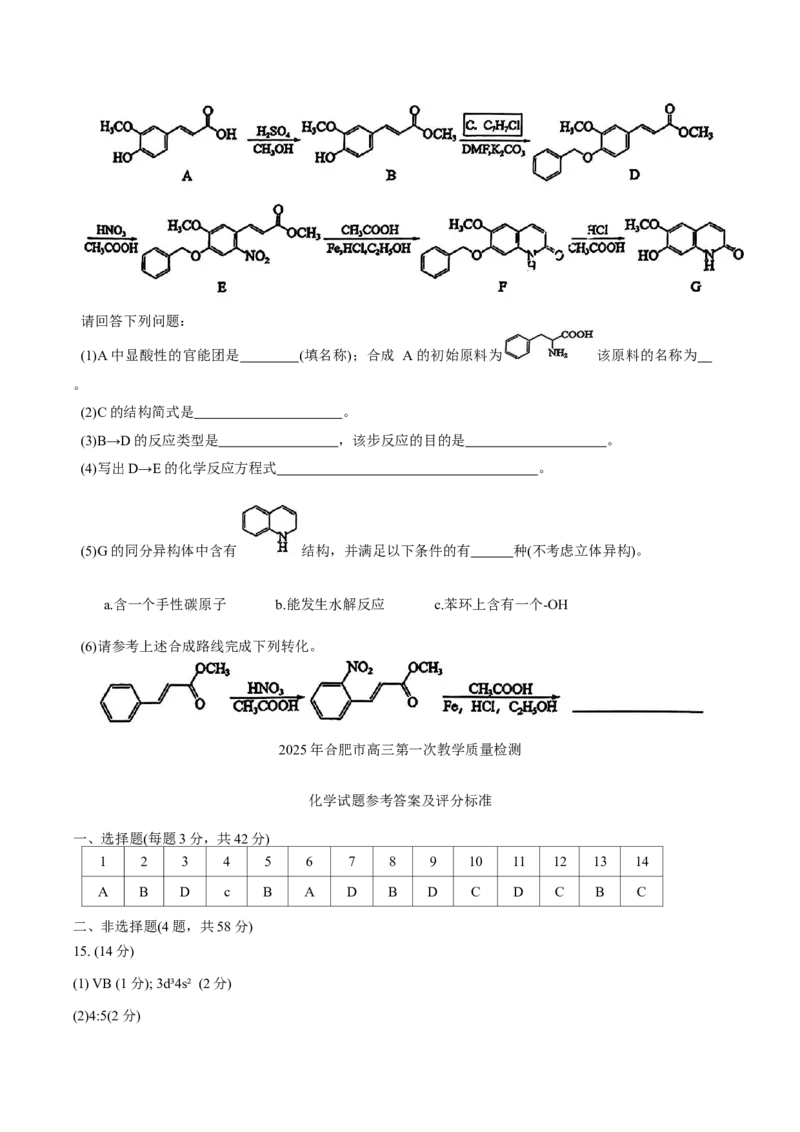
18. (14分)G是一种重要的抗肿瘤药物中间体,其合成路线如下:请回答下列问题:
(1)A中显酸性的官能团是 (填名称);合成 A 的初始原料为 该原料的名称为
。
(2)C的结构简式是 。
(3)B→D的反应类型是 ,该步反应的目的是 。
(4)写出D→E的化学反应方程式 。
(5)G的同分异构体中含有 结构,并满足以下条件的有 种(不考虑立体异构)。
a.含一个手性碳原子 b.能发生水解反应 c.苯环上含有一个-OH
(6)请参考上述合成路线完成下列转化。
2025年合肥市高三第一次教学质量检测
化学试题参考答案及评分标准
一、选择题(每题3分,共42分)
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A B D c B A D B D C D C B C
二、非选择题(4题,共58分)
15. (14分)
(1) VB (1分); 3d³4s² (2分)
(2)4:5(2分)(3)Ca(V O ) +4H++SO2=2V O−+CaSO +2H O(2分);
3 2 4 2 4 2
生成的CaSO₄包裹在 Ca(VO₃)₂ 表面,不利于其浸出(其他合理答案也可)(2分)
(4) Fe₂O₃(2分)
煅烧
4N H V O +3O
(5) 酸浸 (1分); 4 3 2 _______ (2分)
2N +2V O+8H O¿
¿ 2 2 2
16. (15分)
(1) 使 Fe²⁺氧化成Fe³⁺;(2分) Cu(OH)₂+4NH₃=[Cu(NH₃)₄]²⁺+2OH⁻(2分)
(2)B(2分)
(3)①③(2分)
(4) 偏低(1分)
(5)CuI(s)+SCN (aq)=CuSCN(s)+I(aq),使CuI转化为更难溶的CuSCN, 以减少对 I₂的吸附。(2分)
(6) 0.25V%或 2.5×10⁻³V ×100% (2分)
(7)配位键和氢键(2分)
17.(15分)
(1)+123 (1分)
(2) BC (2分)
(3) ①p₃>p₂>p₁(2分);
②升高反应体系温度,减小1-丁烯分压,使平衡正向移动(2分)
(4) B(2分);
空速过小时,1-丁烯与氧气接触时间长被深度氧化生成COₓ;空速过大时,反应物与催化剂接触时间短不
能被充分氧化(2分)
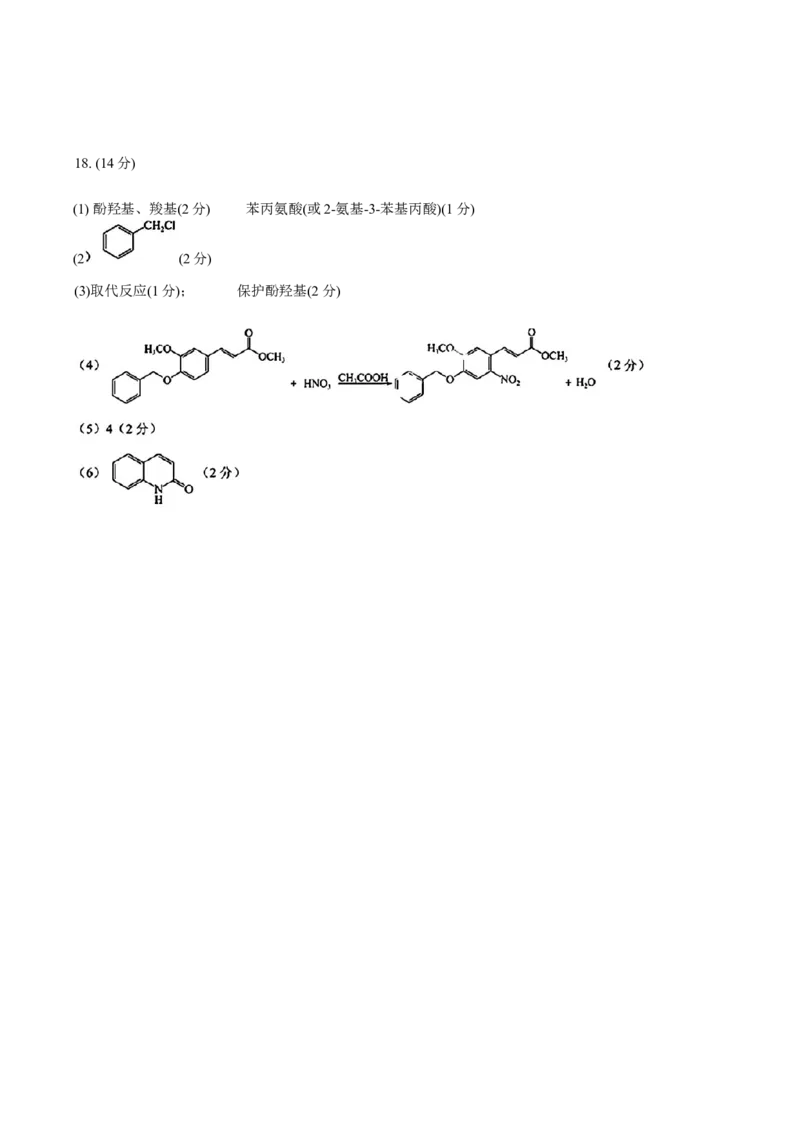
(6)CO₂和直接脱氢产物H₂反应,使平衡正向移动,增大反应物平衡转化率 (2分)18. (14分)
(1) 酚羟基、羧基(2分) 苯丙氨酸(或2-氨基-3-苯基丙酸)(1分)
(2 (2分)
(3)取代反应(1分); 保护酚羟基(2分)