文档内容
高途高中·化学
点睛卷
2024
广东省-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2024 年广东省普通高中学业水平选择性考试模拟测试卷
化 学
本试卷共9页,20 小题,满分 100分,考试用时75分钟。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Na-23 Ca-40 Fe-56 As-75
一、选择题:本题共16小题,共44分。第1~10 小题,每小题 2分;第11~16小题,每小题
4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.近年来,我国基础研究和原始创新不断加强,一些关键核心技术实现突破。下列科技成果中所涉及的
合金不属于新型合金的是
A.国产大飞机 C919 窝扇用 B.“中国天眼”使用的碳 C.“蛟龙”号载人舱是用钛 D.新能源汽车储
的是耐高温的合金材料 化硅 合金制的 氢材料
A.A B.B C.C D.D
2.保护文物就是保护历史传承文明,化学在文物的研究和修复中有重要作用。下列说法错误的是
A.古壁画颜料中所用的铁红,其成分为Fe O
2 3
B.古陶瓷修复所用的熟石膏,其成分为Ca(OH)
2
C.龟甲的成分之一羟基磷灰石属于无机物
D.14C可以用来测定文物年代,碳原子的价电子轨道表示式
3.建设现代化产业体系、全面推进乡村振兴的道路上,离不开化学的发展,下列说法正确的是
A.在燃煤中添加生石灰的主要目的是有效减缓温室效应
B.工业上利用新型高效手性螺环催化剂可以增大原料转化率提高产率
C.SiO 是重要的半导体材料,可以作为太阳能光伏电池的基底材料
2
D. 有机磷农药多为磷酸酯或硫代磷酸酯类物质,肥皂水因有利于其水解而解毒
试卷第2页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
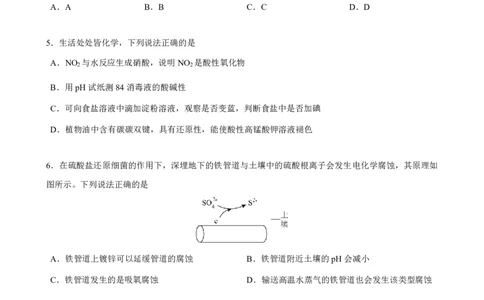
4.氯及其化合物应用广泛,实验室欲由下列装置制取高浓度的HClO溶液,有关实验装置和原理能达到各
自实验目的的是
选项 A B C D
装置
目的 制取氯气 制取氯水 提高HClO浓度 分离HClO
A.A B.B C.C D.D
5.生活处处皆化学,下列说法正确的是
A.NO 与水反应生成硝酸,说明NO 是酸性氧化物
2 2
B.用pH试纸测84消毒液的酸碱性
C.可向食盐溶液中滴加淀粉溶液,观察是否变蓝,判断食盐中是否加碘
D.植物油中含有碳碳双键,具有还原性,能使酸性高锰酸钾溶液褪色
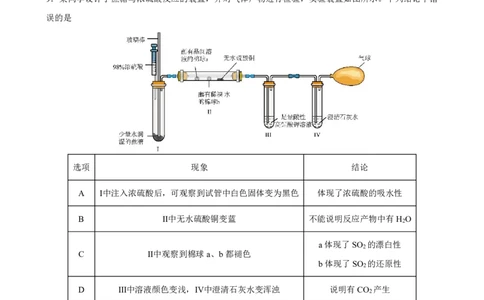
6.在硫酸盐还原细菌的作用下,深埋地下的铁管道与土壤中的硫酸根离子会发生电化学腐蚀,其原理如
图所示。下列说法正确的是
A.铁管道上镀锌可以延缓管道的腐蚀 B.铁管道附近土壤的pH会减小
C.铁管道发生的是吸氧腐蚀 D.输送高温水蒸气的铁管道也会发生该类型腐蚀
7.下列过程与所述化学知识有关联的是
选项 过程 知识
A 用氢氟酸制作雕花玻璃 SiO 是酸性氧化物
2
B 电解NaCl-KCl-AlCl 熔融盐制铝 熔融的AlCl 易电离
3 3
C 栽培韭菜施加草木灰 草木灰中含K CO 等
2 3
D 供港蔬菜的运输车厢使用聚苯乙烯材料 聚苯乙烯有催熟作用
试卷第3页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
8.对乙酰氨基酚(T)为非甾体类抗炎药,具有解热镇痛作用。其结构简式如图所示,下列有关说法错误的
是
A.1molT最多能与2molNaOH反应 B.能与饱和溴水发生取代反应
C.T中含有两种官能团 D.能与Na CO 反应放出CO
2 3 2
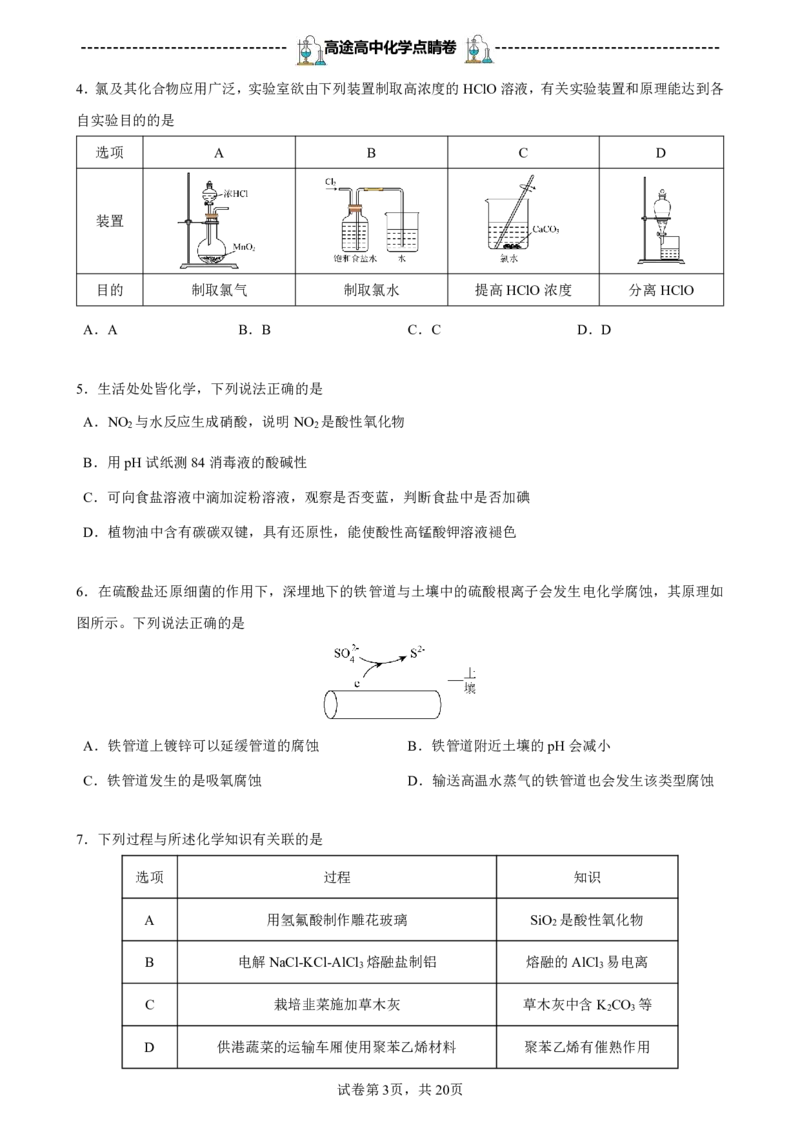
9.某同学设计了蔗糖与浓硫酸反应的装置,并对气体产物进行检验,实验装置如图所示。下列结论中错
误的是
选项 现象 结论
A Ⅰ中注入浓硫酸后,可观察到试管中白色固体变为黑色 体现了浓硫酸的吸水性
B Ⅱ中无水硫酸铜变蓝 不能说明反应产物中有H O
2
a体现了SO 的漂白性
2
C Ⅱ中观察到棉球a、b都褪色
b体现了SO 的还原性
2
D Ⅲ中溶液颜色变浅,Ⅳ中澄清石灰水变浑浊 说明有CO 产生
2
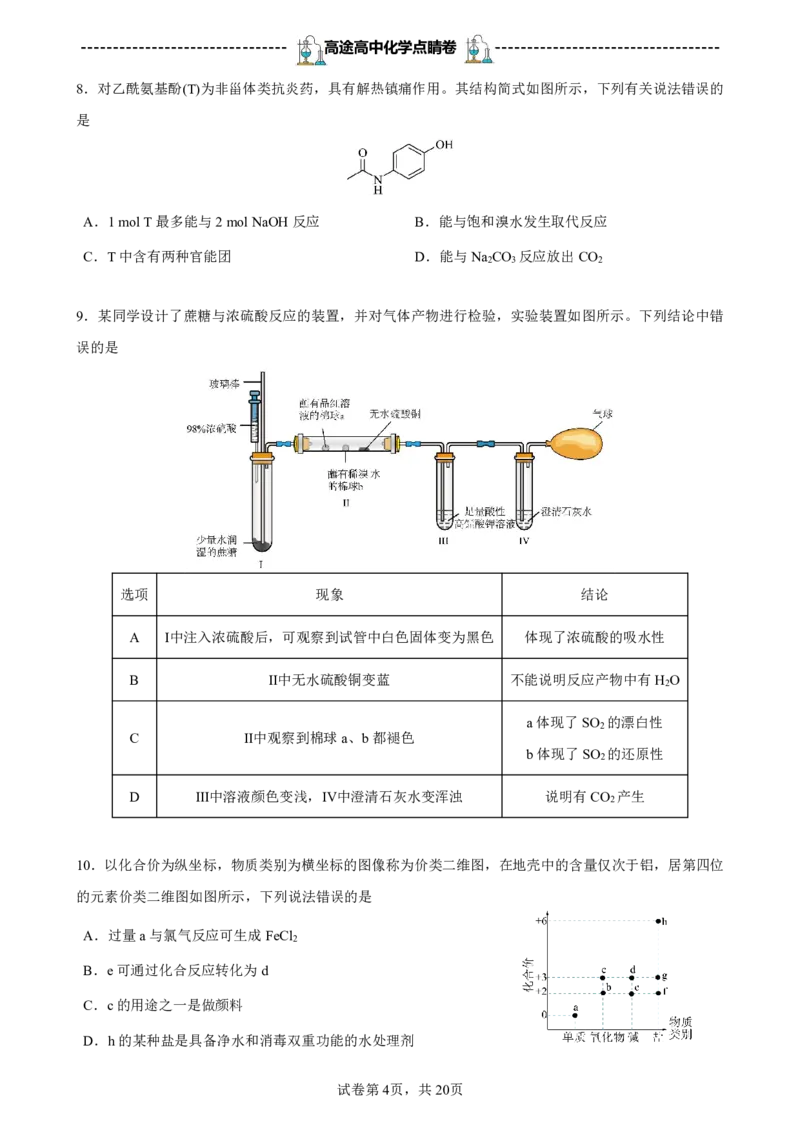
10.以化合价为纵坐标,物质类别为横坐标的图像称为价类二维图,在地壳中的含量仅次于铝,居第四位
的元素价类二维图如图所示,下列说法错误的是
A.过量a与氯气反应可生成FeCl
2
B.e可通过化合反应转化为d
C.c的用途之一是做颜料
D.h的某种盐是具备净水和消毒双重功能的水处理剂
试卷第4页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
11.N 代表阿伏加德罗常数的值。下列说法正确的是
A
A. 在标准状况下, 11.2LHF分子中含氢原子数目为0.5N
A
B. 标准状况下,11.2LCl 溶于水,溶液中Cl、ClO和HClO的微粒数之和为N
2 A
C.
向0.1mol/L盐酸中滴加氨水至中性,溶液中含有的NH+数目为0.1N
4 A
D.0.2mol吡咯( )分子中含有σ键数为2N
A
12.下列对化学实验及现象的解释合理的是
选项 化学实验及现象 解释
A 久置的Na O 遇盐酸有气泡产生 Na O 已完全转化为Na CO
2 2 2 2 2 3
CH 与Cl 光照下反应产生的气体使湿润的蓝色
4 2
B 气态氯代甲烷溶于水显酸性
石蕊试纸变红
C 酸性: 强于 羟基极性: 强于
向0.01mol·L-1FeCl 溶液中,加入少量 FeCl 固
3 3
D Fe3水解程度增大
体,溶液颜色加深
13.电解法制备碘仿(CHI )的原理及主要原料如图,选择性交换膜只允许Na+通过,已知生成CHI 的方
3 3
程式:CH COCH 3IO CHI CH COO 2OH。下列叙述不正确的是
3 3 3 3
A.制备过程中需要不断搅拌,使丙酮与离子充分接触
B.左室生成IO的反应:2I 2e I 、I 2OH I IO H O
2 2 2
C.制备1mol碘仿实际消粍的电量大于理论值,可能的原因是3IO 2I IO
3
D.电解一段时间后,左室混合溶液的碱性增强
试卷第5页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
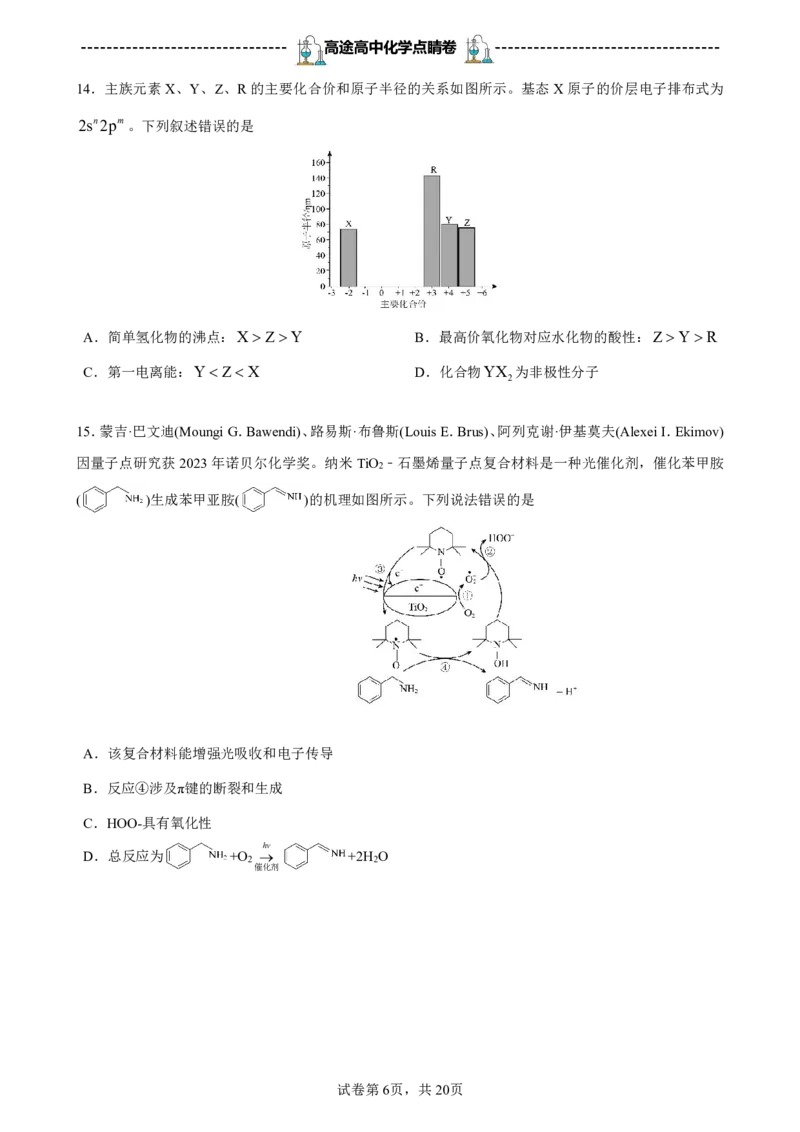
14.主族元素X、Y、Z、R的主要化合价和原子半径的关系如图所示。基态X原子的价层电子排布式为
2sn2pm。下列叙述错误的是
A.简单氢化物的沸点:XZY B.最高价氧化物对应水化物的酸性:ZYR
C.第一电离能:YZX D.化合物YX 为非极性分子
2
15.蒙吉·巴文迪(MoungiG.Bawendi)、路易斯·布鲁斯(LouisE.Brus)、阿列克谢·伊基莫夫(AlexeiI.Ekimov)
因量子点研究获2023年诺贝尔化学奖。纳米TiO ﹣石墨烯量子点复合材料是一种光催化剂,催化苯甲胺
2
( )生成苯甲亚胺( )的机理如图所示。下列说法错误的是
A.该复合材料能增强光吸收和电子传导
B.反应④涉及π键的断裂和生成
C.HOO‑具有氧化性
hv
D.总反应为 +O +2H O
2 2
催化剂
试卷第6页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
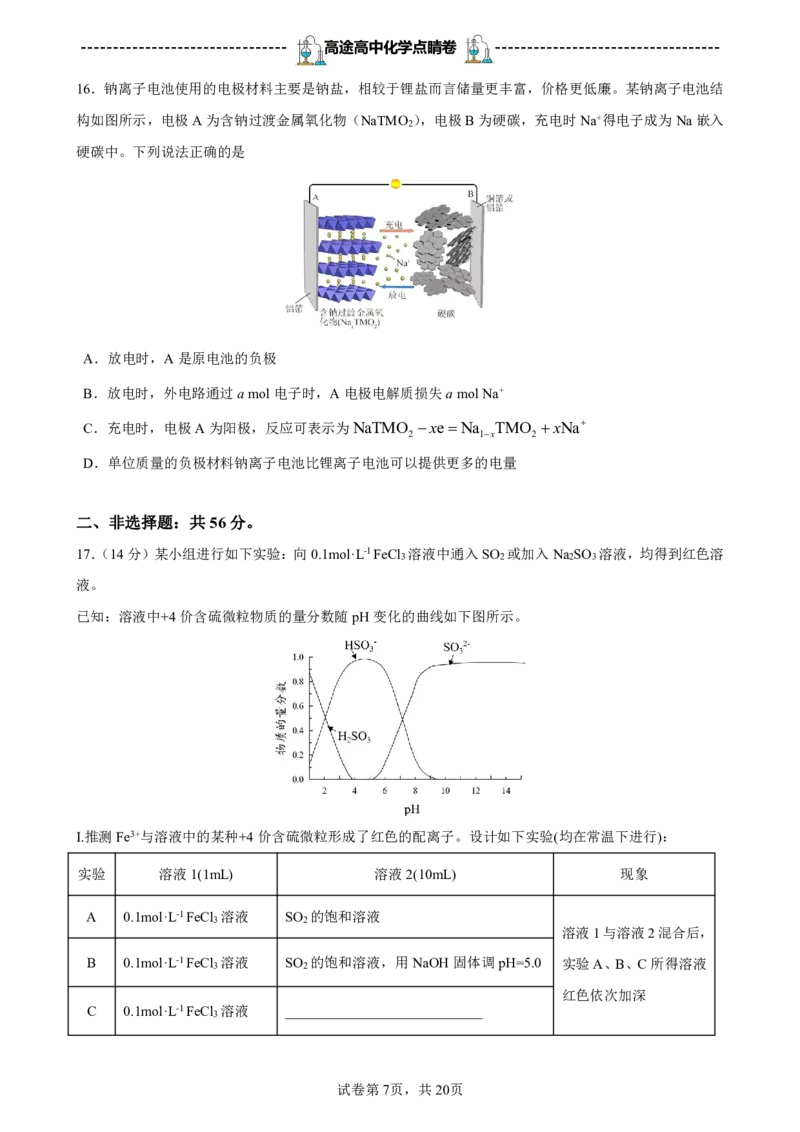
16.钠离子电池使用的电极材料主要是钠盐,相较于锂盐而言储量更丰富,价格更低廉。某钠离子电池结
构如图所示,电极A为含钠过渡金属氧化物(NaTMO ),电极B为硬碳,充电时Na+得电子成为Na嵌入
2
硬碳中。下列说法正确的是
A.放电时,A是原电池的负极
B.放电时,外电路通过amol电子时,A电极电解质损失amolNa+
C.充电时,电极A为阳极,反应可表示为NaTMO xe Na TMO xNa
2 1x 2
D.单位质量的负极材料钠离子电池比锂离子电池可以提供更多的电量
二、非选择题:共 56分。
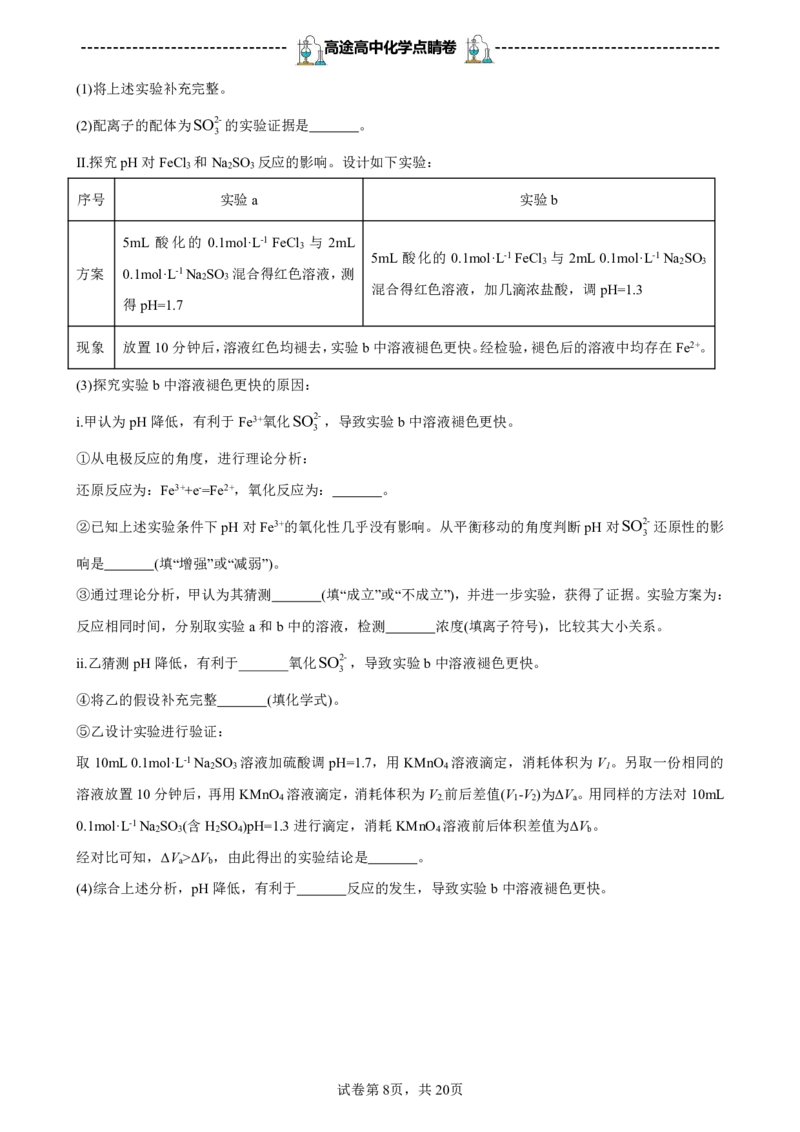
17.(14分)某小组进行如下实验:向0.1mol·L-1FeCl 溶液中通入SO 或加入Na SO 溶液,均得到红色溶
3 2 2 3
液。
已知:溶液中+4价含硫微粒物质的量分数随pH变化的曲线如下图所示。
I.推测Fe3+与溶液中的某种+4价含硫微粒形成了红色的配离子。设计如下实验(均在常温下进行):
实验 溶液1(1mL) 溶液2(10mL) 现象
A 0.1mol·L-1FeCl 溶液 SO 的饱和溶液
3 2
溶液1与溶液2混合后,
B 0.1mol·L-1FeCl
3
溶液 SO
2
的饱和溶液,用NaOH固体调pH=5.0 实验A、B、C所得溶液
红色依次加深
C 0.1mol·L-1FeCl 溶液 ____________________________
3
试卷第7页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(1)将上述实验补充完整。
(2)配离子的配体为SO2-的实验证据是 。
3
II.探究pH对FeCl 和Na SO 反应的影响。设计如下实验:
3 2 3
序号 实验a 实验b
5mL 酸化的 0.1mol·L-1 FeCl 与 2mL
3
5mL 酸化的 0.1mol·L-1FeCl 与 2mL0.1mol·L-1Na SO
3 2 3
方案 0.1mol·L-1Na SO 混合得红色溶液,测
2 3
混合得红色溶液,加几滴浓盐酸,调pH=1.3
得pH=1.7
现象 放置10分钟后,溶液红色均褪去,实验b中溶液褪色更快。经检验,褪色后的溶液中均存在Fe2+。
(3)探究实验b中溶液褪色更快的原因:
i.甲认为pH降低,有利于Fe3+氧化SO2-,导致实验b中溶液褪色更快。
3
①从电极反应的角度,进行理论分析:
还原反应为:Fe3++e-=Fe2+,氧化反应为: 。
②已知上述实验条件下pH对Fe3+的氧化性几乎没有影响。从平衡移动的角度判断pH对SO2-还原性的影
3
响是 (填“增强”或“减弱”)。
③通过理论分析,甲认为其猜测 (填“成立”或“不成立”),并进一步实验,获得了证据。实验方案为:
反应相同时间,分别取实验a和b中的溶液,检测 浓度(填离子符号),比较其大小关系。
ii.乙猜测pH降低,有利于_______氧化SO2-,导致实验b中溶液褪色更快。
3
④将乙的假设补充完整 (填化学式)。
⑤乙设计实验进行验证:
取10mL0.1mol·L-1Na SO 溶液加硫酸调pH=1.7,用KMnO 溶液滴定,消耗体积为V 。另取一份相同的
2 3 4 1
溶液放置10分钟后,再用KMnO 溶液滴定,消耗体积为V 前后差值(V -V )为ΔV 。用同样的方法对10mL
4 2. 1 2 a
0.1mol·L-1Na SO (含H SO )pH=1.3进行滴定,消耗KMnO 溶液前后体积差值为ΔV 。
2 3 2 4 4 b
经对比可知,ΔV>ΔV ,由此得出的实验结论是 。
a b
(4)综合上述分析,pH降低,有利于 反应的发生,导致实验b中溶液褪色更快。
试卷第8页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
18.(14 分)生产硫酸时产生的硫铁矿渣是一种重要的化工中间产物。研究人员利用某硫铁矿渣
[Fe O
38.36%
、FeO
12.43%
、SiO
35.88%
、CaO
1.76%
、Al
O
3.85%
,还有FeS、MnO、
2 3 2 2 3
CuO、PbS等]制备出高纯氧化铁,工艺流程如下:
溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3 Fe2 Al3 Mn2 Cu2
开始沉淀pH(c=1molL1 ) 1.1 5.8 3.0 4.4 4.2
完全沉淀pH(c=105 molL1 ) 2.8 8.3 4.7 10.1 6.7
已知K CaSO 4.9105,回答下列问题:
sp 4
(1)残渣的成分含有CuS、CaSO 、PbS、SiO 、 。
4 2
(2)流程中“中和”应调节溶液pH (填“3.0”、“2.8”或“2.8~3.0”),原因是 。
(3)烧渣中的 MnO 可制备 MnS , MnS 是一种 H S 的分解催化剂,某课题组用MnS ,在
2
Na S/Na SO 溶液中分解H S制备H ,反应部分历程如下(用h 表示催化剂):
2 2 3 2 2 VB
h VB 光 h VB e H 2 SHS H 2S2 2h VB S 2 2 HS 2h VB SH
SO2-+S2- S O2-+S2- SO2 SS O2 SO2 S2 2h S O2
3 2 2 3 3 2 3 3 VB 2 3
写出反应总离子方程式 ,反应中可重复利用的物质是 。
(4)由砷,铁,钙组成的某种新材料Ca Fe As ,的晶胞结构如图所示。已知:90,底边
x 2x 2x
1
边长为anm,高为bnm,1号原子的高为 bnm。
8
①距离2号原子最近的As原子有 个。
②该晶体密度为 gcm3 (N 为阿伏加德罗常数的值)。
A
(5)利用Ksp的计算可以判断沉淀的生成及转化,请写出一种沉淀的转化在生产生活中的用途____________。
试卷第9页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
19.(14分)随着时代的进步,人类对能源的需求量与日俱增,我国全球首套焦炉气化学合成法生产无水
乙醇的工业示范项目打通全流程实现,项目投产成功。
(1) 已知:i.2CO g 4H g CH OCH g H O g ΔH
2 3 3 2 1
ii.CH OCH g CO g CH COOCH g ΔH
3 3 3 3 2
iii.CH COOCH g 2H g CH CH OH g CH OH g ΔH
3 3 2 3 2 3 3
3CO g 6H g CH CH OH g CH OH g H O g H (用含ΔH 、ΔH 、
2 3 2 3 2 1 2
ΔH 的代数式表示),反应ii产物中C原子的杂化方式为_________。
3
(2)在恒温恒容密闭容器中充入3molCO(g)和6molH (g)仅发生反应
2
3CO
g
6H
g
CH CH OH
g
CH
OH
g
H
O
g
,下列叙述不正确的是___________(填
2 3 2 3 2
标号)。
A.混合气体总压强不随时间变化时,反应达到平衡状态
B.反应达到平衡时,CH OH体积分数可能为33.33%
3
C.反应达到平衡后,再同比例充入CO、H ,则CO、H 的平衡转化率不变
2 2
D.反应达到平衡后,再加入高效催化剂,乙醇平衡产率保持不变
(3)醋酸酯加氢制乙醇是一个乙酰基产物制备乙醇的路线,历程一般认为可分为如下步骤(*代表催化剂位点,
已知:CH CO*HCH CHO);
3 3
a.CH COOCH CH COCH O b.CH O CH O* (快)
3 3 3 3 3 3
c.CH CO* CH CO* (慢) d.CH CO*3HCH CH OH
3 3 3 3 2
e.CH O*HCH OH ……
3 3
其中,在b和c的步骤中,活化能较小的是 (填标号,下同),控制总反应速率的步骤是 ,
分析上述步骤,副产物除CH OH外,还可能有 (写一种即可,合理即可)。
3
(4)甲醇也是新能源的重要组成部分。以CO 、H 为原料合成CH OH涉及的反应如下:
2 2 3
iv.CO g 3H g CH OH g H O g ΔH <0
2 2 3 2 4
v.CO g H g CO g H O g ΔH >0
2 2 2 5
vi.CO g 2H g CH OH g ΔH <0
2 3 6
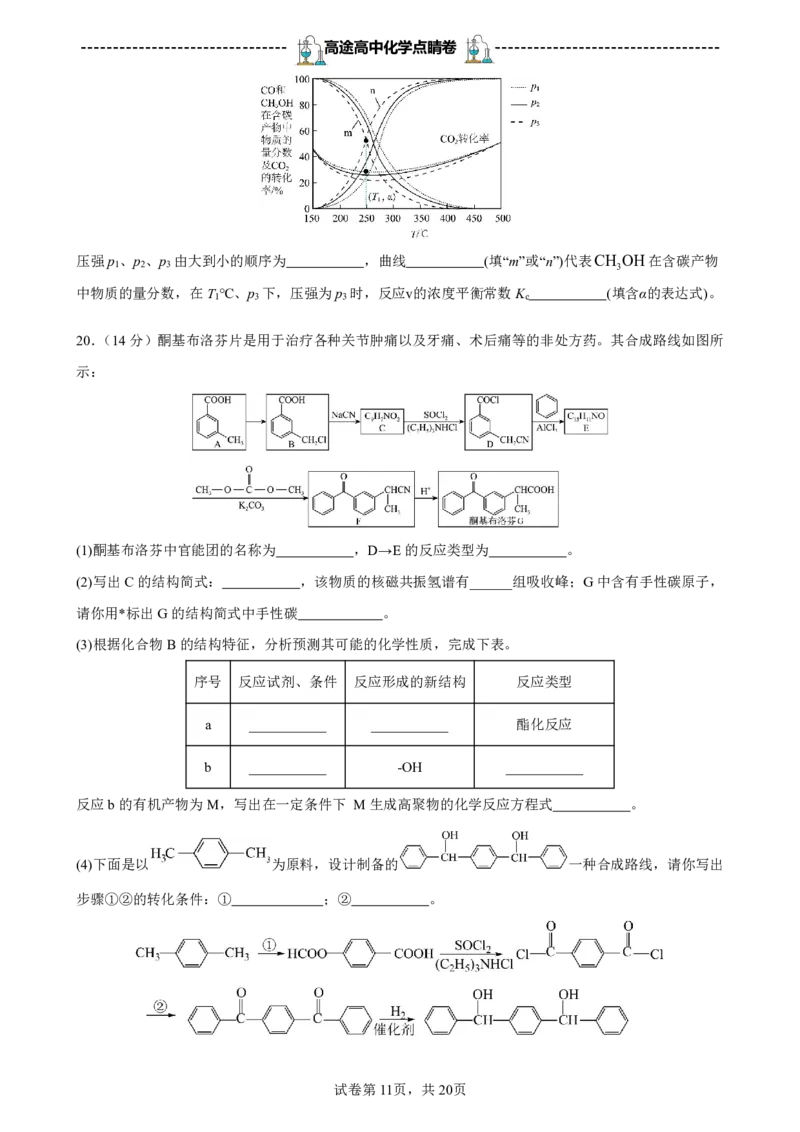
在不同压强下、按照n CO :n H 1:3进行投料,在容器中发生上述3个反应,平衡时,CO和CH OH
2 2 3
在含碳产物(即CH OH和CO)中物质的量分数及CO 的转化率α随温度的变化如图,
3 2
试卷第10页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
压强p 、p 、p 由大到小的顺序为 ,曲线 (填“m”或“n”)代表CH OH在含碳产物
1 2 3 3
中物质的量分数,在T ℃、p 下,压强为p 时,反应ⅴ的浓度平衡常数K (填含α的表达式)。
1 3 3 c
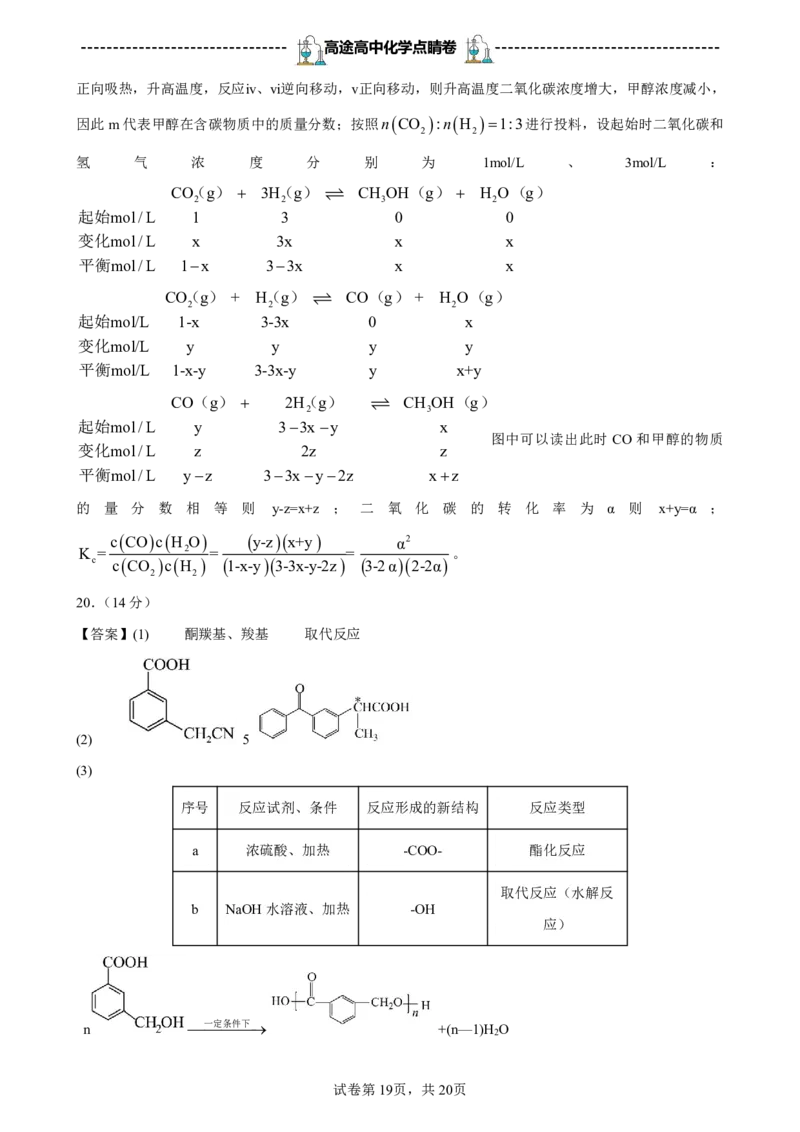
20.(14分)酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所
示:
(1)酮基布洛芬中官能团的名称为 ,D→E的反应类型为 。
(2)写出C的结构简式: ,该物质的核磁共振氢谱有______组吸收峰;G中含有手性碳原子,
请你用*标出G的结构简式中手性碳 。
(3)根据化合物B的结构特征,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
a ___________ ___________ 酯化反应
b ___________ -OH ___________
反应b的有机产物为M,写出在一定条件下 M生成高聚物的化学反应方程式 。
(4)下面是以 为原料,设计制备的 一种合成路线,请你写出
步骤①②的转化条件:① ;② 。
试卷第11页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2023 年广东省普通高中学业水平选择性考试模拟测试卷
化学参考答案
1.【答案】B
【详解】A.飞机涡扇的耐高温的合金材料是钛合金,属于新型合金,A不符合题意;
B.碳化硅属于无机非金属材料,B符合题意;
C.钛合金的硬度大、耐酸碱的腐蚀,因此可用于蛟龙号载人舱的舱体材料等,属于新型合金,C不符合
题意;
D.新能源汽车储氢材料,有LaNi 、Mg Cu、Mg Ni等,属于新型合金,D不符合题意;
5 2 2
故选B。
2.【答案】B
【详解】A.古壁画颜料中所用的铁红,其成分为Fe O ,为红色固体,故A正确;
2 3
B.古陶瓷修复所用的熟石膏,其成分为2CaSO ⋅H O,Ca(OH) 是消石灰,故B错误;
4 2 2
C.龟甲的成分之一羟基磷灰石,组成上分析为盐类化合物,属于无机物,故C正确;
D.碳原子的价电子轨道表示式 ,故D正确;
故答案选B。
3.【答案】D
【解析】A. 在燃煤中添加生石灰的主要目的是减少二氧化硫的排放,A错误;
B. 催化剂不能改变转化率,B错误;
C. 单晶硅是重要的半导体材料,可以作为太阳能光伏电池的基底材料,C错误;
D. 有机磷农药多为磷酸酯或硫代磷酸酯类物质,肥皂水因有利于其水解而解毒,D正确。
4.【答案】C
【详解】A.浓盐酸与MnO 加热条件制取Cl ,该装置中少了酒精灯,A项不能达到实验目的;
2 2
B.制取的Cl 含有HCl,需要用饱和氯化钠洗气装置长进短出,该装置达到无法除杂的目的,B项不能达
2
到实验目的;
C.氯气溶于水存在平衡Cl +H OHCl+HClO,加入CaCO 消耗HCl使平衡正向移动HClO浓度增大,
2 2 3
C项能达到实验目的;
D.最终得到浓的HClO中含有CaCO 固体,需要进行过滤除去,该装置错误,D项不能达到实验目的;
3
故选C。
5.【答案】D
试卷第12页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
【解析】A.酸性氧化物与水反应只生成对应的酸,NO 与水反应除了生成硝酸,还生成了NO,则NO
2 2
不属于酸性氧化物,故A错误;
B.84消毒液有强氧化性,不能用pH试纸测pH,B错误;
C.食盐中含有碘酸钾,不能使淀粉变蓝,选项C错误;
D.植物油中含有碳碳双键,具有还原性,能发生氧化反应,使酸性高锰酸钾溶液褪色,选项D正确;
6.【答案】A
【分析】根据图示可知该电化学腐蚀中,硫酸根离子得电子生成硫离子,电极反应式为:
SO2-+8e-+4H O=S2-+8OH-,铁管道做负极,发生失电子的氧化反应生成亚铁离子,据此结合电化学腐
4 2
蚀原理分析解答。
【详解】A. 锌的金属活动性大于铁的,所以铁管道上镀锌,锌隔绝了铁与外界的接触,既使锌破损,锌
做负极,铁做正极,被保护,可以延缓管道的腐蚀,A正确;
B.根据铁管道的正极反应:SO2-+8e-+4H O=S2-+8OH-可知,该腐蚀会使铁管道附近土壤的pH增大,
4 2
B错误;
C.根据上述分析可知,铁管道正极不是氧气得电子,发生的不是吸氧腐蚀,C错误;
D.高温下,水蒸气与铁发生氧化还原反应生成四氧化三铁和氢气,与上述类型腐蚀不同,D错误;
答案选C。
7.【答案】C
【详解】A.用氢氟酸制作雕花玻璃,是因为SiO 能与氢氟酸发生反应,与是否是酸性氧化物无关,A错
2
误;
B.熔融的AlCl 不发生电离,B错误;
3
C.草木灰主要成分为碳酸钾,属于钾肥,栽培韭菜施加草木灰,可使韭菜长的浓绿粗壮,C正确;
D.聚苯乙烯材料有保温隔热的作用,车厢使用聚苯乙烯材料可保持车厢温度恒定,D错误;
故选C。
8.【答案】D
【详解】A.分子中酰胺基、酚羟基均会和氢氧化钠溶液反应,故1molT最多能与2molNaOH反应,A正
确;
B.对乙酰氨基酚中酚羟基邻对位上的氢可以和浓溴水发生取代反应,B正确;
C.分子中含有酰胺基、酚羟基两种官能团,C正确;
D.酚羟基与碳酸钠反应生成碳酸氢钠,不能生成CO ,D错误;
2
故选D。
试卷第13页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
9.【答案】A
【详解】A.蔗糖遇到浓硫酸变黑,是由于浓硫酸具有脱水性,将蔗糖中氢元素和氧元素以水的比例脱出,
不是吸水性,故A错误;
B.无水硫酸铜变蓝,可以用来检验水,但是品红溶液和溴水都有水,不确定使硫酸铜变蓝的水是否由反
应分解产生的,B正确;
C.a中品红褪色,体现二氧化硫的漂白性,b中溴水褪色,体现二氧化硫的还原性,C正确;
D.Ⅲ中溶液颜色变浅,说明二氧化硫反应完全了,Ⅳ中澄清石灰水变浑浊了,说明产生了二氧化碳气体,
D正确;
故选A。
10.【答案】A
【分析】由题中信息可知,在地壳中的含量仅次于铝,居第四位的元素是Fe元素,由Fe元素的化合价和
物质类别,推断a为Fe、b为FeO、c为Fe O 、d为Fe(OH) 、eFe(OH) 、f为Fe2+、g为Fe3+、h为FeO2,
2 3 3 2 3
据此解答;
【详解】A.铁与氯气发生化合反应会生成FeCl ,A错误;
3
B.Fe(OH)
2
可以和O
2
、H
2
O反应生成Fe(OH)
3
,方程式为:4FeOH O 2H O 4FeOH ,该反应为
2 2 2 3
化合反应,B正确;
C.Fe O 是红色的,用途之一是做颜料,C正确;
2 3
D.FeO2具有强氧化性,能够杀菌消毒, +6价的铁被还原成+3价,铁离子水解形成氢氧化铁胶体具有
3
较大的表面积,吸附悬浮杂质可以做净水剂,D正确;
答案选A。
11.【答案】D
【解析】A. 在标准状况下,HF为液体,不能用气体摩尔体积计算其物质的量,A错误;
B. 氯气和水是可逆反应,标况下11.2LCl 的物质的量为0.5mol,含氯原子数为N ,11.2LCl 溶于水,
2 A 2
一部分氯气未反应,所以依据氯原子守恒,溶液中Cl、ClO和HClO的微粒数之和小于N ,B错误;
A
C. 没给体积,无法计算离子数目,C错误;
D.1个吡咯分子中有4个C-Hσ键、3个C Cσ键,2个C Nσ键和1个N Hσ键,共10个σ键,0.2mol
含有σ键数为2N ,D正确。
A
12.【答案】C
【详解】A.过氧化钠在空气中久置变为碳酸钠,过氧化钠、碳酸钠与盐酸反应都能产生气体,不能说明
试卷第14页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
过氧化钠完全转化为碳酸钠,A错误;
B.CH 与Cl 光照下反应产生的气体为氯代甲烷和HCl,氯代甲烷难溶于水,HCl使湿润的蓝色石蕊试
4 2
纸变红,B错误;
C.Cl原子的电负性大于H,使羟基极性增强,易发生断裂,导致酸性增强,故C正确;
D.向0.01molL1FeCl 溶液中,加入少量FeCl 固体,Fe3浓度增大,平衡正向移动,因为生成氢氧
3 3
化铁也会导致溶液颜色加深,故D错误;
故选C。
13.【答案】D
【分析】本题属于电解池,右侧石墨为阴极,电极反应为:2H++2e-=H ,左侧石墨为阳极,电极反应为:
2
2I--2e-=I ,随后单质碘和氢氧化钠反应生成碘离子和次碘酸根离子,以此解题。
2
【详解】A.通过搅拌,可以使反应物接触更加充分,提高转化率,A正确;
B.根据分析可知,左室生成IO的反应:2I 2e I 、I 2OH I IO H O,B正确;
2 2 2
C.制备1mol碘仿实际消粍的电量大于理论值,可能是次碘酸根离子发生歧化反应而被消耗,歧化反应的
方程式为:3IO 2I IO,C正确;
3
D.根据选项B分析可知,电解过程中左室会消耗氢氧根离子,则电解一段时间后,左室混合溶液的碱性
会减弱,D错误;
故选D。
14.【答案】C
【分析】基态X原子的价层电子排布式为2sn2pm,化合价为-2价,说明最外层是6个电子第二周期元素,
X为O元素,Y和Z原子半径与氧元素相差不大,化合价为+4和+5价,说明和氧元素是同周期相邻元素,
分别为C和N元素,R的半径较大,化合价为+3价,R是Al元素。
【详解】A.简单氢化物的沸点:H O>NH >CH ,A正确;
2 3 4
B.最高价氧化物对应水化物的酸性:HNO >H CO >Al(OH) ,B正确;
3 2 3 3
C.第一电离能:CΔV 可知,在空气中放置相同时间,结果酸性弱的溶液中SO2-消耗高锰酸钾的量少,酸
a b 3
性强的溶液中SO2-消耗高锰酸钾的量多,说明pH降低不利于O 氧化SO2-,乙猜测不成立。
3 2 3
(4)溶液酸性增强,会发生反应H++SO2-⇌HSO ,H++HSO ⇌H
SO
,pH降低,有利于SO2-与H+反应
3 3 3 2 4 3
的发生,导致实验b中溶液褪色更快。
18.(14分)
【答案】(1) S
(2)3.0 Fe2氧化会产生H,氧化完后溶液pH2.8~3.0,使Fe3沉淀而Mn2、Cu2、A13、
不沉淀(4Fe2 O 10H O4Fe(OH) 8H 或4Fe2 O 6H O4FeO(OH)8H 代替“Fe2
2 2 3 2 2
氧化会产生H ”也可)
催化剂 6.041023
(3) 2SO2-+2H S 2S O2-+2H Na SO (4)8 (5)除水垢
3 2 2 3 2 2 3 a2bN
A
【分析】硫铁矿渣用硫酸“酸浸”,得到硫酸锰、硫酸铁、硫酸亚铁、硫酸铝、硫酸铜等,二氧化硅、PbS
不溶解,钙转化为微溶的硫酸钙沉淀,FeS溶于酸生成S2,S2能被Fe3氧化为S,CuS的K 很小,
sp
部分CuO会转化为CuS,故滤渣1为二氧化硅、CuS、CaSO 、PbS、S;滤液中和后通入空气,空
4
气中氧气将亚铁离子氧化为铁离子,铁离子转化为沉淀,洗涤、干燥、煅烧后得到产品;
【详解】(1)烧渣化学成分主要是Fe O (38.36%)、FeO(12.43%)、SiO (35.88%)、CaO(1.76%)、
2 3 2
Al O (3.85%)、还有FeS、MnO、CuO、PbS等,加入硫酸后不溶物有SiO 、CaSO 、PbS,Mn是
2 3 2 4
比较活泼的金属,因此MnO溶于硫酸,FeS溶于酸生成S2,S2能被Fe3氧化为S,因CuS的K 很
sp
小,部分CuO会转化为CuS;故得到残渣的成分含SiO 、CuS、CaSO 、PbS、S;
2 4
(2)滤液中含有Fe3、Fe2、Al3、Mn2、Cu2、少量Ca2,“中和”调节溶液pH,使Fe3沉淀,而
Al3、Mn2、Cu2 不 沉 淀 , 应 使 2.8pH3 , 之 后 氧 化 环 节 Fe2 Fe3 ,
4Fe2 O 10H O 4Fe(OH) 8H,该过程产生H,影响Fe3的沉淀,因此提前多加入碱中和掉
2 2 3
产生的酸,因此需多加碱,需调节pH3.0,此时Al3等会沉淀,但氧化完后就溶解了;
试卷第17页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
(3)由题意可知,用MnS,在Na S/Na SO 溶液中分解H S制备H ,结合历程可知,总反应为SO2-
2 2 3 2 2 3
催化剂
和硫化氢在催化剂下生成S O2-和氢气,故反应为:2SO2-+2H S 2S O2-+2H ;反应中生成S O2-,
2 3 3 2 2 3 2 2 3
S O2-在酸性条件下歧化为二氧化硫和硫单质,二氧化硫被碱液吸收生成亚硫酸根离子和水,故反应中可
2 3
重复利用的物质是Na SO ,
2 3
(4)①2号原子为Ca原子,距离2号原子最近的As为8个(黑球或白球);
240456475 604
②该晶胞中含有Ca原子2个,Fe原子4个,As原子4个,晶胞的质量为 g= g,
N N
A A
6.041023
晶胞的体积为a2b×10-21cm3,该晶体的密度为 g/cm3。
a2bN
A
19.(14分)
【答案】(1)ΔH +ΔH +ΔH ,sp2、sp3
1 2 3
(2)BC
(3)b c 乙醛
α2
(4)P>P>P
m
1 2 3
3-2α 2-2α
【详解】(1)由盖斯定律可知:目标反应=ⅰ+ⅱ+ⅲ,则ΔH=ΔH +ΔH +ΔH ;乙酸甲酯中甲基的C原子为
1 2 3
sp3杂化,酯基中的C原子为sp2杂化。
(2)恒容容器中反应正向体积减小,总压强不变说明各组分含量不再变化,达到平衡,A正确;设CO变
化量为3xmol,则CO、H 、CH CH OH、CH OH、H O,的平衡量分别为(3-3x)mol、(6-6x)mol、xmol、
2 3 2 3 2
x
xmol、xmol,CH OH的体积分数为 ,当x=1时其体积分数为33.33%,该反应是可逆反应,3x≠3,
3
96x
则x≠1,B错误;反应达到平衡后,再同比例充入CO、H ,恒温恒容容器中相当于增大压强,平衡正向
2
移动,CO、H 转化率增大,C错误;催化剂不能改变反应限度,因此加入催化剂乙醇的平衡转化率不变,
2
D正确;
(3)活化能越小反应越快,总反应速率取决于速度慢的步骤,因此活化能较小的是b,控制总反应速率的
步骤是c,根据反应历程可知,副产物可能还有乙醛;
(4)反应ⅳ、ⅵ正向体积减小,ⅴ体积不变,增大压强二氧化碳的转化率增大,相同温度下二氧化碳转化
率从小到大对应的压强顺序为P 、P 、P ,则压强从大到小的顺序为P>P>P ;反应ⅳ、ⅵ正向放热,ⅴ
3 2 1 1 2 3
试卷第18页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
正向吸热,升高温度,反应ⅳ、ⅵ逆向移动,ⅴ正向移动,则升高温度二氧化碳浓度增大,甲醇浓度减小,
因此m代表甲醇在含碳物质中的质量分数;按照n CO :n H 1:3进行投料,设起始时二氧化碳和
2 2
氢 气 浓 度 分 别 为 1mol/L 、 3mol/L :
CO(g) 3H(g) CH OH(g) H O(g)
2 2 3 2
起始mol/L 1 3 0 0
变化mol/L x 3x x x
平衡mol/L 1x 33x x x
CO(g) + H(g) CO(g) + H O(g)
2 2 2
起始mol/L 1-x 3-3x 0 x
变化mol/L y y y y
平衡mol/L 1-x-y 3-3x-y y x+y
CO(g) 2H(g) CH OH(g)
2 3
起始mol/L y 33x y x
图中可以读出此时 CO 和甲醇的物质
变化mol/L z 2z z
平衡mol/L yz 33xy2z xz
的 量 分 数 相 等 则 y-z=x+z ; 二 氧 化 碳 的 转 化 率 为 α 则 x+y=α ;
c CO c H O y-z x+y α2
K = 2 = = 。
c c CO c H 1-x-y 3-3x-y-2z 3-2α 2-2α
2 2
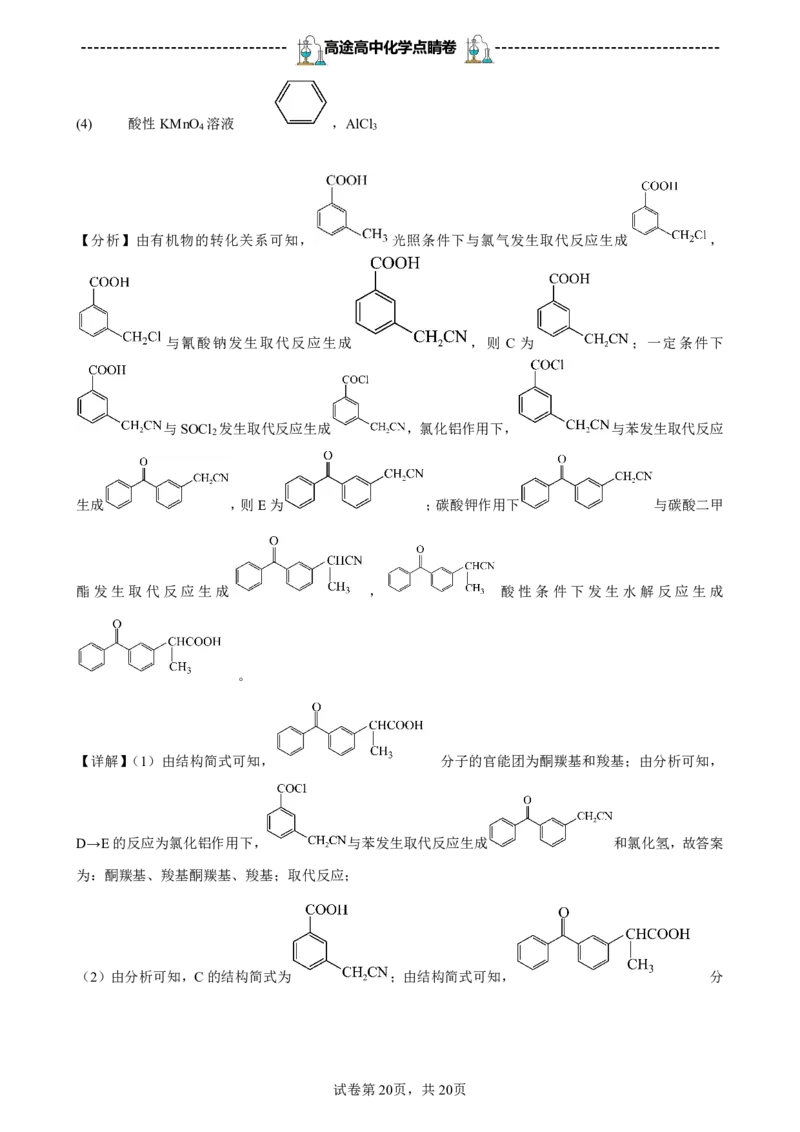
20.(14分)
【答案】(1) 酮羰基、羧基 取代反应
(2) 5
(3)
序号 反应试剂、条件 反应形成的新结构 反应类型
a 浓硫酸、加热 -COO- 酯化反应
取代反应(水解反
b NaOH水溶液、加热 -OH
应)
n
一定条件下
+(n—1)H O
2
试卷第19页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
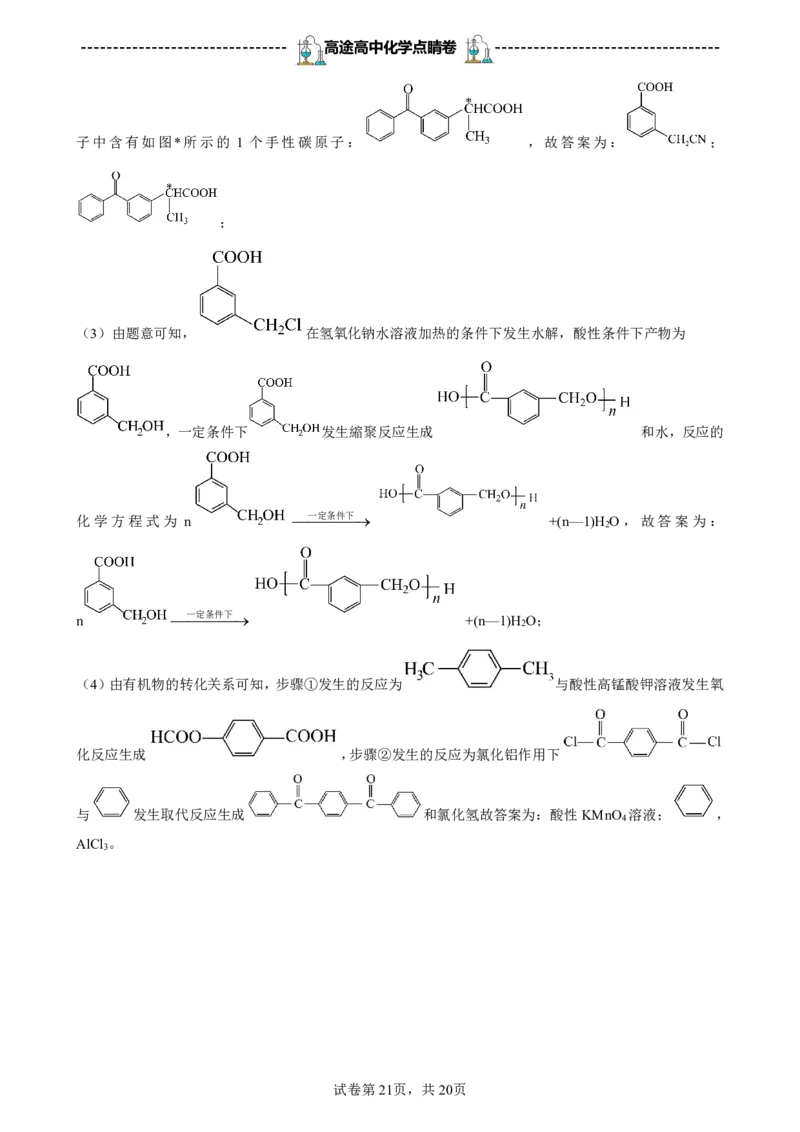
(4) 酸性KMnO 溶液 ,AlCl
4 3
【分析】由有机物的转化关系可知, 光照条件下与氯气发生取代反应生成 ,
与氰酸钠发生取代反应生成 ,则 C 为 ;一定条件下
与SOCl 发生取代反应生成 ,氯化铝作用下, 与苯发生取代反应
2
生成 ,则E为 ;碳酸钾作用下 与碳酸二甲
酯发生取代反应生成 , 酸性条件下发生水解反应生成
。
【详解】(1)由结构简式可知, 分子的官能团为酮羰基和羧基;由分析可知,
D→E的反应为氯化铝作用下, 与苯发生取代反应生成 和氯化氢,故答案
为:酮羰基、羧基酮羰基、羧基;取代反应;
(2)由分析可知,C的结构简式为 ;由结构简式可知, 分
试卷第20页,共20页-------------------------------- 高途高中化学点睛卷 -----------------------------------
子中含有如图*所示的 1 个手性碳原子: ,故答案为: ;
;
(3)由题意可知, 在氢氧化钠水溶液加热的条件下发生水解,酸性条件下产物为
,一定条件下 发生縮聚反应生成 和水,反应的
化学方程式为 n 一定条件下 +(n—1)H O,故答案为:
2
n 一定条件下 +(n—1)H O;
2
(4)由有机物的转化关系可知,步骤①发生的反应为 与酸性高锰酸钾溶液发生氧
化反应生成 ,步骤②发生的反应为氯化铝作用下
与 发生取代反应生成 和氯化氢故答案为:酸性KMnO 溶液; ,
4
AlCl 。
3
试卷第21页,共20页