文档内容
南宁二中· 年 月高三冲刺考
2025 5
化学 答案
一、选择题:本大题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.A
【详解】A.Fe O 为黑色固体,具有磁性,可用于制作打印机的墨粉,A错误;B.SiO 具有良好的
3 4 2
光学性能,可用于制作光导纤维,用于通信,B正确;C.NaN 受到撞击时能迅速产生大量N ,
3 2
在汽车安全气囊中作气体发生剂,C正确;D.抗坏血酸具有还原性,可用作水果罐头中抗氧
化剂,防止食物氧化变质,D正确;故选A。
2. B
【详解】A.在化合物中,通常连接H的N、O、F原子可与连接在N、O、F原子上的H原子间形成
氢键,图中所画虚线右侧的H原子连在C原子上,不能形成氢键,A错误;
B. 的官能团为羧基,命名时,羧基碳原子的编号为1,连接甲基的
主链碳原子编号为2,连接苯基的主链碳原子编号为3,则名称为2-甲基-3-苯基丙酸,B正确;
C.图中所示结构中,两个-CH -位于双键碳原子的同一侧,为顺式结构,C错误;D.图中所
2
示重叠,为N原子的2p轨道肩并肩重叠,形成π键,σ键应是头碰头重叠形成,D错误;故选
B。
3. D
616
【详解】A.SF 中S原子的价层电子对数为 =6,发生sp3d2杂化,其VSEPR模型为正八面体,
6
2
62
A正确;B.SO2中S原子的价层电子对数为 =4,发生sp3杂化,SO 中S原子的价层
4 2 3
6
电子对数为 =3,发生sp2杂化,则OSO:SO2小于SO ,B正确;C.O 中,中心
2 4 3 3
6
O原子的价层电子对数为 =3,发生sp2杂化,其最外层含有1个孤电子对,O-O键为极性
2
键,O 为极性分子,C正确;D.基态硒的简化电子排布式为 Ar 3d104s24p4,D项错误;
3
4.A
【详解】A.乙醇和乙醇在浓硫酸、加热的条件下发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,
分水器可以分离产生的H O,促进平衡正向移动,可以提高乙酸乙酯的产率,A正确;B.配
2
制银氨溶液时应该向硝酸银溶液中滴加氨水直至最初生成的沉淀恰好完全溶解,B错误;C.乙
酸乙酯中的乙酸、乙醇互溶,应该用蒸馏的方法分离,C错误;D.分离苯和硝基苯的混合物
时,蒸馏装置中温度计的水银球应该放在支管口,D错误;故选A。
5.D
【解析】A.Y中苯环上碳为sp2杂化,-CN中碳为sp杂化,甲基上的碳为sp3杂化,A错误;B.X
高三化学答案 第 1 页 共 9 页与稀硫酸,氨基为碱性基团与氢离子结合生成盐,-CN在酸性条件下发生水解,B错误;C.Y
上有一个N连接三个单键,为sp3杂化,所有原子不可能共面,C错误; D.X和氢气完全
加成后苯环变成环己烷环,三个支链位置的碳都是手性碳,故分子中有3个手性碳,D正确;
答案选D。
6.C
【详解】A.酸性:H CO>HClO>HCO- ,CO2通入足量的NaClO溶液中:CO +ClO−+H O=HClO+HCO-,
2 3 3 2 2 3
故A错误;B.用惰性电极电解CuCl2水溶液,阳极氯离子放电生成氯气,阴极铜离子得电
子生成铜:2Cl−+Cu2+ 通电 Cu+Cl2↑,故B错误;C.用Na SO 溶液吸收少量Cl2生成亚硫酸
2 3
氢钠:3SO2+Cl2+H2O=2HSO+2Cl−+SO2,故C正确;D.草酸是弱电解质,用高锰酸钾
3 3 4
标准溶液滴定草酸:2MnO+5H C O +6H+=2Mn2++10CO2↑+8H O,故D错误;故选C。
4 2 2 4 2
7.B
【分析】已知X、Y、Z、L、M、R为短周期主族元素,原子序数依次递增,X的单质保存在固态石蜡
中,X可以形成X+,X为Li元素,Y形成4个共价键,则Y为C元素,L形成2个共价晶,
L为O元素,R形成6个共价键,R为S元素,M形成1个共价键,M为F元素,整个阴离
子带一个单位的负电荷,所以Z为N元素,以此解答。
【详解】A.C元素氢化物较多(如苯),沸点不一定比NH 低,A错误;B.Li的金属性弱于Na、K,
3
Li和O 反应生成的化合物只有Li O,种类少于Li的其它同族金属元素,B正确;C.M为F
2 2
元素,第二周期中第一电离能最大的是Ne,C错误;D.H O和OF 中心O原子价层电子对
2 2
1
数均为2 621 =4,都含有2个孤电子对,由于氟的电负性比氧大,OF 中电子对更
2
2
偏向氟原子,中心氧原子周围电子云密度降低,孤电子对间的排斥作用减弱,而H O中氧的
2
电负性比氢大,电子对更偏向氧原子,氧原子周围电子云密度较大,孤电子对间的排斥作用
较强,所以H O的键角更大,D错误;故选B。
2
8.A
【详解】A.硫化钠溶液与足量硫酸锌溶液完全反应生成硫化锌沉淀和硫酸钠,向反应后的溶液中再加
入少量硫酸铜溶液,白色沉淀转化为黑色沉淀说明硫化锌的溶度积大于硫化铜,A正确;B.向
氯化钙溶液中通入CO ,未出现白色沉淀,是因为碳酸的酸性比盐酸的酸性弱,氯化钙和CO
2 2
不反应,B错误;C.二氧化硫在水中的溶解度大于二氧化碳,二氧化硫饱和溶液中亚硫酸的
浓度大于二氧化碳饱和溶液中碳酸的浓度,则前者饱和溶液的 pH小于后者不能说明亚硫酸
的酸性强于碳酸,C错误;D.氯化铁在溶液中水解使溶液呈酸性,氯化铁溶液加水稀释后溶
液pH变大,是因为加水稀释,溶液中氢离子浓度减小,与水解程度增大无关,D错误;故选
A。
9.C
【分析】二氧化钛废渣与铝粉进行铝热还原生成 TiO 1x1.5 和难溶于酸和碱的 Al O ,同
x 2 3
时铁的氧化物转化为铁单质,加入盐酸后,TiOₓ、Fe与盐酸反应生成Fe2+、Ti3+和氢气,难溶
的 αAl O 为滤渣,滤液中 Fe2、Ti3被 H O 氧化生成 Fe3和 Ti4,Ti4水解生成
2 3 2 2
TiO xH O,过滤分离,滤液含有 Fe3和Ca2。
2 2
【详解】A.TiO 中 Ti为高价态,具有弱氧化性,A 正确;B.“浸取”过程中,不需要惰性气体保护,
2
产生的 Ti3在下一步需要氧化生成 Ti4,B正确;C.若快速加入 H O ,H O 会在生成的
2 2 2 2
高三化学答案 第 2 页 共 9 页Fe3催化作用下分解,C错误;D.铝热反应中铁的氧化物转化为铁单质, TiO 转化为
2
TiO (1≤x≤1.5),故氢气可能是铁、过量铝粉及 Ti2与盐酸反应产生的,D正确;答案选C。
x
10.D
【详解】A.由电池中硫还原反应涉及从S 分子到Li S固体的复杂的16电子转化过程可知,电池总反
8 2
应为16Li+S =8Li S,故A正确;B.由图可知,Li S 转化生成的Li S 和Li S 最终转化为
8 2 2 4 2 2 2 3
Li S,说明Li S 是控制整体疏还原反应过程的关键电化学中间体,故B正确; C.由题给
2 2 4
信息可知,Li S的水溶性较差,所以选择合适的溶剂,有利于增强电解质溶液的导电性,能
2
让电池保持稳定的电流输出,故C正确;D.充电时,与直流电源正极相连的左侧电极为电
解池的阳极,Li S在阳极失去电子发生氧化反应生成淡黄色S 和锂离子,S2-中x减小,则
2 8 x
正极附近颜色变浅,由红色变到黄色,S 为淡黄色固体,所以颜色不可能最后变成无色,故
8
D错误;故选D。
11.B
1 1
【分析】晶胞中黑球的个数是8 1 2,白球的个数是4 2 4,则黑球代表Ru,白球代表O,
8 2
据此解答。
【详解】A.以晶胞内部的O为研究对象,由结构可知,其与周围最近的3个Ru相连,则O原子的
配位数为3,A正确;B.晶体中O原子构成的正八面体空隙均有Ru原子填充(位于体心的
Ru原子),但若晶胞中由O原子围成的非正八面体未必有Ru原子填充,B错误;C.体心与
2a2+b2
顶点的距离为体对角线的一半,解三角形可得该距离为 nm,C正确;D.由分析可
2
266
知,晶体质量为 g,体积为a2b1021cm3,
N
A
266 2.661023
则晶胞密度为 gcm-3 gcm-3,D正确;故选B。
a2b1021N a2bN
A A
12.A
33
【详解】A.苯分子中,C原子的价层电子对数为 =3,发生sp2杂化,在 中,与-R相
2
44
连的碳原子,价层电子对数为 =4,发生sp3杂化,对溴苯分子,相当于苯分子中有1个
2
H原子被1个Br原子取代,C原子的杂化方式不变,所以C经历的杂化为:sp2 sp3 sp2,
A正确;B.从反应过程可以看出,AlCl 是该反应的催化剂,则其能改变反应速率但不能改
3
变平衡的转化率,B不正确; C.反应过程中若加入NaOH,会与AlCl 反应生成Al(OH) 沉
3 3
淀等,从而降低AlCl 的催化活性,会使反应速率降低,不利于反应进行,不能提高烷基化转
3
化率,C不正确;D.酚羟基是邻、对位定位基,苯酚在AlCl 催化下与溴乙烷发生取代反应
3
时,羟基碳邻、对位(碳)上的氢原子容易被取代,间位(碳)上的氢原子难被取代,则能得到大
量邻乙基苯酚和少量间乙基苯酚,D不正确;故选A。
高三化学答案 第 3 页 共 9 页13.C
【分析】随着反应进行,甲苯含量减小,苯甲醇、苯甲醛含量增大,反应均为放热反应,在绝热容器
中进行,随着反应进行温度升高,由题意:140℃时,c /c 0.5,170℃时,c /c 0.6,
1 2 1 2
则升高温度后,苯甲醇选择性增大而苯甲醛选择性减小,则XYZ分别为甲苯、苯甲醇、苯甲
醛;
【详解】A.由分析,Z曲线代表的是苯甲醛,A正确; B.由分析,升高反应温度,苯甲醛的选择
性降低,B正确;C.增加氧化剂氧气的浓度,可以提高反应物甲苯的转化率,但氧气浓度过
大,会继续氧化苯甲醛为苯甲酸,不利于提高苯甲醛的选择性,C错误; D.在一定的反应
时间内,选择对生成苯甲醇更有利的催化剂,可以提高生成苯甲醇的比例,D正确;故选C。
14.D
【详解】A.图1中,随着溶液pH值的增大,δ(H S)逐渐减小、δ(HS-)先增大后减小、δ(S2-)逐渐增大,
2
则曲线①②③分别表示δ(H S)、δ(HS-)、δ(S2-)与pH值的关系,pH=6.97时,δ(H S)=δ(HS-),
2 2
c HS- c(H+)
则c(H S)=c(HS-),K = =10-6.97,pH=12.90时,δ(HS-)=δ(S2-),c(HS-)=c(S2-),
2 a1
c H S
2
c S2- c(H+)
K = =10-12.90,NaHS溶液中HS-的电离常数K =10-12.90,水解常数
a2
c
HS- a2
K 10-14
K = w = =10-7.03>10-12.90,以水解为主,故溶液显碱性;故A正确;B.图2中P点pH=8.94,
h2 K 10-6.97
a1
c HS- c(H+) c HS- c S2- c(H+) c S2-
K = = 108.94=10-6.97,K = 108.94 =10-12.90,这
a1 c H S c H S a2 c HS- c HS-
2 2
c S2-
两个式子相乘得 =10-1.99,H S饱和溶液浓度为0.1mol/L,电离程度非常小,所以溶液
2
c H S
2
中c(H S)≈0.1mol/L,c(S2-)≈10-2.99mol/L,-lgc=23.11,则c=10-23.11mol/L,
2
K (M S)=c2(M+)•c(S2-)=(10-23.11)2×10-2.99=10-49.21,K (NS)=c(N2+)•c(S2-)=10-23.11×10-2.99=10-26.1,随
sp 2 sp
着pH值的增大,c(S2-)增大,金属阳离子浓度减小,但c(N2+)减小的更快,所以⑤表示H S
2
饱和溶液中N2+的-lgc与pH的关系;故B正确; C.根据图2知,逐滴加入H S饱和溶液,
2
1049.21
浓度均为0.01mol/L的M+、N2+的混合溶液,当c(S2-)= mol/L=10-45.21mol/L时M+开始
(0.01)2
1026.1
沉淀,当c(S2-)= mol/L=10-24.1mol/L时,N2+开始沉淀,则M+先沉淀,当M+沉淀完全时,
0.01
1049.21
溶液中c(S2-)= mol/L=10-39.21mol/L<10-24.1mol/L,此时N2+还没有开始沉淀,所以能通
(105)2
过滴加H S饱和溶液实现分离,故C正确;D.由B项分析可知,
2
K (NS)=c(N2+)•c(S2-)=10-23.11×10-2.99=10-26.1,故D错误;答案选D。
sp
高三化学答案 第 4 页 共 9 页15. (14分,除标注外,每空2分)
(1)①. 四 (1分) ②.VIB (1分)
高温
(2)4FeCr O +8Na CO +7O 2Fe O +8Na CrO +8CO
2 4 2 3 2 2 3 2 4 2
(3)Fe O
2 3
(4)①.2Na++2CrO2-+2CO +H O=Cr O2-+2NaHCO
4 2 2 2 7 3
②.析出的白色晶体碳酸氢钠加热后产生的Na CO 、CO 能循环利用;或CO 来源丰富,廉价
2 3 2 2
易得等合理答案均可
(5)8.37
(6)A
【分析】铬铁矿(FeCr O 含有少量Fe O 和Al O 等杂质)加入碳酸钠灼烧,将FeCr O 转化为
2 4 2 3 2 3 2 4
Na CrO ,“焙烧” 所得固体为Na CrO 、Na[Al(OH)] 和Fe O ,加水浸取,滤渣为难溶性的Fe O ,
2 4 2 4 4 2 3 2 3
滤液中含有可溶性的Na CrO 、Na[Al(OH)] ,加入CO 中和,得到沉淀Al(OH) ,则滤渣为Al(OH) ,
2 4 4 2 3 3
再通入足量CO 2 酸化,CrO 2 4 -转化为Cr 2 O 7 2-,向溶液中加入KCl,得到溶解度较小的K 2 Cr 2 O 7 ,以此解
答。
【小问1详解】Cr是24号元素,位于元素周期表第四周期,第VIB族。
【小问2详解】“煅烧”时FeCr O 和Na CO 、O 反应转化为Na CrO ,同时有Fe O 和CO 生成,根
2 4 2 3 2 2 4 2 3 2
据得失电子守恒和原子守恒配平化学方程式为:
高温
4FeCr O +8Na CO +7O 2Fe O +8Na CrO +8CO 。
2 4 2 3 2 2 3 2 4 2
【小问3详解】由分析可知,“滤渣1”的主要成分为Fe O 。
2 3
【小问4详解】“酸化”过程中CrO 2-转化为Cr O 2-,发生反应的离子方程式为
4 2 7
2Na++2CrO2-+2CO +H O=Cr O2-+2NaHCO ,选择CO 的优点是析出的白色晶体碳酸氢钠加热
4 2 2 2 7 3 2
后产生的Na CO 、CO 能循环利用;或CO 来源丰富,廉价易得。
2 3 2 2
【小问5详解】室温下“中和”: Al(OH) - +H+ Al(OH) +H O,平衡常数
4 3 2
c Al(OH) - c H+ c OH-
K=c Al(OH) - c H+ = 4 =KK =10-13.37, Al(OH) -恰好沉淀完全时,
4 c OH- W 4
10-13.37
溶液中浓度为110-5mol/L,则c(H+)= mol/L=10-8.37mol/L,pH=8.37。
10-5
【小问6详解】用分光光度法测定K Cr O 时,若配制溶液时缺少了某种强酸,以保持溶液的酸性,
2 2 7
会有部分Cr O 2-转化为CrO 2-,则测得Cr O 2-的质量分数会偏低,另外氢碘酸能够和Cr O 2-发生氧化还
2 7 4 2 7 2 7
原反应,导致Cr O 2-的量减小,则少加的试剂为硫酸,故答案选 A。
2 7
高三化学答案 第 5 页 共 9 页16.(15分,除标注外,每空2分)
(1)恒压滴液漏斗 (1分)
(2)①.稀释Cl O,防止发生爆炸(2分)
2
②.将装置中的氯气全部排入装置戊中被吸收,防止污染空气 (2分)
(3)①.V形 (2分) ②. 不能 (2分)
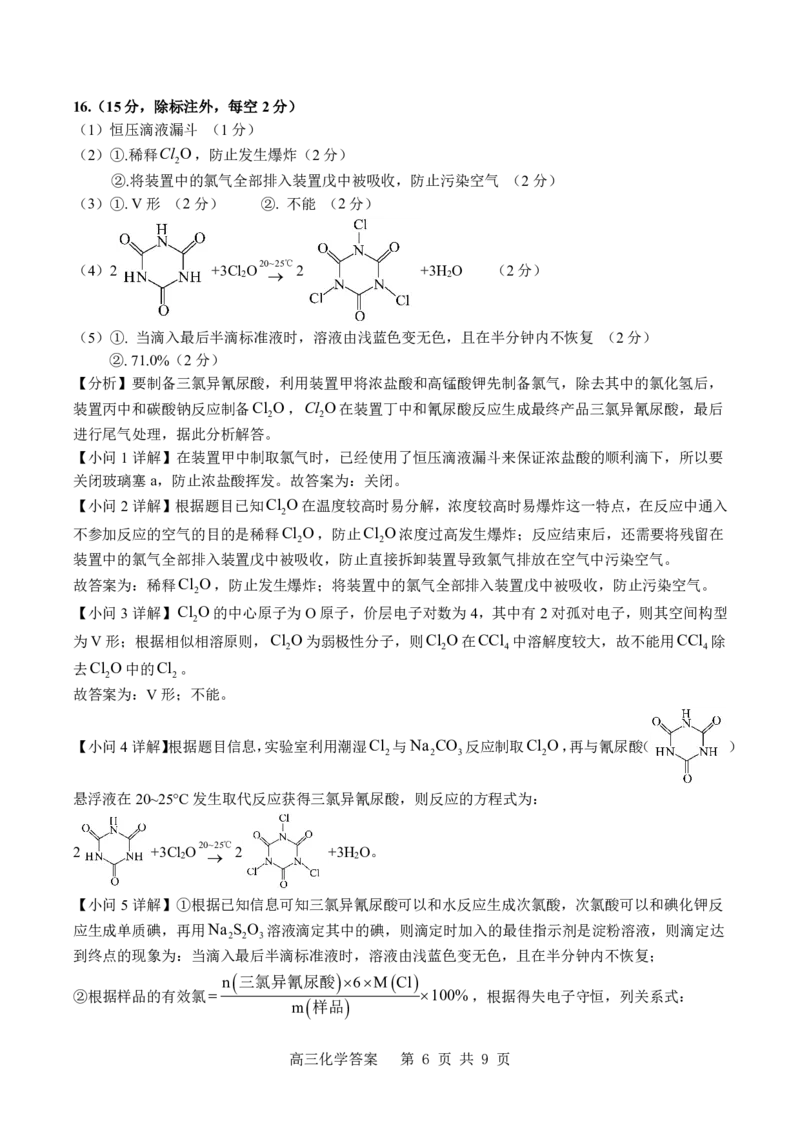
(4)2 +3Cl 2 O 20 ~25℃ 2 +3H 2 O (2分)
(5)①. 当滴入最后半滴标准液时,溶液由浅蓝色变无色,且在半分钟内不恢复 (2分)
②.71.0%(2分)
【分析】要制备三氯异氰尿酸,利用装置甲将浓盐酸和高锰酸钾先制备氯气,除去其中的氯化氢后,
装置丙中和碳酸钠反应制备Cl O,Cl O在装置丁中和氰尿酸反应生成最终产品三氯异氰尿酸,最后
2 2
进行尾气处理,据此分析解答。
【小问1详解】在装置甲中制取氯气时,已经使用了恒压滴液漏斗来保证浓盐酸的顺利滴下,所以要
关闭玻璃塞a,防止浓盐酸挥发。故答案为:关闭。
【小问2详解】根据题目已知Cl O在温度较高时易分解,浓度较高时易爆炸这一特点,在反应中通入
2
不参加反应的空气的目的是稀释Cl O,防止Cl O浓度过高发生爆炸;反应结束后,还需要将残留在
2 2
装置中的氯气全部排入装置戊中被吸收,防止直接拆卸装置导致氯气排放在空气中污染空气。
故答案为:稀释Cl O,防止发生爆炸;将装置中的氯气全部排入装置戊中被吸收,防止污染空气。
2
【小问3详解】Cl O的中心原子为O原子,价层电子对数为4,其中有2对孤对电子,则其空间构型
2
为V形;根据相似相溶原则,Cl O为弱极性分子,则Cl O在CCl 中溶解度较大,故不能用CCl 除
2 2 4 4
去Cl O中的Cl 。
2 2
故答案为:V形;不能。
【小问4详解】根据题目信息,实验室利用潮湿Cl 与Na CO 反应制取Cl O,再与氰尿酸( )
2 2 3 2
悬浮液在20~25°C发生取代反应获得三氯异氰尿酸,则反应的方程式为:
2 +3Cl 2 O 20 ~25℃ 2 +3H 2 O。
【小问5详解】①根据已知信息可知三氯异氰尿酸可以和水反应生成次氯酸,次氯酸可以和碘化钾反
应生成单质碘,再用Na S O 溶液滴定其中的碘,则滴定时加入的最佳指示剂是淀粉溶液,则滴定达
2 2 3
到终点的现象为:当滴入最后半滴标准液时,溶液由浅蓝色变无色,且在半分钟内不恢复;
n
三氯异氰尿酸6M
Cl
②根据样品的有效氯 100%,根据得失电子守恒,列关系式:
m
样品
高三化学答案 第 6 页 共 9 页C N Cl O ~3HClO~3I ~ 6S O2
3 3 3 3 2 2 3
1mol 6mol ,
n 三氯异氰尿酸 0.200mol L120.00 103L
4
解得n 三氯异氰尿酸 103mol,
6
4
103mol635.5gmol1
则样品有效氯 6 。
100% 71.0%
0.2000g
故答案为:当滴入最后半滴标准液时,溶液由浅蓝色变无色,且在半分钟内不恢复;71.0%。
17.(共14分,每空2分)
(1)41
0.5 1
2020
(2)z 20% <
3
4 14
2020
(3)0.0625k
(4)BC
【详解】(1)焓变为生成物与反应物焓值差,根据题干信息,稳定单质的焓(H)为0,结合各物质含可
知,H
111242
kJmol1 394kJmol1 41kJmol1
2
(2)①反应i为放热反应,反应ii为吸热反应,升高温度,反应i逆向移动,反应ii正向移动,二氧
化碳转化率受两个反应影响,温度高于250℃时,以反应ii为主,随温度升高,平衡正向移动,温度
低于250℃时,以反应i为主,随温度升高,平衡逆向移动,所以表示平衡时CO 的转化率的曲线是z;
2
②250℃时,平衡体系共有0.5molCH OH,结合图像可知,选择性S50%,说明此时ΔnCO 1mol,
3 2
1mol
其平衡转化率: 100%20%;
5mol
CO g 3H g CH OH g H O g
2 2 3 2 ,
转化/mol 0.5 1.5 0.5 0.5
CO g H g CO g H O g
2 2 2 ,
转化/mol 0.5 0.5 0.5 0.5
平衡时二氧化碳物质的量:4mol,氢气物质的量:14mol,水物质的量:1mol,一氧化碳物质的量:0.5mol,
0.5 1
2020
甲醇物质的量0.5mol,总物质的量:20mol,则 ;
3
4 14
2020
③根据图像,p点位于曲线y之上,q点位于曲线y之下,则p、q两点反应i的正反应速率大小:
v p<v q;
正 正
p xCOp xH O xCO x H O
(3)K 总 总 2 2 ,
p p xCO p xH xCO x H
总 2 总 2 2 2
高三化学答案 第 7 页 共 9 页xCOxH O
vk 2 molL1h1 xCO xH km ol L1 h1 0.0625kmol L1 h 1;
K 2 2
p
(4)A.二氧化碳加氢制甲醇反应:CO H CH OHH O ,原子利用率小于100%,A错误;B.根
2 2 3 2
据反应历程图可知,带*标记的物质在反应过程中最终被消耗,则表示中间产物,B正确;C.根据反
应历程图可知,第④步的反应式为*H*HOH O,C正确;D.根据反应①可知反应过程中碳氧双
2
键中的π键断裂,D错误。
18. (共15分,除标注外,每空2分)
(1)取代反应
(2)
(3)AC
(4)酸催化会导致酯基水解
(5)
(6)a>c>b
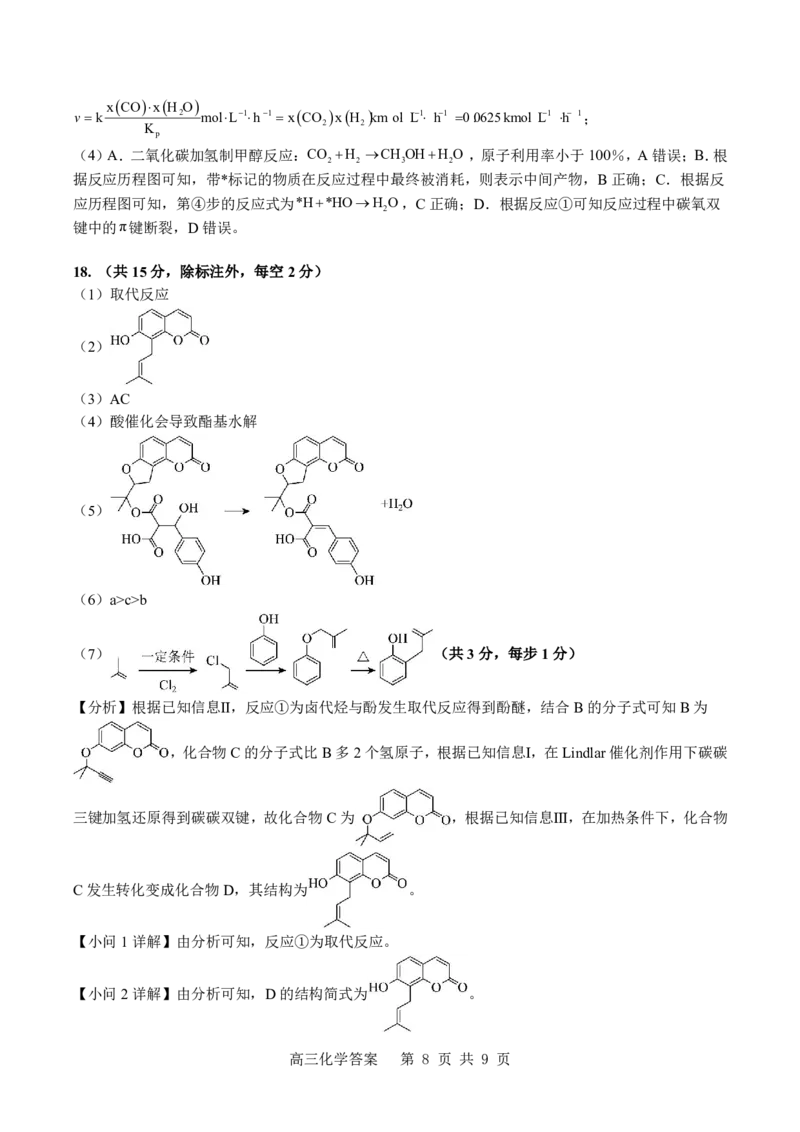
(7) (共3分,每步1分)
【分析】根据已知信息Ⅱ,反应①为卤代烃与酚发生取代反应得到酚醚,结合B的分子式可知B为
,化合物C的分子式比B多2个氢原子,根据已知信息Ⅰ,在Lindlar催化剂作用下碳碳
三键加氢还原得到碳碳双键,故化合物C为 ,根据已知信息Ⅲ,在加热条件下,化合物
C发生转化变成化合物D,其结构为 。
【小问1详解】由分析可知,反应①为取代反应。
【小问2详解】由分析可知,D的结构简式为 。
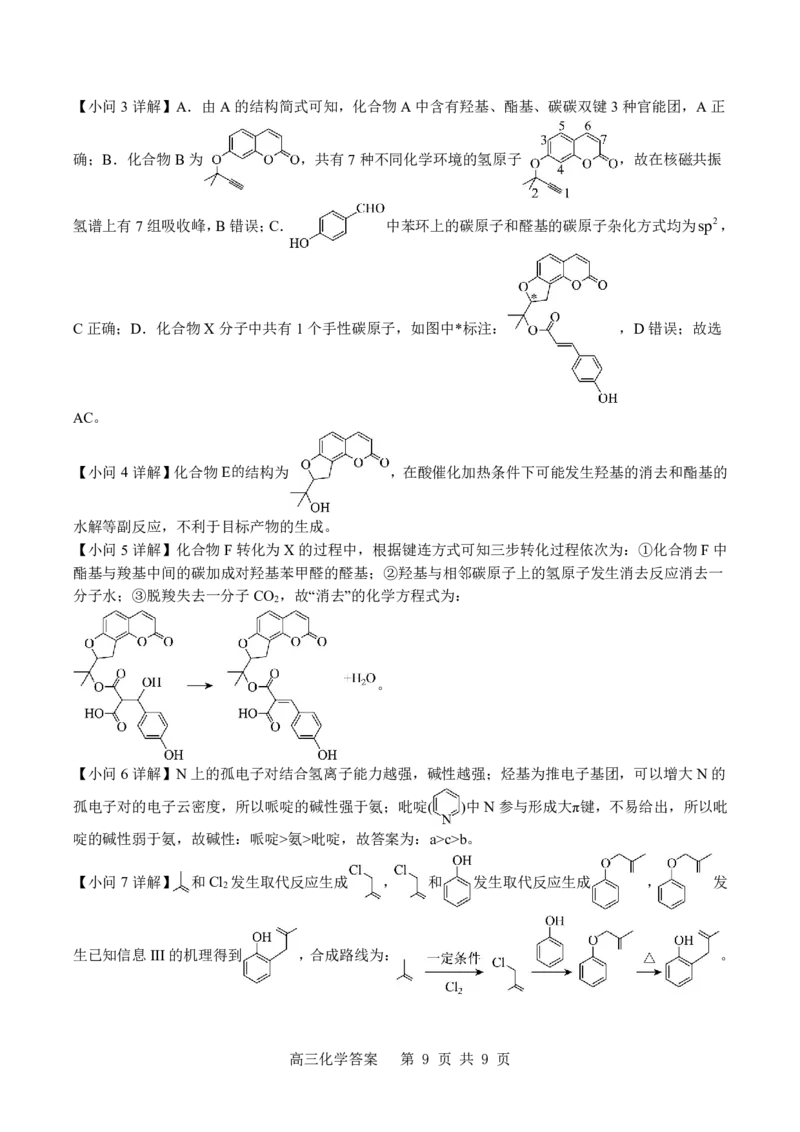
高三化学答案 第 8 页 共 9 页【小问3详解】A.由A的结构简式可知,化合物A中含有羟基、酯基、碳碳双键3种官能团,A正
确;B.化合物B为 ,共有7种不同化学环境的氢原子 ,故在核磁共振
氢谱上有7组吸收峰,B错误;C. 中苯环上的碳原子和醛基的碳原子杂化方式均为sp2,
C正确;D.化合物X分子中共有1个手性碳原子,如图中*标注: ,D错误;故选
AC。
【小问4详解】化合物E的结构为 ,在酸催化加热条件下可能发生羟基的消去和酯基的
水解等副反应,不利于目标产物的生成。
【小问5详解】化合物F转化为X的过程中,根据键连方式可知三步转化过程依次为:①化合物F中
酯基与羧基中间的碳加成对羟基苯甲醛的醛基;②羟基与相邻碳原子上的氢原子发生消去反应消去一
分子水;③脱羧失去一分子CO ,故“消去”的化学方程式为:
2
。
【小问6详解】N上的孤电子对结合氢离子能力越强,碱性越强;烃基为推电子基团,可以增大N的
孤电子对的电子云密度,所以哌啶的碱性强于氨;吡啶( )中N参与形成大π键,不易给出,所以吡
啶的碱性弱于氨,故碱性:哌啶>氨>吡啶,故答案为:a>c>b。
【小问7详解】 和Cl 发生取代反应生成 , 和 发生取代反应生成 , 发
2
生已知信息III的机理得到 ,合成路线为: 。
高三化学答案 第 9 页 共 9 页