文档内容
高三化学自主学习效果评估
可能用到的相对原子质量:H 1 N 14 Ag 108
一、单项选择题:共 13 题,每题 3 分,共 39 分。每题只有一个选项最符合题意。
1.化学知识与科技、生产和生活有密切的关系。下列叙述不正确的是
A.ClO 是一种绿色消毒剂,可用于自来水杀菌消毒
2
B.红酒中添加微量SO ,利用了SO 的氧化性
2 2
C.利用NH HPO 作灭火剂,是因为其分解且吸热,分解产物不支持燃烧
4 2 4
D.利用Na+KCl K↑+NaCl制取K,该反应不能说明Na的金属性强于K
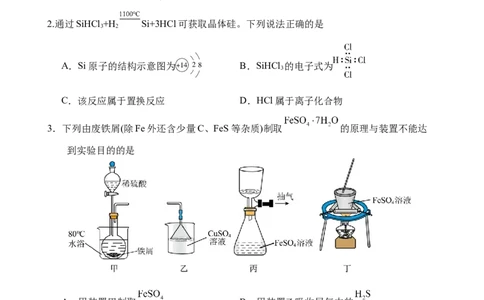
2.通过SiHCl +H Si+3HCl可获取晶体硅。下列说法正确的是
3 2
A.Si原子的结构示意图为 B.SiHCl 的电子式为
3
C.该反应属于置换反应 D.HCl属于离子化合物
3.下列由废铁屑(除Fe外还含少量C、FeS等杂质)制取 的原理与装置不能达
到实验目的的是
A.用装置甲制取 B.用装置乙吸收尾气中的
C.用装置丙过滤得到 溶液 D.用装置丁蒸发结晶获得
4 .元素 C 、N 、O 位于周期表中第二周期。下列说法正确的是
A .原子半径:r(C)<r(N)<r(O) B .酸性:H2CO3<HNO3
C .第一电离能:I(C)<I(N)<I(O) D .沸点:NH3<PH3
阅读下列资料,完成 5~7 题:氯气与碱反应可以得到次氯酸盐、氯酸盐等含氧酸盐,
次氯酸盐应用广泛。通过 KClO溶液在碱性条件下与 Fe(NO3)3溶液反应制备高效水处
试卷第1页,共3页
学科网(北京)股份有限公司理剂 K2FeO4 ,K2FeO4 在强碱性溶液中稳定;通过 KClO溶液在碱性条件下与尿素
[CO(NH2)2]水溶液制备 N2H4,N2H4(l)的标准燃烧热为 642kJ·mol -1 ,具有强还原
性,能与 KClO 剧烈反应生成 N2;通过 KClO溶液与Ag反应可以回收光盘金属层中
的少量 Ag,其反应产物为 AgCl 、KOH 和 O2;通过 KClO 溶液在碱性条件下与
NiSO4反应可制得电极材料 NiO(OH)。
5 .下列说法正确的是
+
A .32g N2H4中含 5mol σ键 B .基态 K 的核外三个电子能层均充满电子
C .ClO3-与 ClO4-的键角相等 D .N2与O2固态时晶体类型均为共价晶体
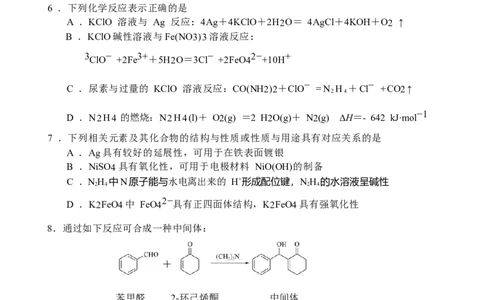
6 .下列化学反应表示正确的是
A .KClO 溶液与 Ag 反应:4Ag+4KClO+2H2O= 4AgCl+4KOH+O2 ↑
B .KClO碱性溶液与Fe(NO3)3溶液反应:
3
ClO
−
+2Fe
3++5H2O=3Cl −
+2FeO4
2−
+10H
+
C .尿素与过量的 KClO 溶液反应:CO(NH2)2+ClO − =N H +Cl − +CO2↑
2 4
D .N2H4 的燃烧:N2H4(l)+ O2(g) =2 H2O(g)+ N2(g) ΔH=- 642 kJ·mol −1
7 .下列相关元素及其化合物的结构与性质或性质与用途具有对应关系的是
A .Ag具有较好的延展性,可用于在铁表面镀银
B .NiSO4具有氧化性,可用于电极材料 NiO(OH)的制备
C .NH 中N原子能与水电离出来的 H+形成配位键,NH 的水溶液呈碱性
2 4 2 4
D .K2FeO4中 FeO4 2−具有正四面体结构,K2FeO4具有强氧化性
8.通过如下反应可合成一种中间体:
苯甲醛 2-环己烯酮 中间体
下列说法正确的是
A .2-环己烯酮中所有的原子可能共平面
B .苯甲醛分子中所有碳原子杂化方式相同
C .可用酸性高锰酸钾溶液鉴别中间体和 2-环己烯酮
D .中间体与足量 H2 加成后所得分子中含有 4 个手性碳原子
9.在给定条件下,下列物质间所示的转化可以实现的是
A.NaCl(aq) Cl(g) B.Cl(g) HClO(aq)
2 2
试卷第2页,共3页
学科网(北京)股份有限公司C.FeI(aq) FeCl (aq) D.NaClO(aq) HClO(aq)
2 3 4 4
10.热电池是一种需要达到一定温度才能工作的电池。一种热电池的结构如下图所示,电池
工作时需用引燃剂引发Fe和 的反应,产生的热量会使LiCl、KCl熔化,电池开始工
作。电池放电后有 、Fe和 生成。下列说法正确的是
A.该热电池常温下不能工作的原因是LiCl、KCl常温下不含离子
B.Fe和KClO 反应后的产物可能是KCl、FeCl 和 O
4 3 2
C.放电时 电极上所发生反应为
D.电路上每转移1mol电子,消耗FeS 的物质的量为0.25mol
2
11 .根据下列实验操作和现象所得到的结论正确的是
选项 实验操作和现象 结论
A
将硫酸酸化的 H2O2 滴入 Fe(NO3)2 溶液中, H
2
O
2
的氧化性强于 Fe3+的氧化
溶液变黄色 性
向 NaCl、NaI 的混合稀溶液中滴入少量稀
B Ksp(AgCl) >Ksp(AgI)
AgNO3 溶液,有黄色沉淀生成
向沸水中逐滴滴加 5~6滴饱和FeCl 溶液, Fe3+先水解得到 Fe(OH) 胶
C 3 3
持续煮沸。溶液先变成红褐色,后析出沉淀 体,后聚集成Fe(OH) 沉淀
3
用电导率传感器分别测定等浓度的醋酸溶液
D
和盐酸的电导率,盐酸的导电性强 HCl 为强电解质
12.草酸亚铁(FeC O)是生产磷酸铁锂电池的原料,实验室可通过如图反应制取:
2 4
已知室温时:K (H C O)=5.6×10−2、K (H C O)=1.5×10−4、K (FeC O)=2.1×10−7。
a1 2 2 4 a2 2 2 4 sp 2 4
下列说法正确的是
A.酸化、溶解后的溶液中存在:2c(Fe2+)+c(H+)<c(NH )+c(OH-)
试卷第3页,共3页
学科网(北京)股份有限公司B.室温下,0.10 mol∙L−1NaHC O 溶液中存在:c(C O )<c(HC O)
2 4 2 2 2 4
C.向稀硫酸酸化的KMnO 溶液中滴加NaC O 溶液至溶液褪色,反应的离子方程式
4 2 2 4
为:5C O +2MnO +8H O=10CO↑+2Mn2++16OH-
2 2 2
D.室温时反应Fe2++H C O=FeC O+2H+的平衡常数K=40
2 2 4 2 4
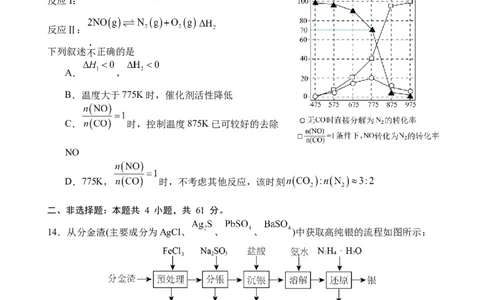
13.飞机在平流层飞行时,尾气中的NO会破坏臭氧层。如何有效消除NO成为环保领域的
重要课题。某研究小组用新型催化剂对CO、NO催化转化进行研究,测得一段时间内NO
的转化率、CO剩余的百分率随温度变化情况如图所示。已知NO可发生下列反应:
反应I:
反应Ⅱ:
下列叙述不正确的是
A. ,
B.温度大于775K时,催化剂活性降低
C. 时,控制温度875K已可较好的去除
NO
D.775K, 时,不考虑其他反应,该时刻
二、非选择题:本题共 4 小题,共 61 分。
14.从分金渣(主要成分为AgCl、 、 、 )中获取高纯银的流程如图所示:
已知:在上述反应的温度下 ,
(1)“预处理”加入 溶液将 转化为AgCl,反应的化学方程式为 ▲ 。
(2)氯化银的晶胞如图, 周围最近且等距离的 数
目为 ▲ 。
试卷第4页,共3页
学科网(北京)股份有限公司(3)已知: , ,“分银”时,AgCl与 反应
生成 ,该反应的平衡常数 ▲ 。
(4)“分银”时, 的浓度与溶液pH的关系如图1; 及其与 形成的微粒的
浓度分数 随溶液pH变化的关系如图2。“分银”时,终点pH需控制的范围及原因为 ▲
。
(5)“还原”时发生反应的离子方程式为 ▲ 。
(6)已如 (白色),测定所制银样品纯度的过程为(杂质不反应):
①称取制备的银样品1.0800g,加适量稀硝酸溶解,定容到100mL容量瓶中。
②准确量取25.00mL溶液于锥形瓶中,酸化后滴入几滴 溶液作指示剂,再用
标准溶液滴定,滴定终点时溶液变为血红色。
③重复②的操作2次,所用 标准溶液的平均体积为24.00mL。
计算样品中银的质量分数(写出计算过程) ▲ 。
15.化合物G是合成氢化橙酮衍生物的中间体,其人工合成路线如下:
试卷第5页,共3页
学科网(北京)股份有限公司注:Bz基团为苯甲酰基,结构式为
(1)A中碳原子和氧原子杂化类型分别为 ▲ 、 ▲ 。
(2)E→F的反应类型为 ▲ 。
(3)C的结构简式为 ▲ 。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式: ▲ 。
①分子中不同化学环境的氢原子数目比为2∶2∶2∶1。
②碱性条件下水解,酸化后得2种产物,其中一种产物分子只含一种含氧官能团,另一种产
物含有2种含氧官能团且能与 发生显色反应
(5) 写出以 和 、 为原料制备
的合成路线流程图 ▲ 。(无机
试剂任用,合成路线示例见本题题干)。
16.硒是人体所需微量元素之一,也是一种重要的工业原料。工业上从铜阳极泥(含有Se、
Au、Ag、Cu、CuSe、 等)中提取硒的过程如下:
(1)“焙烧”时, 与 反应每消耗1mol ,转移电子数为 ▲ 。
试卷第6页,共3页
学科网(北京)股份有限公司(2)甲酸还原 反应的装置如图所示,反应的化学方程
式为 ▲ 。
(3)还原时,进行了下述实验:向10mL 亚硒酸溶
液中先加入10mL氨水,再加入10mL甲酸溶液,加热至沸
腾(103℃),反应10小时。当氨水浓度在 之
间,随着氨水浓度逐渐增大,亚硒酸还原率逐渐升高,其可能的原因是 ▲ 。
(4)粗硒的精制经过 浸出[Se转化成硒代硫酸钠 ] 净化
酸化等步骤。
①加入一定体积 溶液可除去 、 等杂质金属离子, 浓度对粗硒除杂的影响
如图所示,当 的浓度大于2.0g∙L-1时,精硒中的杂质含量上升的原因是 ▲ 。
②在搅拌下向100mL 1mol∙L-1 硒代硫酸钠(Na SeSO )溶液中缓慢滴加1mol∙L-1 溶液,
2 3
过滤、洗涤、干燥,得到Se固体。需加入 溶液的体积约为 ▲ 。
(5)实验室中可以用 还原 溶液制取硒单质,请补充完整实验方案:取一定量
溶液, ▲ ,得硒单质。(须使用的试剂:SO 、BaCl 溶液、1mol∙L-1NaOH溶液)
2 2
17.为了缓解温室效应与能源供应之间的冲突,从空气中捕集CO 并将其转化为燃料或增值
2
化学品成为了新的研究热点。
(1)二氧化碳通过催化方法还原可以生产多种高价值的基础化学品,受到了研究人员的广泛
关注。二氧化碳加氢制甲烷过程中的主要反应为:
;
试卷第7页,共3页
学科网(北京)股份有限公司;
在密闭容器中, 时, 平衡转化率、在催化剂作
用下反应相同时间所测得的 实际转化率随温度的变化如图所示。 的选择性可表示
为 。
①反应 ▲ ;
②580℃以后 平衡转化率升高的主要原因是 ▲ 。
③某同学认为该反应的最佳温度范围为360℃~400℃,你是否赞同,并说明理由: ▲
。
(2)为了进一步研究 的甲烷化反应,科学家
研究催化剂 (M表示Ni或Ru)在300℃光
照的条件下进行反应,催化反应的核心过程如题
图所示:
①步骤Ⅲ发生的反应为 ▲ 。(用“*X”代表
吸附态中间体)
②研究发现,光诱导电子从TiO 转移到M,富
2
电子的M表面可以促进 的解离和 的活
化,从而提高反应效率。已知Ni和Ru的电负性分别为1.91和2.20,使用 催化剂的
试卷第8页,共3页
学科网(北京)股份有限公司反应效率 ▲ (填“高于”或“低于”)使用 作催化剂的反应效率。
(3)用光电化学法将 还原为有机物实现碳资源的再生利用,其装置如图1所示。其他条
件一定时,含碳还原产物的法拉第效率[ ]随电压的
变化如图2所示。
①当电解电压为 ,阴极发生的电极反应式为 ▲ 。
②电解电压为 时,电解生成的HCHO和HCOOH的物质的量之比为 ▲ 。
试卷第9页,共3页
学科网(北京)股份有限公司高三化学自主学习效果评估参考答案
1 2 3 4 5 6 7
B C D B A A C
8 9 10 11 12 13
B A D C D B
14.(15分)
(1) (2分)
(2)12(2分)
(3) (2分)
(4)8~9;pH8~9时 浓度较大,有利于AgCl与 反应生成 (3分)
(5) (2分)
(6)已如Ag++SCN-=AgSCN↓(白色),则n(Ag)=n(SCN-)=24.00×10-3L×0.1000 mol/L×
=9.6×10-3mol,则样品中银的质量分数为 =96.00%。
(4分)
15.(15分)
(1) (2分)
(2)取代反应(2分)
(3) (3分)
(4) (3分)
高三化学 第 3 页(共 8 页)
学科网(北京)股份有限公司(5)(5分)
16.(15分)
(1)6mol(2分)
(2) (2分)
(3)在实验条件下, 比 更容易被甲酸还原,随着氨水浓度逐渐增大,溶液中
浓度逐渐增大,反应速率加快(3分)
(4) ①后续加硫酸时,硫离子与亚硫酸根反应生成硫单质(2分)
②100mL或0.1L(2分)
(5)(4分)在不断搅拌下,向 溶液中缓缓通入 气体至不再产生沉淀为止(1
分),同时用 NaOH溶液吸收多余的尾气(1分),静置,过滤,(1分)洗涤,
直至取最后一次洗涤滤液,加入 溶液无沉淀生成,干燥(1分)
17.(16分)
(1) ① -247.1 (2分)
② 反应Ⅰ为放热反应,温度升高CO 平衡转化率降低;反应Ⅱ为吸热反应,温度升
2
高CO 平衡转化率升高,580℃以后,温度对反应Ⅱ平衡移动的影响大于反应Ⅰ(3分)
2
③不赞同。虽然反应温度为360℃~400℃时CO 转化率较高,但CO 生成CH 的选
2 2 4
择性的大小无法确定(CH 选择性大小无法确定)(3分)
4
(2) ① *COOH→*CO+*OH (2分) ②高于(2分)
(3) ① CO +2e-+2H+=HCOOH (2分) ② 2:1(2分)
2
高三化学 第 3 页(共 8 页)
学科网(北京)股份有限公司