文档内容
2024 年上海市等级考化学试题
一、单选题
1.下列关于氟元素的性质说法正确的是
A.原子半径最小 B.原子第一电离能最大
C.元素的电负性最强 D.最高正化合价为+7
【答案】C
【解析】A.同一周期主族元素从左至右,原子序数递增、原子半径递减,氟原子在本周期主族元素中半径最小,
但氢原子半径小于氟原子半径,A错误;
B.同一周期主族元素从左至右,第一电离能有增大的趋势,氟原子在本周期主族元素中第一电离能最大,但氦原
子的第一电离能大于氟原子,B错误;
C.据同一周期主族元素从左至右电负性增强、同一主族从上至下电负性减弱可知,氟元素的电负性最强,C正确;
D.氟元素无正化合价,D错误;
故选C。
2.下列关于18F与19F说法正确的是
A.是同种核素 B.是同素异形体
C.19F比18F多一个电子 D.19F比18F多一个中子
【答案】D
【解析】A.18F与19F质子数相同、中子数不同,因此两者是不同种核素,A错误;
B.同素异形体指的是同种元素的不同单质;18F与19F是两种不同的原子,不是单质,所以两者不是同素异形体,B
错误;
C.同位素之间质子数和电子数均相同,19F比18F多一个中子,C错误;
D.19F的中子数是10,18F只有9个中子,19F比18F多一个中子,D正确。
故选D。
二、填空题
3.萤石(CaF )与浓硫酸共热可制备HF气体,写出该反应的化学方程式: ,该反应中体现浓硫酸的性质是 。
2
A.强氧化性 B.难挥发性 C.吸水性 D.脱水性
【答案】 CaF +H SO (浓)=CaSO +2HF ↑ BC
2 2 4 ∆ 4
【解析】萤石(CaF )与浓硫酸共热可发生复分解反应,生成硫酸钙和HF气体,该反应的化学方程式为
2
CaF +H SO (浓)=CaSO +2HF ↑,该反应为难挥发性酸制取易挥发性酸,且浓硫酸具有吸水性,可减少HF气体
2 2 4 ∆ 4
在水中的溶解,故该反应中体现浓硫酸的性质是难挥发性和吸水性。AD错误。
故选BC。
4.液态氟化氢(HF)的电离方式为:3HFX+HF
2
,其中X为 。HF
2
的结构为F-HF−,其中F−与HF依靠
相连接。
【答案】 H F 氢键
2
【解析】有原子守恒可知,X为H
2
F。HF
2
的结构为F-HF−,其中F-与HF之间依靠氢键连接。
答案:氢键
三、解答题
5.回答下列问题:(1)氟单质常温下能腐蚀Fe、Ag等金属,但工业上却可用Cu制容器储存,其原因是 。
PtF 是极强的氧化剂,用Xe和PtF 可制备稀有气体离子化合物,六氟合铂氙[XeF]+[ Pt F ]−的制备方式如图所示
6 6 2 11
(2)上述反应中的催化剂为_______。
A.PtF B.PtF− C.F− D.XeF+
6 7
(3)上述过程中属于氧化还原反应的是_______。
A.② B.③ C.④ D.⑤
(4)氟气通入氙(Xe)会产生XeF、XeF、XeF 三种氟化物气体。现将1mol的Xe和9mol的F 同时通入50L的容器中,
2 4 6 2
反应10min后,测得容器内共有8.9mol气体,且三种氟化物的比例为XeF :XeF :XeF =1:6:3,则l0min内XeF 的
2 4 6 4
速率v(XeF )= 。
4
【答案】(1)氟单质与铜制容器表面的铜反应形成一层保护性的氯化铜薄膜,可阻止氟与铜进一步反应
(2)A
(3)AB
(4)0.0004mol⋅L−1⋅min−1
【解析】(1)氟单质常温下能腐蚀Fe、Ag等金属,但工业上却可用Cu制容器储存。类比铝在空气中不易被腐蚀的
原理,可用Cu制容器储存氟单质的原因是氟单质与铜制容器表面的铜反应形成一层保护性的氯化铜薄膜,可阻止
氟与铜进一步反应。
(2)读图可知,PtF 参与了反应过程,但最后又生成了PtF ,因此上述反应中的催化剂为PtF 。
6 6 6
故选A。
(3)看图中信息可知,反应②的化学方程式为PtF−+Xe→PtF−+XeF,反应③的化学方程式为
7 6
PtF−+XeF→PtF +XeF+,这两步反应中Xe和Pt的化合价都发生了变化,因此,上述过程中属于氧化还原反应的
6 6
是②和③;反应④的化学方程式为PtF− →PtF +F−,反应⑤的化学方程式为PtF−+PtF →[Pt F ]−,这两步反应中
6 5 6 5 2 11
元素的化合价没有变化,这两个反应不是氧化还原反应,
故选AB。
(4)氟气通入氙(Xe)会产生XeF、XeF、XeF 三种氟化物气体。现将1mol的Xe和9mol的F 同时通入50L的容器中,
2 4 6 2
反应10min后,测得容器内共有8.9mol气体,且三种氟化物的比例为XeF :XeF :XeF =1:6:3。假设
2 4 6
XeF、XeF、XeF 的物质的量分别为x、6x、3x,则1mol+9mol+10x-10x-x-6x×2-3x×6÷2=8.9mol,解之得
2 4 6
0.05mol×4
x=0.05mol,l0min内XeF 的速率v(XeF )= =0.0004mol⋅L−1⋅min−1。
4 4 50L×10min
6.粗盐中含有SO2−,K+,Ca2+,Mg2+等杂质离子,实验室按下面的流程进行精制:
4已知:KCl和NaCl的溶解度如图所示:
(1)步骤①中BaCl 要稍过量。请描述检验BaCl 是否过量的方法: 。
2 2
(2)若加BaCl 后不先过滤就加氢氧化钠和碳酸钠,会导致_______。
2
A.SO2−不能完全去除 B.消耗更多NaOH
4
C.Ba+不能完全去除 D.消耗更多Na CO
2 3
(3)过滤操作中需要的玻璃仪器。除烧杯和玻璃棒外,还需要_______。
A.分液漏斗 B.漏斗 C.容量瓶 D.蒸发皿
(4)步骤④中用盐酸调节pH至3~4,除去的离子有 。
(5)“一系列操作”是指_______。
A.蒸发至晶膜形成后,趁热过滤 B.蒸发至晶膜形成后,冷却结晶
C.蒸发至大量晶体析出后,趁热过滤 D.蒸发至大量晶体析出后,冷却结晶
(6)请用离子方程式表示加入盐酸后发生的反应 。
另有两种方案选行粗盐提纯。
方案2:向粗盐水中加入石灰乳[主要成分为Ca(OH) ]除去Mg2+,再通入含NH ,CO 的工业废气除去Ca2+;
2 3 2
方案3:向粗盐水中加入石灰乳除去Mg2+,再加入碳酸钠溶液除去Ca2+。
(7)相比于方案3,方案2的优点是 。
(8)已知粗盐水中MgCl 含量为0.38g⋅L−1,CaCl 含量为1.11g⋅L−1,现用方案3提纯10L该粗盐水,求需要加入石灰
2 2
乳(视为CaO)和碳酸钠的物质的量 。
【答案】(1)取少量该步骤所得的上清液于试管中,再滴入几滴稀硫酸溶液,若溶液未变浑浊,表明BaCl 已过量
2
(2)AD
(3)B
(4)OH−、CO2−
3
(5)C
(6)H++OH− =H O、2H++CO2− =H O+CO ↑
2 3 2 2
(7)提纯粗盐的同时,可变废为宝,将含NH 和CO 的工业废气转化为氮肥,同时减少了废气的排放,有利于保护
3 2
环境
(8)0.04mol;0.14mol【分析】粗盐中含有SO2−,K+,Ca2+,Mg2+等杂质离子,加入稍过量的BaCl 溶液,生成BaSO 沉淀,除去SO2−,过
4 2 4 4
滤,滤液中加入稍过量NaOH溶液,生成Mg(OH) 沉淀,除去Mg2+,加入稍过量Na CO 溶液,生成BaCO 和
2 2 3 3
CaCO
3
沉淀,除去Ba2+和Ca2+,过滤,滤液中加入稀盐酸,除去OH−、CO
3
2−,经过一系列操作后得到精盐。
【解析】(1)步骤①中若BaCl 过量,则溶液中存在Ba2+,故判断过量的方法是:取少量该步骤所得的上清液于试
2
管中,再滴入几滴稀硫酸溶液,若溶液未变浑浊,表明BaCl 已过量;
2
(2)相同条件下,因为BaCO 和BaSO 的K 较为接近,若加BaCl 后不先过滤就加氢氧化钠和碳酸钠,可能发
3 4 sp 2
生沉淀的转化:BaSO (s)+CO2−(aq) BaCO (s)+SO2−(aq),使得SO2−不能完全去除,且消耗更多的Na CO 溶
4 3 3 4 4 2 3
液,
故选AD;
(3)过滤操作中需要的玻璃仪器,除烧杯和玻璃棒外,还需要漏斗,
故选B。
(4)步骤④中用盐酸调节pH至3~4,H+能与多余的NaOH和Na
2
CO
3
反应,除去的离子有:OH−、CO
3
2−;
(5)由图可知,KCl的溶解度受温度影响较大,而NaCl的溶解度受温度影响较小,因此先蒸发至大量晶体析出,
此时KCl在滤液中,趁热过滤,可得到精盐。
故选C;
(6)加入盐酸后,H+能与多余的NaOH和Na CO 反应,离子方程式分别为:H++OH− =H O、
2 3 2
2H++CO2− =H O+CO ↑;
3 2 2
(7)方案2加入石灰乳[主要成分为Ca(OH) ]除去Mg2+后,通入含NH ,CO 的离子方程式为:
2 3 2
Ca2+ +2NH +CO +H O=CaCO ↓+2NH+,相比于方案3,方案2的优点是:提纯粗盐的同时,可变废为宝,将
3 2 2 3 4
含NH 和CO 的工业废气转化为氮肥,同时减少了废气的排放,有利于保护环境;
3 2
0.38g
(8)MgCl 含量为0.38g⋅L−1,即 95g/mol ,根据关系式:MgCl Ca(OH) CaO可得,
2 c(MgCl )= =0.004mol/L 2 2
2 1L
提纯10L该粗盐水,需要加入石灰乳(视为CaO)物质的量为0.004mol/L×10L=0.04mol;粗盐水中CaCl 含量为
2
1.11g
1.11g⋅L−1,即 111g/mol ,n
( Ca2+)
=0.01mol/L×10L=0.1mol,加入石灰乳(视为CaO)物质的
c(CaCl )= =0.01mol/L
2 1L
量为0.04mol,即此时溶液中Ca2+总物质的量为:0.1mol+0.04mol=0.14mol,由关系式:Ca2+ CO2−可得,需加入
3
Na CO 的物质的量为0.14mol。
2 3
四、填空题
7.已知AlBr 可二聚为下图的二聚体:
3
(1)该二聚体中存在的化学键类型为_______。
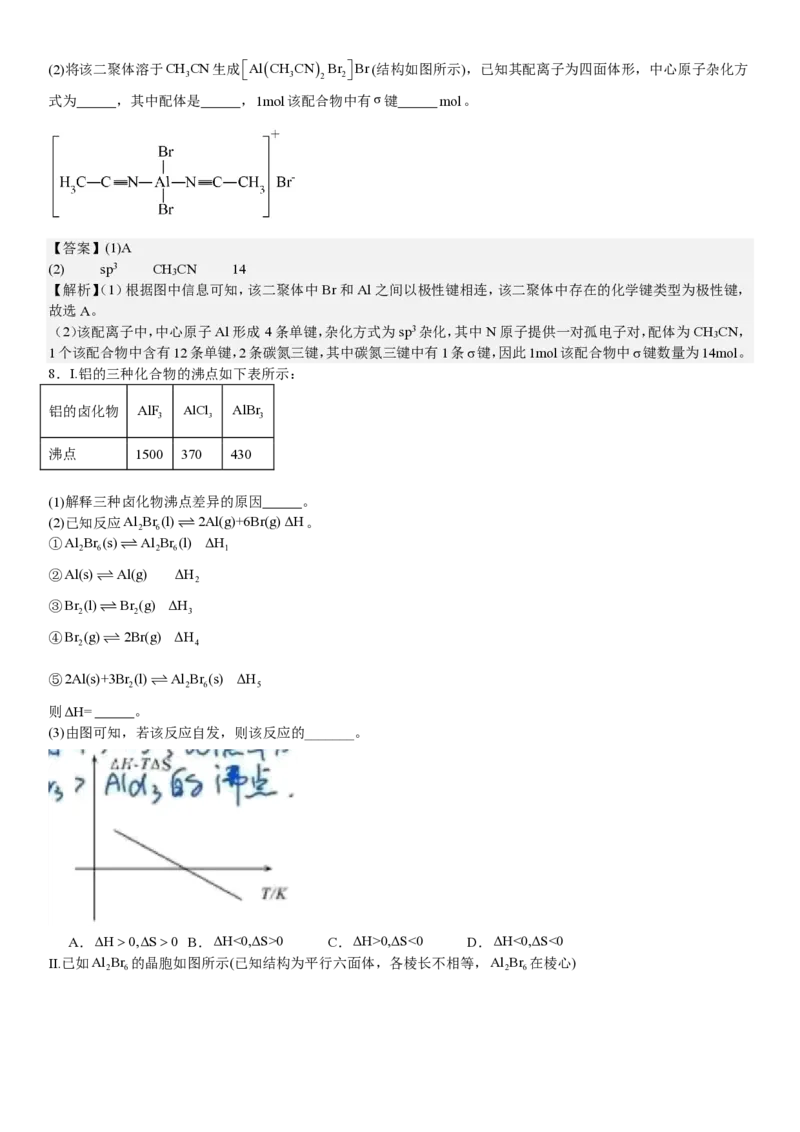
A.极性键 B.非极性键 C.离子键 D.金属键(2)将该二聚体溶于CH
3
CN生成
Al(CH
3
CN)
2
Br
2
Br(结构如图所示),已知其配离子为四面体形,中心原子杂化方
式为 ,其中配体是 ,1mol该配合物中有σ键 mol。
【答案】(1)A
(2) sp3 CH CN 14
3
【解析】(1)根据图中信息可知,该二聚体中Br和Al之间以极性键相连,该二聚体中存在的化学键类型为极性键,
故选A。
(2)该配离子中,中心原子Al形成4条单键,杂化方式为sp3杂化,其中N原子提供一对孤电子对,配体为CH CN,
3
1个该配合物中含有12条单键,2条碳氮三键,其中碳氮三键中有1条σ键,因此1mol该配合物中σ键数量为14mol。
8.I.铝的三种化合物的沸点如下表所示:
铝的卤化物 AlF AlCl AlBr
3 3 3
沸点 1500 370 430
(1)解释三种卤化物沸点差异的原因 。
(2)已知反应Al Br (l)2Al(g)+6Br(g) ΔH。
2 6
①Al Br (s)Al Br (l) ΔH
2 6 2 6 1
②Al(s)Al(g) ΔH
2
③Br (l)Br (g) ΔH
2 2 3
④Br (g)2Br(g) ΔH
2 4
⑤2Al(s)+3Br (l)Al Br (s) ΔH
2 2 6 5
则ΔH= 。
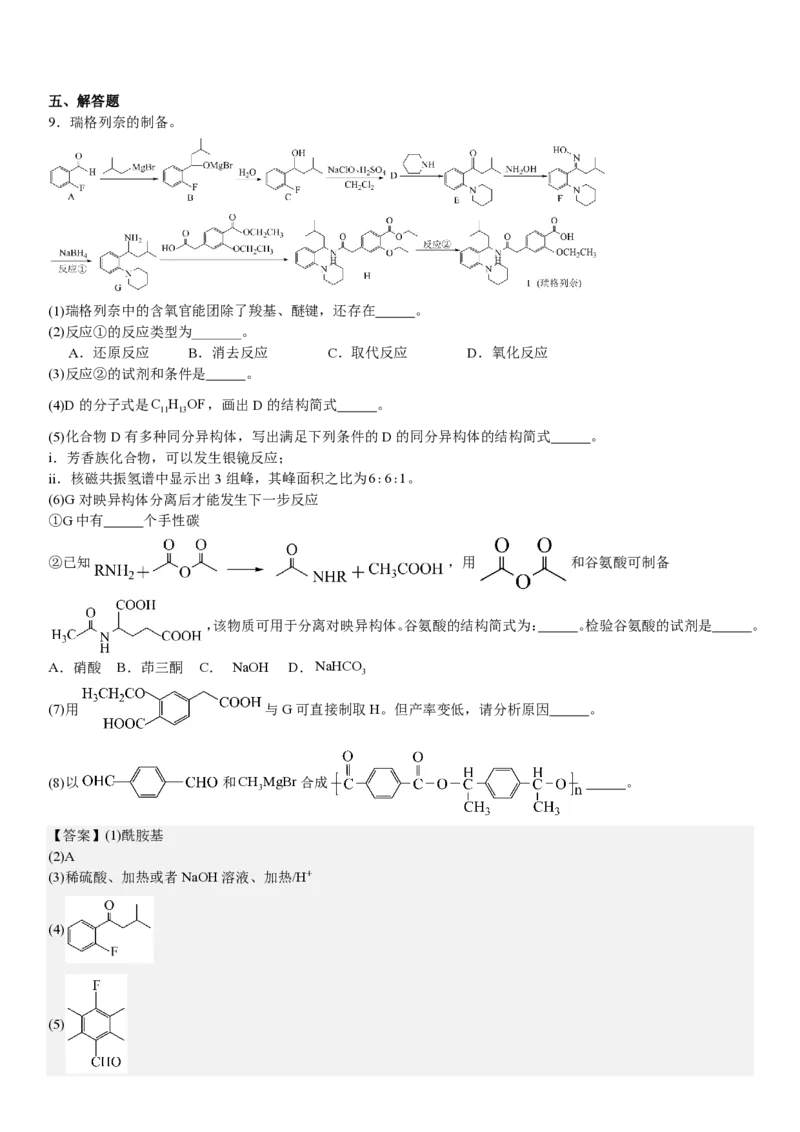
(3)由图可知,若该反应自发,则该反应的_______。
A.∆H>0,∆S>0 B.ΔH<0,ΔS>0 C.ΔH>0,ΔS<0 D.ΔH<0,ΔS<0
II.已如Al Br 的晶胞如图所示(已知结构为平行六面体,各棱长不相等,Al Br 在棱心)
2 6 2 6(4)该晶体中,每个Al Br ,距离其最近的Al Br 有_______个。
2 6 2 6
A.4 B.5 C.8 D.12
(5)已知N =6.02×1023mol-1,一个晶胞的体积C=5.47×10-22cm3。求Al Br 的晶胞密度 。
A 2 6
(6)AlBr 水解可得Al(OH) 胶体,请解释用Al(OH) 可净水的原因 。
3 3 3
(7)用上述制得的胶体做电泳实验时,有某种胶体粒子向阴极移动,该粒子可能是_______。
A.mAl(OH) ⋅nAl3+⋅(3n-x)Br- x+ B.mAl(OH) ⋅nBr-⋅xAl3+ 3x-
3 3
C.mAl(OH) ⋅nOH-⋅(n-x)H+ x- D.mAl(OH) ⋅nAl3+⋅(n-x)Br- x-
3 3
【答案】(1)AlF 为离子晶体,AlCl 和AlBr 为分子晶体,故AlF 的沸点最高;AlBr 的相对分子质量大于AlCl ,
3 3 3 3 3 3
故AlBr 的分子间作用力大于AlCl ,所以AlBr 的沸点高于AlCl 。
3 3 3 3
(2)−∆H +2∆H +3∆H +3∆H −∆H
1 2 3 4 5
(3)A
(4)A
(5)3.24g·cm-3
(6)氢氧化铝胶体粒子有很大的比表面积,具有较好的吸附性,能吸附水中的悬浮颗粒并使其沉降,因而常用于水的
净化
(7)A
【解析】(1)AlF 为离子晶体,AlCl 和AlBr 为分子晶体,故AlF 的沸点最高;AlBr 的相对分子质量大于AlCl ,
3 3 3 3 3 3
故AlBr 的分子间作用力大于AlCl ,所以AlBr 的沸点高于AlCl 。
3 3 3 3
(2)由题中所给的热化学方程式,根据盖斯定律可知,目标热化学方程式可由①×(-1)+②×2+③×3+④×3+⑤×(-1)
得到,故∆H=−∆H +2∆H +3∆H +3∆H −∆H 。
1 2 3 4 5
(3)由∆G=∆H−T∆S可得∆G=−∆ST +∆H,由图像可知,该直线解析式得斜率小于0,纵截距大于0,即−∆S<0,
∆H>0;故结果为∆S>0,∆H>0。
A正确。
(4)选取晶胞中宽上的棱心分子,由于各棱长不相等,与该棱心分子距离最近的分子为该晶胞中相邻两条高中的
棱心分子以及相邻晶胞中两条高中的棱心分子,共有4个。
故选A。
1
(5)根据Al Br 的晶胞图可知,根据均摊法,一个晶胞中Al Br 的个数为8× =2,则一个晶胞的质量为
2 6 2 6
4
2×534
m=
6.02×1023
g,一个晶胞的体积C=5.47×10−22cm3,则Al
2
Br
6
的晶胞密度为
𝑚𝑚 −3
(6)由于氢氧化铝胶体粒子有很大的比表面积,具有较好的吸附性,能吸附水𝐶𝐶中≈的3悬.24浮𝑔𝑔颗·𝑐𝑐粒𝑚𝑚并使其沉降,因而常
用于水的净化。。
(7)某种胶体粒子向阴极移动,说明该粒子带正电。
故选A。五、解答题
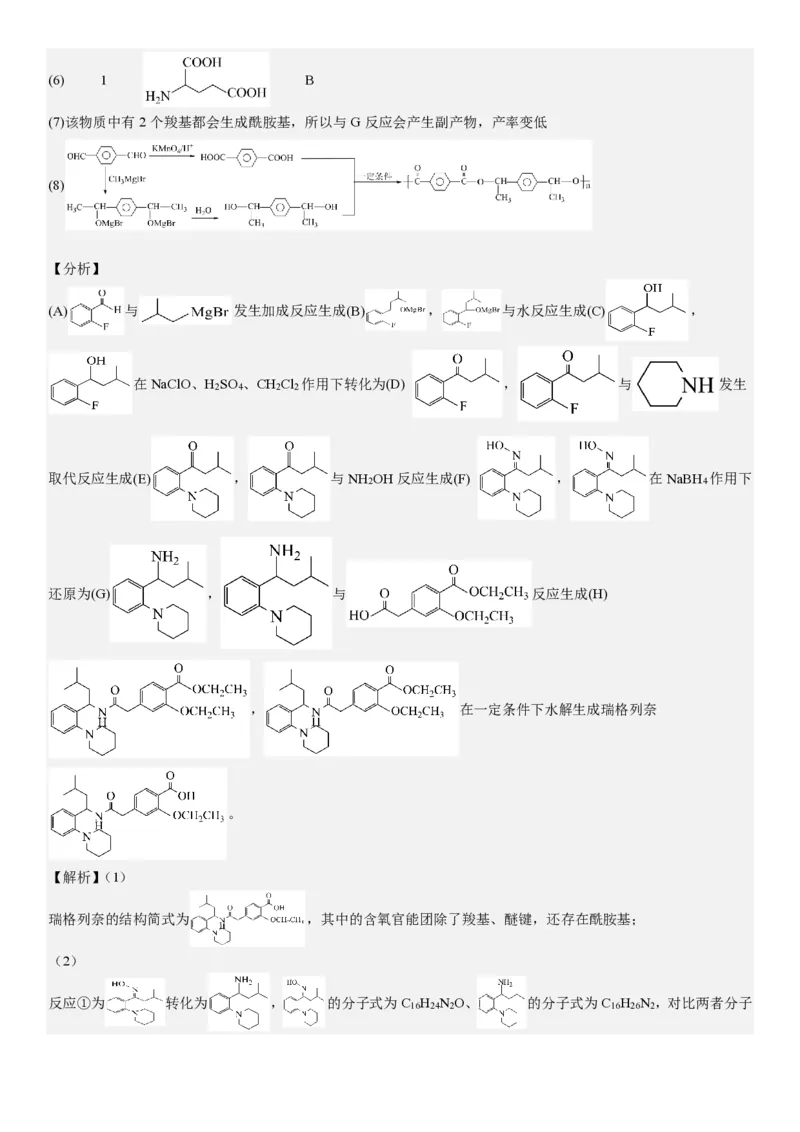
9.瑞格列奈的制备。
(1)瑞格列奈中的含氧官能团除了羧基、醚键,还存在 。
(2)反应①的反应类型为_______。
A.还原反应 B.消去反应 C.取代反应 D.氧化反应
(3)反应②的试剂和条件是 。
(4)D的分子式是C H OF,画出D的结构简式 。
11 13
(5)化合物D有多种同分异构体,写出满足下列条件的D的同分异构体的结构简式 。
i.芳香族化合物,可以发生银镜反应;
ii.核磁共振氢谱中显示出3组峰,其峰面积之比为6:6:1。
(6)G对映异构体分离后才能发生下一步反应
①G中有 个手性碳
②已知 ,用 和谷氨酸可制备
,该物质可用于分离对映异构体。谷氨酸的结构简式为: 。检验谷氨酸的试剂是 。
A.硝酸 B.茚三酮 C. NaOH D.NaHCO
3
(7)用 与G可直接制取H。但产率变低,请分析原因 。
(8)以 和CH MgBr合成 。
3
【答案】(1)酰胺基
(2)A
(3)稀硫酸、加热或者NaOH溶液、加热/H+
(4)
(5)(6) 1 B
(7)该物质中有2个羧基都会生成酰胺基,所以与G反应会产生副产物,产率变低
(8)
【分析】
(A) 与 发生加成反应生成(B) , 与水反应生成(C) ,
在NaClO、H SO 、CH Cl 作用下转化为(D) , 与 发生
2 4 2 2
取代反应生成(E) , 与NH OH反应生成(F) , 在NaBH 作用下
2 4
还原为(G) , 与 反应生成(H)
, 在一定条件下水解生成瑞格列奈
。
【解析】(1)
瑞格列奈的结构简式为 ,其中的含氧官能团除了羧基、醚键,还存在酰胺基;
(2)
反应①为 转化为 , 的分子式为C H N O、 的分子式为C H N ,对比两者分子
16 24 2 16 26 2式可知, 分子中加2个H原子、减1个O原子转化为 ,再对比两者的结构简式可知, 转
化为 时,分子中碳氮双键转化为饱和键,所以该反应类型为还原反应,故答案为:A;
(3)
反应②为 在一定条件下转化为瑞格列奈 ,对比两者的结构简式可知,反应实质
为 分子中的酯基转化为羧基,即为酯基水解,所以反应的试剂和条件是稀硫酸、加热或者NaOH
溶液、加热/H+;
(4)
C的结构简式 、分子式为C H OF,D的分子式为C H OF,对比两者的分子式可知,D比C少2
11 15 11 13
个H,C中官能团为氟原子和羟基,所以C转化为D为羟基的去氢氧化,即羟基转化为酮羰基,所以D的结构简
式 ;
(5)化合物D的结构简式为 、分子式为C H OF,满足条件的同分异构体中有苯环、醛基,且分子对
11 13
称性较强,核磁共振氢谱中显示出3组峰,其峰面积之比为6:6:1,则其结构简式为 ;
(6)①G的结构简式为 ,其中有1个手性碳,为图中标记星号的碳原子: ;
②根据信息 可知,谷氨酸分子中氨基H原子被CH CO-取代后生成
3
,所以谷氨酸的结构简式为 ;谷氨酸的结构简式为 ,即谷氨
酸为α-氨基酸,所以可用茚三酮检验谷氨酸,
答案:B。
(7)G的结构简式为 、H的结构简式为 ,用 与
可直接制取 ,但 分子中有2个羧基,在与 反应
时,2个羧基都会参与反应生成酰胺基,即生成副产物,所以产率变低;(8)以 和CH MgBr合成 时,需由 分别制取
3
和 ,然后 和 在一定条件下发生缩聚反应生成 ,根据题中信
息,合成途径为: 。
10.已知:Ca2++2HCO− CaCO +H CO
3 3 2 3
①HCO− H++CO2−
3 3
②Ca2++CO2− CaCO
3 3
③HCO−+H+ H CO
3 2 3
(1)以下能判断总反应达到平衡状态的是_______。
c
( HCO−)
A.钙离子浓度保持不变 B. 3 保持不变
c
( CO2-)
3
C.v ( Ca2+) =v (CaCO ) D.v (H CO ):v ( HCO−) =2:1
正 逆 3 正 2 3 逆 3
(2)pH增大有利于珊瑚的形成,请解释原因 。
(3)已知H CO 的K =4.2×10-7,K =5.6×10-11,K (CaCO )=2.8×10-9,c(H+)=8.4×10-9mol⋅L-1,
2 3 al a2 sp 3
c ( HCO−) =1×10-4mol⋅L-1,c(H CO )为 。当c ( Ca2+) = mol⋅L-1时,开始产生CaCO 沉淀。
3 2 3 3
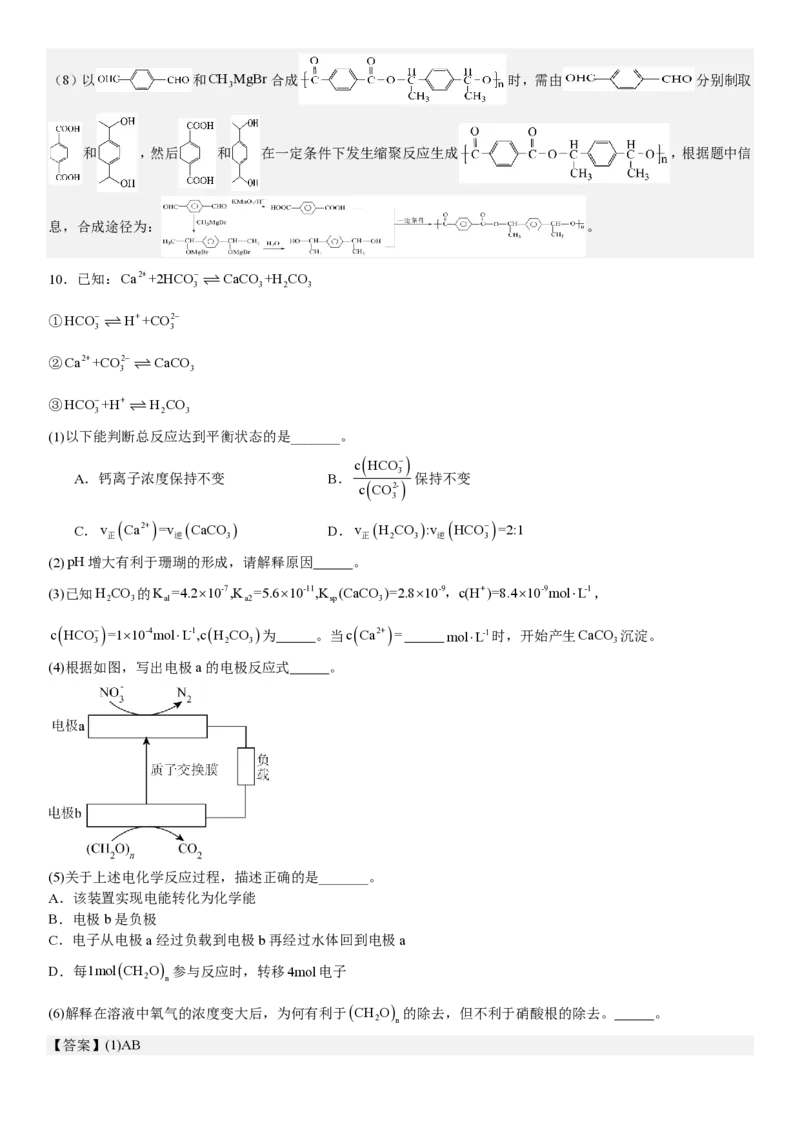
(4)根据如图,写出电极a的电极反应式 。
(5)关于上述电化学反应过程,描述正确的是_______。
A.该装置实现电能转化为化学能
B.电极b是负极
C.电子从电极a经过负载到电极b再经过水体回到电极a
D.每1mol(CH O) 参与反应时,转移4mol电子
2 n
(6)解释在溶液中氧气的浓度变大后,为何有利于(CH O) 的除去,但不利于硝酸根的除去。 。
2 n
【答案】(1)AB(2)pH越大,即c(H+)越小,促进H CO H++HCO−的平衡正向移动,即c ( HCO−) 增大,方程式
2 3 3 3
Ca2++2HCO
3
− CaCO
3
+H
2
CO
3
平衡正向移动,有利于生成CaCO
3
;
(3) 2×10−6mol/L 4.2×10-3
(4)2NO−+10e−+12H+ =N ↑+6H O
3 2 2
(5)B
(6)氧气浓度变大后,O 在正极放电,使得硝酸根的去除率减小,等物质的量的O 得电子的数目大于NO−,使得转
2 2 3
移电子数增大,有机物的去除率增大
【解析】(1)A.钙离子浓度保持不变,说明此时v =v ,反应达到平衡,A正确;
正 逆
c
( H+)
c
( CO2−)
c
( HCO−)
c
( H+)
c
( HCO−)
B.反应①中K= 3 ,即 3 = ,K只与温度有关, 3 保持不变,即c(H+) 保持不变,
c
( HCO−)
c
( CO2-)
K c
( CO2-)
3 3 3
说明此时v =v ,反应达到平衡,B正确;
正 逆
C.CaCO 为固体,其浓度为常数,一般不用固体来表示化学反应速率,C错误;
3
D.不同物质表示正逆反应速率,且之比不等于化学计量数之比,说明正反应速率不等于逆反应速率,反应未达到
平衡状态,D错误;
故选AB;
(2)pH越大,即c(H+)越小,促进H CO H++HCO−的平衡正向移动,即c ( HCO−) 增大,方程式
2 3 3 3
Ca2++2HCO
3
− CaCO
3
+H
2
CO
3
平衡正向移动,有利于生成CaCO
3
;
(3)c(H+)=8.4×10-9mol⋅L-1,c ( HCO−) =1×10-4mol⋅L-1,H CO 的K =
c
( H+)
c
(
HCO
3
−)
=
8.4×10-9×1×10−4
=4.2×10-7,
3 2 3 al c(H CO ) c(H CO )
2 3 2 3
c(H 2 CO 3 )=2×10−6mol/L;K a2 = c ( H c ( + H ) c C ( O C − O ) 3 2−) = 8.4×1 1 0 × - 1 9c 0 ( − C 4 O 3 2−) =5.6×10-11,即c ( CO 3 2−) = 2 3 ×10−6 mol/L
3
K (CaCO )=c ( Ca+) ×c ( CO2−) =c ( Ca+) × 2 ×10−6 =2.8×10-9,c ( Ca+) =4.2×10−3mol/L;
sp 3 3 3
(4)电极a上NO−得到电子变为N ,电极反应式为:2NO−+10e−+12H+ =N ↑+6H O;
3 2 3 2 2
(5)A.看图可知,电极与负载相连接,该装置为原电池,能实现化学能到电能的转化,A错误;
B.电极b上(CH O)失去电子变为CO ,电极b是负极,B正确;
2 2
C.电极a为正极,电极b为负极,电子从电极b经过负载到电极a,电子不会进入水体中,C错误;
D.电极b的电极反应式为:(CH O) −4ne−+nH O=nCO ↑+4nH+,每1mol(CH O) 参与反应时,转移4nmol电
2 n 2 2 2 n
子,D错误;
故选B;
(6)氧气浓度变大后,O 在正极放电,使得硝酸根的去除率减小,等物质的量的O 得电子的数目大于NO−,使
2 2 3
得转移电子数增大,有机物的去除率增大。