文档内容
南昌二中 2025-2026 学年度上学期高三化学月考(一)
命题人:孟哲 审题人:孟哲
可能用到的相对原子质量:
H-1 C-12 N-14 O-16 Na-23 Fe-56 Cl-35.5 Sr-88
一、选择题:本题共 14 小题,每小题 3 分,共 42 分。每小题只有一项符合题目要求。
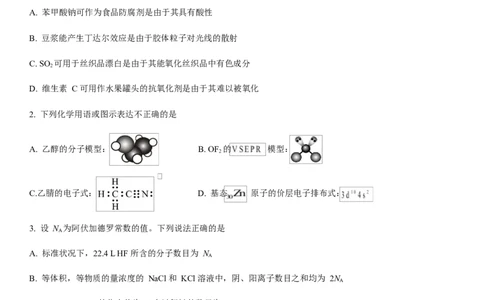
1. 化学与生活密切相关,下列说法正确的是
A. 苯甲酸钠可作为食品防腐剂是由于其具有酸性
B. 豆浆能产生丁达尔效应是由于胶体粒子对光线的散射
C. SO 可用于丝织品漂白是由于其能氧化丝织品中有色成分
2
D. 维生素 C 可用作水果罐头的抗氧化剂是由于其难以被氧化
2. 下列化学用语或图示表达不正确的是
A. 乙醇的分子模型: B. OF 的 模型:
2
C.乙腈的电子式: D. 基态 原子的价层电子排布式:
3. 设 N 为阿伏加德罗常数的值。下列说法正确的是
A
A. 标准状况下,22.4 L HF 所含的分子数目为 N
A
B. 等体积,等物质的量浓度的 NaCl 和 KCl 溶液中,阴、阳离子数目之和均为 2N
A
C. 1 mol CrO (Cr 的化合价为+6)含过氧键的数目为 2N
5 A
D. 标准状况下,11.2 L NH 溶于水溶液中 、 的微粒数之和
3
4.下列关于实验事故或药品的处埋方法中不正确的是
A.制备金属镁的电解装置失火时,不可以使用二氧化碳灭火器灭火
B.不慎将金属汞洒落桌面,必须尽可能收集,并深埋处理
1C.“84”消毒液和“洁厕灵”不能混合使用
D.做“钾与水的反应”实验时,需要佩戴护目镜
5. 下列有关反应的离子方程式正确的是
A. 溶液中加入过量氨水:
B. 向 溶液中通入少量 :
C. 用 溶液除去乙炔中的
D. 碳酸氢镁与足量的 NaOH 溶液反应:Mg2++2HCO 3−+2OH-===MgCO
3
↓+CO 32−+2H
2
O
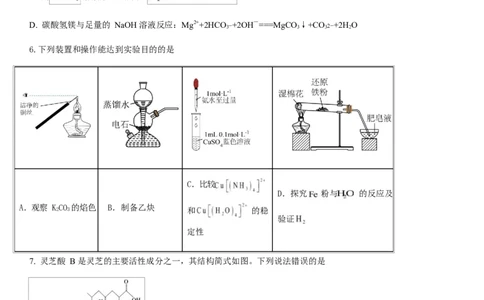
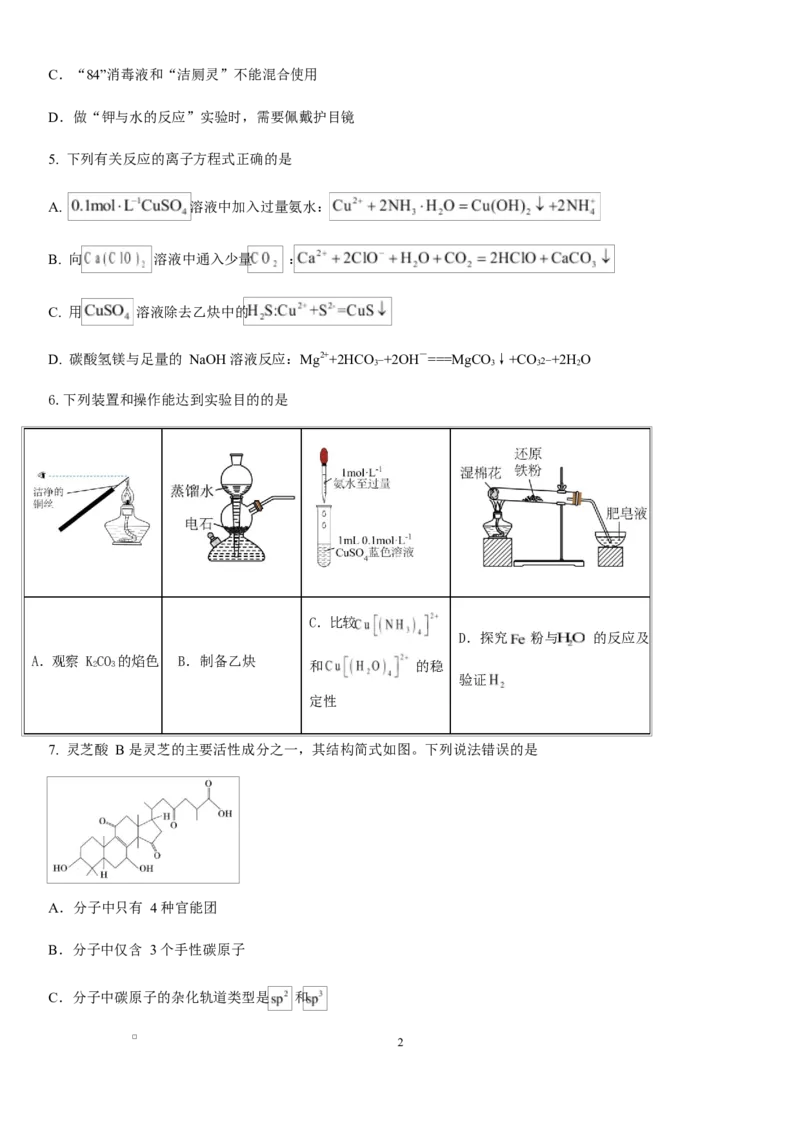
6.下列装置和操作能达到实验目的的是
C.比较
D.探究 粉与 的反应及
A.观察 KCO 的焰色 B.制备乙炔
2 3 和 的稳
验证
定性
7. 灵芝酸 B 是灵芝的主要活性成分之一,其结构简式如图。下列说法错误的是
A.分子中只有 4 种官能团
B.分子中仅含 3 个手性碳原子
C.分子中碳原子的杂化轨道类型是 和
2D.1 mol 该物质与 Na、NaOH、NaHCO 反应的物质的量之比为 3:1:1
3
8. 依据下列事实进行的推测正确的是
事实 推测
A 固体与浓硫酸反应可制备 气体 固体与浓硫酸反应可制备 HI 气体
B 难溶于盐酸,可作“钡餐”使用 可代替 作“钡餐”
C 电解熔融氯化钠可得到钠 电解熔融氯化铝可得到铝
D 的沸点高于 的沸点高于
9.我国科学家最近研究的一种无机盐 纳米药物具有高效的细胞内亚铁离子捕获和抗氧化能力。W、X、
Y、Z 的原子序数依次增加,且 W、X、Y 属于不同族的短周期元素。W 的外层电子数是其内层电子数的 2 倍,X
和 Y 的第一电离能都比左右相邻元素的高。Z 的 M 层未成对电子数为 4。下列叙述错误的是
A.W、X、Y、Z 四种元素的单质中 Z 的熔点最高
B.在 X 的简单氢化物中 X 原子轨道杂化类型为
C.Y 的氢氧化物难溶于 NaCl 溶液,可以溶于 溶液
D. 中 提供电子对与 形成配位键
10.低品位热(温度低于 150℃ )是一种丰富且广泛存在的可持续能源,一种新型的 37℃ 热富集铂电极电池如图
所示。利用从热区至冷区的 pH 梯度驱动对苯醌和对苯二酚的转换: 。下列说法错误的是
3A.左侧电极为冷端电极
B.工作中热端电极的电极反应式为 -2e -= + 2H+
C.工作中无需补充对苯醌或对苯二酚
D.该电池可反复充放电使用
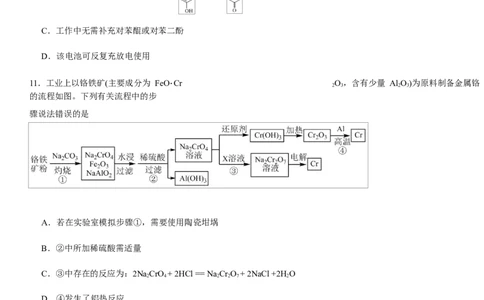
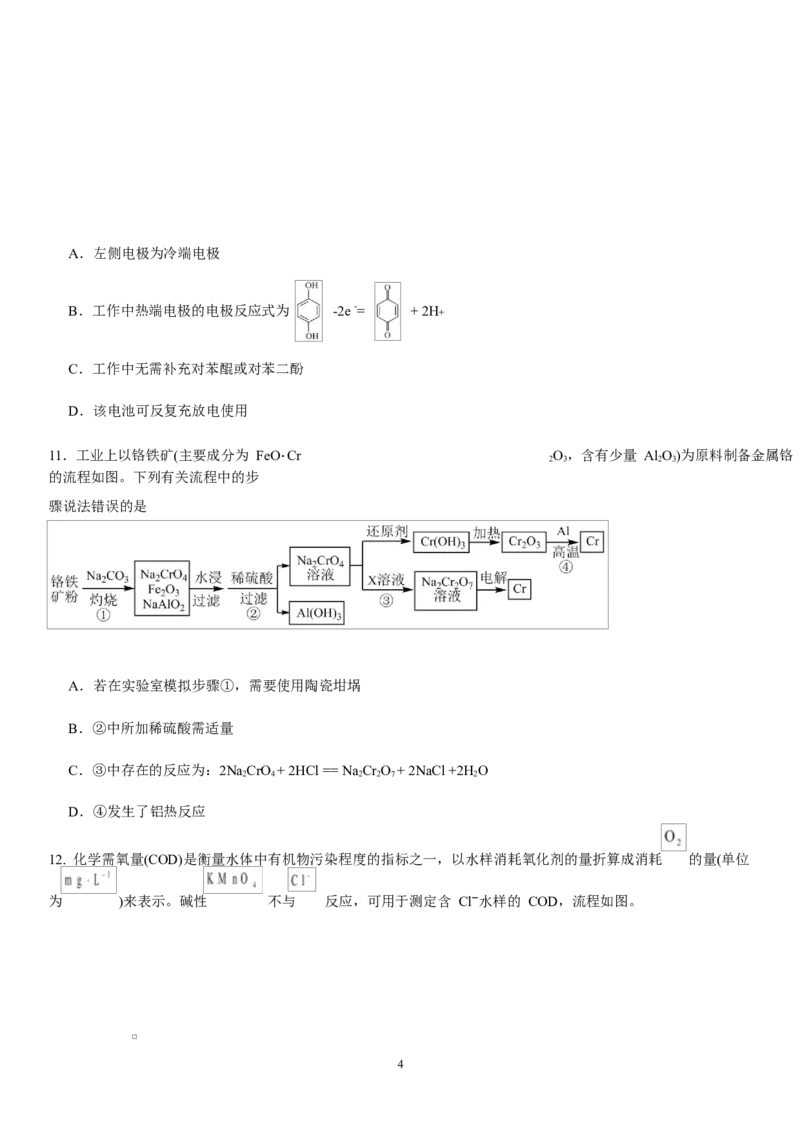
11.工业上以铬铁矿(主要成分为 FeO⋅Cr
2
O
3
,含有少量 Al
2
O
3
)为原料制备金属铬
的流程如图。下列有关流程中的步
骤说法错误的是
A.若在实验室模拟步骤①,需要使用陶瓷坩埚
B.②中所加稀硫酸需适量
C.③中存在的反应为:2NaCrO + 2HCl == Na Cr O + 2NaCl +2HO
2 4 2 2 7 2
D.④发生了铝热反应
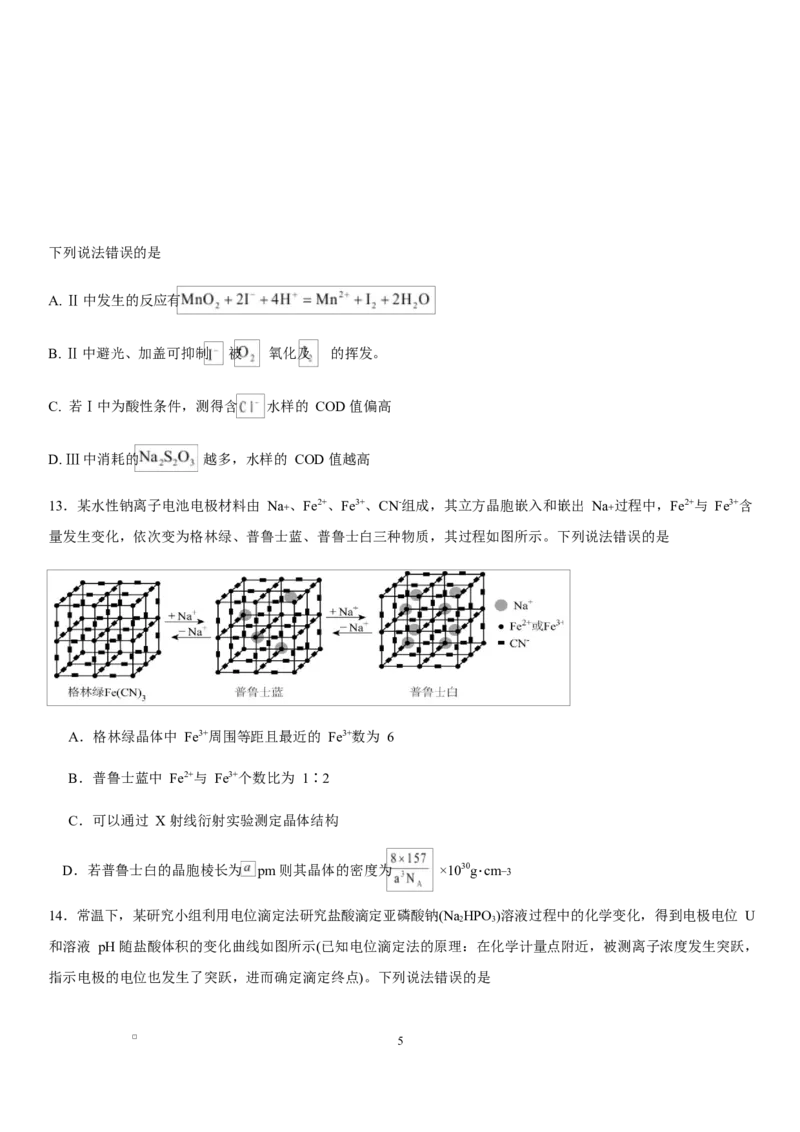
12. 化学需氧量(COD)是衡量水体中有机物污染程度的指标之一,以水样消耗氧化剂的量折算成消耗 的量(单位
为 )来表示。碱性 不与 反应,可用于测定含 Cl⁻水样的 COD,流程如图。
4下列说法错误的是
A. Ⅱ中发生的反应有
B. Ⅱ中避光、加盖可抑制 被 氧化及 的挥发。
C. 若Ⅰ中为酸性条件,测得含 水样的 COD 值偏高
D. Ⅲ中消耗的 越多,水样的 COD 值越高
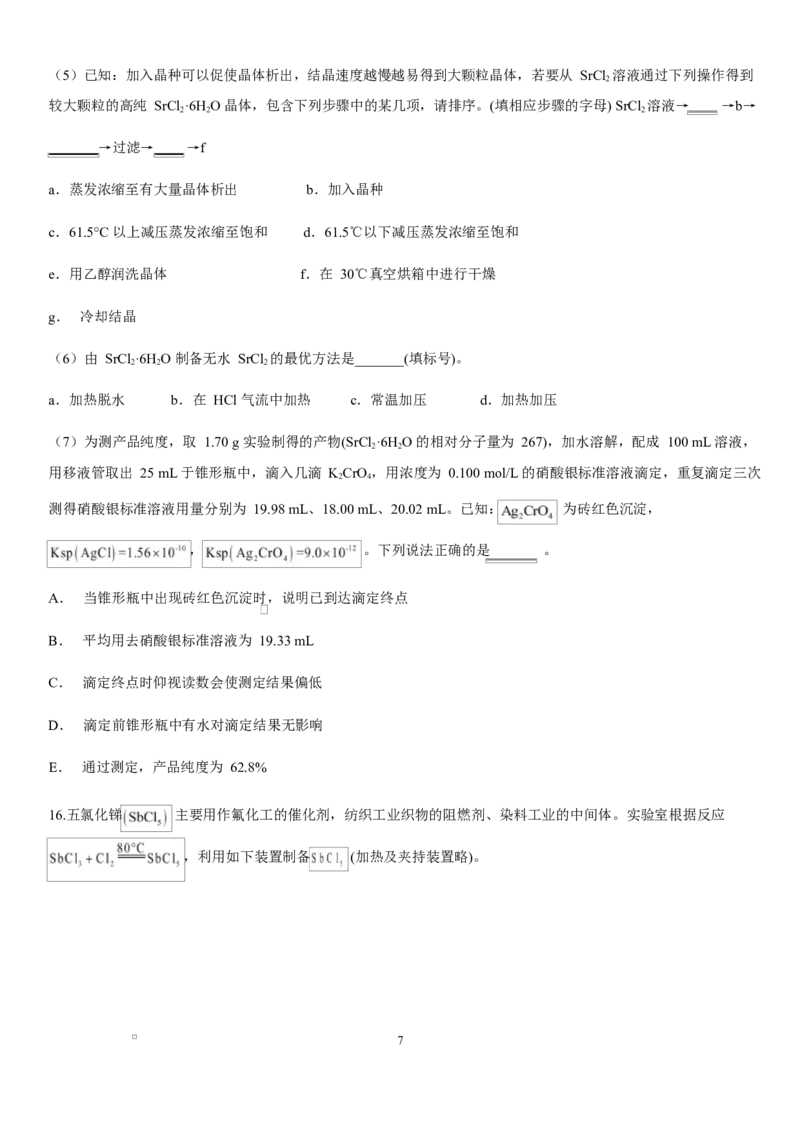
13.某水性钠离子电池电极材料由 Na+ 、Fe2+、Fe3+、CN-组成,其立方晶胞嵌入和嵌出 Na+ 过程中,Fe2+与 Fe3+含
量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。下列说法错误的是
A.格林绿晶体中 Fe3+周围等距且最近的 Fe3+数为 6
B.普鲁士蓝中 Fe2+与 Fe3+个数比为 1∶2
C.可以通过 X 射线衍射实验测定晶体结构
D.若普鲁士白的晶胞棱长为 pm 则其晶体的密度为 ×1030g⋅cm−3
14.常温下,某研究小组利用电位滴定法研究盐酸滴定亚磷酸钠(Na HPO )溶液过程中的化学变化,得到电极电位 U
2 3
和溶液 pH 随盐酸体积的变化曲线如图所示(已知电位滴定法的原理:在化学计量点附近,被测离子浓度发生突跃,
指示电极的电位也发生了突跃,进而确定滴定终点)。下列说法错误的是
5A.亚磷酸(H
3
PO
3
)为二元弱酸 ,a 到 b 过程的反应方程式: H+ + HPO == H
2
PO
B.常温下,HPO 的 K 近似为 10-6.7
3 3 a2
C.c 点由水电离出的 c(H+)>10-7mol•L-1
D.d 点对应的溶液中存在:c(Cl-)=2c(H PO )+2c(H PO )+2c(HPO )
3 3 2
二、非选择题:本题共 4 小题,共 58 分。
15. 某含锶( )废渣主要含有 和 等,一种提取该废渣中锶 流程如下图
所示。
已知:① 时,
②SrCl ·6H O 在 61.5°C 以上即会失去结晶水生成二水氯化锶结晶。
2 2
回答下列问题:
(1)锶位于元素周期表第五周期第ⅡA 族。基态原子价电子排布式 _______。
(2)“浸出液”中主要的金属离子有 Sr2+、_______(填离子符号)。
(3)“盐浸”中 SrSO 转化反应的离子方程式为_______; 时,向 0.01molSrSO 粉末中加入 100ml0.11 mol·
4 4
L-1BaCl 溶液,充分反应后,理论上溶液中 c(Sr2+)·c(SO 2-)= _______ (忽略溶液体积的变化)。
2 4
(4)“浸出渣 2”中主要含有 SrSO、_______(填化学式)。
4
6(5)已知:加入晶种可以促使晶体析出,结晶速度越慢越易得到大颗粒晶体,若要从 SrCl 溶液通过下列操作得到
2
较大颗粒的高纯 SrCl ·6H O 晶体,包含下列步骤中的某几项,请排序。(填相应步骤的字母) SrCl 溶液→ →b→
2 2 2
→过滤→ →f
a.蒸发浓缩至有大量晶体析出 b.加入晶种
c.61.5°C 以上减压蒸发浓缩至饱和 d.61.5℃以下减压蒸发浓缩至饱和
e.用乙醇润洗晶体 f.在 30℃真空烘箱中进行干燥
g. 冷却结晶
(6)由 SrCl ·6H O 制备无水 SrCl 的最优方法是_______(填标号)。
2 2 2
a.加热脱水 b.在 HCl 气流中加热 c.常温加压 d.加热加压
(7)为测产品纯度,取 1.70 g 实验制得的产物(SrCl ·6H O 的相对分子量为 267),加水溶解,配成 100 mL 溶液,
2 2
用移液管取出 25 mL 于锥形瓶中,滴入几滴 KCrO,用浓度为 0.100 mol/L 的硝酸银标准溶液滴定,重复滴定三次
2 4
测得硝酸银标准溶液用量分别为 19.98 mL、18.00 mL、20.02 mL。已知: 为砖红色沉淀,
, 。下列说法正确的是 。
A. 当锥形瓶中出现砖红色沉淀时,说明已到达滴定终点
B. 平均用去硝酸银标准溶液为 19.33 mL
C. 滴定终点时仰视读数会使测定结果偏低
D. 滴定前锥形瓶中有水对滴定结果无影响
E. 通过测定,产品纯度为 62.8%
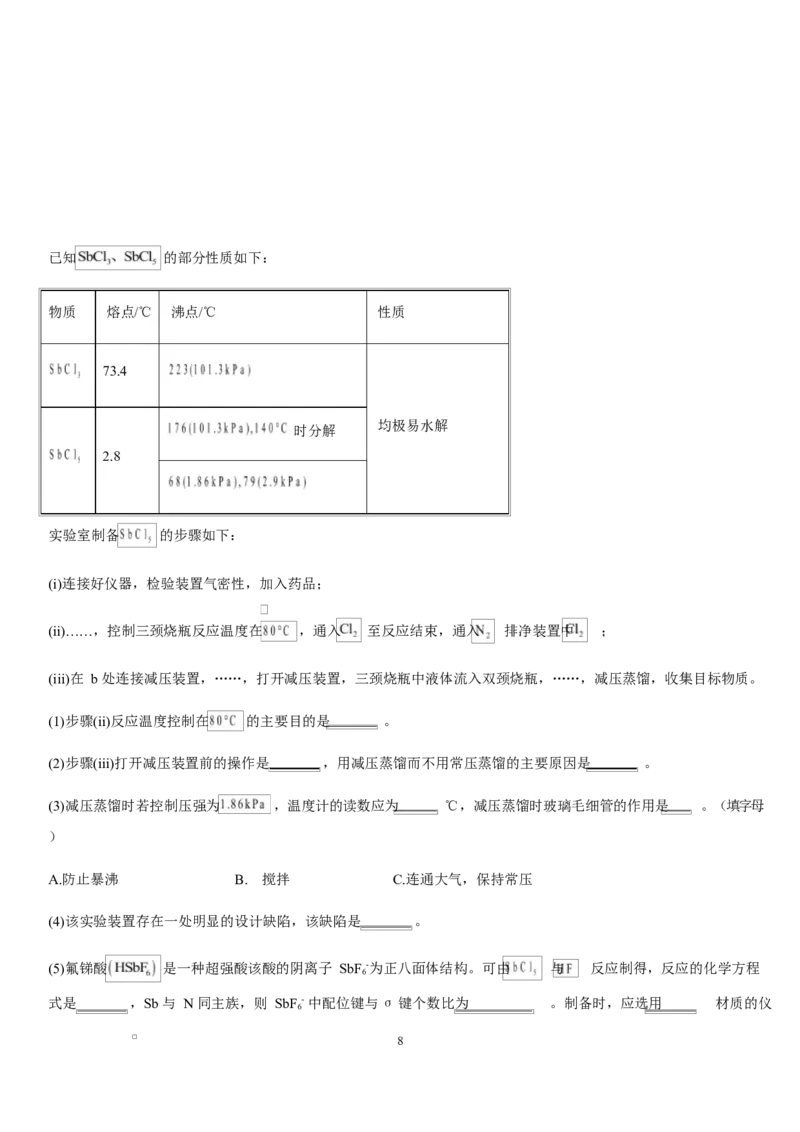
16.五氯化锑 主要用作氟化工的催化剂,纺织工业织物的阻燃剂、染料工业的中间体。实验室根据反应
,利用如下装置制备 (加热及夹持装置略)。
7已知 的部分性质如下:
物质 熔点/℃ 沸点/℃ 性质
73.4
均极易水解
时分解
2.8
实验室制备 的步骤如下:
(i)连接好仪器,检验装置气密性,加入药品;
(ii)……,控制三颈烧瓶反应温度在 ,通入 至反应结束,通入 排净装置中 ;
(iii)在 b 处连接减压装置,……,打开减压装置,三颈烧瓶中液体流入双颈烧瓶,……,减压蒸馏,收集目标物质。
(1)步骤(ii)反应温度控制在 的主要目的是 。
(2)步骤(iii)打开减压装置前的操作是 ,用减压蒸馏而不用常压蒸馏的主要原因是 。
(3)减压蒸馏时若控制压强为 ,温度计的读数应为 ℃,减压蒸馏时玻璃毛细管的作用是 。(填字母
)
A.防止暴沸 B. 搅拌 C.连通大气,保持常压
(4)该实验装置存在一处明显的设计缺陷,该缺陷是 。
(5)氟锑酸 是一种超强酸该酸的阴离子 SbF -为正八面体结构。可由 与 反应制得,反应的化学方程
6
式是 ,Sb 与 N 同主族,则 SbF - 中配位键与σ键个数比为 。制备时,应选用 材质的仪
6
8器(填标号)。
A.玻璃 B.陶瓷 C.铁或铝 D.聚四氟乙烯
17. 随着温室效应越来越严重,降低空气中二氧化碳含量成为研究热点,回答下列问题。
将二氧化碳转化为甲醇是目前重要的碳中和方法,体系中发生如下反应:
反应Ⅰ:
反应Ⅱ:
反应Ⅲ:
(1) ,反应Ⅲ自发进行的条件是 填(“高温”、“低温”或“任何温度”)。
(2)某条件下只发生反应Ⅱ,改变 的平衡转化率的措施有___________。
A.温度 B.压强 C.催化剂 D.投料比
(3)某温度下,1L 恒容密闭容器中加入 1molCO (g)和 3molH (g),发生反应①和反应②,平衡时 CO 的转化率为α,
2 2 2
CO(g)的物质的量为 bmol,计算反应①的平衡常数 K= (用含有α、b 的计算式表示)。
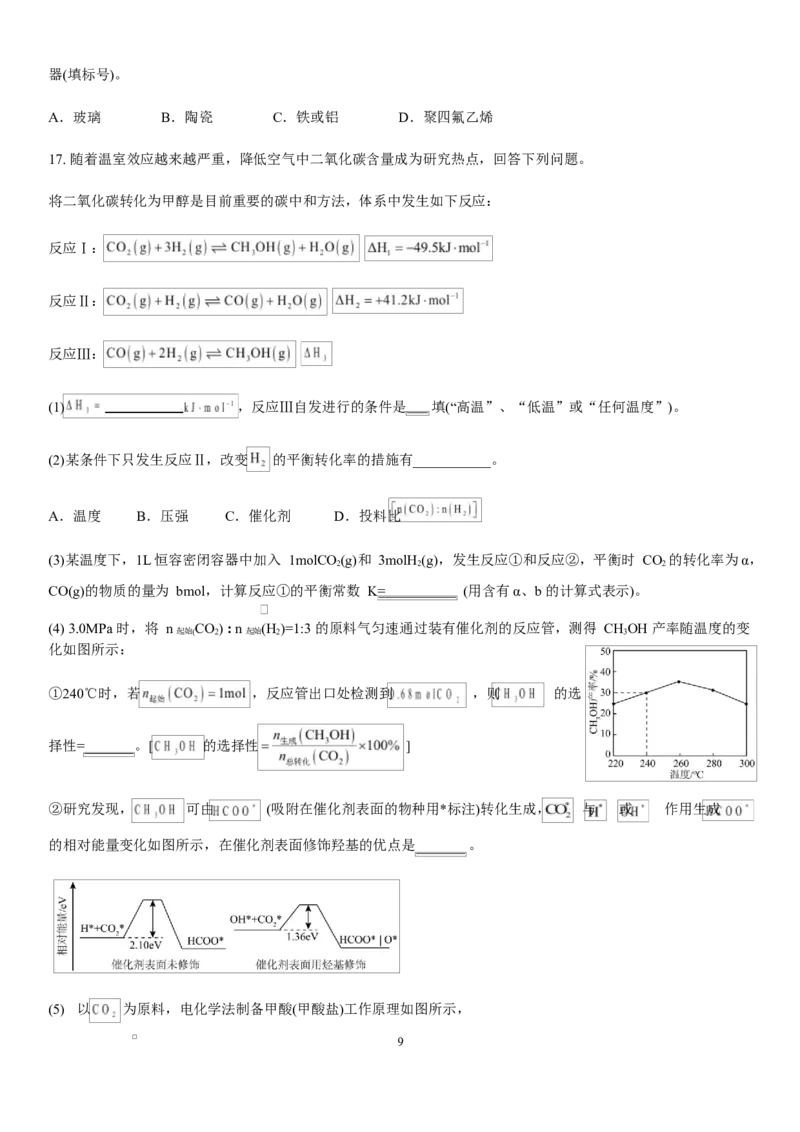
(4) 3.0MPa 时,将 n CO) : n (H )=1:3 的原料气匀速通过装有催化剂的反应管,测得 CHOH 产率随温度的变
起始( 2 起始 2 3
化如图所示:
①240℃时,若 ,反应管出口处检测到 ,则 的选
择性= 。[ 的选择性 ]
②研究发现, 可由 (吸附在催化剂表面的物种用*标注)转化生成, 与 或 作用生成
的相对能量变化如图所示,在催化剂表面修饰羟基的优点是 。
(5) 以 为原料,电化学法制备甲酸(甲酸盐)工作原理如图所示,
9①HCOO-的空间构型为 。
②阴极表面发生的总电极反应式为 。
(6) 甲醇与金属钠反应生成甲醇钠,已知甲醇钠的碱性强于氢氧化钠,请从结构角度解释原因: 。
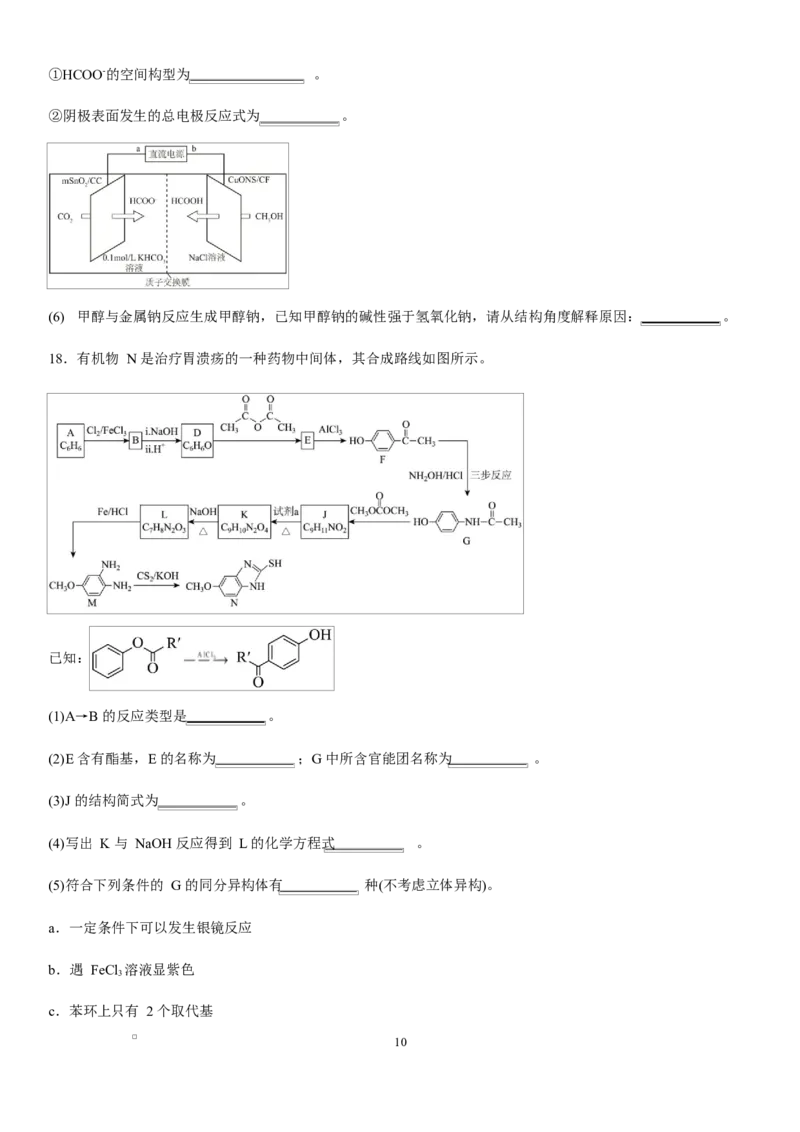
18.有机物 N 是治疗胃溃疡的一种药物中间体,其合成路线如图所示。
已知:
(1)A→B 的反应类型是 。
(2)E 含有酯基,E 的名称为 ;G 中所含官能团名称为 。
(3)J 的结构简式为 。
(4)写出 K 与 NaOH 反应得到 L 的化学方程式 。
(5)符合下列条件的 G 的同分异构体有 种(不考虑立体异构)。
a.一定条件下可以发生银镜反应
b.遇 FeCl 溶液显紫色
3
c.苯环上只有 2 个取代基
10(6)F 与 NH OH 反应生成 G 的过程如图。
2
已知:ⅰ.发生加成反应时, 断开 键
ⅱ.同一个碳上连着一个羟基和一个氨基 或取代的氨基 时不稳定,易脱水生成亚胺 ,写出 Q
的结构简式: 。
参考答案
1-5 B B C B B 6-10 C B D A D 11-14 A D B C
15. (15 分)
(1) (1 分) (2) 、
(3)① ②
(4) 、 (5) d g e (6) a (7) ADE
16. (15 分)
(1) 增大接触面积,提高 与氯气的反应速率
(2) 关闭活塞 1、打开活塞 2 防止 SbCl 分解(1 分)
5
(3) 68 (1 分) AB
(4)球形冷凝管上方缺少盛有碱石灰的干燥装置
(5) SbCl + 6HF = HSbF + 5HCl 1:5 D(1 分)
5 6
17.(15 分)
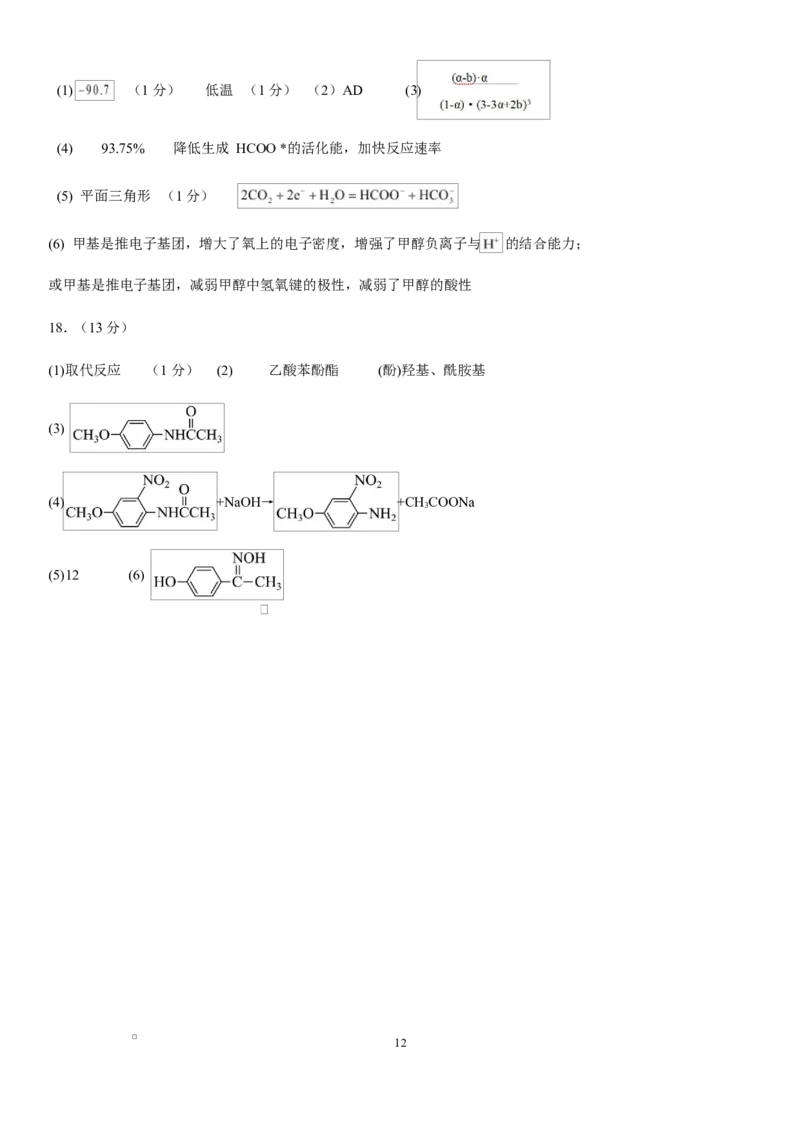
11(1) (1 分) 低温 (1 分) (2)AD (3)
(4) 93.75% 降低生成 HCOO *的活化能,加快反应速率
(5) 平面三角形 (1 分)
(6) 甲基是推电子基团,增大了氧上的电子密度,增强了甲醇负离子与 的结合能力;
或甲基是推电子基团,减弱甲醇中氢氧键的极性,减弱了甲醇的酸性
18.(13 分)
(1)取代反应 (1 分) (2) 乙酸苯酚酯 (酚)羟基、酰胺基
(3)
(4) +NaOH→ +CH COONa
3
(5)12 (6)
12