文档内容
2024—2025 学年度第二学期高三第五次月考试题
化 学
一、选择题:本题共8小题,每小题2分,共16分。在每小题给出的四个选项中,
只有一项是符合题目要求的。
1.《天工开物》记载:软浆车榨蔗汁,一石汁下石灰五合,取汁煎糖,冷凝成黑沙,
黄泥水淋下成白糖。下列说法错误的是
A.石灰可中和蔗汁中的酸性物质 B.“冷凝成黑沙”是结晶过程
C.“黄泥水淋下”的目的是脱色 D.“白糖”的主要成分是葡萄糖
2.化学与人类生活、生产密切相关。下列说法正确的是
A.β-胡萝卜素是一种天然色素,可用作食品的着色剂
B.抗坏血酸具有较强氧化性,水果罐头中常用作抗氧化剂
C.乙二醇的水溶液凝固点很高,可作汽车发动机的抗冻剂
D.表面活性剂能溶解油脂,是因为其分子具有极性较大的亲油基团
3.下列有关化学概念或性质的判断错误的是
A. 分子是正四面体结构,则 没有同分异构体
B.CH +和CH -中C原子的杂化类型不同
3 3
C.船式C H ( )比椅式C H ( )稳定
6 12 6 12
D.由 与 组成的离子液体常温下呈液态,与其离子的体积较大有关
4.下列化学反应与方程式不相符的是
点燃
A.黑火药爆炸:S+2KNO +3C====K S+N ↑+3CO ↑
3 2 2 2
△
B.四氯化钛水解: ==
C.硫化钠溶液在空气中氧化变质:2S2-+O +4H+=2S↓+2H O
2 2
D.硬脂酸甘油酯在 溶液中皂化:
△
+3NaOH +3C H COONa
17 35
5.N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.标准状况下,2.24 L HF中含有的原子的数目为0.2N
A
B.25℃,pH=11的Na CO 溶液中OH-的数目为0.001N
2 3 A
C.32 g甲醇分子中含有C—H键的数目为4N
A
D.4.4 g由N O和CO 组成的混合物中含有的原子数为0.3N
2 2 A
6.实验室中下列做法错误的是
A.含重金属离子(如 等)的废液,加水稀释后排放
高三化学 第1 页 (共8页)
学科网(北京)股份有限公司高三化学 第1 页 (共8页)
B.轻微烫伤时,先用洁净的冷水处理,再涂抹烫伤药膏
C.乙炔等可燃性气体点燃前要检验纯度
D.水银易挥发,若不慎有水银洒落,可用硫粉处理
7.对反应 (I为中间产物),相同条件下:①加入催化剂,反应达到平衡所
需时间大幅缩短;②提高反应温度, 增大, 减小。基于以上
事实,可能的反应历程示意图(——为无催化剂,-----为有催化剂)为
A.
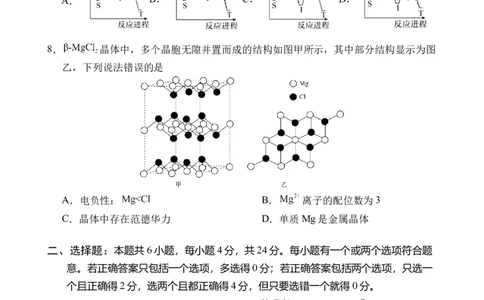
8. 晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示为图
乙,下列说法错误的是
A.电负性: B. 离子的配位数为3
C.晶体中存在范德华力 D.单质Mg是金属晶体
二、选择题:本题共6小题,每小题4分,共24分。每小题有一个或两个选项符合题
意。若正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一
个且正确得2分,选两个且都正确得4分,但只要选错一个就得0分。
9.在 水溶液中,电化学方法合成高能物质 时,伴随少量 生成,电解原
理如图所示,下列说法正确的是
A.电解时, 向Pt电极移动
B.生成 的电极反应:
C.电解一段时间后,溶液pH升高
D.每生成1 mol H 的同时,生成0.5
2
10.环六糊精(D-吡喃葡萄糖缩合物)具有空腔结构(如图1),腔内极性较小,腔外极
高三化学 第2 页 (共8页)
学科网(北京)股份有限公司高三化学 第2 页 (共8页)
性较大,可包合某些分子形成超分子(如图2),图3表示超分子在反应选择性方
面的相关应用。下列说法错误的是
A.环六糊精属于寡糖
B.非极性分子均可被环六糊精包合形成超分子
C.图2中甲氧基对位暴露在反应环境中
D.可用萃取法分离环六糊精和氯代苯甲醚
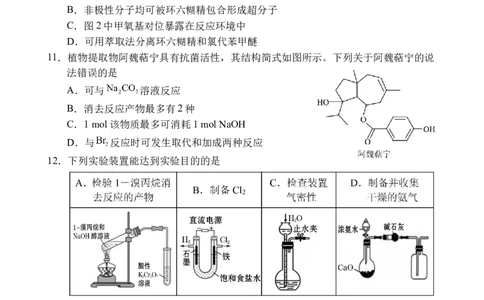
11.植物提取物阿魏萜宁具有抗菌活性,其结构简式如图所示。下列关于阿魏萜宁的说
法错误的是
A.可与 溶液反应
B.消去反应产物最多有2种
C.1 mol该物质最多可消耗1 mol NaOH
D.与 反应时可发生取代和加成两种反应
12.下列实验装置能达到实验目的的是
13.如图为某实验测得0.1 mol·L-1 溶液在升温过程中(不考虑水挥发)的pH变
化曲线。下列说法正确的是
A.a点溶液的 比c点溶液的小
B.a点时, K >K (H CO )·K (H CO )
w a1 2 3 a2 2 3
C.b点溶液中,
D.ab段,pH减小说明升温抑制了 的水解
14.室温下,根据下列实验过程及现象,能验证相应实验结论的是
高三化学 第3 页 (共8页)
学科网(北京)股份有限公司高三化学 第3 页 (共8页)
选项 实验过程及现象 实验结论
用0.1 mol·L-1 NaOH溶液分别中和等体积的
酸性:
A 0.1 mol·L - 1 H SO 溶 液 和 0.1 mol·L - 1
2 4
CH COOH溶液,H SO 消耗的NaOH溶液多
3 2 4
向KI溶液中持续滴加氯水,溶液先由无色变为 氯水具有氧化性和漂
B
棕黄色,一段时间后褪色 白性
向2 mL浓度均为0.1 mol·L-1的CaCl 和BaCl
2 2 溶度积常数:
C 混合溶液中滴加少量 0.1 mol·L-1 Na CO 溶
2 3
液,振荡,产生白色沉淀
将等体积等浓度的KI溶液和FeCl 溶液混合, I-和 Fe3+的反应是可
3
D
充分反应后滴入KSCN溶液,溶液变红 逆反应
三、非选择题:共5题,共60分。
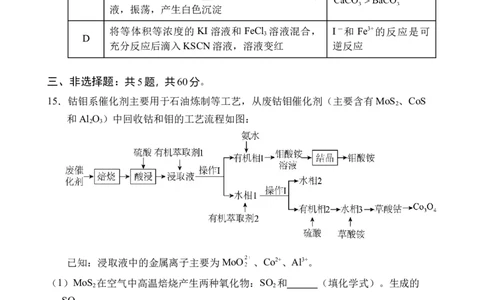
15.钴钼系催化剂主要用于石油炼制等工艺,从废钴钼催化剂(主要含有MoS 、CoS
2
和Al O )中回收钴和钼的工艺流程如图:
2 3
已知:浸取液中的金属离子主要为MoO 、Co2+、Al3+。
(1)MoS 在空气中高温焙烧产生两种氧化物:SO 和 (填化学式)。生成的
2 2
SO
2
被石灰乳充分吸收的化学方程式为 。
(2)Co2+萃取的反应原理为Co2++2HR CoR +2H+,向有机相2中加入H SO 能进行
2 2 4
反萃取的原因是 (结合平衡移动原理解释)。
(3)水相2中的主要溶质除了H SO ,还有 (填化学式)。
2 4
(4)Co O 可用作电极,若选用KOH电解质溶液,通电时可转化为CoOOH,则阳极电
3 4
极反应式为 。
16.为了实现“碳达峰”和“碳中和”的目标,将 转化成可利用的化学能源的
高三化学 第4 页 (共8页)
学科网(北京)股份有限公司高三化学 第4 页 (共8页)
“负碳”技术是世界各国关注的焦点。回答下列问题:
方法Ⅰ: 催化加氢制甲醇。
以 、 为原料合成 涉及的反应如下:
反应ⅰ:
反应ⅱ:
反应ⅲ:
(1)计算反应ⅲ的 。
(2)现利用ⅰ和ⅲ两个反应合成CH OH,已知CO可使反应的催化剂寿命降低。若
3
氢碳比表示为x= ,则理论上x= 时,平衡混合物中生成物
含 量 最 高 。 但 生 产 中 往 往 采 用 略 高 于 该 值 的 氢 碳 比 , 理 由 是
。
(3) ,在甲(容积为 )、乙(容积为 )两刚性容器中分别充入2 mol CO
2
和
6 mol H ,在适宜的催化剂作用下发生反应ⅰ,容器内总压强随时间变化如图
2
所示:
其中B曲线对应 容器中压强的变化情况(填
“甲”或“乙”);利用图中数据计算 该反应的分压平衡
常数K = (列出计算式即可)。
p
方法Ⅱ: 催化加氢制甲酸。
(4)科研工作者通过开发新型催化剂,利用太阳能电池将工业
排放的 转化为HCOOH,实现碳中和的目标。
已知 。
温度为T ℃达到平衡时,化学平衡常数 。实验测得:
1
, , 、 为速率常数。T ℃时,
1
高三化学 第5 页 (共8页)
学科网(北京)股份有限公司高三化学 第5 页 (共8页)
;若温度为 达到平衡时, ,则
(填“>”、“<”或“=”)。
17 . 某研究小组探究 AlCl 催化氯苯与氯化亚砜 (SOCl ) 转化为化合物 Z(
3 2
) 的反应。实验流程为:
已知:
①实验在通风橱内进行。
②SOCl 遇水即放出SO 和HCl;AlCl 易升华。
2 2 3
③氯苯溶于乙醚,难溶于水;Z易溶于乙醚,难溶于水;乙醚不易溶于水。
图1 图2
(1)在无水气氛中提纯少量AlCl 的简易升华装置如图1所示,此处漏斗的作用
3
是 。
(2)写出图2中干燥管内可用的酸性固体干燥剂 (填1种)。
(3)写出生成Z的化学方程式 。
(4)步骤Ⅱ,加入冰水的作用是 。
(5)步骤Ⅲ,从混合物M 中得到Z粗产物的所有操作如下,请排序 (填序号)。
2
①减压蒸馏
②用乙醚萃取、分液,重复2-3次
③过滤
④加入无水Na SO 干燥剂吸水
2 4
(6)AlCl 可促进氯苯与SOCl 反应中S-Cl键的断裂,从配合物角度分析,原因是
3 2
高三化学 第6 页 (共8页)
学科网(北京)股份有限公司高三化学 第6 页 (共8页)
。
18.可降解聚合物P{ }是一种重要的医用原
材料,其合成路线如下:
已知:
(1)A的化学名称是 。
(2)B中的官能团名称是 。
(3)F→P的反应类型为 。
(4)D的结构简式是 。
(5)F中有三个六元环,E→F的化学方程式是 。
(6)D有多种同分异构体,满足下列条件的结构有 种。
①属于芳香族化合物
②能水解,且水解产物能使 溶液显色
(7)以A为原料,设计合成 的路线
。
高三化学 第7 页 (共8页)
学科网(北京)股份有限公司高三化学 第7 页 (共8页)
19.氧是构建化合物的重要元素。请回答:
(1)Cu2+能与H O、OH-等形成配位数为4的配合物,画出Cu2+与乙二胺
2
以 形成的配离子结构为 。
(2) 中 的配位数为 ;粒子中的大 键可用符号
表示,其中m代表参与形成大 键的原子数,n代表参与形成大 键的电子数
(如
苯分子中的大 键可表示为 ),则配体中 的大 键可表示为 ,其
空间结构为 。
(3)化合物 的结构如图。
和 中羟基与水均可形成氢键(—O—H…OH),按照氢键由强到弱对
三种酸排序 ,请说明理由 。
(4)铈的某种氧化物具有面心立方晶体结构,结构如下图,若晶胞中无氧空位时,
该理想晶体的化学式为 。高温下,该氧化物失去氧形成氧空位,每失
去 ,理论上有 mol 生成。
高三化学 第8 页 (共8页)
学科网(北京)股份有限公司高三化学 第8 页 (共8页)
高三化学 第9 页 (共8页)
学科网(北京)股份有限公司