文档内容
2025-2026 学年上学期
东北师大附中(化学)科试卷
高三年级第一次摸底考试
注意事项:
1.答题前,考生需将自己的姓名、班级、考场座位号填写在答题卡指定位置上,并粘贴条形
码。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。择
如需改动,用橡皮擦干净后,再选涂其它答案标号。
3.回答非选择题时,请使用0.5毫米黑色字迹签字笔将答案写在答题卡各题目的答题区域内,
超出答题区域或在草稿纸、本试题卷上书写的答案无效。
4.保持卡面清洁,不要折叠、不要弄皱、弄破,不准使用涂改液、修正带、刮纸刀。
可能用到的相对原子质量:H1 Li7 O16 A127 S32 Fe56
一、选择题:本题共10小题,每小题2分,共20分。在每小题给出的四个选项中,只有一1
项符合题目要求。
1. 化学与生产、生活紧密联系,下列有关说法正确的是
A. 电热水器利用外加电流法的原理镶上镁棒防止内胆腐蚀
B. 碳酸氢铵可用作食品膨松剂
C. 为防止茶叶氧化变质,常在包装袋中放入生石灰
D. 工业上常利用电解熔融氯化物获取钠、镁、铝等活泼金属
2. 关于物质性质及应用,下列说法正确的是
的
A. 利用浓硫酸 吸水性,可除去HCl中的水蒸气
B. 漂白粉进行漂白时可加入浓盐酸,增强其漂白效果
C. 铁比铜活泼,故电子工业中常用Fe与含Cu2+的溶液反应来蚀刻电路板
D. 工业上常将热空气吹出的溴蒸汽用NaCO 溶液吸收,利用了Br 的挥发性和强氧化性
2 3 2
3. 设 为阿伏加德罗常数的值。下列说法正确的是
A. 的中子数,比 的多
第1页/共12页
学科网(北京)股份有限公司B. 与水蒸气完全反应,生成 的数目为
C. 在 的 溶液中, 的数目为
D. 标准状况下的 与足量 反应,形成的共价键数目为
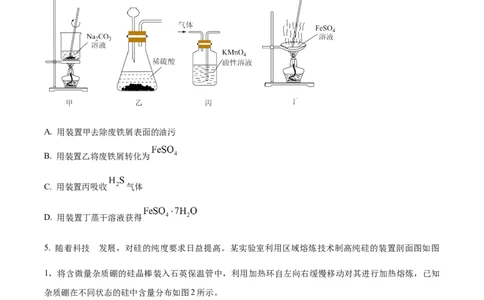
4. 以废铁屑(主要成分为Fe,含少量 、FeS等)为原料制备 。下列相关原理、装置及操
作正确的是
A. 用装置甲去除废铁屑表面的油污
B. 用装置乙将废铁屑转化为
C. 用装置丙吸收 气体
D. 用装置丁蒸干溶液获得
的
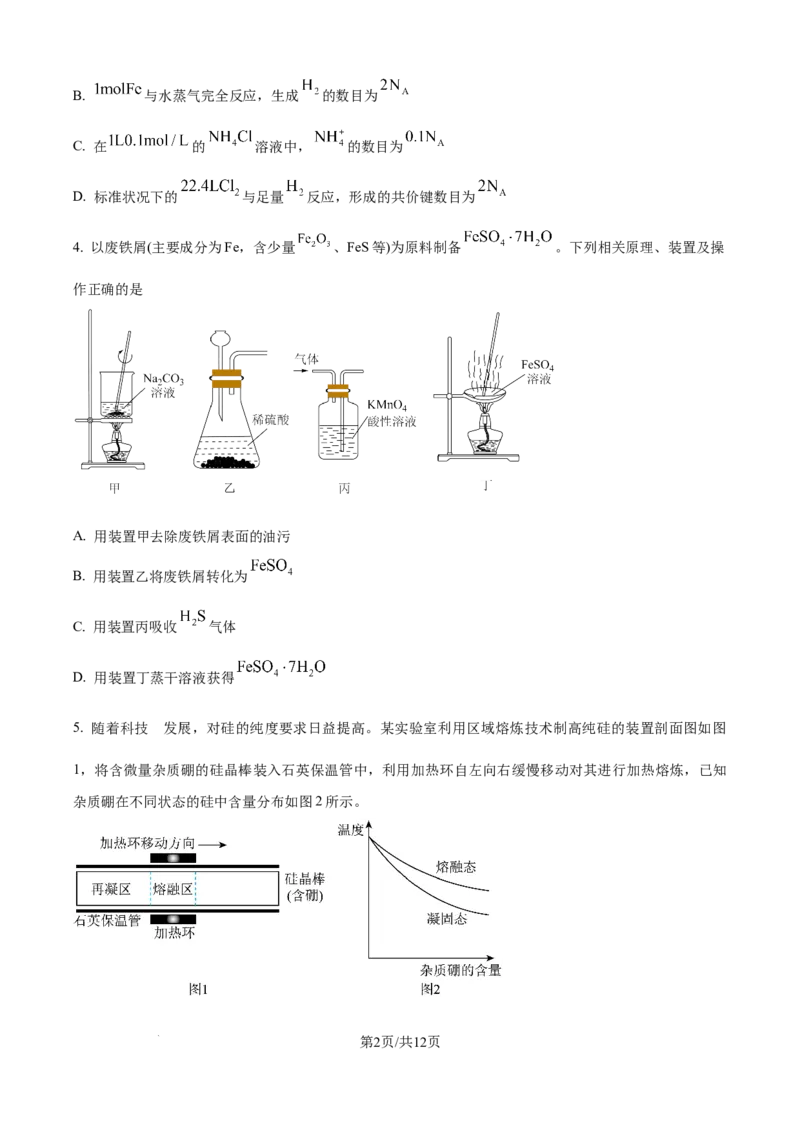
5. 随着科技 发展,对硅的纯度要求日益提高。某实验室利用区域熔炼技术制高纯硅的装置剖面图如图
1,将含微量杂质硼的硅晶棒装入石英保温管中,利用加热环自左向右缓慢移动对其进行加热熔炼,已知
杂质硼在不同状态的硅中含量分布如图2所示。
第2页/共12页
学科网(北京)股份有限公司下列说法中错误的是
A. 混有杂质硼的硅晶棒熔点低于纯硅
B. 熔炼前,石英保温管中应排净空气后充入氩气
C. 熔炼时,加热环移动速度过快可能导致杂质硼分离不彻底
D. 熔炼后,硅晶棒纯度右端高于左端
6. 能满足下列物质间直接转化关系,且推理成立的是
单质X 氧化物1 氧化物2 酸(或碱) 盐
A. X可为铝,盐的水溶液可能显酸性
B. X可为硫,氧化物1可使品红溶液或酸性高锰酸钾溶液褪色
C. X可为钠,氧化物2可与水反应生成H
2
D. X可为碳,盐的热稳定性和水中的溶解性:NaHCO >Na CO
3 2 3
7. 下列实验产生的废液中,可能大量存在的粒子组是
选
实验 粒子组
项
A 稀硝酸与铜片制
B 硫酸与 制
C 浓盐酸与 制
D 双氧水与 溶液制
A. A B. B C. C D. D
8. 在给定条件下,下列制备过程涉及的物质转化均可实现的是
A. HCl制备:
B. 工业制镁:
C. 制纯碱:
D. 漂白粉制备:
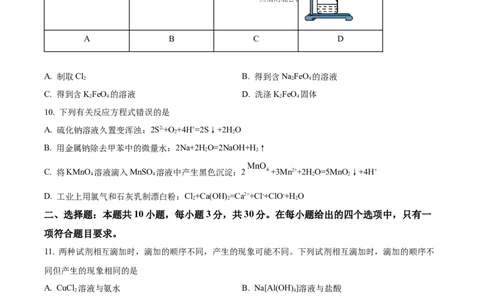
9. 高铁酸钾(K FeO)是具有极强氧化性的消毒剂,可用NaClO溶液(Cl 与NaOH溶液反应生成)在碱性
2 4 2
第3页/共12页
学科网(北京)股份有限公司条件下氧化Fe(NO ) 后经转化分离制得。某实验小组按照图示步骤(夹持、加热装置均略去)依次操作,
3 3
制备KFeO 固体。常温下的溶解度:NaFeO>K FeO。下列步骤中的装置和原理无法达成相应实验目的的
2 4 2 4 2 4
是
A B C D
A. 制取Cl B. 得到含NaFeO 的溶液
2 2 4
C. 得到含KFeO 的溶液 D. 洗涤KFeO 固体
2 4 2 4
10. 下列有关反应方程式错误的是
A. 硫化钠溶液久置变浑浊:2S2-+O +4H+=2S↓+2H O
2 2
B. 用金属钠除去甲苯中的微量水:2Na+2HO=2NaOH+H ↑
2 2
C. 将KMnO 溶液滴入MnSO 溶液中产生黑色沉淀:2 +3Mn2++2H O=5MnO ↓+4H+
4 4 2 2
D. 工业上用氯气和石灰乳制漂白粉:Cl+Ca(OH) =Ca2++Cl-+ClO-+H O
2 2 2
二、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一
项符合题目要求。
11. 两种试剂相互滴加时,滴加的顺序不同,产生的现象可能不同。下列试剂相互滴加时,滴加的顺序不
同但产生的现象相同的是
A. CuCl 溶液与氨水 B. Na[Al(OH)]溶液与盐酸
2 4
C. NaHCO 溶液与澄清的石灰水 D. FeBr 溶液与Cl 的四氯化碳溶液
3 2 2
12. 卤化铵( )的能量关系如图所示,下列说法正确的是
第4页/共12页
学科网(北京)股份有限公司A. ,
B. 相同条件下, 的 比 的大
C. 相同条件下, 的 比 的小
D.
13. 实验室测定氧化物X(FeO)的组成实验如下:
x
下列有关说法正确的是
A. 样品X中氧元素的质量分数约为26.3%
B. 溶液Y中c(Fe2+):c(Fe3+)=2:1
C. 用酸性高锰酸钾溶液检验溶液Z中是否含有Fe2+
D. 根据步骤I、Ⅱ可以判断X的组成为Fe O
0.75
14. 与下列实验操作对应的现象、结论均正确的是
实验操作 现象 结论
通入SO 产生白色沉
向BaCl 溶液中通入SO ,再滴 2 白色沉淀为BaSO,
A 2 2 淀,滴加稀HNO 后白 3
加稀HNO 溶液 3 后转化成BaSO
3 色沉淀不溶解 4
B 向NaSO 溶液中加入稀硫酸 溶液变浑浊 HSO 具有氧化性
2 2 3 2 4
室温下取少量NaHCO 固体于试
3 NaHCO 固体溶解放
C 管中,加几滴水,振荡,将温度 温度计示数升高 3
热
计插入试剂中
D 往装有碘的CCl 溶液的试管中加 下层由紫红色变浅至几 碘在浓KI溶液中的溶
4
第5页/共12页
学科网(北京)股份有限公司入等体积的浓KI溶液,振荡、 解度大于在CCl 中的
乎无色,上层呈棕黄色 4
静置分层 溶解度
A. A B. B C. C D. D
15. 实验室用如下方法制备饮用水消毒剂ClO
2
已知:NCl 为强氧化剂,其中N元素为-3价
3
下列说法不正确的是
A. NH Cl的电子式为
4
B. 电解池中总反应的化学方程式为NH Cl+2HCl NCl +3H ↑
4 3 2
C. 若NaClO 与NCl 恰好完全反应,则X为NaCl
2 3
D. 饮用水中残留的ClO 可用适量FeSO 溶液去除
2 4
16. 化学上常用标准电极电势φ (氧化型/还原型)比较物质氧化能力。φ 值越高,氧化型物质的氧化能力越
强,φ 值与体系的pH有关。利用表格所给的数据分析,以下说法错误的是
氧化型/还原型 φ (Co3+/Co2+) φ (HClO/Cl-)
酸性介质 1.84V 1.49V
氧化型/还原型 φ [Co(OH) /Co(OH) ] φ (ClO-/Cl-)
3 2
碱性介质 0.17V x
A. 推测:x<1.49V
B. Co O 与浓盐酸发生反应:Co O+8H+=Co2++2Co3++4H O
3 4 3 4 2
C. 若x=0.81V,碱性条件下可发生反应:2Co(OH) +NaClO+H O=2Co(OH) +NaCl
2 2 3
D. 从图中数据可知,氧化型物质的氧化性随着溶液酸性增强而增强
第6页/共12页
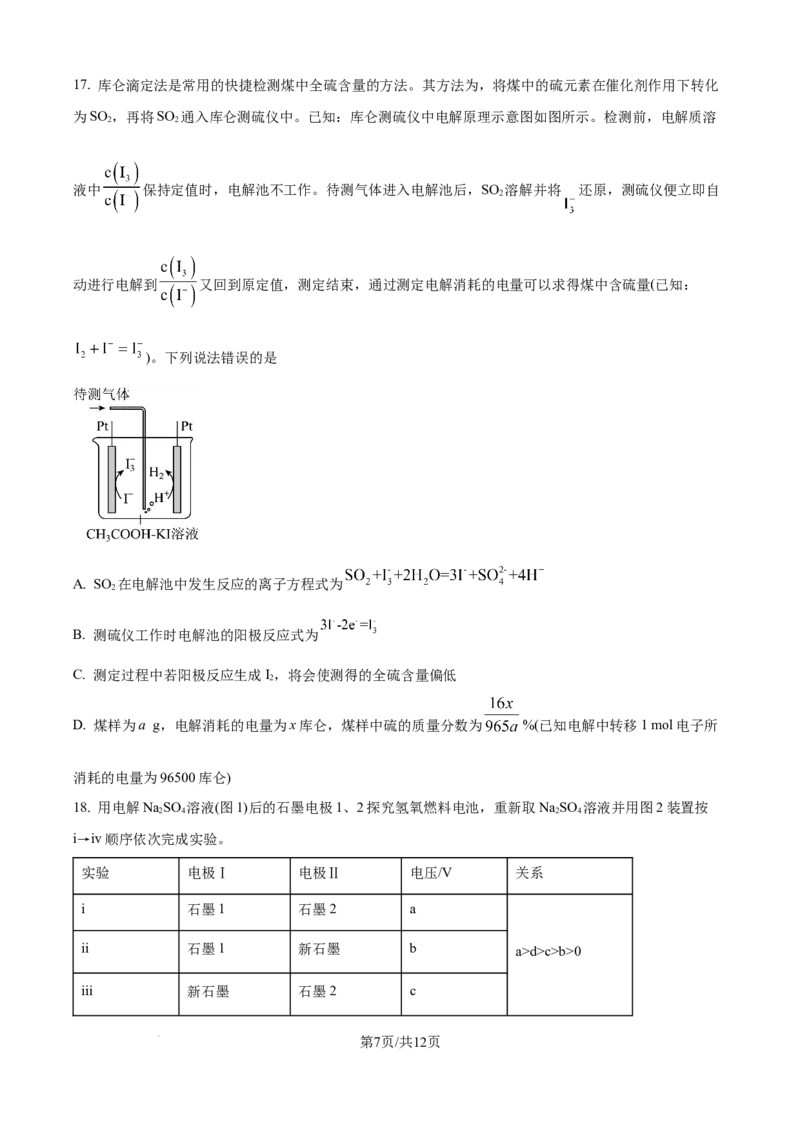
学科网(北京)股份有限公司17. 库仑滴定法是常用的快捷检测煤中全硫含量的方法。其方法为,将煤中的硫元素在催化剂作用下转化
为SO ,再将SO 通入库仑测硫仪中。已知:库仑测硫仪中电解原理示意图如图所示。检测前,电解质溶
2 2
液中 保持定值时,电解池不工作。待测气体进入电解池后,SO 溶解并将 还原,测硫仪便立即自
2
动进行电解到 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量(已知:
)。下列说法错误的是
A. SO 在电解池中发生反应的离子方程式为
2
B. 测硫仪工作时电解池的阳极反应式为
C. 测定过程中若阳极反应生成I,将会使测得的全硫含量偏低
2
D. 煤样为a g,电解消耗的电量为x库仑,煤样中硫的质量分数为 %(已知电解中转移1 mol电子所
消耗的电量为96500库仑)
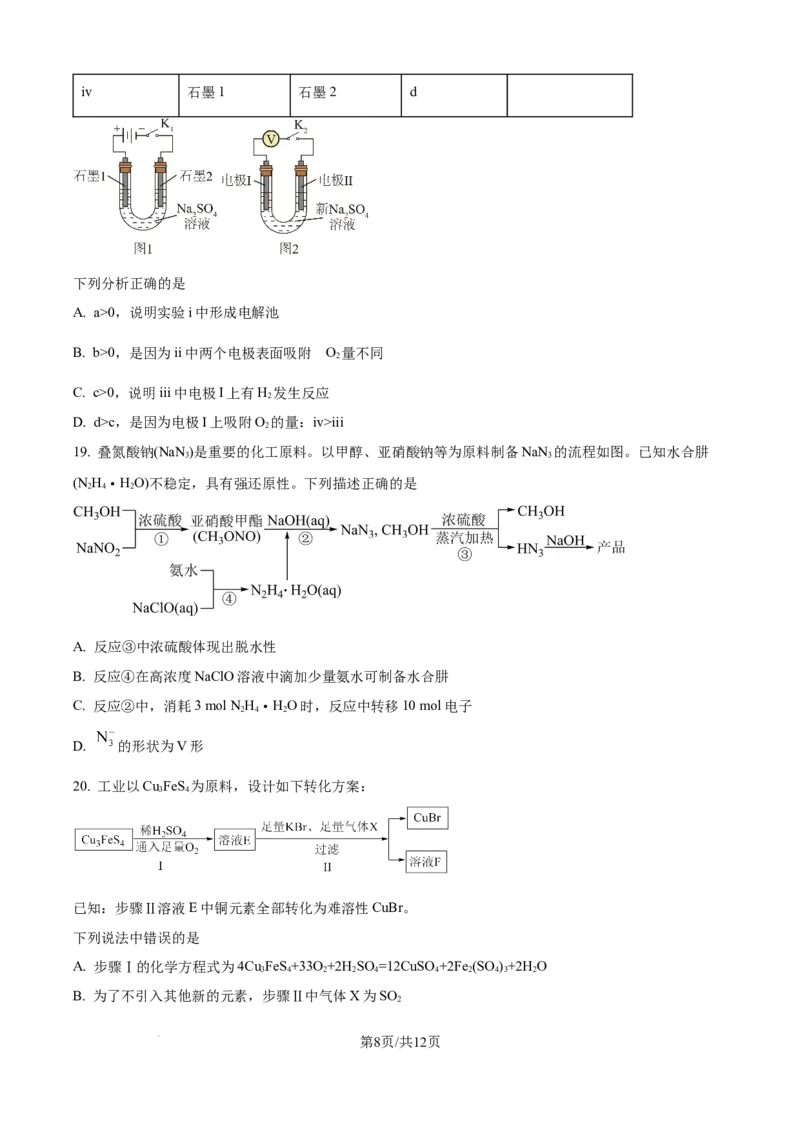
18. 用电解NaSO 溶液(图1)后的石墨电极1、2探究氢氧燃料电池,重新取NaSO 溶液并用图2装置按
2 4 2 4
i→iv顺序依次完成实验。
实验 电极Ⅰ 电极Ⅱ 电压/V 关系
i 石墨1 石墨2 a
ii 石墨1 新石墨 b a>d>c>b>0
iii 新石墨 石墨2 c
第7页/共12页
学科网(北京)股份有限公司iv 石墨1 石墨2 d
下列分析正确的是
A. a>0,说明实验i中形成电解池
的
B. b>0,是因为ii中两个电极表面吸附 O 量不同
2
C. c>0,说明iii中电极I上有H 发生反应
2
D. d>c,是因为电极I上吸附O 的量:iv>iii
2
19. 叠氮酸钠(NaN )是重要的化工原料。以甲醇、亚硝酸钠等为原料制备NaN 的流程如图。已知水合肼
3 3
(N H·HO)不稳定,具有强还原性。下列描述正确的是
2 4 2
A. 反应③中浓硫酸体现出脱水性
B. 反应④在高浓度NaClO溶液中滴加少量氨水可制备水合肼
C. 反应②中,消耗3 mol N H·HO时,反应中转移10 mol电子
2 4 2
D. 的形状为V形
20. 工业以Cu FeS 为原料,设计如下转化方案:
3 4
已知:步骤Ⅱ溶液E中铜元素全部转化为难溶性CuBr。
下列说法中错误的是
A. 步骤Ⅰ的化学方程式为4Cu FeS+33O +2H SO =12CuSO+2Fe (SO )+2H O
3 4 2 2 4 4 2 4 3 2
B. 为了不引入其他新的元素,步骤Ⅱ中气体X为SO
2
第8页/共12页
学科网(北京)股份有限公司C. 溶液F中除K+、H+、Br-外,浓度最高的离子为Fe2+
D. 将Cu FeS 研成粉末有利于提高反应速率和原料的利用率
3 4
三、非选择题:本题共4小题,共50分
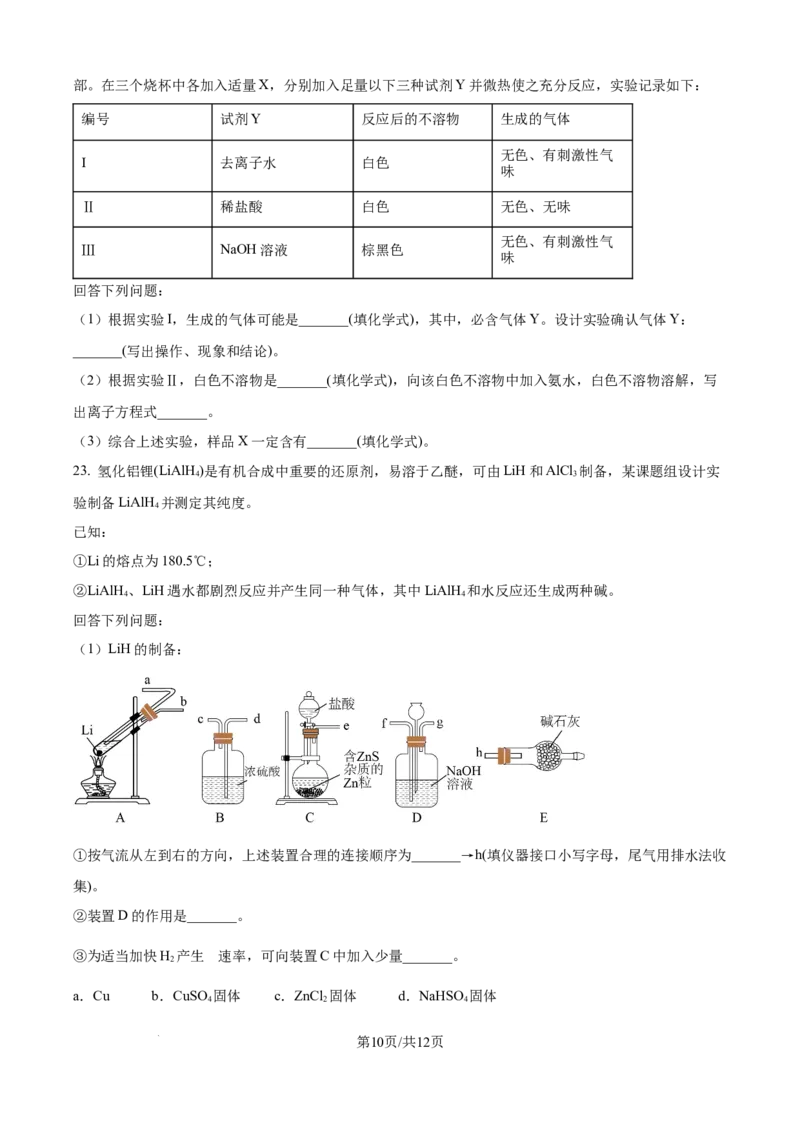
21. 铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化氧化膜结构,
增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定氧化膜厚度,操作步骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2 mol·L-1的NaOH溶液在60~70℃下洗涤,除去铝表面的薄氧化膜,反应的离
子方程式为_______;再用10%(质量分数)的HNO 溶液对铝片表面进行化学抛光。
3
(2)电解氧化
取预处理过的铝片和铅作电极,控制电流恒定为0.06A,用直流电源在5~6 mol·L-1的硫酸中进行电解。
产生氧化膜的电极反应式为_______。氧化膜的生长过程,可大致分为A、B、C三个阶段(如图所示),A
阶段中电压逐渐增大的原因是_______。
(3)氧化膜的质量检验
取出经阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3g
KCr O+75mL水+25mL浓硫酸),用秒表测定铝片表面颜色变为绿色(产生Cr3+)所需的时间,即可判断氧化
2 2 7
膜的耐腐蚀性。写出该变色反应的离子方程式:_______。
(4)氧化膜厚度的测定
的
①取氧化完毕 铝片,测得其表面积为4.0cm2,洗净吹干,称得质量为0.7654g;
②将铝片浸于60℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片的质量为0.7442g。
已知氧化膜的密度为2.7g·cm-3,可以计算出氧化膜的厚度为_______μm(氧化膜的厚度=
,保留3位有效数字)。
22. 白色固体样品X,可能含有AgNO、NH NO 、BaCl 、KCl、NaSO 、NaCO、Al O 之中的几种或全
3 4 3 2 2 3 2 3 2 3
第9页/共12页
学科网(北京)股份有限公司部。在三个烧杯中各加入适量X,分别加入足量以下三种试剂Y并微热使之充分反应,实验记录如下:
编号 试剂Y 反应后的不溶物 生成的气体
无色、有刺激性气
I 去离子水 白色
味
Ⅱ 稀盐酸 白色 无色、无味
无色、有刺激性气
Ⅲ NaOH溶液 棕黑色
味
回答下列问题:
(1)根据实验I,生成的气体可能是_______(填化学式),其中,必含气体Y。设计实验确认气体Y:
_______(写出操作、现象和结论)。
(2)根据实验Ⅱ,白色不溶物是_______(填化学式),向该白色不溶物中加入氨水,白色不溶物溶解,写
出离子方程式_______。
(3)综合上述实验,样品X一定含有_______(填化学式)。
23. 氢化铝锂(LiAlH )是有机合成中重要的还原剂,易溶于乙醚,可由LiH和AlCl 制备,某课题组设计实
4 3
验制备LiAlH 并测定其纯度。
4
已知:
①Li的熔点为180.5℃;
②LiAlH 、LiH遇水都剧烈反应并产生同一种气体,其中LiAlH 和水反应还生成两种碱。
4 4
回答下列问题:
(1)LiH的制备:
①按气流从左到右的方向,上述装置合理的连接顺序为_______→h(填仪器接口小写字母,尾气用排水法收
集)。
②装置D的作用是_______。
的
③为适当加快H 产生 速率,可向装置C中加入少量_______。
2
a.Cu b.CuSO 固体 c.ZnCl 固体 d.NaHSO 固体
4 2 4
第10页/共12页
学科网(北京)股份有限公司(2)LiAlH 的制备:将(1)中制得的LiH加入反应器中,加入乙醚和AlCl 及少量LiAlH (作引发剂),充分
4 3 4
反应后过滤除去LiCl沉淀,滤液经一系列操作得白色晶体,经真空足量水干燥可得产品LiAlH 。写出生成
4
LiAlH 的化学方程式:_______。LiAlH 为离子化合物,其电子式为_______。
4 4
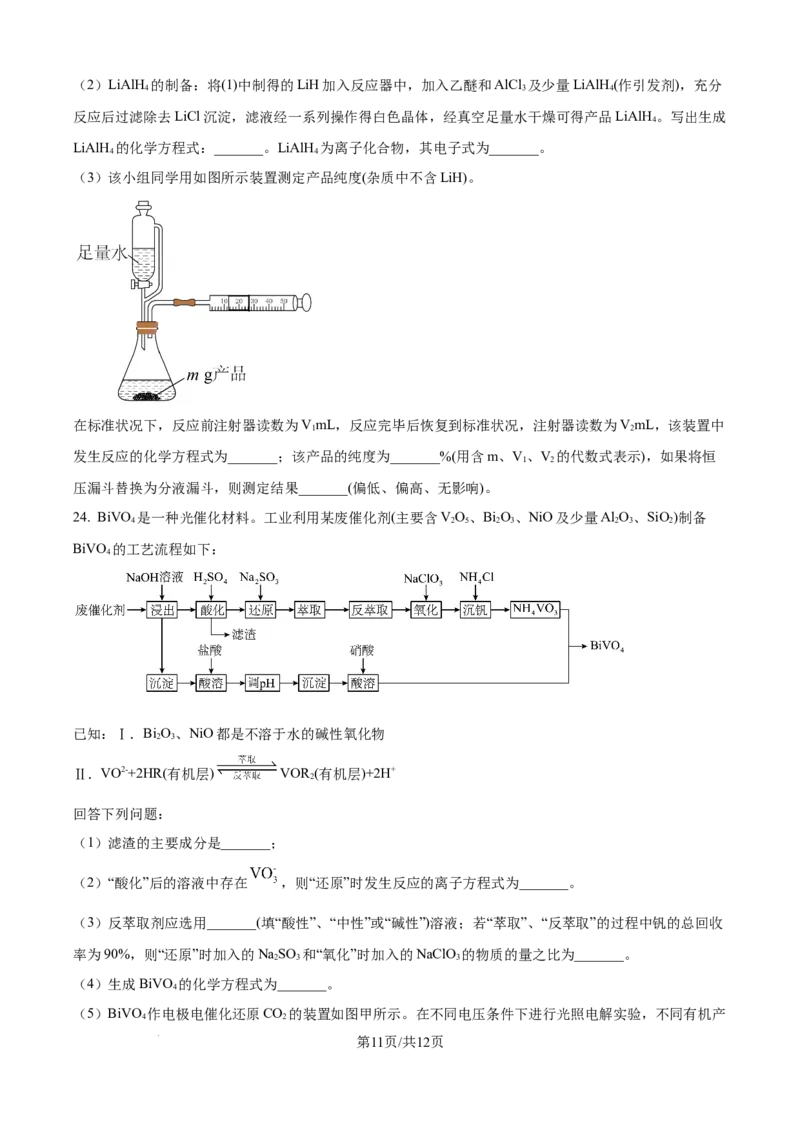
(3)该小组同学用如图所示装置测定产品纯度(杂质中不含LiH)。
在标准状况下,反应前注射器读数为VmL,反应完毕后恢复到标准状况,注射器读数为VmL,该装置中
1 2
发生反应的化学方程式为_______;该产品的纯度为_______%(用含m、V、V 的代数式表示),如果将恒
1 2
压漏斗替换为分液漏斗,则测定结果_______(偏低、偏高、无影响)。
24. BiVO 是一种光催化材料。工业利用某废催化剂(主要含VO、BiO、NiO及少量Al O、SiO)制备
4 2 5 2 3 2 3 2
BiVO 的工艺流程如下:
4
已知:Ⅰ.BiO、NiO都是不溶于水的碱性氧化物
2 3
Ⅱ.VO2-+2HR(有机层) VOR (有机层)+2H+
2
回答下列问题:
(1)滤渣的主要成分是_______;
(2)“酸化”后的溶液中存在 ,则“还原”时发生反应的离子方程式为_______。
(3)反萃取剂应选用_______(填“酸性”、“中性”或“碱性”)溶液;若“萃取”、“反萃取”的过程中钒的总回收
率为90%,则“还原”时加入的NaSO 和“氧化”时加入的NaClO 的物质的量之比为_______。
2 3 3
(4)生成BiVO 的化学方程式为_______。
4
(5)BiVO 作电极电催化还原CO 的装置如图甲所示。在不同电压条件下进行光照电解实验,不同有机产
4 2
第11页/共12页
学科网(北京)股份有限公司物的法拉第效率(FE)随电压变化如图乙所示。
已知:FE%= ×100%,其中,Q=nF,n表示电解生成还原产物X所
x
转移电子的物质的量,F表示法拉第常数。
①电势比较:泡沫Ni网电极_______BiVO 电极(填“>”“<”或“=”)。
4
②BiVO 电极发生的电极反应式为_______。
4
③维持电压为UV,电解一段时间后,生成的HCHO和HCOOH的物质的量之比为5∶3,则生成HCOOH
3
的法拉第效率m为_______。
第12页/共12页
学科网(北京)股份有限公司