文档内容
2025 届高三第七次模拟考试
化学试卷
本试卷满分100分,考试时间75分钟
一、选择题(共15题,每题3分,共45分)
1.中国古代化学工艺是中华璀璨文明的一部分,下列有关说法不正确的是
...
A.东汉成书记载有“石胆化铁则为铜”,该过程涉及了置换反应
B.历史悠久的景德镇瓷器是由黏土经高温烧结而成
C.古代炼丹家由丹砂(HgS)炼水银的方法属于现代金属冶炼工艺中的热还原法
D.用青铜铸剑利用了青铜比纯铜熔点低、硬度大的优点
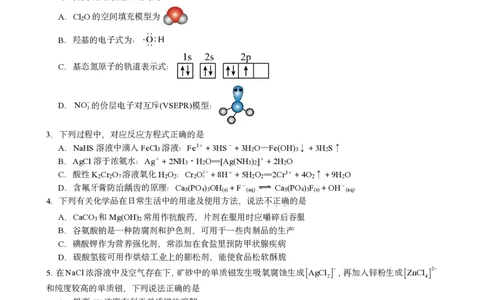
2.下列化学用语表达正确的是
A.Cl O的空间填充模型为
2
B.羟基的电子式为:
C.基态氮原子的轨道表示式:
D.NO 的价层电子对互斥(VSEPR)模型:
3
3.下列过程中,对应反应方程式正确的是
A.NaHS溶液中滴入FeCl 溶液:Fe3++3HS-+3H O Fe(OH) ↓+3H S↑
3 2 3 2
B.AgCl溶于浓氨水:Ag++2NH ·H O [Ag(NH ) ]++2H O
3 2 3 2 2
C.酸性K Cr O 溶液氧化H O :Cr O2-+8H++5H O 2Cr3++4O ↑+9H O
2 2 7 2 2 2 7 2 2 2 2
D.含氟牙膏防治龋齿的原理:Ca (PO ) OH +F- Ca (PO ) F +OH-
5 4 3 (s) (aq) 5 4 3 (s) (aq)
4.下列有关化学品在日常生活中的用途及使用方法,说法不正确的是
...
A.CaCO 和Mg(OH) 常用作抗酸药,片剂在服用时应嚼碎后吞服
3 2
B.谷氨酸钠是一种防腐剂和护色剂,可用于一些肉制品的生产
C.碘酸钾作为营养强化剂,常添加在食盐里预防甲状腺疾病
D.碳酸氢铵可用作烘焙工业上的膨松剂,能使食品松软酥脆
5.在NaCl浓溶液中及空气存在下,矿砂中的单质银发生吸氧腐蚀生成 AgCl ,再加入锌粉生成 ZnCl 2
2 4
和纯度较高的单质银,下列说法正确的是
A.提高Cl浓度有利于单质银的溶解
B.发生腐蚀时正极的电极反应式为:4H++O +4e- 2H O
2 2
C.随着腐蚀的进行,溶液的pH减小
D.加入锌粉反应后,溶液中阴离子总浓度增大
试卷第1页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}6.下列实验能达成预期目的的是
实
验
目 A.制备银氨 B.滴定未知浓度的
C.铁制镀件电镀铜 D.制备乙酸乙酯
的 溶液 HCl溶液
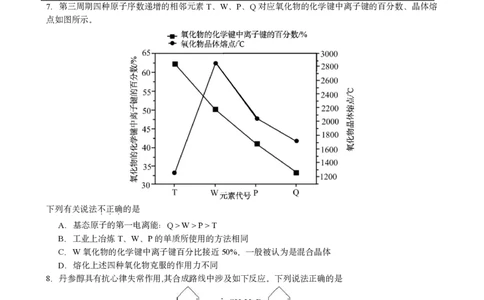
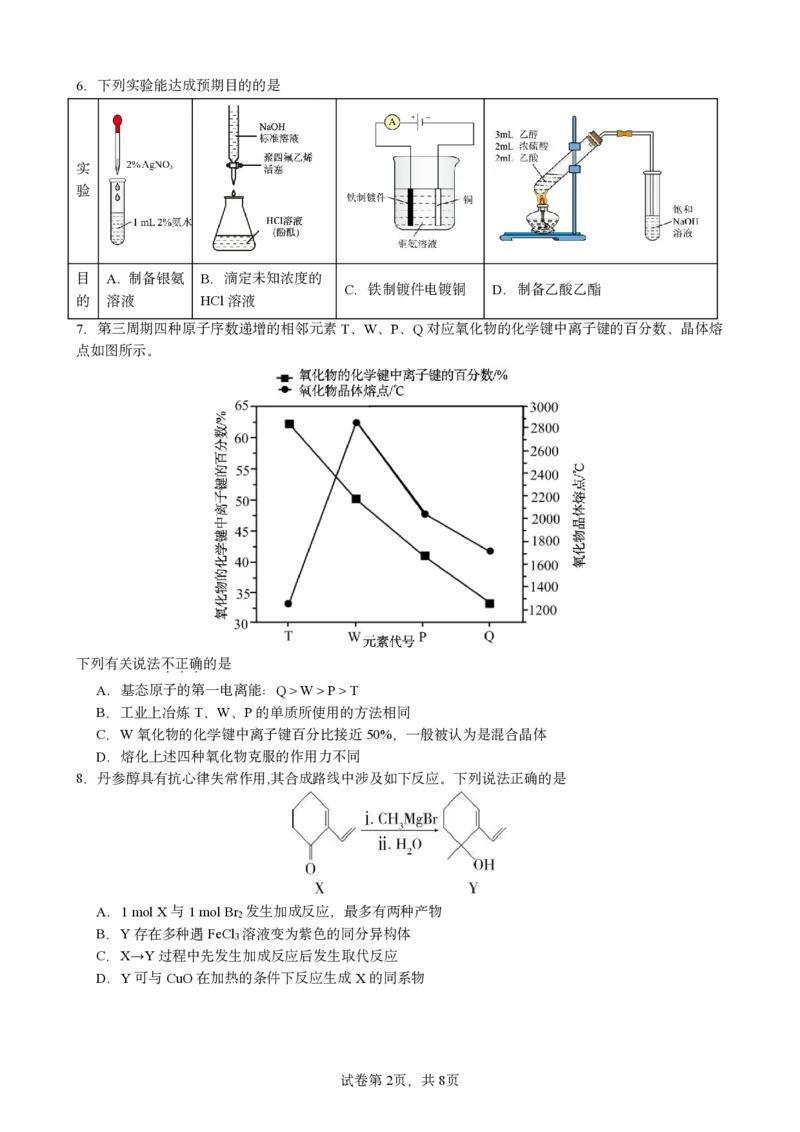
7.第三周期四种原子序数递增的相邻元素T、W、P、Q对应氧化物的化学键中离子键的百分数、晶体熔
点如图所示。
下列有关说法不正确的是
...
A.基态原子的第一电离能:Q>W>P>T
B.工业上冶炼T、W、P的单质所使用的方法相同
C.W氧化物的化学键中离子键百分比接近50%,一般被认为是混合晶体
D.熔化上述四种氧化物克服的作用力不同
8.丹参醇具有抗心律失常作用,其合成路线中涉及如下反应。下列说法正确的是
A.1molX与1molBr 发生加成反应,最多有两种产物
2
B.Y存在多种遇FeCl 溶液变为紫色的同分异构体
3
C.X→Y过程中先发生加成反应后发生取代反应
D.Y可与CuO在加热的条件下反应生成X的同系物
试卷第2页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}9.X、Y、Z、M为原子序数依次增大的前四周期元素。X、Y、Z位于同一周期,基态X原子电子占据3
个能级,且每个能级所含的电子数相同,Y的第一电离能大于Z的第一电离能,M的合金是我国使用最早
的合金。下列说法正确的是
A.基态X原子的核外电子共有3种空间运动状态
B.X、Y、Z的简单氢化物均可与M的阳离子形成配位键
C.X、Y、Z与氢元素形成的四元素化合物均为共价化合物
D.与基态M原子最外层电子数相同的同周期元素还有2种
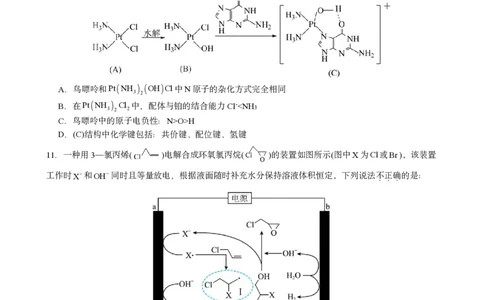
10.在铜转运蛋白的作用下,顺铂PtNH Cl 进入人体细胞发生水解,生成的PtNH OHCl与鸟嘌
3 2 2 3 2
呤作用进而破坏DNA的结构,阻止癌细胞增殖,过程如图所示。其中鸟嘌呤为扁平结构,下列说法正确
的是
A.鸟嘌呤和PtNH OHCl中N原子的杂化方式完全相同
3 2
B.在PtNH Cl 中,配体与铂的结合能力Cl-O>H
D.(C)结构中化学键包括:共价键、配位键、氢键
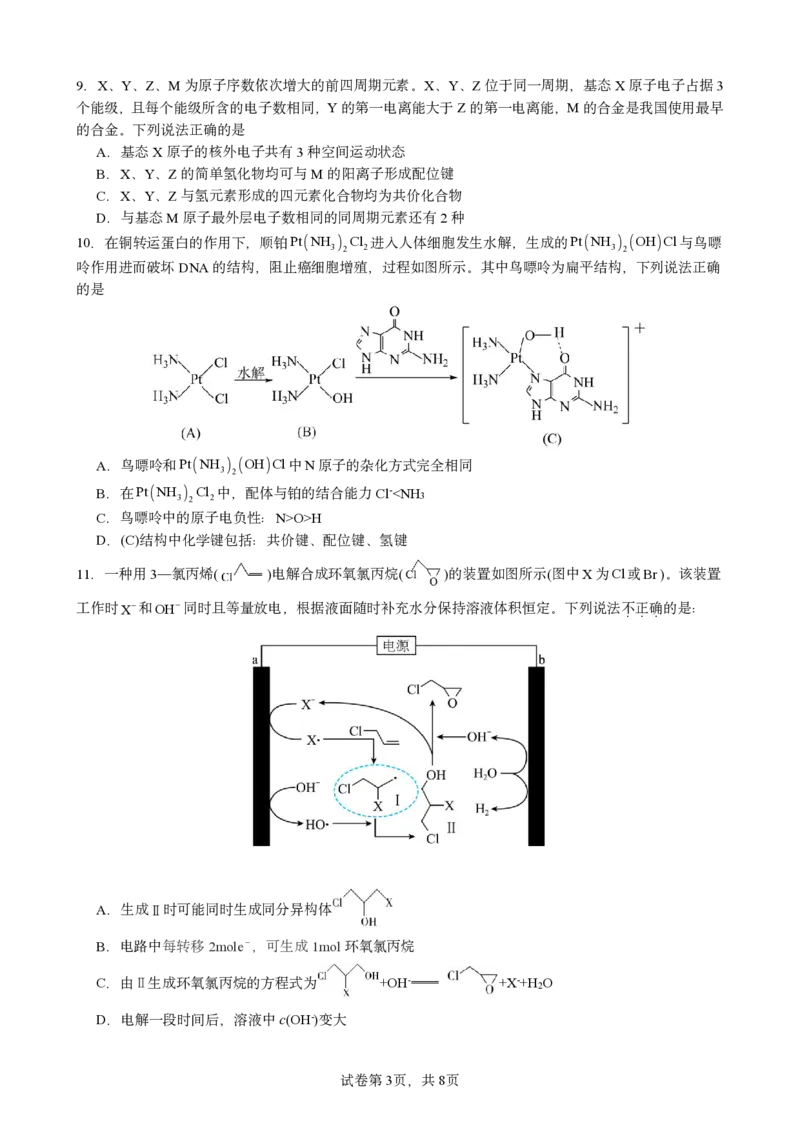
11.一种用3—氯丙烯( )电解合成环氧氯丙烷( )的装置如图所示(图中X为Cl或Br)。该装置
工作时X和OH同时且等量放电,根据液面随时补充水分保持溶液体积恒定。下列说法不正确的是:
...
A.生成Ⅱ时可能同时生成同分异构体
B.电路中每转移2mole-,可生成1mol环氧氯丙烷
C.由 生成环氧氯丙烷的方程式为 +OH- +X-+H O
Ⅱ 2
D.电解一段时间后,溶液中c(OH-)变大
试卷第3页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}12.聚苯胺是一种新型材料,其结构如图所示,其中完全还原型(y=1)和完全氧化型(y=0)都为绝缘体。由
于脱氢程度不同,得到的聚苯胺结构中的y值不同,以特定比例结合经过掺杂处理后会产生良好的导电性。
下列说法不正确的是
...
A.聚苯胺由苯胺通过加成聚合制得
B.苯胺具有碱性,能与盐酸反应
C.当y=0.5时,聚苯胺可能具有最佳的导电性
D.苯胺脱氢程度越高,y值越小
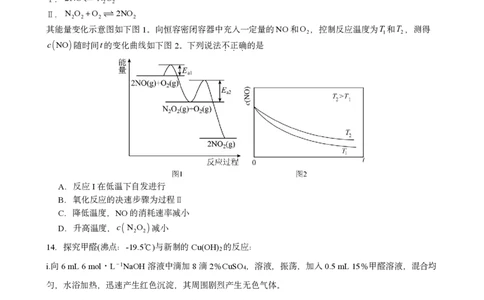
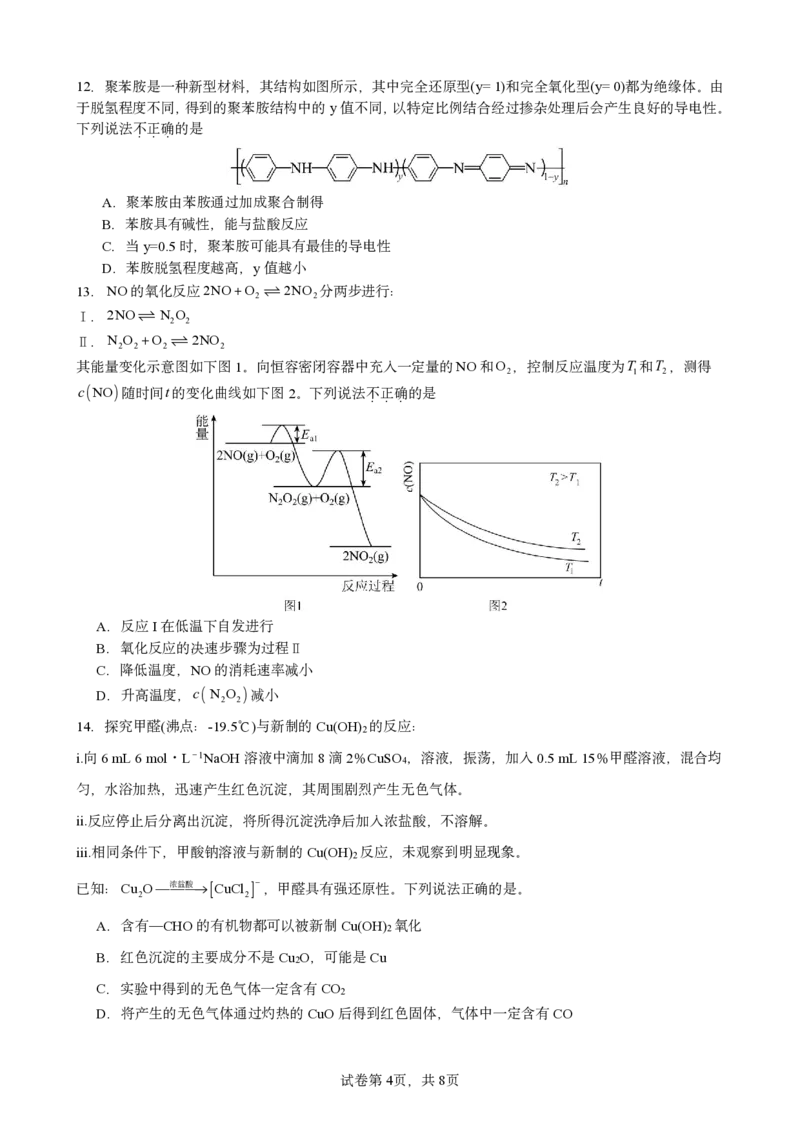
13.NO的氧化反应2NOO 2NO 分两步进行:
2 2
.2NO N O
Ⅰ 2 2
.N O O 2NO
Ⅱ 2 2 2 2
其能量变化示意图如下图1。向恒容密闭容器中充入一定量的NO和O ,控制反应温度为T 和T ,测得
2 1 2
cNO 随时间t的变化曲线如下图2。下列说法不正确的是
...
A.反应I在低温下自发进行
B.氧化反应的决速步骤为过程
Ⅱ
C.降低温度,NO的消耗速率减小
D.升高温度,c N O 减小
2 2
14.探究甲醛(沸点:-19.5 )与新制的Cu(OH) 的反应:
℃ 2
i.向6mL6mol·L-1NaOH溶液中滴加8滴2%CuSO ,溶液,振荡,加入0.5mL15%甲醛溶液,混合均
4
匀,水浴加热,迅速产生红色沉淀,其周围剧烈产生无色气体。
ii.反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解。
iii.相同条件下,甲酸钠溶液与新制的Cu(OH) 反应,未观察到明显现象。
2
已知:Cu O浓盐酸CuCl ,甲醛具有强还原性。下列说法正确的是。
2 2
A.含有—CHO的有机物都可以被新制Cu(OH) 氧化
2
B.红色沉淀的主要成分不是Cu O,可能是Cu
2
C.实验中得到的无色气体一定含有CO
2
D.将产生的无色气体通过灼热的CuO后得到红色固体,气体中一定含有CO
试卷第4页,共8页
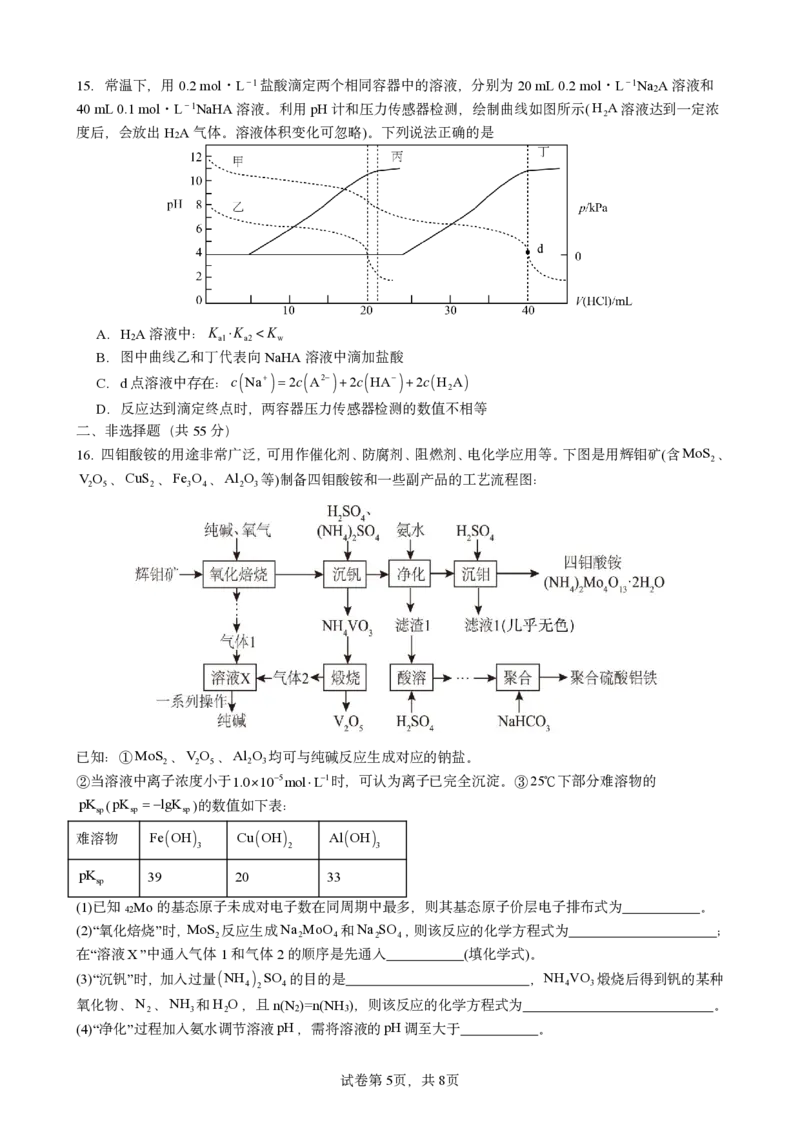
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}15.常温下,用0.2mol·L-1盐酸滴定两个相同容器中的溶液,分别为20mL0.2mol·L-1Na A溶液和
2
40mL0.1mol·L-1NaHA溶液。利用pH计和压力传感器检测,绘制曲线如图所示(H A溶液达到一定浓
2
度后,会放出H A气体。溶液体积变化可忽略)。下列说法正确的是
2
A.H A溶液中:K K K
2 a1 a2 w
B.图中曲线乙和丁代表向NaHA溶液中滴加盐酸
C.d点溶液中存在:c Na 2c A2 2c HA 2cH A
2
D.反应达到滴定终点时,两容器压力传感器检测的数值不相等
二、非选择题(共55分)
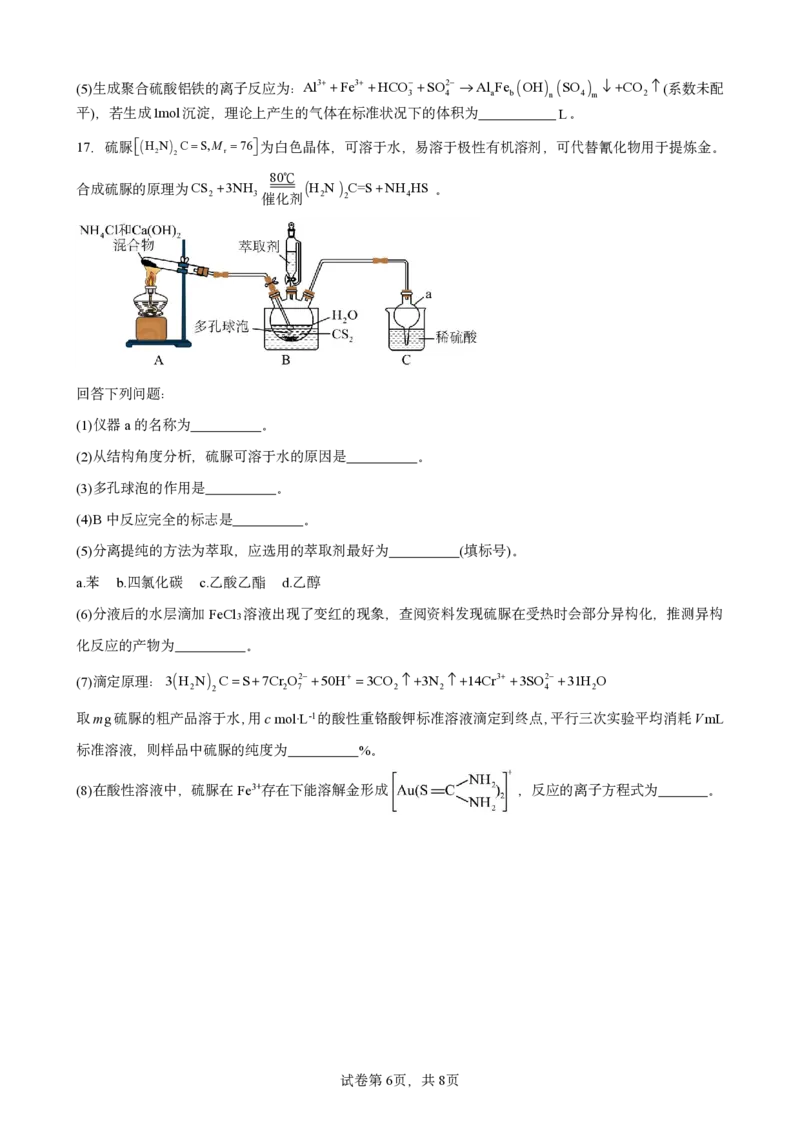
16.四钼酸铵的用途非常广泛,可用作催化剂、防腐剂、阻燃剂、电化学应用等。下图是用辉钼矿(含MoS 、
2
VO 、CuS 、Fe O 、Al O 等)制备四钼酸铵和一些副产品的工艺流程图:
2 5 2 3 4 2 3
已知: MoS 、VO 、Al O 均可与纯碱反应生成对应的钠盐。
① 2 2 5 2 3
当溶液中离子浓度小于1.0105molL1时,可认为离子已完全沉淀。 25℃下部分难溶物的
② ③
pK (pK lgK )的数值如下表:
sp sp sp
难溶物
FeOH CuOH AlOH
3 2 3
pK 39 20 33
sp
(1)已知 Mo的基态原子未成对电子数在同周期中最多,则其基态原子价层电子排布式为 。
42
(2)“氧化焙烧”时,MoS 反应生成Na MoO 和Na SO ,则该反应的化学方程式为 ;
2 2 4 2 4
在“溶液X”中通入气体1和气体2的顺序是先通入 (填化学式)。
(3)“沉钒”时,加入过量 NH SO 的目的是 ,NH VO 煅烧后得到钒的某种
4 2 4 4 3
氧化物、N 、NH 和H O,且n(N )=n(NH ),则该反应的化学方程式为 。
2 3 2 2 3
(4)“净化”过程加入氨水调节溶液pH,需将溶液的pH调至大于 。
试卷第5页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}(5)生成聚合硫酸铝铁的离子反应为:Al3Fe3HCOSO2 Al Fe OH SO CO (系数未配
3 4 a b n 4 m 2
平),若生成1mol沉淀,理论上产生的气体在标准状况下的体积为 L。
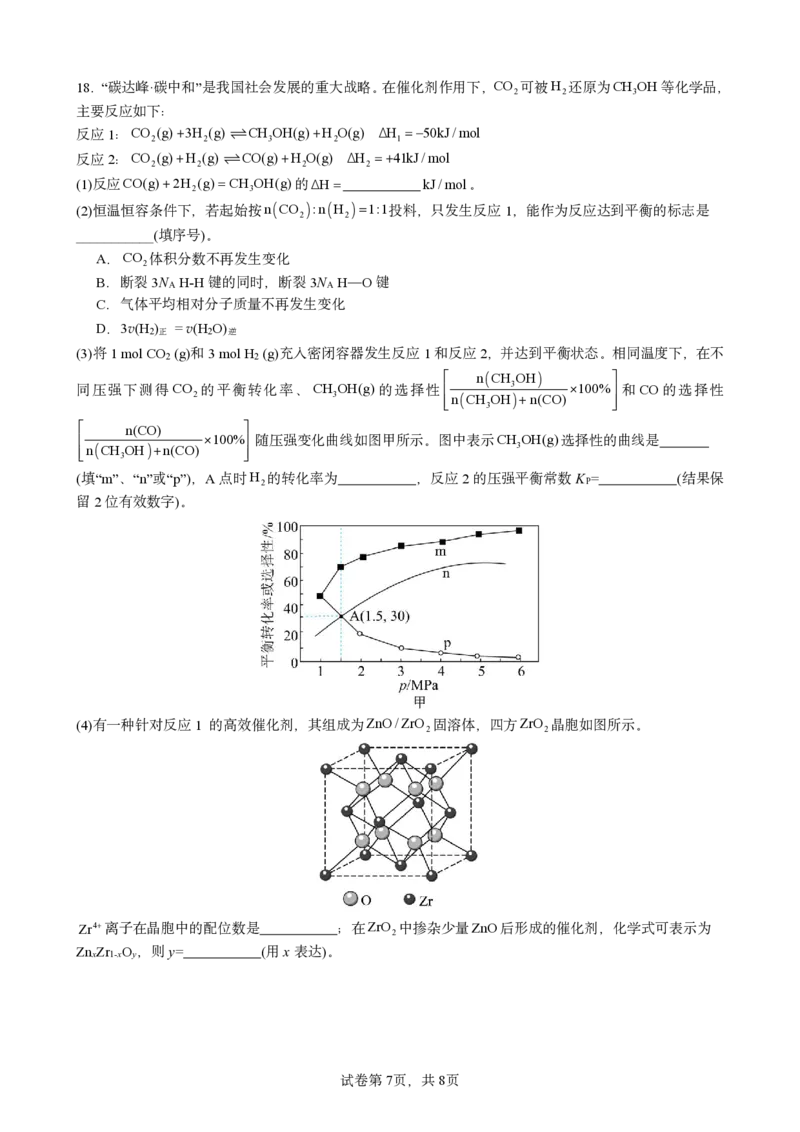
17.硫脲 H 2 N 2 CS,M r 76 为白色晶体,可溶于水,易溶于极性有机溶剂,可代替氰化物用于提炼金。
80℃
合成硫脲的原理为CS 3NH H N C=SNH HS 。
2 3催化剂 2 2 4
回答下列问题:
(1)仪器a的名称为 。
(2)从结构角度分析,硫脲可溶于水的原因是 。
(3)多孔球泡的作用是 。
(4)B中反应完全的标志是 。
(5)分离提纯的方法为萃取,应选用的萃取剂最好为 (填标号)。
a.苯 b.四氯化碳 c.乙酸乙酯 d.乙醇
(6)分液后的水层滴加FeCl 溶液出现了变红的现象,查阅资料发现硫脲在受热时会部分异构化,推测异构
3
化反应的产物为 。
(7)滴定原理:3H N CS7CrO250H 3CO 3N 14Cr33SO231H O
2 2 2 7 2 2 4 2
取mg硫脲的粗产品溶于水,用cmol∙L-1的酸性重铬酸钾标准溶液滴定到终点,平行三次实验平均消耗VmL
标准溶液,则样品中硫脲的纯度为 %。
(8)在酸性溶液中,硫脲在Fe3+存在下能溶解金形成 ,反应的离子方程式为 。
试卷第6页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}18.“碳达峰∙碳中和”是我国社会发展的重大战略。在催化剂作用下,CO 可被H 还原为CH OH等化学品,
2 2 3
主要反应如下:
反应1:CO (g)3H (g) CH OH(g)H O(g) H 50kJ/mol
2 2 3 2 1
反应2:CO (g)H (g) CO(g)H O(g) H 41kJ/mol
2 2 2 2
(1)反应CO(g)2H (g)CH OH(g)的H kJ/mol。
2 3
(2)恒温恒容条件下,若起始按nCO :nH 1:1投料,只发生反应1,能作为反应达到平衡的标志是
2 2
___________(填序号)。
A.CO 体积分数不再发生变化
2
B.断裂3N H-H键的同时,断裂3N H—O键
A A
C.气体平均相对分子质量不再发生变化
D.3v(H
2
)
正
=v(H
2
O)
逆
(3)将1molCO (g)和3molH (g)充入密闭容器发生反应1和反应2,并达到平衡状态。相同温度下,在不
2 2
nCH OH
同压强下测得CO 的平衡转化率、CH OH(g)的选择性 3 100% 和CO的选择性
2 3 nCH
3
OHn(CO)
n(CO)
100% 随压强变化曲线如图甲所示。图中表示CH OH(g)选择性的曲线是
nCH
3
OHn(CO)
3
(填“m”、“n”或“p”),A点时H 的转化率为 ,反应2的压强平衡常数K = (结果保
2 P
留2位有效数字)。
(4)有一种针对反应1 的高效催化剂,其组成为ZnO/ZrO 固溶体,四方ZrO 晶胞如图所示。
2 2
Zr4离子在晶胞中的配位数是 ;在ZrO 中掺杂少量ZnO后形成的催化剂,化学式可表示为
2
Zn Zr O ,则y= (用x 表达)。
x 1-x y
试卷第7页,共8页
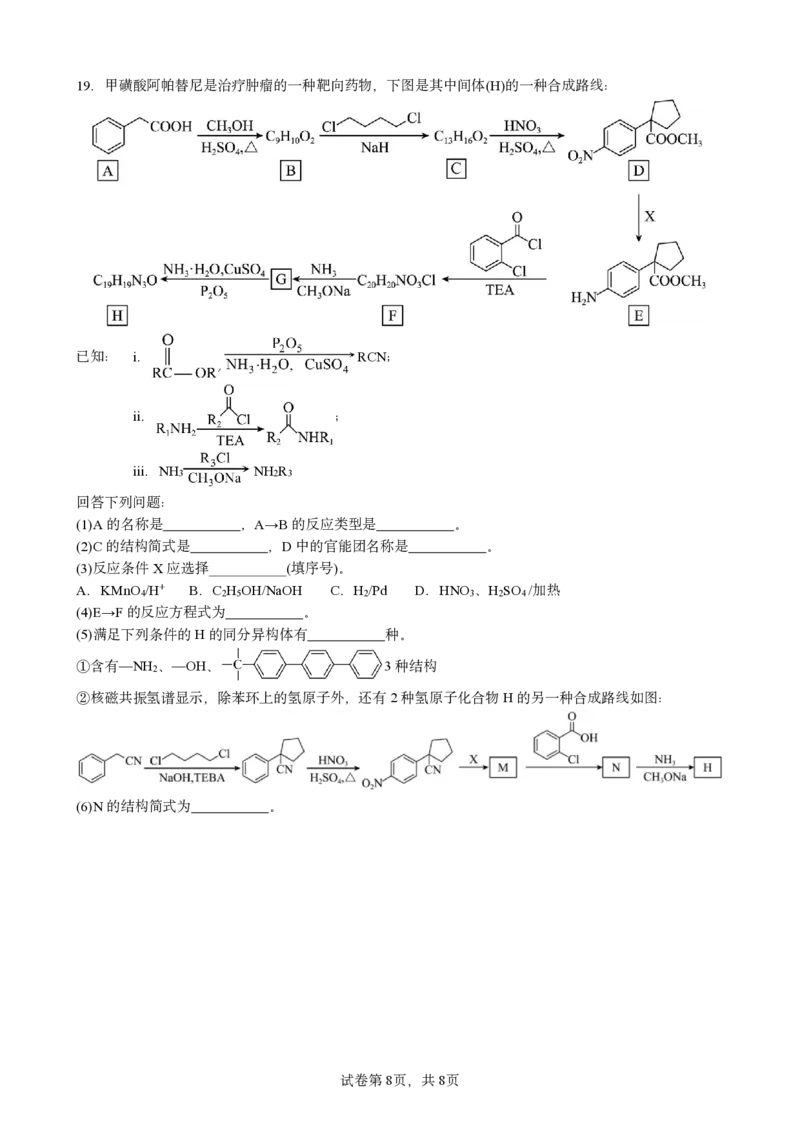
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}19.甲磺酸阿帕替尼是治疗肿瘤的一种靶向药物,下图是其中间体(H)的一种合成路线:
已知: i. RCN;
ii. ;
iii.NH NH R
3 2 3
回答下列问题:
(1)A的名称是 ,A→B的反应类型是 。
(2)C的结构简式是 ,D中的官能团名称是 。
(3)反应条件X应选择___________(填序号)。
A.KMnO /H+ B.C H OH/NaOH C.H /Pd D.HNO 、H SO /加热
4 2 5 2 3 2 4
(4)E→F的反应方程式为 。
(5)满足下列条件的H的同分异构体有 种。
含有—NH 、—OH、 3种结构
① 2
核磁共振氢谱显示,除苯环上的氢原子外,还有2种氢原子化合物H的另一种合成路线如图:
②
(6)N的结构简式为 。
试卷第8页,共8页
{#{QQABLYGswggYkASACQ5KA0HiCgsQkIKiJUoMRQAZuAxLwYFIBIA=}#}