文档内容
专题57 化学反应速率与平衡综合问题
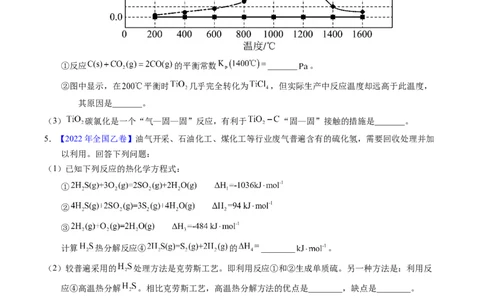
1.【2023年6月浙江卷】一定条件下, 苯基丙炔( )可与 发生催化加成,反应如下:
反应过程中该炔烃及反应产物的占比随时间的变化如图(已知:反应I、Ⅲ为放热反应),下列说法不正确的
是
A.反应焓变:反应I>反应Ⅱ
B.反应活化能:反应I<反应Ⅱ
C.增加 浓度可增加平衡时产物Ⅱ和产物I的比例
D.选择相对较短的反应时间,及时分离可获得高产率的产物Ⅰ
2.(2021·北京真题)有科学研究提出:锂电池负极材料(Li)由于生成LH而不利于电池容量的保持。一定温
度下,利用足量重水(D O)与含LiH的Li负极材料反应,通过测定n(D )/n(HD)可以获知
2 2
n(Li)/n(LiH)。
已知:①LiH+H O=LiOH+H ↑
2 2
②2Li(s)+H 2⇌2LiH △H<0
下列说法不正确的是
A.可用质谱区分D 和HD
2
B.Li与DO的反应:2Li+2DO=2LiOD+D ↑
2 2 2
C.若n(Li)/n(LiH)越大,则n(D )/n(HD)越小
2
D.80℃反应所得n(D )/n(HD)比25℃反应所得n(D )/n(HD)大
2 2
3.【2021年江苏卷】NH 与O 作用分别生成N、NO、NO的反应均为放热反应。工业尾气中的NH 可
3 2 2 2 3
通过催化氧化为N 除去。将一定比例的NH 、O 和N 的混合气体以一定流速通过装有催化剂的反应
2 3 2 2
管,NH 的转化率、生成N 的选择性[ 100%]与温度的关系如图所示。
3 2下列说法正确的是
A.其他条件不变,升高温度,NH 的平衡转化率增大
3
B.其他条件不变,在175~300 ℃范围,随温度的升高,出口处N 和氮氧化物的量均不断增大
2
C.催化氧化除去尾气中的NH 应选择反应温度高于250 ℃
3
D.高效除去尾气中的NH ,需研发低温下NH 转化率高和N 选择性高的催化剂
3 3 2
4.【2022年全国甲卷】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法之
一是将金红石 转化为 ,再进一步还原得到钛。回答下列问题:
(1) 转化为 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
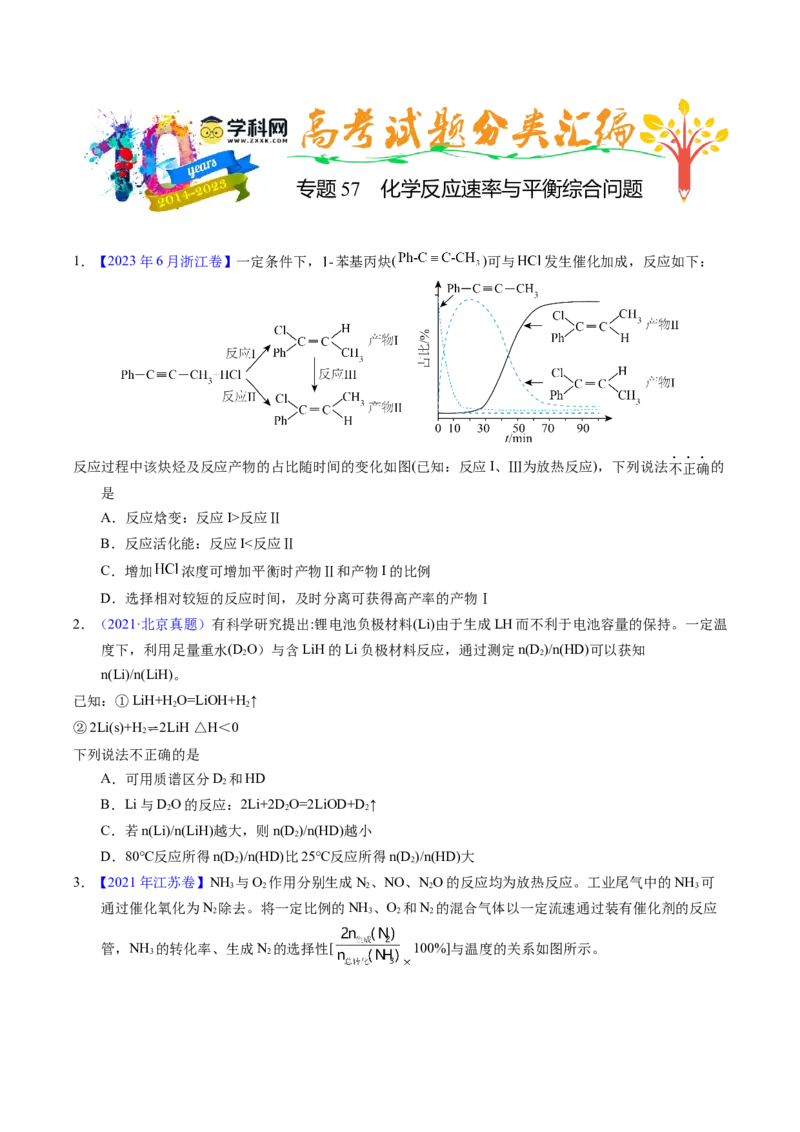
①反应 的 为_______ , _______Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是_______。
③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转
化率_______(填“变大”“变小”或“不变”)。
(2)在 ,将 、C. 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质
的量分数)随温度变化的理论计算结果如图所示。①反应 的平衡常数 _______ 。
②图中显示,在 平衡时 几乎完全转化为 ,但实际生产中反应温度却远高于此温度,
其原因是_______。
(3) 碳氯化是一个“气—固—固”反应,有利于 “固—固”接触的措施是_______。
5.【2022年全国乙卷】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加
以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
③
计算 热分解反应④ 的 ________ 。
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反
应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
(3)在 、 反应条件下,将 的混合气进行 热分解反应。平衡时混合气
中 与 的分压相等, 平衡转化率为________,平衡常数 ________ 。
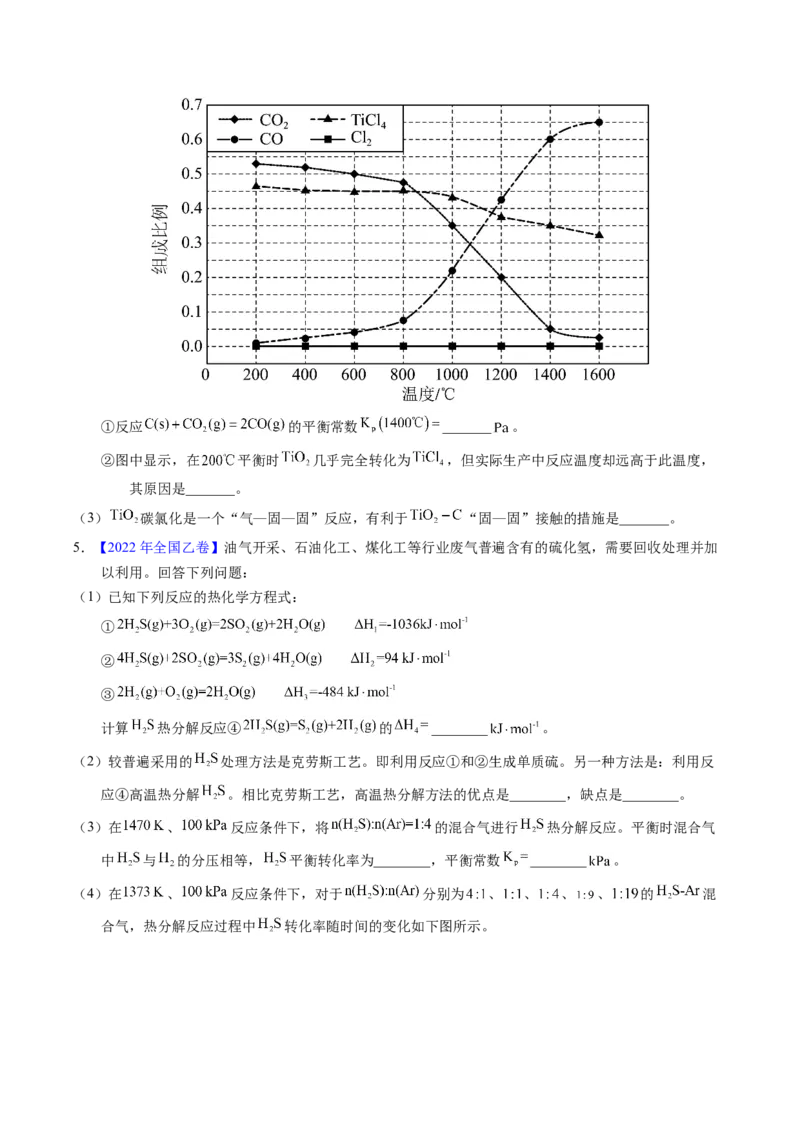
(4)在 、 反应条件下,对于 分别为 、 、 、 、 的 混
合气,热分解反应过程中 转化率随时间的变化如下图所示。① 越小, 平衡转化率________,理由是________。
② 对应图中曲线________,计算其在 之间, 分压的平均变化率为________
。
6.【2022年山东卷】利用 丁内酯(BL)制备1, 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和
丁醇(BuOH)的副反应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压 氛围下进行,故
压强近似等于总压。回答下列问题:
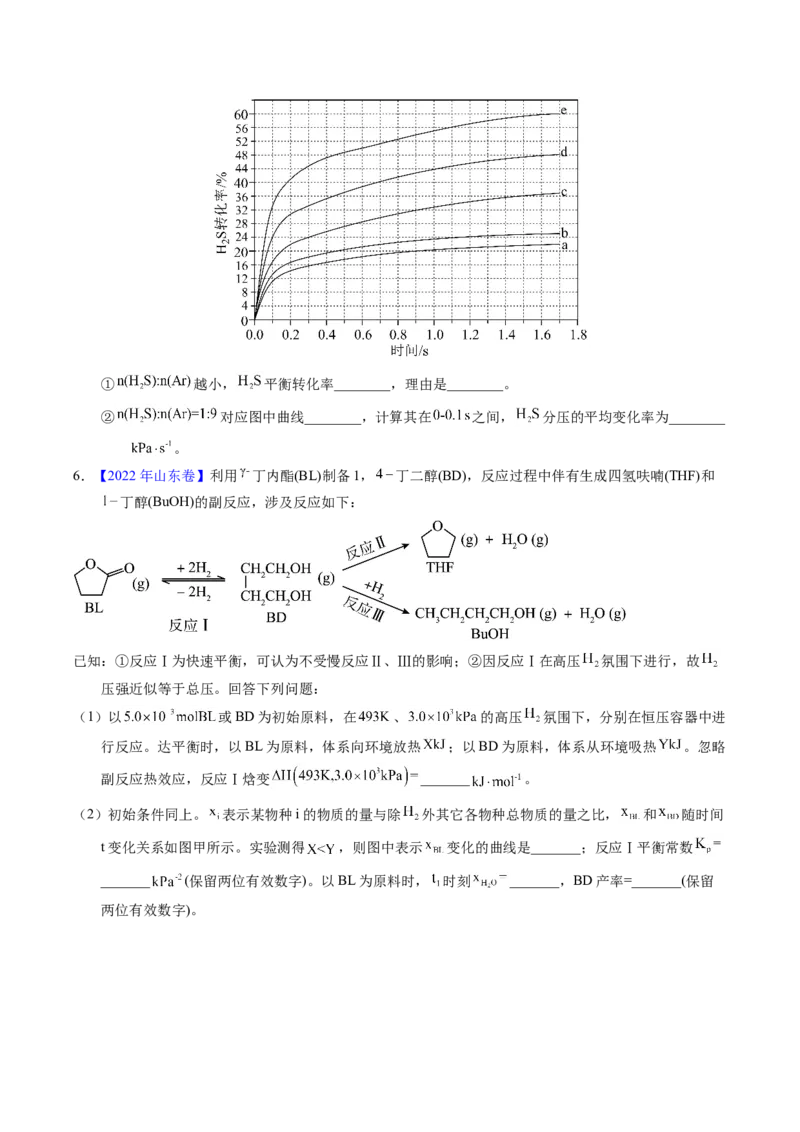
(1)以 或BD为初始原料,在 、 的高压 氛围下,分别在恒压容器中进
行反应。达平衡时,以BL为原料,体系向环境放热 ;以BD为原料,体系从环境吸热 。忽略
副反应热效应,反应Ⅰ焓变 _______ 。
(2)初始条件同上。 表示某物种i的物质的量与除 外其它各物种总物质的量之比, 和 随时间
t变化关系如图甲所示。实验测得 ,则图中表示 变化的曲线是_______;反应Ⅰ平衡常数
_______ (保留两位有效数字)。以BL为原料时, 时刻 _______,BD产率=_______(保留
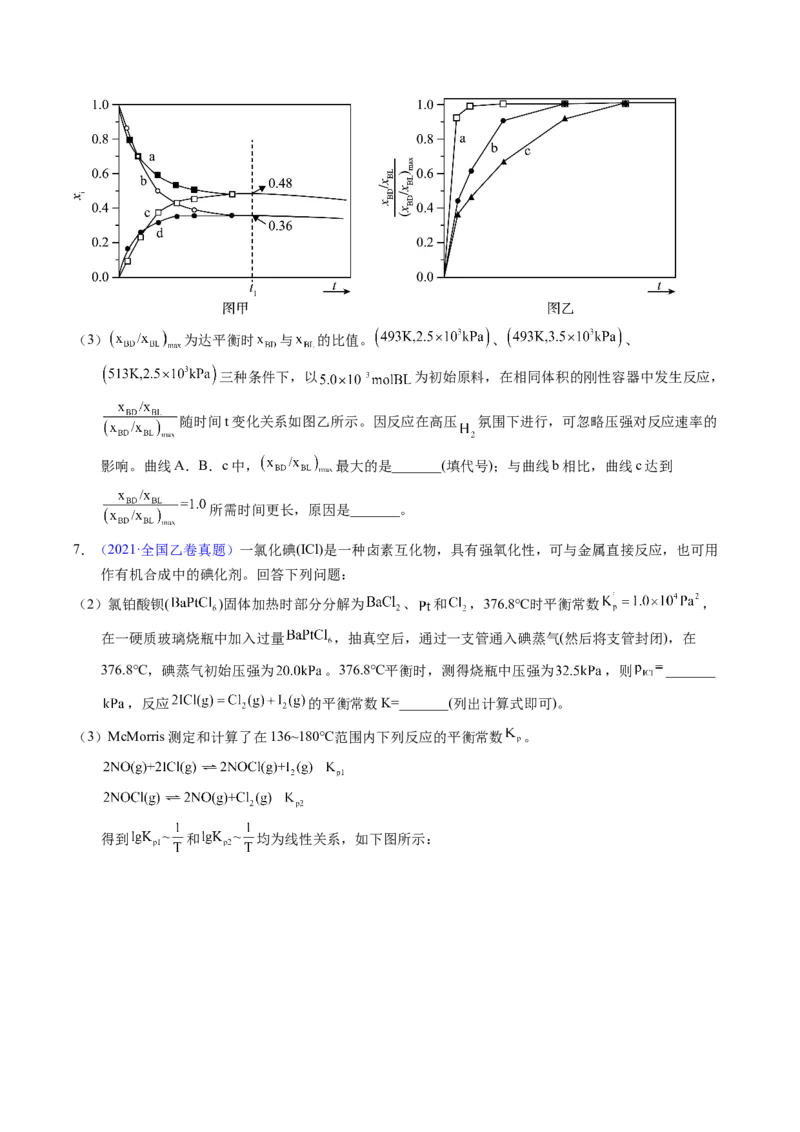
两位有效数字)。(3) 为达平衡时 与 的比值。 、 、
三种条件下,以 为初始原料,在相同体积的刚性容器中发生反应,
随时间t变化关系如图乙所示。因反应在高压 氛围下进行,可忽略压强对反应速率的
影响。曲线A.B.c中, 最大的是_______(填代号);与曲线b相比,曲线c达到
所需时间更长,原因是_______。
7.(2021·全国乙卷真题)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用
作有机合成中的碘化剂。回答下列问题:
(2)氯铂酸钡( )固体加热时部分分解为 、 和 ,376.8℃时平衡常数 ,
在一硬质玻璃烧瓶中加入过量 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在
376.8℃,碘蒸气初始压强为 。376.8℃平衡时,测得烧瓶中压强为 ,则 _______
,反应 的平衡常数K=_______(列出计算式即可)。
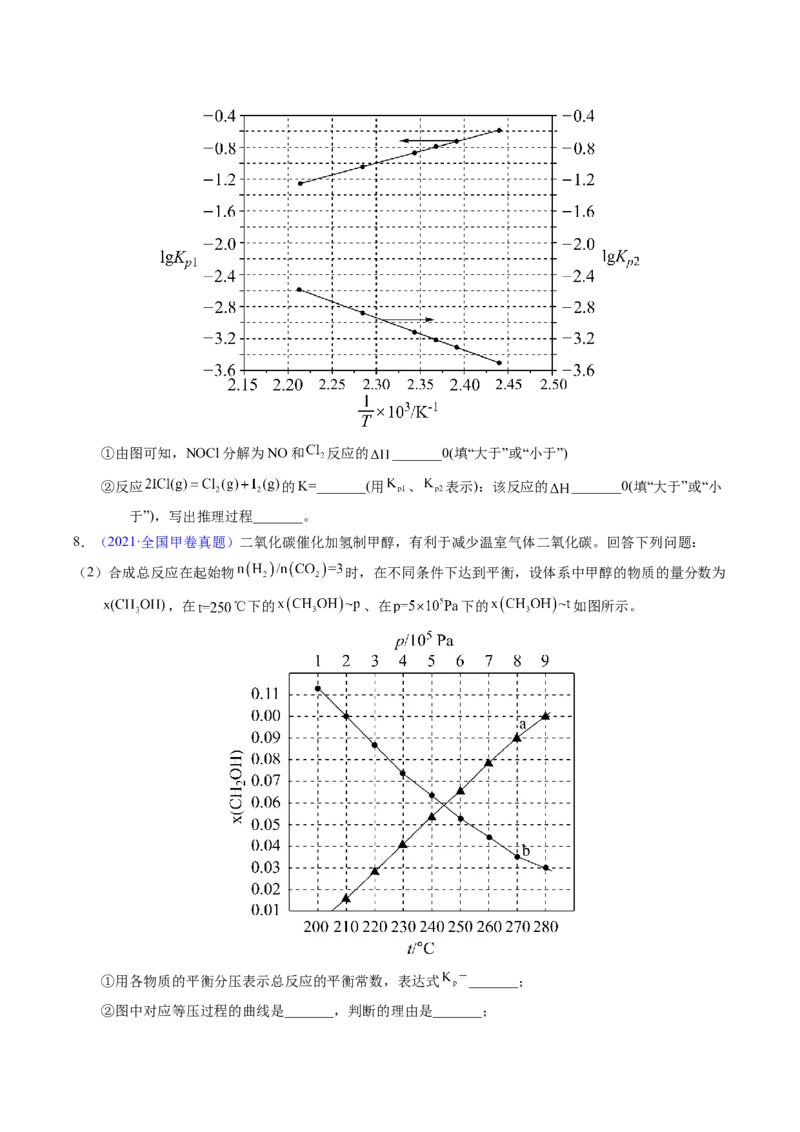
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
得到 和 均为线性关系,如下图所示:①由图可知,NOCl分解为NO和 反应的 _______0(填“大于”或“小于”)
②反应 的K=_______(用 、 表示):该反应的 _______0(填“大于”或“小
于”),写出推理过程_______。
8.(2021·全国甲卷真题)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
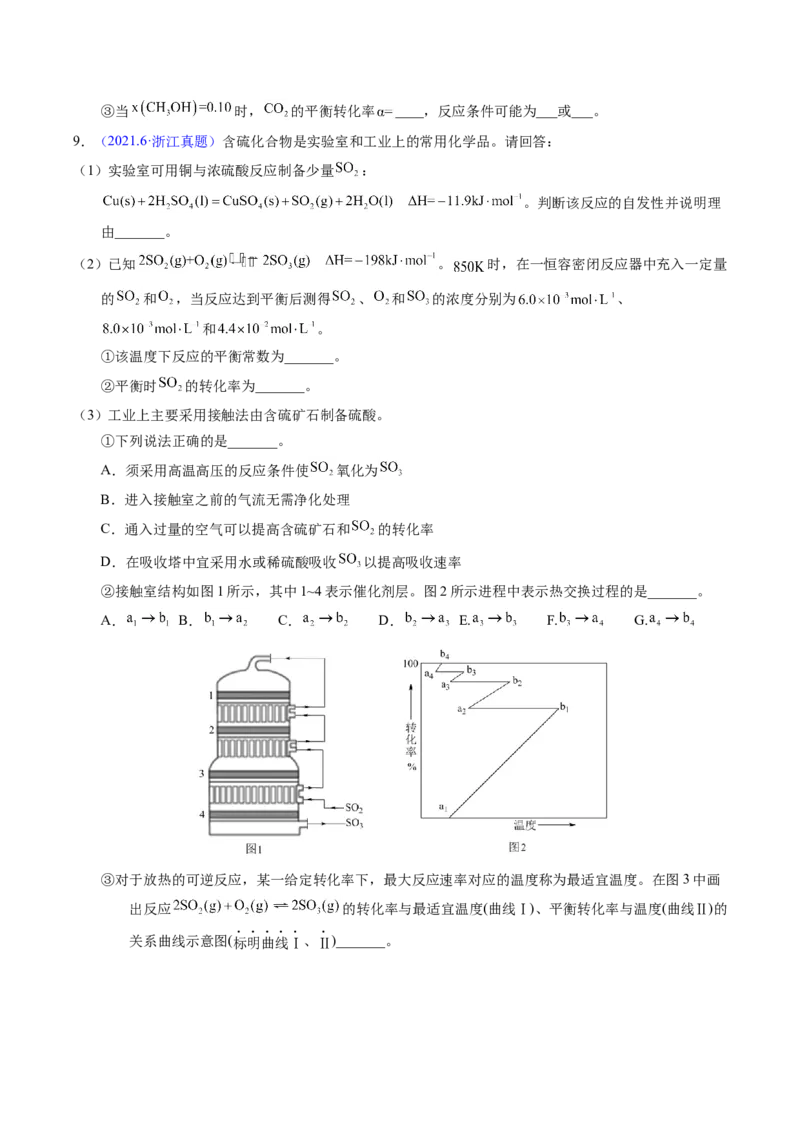
(2)合成总反应在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
,在 ℃下的 、在 下的 如图所示。
①用各物质的平衡分压表示总反应的平衡常数,表达式 _______;
②图中对应等压过程的曲线是_______,判断的理由是_______;③当 时, 的平衡转化率 ____,反应条件可能为___或___。
9.(2021.6·浙江真题)含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
。判断该反应的自发性并说明理
由_______。
(2)已知 。 时,在一恒容密闭反应器中充入一定量
的 和 ,当反应达到平衡后测得 、 和 的浓度分别为 、
和 。
①该温度下反应的平衡常数为_______。
②平衡时 的转化率为_______。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法正确的是_______。
A.须采用高温高压的反应条件使 氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是_______。
A. B. C. D. E. F. G.
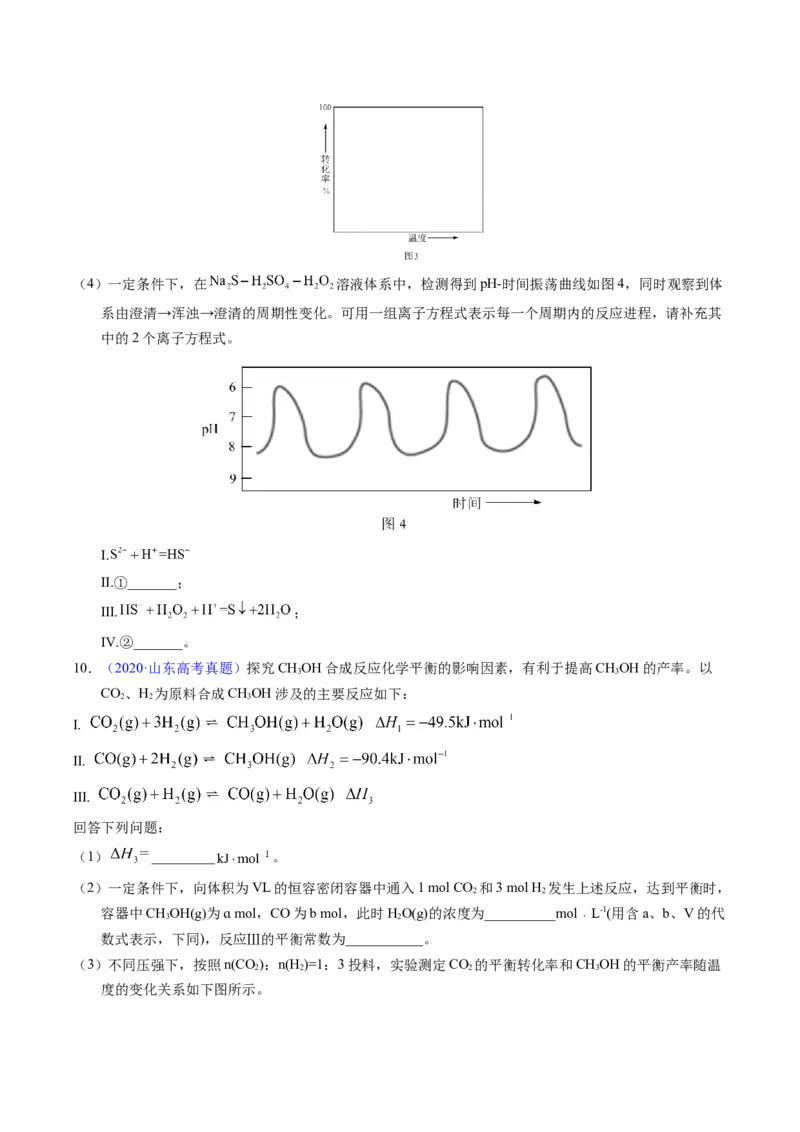
③对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在图3中画
出反应 的转化率与最适宜温度(曲线Ⅰ)、平衡转化率与温度(曲线Ⅱ)的
关系曲线示意图(标明曲线Ⅰ、Ⅱ)_______。(4)一定条件下,在 溶液体系中,检测得到pH-时间振荡曲线如图4,同时观察到体
系由澄清→浑浊→澄清的周期性变化。可用一组离子方程式表示每一个周期内的反应进程,请补充其
中的2个离子方程式。
Ⅰ.
Ⅱ.①_______;
Ⅲ. ;
Ⅳ.②_______。
10.(2020·山东高考真题)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以
3 3
CO、H 为原料合成CHOH涉及的主要反应如下:
2 2 3
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1) _________ 。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为ɑ mol,CO为b mol,此时HO(g)的浓度为__________mol﹒L-1(用含a、b、V的代
3 2
数式表示,下同),反应Ⅲ的平衡常数为___________。
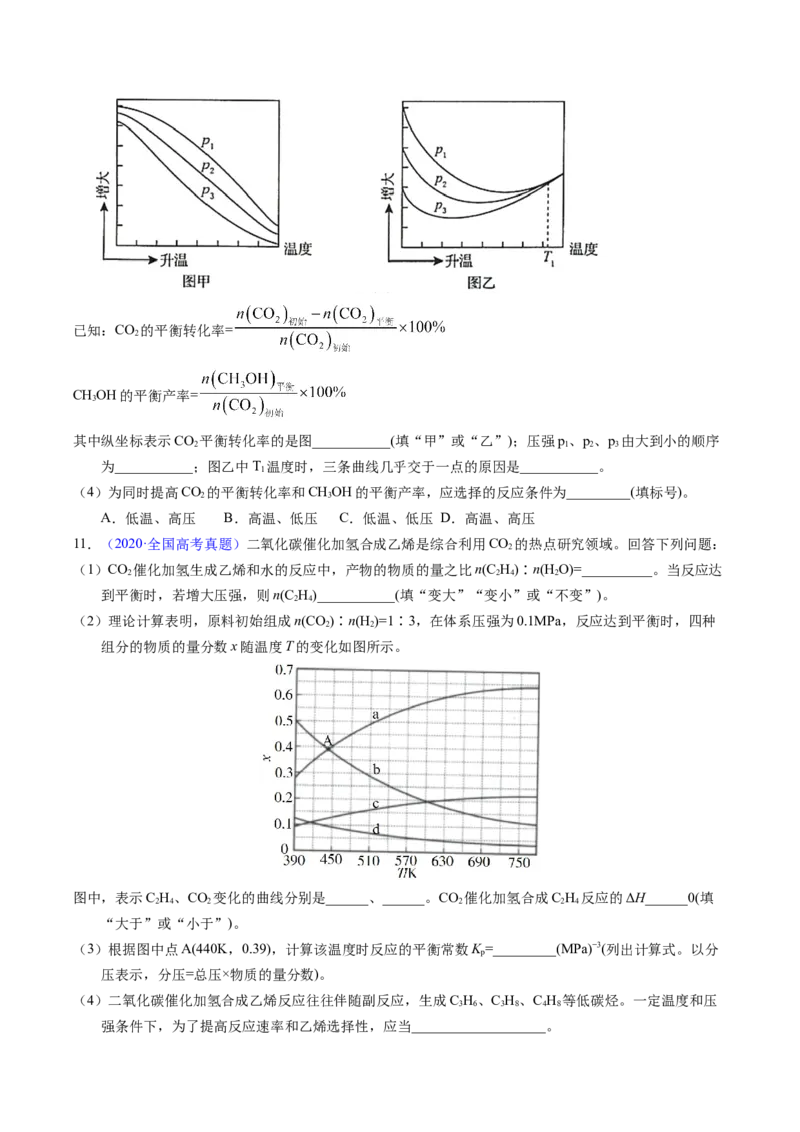
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温
2 2 2 3
度的变化关系如下图所示。已知:CO 的平衡转化率=
2
CHOH的平衡产率=
3
其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序
2 1 2 3
为___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为_________(填标号)。
2 3
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压
11.(2020·全国高考真题)二氧化碳催化加氢合成乙烯是综合利用CO 的热点研究领域。回答下列问题:
2
(1)CO 催化加氢生成乙烯和水的反应中,产物的物质的量之比n(C H)∶n(H O)=__________。当反应达
2 2 4 2
到平衡时,若增大压强,则n(C H)___________(填“变大”“变小”或“不变”)。
2 4
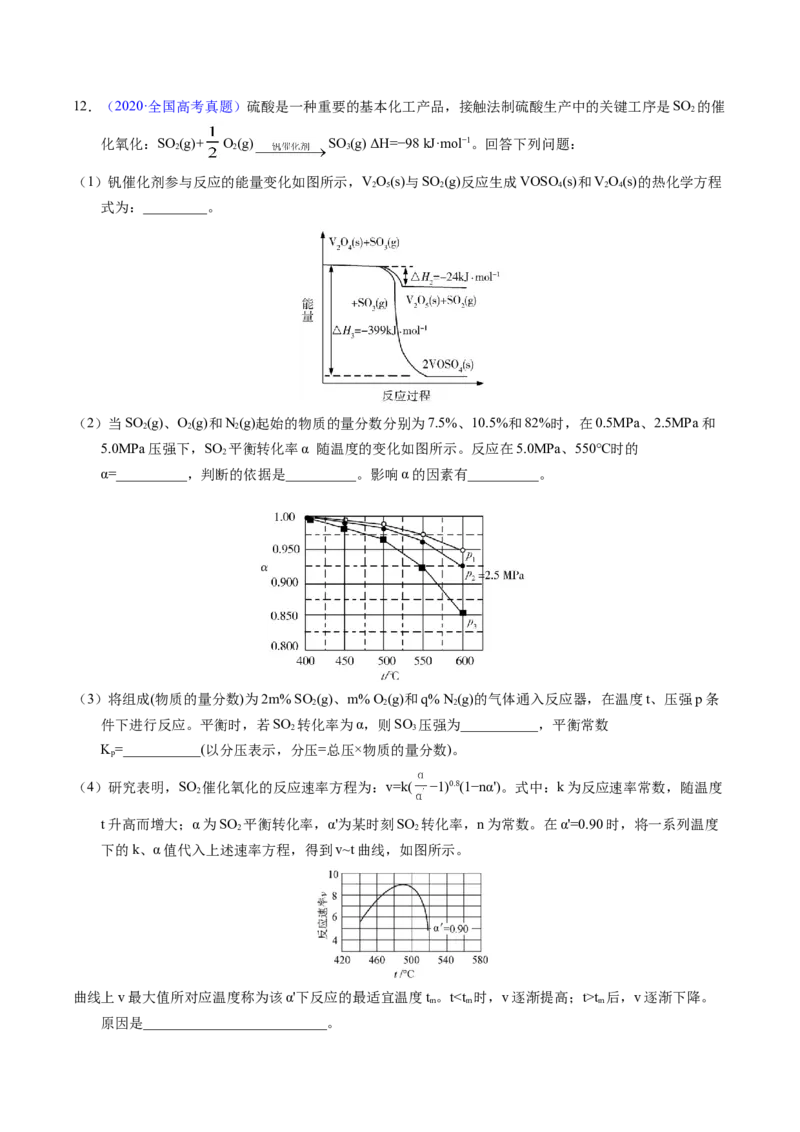
(2)理论计算表明,原料初始组成n(CO)∶n(H )=1∶3,在体系压强为0.1MPa,反应达到平衡时,四种
2 2
组分的物质的量分数x随温度T的变化如图所示。
图中,表示C H、CO 变化的曲线分别是______、______。CO 催化加氢合成C H 反应的ΔH______0(填
2 4 2 2 2 4
“大于”或“小于”)。
(3)根据图中点A(440K,0.39),计算该温度时反应的平衡常数K =_________(MPa)−3(列出计算式。以分
p
压表示,分压=总压×物质的量分数)。
(4)二氧化碳催化加氢合成乙烯反应往往伴随副反应,生成C H、C H、C H 等低碳烃。一定温度和压
3 6 3 8 4 8
强条件下,为了提高反应速率和乙烯选择性,应当___________________。12.(2020·全国高考真题)硫酸是一种重要的基本化工产品,接触法制硫酸生产中的关键工序是SO 的催
2
化氧化:SO (g)+ O(g) SO (g) ΔH=−98 kJ·mol−1。回答下列问题:
2 2 3
(1)钒催化剂参与反应的能量变化如图所示,VO(s)与SO (g)反应生成VOSO(s)和VO(s)的热化学方程
2 5 2 4 2 4
式为:_________。
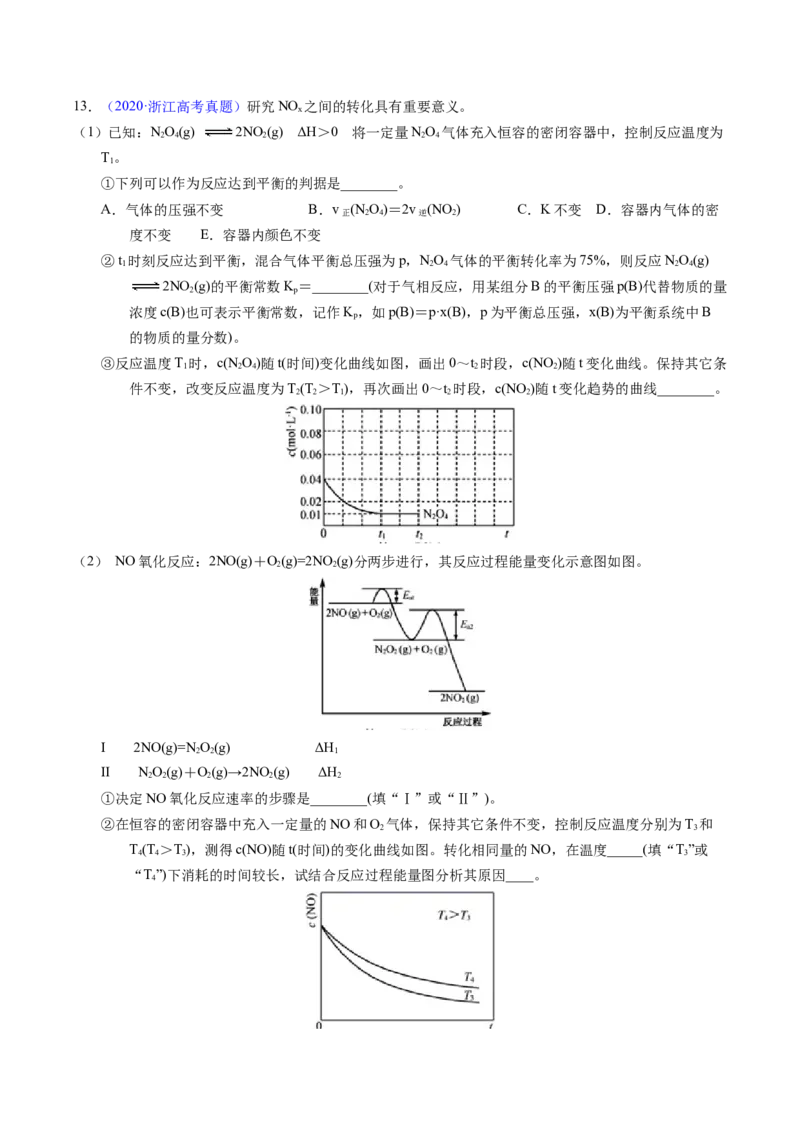
(2)当SO (g)、O(g)和N(g)起始的物质的量分数分别为7.5%、10.5%和82%时,在0.5MPa、2.5MPa和
2 2 2
5.0MPa压强下,SO 平衡转化率α 随温度的变化如图所示。反应在5.0MPa、550℃时的
2
α=__________,判断的依据是__________。影响α的因素有__________。
(3)将组成(物质的量分数)为2m% SO (g)、m% O (g)和q% N (g)的气体通入反应器,在温度t、压强p条
2 2 2
件下进行反应。平衡时,若SO 转化率为α,则SO 压强为___________,平衡常数
2 3
K=___________(以分压表示,分压=总压×物质的量分数)。
p
(4)研究表明,SO 催化氧化的反应速率方程为:v=k( −1)0.8(1−nα')。式中:k为反应速率常数,随温度
2
t升高而增大;α为SO 平衡转化率,α'为某时刻SO 转化率,n为常数。在α'=0.90时,将一系列温度
2 2
下的k、α值代入上述速率方程,得到v~t曲线,如图所示。
曲线上v最大值所对应温度称为该α'下反应的最适宜温度t 。tt 后,v逐渐下降。
m m m
原因是__________________________。13.(2020·浙江高考真题)研究NO 之间的转化具有重要意义。
x
(1)已知:NO(g) 2NO (g) ΔH>0 将一定量NO 气体充入恒容的密闭容器中,控制反应温度为
2 4 2 2 4
T。
1
①下列可以作为反应达到平衡的判据是________。
A.气体的压强不变 B.v (N O)=2v (NO ) C.K不变 D.容器内气体的密
正 2 4 逆 2
度不变 E.容器内颜色不变
②t 时刻反应达到平衡,混合气体平衡总压强为p,NO 气体的平衡转化率为75%,则反应NO(g)
1 2 4 2 4
2NO (g)的平衡常数K=________(对于气相反应,用某组分B的平衡压强p(B)代替物质的量
2 p
浓度c(B)也可表示平衡常数,记作K,如p(B)=p·x(B),p为平衡总压强,x(B)为平衡系统中B
p
的物质的量分数)。
③反应温度T 时,c(NO)随t(时间)变化曲线如图,画出0~t 时段,c(NO )随t变化曲线。保持其它条
1 2 4 2 2
件不变,改变反应温度为T(T >T),再次画出0~t 时段,c(NO )随t变化趋势的曲线________。
2 2 1 2 2
(2) NO氧化反应:2NO(g)+O(g)=2NO (g)分两步进行,其反应过程能量变化示意图如图。
2 2
Ⅰ 2NO(g)=N O(g) ΔH
2 2 1
Ⅱ N O(g)+O(g)→2NO (g) ΔH
2 2 2 2 2
①决定NO氧化反应速率的步骤是________(填“Ⅰ”或“Ⅱ”)。
②在恒容的密闭容器中充入一定量的NO和O 气体,保持其它条件不变,控制反应温度分别为T 和
2 3
T(T >T),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度_____(填“T”或
4 4 3 3
“T”)下消耗的时间较长,试结合反应过程能量图分析其原因____。
414.(2019·全国高考真题)水煤气变换[CO(g)+H O(g)=CO(g)+H(g)]是重要的化工过程,主要用于合成氨、
2 2 2
制氢以及合成气加工等工业领域中。回答下列问题:
(1)Shibata曾做过下列实验:①使纯H 缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还
2
原为金属钴(Co),平衡后气体中H 的物质的量分数为0.0250。
2
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192。
根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO_________H (填“大于”或“小于”)。
2
(2)721 ℃时,在密闭容器中将等物质的量的CO(g)和HO(g)混合,采用适当的催化剂进行反应,则平衡
2
时体系中H 的物质的量分数为_________(填标号)。
2
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
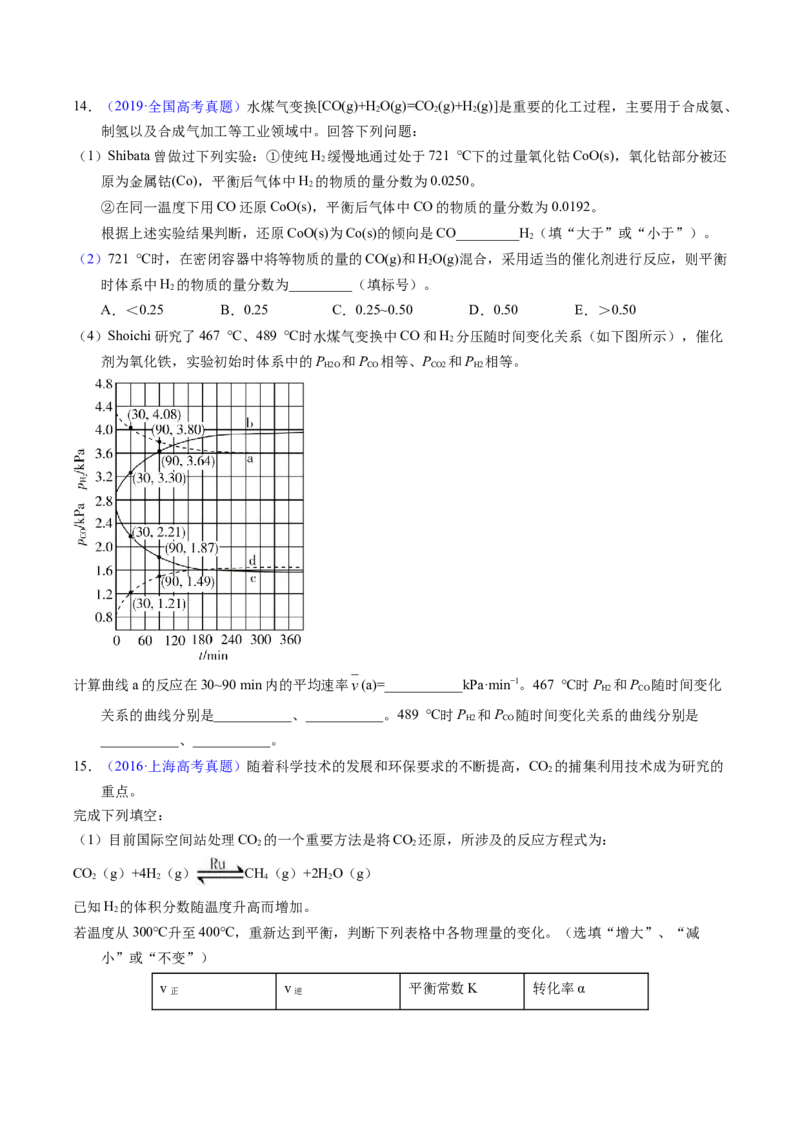
(4)Shoichi研究了467 ℃、489 ℃时水煤气变换中CO和H 分压随时间变化关系(如下图所示),催化
2
剂为氧化铁,实验初始时体系中的P 和P 相等、P 和P 相等。
H2O CO CO2 H2
计算曲线a的反应在30~90 min内的平均速率 (a)=___________kPa·min−1。467 ℃时P 和P 随时间变化
H2 CO
关系的曲线分别是___________、___________。489 ℃时P 和P 随时间变化关系的曲线分别是
H2 CO
___________、___________。
15.(2016·上海高考真题)随着科学技术的发展和环保要求的不断提高,CO 的捕集利用技术成为研究的
2
重点。
完成下列填空:
(1)目前国际空间站处理CO 的一个重要方法是将CO 还原,所涉及的反应方程式为:
2 2
CO(g)+4H (g) CH(g)+2H O(g)
2 2 4 2
已知H 的体积分数随温度升高而增加。
2
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减
小”或“不变”)
v v 平衡常数K 转化率α
正 逆(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO]/mol·L-1 [H ]/mol·L-1 [CH]/mol·L-1 [H O]/mol·L-1
2 2 4 2
平衡Ⅰ a b c d
平衡Ⅱ m n x y
a、b、c、d与m、n、x、y之间的关系式为_________。
(3)碳酸:HCO,K =4.3×10-7,K =5.6×10-11
2 3 i1 i2
草酸:HC O,K =5.9×10-2,K =6.4×10-5
2 2 4 i1 i2
0.1 mol/L Na CO 溶液的pH____________0.1 mol/L Na C O 溶液的pH。(选填“大于”、“小于”或“等
2 3 2 2 4
于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___________。
若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是_____。(选填
编号)
a.[H+]>[HC O-]>[HCO -]>[CO2-]
2 4 3 3
B.[HCO -]>[HC O-]>[C O2-]>[CO2-]
3 2 4 2 4 3
c.[H+]>[HC O-]>[C O2-]>[CO2-]
2 4 2 4 3
D.[H CO] >[HCO -]>[HC O-]>[CO2-]
2 3 3 2 4 3
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++ HCO - HCO,当有少量酸性或碱性物质进入血
3 2 3
液中时,血液的pH变化不大,用平衡移动原理解释上述现象。
____________________________________________________________________________________
16.(2008·宁夏高考真题)已知可逆反应:M(g)+N(g) P(g)+Q(g);△H>0,
请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c(M)=1 mol·L-1, c(N)=2.4mol·L-1,达到平衡后,M的转化率
为60%,此时N的转化率为__________。
(2)若反应温度升高,M的转化率______(填“增大”“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为:c(M)= 4 mol·L-1,c(N)=amol·L-1;达到平衡后,c(P)=2
mol·L-1,a=________。
(4)若反应温度不变,反应物的起始浓度为:c(M)=c(N)= bmol·L-1,达到平衡后,M的转化率为
_____________。
17.(2007·上海高考真题)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催
化剂为Cu O/ZnO):CO(g)+2H(g) CHOH(g)。
2 2 3根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=_______________,升高温度,K值_______(填“增大”、
“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H )=_____________。
2
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的
是_______:
a.氢气的浓度减少 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H )/n(CHOH)增大
2 3
(4)据研究,反应过程中起催化作用的为Cu O,反应体系中含少量CO 有利于维持催化剂Cu O的量不
2 2 2
变,原因是:_______________________(用化学方程式表示)。
18.(2014·全国高考真题)在容积为1.00L的容器中,通入一定量的NO,发生反应NO(g)
2 4 2 4
2NO (g),随温度升高,混合气体的颜色变深。
2
回答下列问题:
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。
在0~60s时段,反应速率v(N O)为___________mol·L-1·s-1反应的平衡常数K 为___________。
2 4 1
(2)100℃时达到平衡后,改变反应温度为T,c(NO)以0.0020 mol·L-1·s-1的平均速率降低,经10s又达到
2 4
平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K___________
2
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反
应”)方向移动,判断理由是___________。19.(2011·上海高考真题)自然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,
压强增大约25000~30000 kPa。在地壳内SiO
2
和HF存在以下平衡:SiO
2
(s) +4HF(g)⇌SiF
4
(g)+ 2H
2
O(g)
+148.9 kJ。根据题意完成下列填空:
(1)在地壳深处容易有_____________气体逸出,在地壳浅处容易有___________沉积。
(2)如果上述反应的平衡常数K值变大,该反应_____________(选填编号)。
A.一定向正反应方向移动 B.在平衡移动时正反应速率先增大后减小
C.一定向逆反应方向移动 D.在平衡移动时逆反应速率先减小后增大
(3)如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时,________(选填编号)。
A.2v (HF)=v (H O) B.v(H O)=2v(SiF)
正 逆 2 2 4
C.SiO 的质量保持不变 D.反应物不再转化为生成物
2
(4)若反应的容器容积为2.0L,反应时间8.0 min,容器内气体的密度增大了0.12 g/L,在这段时间内HF
的平均反应速率为____________。
20.(2012·上海高考真题)用氮化硅(Si N)陶瓷代替金属制造发动机的耐热部件,能大幅度提高发动机的
3 4
热效率。工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl (g)+2N(g)+6H(g) Si N(s)
4 2 2 3 4
+12HCl(g)+Q(Q>0)。完成下列填空:
(1)在一定温度下进行上述反应,若反应容器的容积为2 L,3 min后达到平衡,测得固体的质量增加了
2.80 g,则H 的平均反应速率___ mol/(L·min);该反应的平衡常数表达式K=_____
2
(2)上述反应达到平衡后,下列说法正确的是_____。
a.其他条件不变,压强增大,平衡常数K减小
b.其他条件不变,温度升高,平衡常数K减小
c.其他条件不变,增大Si N 物质的量平衡向左移动
3 4
d.其他条件不变,增大HCl物质的量平衡向左移动
(3)一定条件下,在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是__。
a.3v (N )=v (H ) b.v (HCl)=4v (SiCl )
逆 2 正 2 正 正 4
c.混合气体密度保持不变 d.c(N ):c(H ):c(HCl)=1:3:6
2 2
(4)若平衡时H 和HCl的物质的量之比为 ,保持其它条件不变,降低温度后达到新的平衡时,H 和
2 2
HCl的物质的量之比___ (填“>”、“=”或“<”)。
21.(2015·全国高考真题)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO
2
和H)在催化剂的作用下合成甲醇,发生的主反应如下:
2
①CO(g)+2H (g) CHOH(g) △H
2 3 1
②CO(g)+3H (g) CHOH(g)+H O(g) △H
2 2 3 2 2
③CO(g)+H (g) CO(g)+H O(g) △H
2 2 2 3
回答下列问题:(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H=__kJ·mol-1,已知△H=-58kJ·mol-1,则△H=__kJ·mol-1。
1 2 3
(2)反应①的化学平衡常数K的表达式为__________;图1中能正确反映平衡常数K随温度变化关系的
曲线为_________(填曲线标记字母),其判断理由是_________________。
(3)合成气的组成n(H)/n(CO+CO)=2.60时,体系中的CO平衡转化率(α)与温度和压强的关系
2 2
如图2所示。α(CO)值随温度升高而_______(填“增大”或“减小”),其原因是_______。图2
中的压强由大到小为_____,其判断理由是_____。
22.(2011·全国高考真题)反应aA(g)+bB(g) cC(g)( H<0)在等容条件下进行。改
变其他反应条件,在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示:
回答问题:
(1)反应的化学方程式中,a:b:c为 ;
(2)A的平均反应速率 (A)、 (A)、 (A)从大到小排列次序为 ;
(3)B的平衡转化率 中最小的是 ,其值是 ;(4)由第一次平衡到第二次平衡,平衡移动的方向是 ,采取的措施是
;
(5)比较第II阶段反应温度( )和第III阶段反应速度( )的高低:
填“>、=、<”判断的理由是 ;
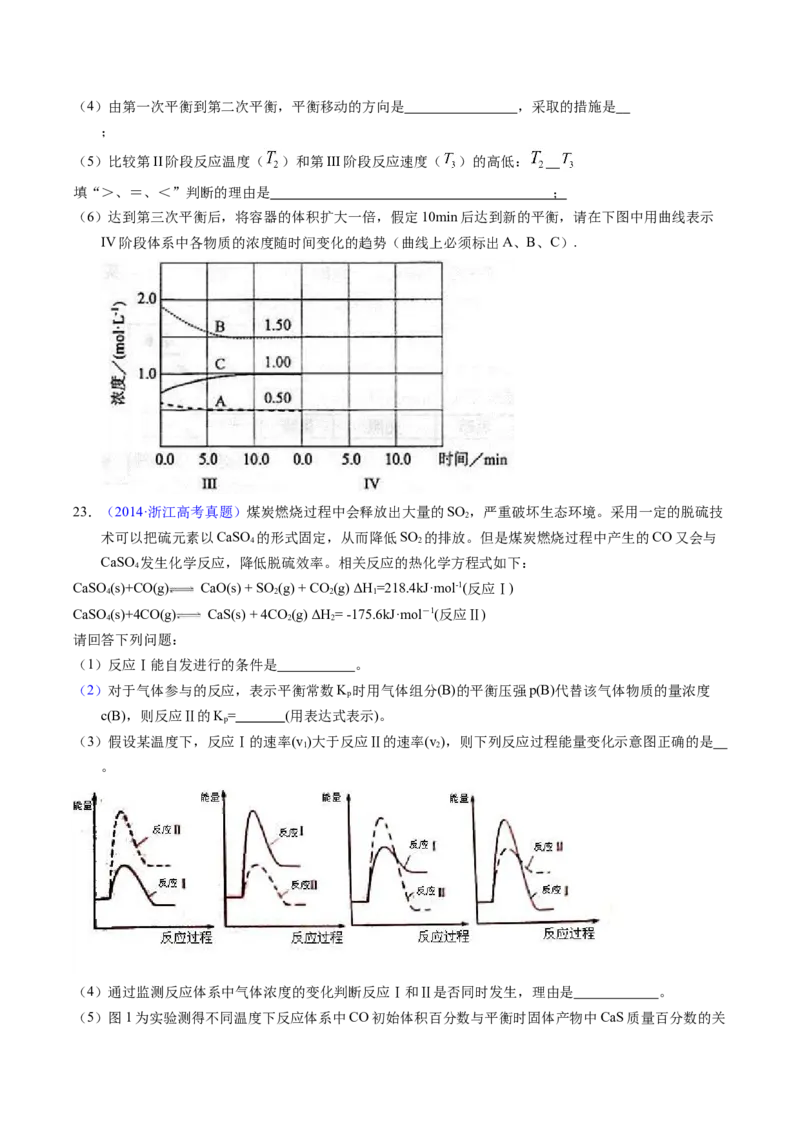
(6)达到第三次平衡后,将容器的体积扩大一倍,假定10min后达到新的平衡,请在下图中用曲线表示
IV阶段体系中各物质的浓度随时间变化的趋势(曲线上必须标出A、B、C).
23.(2014·浙江高考真题)煤炭燃烧过程中会释放出大量的SO ,严重破坏生态环境。采用一定的脱硫技
2
术可以把硫元素以CaSO 的形式固定,从而降低SO 的排放。但是煤炭燃烧过程中产生的CO又会与
4 2
CaSO 发生化学反应,降低脱硫效率。相关反应的热化学方程式如下:
4
CaSO(s)+CO(g) CaO(s) + SO (g) + CO (g) ΔH =218.4kJ·mol-1(反应Ⅰ)
4 2 2 1
CaSO(s)+4CO(g) CaS(s) + 4CO (g) ΔH = -175.6kJ·mol-1(反应Ⅱ)
4 2 2
请回答下列问题:
(1)反应Ⅰ能自发进行的条件是 。
(2)对于气体参与的反应,表示平衡常数K 时用气体组分(B)的平衡压强p(B)代替该气体物质的量浓度
p
c(B),则反应Ⅱ的K= (用表达式表示)。
p
(3)假设某温度下,反应Ⅰ的速率(v)大于反应Ⅱ的速率(v),则下列反应过程能量变化示意图正确的是
1 2
。
(4)通过监测反应体系中气体浓度的变化判断反应Ⅰ和Ⅱ是否同时发生,理由是 。
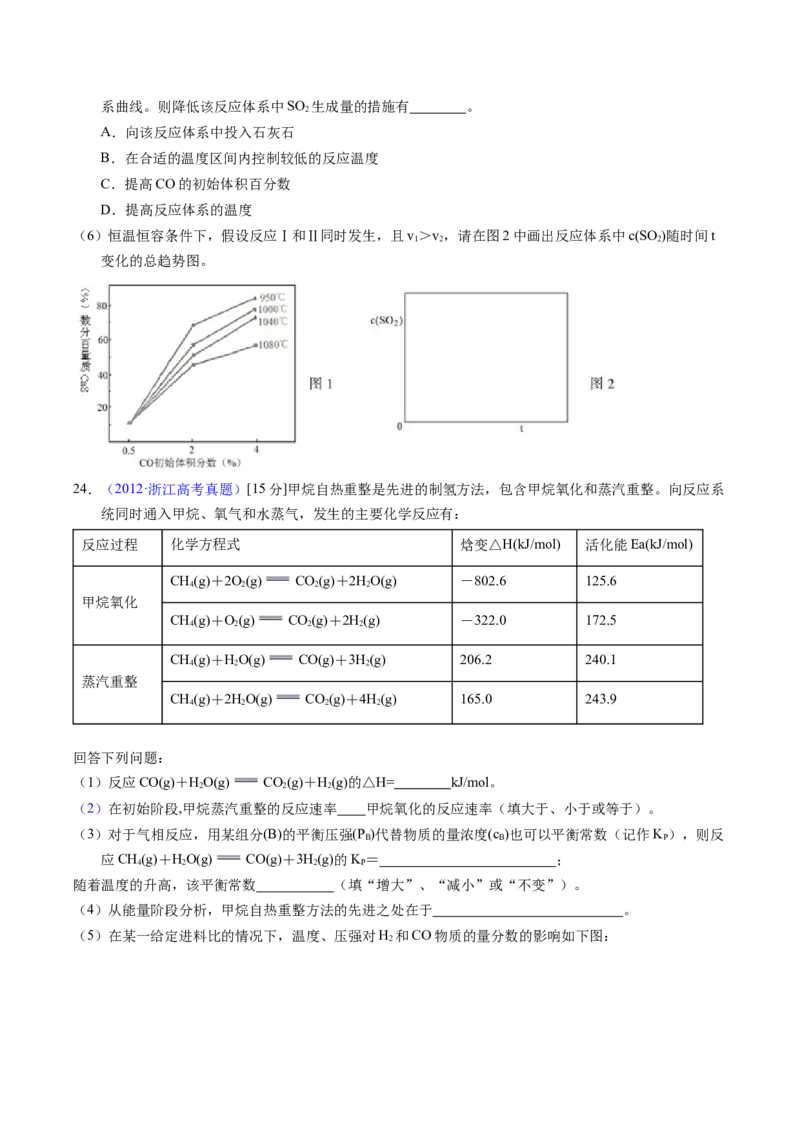
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO 生成量的措施有 。
2
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v>v,请在图2中画出反应体系中c(SO )随时间t
1 2 2
变化的总趋势图。
24.(2012·浙江高考真题)[15分]甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸汽重整。向反应系
统同时通入甲烷、氧气和水蒸气,发生的主要化学反应有:
反应过程 化学方程式 焓变△H(kJ/mol) 活化能Ea(kJ/mol)
CH(g)+2O(g) CO(g)+2HO(g) -802.6 125.6
4 2 2 2
甲烷氧化
CH(g)+O(g) CO(g)+2H(g) -322.0 172.5
4 2 2 2
CH(g)+HO(g) CO(g)+3H(g) 206.2 240.1
4 2 2
蒸汽重整
CH(g)+2HO(g) CO(g)+4H(g) 165.0 243.9
4 2 2 2
回答下列问题:
(1)反应CO(g)+HO(g) CO(g)+H(g)的△H= kJ/mol。
2 2 2
(2)在初始阶段,甲烷蒸汽重整的反应速率 甲烷氧化的反应速率(填大于、小于或等于)。
(3)对于气相反应,用某组分(B)的平衡压强(P )代替物质的量浓度(c )也可以平衡常数(记作K ),则反
B B P
应CH(g)+HO(g) CO(g)+3H(g)的K = ;
4 2 2 P
随着温度的升高,该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量阶段分析,甲烷自热重整方法的先进之处在于 。
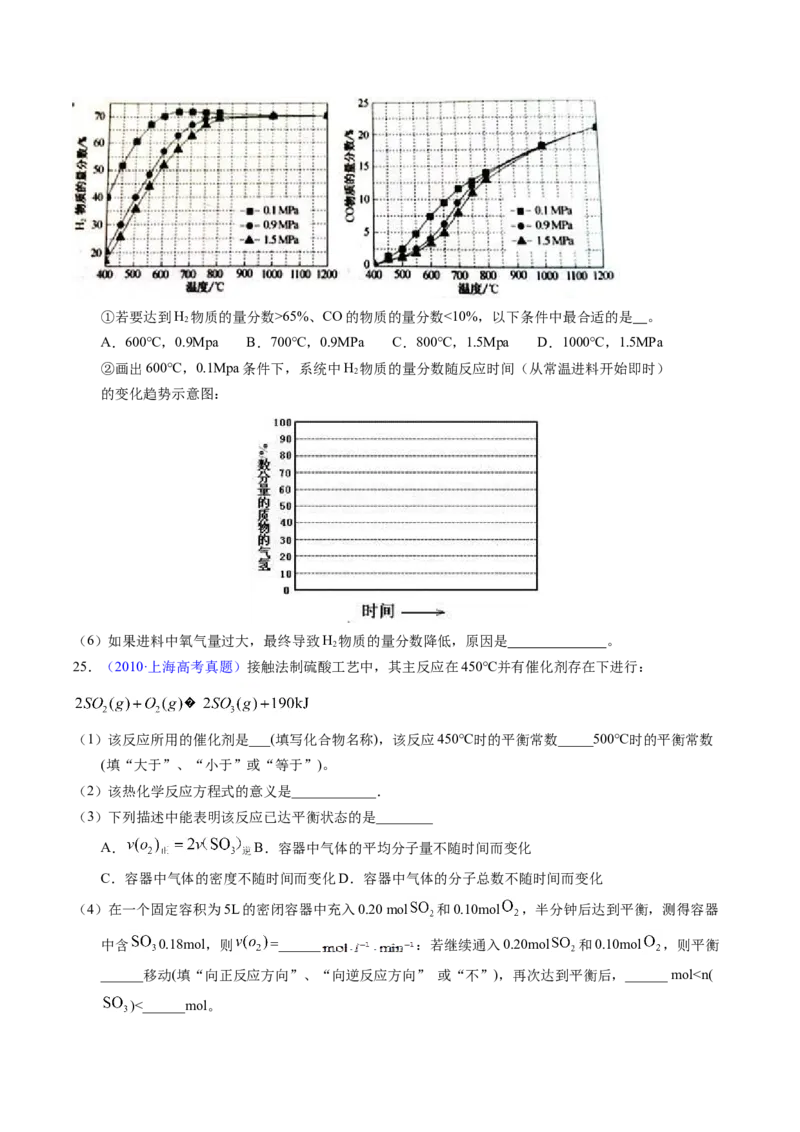
(5)在某一给定进料比的情况下,温度、压强对H 和CO物质的量分数的影响如下图:
2①若要达到H 物质的量分数>65%、CO的物质的量分数<10%,以下条件中最合适的是 。
2
A.600℃,0.9Mpa B.700℃,0.9MPa C.800℃,1.5Mpa D.1000℃,1.5MPa
②画出600℃,0.1Mpa条件下,系统中H 物质的量分数随反应时间(从常温进料开始即时)
2
的变化趋势示意图:
(6)如果进料中氧气量过大,最终导致H 物质的量分数降低,原因是 。
2
25.(2010·上海高考真题)接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
(1)该反应所用的催化剂是___(填写化合物名称),该反应450℃时的平衡常数_____500℃时的平衡常数
(填“大于”、“小于”或“等于”)。
(2)该热化学反应方程式的意义是____________.
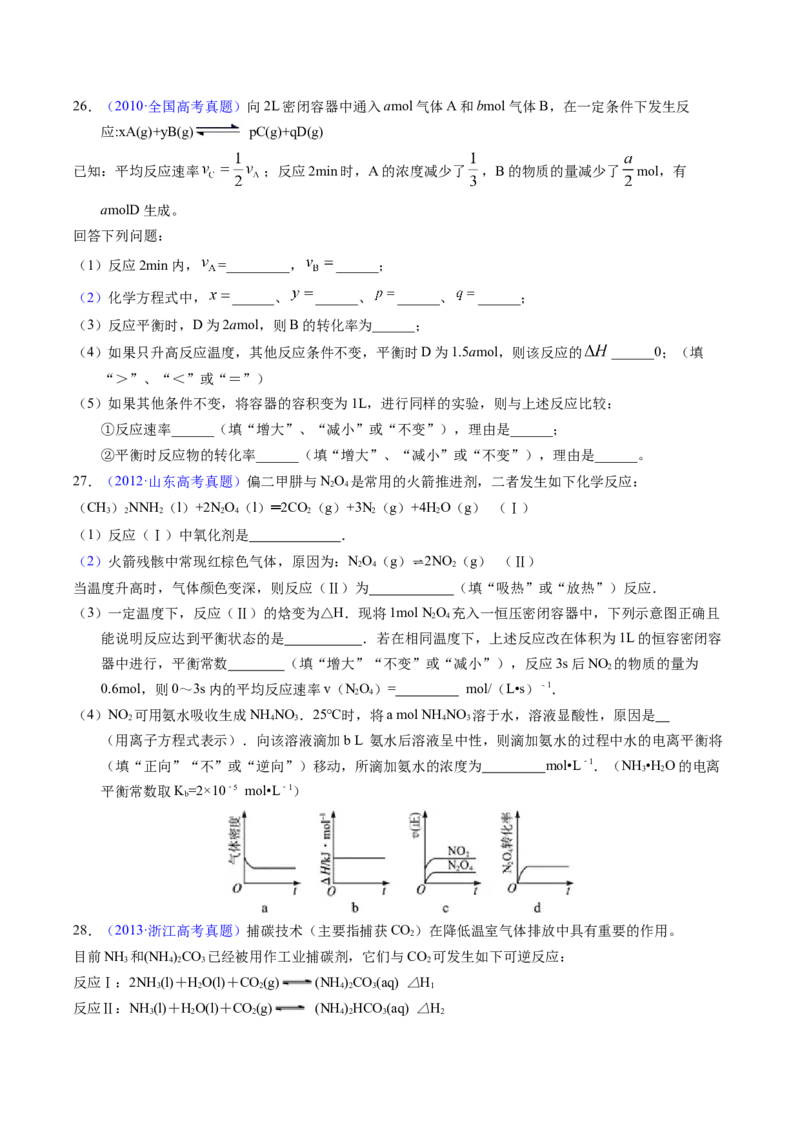
(3)下列描述中能表明该反应已达平衡状态的是________
A. B.容器中气体的平均分子量不随时间而变化
C.容器中气体的密度不随时间而变化D.容器中气体的分子总数不随时间而变化
(4)在一个固定容积为5L的密闭容器中充入0.20 mol 和0.10mol ,半分钟后达到平衡,测得容器
中含 0.18mol,则 =______ :若继续通入0.20mol 和0.10mol ,则平衡
______移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,______ mol