文档内容
专题 64 原理综合题——反应热+化学平
衡
1.【2023年全国甲卷】甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
反应③ 的 ,平衡常数 (用 表
示)。
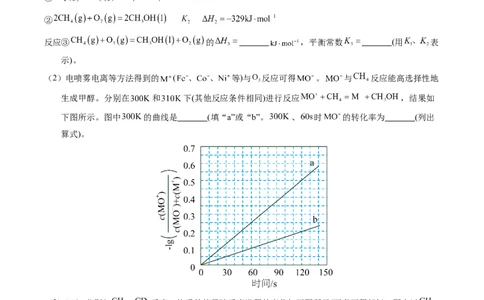
(2)电喷雾电离等方法得到的 ( 等)与 反应可得 。 与 反应能高选择性地
生成甲醇。分别在 和 下(其他反应条件相同)进行反应 ,结果如
下图所示。图中 的曲线是 (填“a”或“b”。 、 时 的转化率为 (列出
算式)。
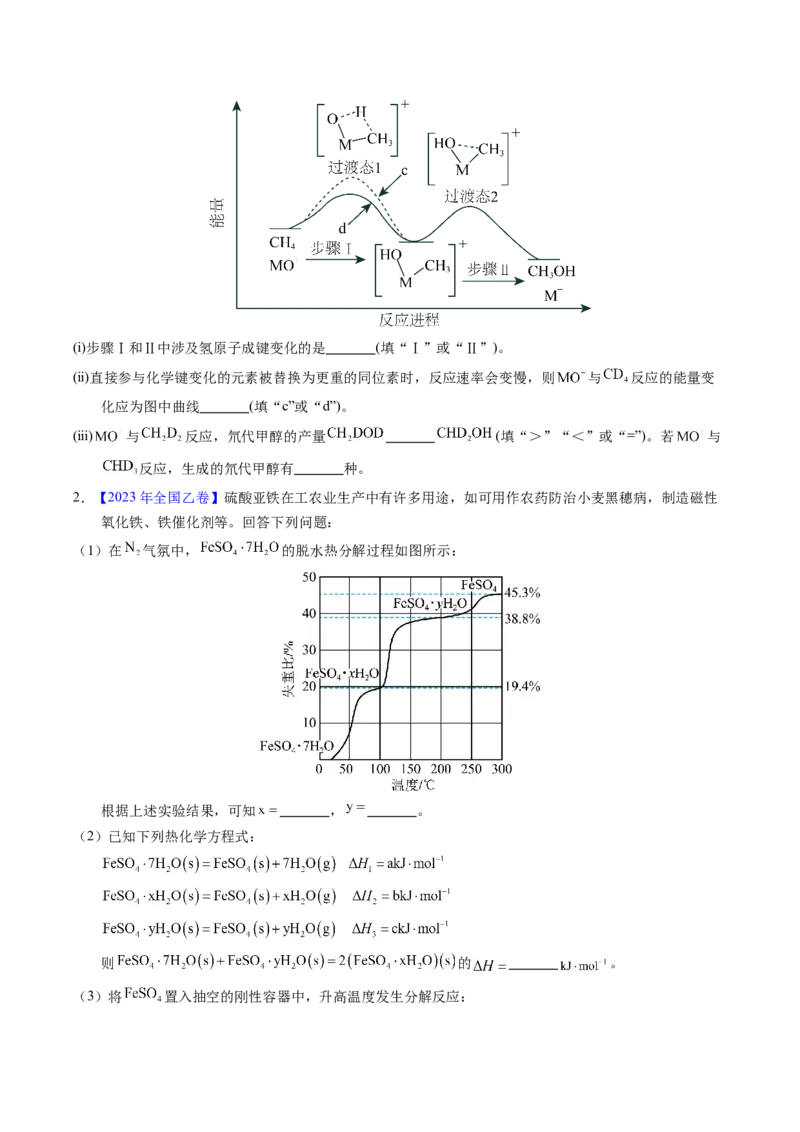
(3) 分别与 反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以
示例)。(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则 与 反应的能量变
化应为图中曲线 (填“c”或“d”)。
(ⅲ) 与 反应,氘代甲醇的产量 (填“>”“<”或“=”)。若 与
反应,生成的氘代甲醇有 种。
2.【2023年全国乙卷】硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性
氧化铁、铁催化剂等。回答下列问题:
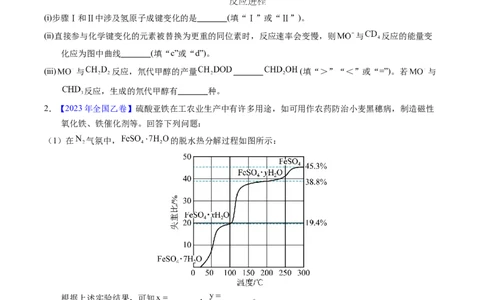
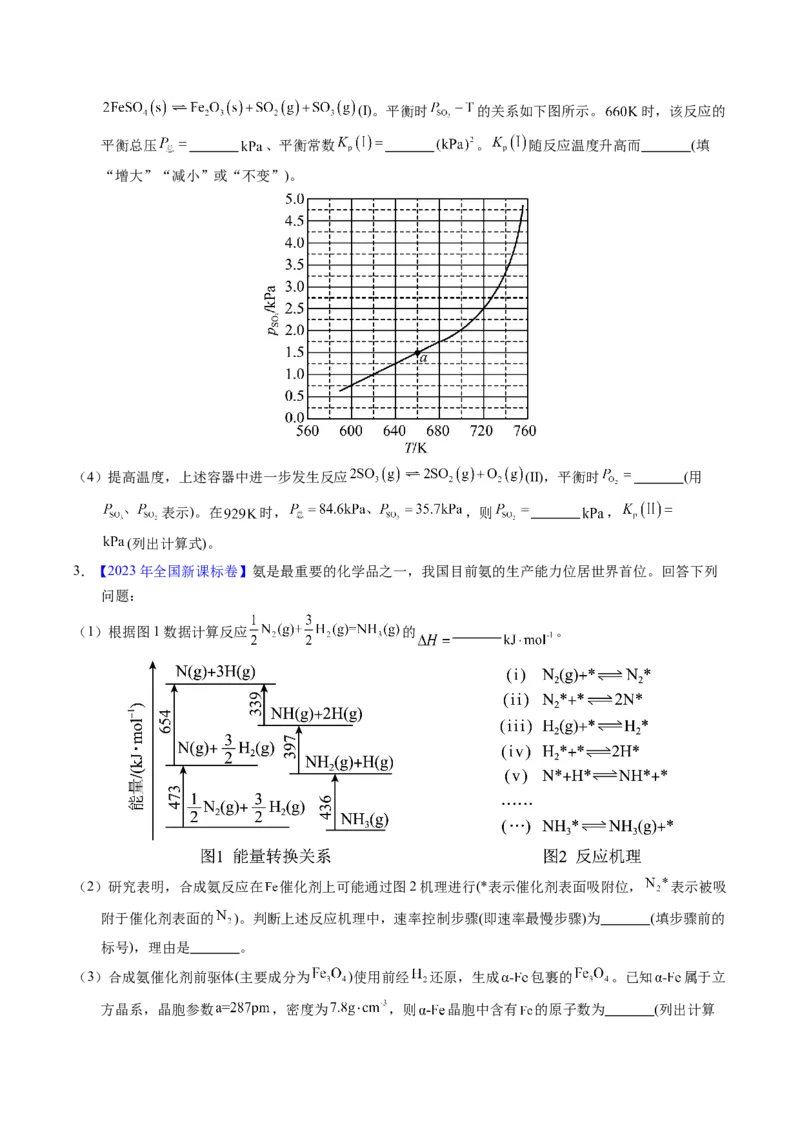
(1)在 气氛中, 的脱水热分解过程如图所示:
根据上述实验结果,可知 , 。
(2)已知下列热化学方程式:
则 的 。
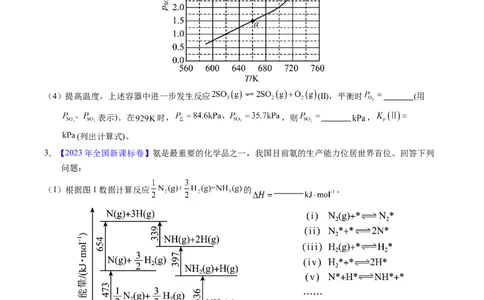
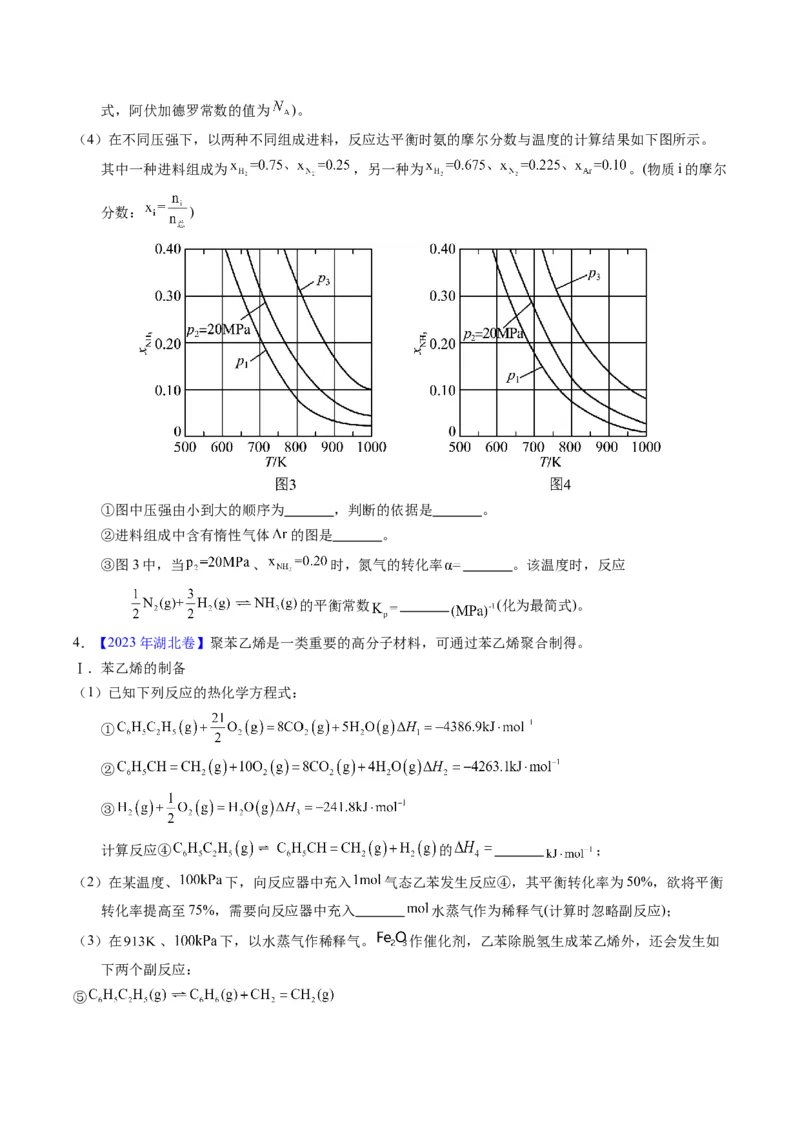
(3)将 置入抽空的刚性容器中,升高温度发生分解反应:(Ⅰ)。平衡时 的关系如下图所示。 时,该反应的
平衡总压 、平衡常数 。 随反应温度升高而 (填
“增大”“减小”或“不变”)。
(4)提高温度,上述容器中进一步发生反应 (Ⅱ),平衡时 (用
表示)。在 时, ,则 ,
(列出计算式)。
3.【2023年全国新课标卷】氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列
问题:
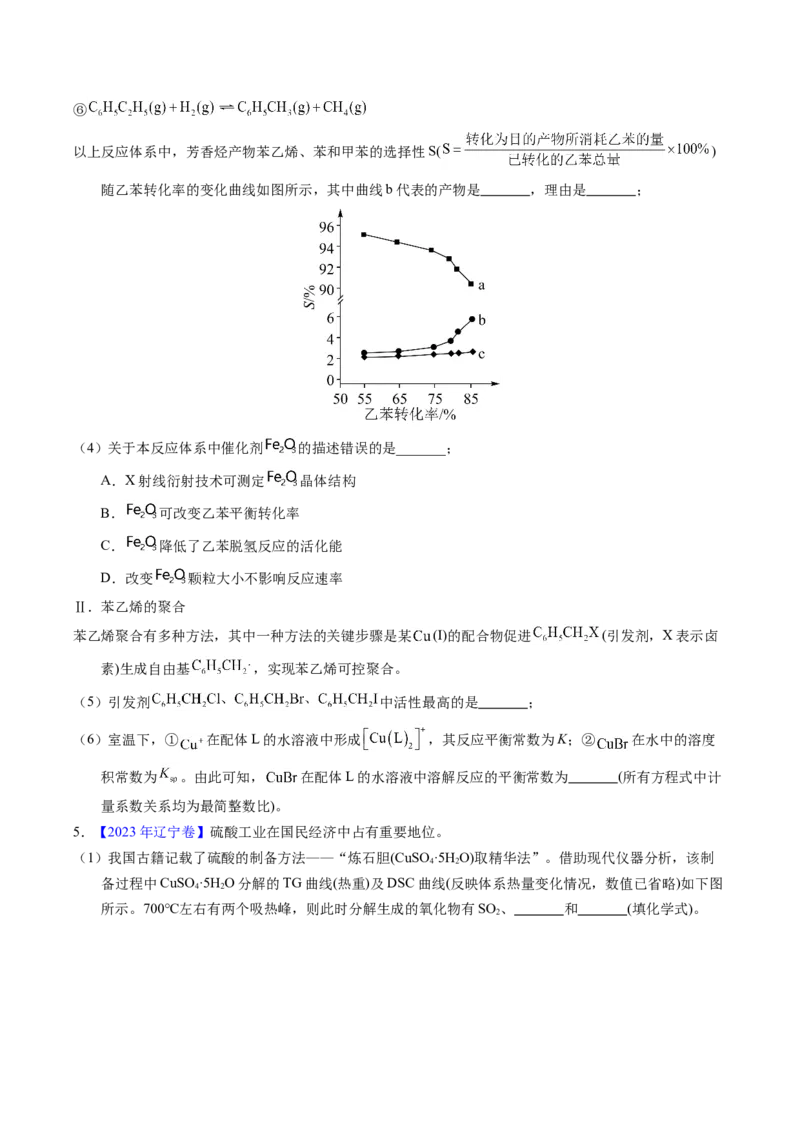
(1)根据图1数据计算反应 的 。
(2)研究表明,合成氨反应在 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位, 表示被吸
附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为 (填步骤前的
标号),理由是 。
(3)合成氨催化剂前驱体(主要成分为 )使用前经 还原,生成 包裹的 。已知 属于立
方晶系,晶胞参数 ,密度为 ,则 晶胞中含有 的原子数为 (列出计算式,阿伏加德罗常数的值为 )。
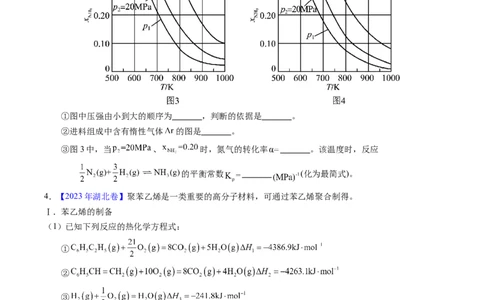
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。
其中一种进料组成为 ,另一种为 。(物质i的摩尔
分数: )
①图中压强由小到大的顺序为 ,判断的依据是 。
②进料组成中含有惰性气体 的图是 。
③图3中,当 、 时,氮气的转化率 。该温度时,反应
的平衡常数 (化为最简式)。
4.【2023年湖北卷】聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
②
③
计算反应④ 的 ;
(2)在某温度、 下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡
转化率提高至75%,需要向反应器中充入 水蒸气作为稀释气(计算时忽略副反应);
(3)在 、 下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如
下两个副反应:
⑤⑥
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S( )
随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是 ,理由是 ;
(4)关于本反应体系中催化剂 的描述错误的是_______;
A.X射线衍射技术可测定 晶体结构
B. 可改变乙苯平衡转化率
C. 降低了乙苯脱氢反应的活化能
D.改变 颗粒大小不影响反应速率
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进 (引发剂,X表示卤
素)生成自由基 ,实现苯乙烯可控聚合。
(5)引发剂 中活性最高的是 ;
(6)室温下,① 在配体L的水溶液中形成 ,其反应平衡常数为K;② 在水中的溶度
积常数为 。由此可知, 在配体L的水溶液中溶解反应的平衡常数为 (所有方程式中计
量系数关系均为最简整数比)。
5.【2023年辽宁卷】硫酸工业在国民经济中占有重要地位。
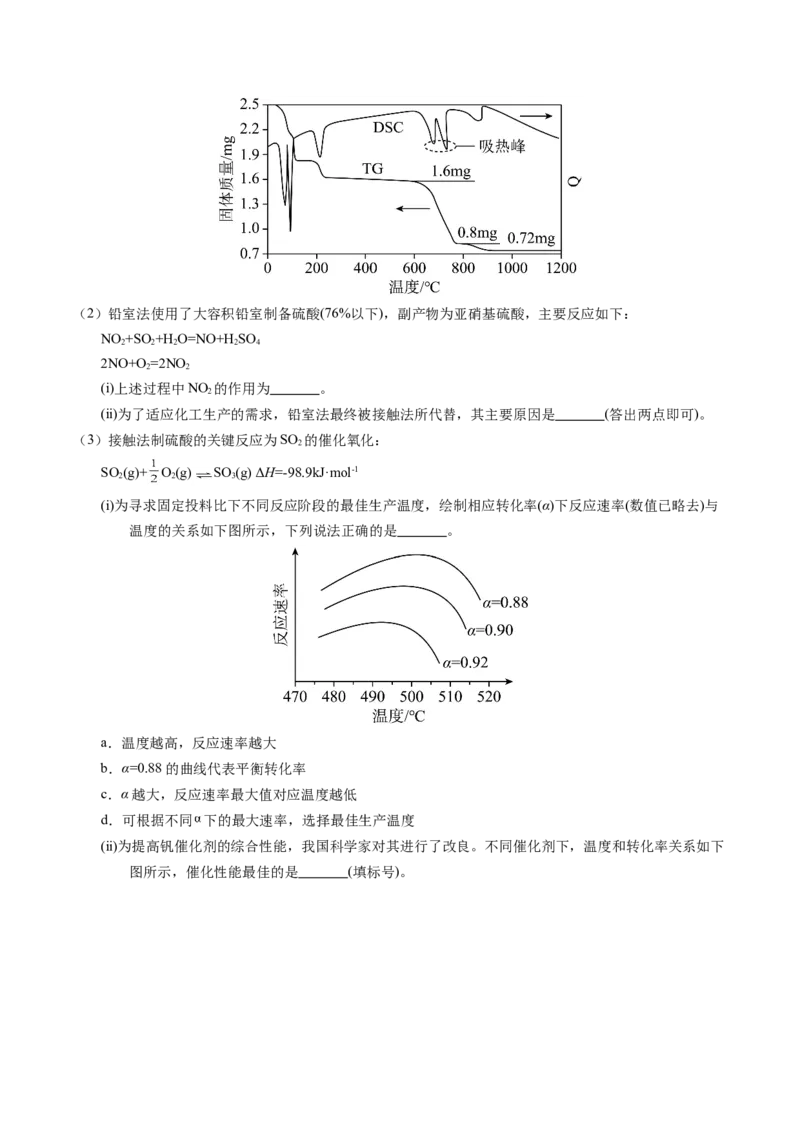
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO ·5H O)取精华法”。借助现代仪器分析,该制
4 2
备过程中CuSO ·5H O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图
4 2
所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有SO 、 和 (填化学式)。
2(2)铅室法使用了大容积铅室制备硫酸(76%以下),副产物为亚硝基硫酸,主要反应如下:
NO +SO+H O=NO+H SO
2 2 2 2 4
2NO+O =2NO
2 2
(ⅰ)上述过程中NO 的作用为 。
2
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是 (答出两点即可)。
(3)接触法制硫酸的关键反应为SO 的催化氧化:
2
SO (g)+ O(g) SO (g) ΔH=-98.9kJ·mol-1
2 2 3
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与
温度的关系如下图所示,下列说法正确的是 。
a.温度越高,反应速率越大
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同 下的最大速率,选择最佳生产温度
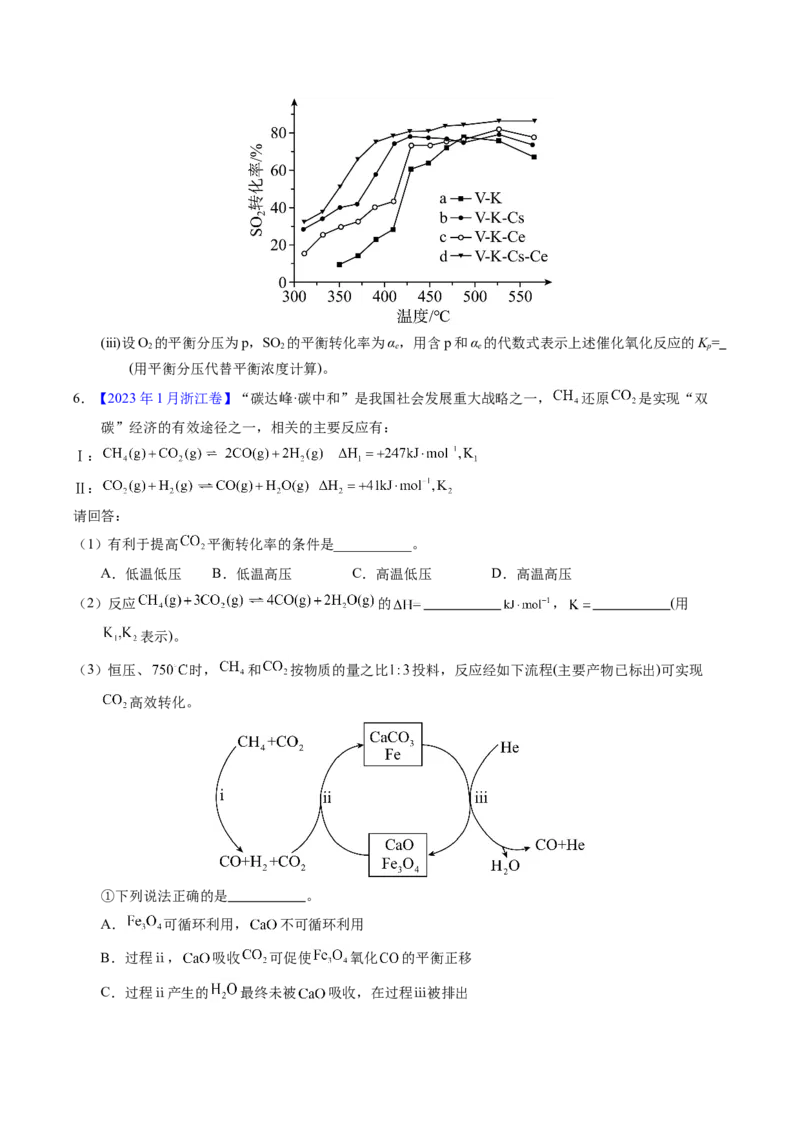
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下
图所示,催化性能最佳的是 (填标号)。(ⅲ)设O 的平衡分压为p,SO 的平衡转化率为α,用含p和α 的代数式表示上述催化氧化反应的K =
2 2 e e p
(用平衡分压代替平衡浓度计算)。
6.【2023年1月浙江卷】“碳达峰·碳中和”是我国社会发展重大战略之一, 还原 是实现“双
碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:
Ⅱ:
请回答:
(1)有利于提高 平衡转化率的条件是___________。
A.低温低压 B.低温高压 C.高温低压 D.高温高压
(2)反应 的 , (用
表示)。
(3)恒压、 时, 和 按物质的量之比 投料,反应经如下流程(主要产物已标出)可实现
高效转化。
①下列说法正确的是 。
A. 可循环利用, 不可循环利用
B.过程ⅱ, 吸收 可促使 氧化 的平衡正移
C.过程ⅱ产生的 最终未被 吸收,在过程ⅲ被排出D.相比于反应Ⅰ,该流程的总反应还原 需吸收的能量更多
②过程ⅱ平衡后通入 ,测得一段时间内 物质的量上升,根据过程ⅲ,结合平衡移动原理,解释
物质的量上升的原因 。
(4) 还原能力 可衡量 转化效率, (同一时段内 与 的物质的
量变化量之比)。
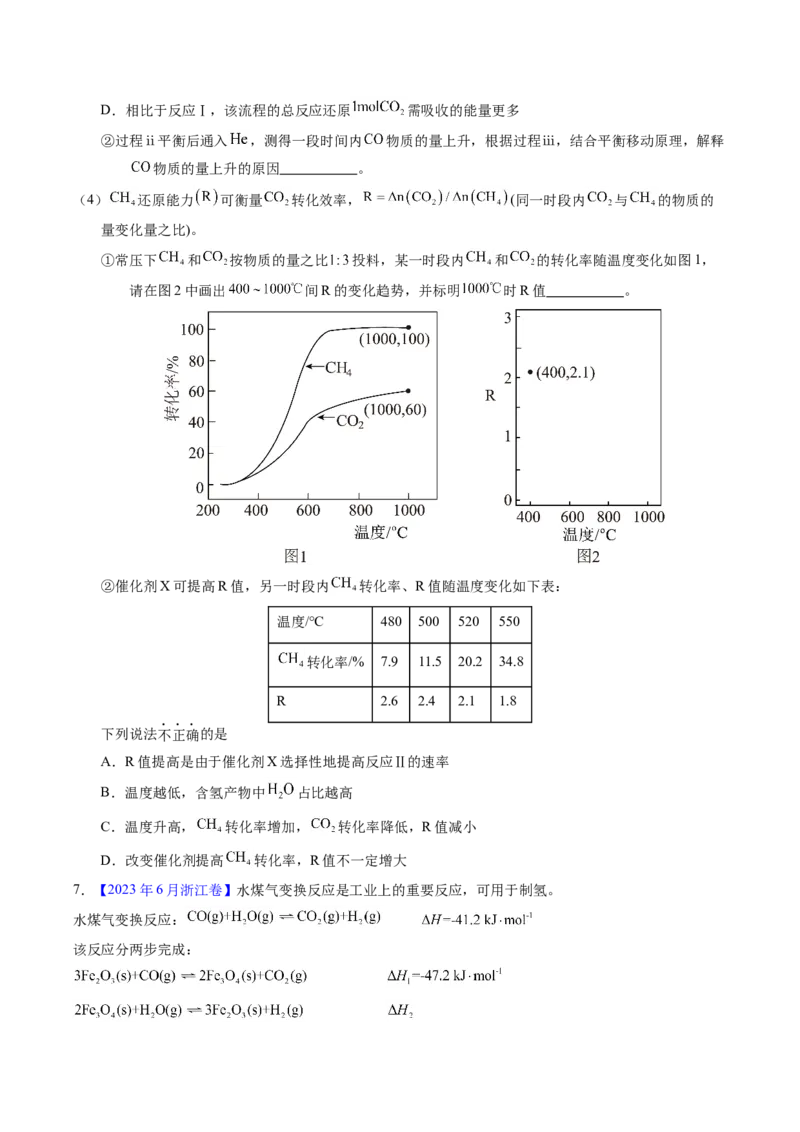
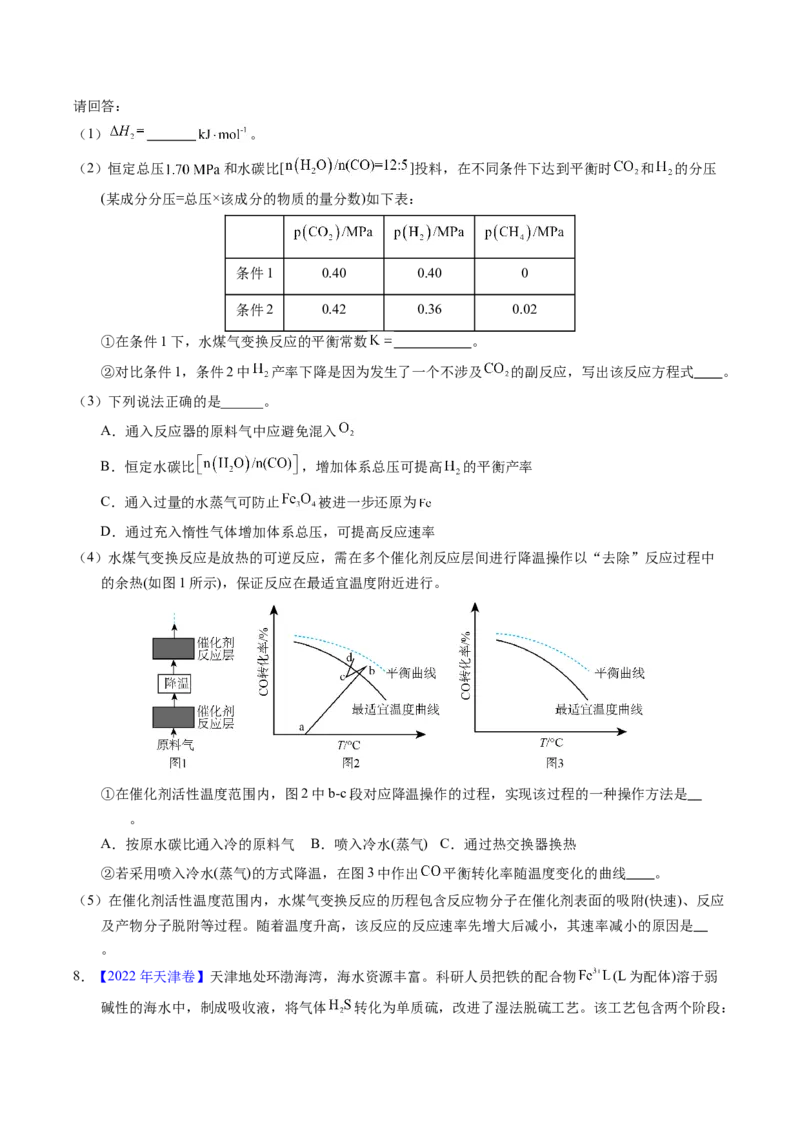
①常压下 和 按物质的量之比 投料,某一时段内 和 的转化率随温度变化如图1,
请在图2中画出 间R的变化趋势,并标明 时R值 。
②催化剂X可提高R值,另一时段内 转化率、R值随温度变化如下表:
温度/℃ 480 500 520 550
转化率/% 7.9 11.5 20.2 34.8
R 2.6 2.4 2.1 1.8
下列说法不正确的是
A.R值提高是由于催化剂X选择性地提高反应Ⅱ的速率
B.温度越低,含氢产物中 占比越高
C.温度升高, 转化率增加, 转化率降低,R值减小
D.改变催化剂提高 转化率,R值不一定增大
7.【2023年6月浙江卷】水煤气变换反应是工业上的重要反应,可用于制氢。
水煤气变换反应:
该反应分两步完成:请回答:
(1) 。
(2)恒定总压 和水碳比[ ]投料,在不同条件下达到平衡时 和 的分压
(某成分分压=总压×该成分的物质的量分数)如下表:
条件1 0.40 0.40 0
条件2 0.42 0.36 0.02
①在条件1下,水煤气变换反应的平衡常数 。
②对比条件1,条件2中 产率下降是因为发生了一个不涉及 的副反应,写出该反应方程式 。
(3)下列说法正确的是______。
A.通入反应器的原料气中应避免混入
B.恒定水碳比 ,增加体系总压可提高 的平衡产率
C.通入过量的水蒸气可防止 被进一步还原为
D.通过充入惰性气体增加体系总压,可提高反应速率
(4)水煤气变换反应是放热的可逆反应,需在多个催化剂反应层间进行降温操作以“去除”反应过程中
的余热(如图1所示),保证反应在最适宜温度附近进行。
①在催化剂活性温度范围内,图2中b-c段对应降温操作的过程,实现该过程的一种操作方法是
。
A.按原水碳比通入冷的原料气 B.喷入冷水(蒸气) C.通过热交换器换热
②若采用喷入冷水(蒸气)的方式降温,在图3中作出 平衡转化率随温度变化的曲线 。
(5)在催化剂活性温度范围内,水煤气变换反应的历程包含反应物分子在催化剂表面的吸附(快速)、反应
及产物分子脱附等过程。随着温度升高,该反应的反应速率先增大后减小,其速率减小的原因是
。
8.【2022年天津卷】天津地处环渤海湾,海水资源丰富。科研人员把铁的配合物 (L为配体)溶于弱
碱性的海水中,制成吸收液,将气体 转化为单质硫,改进了湿法脱硫工艺。该工艺包含两个阶段:① 的吸收氧化;② 的再生。反应原理如下:
①
②
回答下列问题:
(1)该工艺的总反应方程式为___________。1mol 发生该反应的热量变化为___________,
在总反应中的作用是___________。
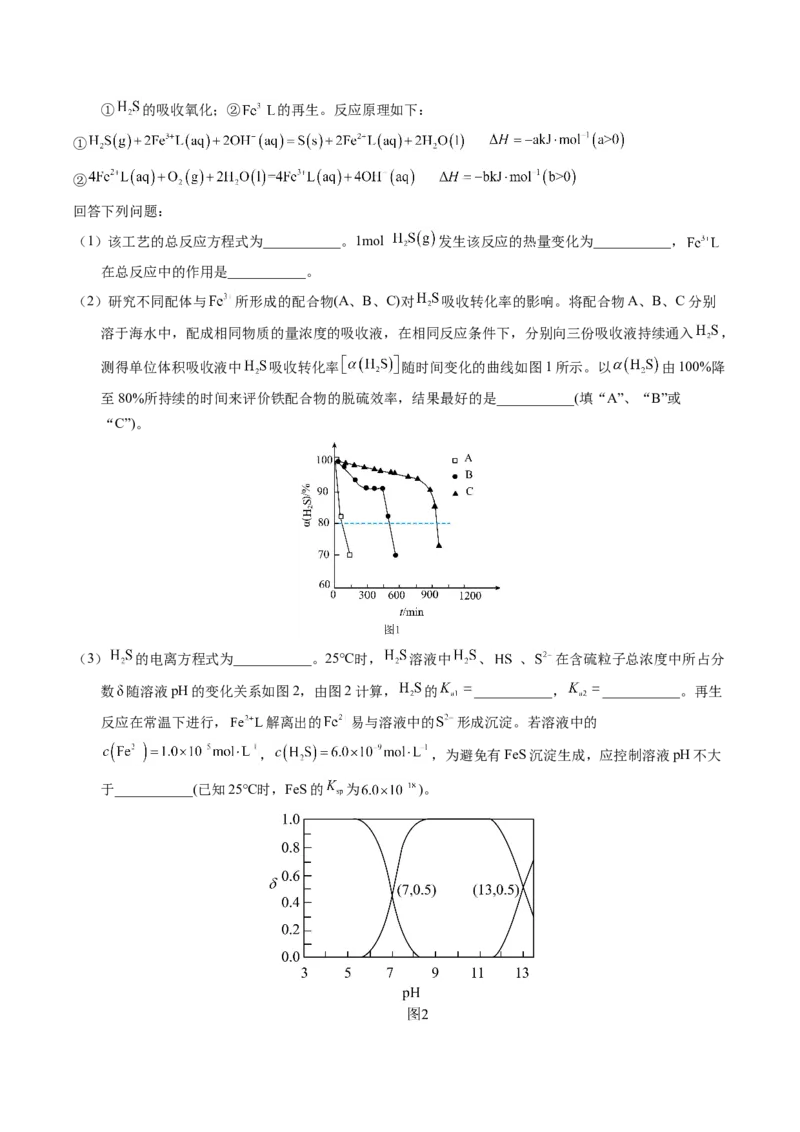
(2)研究不同配体与 所形成的配合物(A、B、C)对 吸收转化率的影响。将配合物A、B、C分别
溶于海水中,配成相同物质的量浓度的吸收液,在相同反应条件下,分别向三份吸收液持续通入 ,
测得单位体积吸收液中 吸收转化率 随时间变化的曲线如图1所示。以 由100%降
至80%所持续的时间来评价铁配合物的脱硫效率,结果最好的是___________(填“A”、“B”或
“C”)。
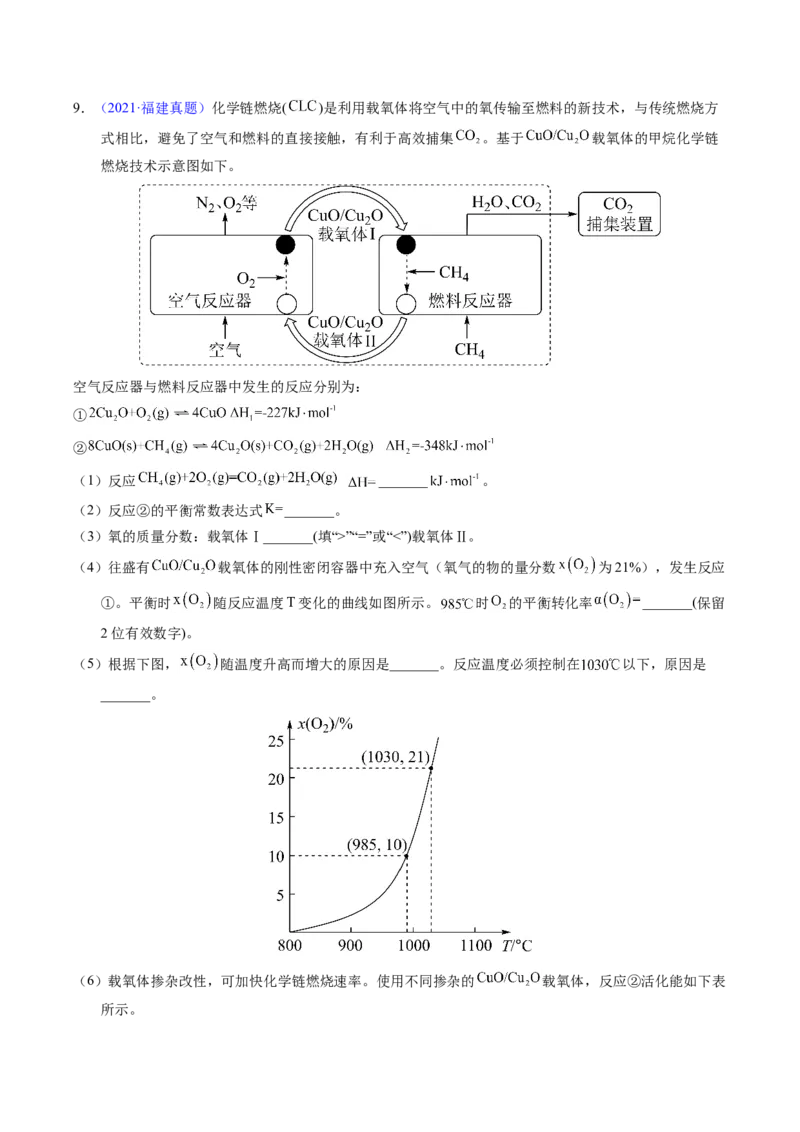
(3) 的电离方程式为___________。25℃时, 溶液中 、 、 在含硫粒子总浓度中所占分
数 随溶液pH的变化关系如图2,由图2计算, 的 ___________, ___________。再生
反应在常温下进行, 解离出的 易与溶液中的 形成沉淀。若溶液中的
, ,为避免有FeS沉淀生成,应控制溶液pH不大
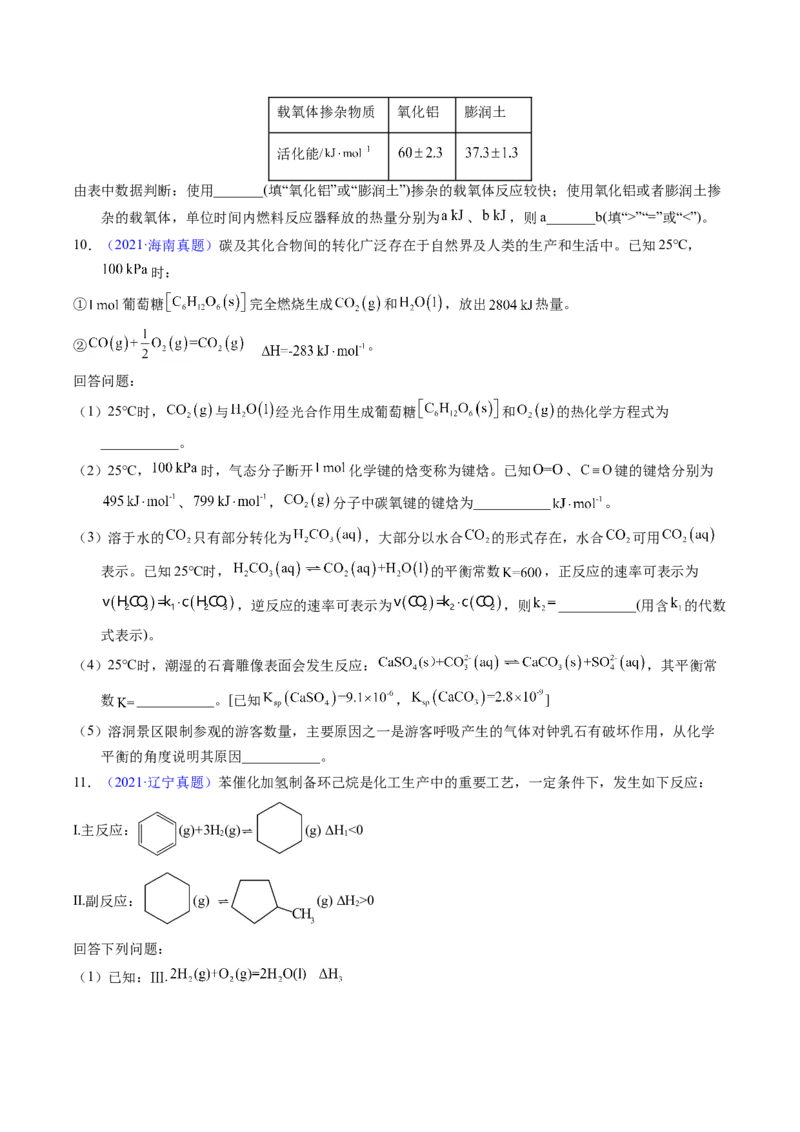
于___________(已知25℃时,FeS的 为 )。9.(2021·福建真题)化学链燃烧( )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方
式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于 载氧体的甲烷化学链
燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
②
(1)反应 _______ 。
(2)反应②的平衡常数表达式 _______。
(3)氧的质量分数:载氧体Ⅰ_______(填“>”“=”或“<”)载氧体Ⅱ。
(4)往盛有 载氧体的刚性密闭容器中充入空气(氧气的物的量分数 为21%),发生反应
①。平衡时 随反应温度T变化的曲线如图所示。 时 的平衡转化率 _______(保留
2位有效数字)。
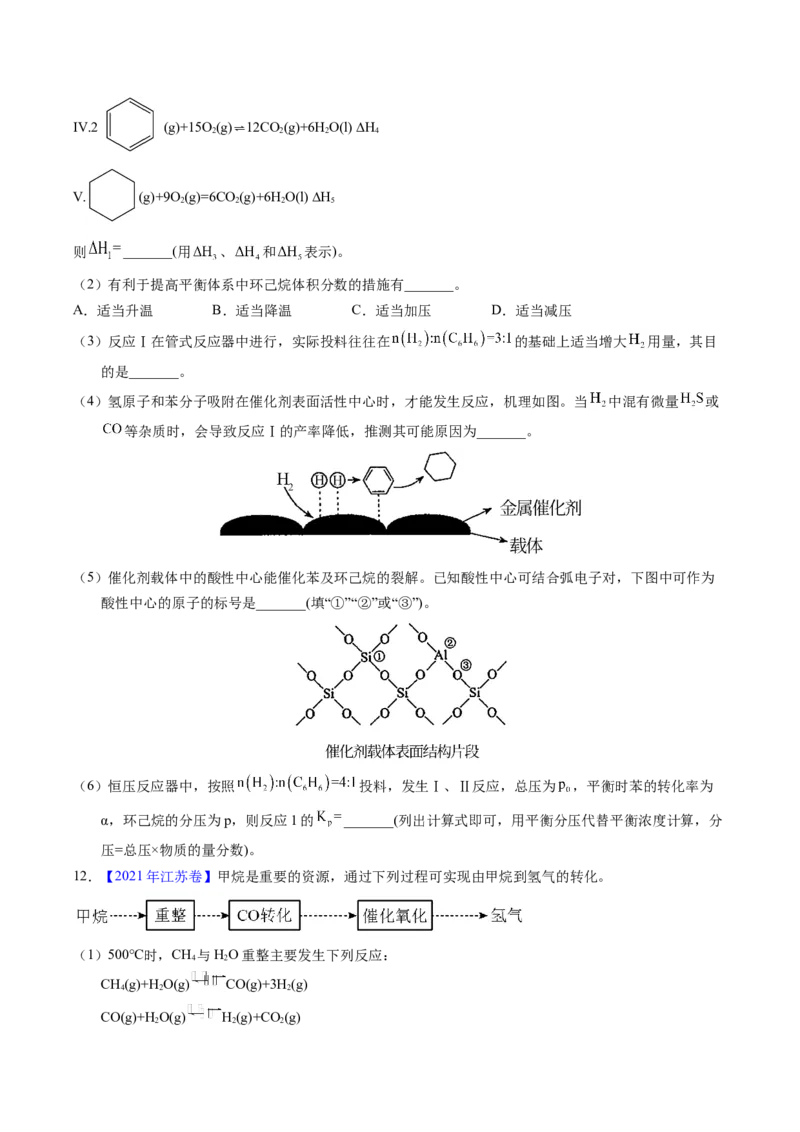
(5)根据下图, 随温度升高而增大的原因是_______。反应温度必须控制在 以下,原因是
_______。
(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下表
所示。载氧体掺杂物质 氧化铝 膨润土
活化能/
由表中数据判断:使用_______(填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺
杂的载氧体,单位时间内燃料反应器释放的热量分别为 、 ,则a_______b(填“>”“=”或“<”)。
10.(2021·海南真题)碳及其化合物间的转化广泛存在于自然界及人类的生产和生活中。已知25℃,
时:
① 葡萄糖 完全燃烧生成 和 ,放出 热量。
② 。
回答问题:
(1)25℃时, 与 经光合作用生成葡萄糖 和 的热化学方程式为
___________。
(2)25℃, 时,气态分子断开 化学键的焓变称为键焓。已知 、 键的键焓分别为
、 , 分子中碳氧键的键焓为___________ 。
(3)溶于水的 只有部分转化为 ,大部分以水合 的形式存在,水合 可用
表示。已知25℃时, 的平衡常数 ,正反应的速率可表示为
,逆反应的速率可表示为 ,则 ___________(用含 的代数
式表示)。
(4)25℃时,潮湿的石膏雕像表面会发生反应: ,其平衡常
数 ___________。[已知 , ]
(5)溶洞景区限制参观的游客数量,主要原因之一是游客呼吸产生的气体对钟乳石有破坏作用,从化学
平衡的角度说明其原因___________。
11.(2021·辽宁真题)苯催化加氢制备环己烷是化工生产中的重要工艺,一定条件下,发生如下反应:
Ⅰ.主反应: (g)+3H
2
(g)⇌ (g) ∆H
1
<0
Ⅱ.副反应: (g) ⇌ (g) ∆H 2 >0
回答下列问题:
(1)已知:Ⅲ.Ⅳ.2 (g)+15O
2
(g)⇌12CO
2
(g)+6H
2
O(l) ∆H
4
Ⅴ. (g)+9O(g)=6CO (g)+6HO(l) ∆H
2 2 2 5
则 _______(用 、 和 表示)。
(2)有利于提高平衡体系中环己烷体积分数的措施有_______。
A.适当升温 B.适当降温 C.适当加压 D.适当减压
(3)反应Ⅰ在管式反应器中进行,实际投料往往在 的基础上适当增大 用量,其目
的是_______。
(4)氢原子和苯分子吸附在催化剂表面活性中心时,才能发生反应,机理如图。当 中混有微量 或
等杂质时,会导致反应Ⅰ的产率降低,推测其可能原因为_______。
(5)催化剂载体中的酸性中心能催化苯及环己烷的裂解。已知酸性中心可结合弧电子对,下图中可作为
酸性中心的原子的标号是_______(填“①”“②”或“③”)。
(6)恒压反应器中,按照 投料,发生Ⅰ、Ⅱ反应,总压为 ,平衡时苯的转化率为
α,环己烷的分压为p,则反应1的 _______(列出计算式即可,用平衡分压代替平衡浓度计算,分
压=总压×物质的量分数)。
12.【2021年江苏卷】甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(1)500℃时,CH 与HO重整主要发生下列反应:
4 2
CH(g)+HO(g) CO(g)+3H(g)
4 2 2
CO(g)+HO(g) H(g)+CO (g)
2 2 2已知CaO(s)+CO (g)=CaCO (s) ΔH=-178.8kJ·mol-1。向重整反应体系中加入适量多孔CaO,其优点是
2 3
___。
(2)CH 与CO 重整的主要反应的热化学方程式为
4 2
反应I:CH(g)+CO (g)=2CO(g)+2H(g) ΔH=246.5kJ·mol-1
4 2 2
反应II:H(g)+CO (g)=CO(g)+HO(g) ΔH=41.2kJ·mol-1
2 2 2
反应III:2CO(g)=CO(g)+C(s) ΔH=-172.5kJ·mol-1
2
①在CH 与CO 重整体系中通入适量HO(g),可减少C(s)的生成,反应3CH(g)+CO (g)+2HO(g)=4CO(g)
4 2 2 4 2 2
+8H (g)的ΔH=___。
2
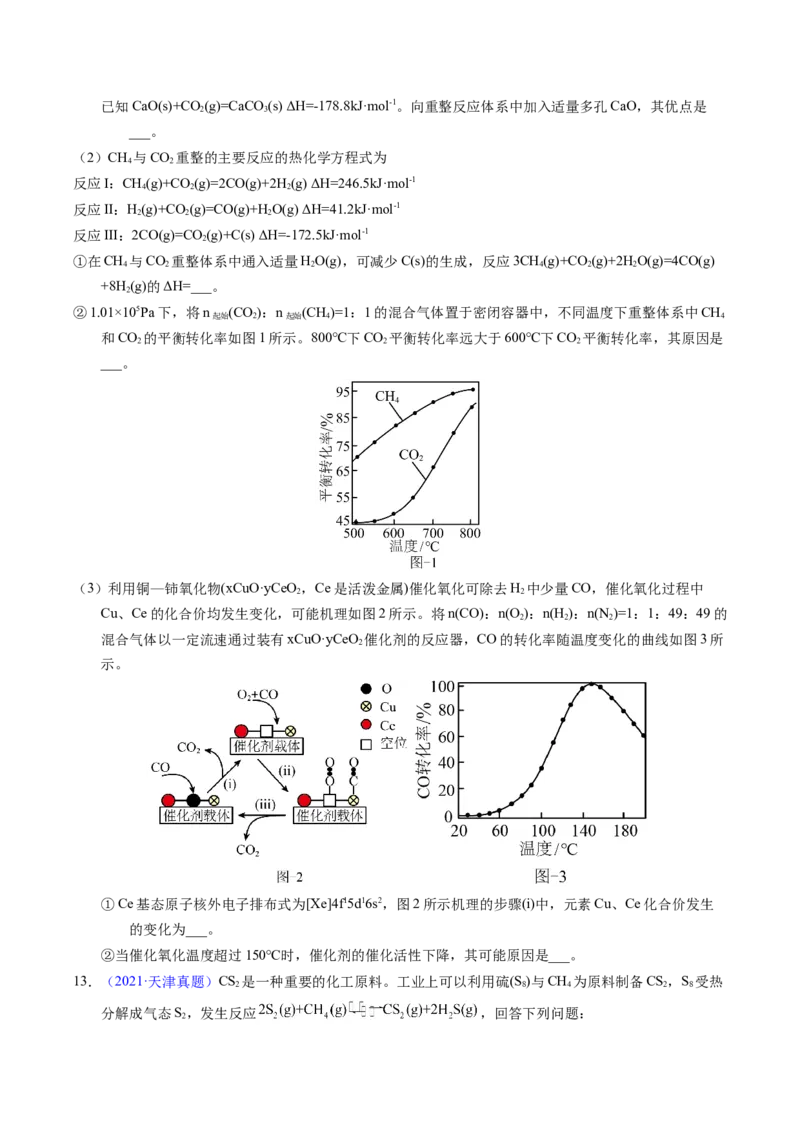
②1.01×105Pa下,将n (CO):n (CH)=1:1的混合气体置于密闭容器中,不同温度下重整体系中CH
起始 2 起始 4 4
和CO 的平衡转化率如图1所示。800℃下CO 平衡转化率远大于600℃下CO 平衡转化率,其原因是
2 2 2
___。
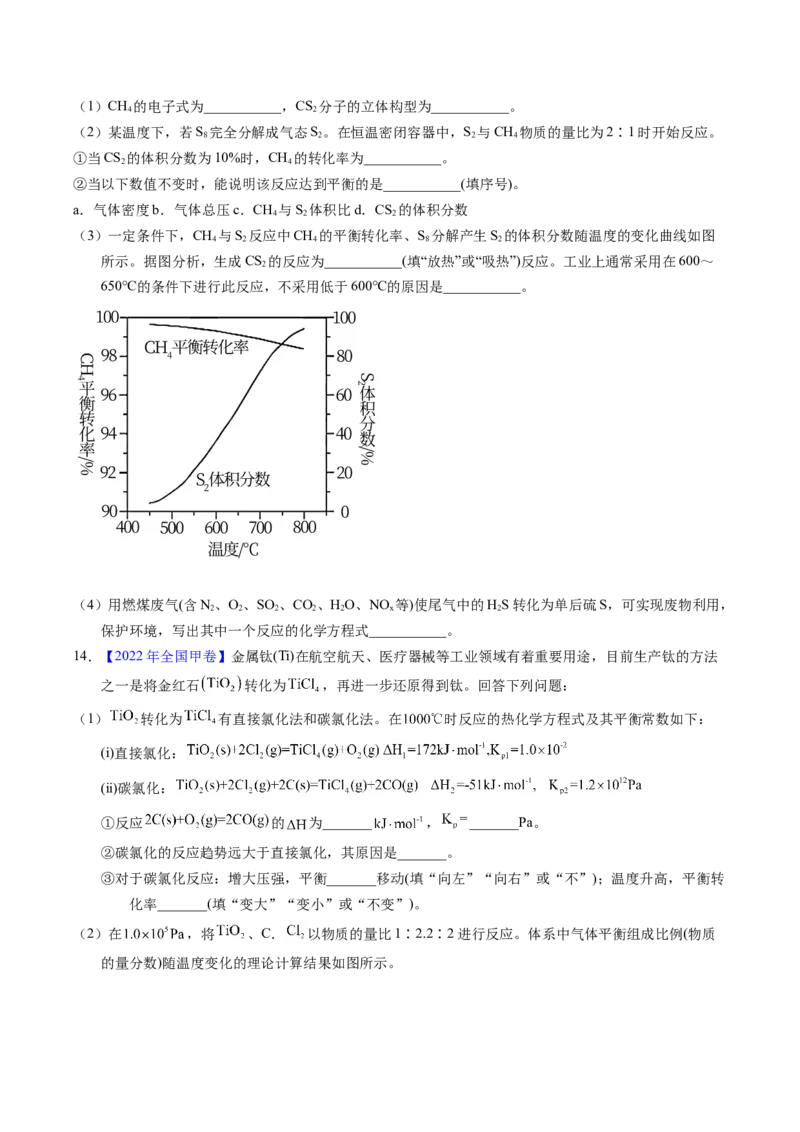
(3)利用铜—铈氧化物(xCuO·yCeO ,Ce是活泼金属)催化氧化可除去H 中少量CO,催化氧化过程中
2 2
Cu、Ce的化合价均发生变化,可能机理如图2所示。将n(CO):n(O ):n(H ):n(N )=1:1:49:49的
2 2 2
混合气体以一定流速通过装有xCuO·yCeO 催化剂的反应器,CO的转化率随温度变化的曲线如图3所
2
示。
①Ce基态原子核外电子排布式为[Xe]4f15d16s2,图2所示机理的步骤(i)中,元素Cu、Ce化合价发生
的变化为___。
②当催化氧化温度超过150℃时,催化剂的催化活性下降,其可能原因是___。
13.(2021·天津真题)CS 是一种重要的化工原料。工业上可以利用硫(S )与CH 为原料制备CS,S 受热
2 8 4 2 8
分解成气态S,发生反应 ,回答下列问题:
2(1)CH 的电子式为___________,CS 分子的立体构型为___________。
4 2
(2)某温度下,若S 完全分解成气态S。在恒温密闭容器中,S 与CH 物质的量比为2∶1时开始反应。
8 2 2 4
①当CS 的体积分数为10%时,CH 的转化率为___________。
2 4
②当以下数值不变时,能说明该反应达到平衡的是___________(填序号)。
a.气体密度b.气体总压c.CH 与S 体积比d.CS 的体积分数
4 2 2
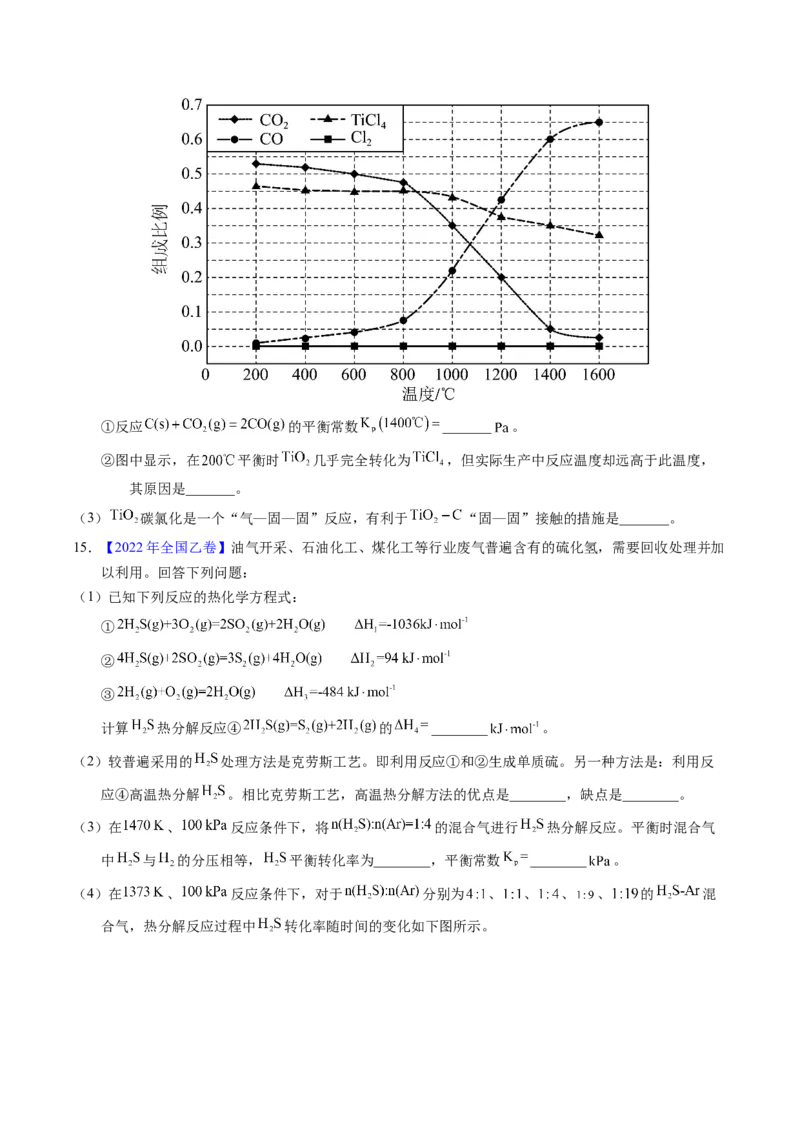
(3)一定条件下,CH 与S 反应中CH 的平衡转化率、S 分解产生S 的体积分数随温度的变化曲线如图
4 2 4 8 2
所示。据图分析,生成CS 的反应为___________(填“放热”或“吸热”)反应。工业上通常采用在600~
2
650℃的条件下进行此反应,不采用低于600℃的原因是___________。
(4)用燃煤废气(含N、O、SO 、CO、HO、NO 等)使尾气中的HS转化为单后硫S,可实现废物利用,
2 2 2 2 2 x 2
保护环境,写出其中一个反应的化学方程式___________。
14.【2022年全国甲卷】金属钛(Ti)在航空航天、医疗器械等工业领域有着重要用途,目前生产钛的方法
之一是将金红石 转化为 ,再进一步还原得到钛。回答下列问题:
(1) 转化为 有直接氯化法和碳氯化法。在 时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:
(ⅱ)碳氯化:
①反应 的 为_______ , _______Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是_______。
③对于碳氯化反应:增大压强,平衡_______移动(填“向左”“向右”或“不”);温度升高,平衡转
化率_______(填“变大”“变小”或“不变”)。
(2)在 ,将 、C. 以物质的量比1∶2.2∶2进行反应。体系中气体平衡组成比例(物质
的量分数)随温度变化的理论计算结果如图所示。①反应 的平衡常数 _______ 。
②图中显示,在 平衡时 几乎完全转化为 ,但实际生产中反应温度却远高于此温度,
其原因是_______。
(3) 碳氯化是一个“气—固—固”反应,有利于 “固—固”接触的措施是_______。
15.【2022年全国乙卷】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加
以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②
③
计算 热分解反应④ 的 ________ 。
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用反
应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
(3)在 、 反应条件下,将 的混合气进行 热分解反应。平衡时混合气
中 与 的分压相等, 平衡转化率为________,平衡常数 ________ 。
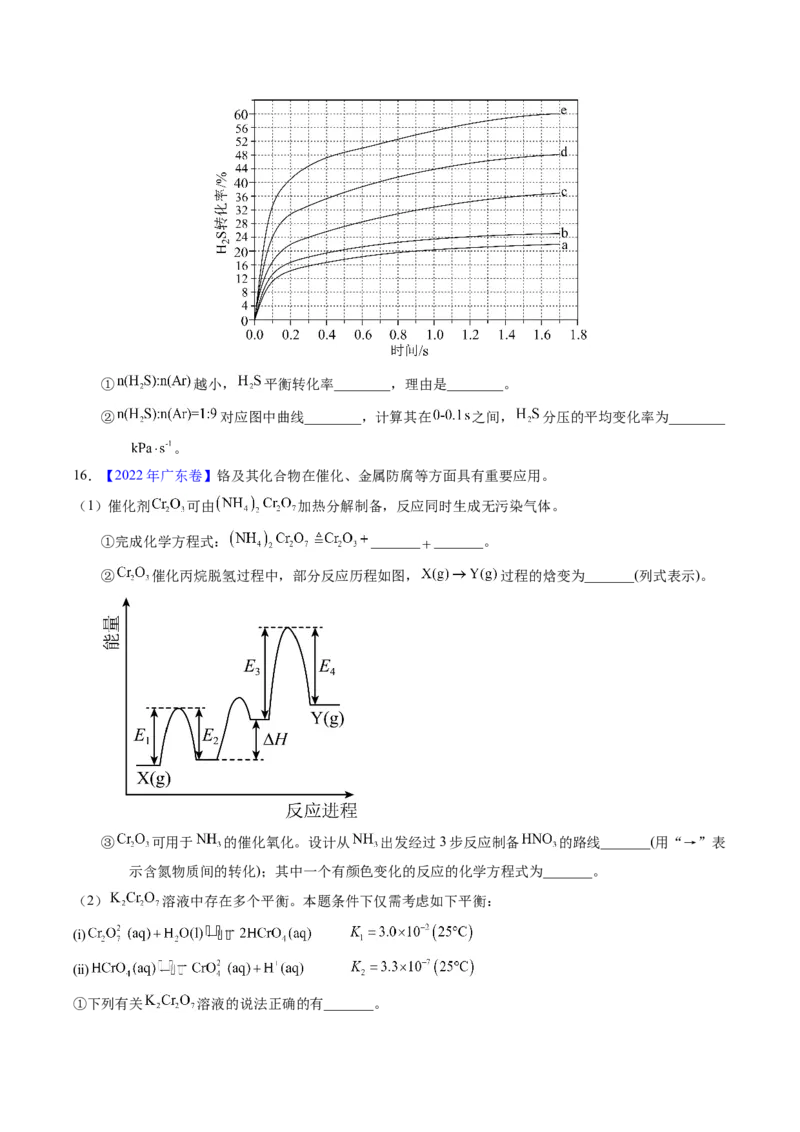
(4)在 、 反应条件下,对于 分别为 、 、 、 、 的 混
合气,热分解反应过程中 转化率随时间的变化如下图所示。① 越小, 平衡转化率________,理由是________。
② 对应图中曲线________,计算其在 之间, 分压的平均变化率为________
。
16.【2022年广东卷】铬及其化合物在催化、金属防腐等方面具有重要应用。
(1)催化剂 可由 加热分解制备,反应同时生成无污染气体。
①完成化学方程式: _______ _______。
② 催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为_______(列式表示)。
③ 可用于 的催化氧化。设计从 出发经过3步反应制备 的路线_______(用“→”表
示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_______。
(2) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(ⅰ)
(ⅱ)
①下列有关 溶液的说法正确的有_______。A.加入少量硫酸,溶液的pH不变
B.加入少量水稀释,溶液中离子总数增加
C.加入少量 溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时 与 的比值保持不变
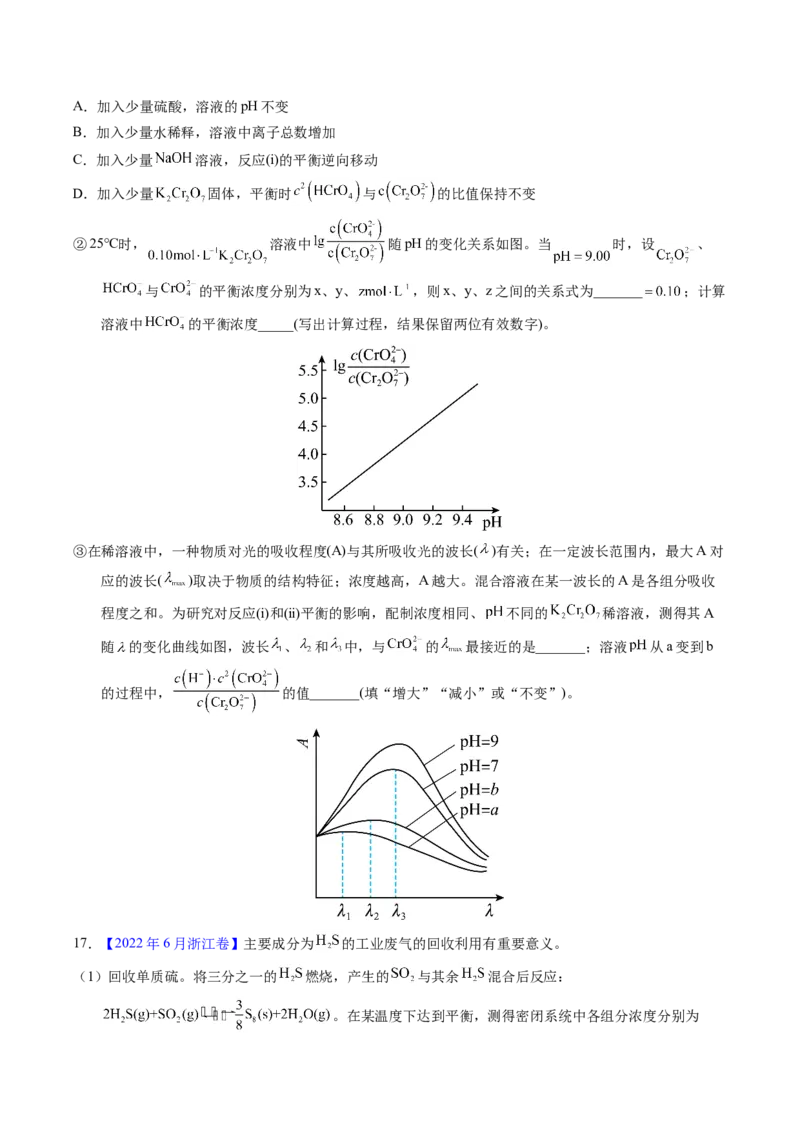
②25℃时, 溶液中 随pH的变化关系如图。当 时,设 、
与 的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为_______ ;计算
溶液中 的平衡浓度_____(写出计算过程,结果保留两位有效数字)。
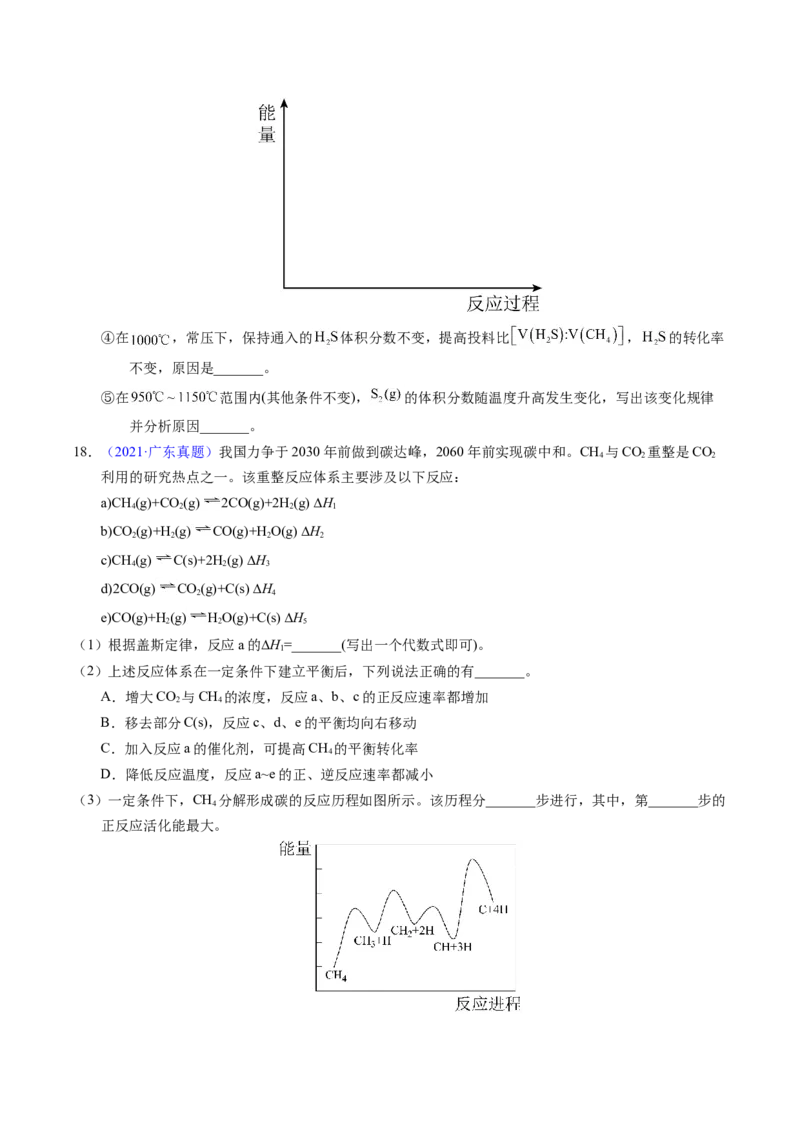
③在稀溶液中,一种物质对光的吸收程度(A)与其所吸收光的波长( )有关;在一定波长范围内,最大A对
应的波长( )取决于物质的结构特征;浓度越高,A越大。混合溶液在某一波长的A是各组分吸收
程度之和。为研究对反应(ⅰ)和(ⅱ)平衡的影响,配制浓度相同、 不同的 稀溶液,测得其A
随 的变化曲线如图,波长 、 和 中,与 的 最接近的是_______;溶液 从a变到b
的过程中, 的值_______(填“增大”“减小”或“不变”)。
17.【2022年6月浙江卷】主要成分为 的工业废气的回收利用有重要意义。
(1)回收单质硫。将三分之一的 燃烧,产生的 与其余 混合后反应:
。在某温度下达到平衡,测得密闭系统中各组分浓度分别为、 、 ,计算该温度下的平衡
常数 _______。
(2)热解 制 。根据文献,将 和 的混合气体导入石英管反应器热解(一边进料,另一边出
料),发生如下反应:
Ⅰ
Ⅱ
总反应:
Ⅲ
投料按体积之比 ,并用 稀释;常压,不同温度下反应相同时间后,测得 和
体积分数如下表:
105
温度/ 950 1000 1100 1150
0.5 1.5 3.6 5.5 8.5
0.0 0.0 0.1 0.4 1.8
请回答:
①反应Ⅲ能自发进行的条件是_______。
②下列说法正确的是_______。
A.其他条件不变时,用Ar替代 作稀释气体,对实验结果几乎无影响
B.其他条件不变时,温度越高, 的转化率越高
C.由实验数据推出 中的 键强于 中的 键
D.恒温恒压下,增加 的体积分数, 的浓度升高
③若将反应Ⅲ看成由反应Ⅰ和反应Ⅱ两步进行,画出由反应原料经两步生成产物的反应过程能量示意
图_______。④在 ,常压下,保持通入的 体积分数不变,提高投料比 , 的转化率
不变,原因是_______。
⑤在 范围内(其他条件不变), 的体积分数随温度升高发生变化,写出该变化规律
并分析原因_______。
18.(2021·广东真题)我国力争于2030年前做到碳达峰,2060年前实现碳中和。CH 与CO 重整是CO
4 2 2
利用的研究热点之一。该重整反应体系主要涉及以下反应:
a)CH(g)+CO (g) 2CO(g)+2H(g) ∆H
4 2 2 1
b)CO(g)+H(g) CO(g)+HO(g) ∆H
2 2 2 2
c)CH(g) C(s)+2H(g) ∆H
4 2 3
d)2CO(g) CO(g)+C(s) ∆H
2 4
e)CO(g)+H(g) HO(g)+C(s) ∆H
2 2 5
(1)根据盖斯定律,反应a的∆H=_______(写出一个代数式即可)。
1
(2)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______。
A.增大CO 与CH 的浓度,反应a、b、c的正反应速率都增加
2 4
B.移去部分C(s),反应c、d、e的平衡均向右移动
C.加入反应a的催化剂,可提高CH 的平衡转化率
4
D.降低反应温度,反应a~e的正、逆反应速率都减小
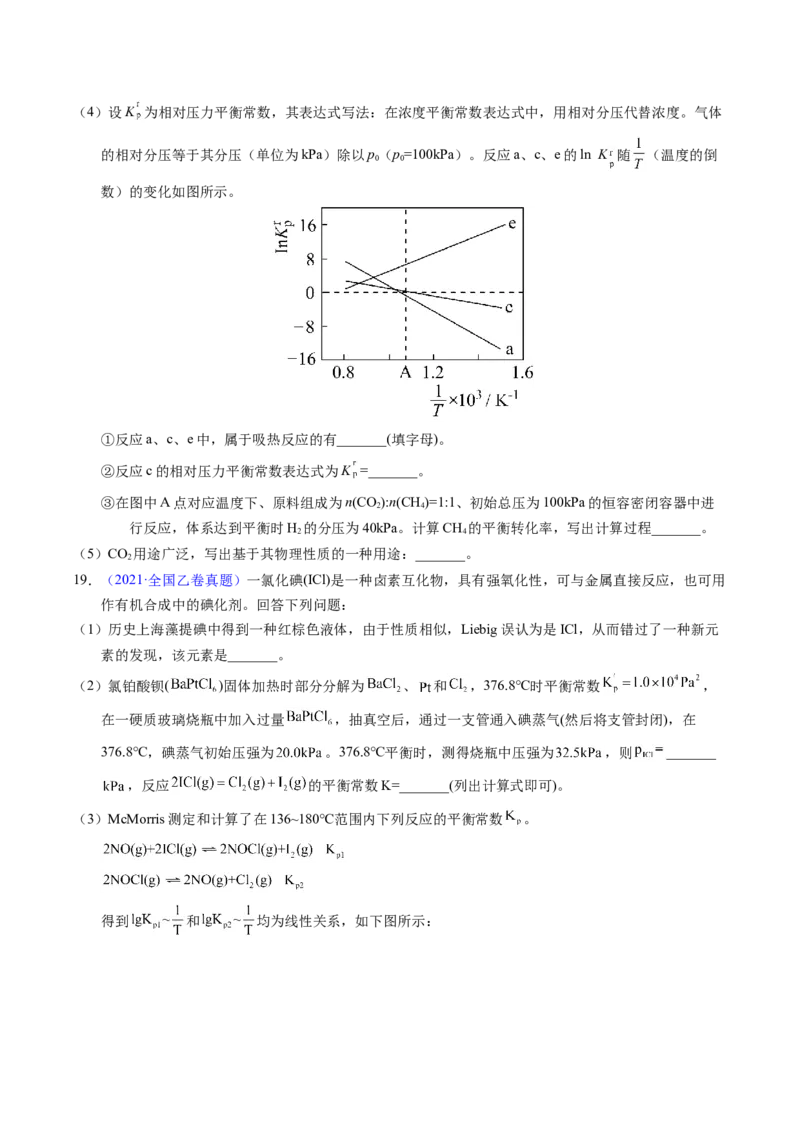
(3)一定条件下,CH 分解形成碳的反应历程如图所示。该历程分_______步进行,其中,第_______步的
4
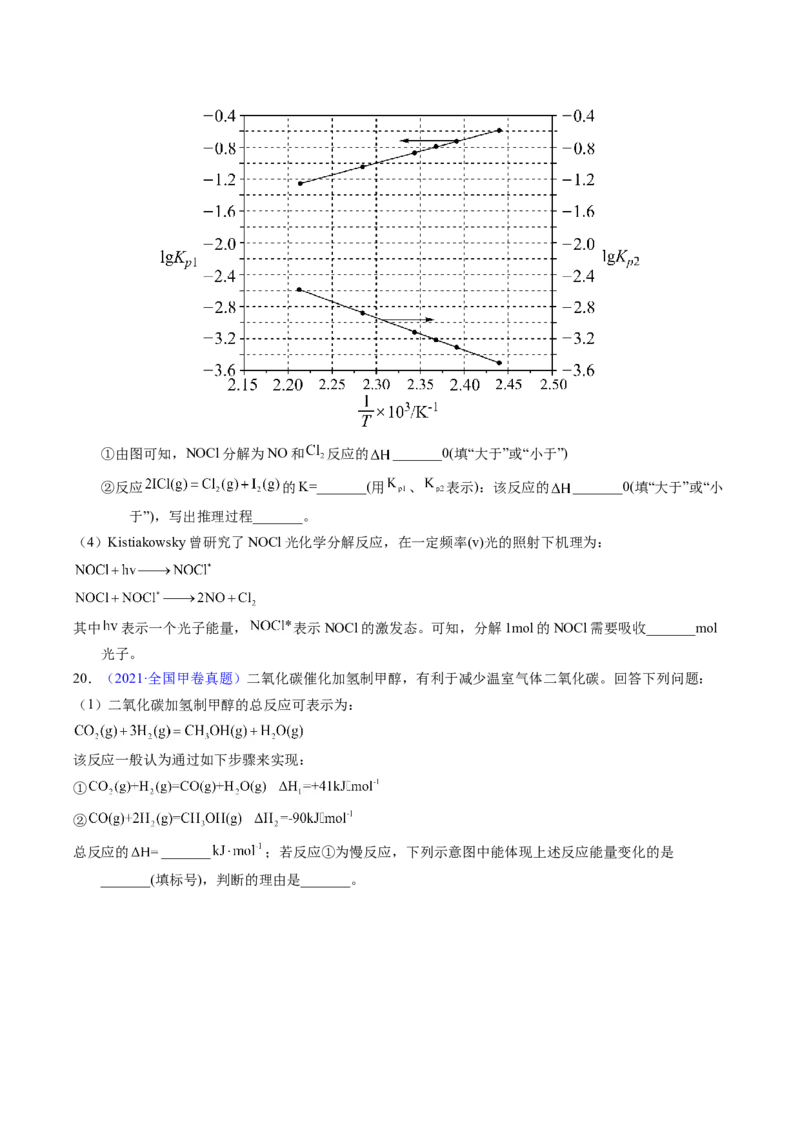
正反应活化能最大。(4)设K 为相对压力平衡常数,其表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体
的相对分压等于其分压(单位为kPa)除以p(p=100kPa)。反应a、c、e的ln K 随 (温度的倒
0 0
数)的变化如图所示。
①反应a、c、e中,属于吸热反应的有_______(填字母)。
②反应c的相对压力平衡常数表达式为K =_______。
③在图中A点对应温度下、原料组成为n(CO):n(CH)=1:1、初始总压为100kPa的恒容密闭容器中进
2 4
行反应,体系达到平衡时H 的分压为40kPa。计算CH 的平衡转化率,写出计算过程_______。
2 4
(5)CO 用途广泛,写出基于其物理性质的一种用途:_______。
2
19.(2021·全国乙卷真题)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用
作有机合成中的碘化剂。回答下列问题:
(1)历史上海藻提碘中得到一种红棕色液体,由于性质相似,Liebig误认为是ICl,从而错过了一种新元
素的发现,该元素是_______。
(2)氯铂酸钡( )固体加热时部分分解为 、 和 ,376.8℃时平衡常数 ,
在一硬质玻璃烧瓶中加入过量 ,抽真空后,通过一支管通入碘蒸气(然后将支管封闭),在
376.8℃,碘蒸气初始压强为 。376.8℃平衡时,测得烧瓶中压强为 ,则 _______
,反应 的平衡常数K=_______(列出计算式即可)。
(3)McMorris测定和计算了在136~180℃范围内下列反应的平衡常数 。
得到 和 均为线性关系,如下图所示:①由图可知,NOCl分解为NO和 反应的 _______0(填“大于”或“小于”)
②反应 的K=_______(用 、 表示):该反应的 _______0(填“大于”或“小
于”),写出推理过程_______。
(4)Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(v)光的照射下机理为:
其中 表示一个光子能量, 表示NOCl的激发态。可知,分解1mol的NOCl需要吸收_______mol
光子。
20.(2021·全国甲卷真题)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:
该反应一般认为通过如下步骤来实现:
①
②
总反应的 _______ ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
_______(填标号),判断的理由是_______。A. B. C.
D.
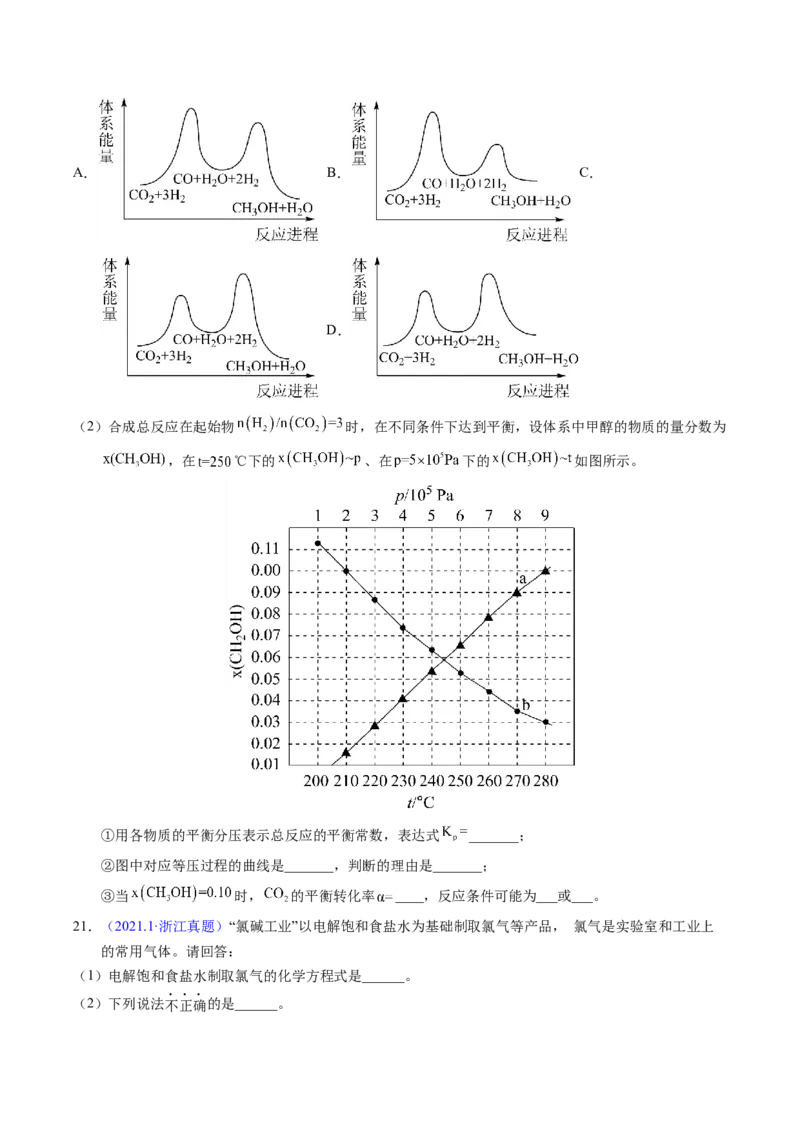
(2)合成总反应在起始物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
,在 ℃下的 、在 下的 如图所示。
①用各物质的平衡分压表示总反应的平衡常数,表达式 _______;
②图中对应等压过程的曲线是_______,判断的理由是_______;
③当 时, 的平衡转化率 ____,反应条件可能为___或___。
21.(2021.1·浙江真题)“氯碱工业”以电解饱和食盐水为基础制取氯气等产品, 氯气是实验室和工业上
的常用气体。请回答:
(1)电解饱和食盐水制取氯气的化学方程式是______。
(2)下列说法不正确的是______。A.可采用碱石灰干燥氯气
B.可通过排饱和食盐水法收集氯气
C.常温下,可通过加压使氯气液化而储存于钢瓶中
D.工业上,常用氢气和氯气反应生成的氯化氢溶于水制取盐酸
(3)在一定温度下,氯气溶于水的过程及其平衡常数为:
Cl
2
(g)⇌Cl
2
(aq) K
1
=c(Cl
2
)/p
Cl
2
(aq) + H
2
O(l)⇌H+ (aq)+Cl- (aq) + HClO(aq) K
2
其中p为Cl(g)的平衡压强,c(Cl )为Cl 在水溶液中的平衡浓度。
2 2 2
①Cl
2
(g)⇌Cl
2
(aq)的焓变ΔH
1
______0。(填”>”、“=”或“<”)
②平衡常数K 的表达式为K=______。
2 2
③氯气在水中的溶解度(以物质的量浓度表示)为c,则c=______。(用平衡压强p和上述平衡常数表示,
忽略HClO的电离)
(4)工业上,常采用“加碳氯化”的方法以高钛渣(主要成分为TiO)为原料生产TiCl ,相应的化学方程式为;
2 4
I.TiO
2
(s)+2Cl
2
(g)⇌TiCl
4
(g)+O
2
(g) ΔH
I
=181 mol·L-1,K
I
=-3.4×10-29
II.2C(s)+O
2
(g)⇌2CO(g) ΔH
II
= - 221 mol·L-1,K
II
=1.2×1048
结合数据说明氯化过程中加碳的理由______ 。
(5)在一定温度下,以I 为催化剂,氯苯和Cl 在CS 中发生平行反应,分别生成邻二氯苯和对二氯苯,
2 2 2
两产物浓度之比与反应时间无关。反应物起始浓度均为0.5 mol·L-1,反应30 min测得氯苯15%转化为
邻二氯苯,25%转化为对二氯苯。保持其他条件不变,若要提高产物中邻二氯苯的比例,可采用的措
施是______。
A.适当提高反应温度 B.改变催化剂
C.适当降低反应温度 D.改变反应物浓度
22.(2020·山东真题)探究CHOH合成反应化学平衡的影响因素,有利于提高CHOH的产率。以CO、
3 3 2
H 为原料合成CHOH涉及的主要反应如下:
2 3
Ⅰ.
Ⅱ.
Ⅲ.
回答下列问题:
(1) _________ 。
(2)一定条件下,向体积为VL的恒容密闭容器中通入1 mol CO 和3 mol H 发生上述反应,达到平衡时,
2 2
容器中CHOH(g)为ɑ mol,CO为b mol,此时HO(g)的浓度为__________mol﹒L-1(用含A.B.V的
3 2
代数式表示,下同),反应Ⅲ的平衡常数为___________。
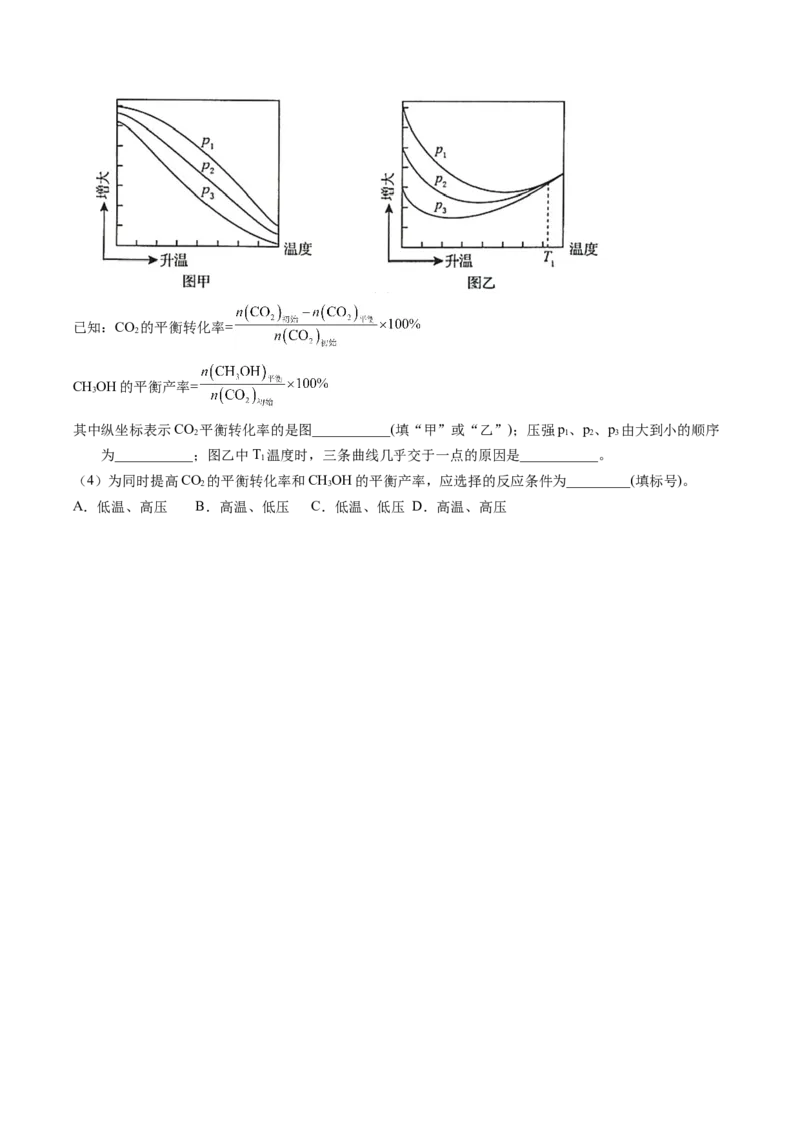
(3)不同压强下,按照n(CO):n(H )=1:3投料,实验测定CO 的平衡转化率和CHOH的平衡产率随温
2 2 2 3
度的变化关系如下图所示。已知:CO 的平衡转化率=
2
CHOH的平衡产率=
3
其中纵坐标表示CO 平衡转化率的是图___________(填“甲”或“乙”);压强p、p、p 由大到小的顺序
2 1 2 3
为___________;图乙中T 温度时,三条曲线几乎交于一点的原因是___________。
1
(4)为同时提高CO 的平衡转化率和CHOH的平衡产率,应选择的反应条件为_________(填标号)。
2 3
A.低温、高压 B.高温、低压 C.低温、低压 D.高温、高压