文档内容
专题65 原理综合题——反应热+速率+平衡
1.【2023年山东卷】一定条件下,水气变换反应 的中间产物是 。为探究
该反应过程,研究 水溶液在密封石英管中的分子反应:
Ⅰ.
Ⅱ.
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ
建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、 ,则该条件下水气变换反应的焓变 (用
含 的代数式表示)。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。 温度下, 电离
平衡常数为 ,当 平衡浓度为 时, 浓度为 ,此时反应Ⅰ应速率
(用含 和k的代数式表示)。
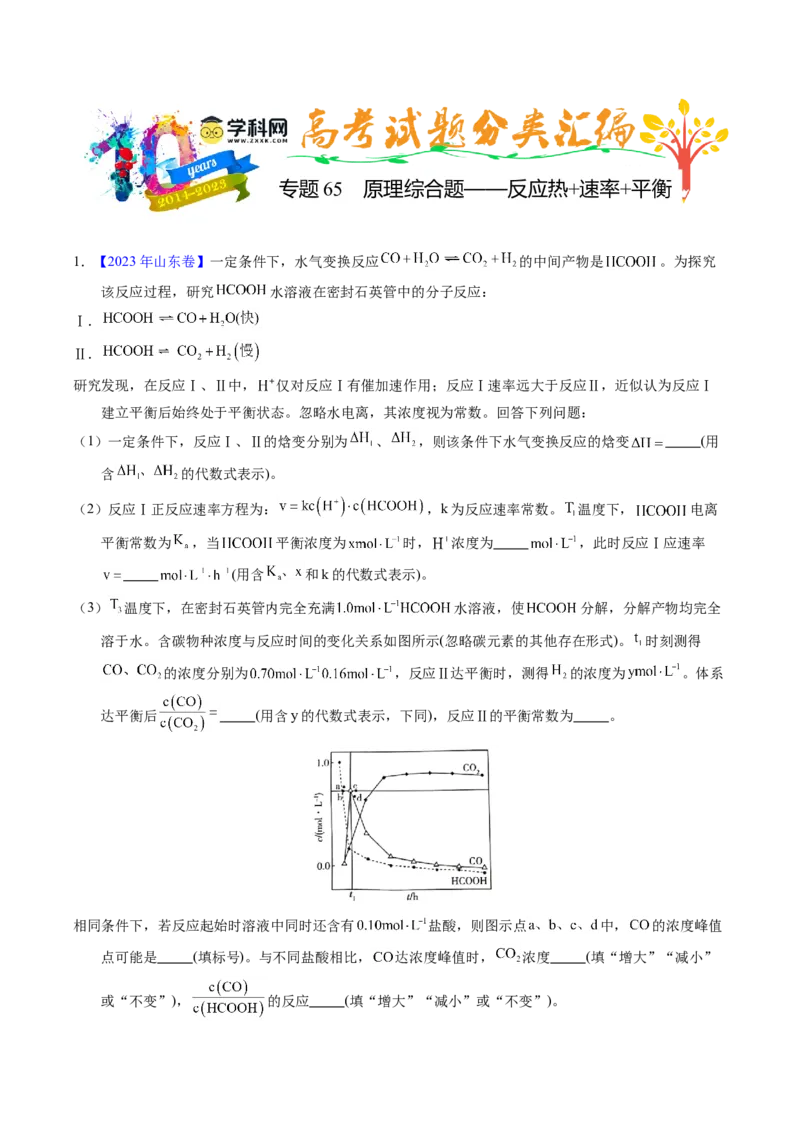
(3) 温度下,在密封石英管内完全充满 水溶液,使 分解,分解产物均完全
溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得
的浓度分别为 ,反应Ⅱ达平衡时,测得 的浓度为 。体系
达平衡后 (用含y的代数式表示,下同),反应Ⅱ的平衡常数为 。
相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点 中, 的浓度峰值
点可能是 (填标号)。与不同盐酸相比, 达浓度峰值时, 浓度 (填“增大”“减小”
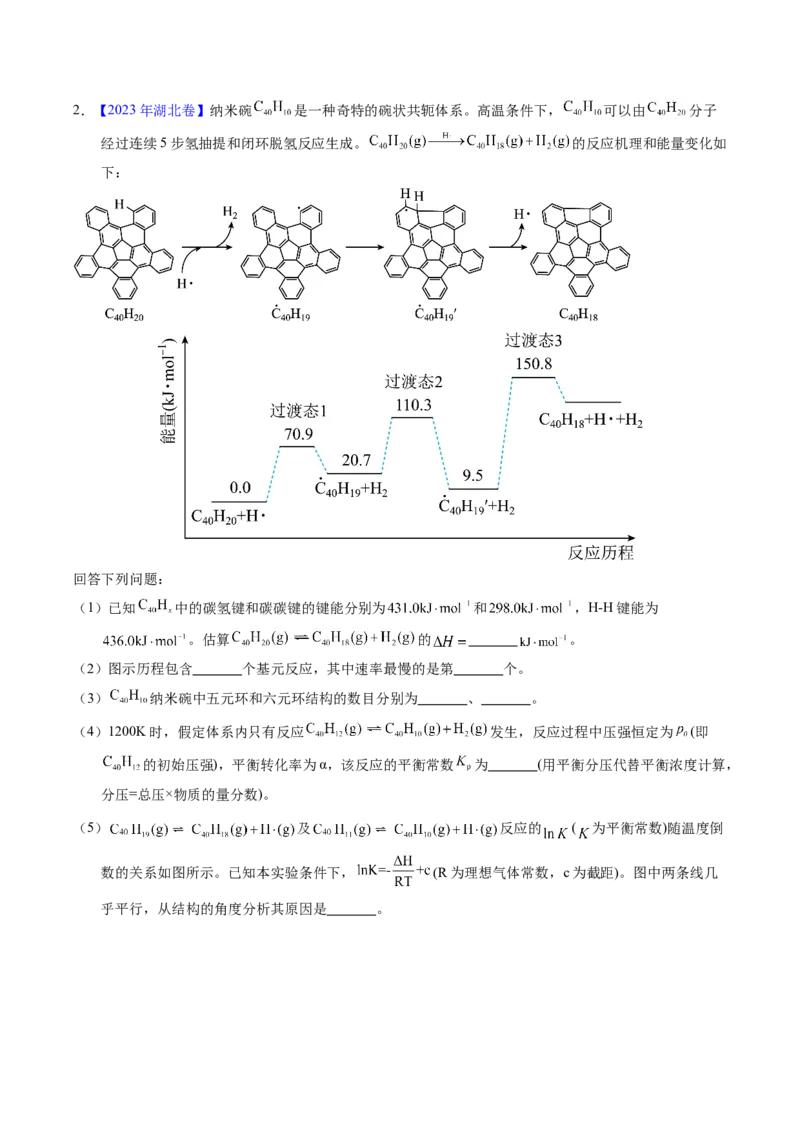
或“不变”), 的反应 (填“增大”“减小”或“不变”)。2.【2023年湖北卷】纳米碗 是一种奇特的碗状共轭体系。高温条件下, 可以由 分子
经过连续5步氢抽提和闭环脱氢反应生成。 的反应机理和能量变化如
下:
回答下列问题:
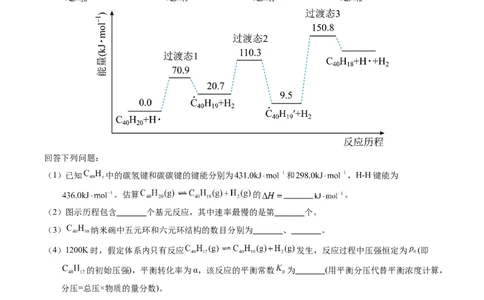
(1)已知 中的碳氢键和碳碳键的键能分别为 和 ,H-H键能为
。估算 的 。
(2)图示历程包含 个基元反应,其中速率最慢的是第 个。
(3) 纳米碗中五元环和六元环结构的数目分别为 、 。
(4)1200K时,假定体系内只有反应 发生,反应过程中压强恒定为 (即
的初始压强),平衡转化率为α,该反应的平衡常数 为 (用平衡分压代替平衡浓度计算,
分压=总压×物质的量分数)。
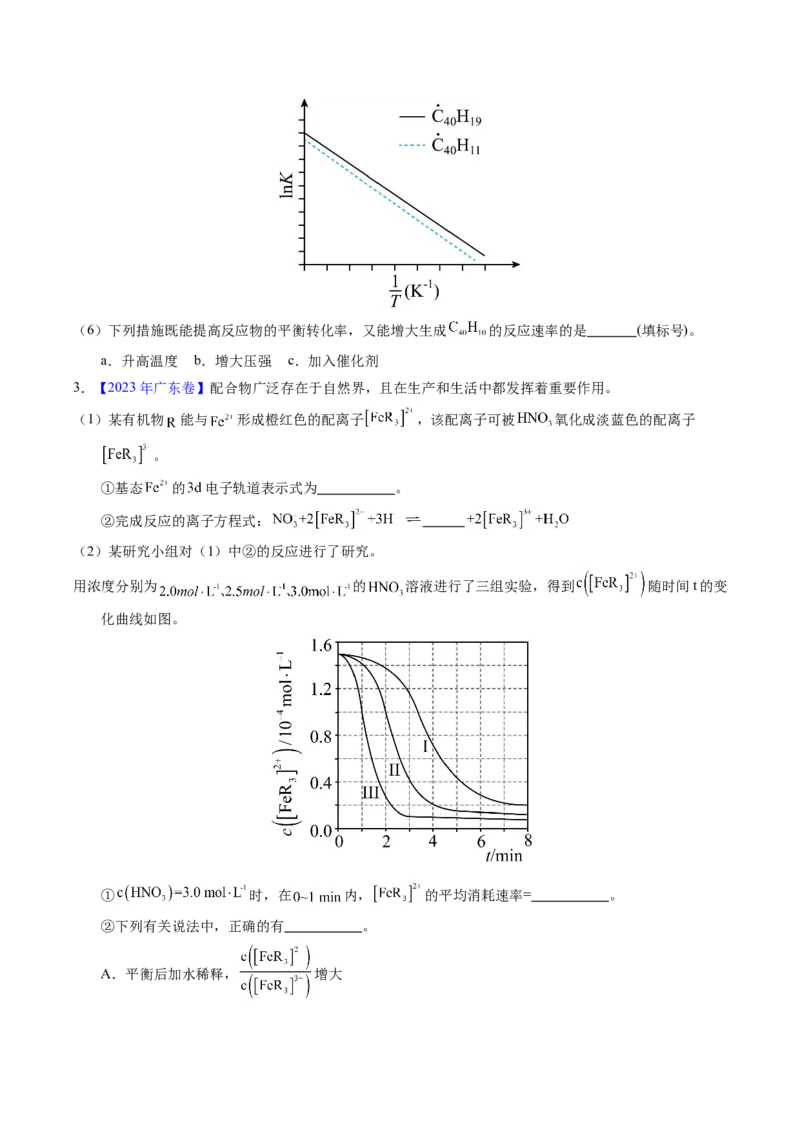
(5) 及 反应的 ( 为平衡常数)随温度倒
数的关系如图所示。已知本实验条件下, (R为理想气体常数,c为截距)。图中两条线几
乎平行,从结构的角度分析其原因是 。(6)下列措施既能提高反应物的平衡转化率,又能增大生成 的反应速率的是 (填标号)。
a.升高温度 b.增大压强 c.加入催化剂
3.【2023年广东卷】配合物广泛存在于自然界,且在生产和生活中都发挥着重要作用。
(1)某有机物 能与 形成橙红色的配离子 ,该配离子可被 氧化成淡蓝色的配离子
。
①基态 的 电子轨道表示式为 。
②完成反应的离子方程式:
(2)某研究小组对(1)中②的反应进行了研究。
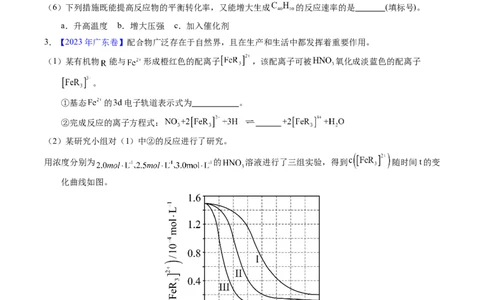
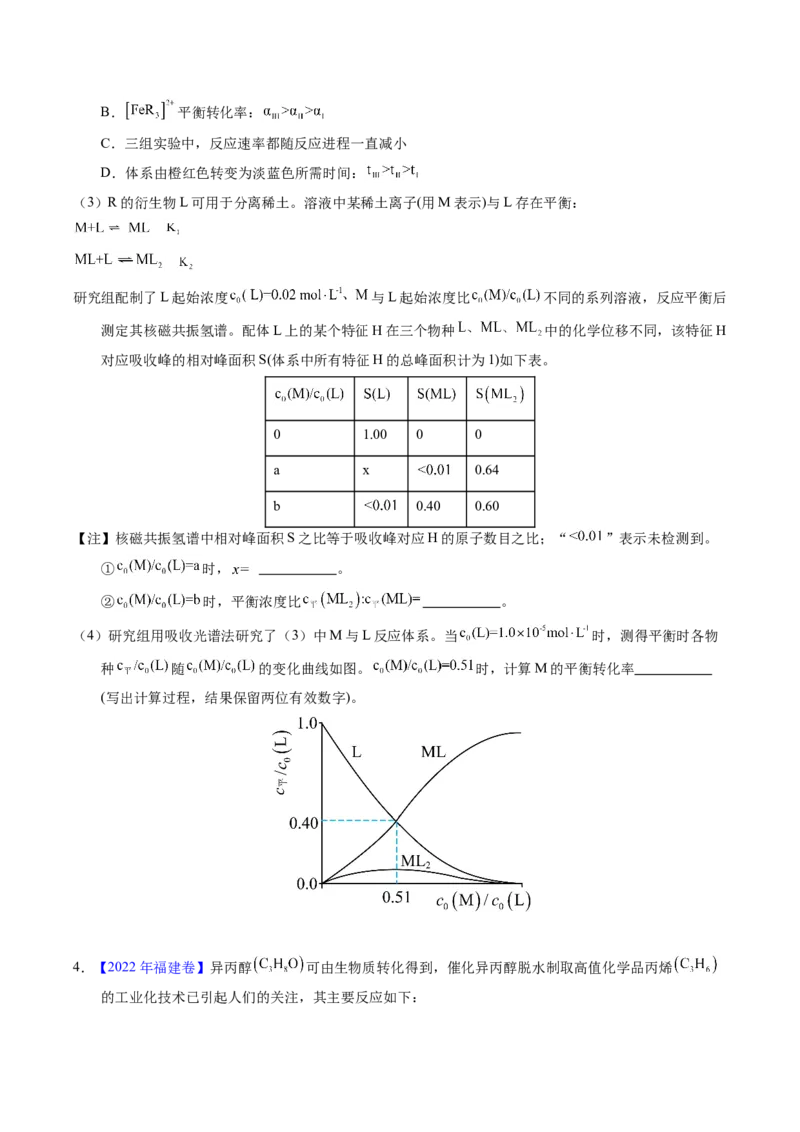
用浓度分别为 的 溶液进行了三组实验,得到 随时间t的变
化曲线如图。
① 时,在 内, 的平均消耗速率= 。
②下列有关说法中,正确的有 。
A.平衡后加水稀释, 增大B. 平衡转化率:
C.三组实验中,反应速率都随反应进程一直减小
D.体系由橙红色转变为淡蓝色所需时间:
(3)R的衍生物L可用于分离稀土。溶液中某稀土离子(用M表示)与L存在平衡:
研究组配制了L起始浓度 与L起始浓度比 不同的系列溶液,反应平衡后
测定其核磁共振氢谱。配体L上的某个特征H在三个物种 中的化学位移不同,该特征H
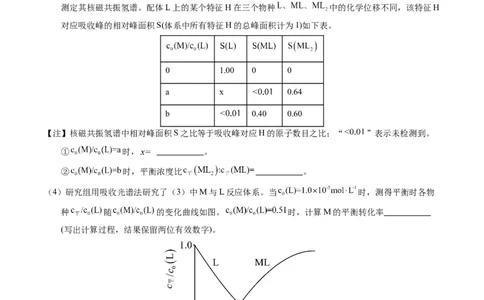
对应吸收峰的相对峰面积S(体系中所有特征H的总峰面积计为1)如下表。
0 1.00 0 0
a x 0.64
b 0.40 0.60
【注】核磁共振氢谱中相对峰面积S之比等于吸收峰对应H的原子数目之比;“ ”表示未检测到。
① 时, 。
② 时,平衡浓度比 。
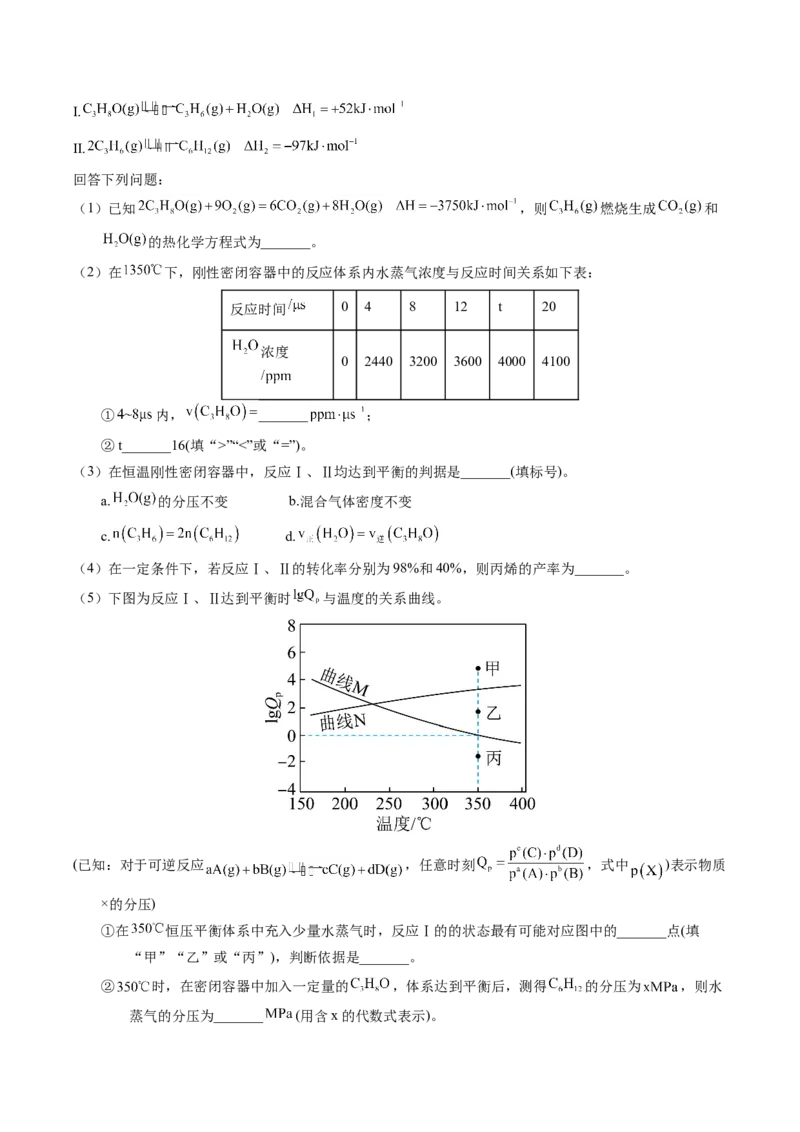
(4)研究组用吸收光谱法研究了(3)中M与L反应体系。当 时,测得平衡时各物
种 随 的变化曲线如图。 时,计算M的平衡转化率
(写出计算过程,结果保留两位有效数字)。
4.【2022年福建卷】异丙醇 可由生物质转化得到,催化异丙醇脱水制取高值化学品丙烯
的工业化技术已引起人们的关注,其主要反应如下:Ⅰ.
Ⅱ.
回答下列问题:
(1)已知 ,则 燃烧生成 和
的热化学方程式为_______。
(2)在 下,刚性密闭容器中的反应体系内水蒸气浓度与反应时间关系如下表:
反应时间 0 4 8 12 t 20
浓度
0 2440 3200 3600 4000 4100
① 内, _______ ;
②t_______16(填“>”“<”或“=”)。
(3)在恒温刚性密闭容器中,反应Ⅰ、Ⅱ均达到平衡的判据是_______(填标号)。
a. 的分压不变 b.混合气体密度不变
c. d.
(4)在一定条件下,若反应Ⅰ、Ⅱ的转化率分别为98%和40%,则丙烯的产率为_______。
(5)下图为反应Ⅰ、Ⅱ达到平衡时 与温度的关系曲线。
(已知:对于可逆反应 ,任意时刻 ,式中 )表示物质
×的分压)
①在 恒压平衡体系中充入少量水蒸气时,反应Ⅰ的的状态最有可能对应图中的_______点(填
“甲”“乙”或“丙”),判断依据是_______。
② 时,在密闭容器中加入一定量的 ,体系达到平衡后,测得 的分压为 ,则水
蒸气的分压为_______ (用含x的代数式表示)。5.【2022年上海卷】利用 催化氮气合成氨气,并生成CO、 等燃料气的方程式如下所示:
反应①:
反应②:
(1)氮原子核外电子排布式为:_______。
(2)比较C、N、O原子的半径大小:_______。
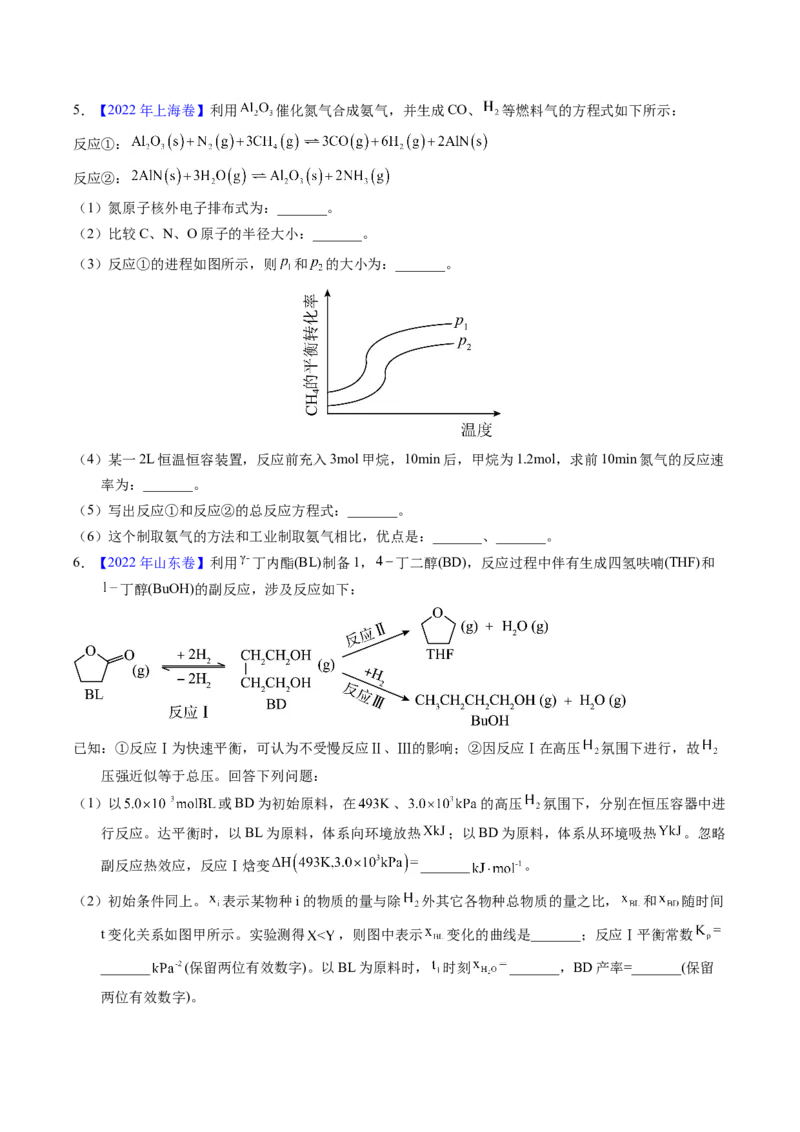
(3)反应①的进程如图所示,则 和 的大小为:_______。
(4)某一2L恒温恒容装置,反应前充入3mol甲烷,10min后,甲烷为1.2mol,求前10min氮气的反应速
率为:_______。
(5)写出反应①和反应②的总反应方程式:_______。
(6)这个制取氨气的方法和工业制取氨气相比,优点是:_______、_______。
6.【2022年山东卷】利用 丁内酯(BL)制备1, 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和
丁醇(BuOH)的副反应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压 氛围下进行,故
压强近似等于总压。回答下列问题:
(1)以 或BD为初始原料,在 、 的高压 氛围下,分别在恒压容器中进
行反应。达平衡时,以BL为原料,体系向环境放热 ;以BD为原料,体系从环境吸热 。忽略
副反应热效应,反应Ⅰ焓变 _______ 。
(2)初始条件同上。 表示某物种i的物质的量与除 外其它各物种总物质的量之比, 和 随时间
t变化关系如图甲所示。实验测得 ,则图中表示 变化的曲线是_______;反应Ⅰ平衡常数
_______ (保留两位有效数字)。以BL为原料时, 时刻 _______,BD产率=_______(保留
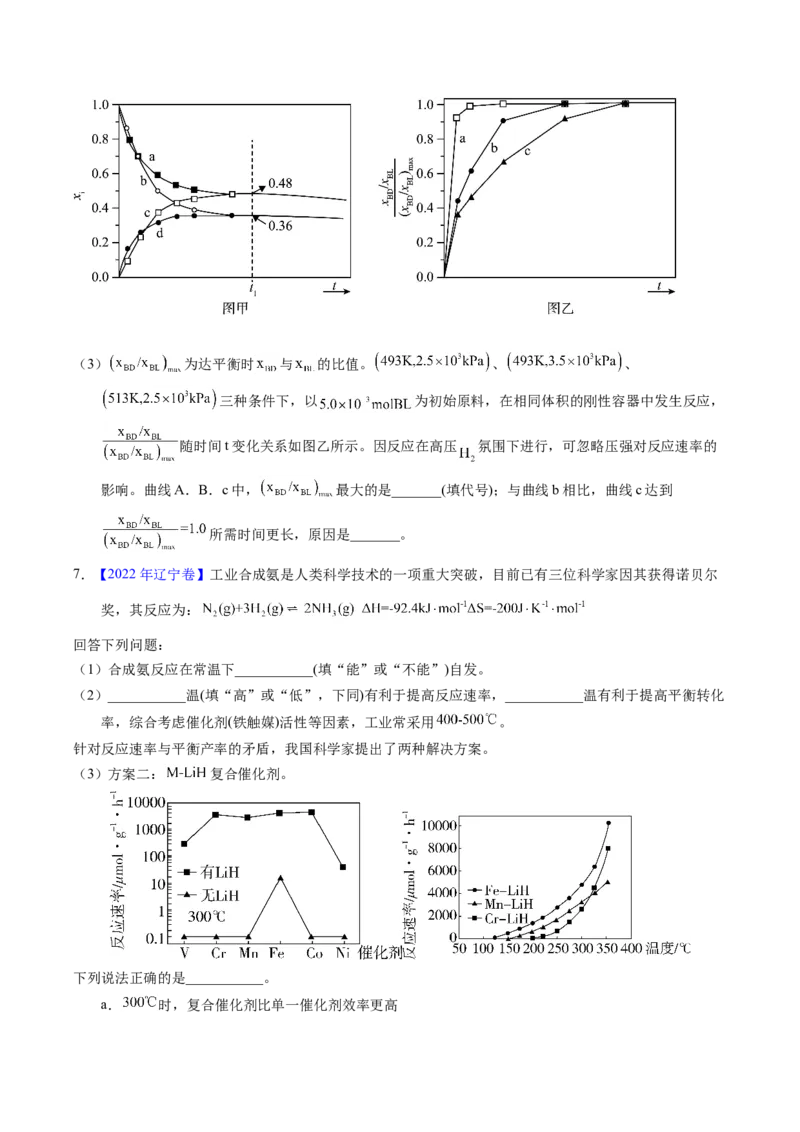
两位有效数字)。(3) 为达平衡时 与 的比值。 、 、
三种条件下,以 为初始原料,在相同体积的刚性容器中发生反应,
随时间t变化关系如图乙所示。因反应在高压 氛围下进行,可忽略压强对反应速率的
影响。曲线A.B.c中, 最大的是_______(填代号);与曲线b相比,曲线c达到
所需时间更长,原因是_______。
7.【2022年辽宁卷】工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔
奖,其反应为:
回答下列问题:
(1)合成氨反应在常温下___________(填“能”或“不能”)自发。
(2)___________温(填“高”或“低”,下同)有利于提高反应速率,___________温有利于提高平衡转化
率,综合考虑催化剂(铁触媒)活性等因素,工业常采用 。
针对反应速率与平衡产率的矛盾,我国科学家提出了两种解决方案。
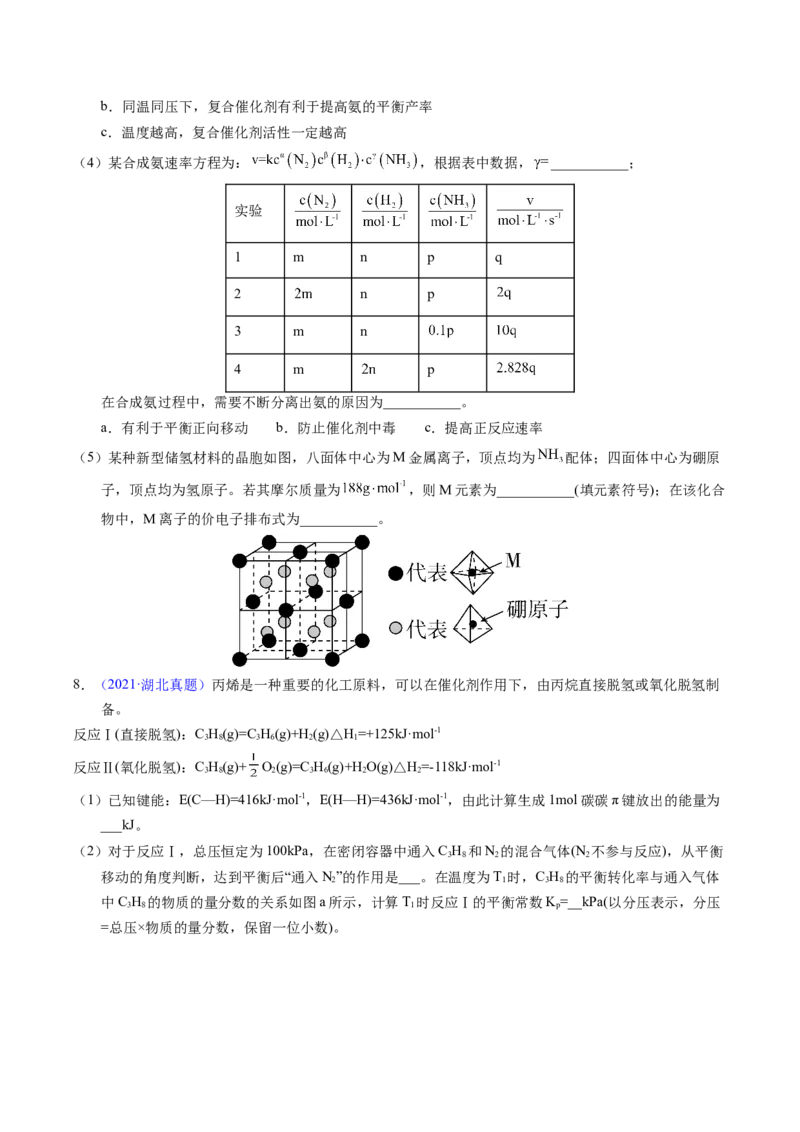
(3)方案二: 复合催化剂。
下列说法正确的是___________。
a. 时,复合催化剂比单一催化剂效率更高b.同温同压下,复合催化剂有利于提高氨的平衡产率
c.温度越高,复合催化剂活性一定越高
(4)某合成氨速率方程为: ,根据表中数据, ___________;
实验
1 m n p q
2 n p
3 m n
4 m p
在合成氨过程中,需要不断分离出氨的原因为___________。
a.有利于平衡正向移动 b.防止催化剂中毒 c.提高正反应速率
(5)某种新型储氢材料的晶胞如图,八面体中心为M金属离子,顶点均为 配体;四面体中心为硼原
子,顶点均为氢原子。若其摩尔质量为 ,则M元素为___________(填元素符号);在该化合
物中,M离子的价电子排布式为___________。
8.(2021·湖北真题)丙烯是一种重要的化工原料,可以在催化剂作用下,由丙烷直接脱氢或氧化脱氢制
备。
反应Ⅰ(直接脱氢):C H(g)=C H(g)+H(g)△H=+125kJ·mol-1
3 8 3 6 2 1
反应Ⅱ(氧化脱氢):C H(g)+ O(g)=C H(g)+HO(g)△H=-118kJ·mol-1
3 8 2 3 6 2 2
(1)已知键能:E(C—H)=416kJ·mol-1,E(H—H)=436kJ·mol-1,由此计算生成1mol碳碳π键放出的能量为
___kJ。
(2)对于反应Ⅰ,总压恒定为100kPa,在密闭容器中通入C H 和N 的混合气体(N 不参与反应),从平衡
3 8 2 2
移动的角度判断,达到平衡后“通入N”的作用是___。在温度为T 时,C H 的平衡转化率与通入气体
2 1 3 8
中C H 的物质的量分数的关系如图a所示,计算T 时反应Ⅰ的平衡常数K=__kPa(以分压表示,分压
3 8 1 p
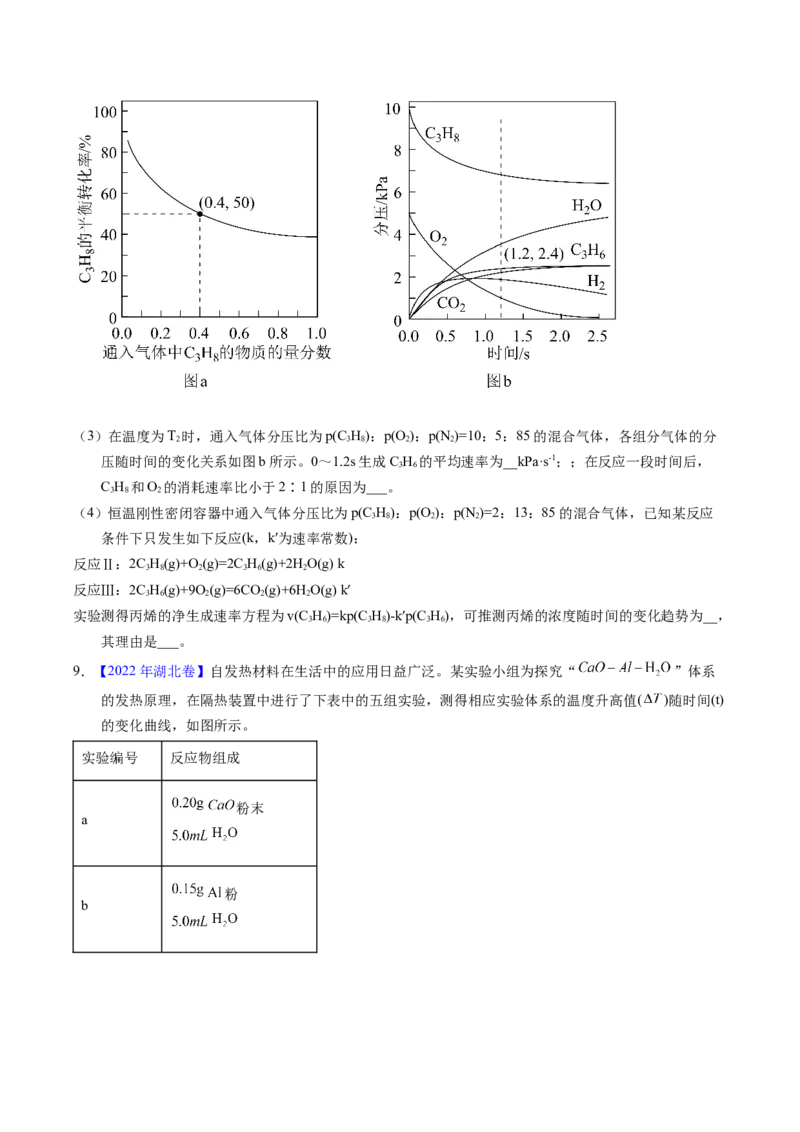
=总压×物质的量分数,保留一位小数)。(3)在温度为T 时,通入气体分压比为p(C H):p(O ):p(N )=10:5:85的混合气体,各组分气体的分
2 3 8 2 2
压随时间的变化关系如图b所示。0~1.2s生成C H 的平均速率为__kPa·s-1;;在反应一段时间后,
3 6
C H 和O 的消耗速率比小于2∶1的原因为___。
3 8 2
(4)恒温刚性密闭容器中通入气体分压比为p(C H):p(O ):p(N )=2:13:85的混合气体,已知某反应
3 8 2 2
条件下只发生如下反应(k,k′为速率常数):
反应Ⅱ:2C H(g)+O(g)=2C H(g)+2HO(g) k
3 8 2 3 6 2
反应Ⅲ:2C H(g)+9O(g)=6CO (g)+6HO(g) k′
3 6 2 2 2
实验测得丙烯的净生成速率方程为v(C H)=kp(C H)-k′p(C H),可推测丙烯的浓度随时间的变化趋势为__,
3 6 3 8 3 6
其理由是___。
9.【2022年湖北卷】自发热材料在生活中的应用日益广泛。某实验小组为探究“ ”体系
的发热原理,在隔热装置中进行了下表中的五组实验,测得相应实验体系的温度升高值( )随时间(t)
的变化曲线,如图所示。
实验编号 反应物组成
粉末
a
粉
b粉
c
饱和石灰水
粉
d
石灰乳
粉
e 粉末
回答下列问题:
(1)已知:
①
②
③
则 的 ___________ 。
(2)温度为T时, ,则 饱和溶液中 ___________(用含x的代数式
表示)。
(3)实验a中, 后 基本不变,原因是___________。
(4)实验b中, 的变化说明 粉与 在该条件下___________(填“反应”或“不反应”)。实验c中,前 的 有变化,其原因是___________; 后 基本不变,其原因是___________微粒
的量有限。
(5)下列说法不能解释实验d在 内温度持续升高的是___________(填标号)。
A.反应②的发生促使反应①平衡右移
B.反应③的发生促使反应②平衡右移
C.气体的逸出促使反应③向右进行
D.温度升高导致反应速率加快
(6)归纳以上实验结果,根据实验e的特征,用文字简述其发热原理___________。
10.【2022年海南卷】某空间站的生命保障系统功能之一是实现氧循环,其中涉及反应:
回答问题:
(1)已知:电解液态水制备 ,电解反应的 。由此计算 的燃烧热(焓)
_______ 。
(2)已知: 的平衡常数(K)与反应温度(t)之间的关系如图1所示。
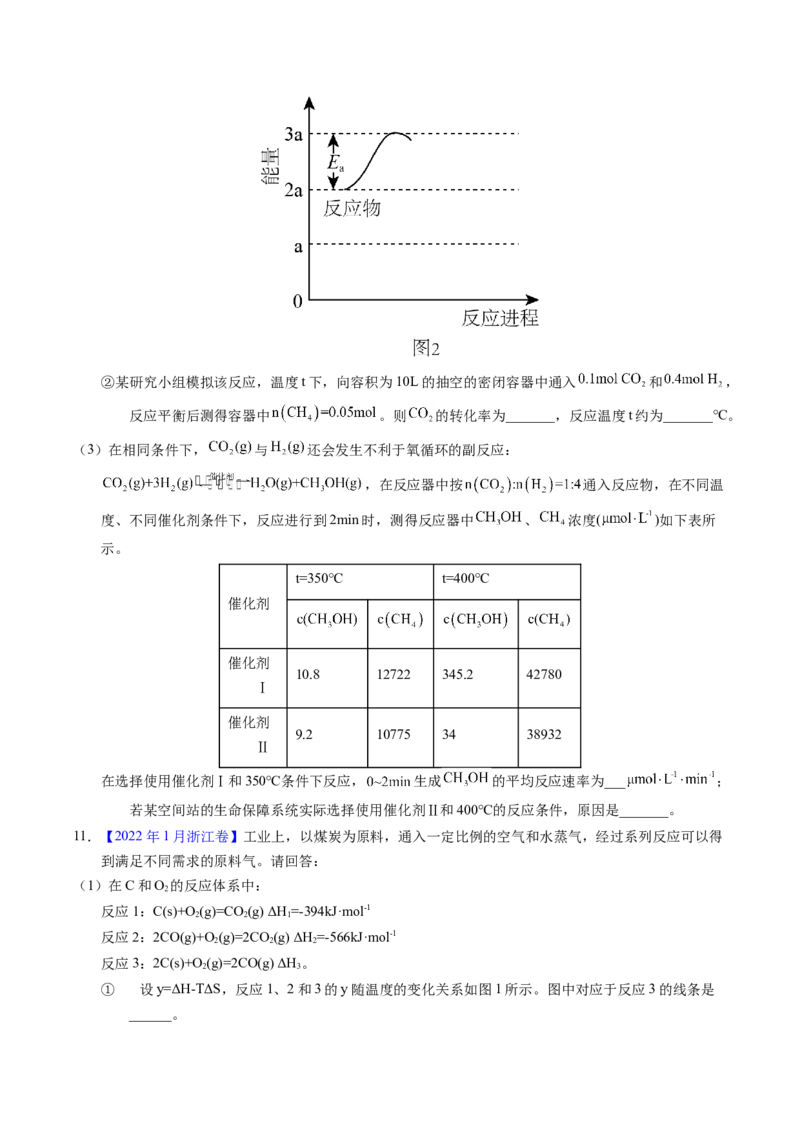
①若反应为基元反应,且反应的 与活化能(Ea)的关系为 。补充完成该反应过程的能量变化
示意图(图2)_______。②某研究小组模拟该反应,温度t下,向容积为10L的抽空的密闭容器中通入 和 ,
反应平衡后测得容器中 。则 的转化率为_______,反应温度t约为_______℃。
(3)在相同条件下, 与 还会发生不利于氧循环的副反应:
,在反应器中按 通入反应物,在不同温
度、不同催化剂条件下,反应进行到2min时,测得反应器中 、 浓度( )如下表所
示。
t=350℃ t=400℃
催化剂
催化剂
10.8 12722 345.2 42780
Ⅰ
催化剂
9.2 10775 34 38932
Ⅱ
在选择使用催化剂Ⅰ和350℃条件下反应, 生成 的平均反应速率为___ ;
若某空间站的生命保障系统实际选择使用催化剂Ⅱ和400℃的反应条件,原因是_______。
11.【2022年1月浙江卷】工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得
到满足不同需求的原料气。请回答:
(1)在C和O 的反应体系中:
2
反应1:C(s)+O(g)=CO (g) ΔH =-394kJ·mol-1
2 2 1
反应2:2CO(g)+O(g)=2CO (g) ΔH =-566kJ·mol-1
2 2 2
反应3:2C(s)+O(g)=2CO(g) ΔH 。
2 3
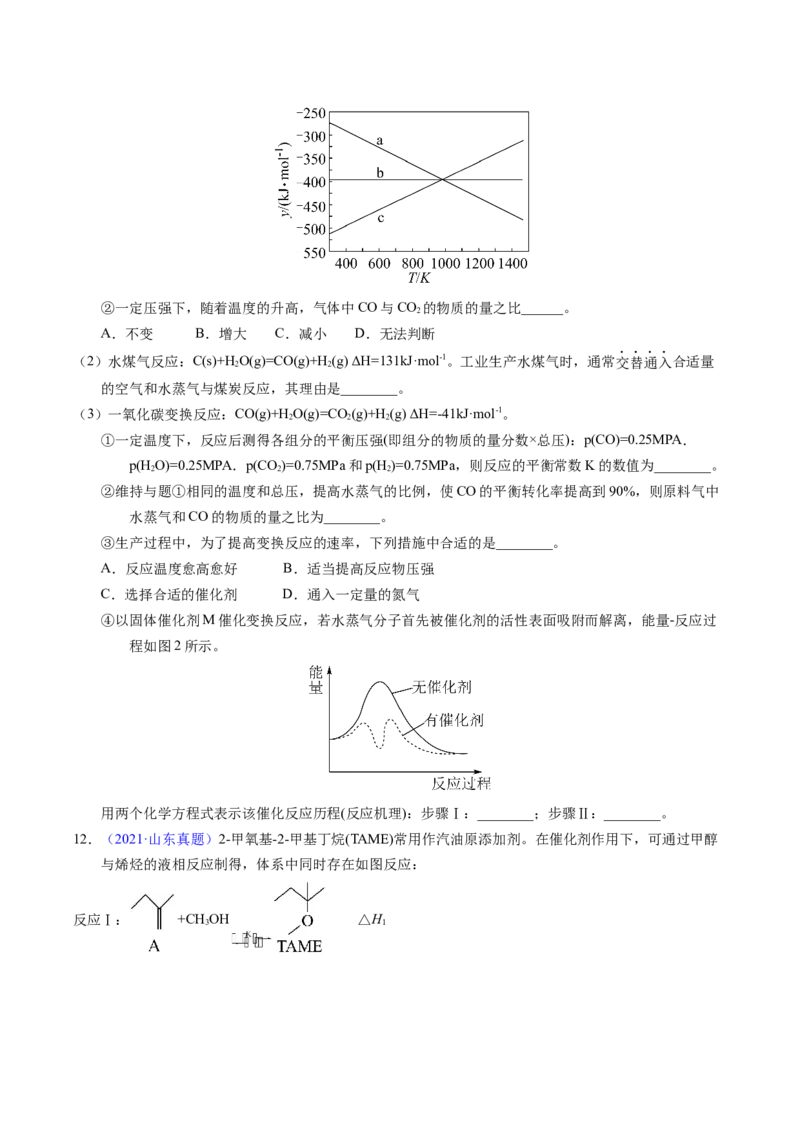
① 设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是
______。②一定压强下,随着温度的升高,气体中CO与CO 的物质的量之比______。
2
A.不变 B.增大 C.减小 D.无法判断
(2)水煤气反应:C(s)+HO(g)=CO(g)+H (g) ΔH=131kJ·mol-1。工业生产水煤气时,通常交替通入合适量
2 2
的空气和水蒸气与煤炭反应,其理由是________。
(3)一氧化碳变换反应:CO(g)+HO(g)=CO(g)+H(g) ΔH=-41kJ·mol-1。
2 2 2
①一定温度下,反应后测得各组分的平衡压强(即组分的物质的量分数×总压):p(CO)=0.25MPA.
p(H O)=0.25MPA.p(CO)=0.75MPa和p(H )=0.75MPa,则反应的平衡常数K的数值为________。
2 2 2
②维持与题①相同的温度和总压,提高水蒸气的比例,使CO的平衡转化率提高到90%,则原料气中
水蒸气和CO的物质的量之比为________。
③生产过程中,为了提高变换反应的速率,下列措施中合适的是________。
A.反应温度愈高愈好 B.适当提高反应物压强
C.选择合适的催化剂 D.通入一定量的氮气
④以固体催化剂M催化变换反应,若水蒸气分子首先被催化剂的活性表面吸附而解离,能量-反应过
程如图2所示。
用两个化学方程式表示该催化反应历程(反应机理):步骤Ⅰ:________;步骤Ⅱ:________。
12.(2021·山东真题)2-甲氧基-2-甲基丁烷(TAME)常用作汽油原添加剂。在催化剂作用下,可通过甲醇
与烯烃的液相反应制得,体系中同时存在如图反应:
反应Ⅰ: +CH OH △H
3 1反应Ⅱ: +CH OH △H
3 2
反应Ⅲ: △H
3
回答下列问题:
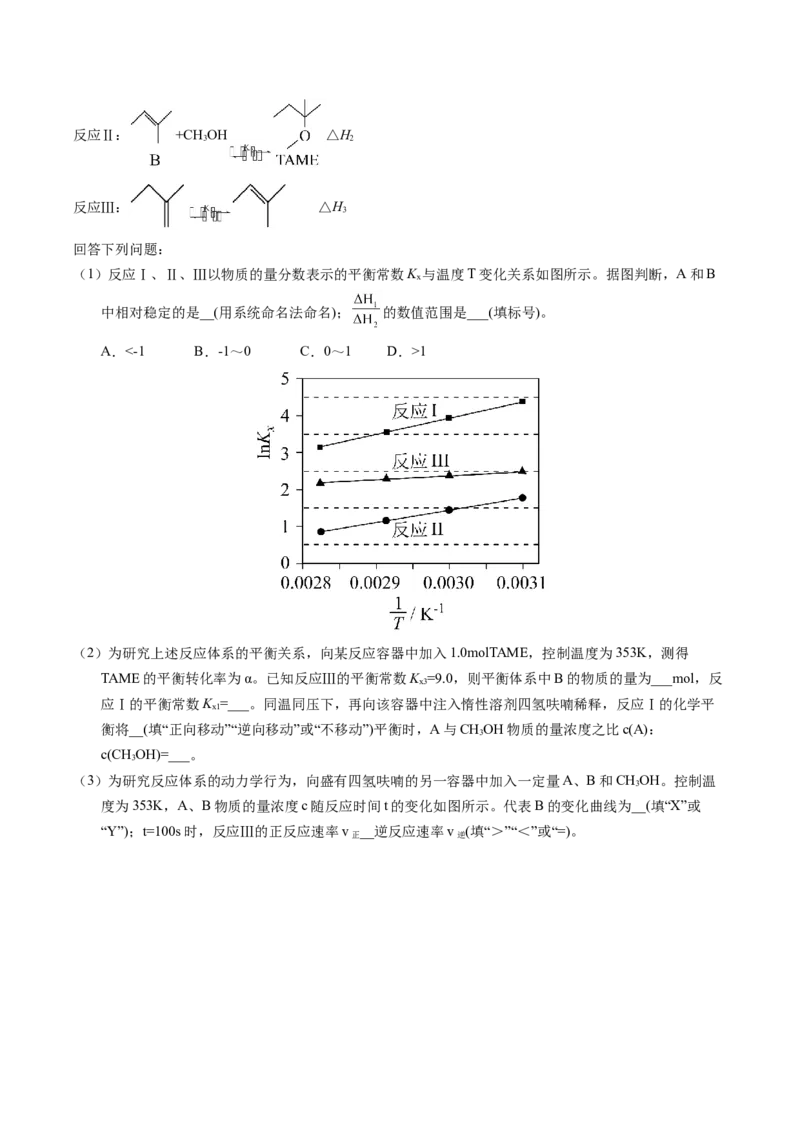
(1)反应Ⅰ、Ⅱ、Ⅲ以物质的量分数表示的平衡常数K 与温度T变化关系如图所示。据图判断,A和B
x
中相对稳定的是__(用系统命名法命名); 的数值范围是___(填标号)。
A.<-1 B.-1~0 C.0~1 D.>1
(2)为研究上述反应体系的平衡关系,向某反应容器中加入1.0molTAME,控制温度为353K,测得
TAME的平衡转化率为α。已知反应Ⅲ的平衡常数K =9.0,则平衡体系中B的物质的量为___mol,反
x3
应Ⅰ的平衡常数K =___。同温同压下,再向该容器中注入惰性溶剂四氢呋喃稀释,反应Ⅰ的化学平
x1
衡将__(填“正向移动”“逆向移动”或“不移动”)平衡时,A与CHOH物质的量浓度之比c(A):
3
c(CHOH)=___。
3
(3)为研究反应体系的动力学行为,向盛有四氢呋喃的另一容器中加入一定量A、B和CHOH。控制温
3
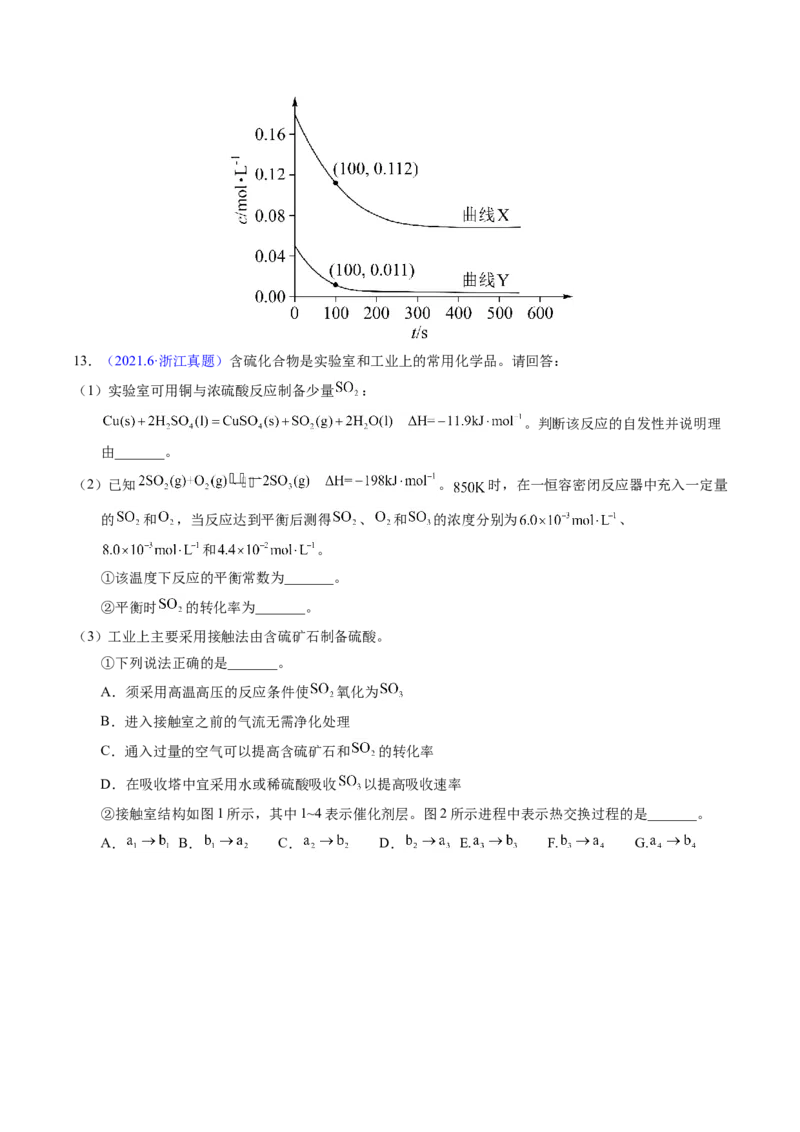
度为353K,A、B物质的量浓度c随反应时间t的变化如图所示。代表B的变化曲线为__(填“X”或
“Y”);t=100s时,反应Ⅲ的正反应速率v __逆反应速率v (填“>”“<”或“=)。
正 逆13.(2021.6·浙江真题)含硫化合物是实验室和工业上的常用化学品。请回答:
(1)实验室可用铜与浓硫酸反应制备少量 :
。判断该反应的自发性并说明理
由_______。
(2)已知 。 时,在一恒容密闭反应器中充入一定量
的 和 ,当反应达到平衡后测得 、 和 的浓度分别为 、
和 。
①该温度下反应的平衡常数为_______。
②平衡时 的转化率为_______。
(3)工业上主要采用接触法由含硫矿石制备硫酸。
①下列说法正确的是_______。
A.须采用高温高压的反应条件使 氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
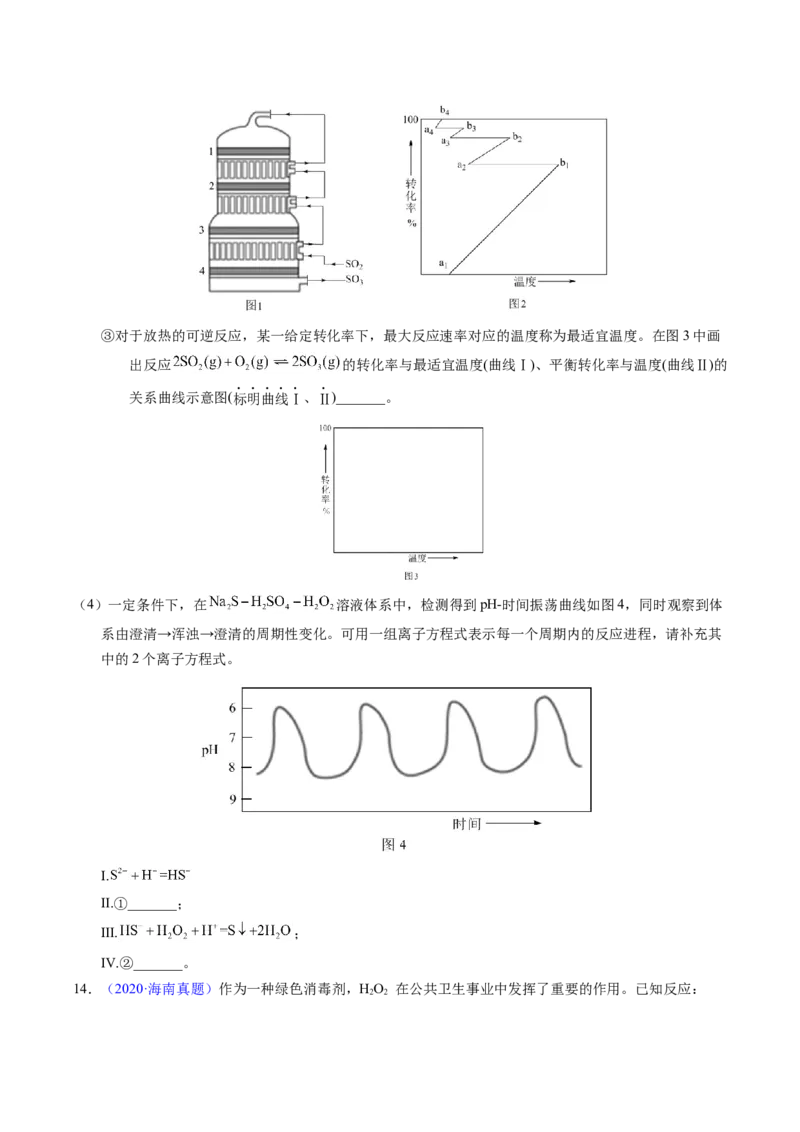
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是_______。
A. B. C. D. E. F. G.③对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在图3中画
出反应 的转化率与最适宜温度(曲线Ⅰ)、平衡转化率与温度(曲线Ⅱ)的
关系曲线示意图(标明曲线Ⅰ、Ⅱ)_______。
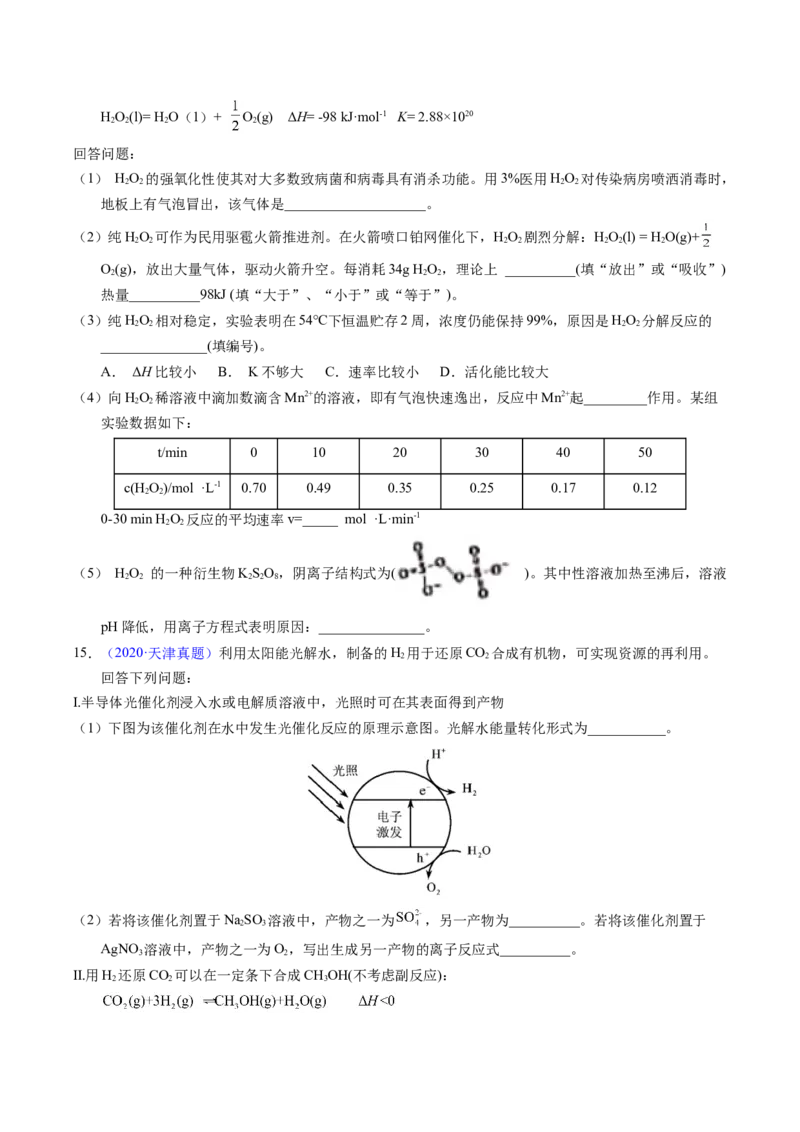
(4)一定条件下,在 溶液体系中,检测得到pH-时间振荡曲线如图4,同时观察到体
系由澄清→浑浊→澄清的周期性变化。可用一组离子方程式表示每一个周期内的反应进程,请补充其
中的2个离子方程式。
Ⅰ.
Ⅱ.①_______;
Ⅲ. ;
Ⅳ.②_______。
14.(2020·海南真题)作为一种绿色消毒剂,HO 在公共卫生事业中发挥了重要的作用。已知反应:
2 2HO(l)= HO(1)+ O(g) ΔH= -98 kJ·mol-1 K= 2.88×1020
2 2 2 2
回答问题:
(1) HO 的强氧化性使其对大多数致病菌和病毒具有消杀功能。用3%医用HO 对传染病房喷洒消毒时,
2 2 2 2
地板上有气泡冒出,该气体是____________________。
(2)纯HO 可作为民用驱雹火箭推进剂。在火箭喷口铂网催化下,HO 剧烈分解:HO(l) = H O(g)+
2 2 2 2 2 2 2
O(g),放出大量气体,驱动火箭升空。每消耗34g H O,理论上 __________(填“放出”或“吸收”)
2 2 2
热量__________98kJ (填“大于”、“小于”或“等于”)。
(3)纯HO 相对稳定,实验表明在54℃下恒温贮存2周,浓度仍能保持99%,原因是HO 分解反应的
2 2 2 2
_______________(填编号)。
A. ΔH比较小 B. K不够大 C.速率比较小 D.活化能比较大
(4)向HO 稀溶液中滴加数滴含Mn2+的溶液,即有气泡快速逸出,反应中Mn2+起_________作用。某组
2 2
实验数据如下:
t/min 0 10 20 30 40 50
c(HO)/mol ·L-1 0.70 0.49 0.35 0.25 0.17 0.12
2 2
0-30 min H O 反应的平均速率v=_____ mol ·L·min-1
2 2
(5) HO 的一种衍生物KSO,阴离子结构式为( )。其中性溶液加热至沸后,溶液
2 2 2 2 8
pH降低,用离子方程式表明原因:_______________。
15.(2020·天津真题)利用太阳能光解水,制备的H 用于还原CO 合成有机物,可实现资源的再利用。
2 2
回答下列问题:
Ⅰ.半导体光催化剂浸入水或电解质溶液中,光照时可在其表面得到产物
(1)下图为该催化剂在水中发生光催化反应的原理示意图。光解水能量转化形式为___________。
(2)若将该催化剂置于NaSO 溶液中,产物之一为 ,另一产物为__________。若将该催化剂置于
2 3
AgNO 溶液中,产物之一为O,写出生成另一产物的离子反应式__________。
3 2
Ⅱ.用H 还原CO 可以在一定条下合成CHOH(不考虑副反应):
2 2 3(3)某温度下,恒容密闭容器中,CO 和H 的起始浓度分别为 a mol‧L-1和3 a mol‧L-1,反应平衡时,
2 2
CHOH的产率为b,该温度下反应平衡常数的值为___________。
3
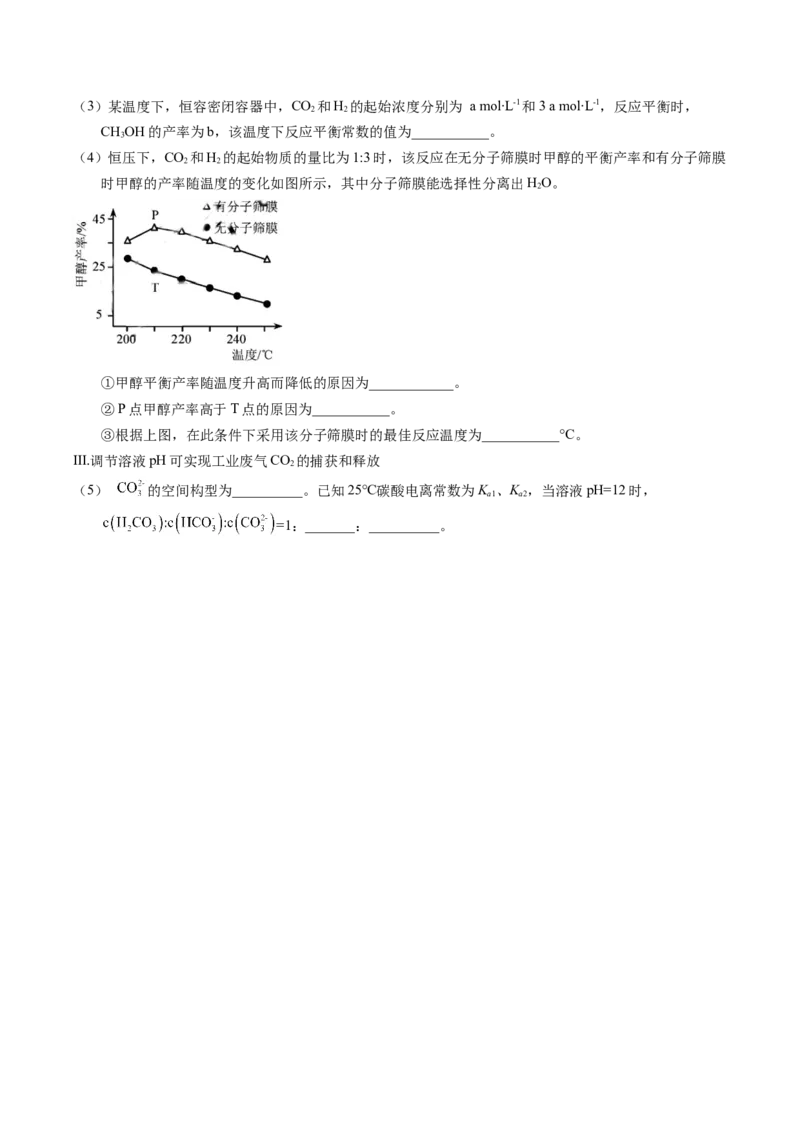
(4)恒压下,CO 和H 的起始物质的量比为1:3时,该反应在无分子筛膜时甲醇的平衡产率和有分子筛膜
2 2
时甲醇的产率随温度的变化如图所示,其中分子筛膜能选择性分离出HO。
2
①甲醇平衡产率随温度升高而降低的原因为____________。
②P点甲醇产率高于T点的原因为___________。
③根据上图,在此条件下采用该分子筛膜时的最佳反应温度为___________°C。
Ⅲ.调节溶液pH可实现工业废气CO 的捕获和释放
2
(5) 的空间构型为__________。已知25℃碳酸电离常数为K 、K ,当溶液pH=12时,
a1 a2
=1:_______:__________。