文档内容
贵阳市第一中学 2025-2026 学年高三上学期开学检测化学
试卷
一、选择题(本大题共 14 小题)
1.广府文化是中华文明的重要组成,其代表有“广绣”“广州彩瓷”“镬耳屋”“广府菜”等。下列
说法错误的是
A.使用蚕丝制作“广绣”,蚕丝的主要成分是蛋白质,属于天然高分子
B.使用黏土烧制“广州彩瓷”,烧制过程中黏土发生了化学变化
C.使用青砖建造“镬耳屋”,青砖的青色来自 Fe(OH)
3
D.添加小苏打蒸制“广府菜”糕点,小苏打是 NaHCO ,属于强电解质
3
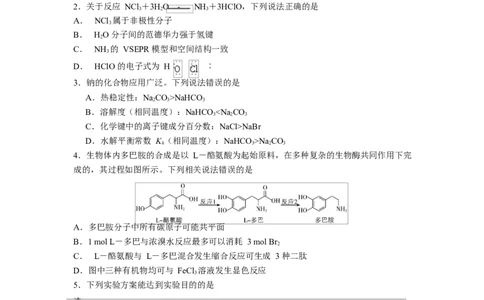
2.关于反应 NCl +3HO NH +3HClO,下列说法正确的是
3 2 3
A. NCl 属于非极性分子
3
B. HO 分子间的范德华力强于氢键
2
C. NH 的 VSEPR 模型和空间结构一致
3
D. HClO 的电子式为 H︰ ︰ ︰
3.钠的化合物应用广泛。下列说法错误的是
A.热稳定性:NaCO>NaHCO
2 3 3
B.溶解度(相同温度):NaHCO NaBr
D.水解平衡常数 K (相同温度):NaHCO >Na CO
h 3 2 3
4.生物体内多巴胺的合成是以 L-酪氨酸为起始原料,在多种复杂的生物酶共同作用下完
成的,其过程如图所示。下列相关说法错误的是
A.多巴胺分子中所有碳原子可能共平面
B.1 mol L-多巴与浓溴水反应最多可以消耗 3 mol Br
2
C. L-酪氨酸与 L-多巴混合发生缩合反应可生成 3 种二肽
D.图中三种有机物均可与 FeCl 溶液发生显色反应
3
5.下列实验方案能达到实验目的的是
选
实验目的 实验方
项 案
将干燥的淀粉- 试纸放于充
A 验证氯气的氧化性 满纯净 的集气瓶口,观
察现
象
配制
B 准确称量 固体 ,加入 水中,充分搅拌
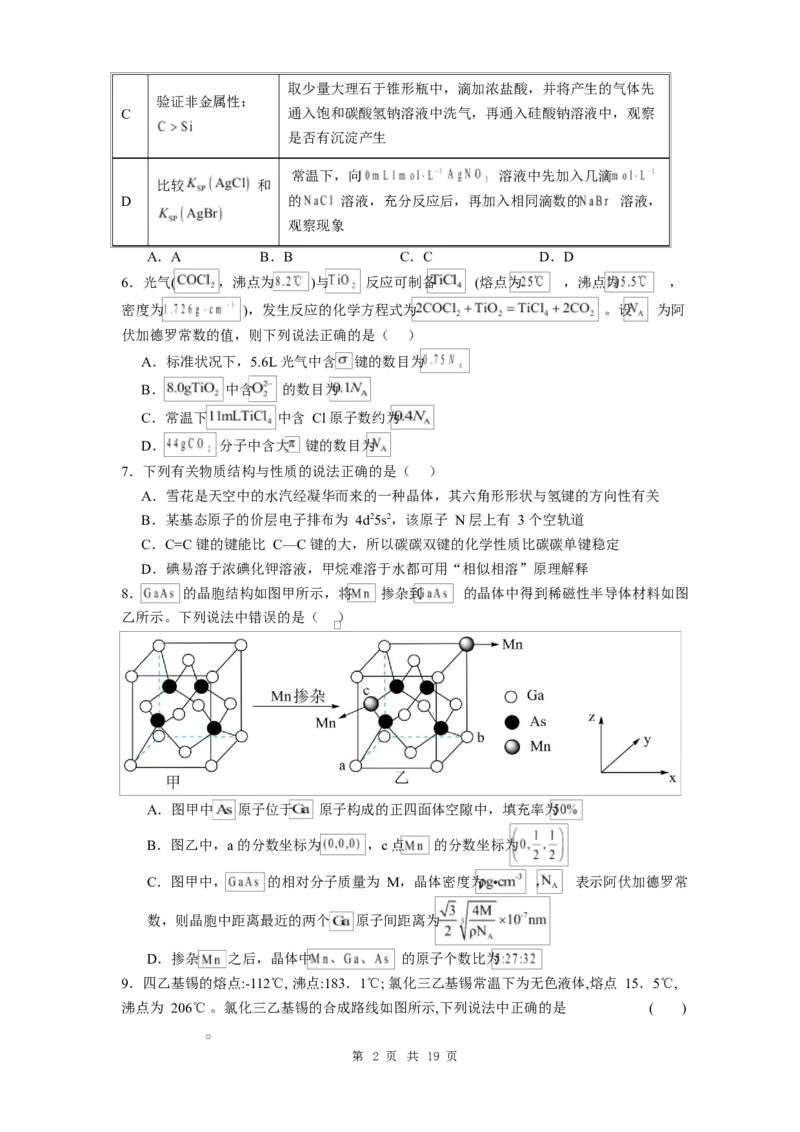
第 1 页 共 19 页取少量大理石于锥形瓶中,滴加浓盐酸,并将产生的气体先
验证非金属性:
C 通入饱和碳酸氢钠溶液中洗气,再通入硅酸钠溶液中,观察
是否有沉淀产生
常温下,向 溶液中先加入几滴
比较 和
D 的 溶液,充分反应后,再加入相同滴数的 溶液,
观察现象
A.A B.B C.C D.D
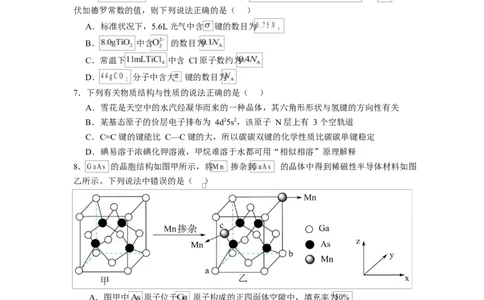
6.光气( ,沸点为 )与 反应可制备 (熔点为 ,沸点为 ,
密度为 ),发生反应的化学方程式为 。设 为阿
伏加德罗常数的值,则下列说法正确的是( )
A.标准状况下,5.6L 光气中含 键的数目为
B. 中含 的数目为
C.常温下 中含 Cl 原子数约为
D. 分子中含大 键的数目为
7.下列有关物质结构与性质的说法正确的是( )
A.雪花是天空中的水汽经凝华而来的一种晶体,其六角形形状与氢键的方向性有关
B.某基态原子的价层电子排布为 4d25s2,该原子 N 层上有 3 个空轨道
C.C=C 键的键能比 C—C 键的大,所以碳碳双键的化学性质比碳碳单键稳定
D.碘易溶于浓碘化钾溶液,甲烷难溶于水都可用“相似相溶”原理解释
8. 的晶胞结构如图甲所示,将 掺杂到 的晶体中得到稀磁性半导体材料如图
乙所示。下列说法中错误的是( )
A.图甲中 原子位于 原子构成的正四面体空隙中,填充率为
B.图乙中,a 的分数坐标为 ,c 点 的分数坐标为
C.图甲中, 的相对分子质量为 M,晶体密度为 , 表示阿伏加德罗常
数,则晶胞中距离最近的两个 原子间距离为
D.掺杂 之后,晶体中 的原子个数比为
9.四乙基锡的熔点:-112℃, 沸点:183.1℃; 氯化三乙基锡常温下为无色液体,熔点 15.5℃,
沸点为 206℃ 。氯化三乙基锡的合成路线如图所示,下列说法中正确的是 ( )
第 2 页 共 19 页A.四乙基锡和氯化三乙基锡中均有 2 种不同化学环境的氢原子
B.氯化三乙基锡和四乙基锡的熔、沸点不同是因其晶体类型不同造成的
C.上述反应中,所有分子中心原子的杂化类型相同,反应前后分子内σ键总数不同
D.氯化三乙基锡中所有原子可能共平面
10.由下列操作及现象不能得出相应结论的是
选
操作及现象
项 结论
向某溶液中先滴
A 加 KSCN 溶 该溶液中含有
液,无明显现
Fe2+
象,再滴加新
制氯水,溶液变
红
B 向浓硝酸中加入红热的碳,产生红棕色气体 碳还原浓硝酸生成 NO
2
向 CuSO 溶液中漓加氨水,生成蓝色沉淀,继续添加氨 乙醇能降低
4
C 水,沉淀溶解得到深蓝色溶液,再加人乙醇,析出深蓝 [Cu(NH )]SO 在水中的
3 4 4
色晶体 溶解度
向对甲基苯甲醛中滴加新制氢氧化铜,加热,产生砖红 对甲基苯甲醛中含有醛
D
色沉淀 基
A.A B.B C.C D.D
11. 和 均可发生水解反应,其中 的水解机理示意图如下:
下列说法错误的是( )
A. 水解过程中只存在极性键的断裂和形成
B. 与 的晶体类型相同
C.分子的极性:
D.由此推断 的水解产物为 和 HClO
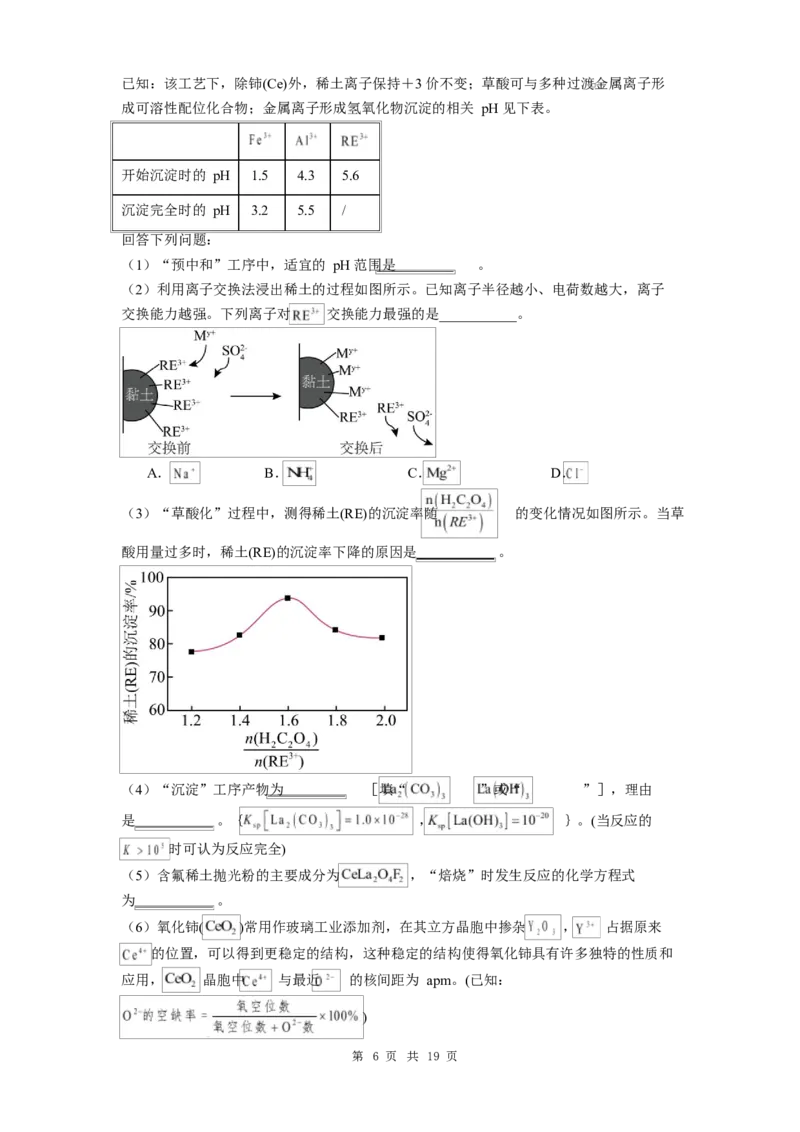
12.硒能增强人体免疫功能,抗氧化,延缓衰老,有效抑制肿瘤生长。实验室模拟工业上
由含硒废料(主要含 、 、 、 、 、 等)制取硒的流程如下:
下列有关说法正确的是
第 3 页 共 19 页A.“分离”前,将废料粉碎可以提高活化分子百分数,加快分离速率
B.“分离”、“酸溶”、“浸取”时都需要用到的玻璃仪器有:烧杯、玻璃棒、分液漏斗
C.“酸化”过程中发生的离子反应为
D.若向“酸溶”所得的滤液中滴入少量 KSCN 溶液,无明显现象
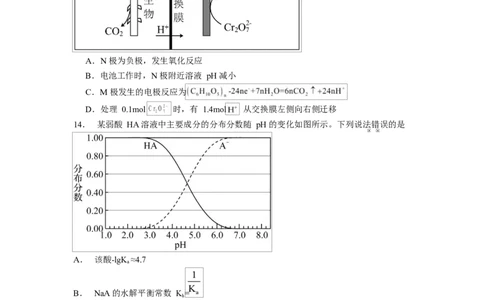
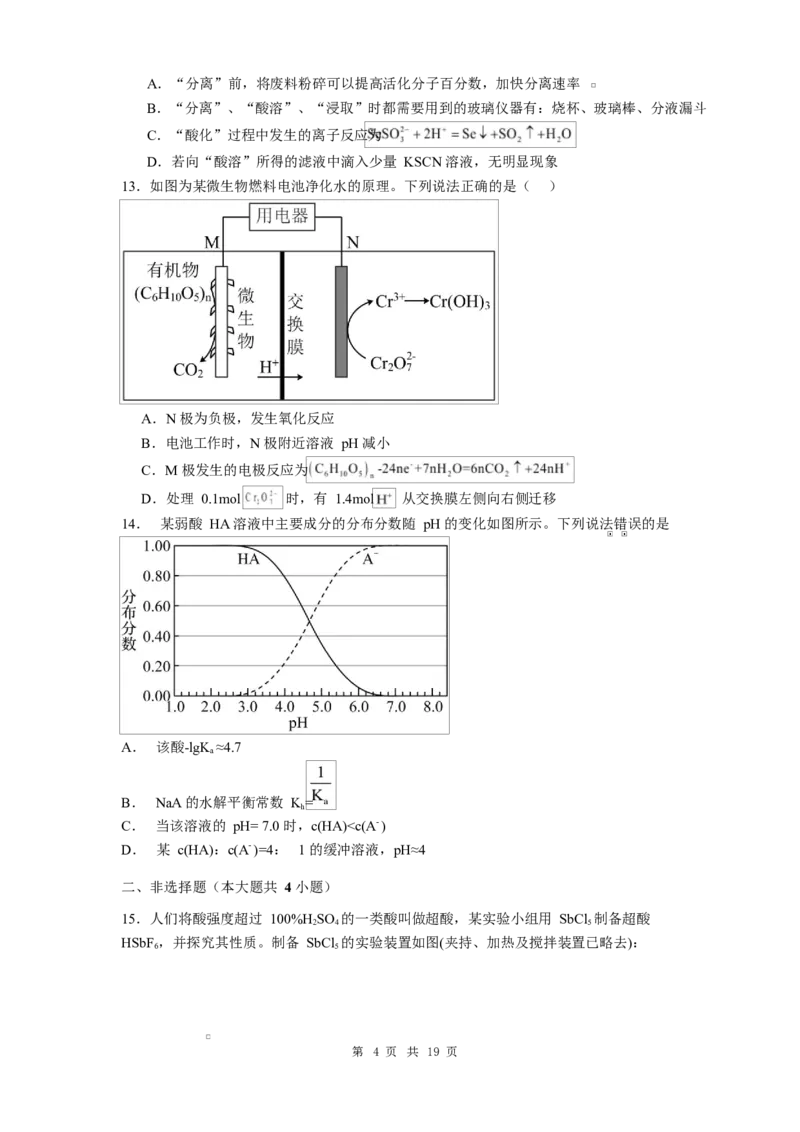
13.如图为某微生物燃料电池净化水的原理。下列说法正确的是( )
A.N 极为负极,发生氧化反应
B.电池工作时,N 极附近溶液 pH 减小
C.M 极发生的电极反应为
D.处理 0.1mol 时,有 1.4mol 从交换膜左侧向右侧迁移
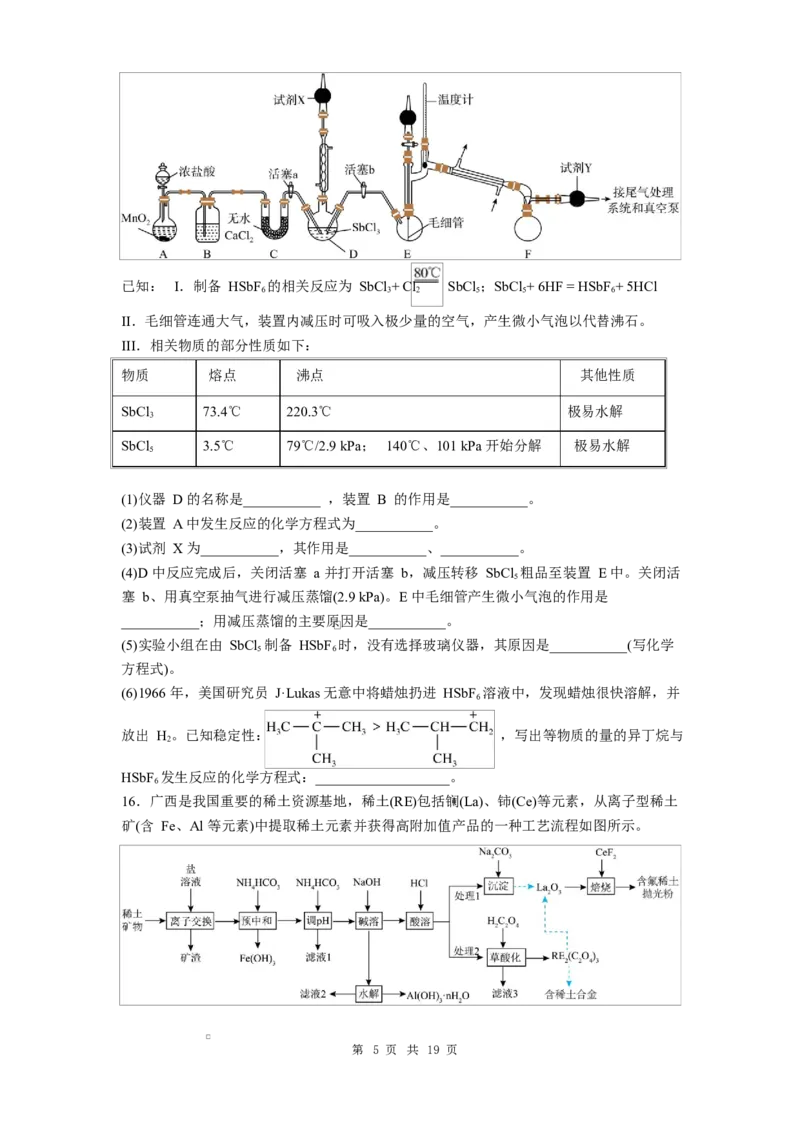
14. 某弱酸 HA 溶液中主要成分的分布分数随 pH 的变化如图所示。下列说法错误的是
A. 该酸-lgK ≈4.7
a
B. NaA 的水解平衡常数 K=
h
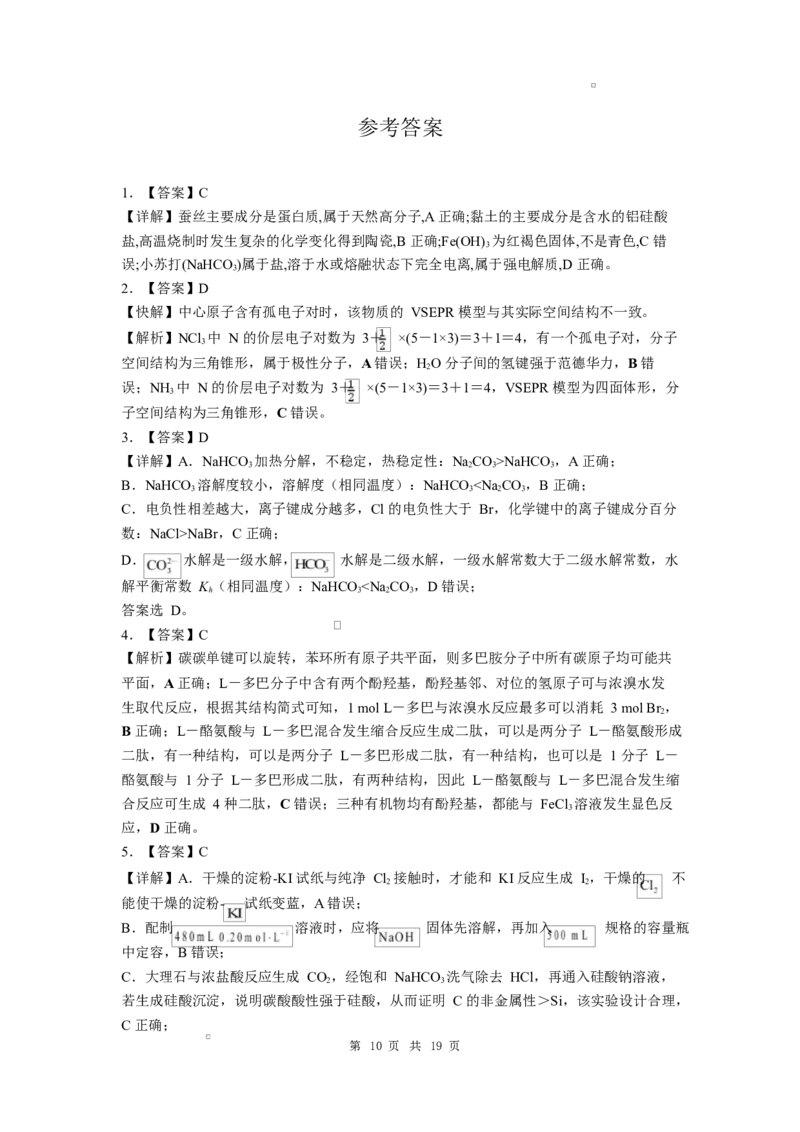
C. 当该溶液的 pH= 7.0 时,c(HA)NaHCO,A 正确;
3 2 3 3
B.NaHCO 溶解度较小,溶解度(相同温度):NaHCO NaBr,C 正确;
D. 水解是一级水解, 水解是二级水解,一级水解常数大于二级水解常数,水
解平衡常数 K (相同温度):NaHCO 105,该反应正向
可以完全转化;
(5)含氟稀土抛光粉的主要成分为 CeLaOF,焙烧时发生的化学反应方程式为:
2 4 2
;
(6)①CeO 晶胞中的 Ce4+数目为 ,则 O2-的数目为 8,掺杂 YO 后,得到
2 2 3
了 n(CeO):n(Y O)=0.6:0.2 的晶体,故晶胞中 n(Ce4+)=0.6×4=2.4mol,n(Y3+)=0.4×
2 2 3
4=1.6mol,n(O2-)=2.4×2+1.6×1.5=7.2mol,故 O2-的空缺率为 ;
② 晶胞中 与最近 的核间距为 apm,CeO 晶胞中 Ce4+与最近的 O2-核间距为体
2
对角线的四分之一,故晶胞的边长为: pm,则该晶胞的密度为
。
17.【答案】(1) ;高温(1 分)
(2) ⅰ;越慢(1 分)
(3) 水蒸气能与 C 发生氧化还原反应,有利于减少积碳,使反应持续进行,且易与产物
分离(合理即可)
(4) 主反应、副反应均为气体体积增大的反应,增大压强,平衡均向逆反应方向移动,
压强越大,乙烷的平衡转化率越小, 条件下乙烷的平衡转化率更小,故压强 更大
(5) 0.57
(6) 温度低于 时,主反应受温度影响较大,随温度升高,乙烯产率增大,温度达
到 时,乙烯产率达到最大值;温度高于 时,副反应受温度影响反应速率加快,
生成大量的 ,抑制了主反应,导致乙烯产率下降
【命题点】以表格的形式直观地展示乙烷裂解过程中化学键的断裂和物质的转化过程,有
助于考生形成对化学反应过程的直观认识,加深对反应机理的理解;以乙烷-二氧化碳催化
氧化制乙烯的工业过程为背景,将理论知识与实际工业应用相结合,使问题具有实际意义。
本题要求考生能够分析多个反应之间的竞争关系,并结合所学知识和图像信息进行推理和
判断,有助于培养考生的知识迁移能力。
【解析】
(1)乙烷、乙烯的标准摩尔生成焓分别为 、 。乙烷热裂解
制乙烯: |
;该反应 , ,自
发进行的条件为高温。
(2)根据表格中乙烷裂解过程各基元反应的活化能比较,活化能最大的反应速率最慢,
为决速步骤,决定反应速率的应该是基元反应ⅰ。
第 15 页 共 19 页(3) 产物中的黑色粉末状物质应为积碳,稀释剂采用水蒸气,除了本身具有稳定、无毒、
廉价、易得、安全等特点外,水蒸气能与 反应发生氧化还原反应,有利于减少积碳,使
反应持续进行,且 易与产物分离。
(4)主反应、副反应均为气体体积增大的反应,增大压强,平衡均向逆反应方向移动,
压强越大,乙烷的平衡转化率越小, 条件下乙烷的平衡转化率更小,故 。
(5)容器容积为 ,加入 和 , 点平衡时乙烷的转化率
为 ,乙烯的选择性为 ,可列三段式:主反应(Ⅰ):
副反应(Ⅱ):
主反应平衡常数 。
(6)一定压强下,以一定流速向反应器中按一定比例通入 和 ,即反应相同的时
间,根据图乙,温度低于 时,主反应受温度影响较大,随温度升高,乙烯产率增大,
温度达到 时,乙烯产率达到最大值;温度高于 时,副反应受温度影响反应速
率加快,生成大量的 ,抑制了主反应,导致乙烯产率下降。
【方法总结】 主副反应共存体系,计算某反应的化学平衡常数,需要各反应均达到平衡
状态时,代入各物质的浓度。
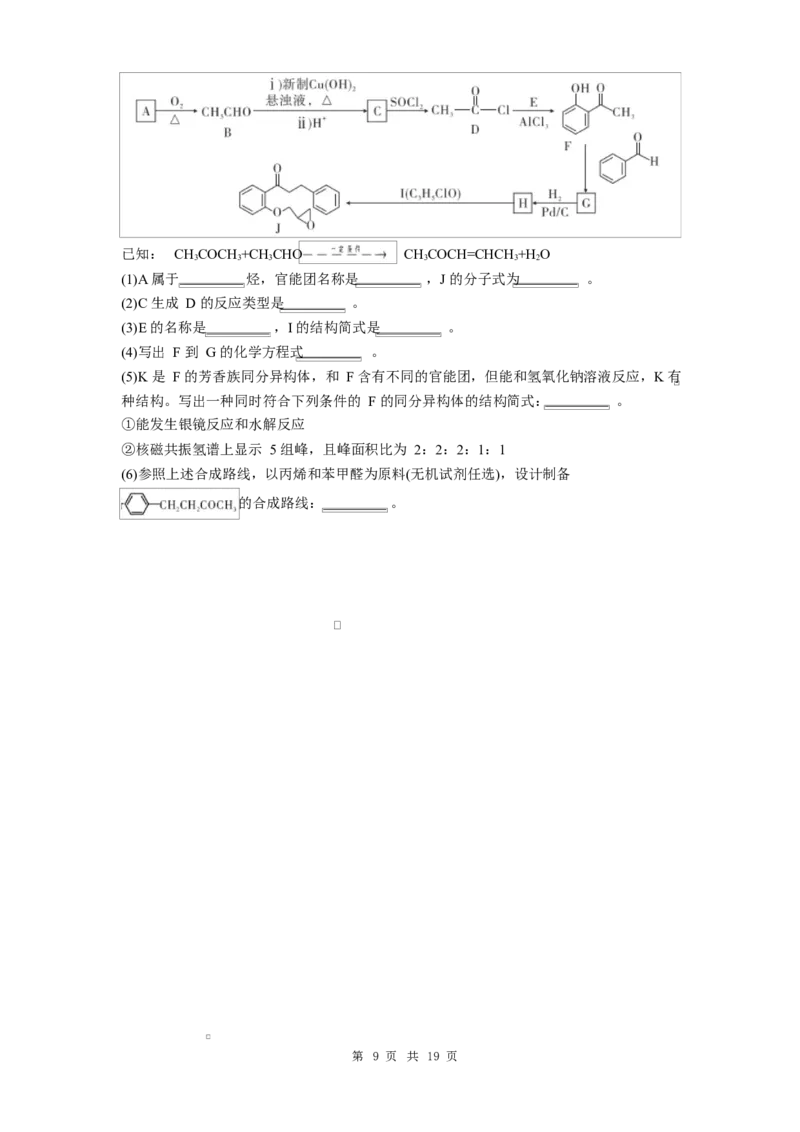
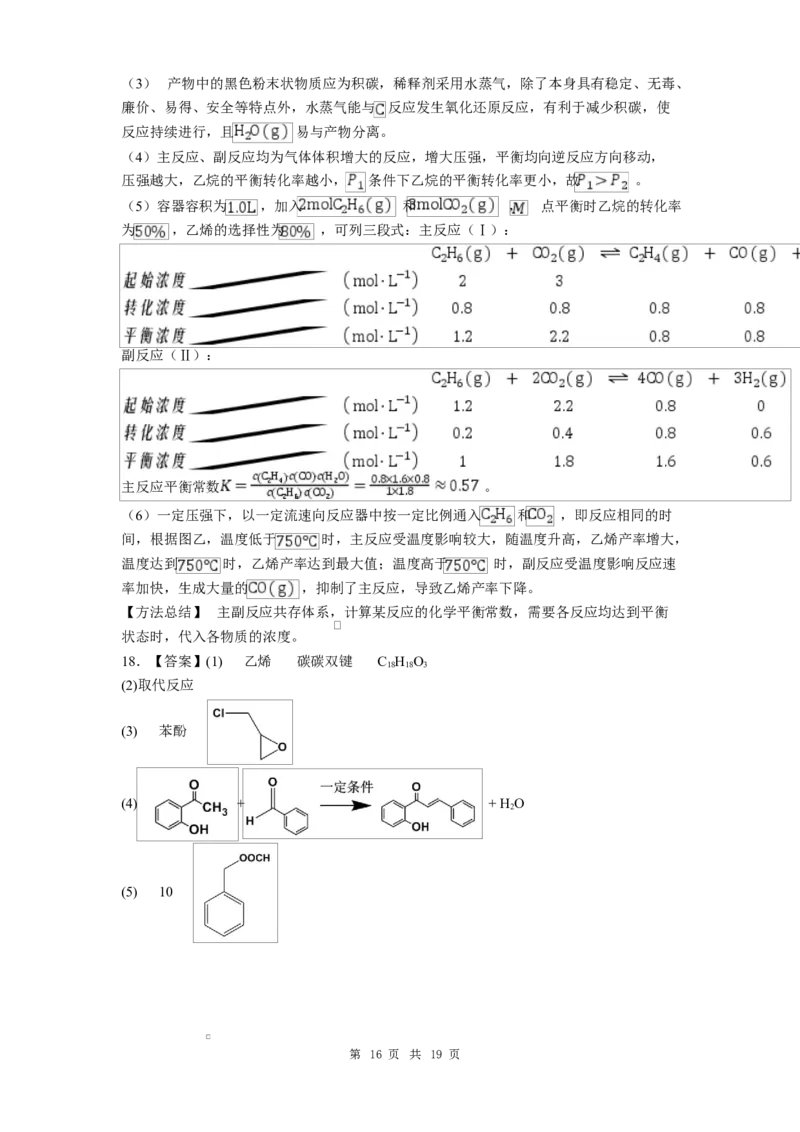
18.【答案】(1) 乙烯 碳碳双键 C H O
18 18 3
(2)取代反应
(3) 苯酚
(4) + + H O
2
(5) 10
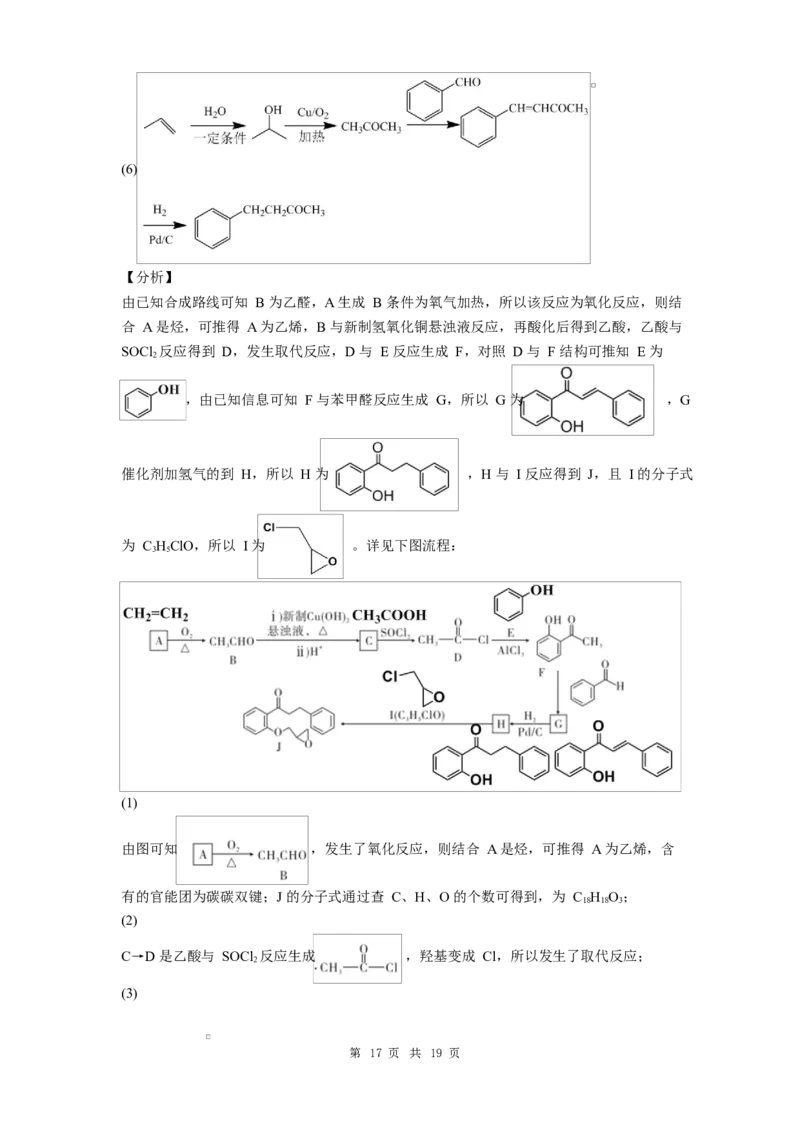
第 16 页 共 19 页(6)
【分析】
由已知合成路线可知 B 为乙醛,A 生成 B 条件为氧气加热,所以该反应为氧化反应,则结
合 A 是烃,可推得 A 为乙烯,B 与新制氢氧化铜悬浊液反应,再酸化后得到乙酸,乙酸与
SOCl 反应得到 D,发生取代反应,D 与 E 反应生成 F,对照 D 与 F 结构可推知 E 为
2
,由已知信息可知 F 与苯甲醛反应生成 G,所以 G 为 ,G
催化剂加氢气的到 H,所以 H 为 ,H 与 I 反应得到 J,且 I 的分子式
为 C HClO,所以 I 为 。详见下图流程:
3 5
(1)
由图可知 ,发生了氧化反应,则结合 A 是烃,可推得 A 为乙烯,含
有的官能团为碳碳双键;J 的分子式通过查 C、H、O 的个数可得到,为 C H O;
18 18 3
(2)
C→D 是乙酸与 SOCl 反应生成 ,羟基变成 Cl,所以发生了取代反应;
2
(3)
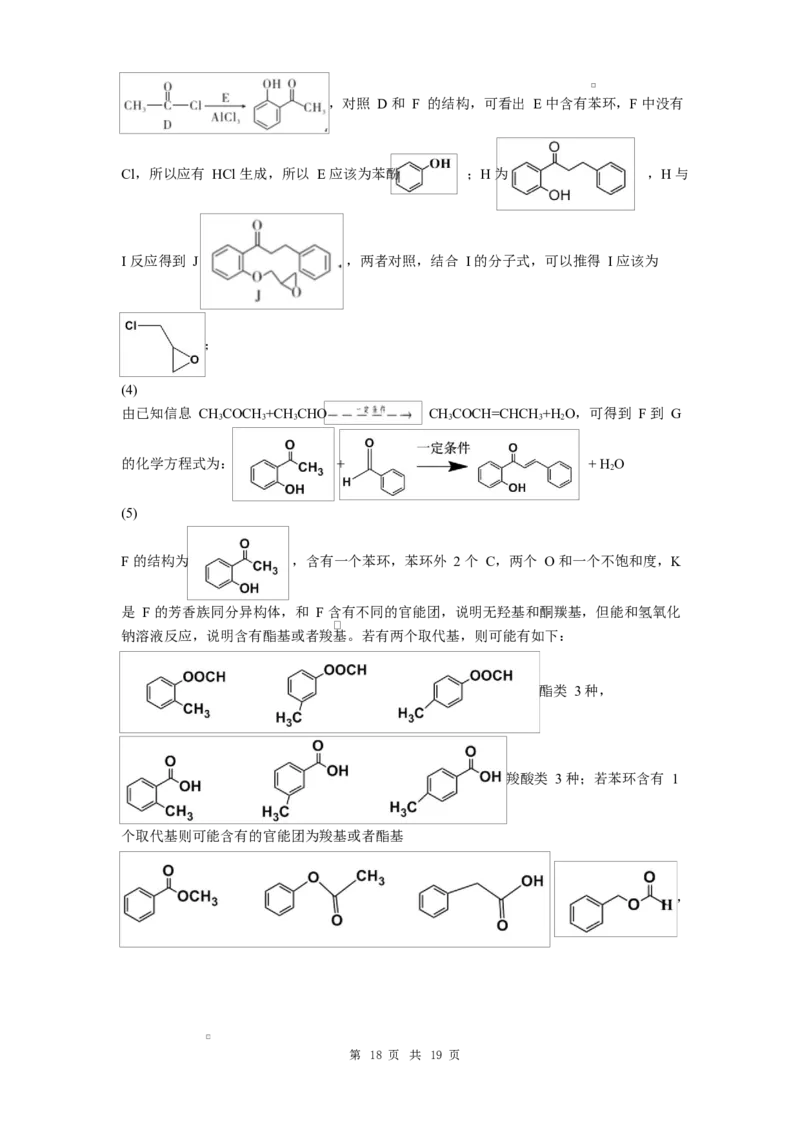
第 17 页 共 19 页,对照 D 和 F 的结构,可看出 E 中含有苯环,F 中没有
Cl,所以应有 HCl 生成,所以 E 应该为苯酚 ;H 为 ,H 与
I 反应得到 J ,两者对照,结合 I 的分子式,可以推得 I 应该为
;
(4)
由已知信息 CHCOCH +CH CHO CHCOCH=CHCH +H O,可得到 F 到 G
3 3 3 3 3 2
的化学方程式为: + + H O
2
(5)
F 的结构为 ,含有一个苯环,苯环外 2 个 C,两个 O 和一个不饱和度,K
是 F 的芳香族同分异构体,和 F 含有不同的官能团,说明无羟基和酮羰基,但能和氢氧化
钠溶液反应,说明含有酯基或者羧基。若有两个取代基,则可能有如下:
酯类 3 种,
羧酸类 3 种;若苯环含有 1
个取代基则可能含有的官能团为羧基或者酯基
,
第 18 页 共 19 页共 4 种,所以共 3+3+4=10 种;K 的结构能发生银镜反应和水解反应,含有官能团 HCOO-,
且核磁共振氢谱上显示 5 组峰,且峰面积比为 2:2:2:1:1,则结构为: ;
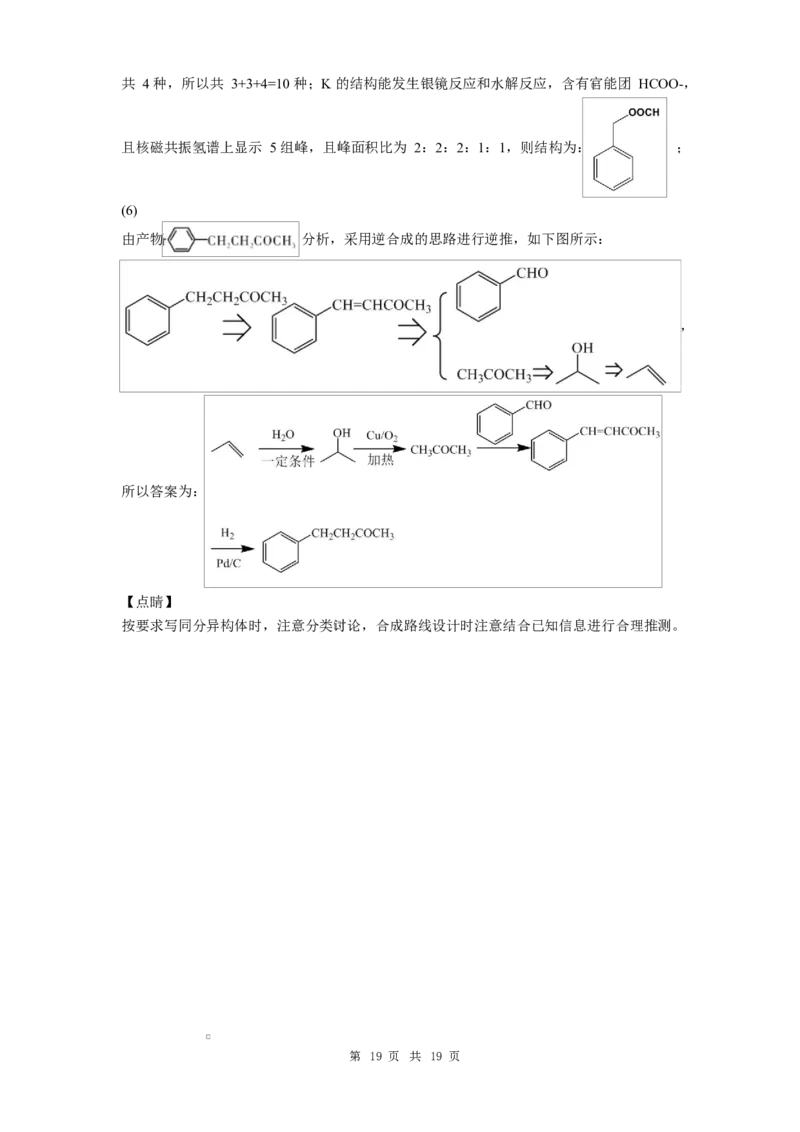
(6)
由产物 分析,采用逆合成的思路进行逆推,如下图所示:
,
所以答案为:
【点睛】
按要求写同分异构体时,注意分类讨论,合成路线设计时注意结合已知信息进行合理推测。
第 19 页 共 19 页