文档内容
【赢在高考·黄金 8 卷】备战 2024 年高考化学模拟卷(新高考七省专用)
黄金卷 05
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Fe 56 Bi 209
第Ⅰ卷
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.“挖掘文物价值,讲好江西故事”。下列文物的主要成分不同于其他三种的是
A.双面神人青铜面具 B.元代青花带盖瓷梅瓶
C.元代“阳平治都功印”铭玉印 D.屈蹲羽人活环玉佩饰
2.下列化学用语或图示表达正确的是
A.HCO的水解方程式为:HCO+H O H O++CO2
3 3 2 3 3
B.H 分子中σ键的电子云轮廓图:
2
C.CaO 的电子式为
2
D.丙烷分子的空间填充模型:
3.下列关于物质性质与用途的说法不正确的是
A.镁在空气中可燃烧,生成氧化镁和氮化镁
B.铝与浓硝酸不反应,可用铝槽运输浓硝酸
C.铁粉具有还原性,可作食品盒中的除氧剂
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002D.二氧化硅导光能力强,可用来制备光导纤维
4.化学与人类生产、生活密切相关,下列有关说法正确的是
A.放置较久的红薯比新挖红薯甜,与葡萄糖的水解有关
B.漂白粉、水玻璃、福尔马林、冰水混合物都是混合物
C.阿司匹林药效释放快,可将它连接在高分子载体上生成长效缓释药物
D.在钢铁部件表面进行发蓝处理属于物理变化
5.在允许加热的前提下,只用一种试剂不能鉴别对应溶液的是
A.用Ba(OH) 溶液鉴别NH Cl、(NH ) SO 、NaCl、Na SO
2 4 4 2 4 2 4
B.用FeCl 溶液鉴别NaI、Ba(OH) 、Na S、NaHCO
3 2 2 3
C.用NaOH溶液鉴别MgCl 、FeCl 、Al (SO ) 、(NH ) SO
2 2 2 4 3 4 2 4
D.用红色石蕊试纸鉴别Na SO 、浓HNO 、NaHCO 、氯水
2 3 3 3
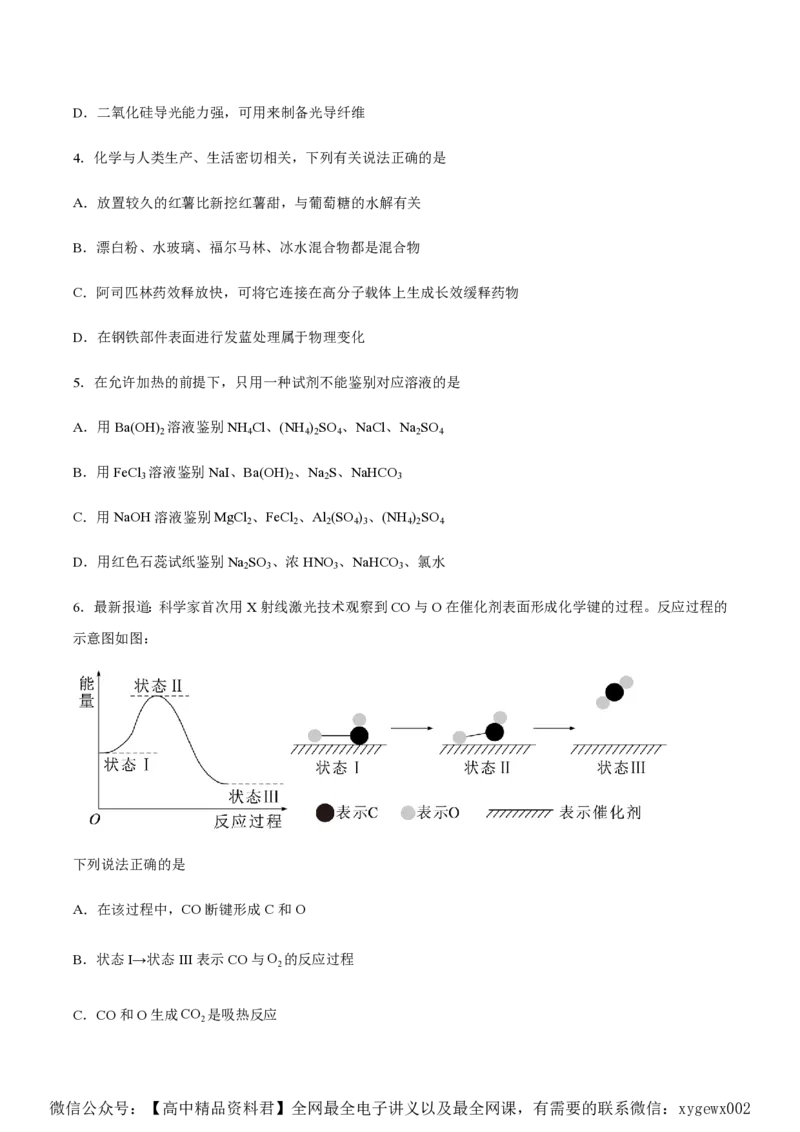
6.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的
示意图如图:
下列说法正确的是
A.在该过程中,CO断键形成C和O
B.状态I→状态III表示CO与O 的反应过程
2
C.CO和O生成CO 是吸热反应
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002D.CO和O生成了具有极性共价键的CO
2
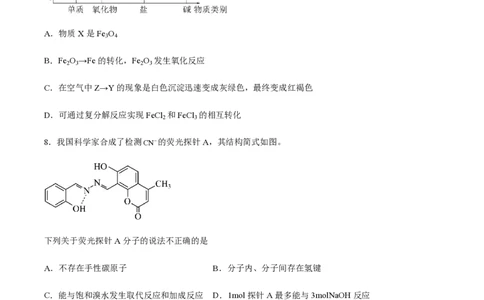
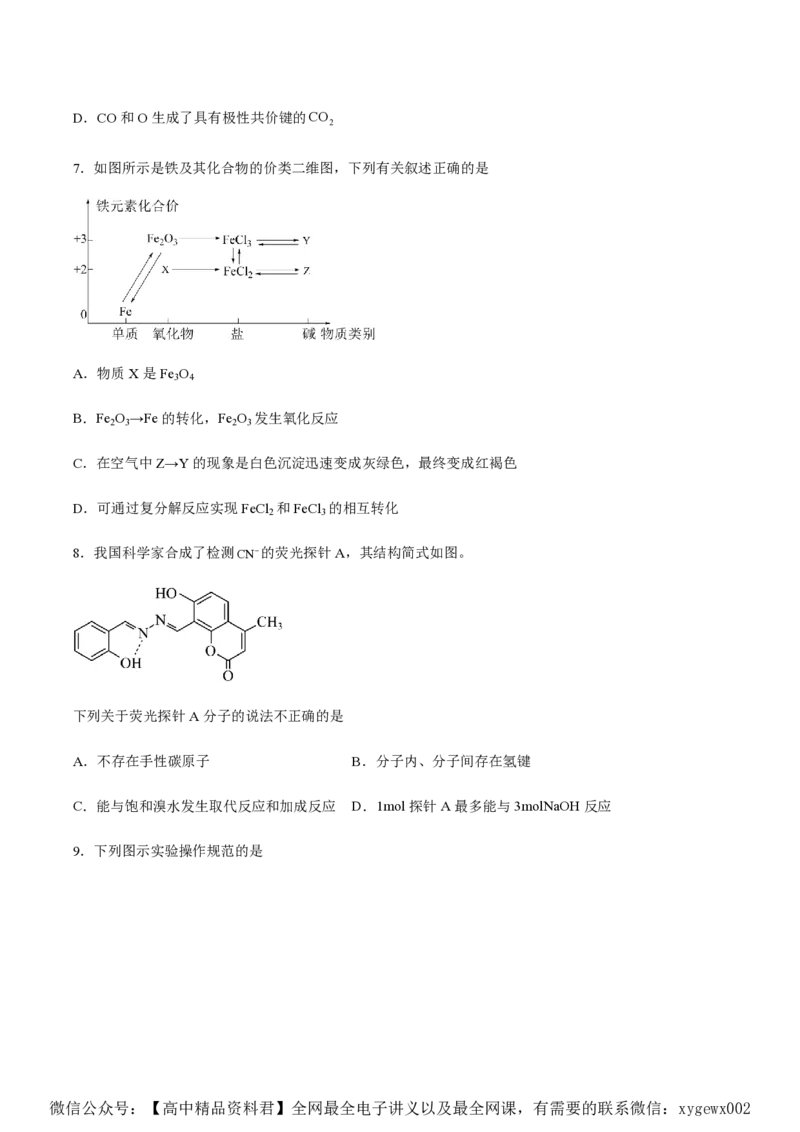
7.如图所示是铁及其化合物的价类二维图,下列有关叙述正确的是
A.物质X是Fe O
3 4
B.Fe O →Fe的转化,Fe O 发生氧化反应
2 3 2 3
C.在空气中Z→Y的现象是白色沉淀迅速变成灰绿色,最终变成红褐色
D.可通过复分解反应实现FeCl 和FeCl 的相互转化
2 3
8.我国科学家合成了检测CN的荧光探针A,其结构简式如图。
下列关于荧光探针A分子的说法不正确的是
A.不存在手性碳原子 B.分子内、分子间存在氢键
C.能与饱和溴水发生取代反应和加成反应 D.1mol探针A最多能与3molNaOH反应
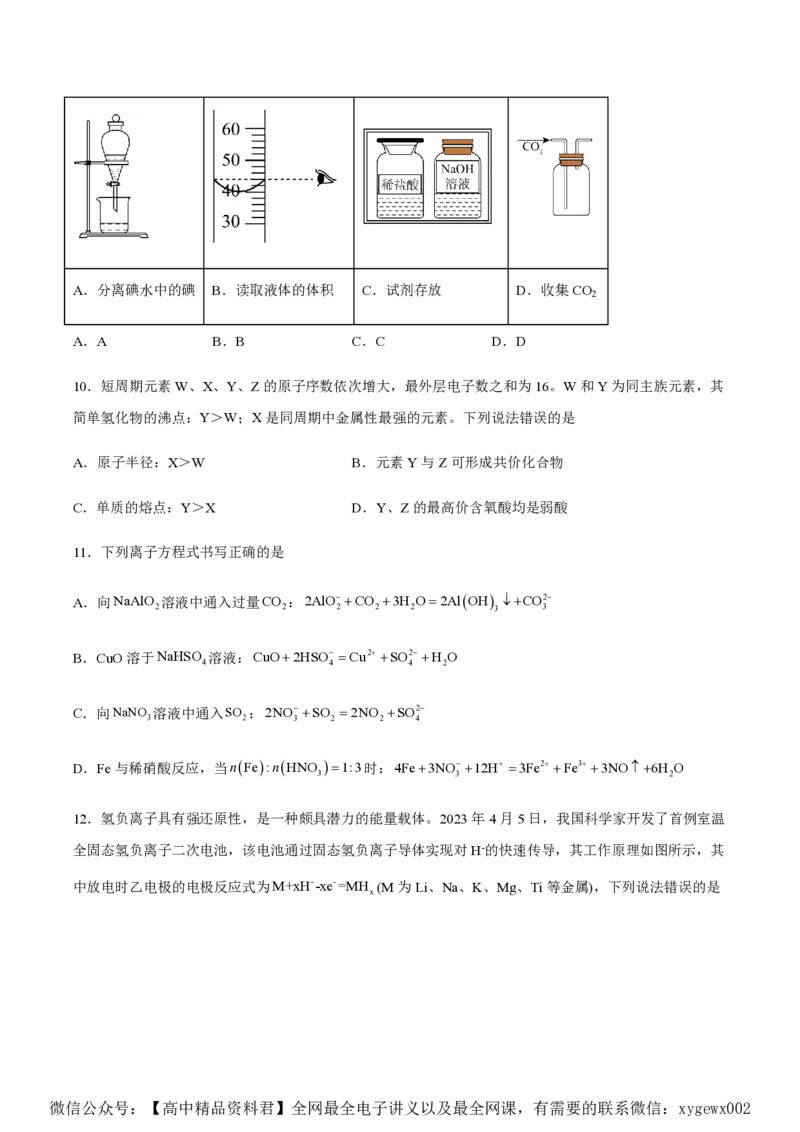
9.下列图示实验操作规范的是
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.分离碘水中的碘 B.读取液体的体积 C.试剂存放 D.收集CO
2
A.A B.B C.C D.D
10.短周期元素W、X、Y、Z的原子序数依次增大,最外层电子数之和为16。W和Y为同主族元素,其
简单氢化物的沸点:Y>W;X是同周期中金属性最强的元素。下列说法错误的是
A.原子半径:X>W B.元素Y与Z可形成共价化合物
C.单质的熔点:Y>X D.Y、Z的最高价含氧酸均是弱酸
11.下列离子方程式书写正确的是
A.向NaAlO 溶液中通入过量CO :2AlOCO 3H O2AlOH CO2
2 2 2 2 2 3 3
B.CuO溶于NaHSO 溶液:CuO2HSO Cu2 SO2H O
4 4 4 2
C.向NaNO 溶液中通入SO :2NOSO 2NO SO2
3 2 3 2 2 4
D.Fe与稀硝酸反应,当nFe:nHNO 1:3时:4Fe3NO12H 3Fe2 Fe3 3NO6H O
3 3 2
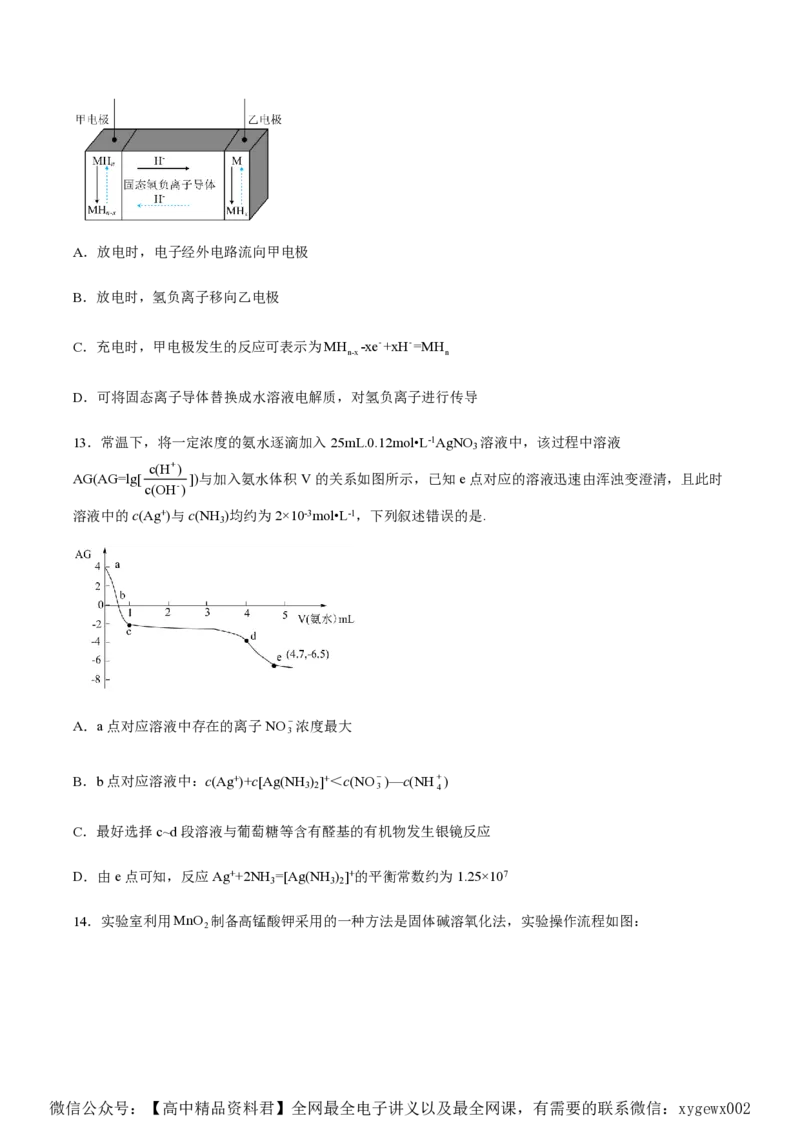
12.氢负离子具有强还原性,是一种颇具潜力的能量载体。2023年4月5日,我国科学家开发了首例室温
全固态氢负离子二次电池,该电池通过固态氢负离子导体实现对H-的快速传导,其工作原理如图所示,其
中放电时乙电极的电极反应式为M+xH--xe-=MH (M为Li、Na、K、Mg、Ti等金属),下列说法错误的是
x
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002A.放电时,电子经外电路流向甲电极
B.放电时,氢负离子移向乙电极
C.充电时,甲电极发生的反应可表示为MH -xe-+xH-=MH
n-x n
D.可将固态离子导体替换成水溶液电解质,对氢负离子进行传导
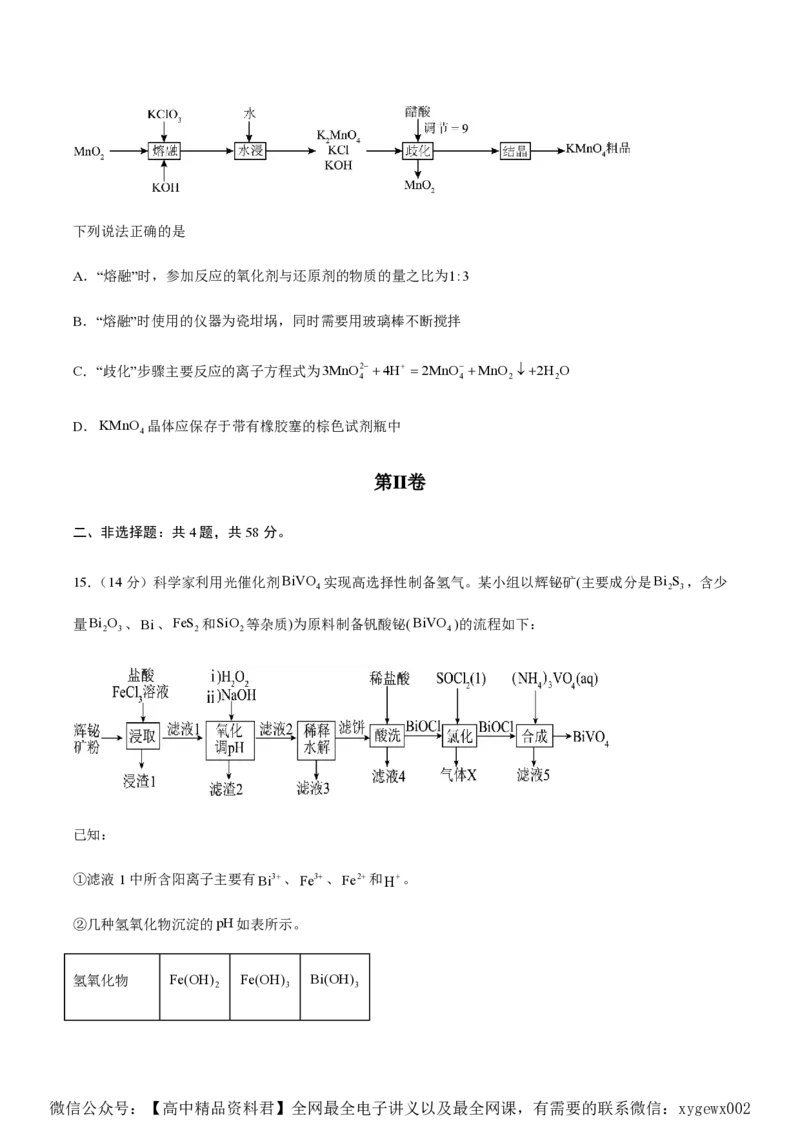
13.常温下,将一定浓度的氨水逐滴加入25mL.0.12mol•L-1AgNO 溶液中,该过程中溶液
3
c(H+)
AG(AG=lg[ ])与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时
c(OH-)
溶液中的c(Ag+)与c(NH )均约为2×10-3mol•L-1,下列叙述错误的是.
3
A.a点对应溶液中存在的离子NO浓度最大
3
B.b点对应溶液中:c(Ag+)+c[Ag(NH ) ]+<c(NO)—c(NH+)
3 2 3 4
C.最好选择c~d段溶液与葡萄糖等含有醛基的有机物发生银镜反应
D.由e点可知,反应Ag++2NH =[Ag(NH ) ]+的平衡常数约为1.25×107
3 3 2
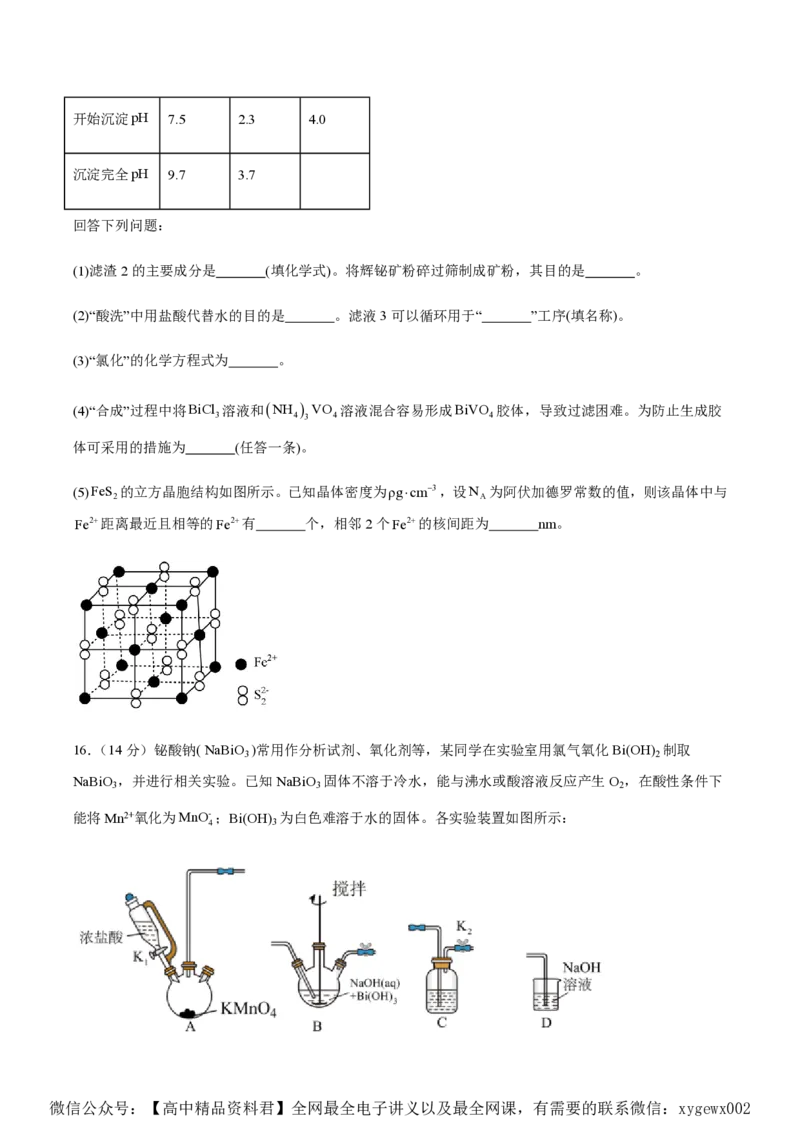
14.实验室利用MnO 制备高锰酸钾采用的一种方法是固体碱溶氧化法,实验操作流程如图:
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002下列说法正确的是
A.“熔融”时,参加反应的氧化剂与还原剂的物质的量之比为1:3
B.“熔融”时使用的仪器为瓷坩埚,同时需要用玻璃棒不断搅拌
C.“歧化”步骤主要反应的离子方程式为3MnO24H 2MnOMnO 2H O
4 4 2 2
D.KMnO 晶体应保存于带有橡胶塞的棕色试剂瓶中
4
第Ⅱ卷
二、非选择题:共4题,共58分。
15.(14分)科学家利用光催化剂BiVO 实现高选择性制备氢气。某小组以辉铋矿(主要成分是Bi S ,含少
4 2 3
量Bi O 、Bi、FeS 和SiO 等杂质)为原料制备钒酸铋(BiVO )的流程如下:
2 3 2 2 4
已知:
①滤液1中所含阳离子主要有Bi3、Fe3、Fe2和H。
②几种氢氧化物沉淀的pH如表所示。
氢氧化物 Fe(OH) Fe(OH) Bi(OH)
2 3 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002开始沉淀pH 7.5 2.3 4.0
沉淀完全pH 9.7 3.7
回答下列问题:
(1)滤渣2的主要成分是 (填化学式)。将辉铋矿粉碎过筛制成矿粉,其目的是 。
(2)“酸洗”中用盐酸代替水的目的是 。滤液3可以循环用于“ ”工序(填名称)。
(3)“氯化”的化学方程式为 。
(4)“合成”过程中将BiCl 溶液和NH VO 溶液混合容易形成BiVO 胶体,导致过滤困难。为防止生成胶
3 4 3 4 4
体可采用的措施为 (任答一条)。
(5)FeS 的立方晶胞结构如图所示。已知晶体密度为ρgcm3,设N 为阿伏加德罗常数的值,则该晶体中与
2 A
Fe2距离最近且相等的Fe2有 个,相邻2个Fe2的核间距为 nm。
16.(14分)铋酸钠( NaBiO )常用作分析试剂、氧化剂等,某同学在实验室用氯气氧化Bi(OH) 制取
3 2
NaBiO ,并进行相关实验。已知NaBiO 固体不溶于冷水,能与沸水或酸溶液反应产生O ,在酸性条件下
3 3 2
能将Mn2+氧化为MnO-;Bi(OH) 为白色难溶于水的固体。各实验装置如图所示:
4 3
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002请回答下列问题:
(1)装置的连接顺序是_____→_______→ ______→ _____(填字母) 。
(2)C中装有的试剂是 ,若没有装置C,可能产生的影响是 。
(3)反应开始时,打开K 和K ,B中Cl 发生的反应有;Cl +2NaOH=NaClO+NaCl+H O,
1 2 2 2 2
(填化学方程式)。
(4)反应结束后,为从装置B中获得尽可能多的产品,需要进行的操作是 、过滤、冷水洗涤、干
燥。
(5)取上述NaBiO 产品w g,加入足量稀硫酸和MnSO 稀溶液使其完全反应,再用c mol·L-1的H C O 标准
3 4 2 2 4
溶液滴定生成的 MnO- ,消耗V mL标准溶液。
4
①不能用c mol·L-1的H C O 标准溶液直接滴定NaBiO 的原因是 。
2 2 4 3
②该产品的纯度为 (用含w 、c、V的代数式表示)。
(6)取少量B中反应后的悬浊液,加入稀硫酸,产生黄绿色气体,经检验气体中含有Cl 。该实验
2
(填“能”或“不能” )证明一定是NaBiO 氧化了Cl-,理由是 。
3
17.(15分)2022年4月16日,中国空间站的3名航天员乘神舟十三号载人飞船平安返回地球。空间站处
理CO 的一种重要方法是对CO 进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为
2 2
以下三步:
Ⅰ.固态胺吸收与浓缩CO
2
在水蒸气存在下固态胺吸收CO 反应生成酸式碳酸盐(该反应是放热反应),再解吸出CO 的简单方法是加
2 2
热。
Ⅱ.CO 的加氢甲烷化
2
H 还原CO 制CH 的部分反应如下:
2 2 4
i.CO
2
(g)+H
2
(g)CO(g)+H
2
O(g) △H
1
=+41kJ•mol-1
ii.CO(g)+3H
2
(g)CH
4
(g)+H
2
O(g) △H
2
=-246kJ•mol-1
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002(1)反应CO
2
(g)+4H
2
(g)CH
4
(g)+2H
2
O(g)的△H= kJ•mol-1。
(2)向恒容绝热的密闭容器中充入amolCO与2amolH (g),进行反应ii,下列能判断反应已达化学平衡状态的
2
是
a.容器中混合气体密度不变 b.混合气体中c(CH )与c(H O)之比不变
4 2
c.v (H )=3v (H O) d.容器内温度不变
正 2 逆 2
Ⅲ.CO
2
和H
2
合成甲烷也是CO
2
资源化利用的重要方法。对于上述(1)的反应CO
2
(g)+4H
2
(g)CH
4
(g)+2H
2
O(g)
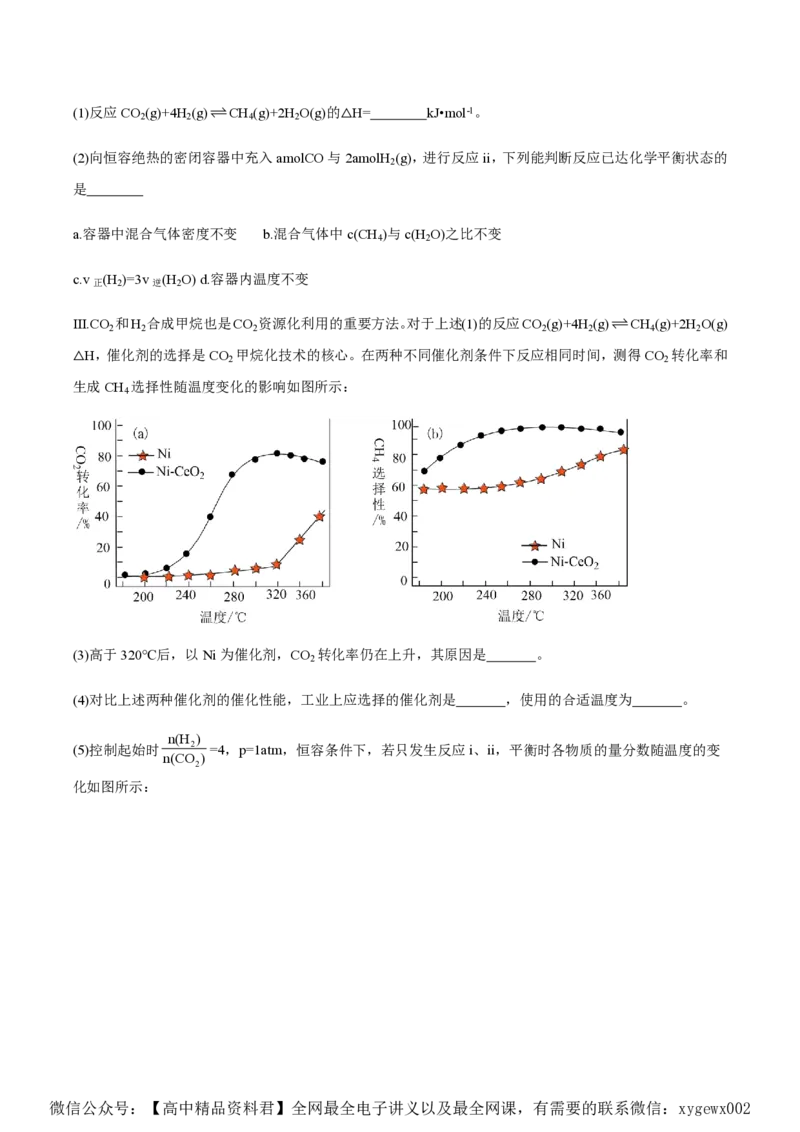
△H,催化剂的选择是CO 甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO 转化率和
2 2
生成CH 选择性随温度变化的影响如图所示:
4
(3)高于320℃后,以Ni为催化剂,CO 转化率仍在上升,其原因是 。
2
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是 ,使用的合适温度为 。
n(H )
(5)控制起始时 2 =4,p=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变
n(CO )
2
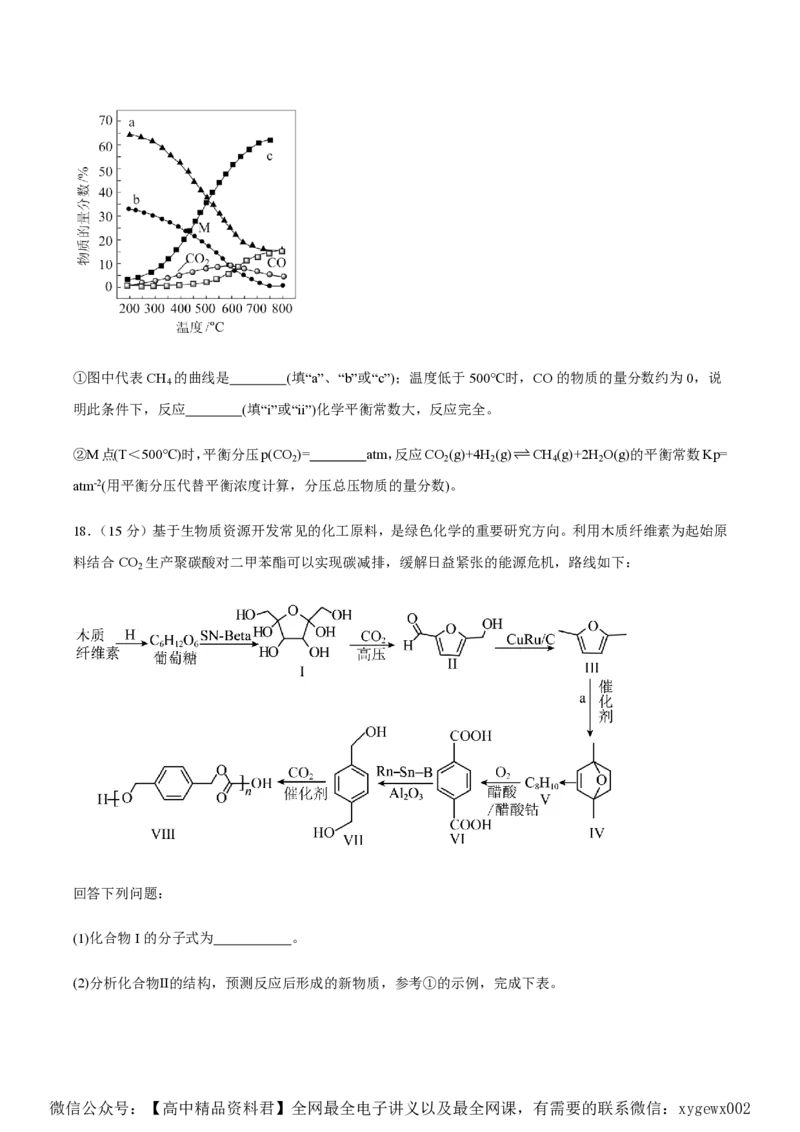
化如图所示:
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002①图中代表CH 的曲线是 (填“a”、“b”或“c”);温度低于500℃时,CO的物质的量分数约为0,说
4
明此条件下,反应 (填“i”或“ii”)化学平衡常数大,反应完全。
②M点(T<500℃)时,平衡分压p(CO
2
)= atm,反应CO
2
(g)+4H
2
(g)CH
4
(g)+2H
2
O(g)的平衡常数Kp=
atm-2(用平衡分压代替平衡浓度计算,分压总压物质的量分数)。
18.(15分)基于生物质资源开发常见的化工原料,是绿色化学的重要研究方向。利用木质纤维素为起始原
料结合CO 生产聚碳酸对二甲苯酯可以实现碳减排,缓解日益紧张的能源危机,路线如下:
2
回答下列问题:
(1)化合物I的分子式为 。
(2)分析化合物Ⅱ的结构,预测反应后形成的新物质,参考①的示例,完成下表。
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002序号 变化的官能团的名称 可反应的试剂(物质) 反应后形成的新物质 反应类型
① 。 O 氧化反应
2
② 。 。 。 加成反应
(3)化合物Ⅲ到化合物Ⅳ的反应是原子利用率100%的反应,且1molⅢ与1mol化合物a反应得到1molⅣ,则
化合物a为 。
(4)已知化合物Ⅴ的核磁共振氢谱有2组峰,且峰面积之比为2:3,写出化合物V的结构简
式: 。
(5)化合物Ⅶ的芳香族同分异构体中符合下列条件的有 种(不含立体异构)。
①最多能与相同物质的量的Na CO 反应;②能与2倍物质的量的Na发生放出H 的反应。
2 3 2
(6)关于Ⅶ生成Ⅷ的反应的说法中,不正确的有___________。
A.反应过程中,有H-O键断裂
B.反应过程中,有C=O双键和C-O单键形成
C.该反应为缩聚反应
D.CO 属于极性分子,分子中存在由p轨道“肩并肩”形成的π键
2
微信公众号:【高中精品资料君】全网最全电子讲义以及最全网课,有需要的联系微信:xygewx002