文档内容
鄂南高中 黄冈中学 黄石二中 荆州中学 龙泉中学
武汉二中 孝感高中 襄阳四中 襄阳五中 宜昌一中 夷陵中学
2023 届高三湖北十一校第二次联考
化 学 试 题
命题学校:黄冈中学 命题人:甘文广 丁沙 审题学校:孝感高中 审题人:李海忠
可能用到的相对原子质量:H1 C12 O16 N14 Na23 Al27 Ca40 Cu64 Zn65
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
1.2022年我省重点建设计划超额完成任务。下列相关说法错误的是
A.第6代半导体显示器件使用的半导体材料是SiO 晶体
2
B.耐水药用玻璃(由石英砂、纯碱、方解石等原料制得)属于硅酸盐材料
C.新冠灭活疫苗应冷藏保存
D.电动汽车使用的锂电池属于二次电池
2.茶叶经过高温“杀青”生成清香味的反式青叶醇,转化过程为:
下列说法正确的是
A.青叶醇的分子式为C H O
6 10
B.青叶醇分子中含有极性键、非极性键和氢键等化学键
C.反式青叶醇能与Br 发生加成反应,且产物中手性碳原子个数为2
2
D.反式青叶醇分子中共平面的原子数目最多为15
3.生产生活中蕴藏着丰富的化学知识。下列项目与所述的化学知识没有关联的是
选项 项目 化学知识
废旧铅酸蓄电池回收PbSO 时加
A 4 Fe2+可作该反应的催化剂
入少量Fe2+
B 冰在室温下自动熔化成水 冰熔化成水时熵值增大
合成氨原料气进入合成塔前需经
C 铜氨溶液可除去CO
过铜氨溶液
D BaSO 作“钡餐” BaSO 是强电解质
4 4
2023 届高三湖北十一校第二次联考 化学试题 第 1 页 (共 8 页)4.下列离子方程式正确且能准确解释相应实验现象的是
A.向苯酚钠溶液中通入少量CO 气体溶液变浑浊:
2
2C H O-+CO +H O===2C H OH+
6 5 2 2 6 5
B.NaClO溶液与FeI 溶液反应溶液变2红−棕色:
2
2ClO-+2Fe2++H O===2Fe3++2Cl-+ C 2 O O 3 H-
2
C.向Fe(SCN) 溶液中滴加NaF溶液,红色褪去:Fe3++6F-===[FeF ]3-
3 6
D.向淀粉KI溶液中通入SO ,溶液变蓝并产生淡黄色沉淀:
2
SO +4I-+4H+===S↓+2I +2H O
2 2 2
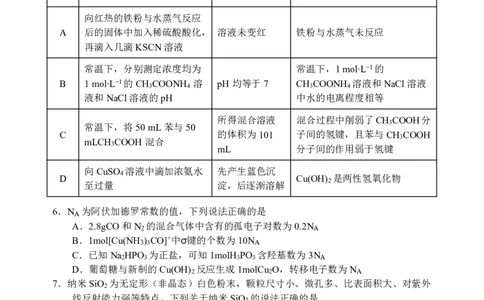
5.下列实验操作、现象与结论相匹配的是
选项 操作 现象 结论
向红热的铁粉与水蒸气反应
A 后的固体中加入稀硫酸酸化, 溶液未变红 铁粉与水蒸气未反应
再滴入几滴KSCN溶液
常温下,分别测定浓度均为 常温下,1mol∙L−1的
B 1mol∙L−1的CH COONH 溶 pH均等于7 CH COONH 溶液和NaCl溶液
3 4 3 4
液和NaCl溶液的pH 中水的电离程度相等
所得混合溶液 混合过程中削弱了CH COOH分
常温下,将50mL苯与50 3
C 的体积为101 子间的氢键,且苯与CH COOH
mLCH COOH混合 3
3 mL 分子间的作用弱于氢键
向CuSO 溶液中滴加浓氨水 先产生蓝色沉
D 4 Cu(OH) 是两性氢氧化物
至过量 淀,后逐渐溶解 2
6.N 为阿伏加德罗常数的值,下列说法正确的是
A
A.2.8gCO和N
2
的混合气体中含有的孤电子对数为0.2NA
B.1mol[Cu(NH3)
3
CO]+中σ键的个数为10NA
C.已知Na
2
HPO
3
为正盐,可知1molH
3
PO
3
含羟基数为3NA
D.葡萄糖与新制的Cu(OH)
2
反应生成1molCu
2
O,转移电子数为NA
7.纳米SiO 为无定形(非晶态)白色粉末,颗粒尺寸小、微孔多、比表面积大、对紫外
2
线反射能力强等特点。下列关于纳米SiO 的说法正确的是
2
A.对光有各向异性
B.熔点与晶体SiO 相同
2
C.与晶体SiO 互为同分异构体
2
D.可用X-射线衍射实验区分纳米SiO 与晶体SiO
2 2
8.硫化亚砷(As S )常用作颜料、还原剂和药物等,几乎不溶于水,易溶于氢氧化钠溶液,
4 6
其反应方程式为:As S +12NaOH=2Na AsO +2Na AsS +6H O。下列说法正确的是
4 6 3 3 3 3 2
A.该反应中有电子的转移 B.As S 晶体中,As S 的配位数为12
4 6 4 6
C.Na AsO 溶液碱性比Na AsS 强 D.As S 极性分子
3 3 3 3 4 6
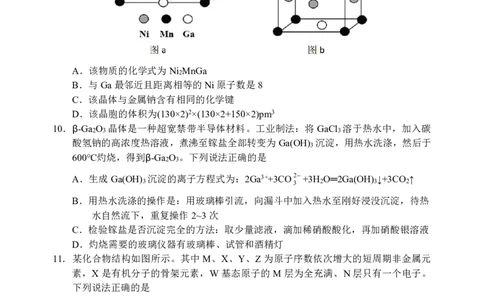
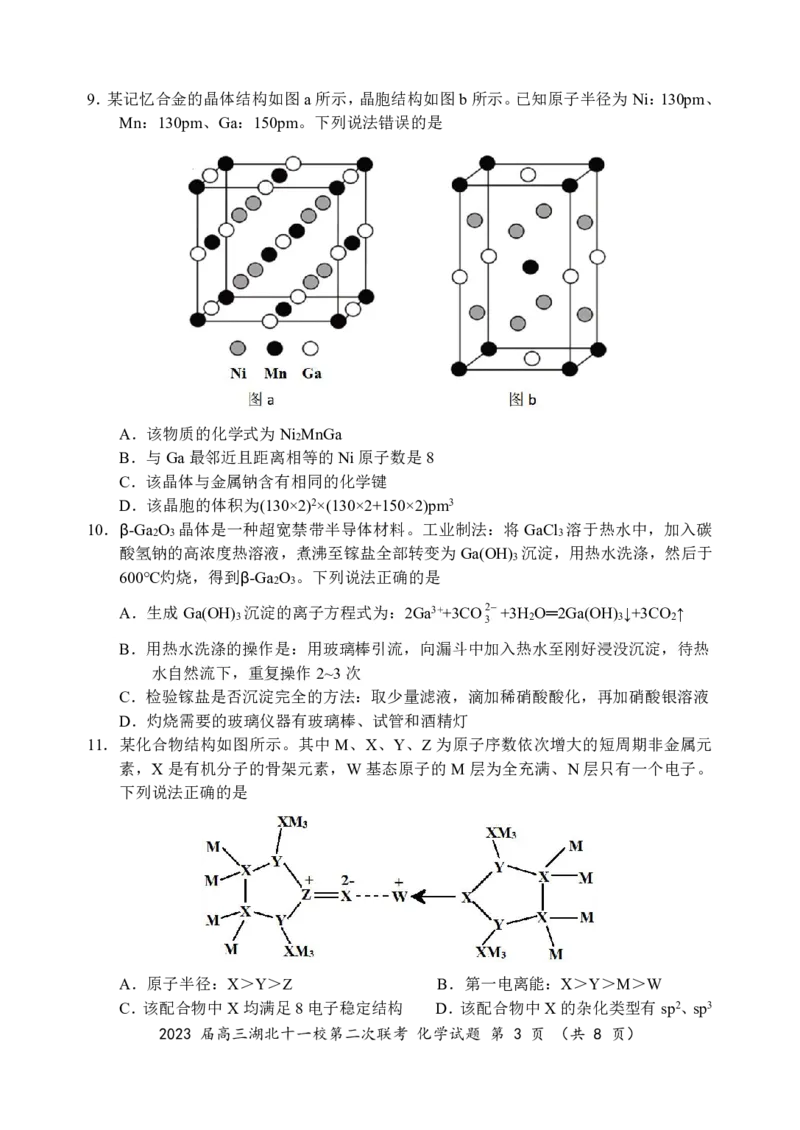
2023 届高三湖北十一校第二次联考 化学试题 第 2 页 (共 8 页)9.某记忆合金的晶体结构如图a所示,晶胞结构如图b所示。已知原子半径为Ni:130pm、
Mn:130pm、Ga:150pm。下列说法错误的是
A.该物质的化学式为Ni MnGa
2
B.与Ga最邻近且距离相等的Ni原子数是8
C.该晶体与金属钠含有相同的化学键
D.该晶胞的体积为(130×2)2×(130×2+150×2)pm3
10.β-Ga O 晶体是一种超宽禁带半导体材料。工业制法:将GaCl 溶于热水中,加入碳
2 3 3
酸氢钠的高浓度热溶液,煮沸至镓盐全部转变为Ga(OH) 沉淀,用热水洗涤,然后于
3
600℃灼烧,得到β-Ga O 。下列说法正确的是
2 3
A.生成Ga(OH) 沉淀的离子方程式为:2Ga3++3CO2 +3H O═2Ga(OH) ↓+3CO ↑
3 3 2 3 2
B.用热水洗涤的操作是:用玻璃棒引流,向漏斗中加入热水至刚好浸没沉淀,待热
水自然流下,重复操作2~3次
C.检验镓盐是否沉淀完全的方法:取少量滤液,滴加稀硝酸酸化,再加硝酸银溶液
D.灼烧需要的玻璃仪器有玻璃棒、试管和酒精灯
11.某化合物结构如图所示。其中M、X、Y、Z为原子序数依次增大的短周期非金属元
素,X是有机分子的骨架元素,W基态原子的M层为全充满、N层只有一个电子。
下列说法正确的是
A.原子半径:X>Y>Z B.第一电离能:X>Y>M>W
C.该配合物中X均满足8电子稳定结构 D.该配合物中X的杂化类型有sp2、sp3
2023 届高三湖北十一校第二次联考 化学试题 第 3 页 (共 8 页)12.在抗击新冠肺炎的过程中“合成材料”发挥了重要的作用。下列有关合成材料的说法
正确的是
A.CH CHOHCOOH 可通过缩聚反应生成可降解的绿色高分子材料
3
B.合成有机硅橡胶的单体是 ,则有机硅橡胶是通过加聚反应制得的
C.合成酚醛树脂( )的单体是苯酚和甲醇
D.天然橡胶的主要成分聚异戊二烯不能使溴水褪色
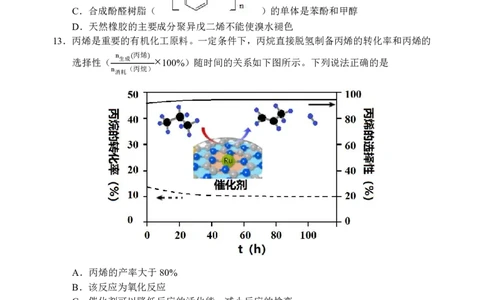
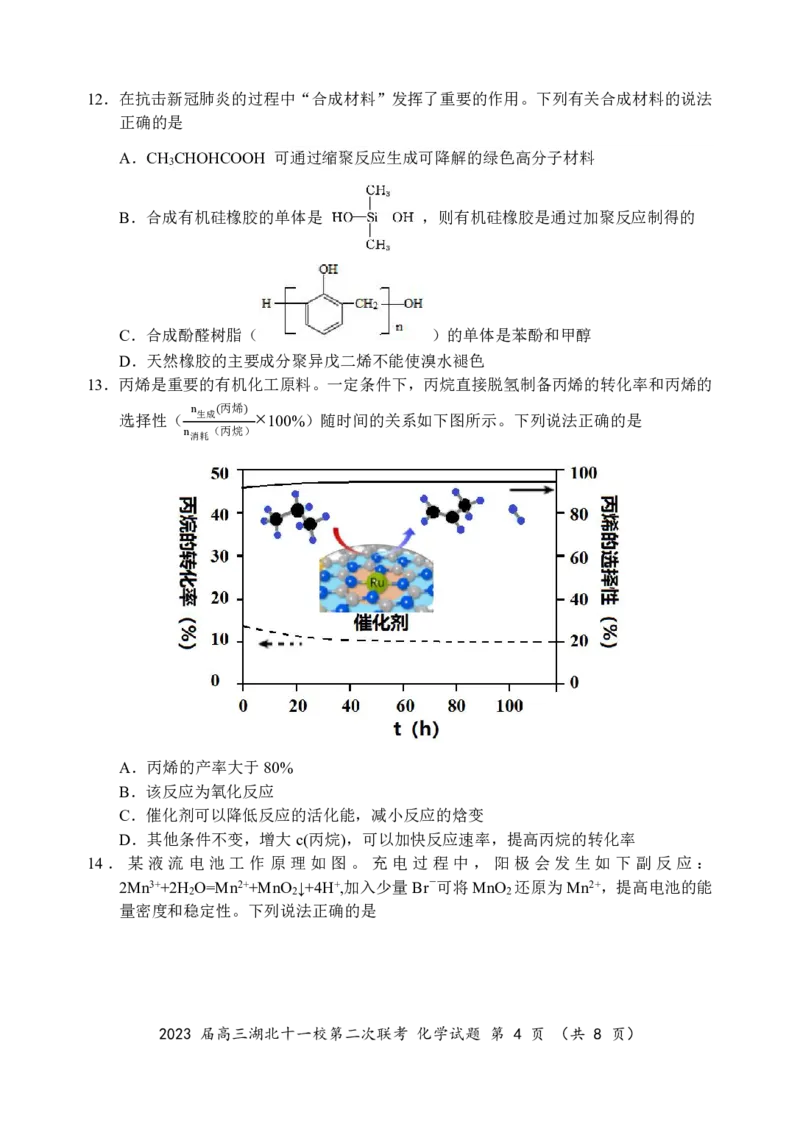
13.丙烯是重要的有机化工原料。一定条件下,丙烷直接脱氢制备丙烯的转化率和丙烯的
丙烯
选择性( 生成 ×100%)随时间的关系如下图所示。下列说法正确的是
消n耗 ((丙烷))
n
A.丙烯的产率大于80%
B.该反应为氧化反应
C.催化剂可以降低反应的活化能,减小反应的焓变
D.其他条件不变,增大c(丙烷),可以加快反应速率,提高丙烷的转化率
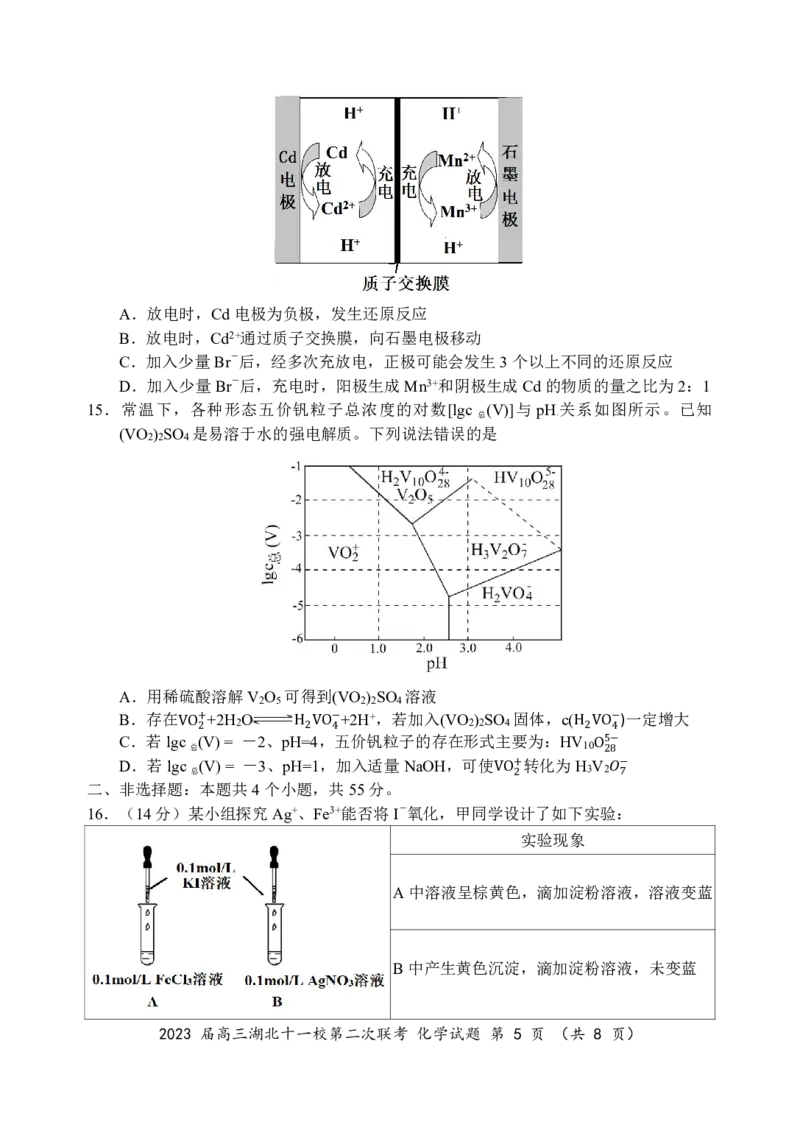
14.某液流电池工作原理如图。充电过程中,阳极会发生如下副反应:
2Mn3++2H O=Mn2++MnO ↓+4H+,加入少量Br-可将MnO 还原为Mn2+,提高电池的能
2 2 2
量密度和稳定性。下列说法正确的是
2023 届高三湖北十一校第二次联考 化学试题 第 4 页 (共 8 页)A.放电时,Cd电极为负极,发生还原反应
B.放电时,Cd2+通过质子交换膜,向石墨电极移动
C.加入少量Br-后,经多次充放电,正极可能会发生3个以上不同的还原反应
D.加入少量Br-后,充电时,阳极生成Mn3+和阴极生成Cd的物质的量之比为2:1
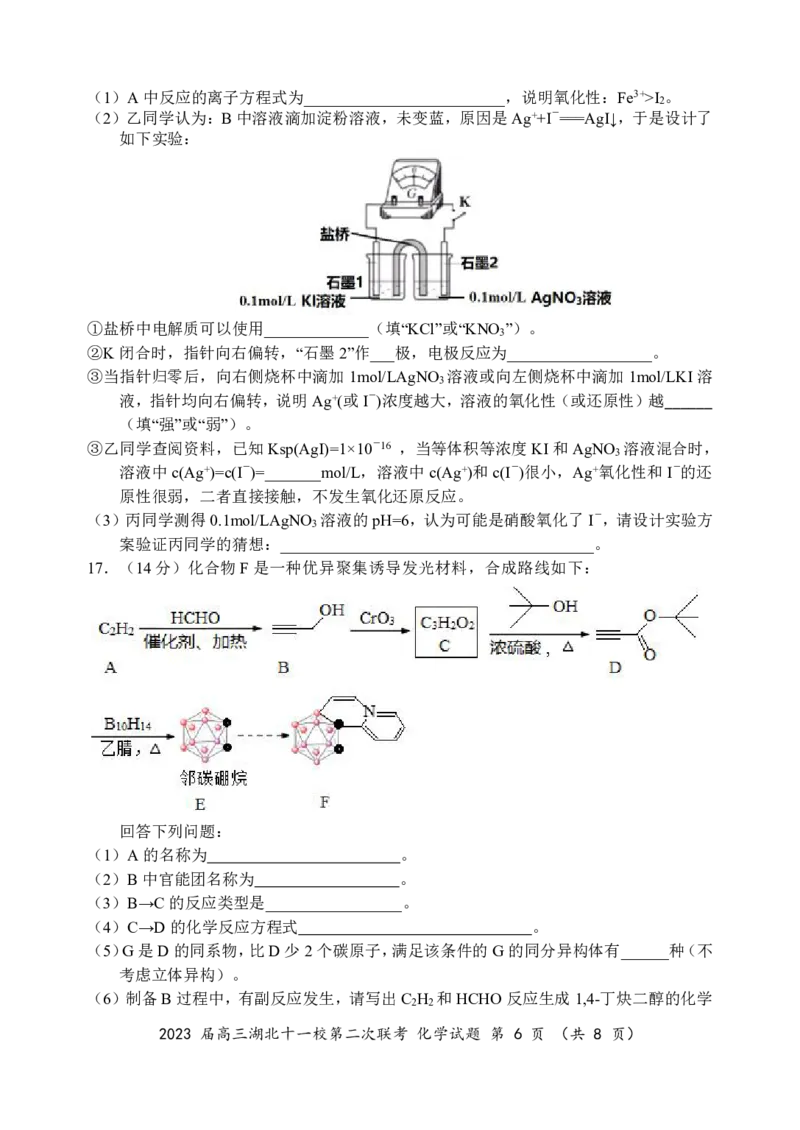
15.常温下,各种形态五价钒粒子总浓度的对数[lgc (V)]与 pH关系如图所示。已知
总
(VO ) SO 是易溶于水的强电解质。下列说法错误的是
2 2 4
A.用稀硫酸溶解V O 可得到(VO ) SO 溶液
2 5 2 2 4
B.存在 +2H O +2H+,若加入(VO ) SO 固体,c( )一定增大
2 2 2 4
C.若lgc +(V)= -2、pH=4,−五价钒粒子的存在形式主要为:HV −
VO 总2 H2VO4 H 120 VO4
D.若lgc (V)= -3、pH=1,加入适量NaOH,可使 转化为H V5−
总 3 O 228
二、非选择题:本题共4个小题,共55分。 + −
VO2 7
16.(14分)某小组探究Ag+、Fe3+能否将I-氧化,甲同学设计了如下实验:
实验现象
A中溶液呈棕黄色,滴加淀粉溶液,溶液变蓝
B中产生黄色沉淀,滴加淀粉溶液,未变蓝
2023 届高三湖北十一校第二次联考 化学试题 第 5 页 (共 8 页)(1)A中反应的离子方程式为_________________________,说明氧化性:Fe3+>I 。
2
(2)乙同学认为:B中溶液滴加淀粉溶液,未变蓝,原因是Ag++I-===AgI↓,于是设计了
如下实验:
①盐桥中电解质可以使用_____________(填“KCl”或“KNO ”)。
3
②K闭合时,指针向右偏转,“石墨2”作___极,电极反应为__________________。
③当指针归零后,向右侧烧杯中滴加1mol/LAgNO 溶液或向左侧烧杯中滴加1mol/LKI溶
3
液,指针均向右偏转,说明Ag+(或I-)浓度越大,溶液的氧化性(或还原性)越______
(填“强”或“弱”)。
③乙同学查阅资料,已知Ksp(AgI)=1×10-16 ,当等体积等浓度KI和AgNO 溶液混合时,
3
溶液中c(Ag+)=c(I-)=_______mol/L,溶液中c(Ag+)和c(I-)很小,Ag+氧化性和I-的还
原性很弱,二者直接接触,不发生氧化还原反应。
(3)丙同学测得0.1mol/LAgNO 溶液的pH=6,认为可能是硝酸氧化了I-,请设计实验方
3
案验证丙同学的猜想:_______________________________________。
17.(14分)化合物F是一种优异聚集诱导发光材料,合成路线如下:
回答下列问题:
(1)A的名称为 。
(2)B中官能团名称为 。
(3)B→C的反应类型是_________________。
(4)C→D的化学反应方程式 。
(5)G是D的同系物,比D少2个碳原子,满足该条件的G的同分异构体有______种(不
考虑立体异构)。
(6)制备B过程中,有副反应发生,请写出C H 和HCHO反应生成1,4-丁炔二醇的化学
2 2
2023 届高三湖北十一校第二次联考 化学试题 第 6 页 (共 8 页)方程式 。
(7)科学家提出一种制备C(C H O )的新工艺,原理为:
3 2 2
CaC +2CO +H O C H O +CaCO
2 2 2 3 2 2 3
乙腈、
CuI
该工艺的优点有____________________ 、∆ _____________________( 写2条)。
18.(13分)电子级氢氟酸是微电子行业的关键性基础材料之一,由萤石粉(主要成分为
CaF ,含有少量SiO 和微量As O 等)制备工艺如下:
2 2 2 3
萤石粉 浓硫酸 硫酸 H O 溶液
2 2
气体1 HF硫酸溶液
酸浸 硫酸吸附 精馏1 氧化 精馏2 产品
H O
2
SiF 4 、HF H 2 SiF 6
回答下列问题:
(1)“酸浸”时生成HF的化学方程式为_______________________________,
工业生产时往往会适当加热,目的是____________________。
(2)“精馏1”设备使用的材料可选用_________________(填序号)。
A.玻璃 B.陶瓷 C.石英 D.金
(3)已知H SiF 是一种配位酸,酸性与硝酸相近,可与KMnO 溶液反应制备极易溶于水
2 6 4
的强酸HMnO ,反应的离子方程式为__________________________________。
4
(4)“氧化”时将AsF 氧化为AsF 。AsF 的沸点高于AsF ,原因是
3 5 5 3
__________________________________________________________________。
(5)液态HF是酸性溶剂,能发生自偶电离:HF H++F-,由于H+和F-都溶剂化,
常表示为:3HF H F++ 。在HF溶剂中AsF 、BF 呈酸性,HClO 、HNO 、
2 5 3 3 3
H O呈碱性,比如AsF 、HClO− 的电离方程式分别为:AsF +2HF +H F+;
2 5 HF23 5 2
HOClO +2HF (HO) ClO++ 。 −
2 2 AsF6
在HF作用下, −
HF2
①写出BF 与HNO 反应的离子方程式_______________________________。
3 3
②已知:H O与 AsF 反应生成 HAsF 。结合 H+的能力:H O_____ (填“>”、
2 5 6 2
“<”或“=”)。 −
AsF6
19.(14分)汽车尾气中含有CO、NO、NO 等大气污染物,可发生以下反应:
2
①NO (g)+CO(g) NO(g)+CO (g) △S =−13.2J•K-1•mol-1
2 2 1
②2NO(g)+2CO(g) N (g)+2CO (g) △S =−197.8J•K-1•mol-1
2 2 2
③2NO (g)+4CO(g) N (g)+4CO (g) △S
2 2 2 3
(1)已知△G=△H﹣T△S,(忽略△H、△S随温度的影响),则△S =
3
______________J·mol-1·K。
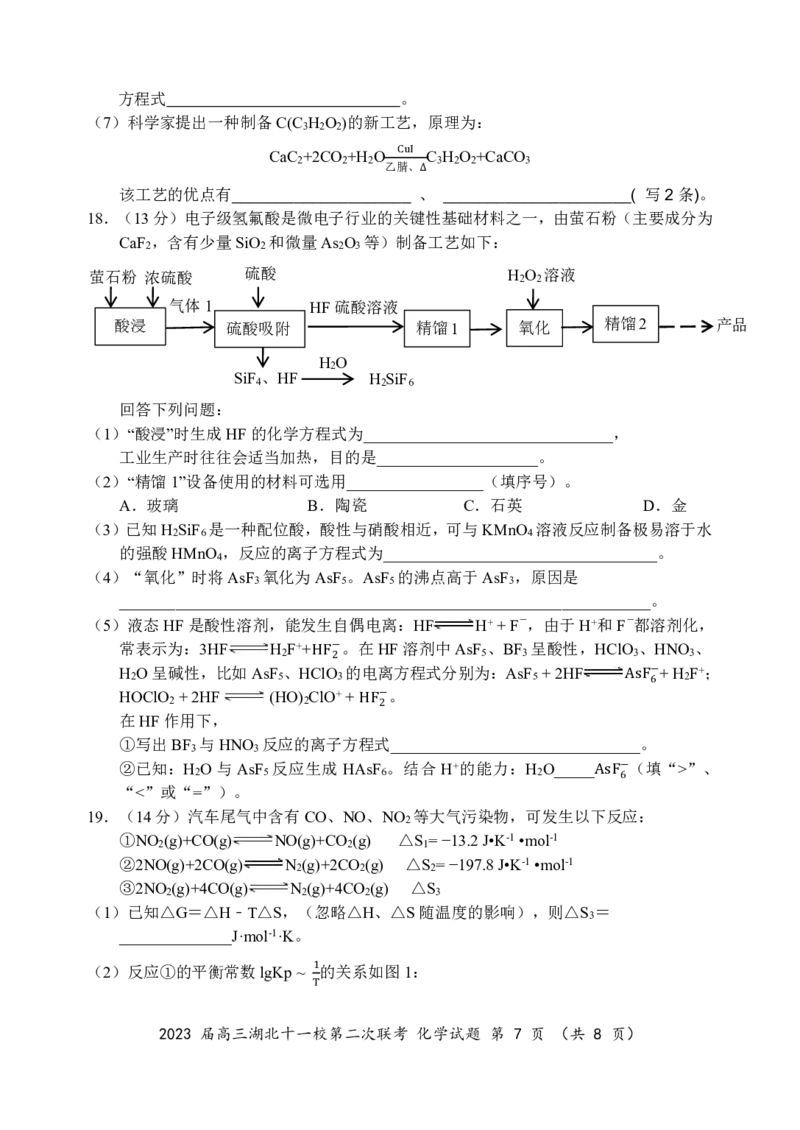
(2)反应①的平衡常数lgKp~ 的关系如图1:
1
T
2023 届高三湖北十一校第二次联考 化学试题 第 7 页 (共 8 页)反应①为_________(填“吸热”或“放热”)反应;温度为tK下,向恒容密闭容器中加入
1molCO(g)和1molNO (g)(若只发生反应①),测得起始压强为20kPa,达到平衡时,
2
NO 的转化率为__________;NO的分压为______kPa。
2
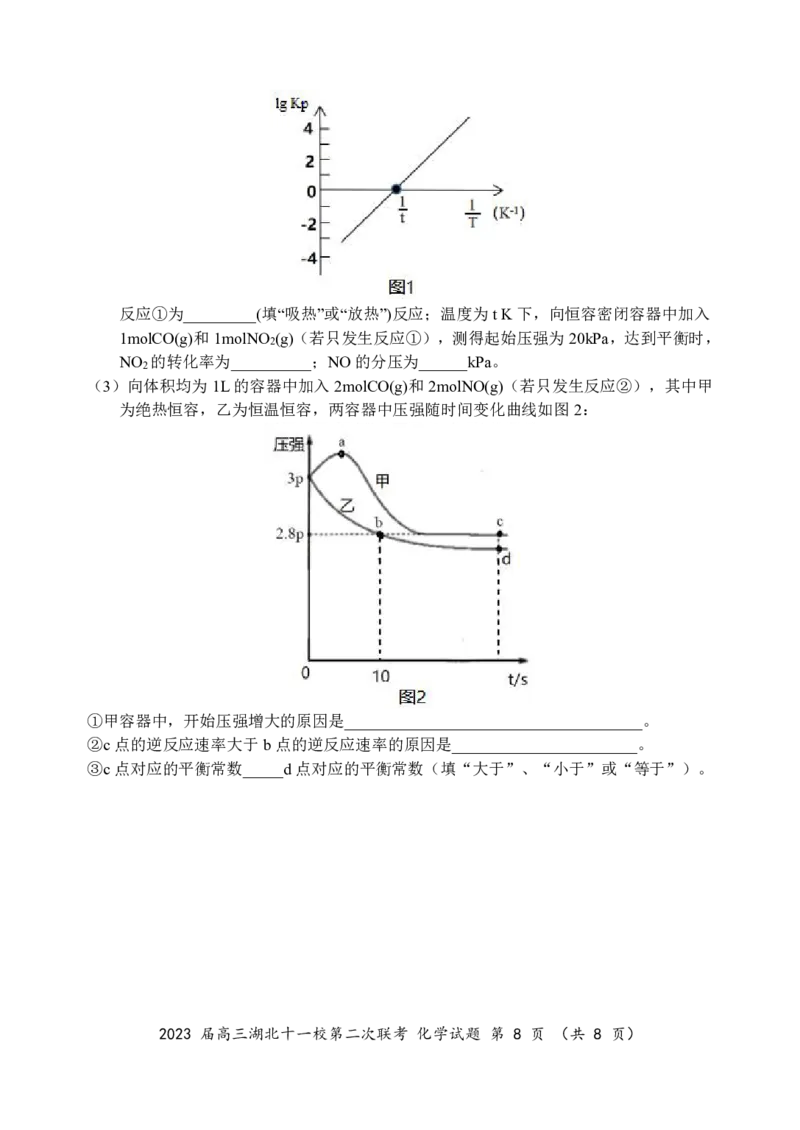
(3)向体积均为1L的容器中加入2molCO(g)和2molNO(g)(若只发生反应②),其中甲
为绝热恒容,乙为恒温恒容,两容器中压强随时间变化曲线如图2:
①甲容器中,开始压强增大的原因是_____________________________________。
②c点的逆反应速率大于b点的逆反应速率的原因是_______________________。
③c点对应的平衡常数_____d点对应的平衡常数(填“大于”、“小于”或“等于”)。
2023 届高三湖北十一校第二次联考 化学试题 第 8 页 (共 8 页)