文档内容
高三期初质量检测试卷·化学
注意事项:
1.本试卷分为选择题和非选择题两部分,共 100分,考试时间 75分钟。
2.请把选择题和非选择题的答案均填写在答题卷的指定栏目内。
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 S 32 Cl 35.5 K 39 Cr 52 Mn
55 Fe 56
一、单项选择题:共 13题,每题 3分,共 39分。每题只有一个选项最符合题意。
1.我国提出2030年碳达峰、2060年碳中和的目标。下列关于CO 的说法不正确是( )
2
A.CO 固体易升华 B.CO 是酸性氧化物
2 2
C.CO 为极性分子 D.CO 属于非电解质
2 2
2.肼(N H )是发射航天飞船常用的高能燃料,可通过反应NaClO2NH ═N H NaClH O制备。
2 4 3 2 4 2
下列说法正确的是( )
A.NaClO既含离子键又含共价键 B.NH 的电子式为H:N:H
3
H
N H
| |
C.N H 的结构式为:H— H═N—H D.Na与Cl具有相同的电子层结构
2 4
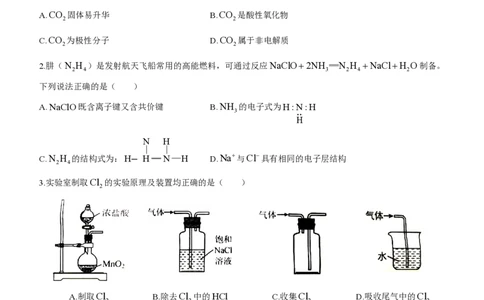
3.实验室制取Cl 的实验原理及装置均正确的是( )
2
A.制取Cl B.除去Cl 中的HCl C.收集Cl D.吸收尾气中的Cl
2 2 2 2
4. N、 P、 As、 Sb是周期表中ⅤA族元素。下列说法正确的是( )
7 15 33 51
A.原子半径:rNrPrAs B.酸性:H AsO H PO HNO
3 4 3 4 3
C.第一电离能:I N I P I As D.ⅤA族元素单质的晶体类型相同
1 1 1
阅读下列材料,完成5~7题:
第三周期元素的单质及其化合物具有重要用途。如在熔融状态下,可用金属钠制备金属钾;MgCl 可制
2
学科网(北京)股份有限公司备多种镁产品;铝—空气电池具有较高的比能量,在碱性电解液中总反应为4Al3O 4OH 6H O═
2 2
4Al(OH) 。高纯硅广泛用于信息技术领域,高温条件下,将粗硅转化为三氯硅烷(SiHCl ),再经氢气
4 3
还原得到高纯硅。硫有多种单质,如斜方硫(燃烧热为297kJmol1)、单斜硫等。H S可除去废水中Hg2
2
等重金属离子,H S水溶液在空气中会缓慢氧化生成S而变浑浊。
2
5.下列说法正确的是( )
A.斜方硫和单斜硫互为同位素 B.H S的沸点比H O低
2 2
C.1mol
Al(OH)
中含有4mol键 D.Si— Si键的键能大于Si— O键的键能
4
6.下列化学反应表示正确的是( )
A.SiHCl 转化为高纯硅:SiHCl H ═Si3HCl
3 3 2
B.向CuSO 溶液中加入小粒金属钠:2NaCu2═Cu2Na
4
C.斜方硫燃烧:S(s,斜方硫)O g═SO g ΔH 297kJmol1
2 2
D.铝—空气电池(碱性电解液)放电时的负极反应,Al3e 4OH═Al(OH)
4
7.下列物质的性质与用途具有对应关系的是( )
A.熔融MgCl 能电解,可用作冶炼镁的原料
2
B.H S具有还原性,可除去废水中的Hg2
2
C.钠的密度比钾大,可用于冶炼金属钾
D.晶体硅熔点高、硬度大,可用作通讯设备的芯片
8.硫及其化合物的转化具有重要应用。下列说法不正确的是 )
△
A.实验室制取少量SO 的原理:Cu2H SO (浓) CuSO SO 2H O
2 2 4 4 2 2
B.实验室检验SO 既具有氧化性也具有还原性:S
Na 2S
SO
K
M
nO4SO2
2 2 4
C.工业上接触法制硫酸过程中物质转化:FeS O2SO O 2 SO H 2O H SO
2 高温 2 倠化剂,Δ 3 2 4
D.工业上用Fe O H O脱除天然气中的H S:Fe O H O3H S═Fe S 4H O
2 3 2 2 2 3 2 2 2 3 2
9.化合物Z是合成药物沙丁胺醇的重要中间体,其合成路线如下:
学科网(北京)股份有限公司已知:X→Y过程中,X先与HCHO发生加成反应,再与HCl发生取代反应。下列说法正确的是( )
A.X分子中所有原子在同一平面上 B.X→Y的中间产物分子式为C H O
9 10 3
C.Z最多能与2mol NaOH反应 D.X、Y、Z可用FeCl 溶液和AgNO 溶液进行鉴别
3 3
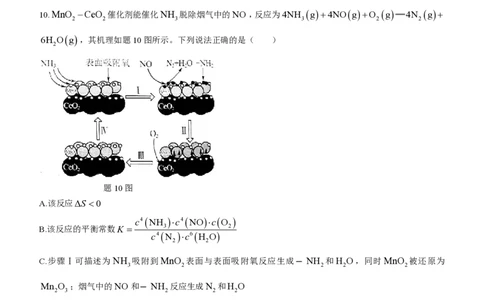
10.MnO CeO 催化剂能催化NH 脱除烟气中的NO ,反应为4NH g4NOgO g═4N g
2 2 3 3 2 2
6H Og,其机理如题10图所示。下列说法正确的是( )
2
题10图
A.该反应ΔS 0
c4NH c4NOcO
B.该反应的平衡常数K 3 2
c4N c6H O
2 2
C.步骤Ⅰ可描述为NH 吸附到MnO 表面与表面吸附氧反应生成— NH 和H O,同时MnO 被还原为
3 2 2 2 2
Mn O ;烟气中的NO 和— NH 反应生成N 和H O
2 3 2 2 2
D.该反应中每消耗1mol O ,转移电子的数目约为46.021023
2
11.室温下,探究0.1molL1 FeCl 溶液的性质,下列实验方案不能达到探究目的的是( )
3
选项 探究目的 实验方案
向2mL0.1molL1 FeCl 溶液滴加几滴KSCN溶液,观察溶液颜色变
A 溶液中是否含有Fe3 3
化
B Fe3是否具有氧化性 向2mL0.1molL1 FeCl 溶液滴加适量Na S溶液,观察生成沉淀的颜
3 2
学科网(北京)股份有限公司色
向 2mL5%H O 溶液中滴加几滴 0.1molL1 FeCl 溶液,观察滴加
Fe3能否催化H O 分 2 2 3
2 2
C
解 FeCl 溶液前后气泡产生情况
3
取2mL0.1molL1 FeCl 溶液和1mL0.1molL1 KI溶液混合,充分
3
Fe3与I的反应是否存
D
反应后,再加2mLCCl ,振荡、静置,取上层清液滴加少量KSCN
4
在限度
溶液,观察溶液颜色变化
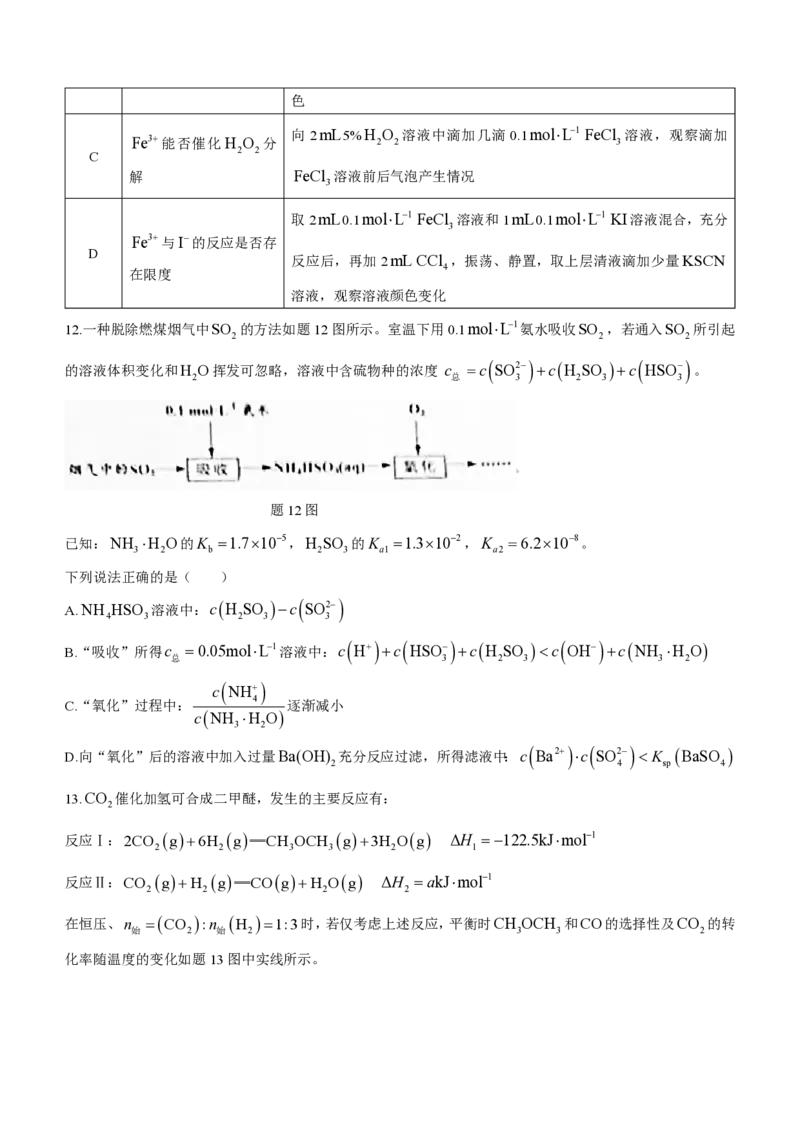
12.一种脱除燃煤烟气中SO 的方法如题12图所示。室温下用0.1molL1氨水吸收SO ,若通入SO 所引起
2 2 2
的溶液体积变化和H O挥发可忽略,溶液中含硫物种的浓度 c c SO2 cH SO c HSO 。
2 总 3 2 3 3
题12图
已知:NH H O的K 1.7105,H SO 的K 1.3102,K 6.2108。
3 2 b 2 3 a1 a2
下列说法正确的是( )
A.NH HSO 溶液中:cH SO c SO2
4 3 2 3 3
B.“吸收”所得c 0.05molL1溶液中:c H c HSO cH SO c OH cNH H O
总 3 2 3 3 2
c
NH
4
C.“氧化”过程中: 逐渐减小
cNH H O
3 2
D.向“氧化”后的溶液中加入过量Ba(OH) 充分反应过滤,所得滤液中:c Ba2 c SO2 K BaSO
2 4 sp 4
13.CO 催化加氢可合成二甲醚,发生的主要反应有:
2
反应Ⅰ:2CO g6H g═CH OCH g3H Og ΔH 122.5kJmol1
2 2 3 3 2 1
反应Ⅱ:CO gH g═COgH Og ΔH akJmol1
2 2 2 2
在恒压、n CO :n H 1:3时,若仅考虑上述反应,平衡时CH OCH 和CO的选择性及CO 的转
始 2 始 2 3 3 2
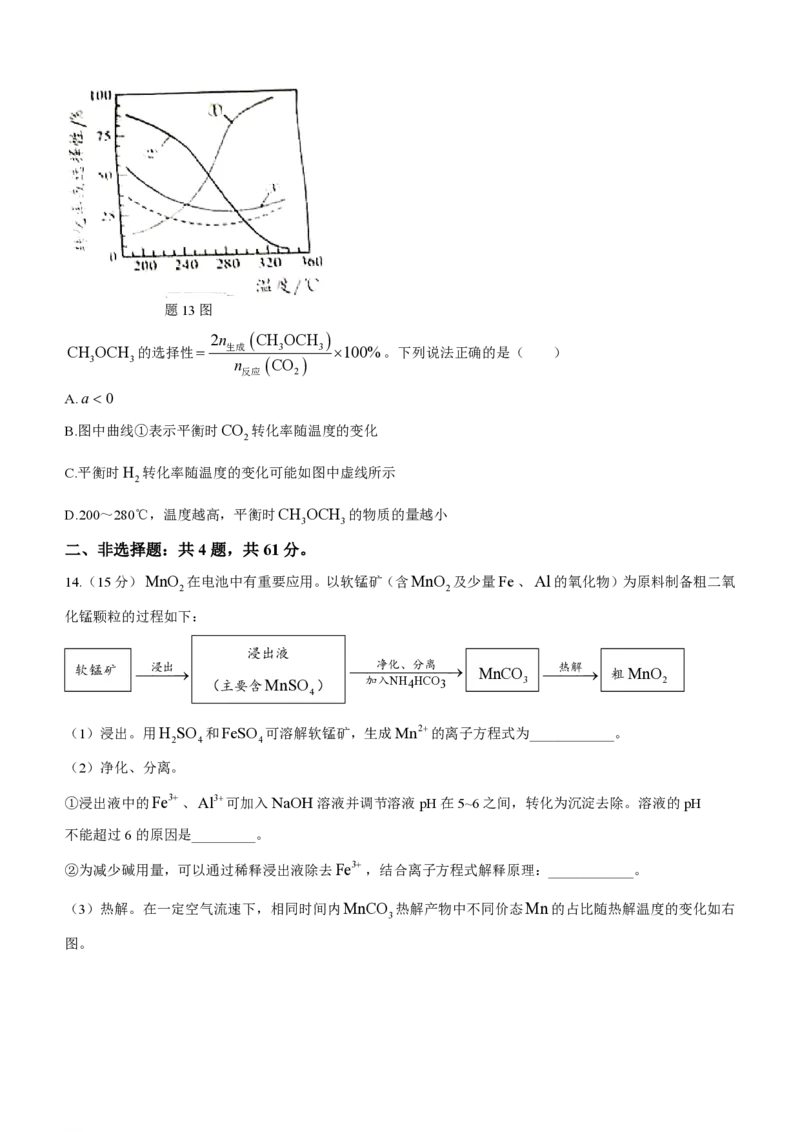
化率随温度的变化如题13图中实线所示。
学科网(北京)股份有限公司题13图
2n CH OCH
CH OCH 的选择性 生成 3 3 100%。下列说法正确的是( )
3 3 n CO
反应 2
A.a 0
B.图中曲线①表示平衡时CO 转化率随温度的变化
2
C.平衡时H 转化率随温度的变化可能如图中虚线所示
2
D.200~280℃,温度越高,平衡时CH OCH 的物质的量越小
3 3
二、非选择题:共 4题,共 61分。
14.(15分)MnO 在电池中有重要应用。以软锰矿(含MnO 及少量Fe、Al的氧化物)为原料制备粗二氧
2 2
化锰颗粒的过程如下:
浸出液
软锰矿 浸 出 净 化、 分 离 MnCO 热 解 粗MnO
(主要含MnSO ) 加入NH4HCO3 3 2
4
(1)浸出。用H SO 和FeSO 可溶解软锰矿,生成Mn2的离子方程式为____________。
2 4 4
(2)净化、分离。
①浸出液中的Fe3、Al3可加入NaOH溶液并调节溶液pH在5~6之间,转化为沉淀去除。溶液的pH
不能超过6的原因是_________。
②为减少碱用量,可以通过稀释浸出液除去Fe3,结合离子方程式解释原理:____________。
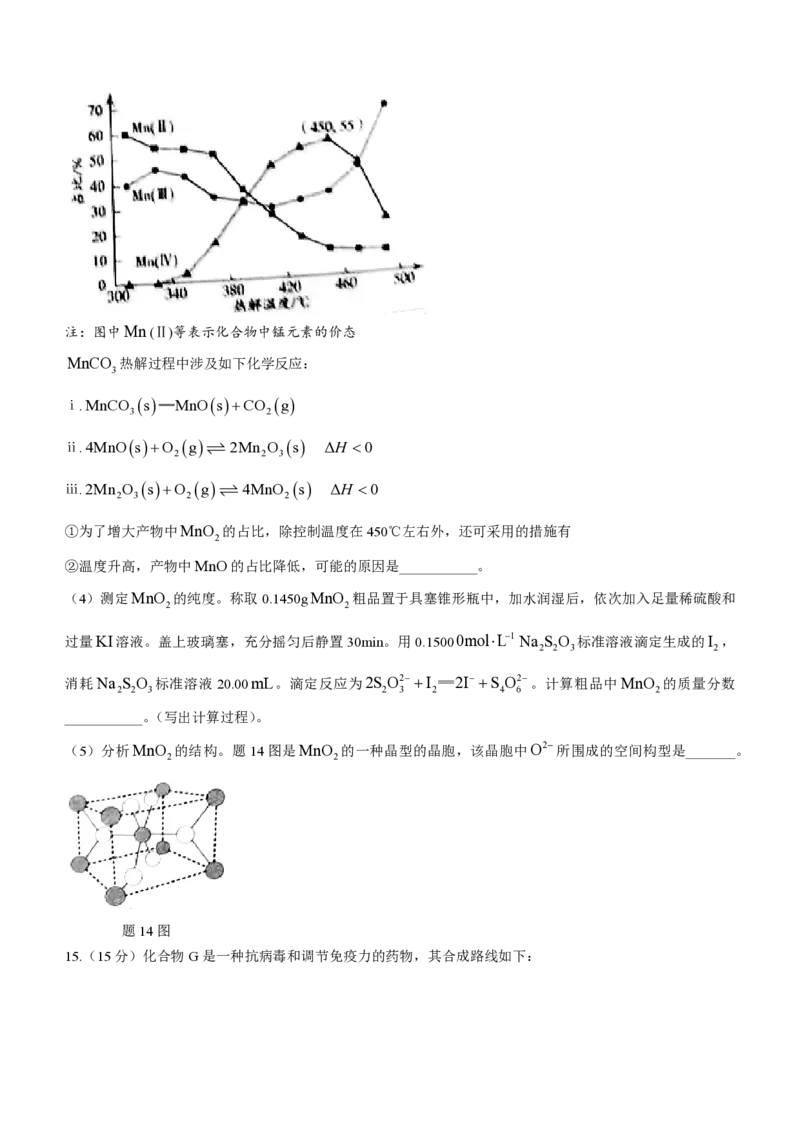
(3)热解。在一定空气流速下,相同时间内MnCO 热解产物中不同价态Mn的占比随热解温度的变化如右
3
图。
学科网(北京)股份有限公司注:图中Mn(Ⅱ)等表示化合物中锰元素的价态
MnCO 热解过程中涉及如下化学反应:
3
ⅰ.MnCO s═MnOsCO g
3 2
ⅱ.4MnOsO g 2Mn O s ΔH 0
2 2 3
ⅲ.2Mn O sO g 4MnO s ΔH 0
2 3 2 2
①为了增大产物中MnO 的占比,除控制温度在450℃左右外,还可采用的措施有
2
②温度升高,产物中MnO的占比降低,可能的原因是___________。
(4)测定MnO 的纯度。称取0.1450gMnO 粗品置于具塞锥形瓶中,加水润湿后,依次加入足量稀硫酸和
2 2
过量KI溶液。盖上玻璃塞,充分摇匀后静置30min。用0.15000molL1 Na S O 标准溶液滴定生成的I ,
2 2 3 2
消耗Na S O 标准溶液 20.00mL。滴定反应为2S O2 I ═2I S O2。计算粗品中MnO 的质量分数
2 2 3 2 3 2 4 6 2
___________。(写出计算过程)。
(5)分析MnO 的结构。题14图是MnO 的一种晶型的晶胞,该晶胞中O2所围成的空间构型是_______。
2 2
题14图
15.(15分)化合物G是一种抗病毒和调节免疫力的药物,其合成路线如下:
学科网(北京)股份有限公司(1)化合物G中碳原子的杂化轨道类型为___________。
(2)D→E的反应类型为___________。
(3)A→B的过程为先发生加成反应,再发生消去反应,写出消去过程中另一种主要副产物(含2个甲基)
的结构简式:___________。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:___________。
分子中含有苯环和四个甲基,核磁共振氢谱有四个峰;能与银氨溶液发生银镜反应。
(5)乙酸和乙酸酐( )均可以发生酯化反应,但C→D反应采用乙酸酐而不采用乙酸的可能原因
是___________。
(6)已知:Ⅰ.
Ⅱ.
写 出 以 、 和 为 原 料 制 备
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见
本题题干)。
16.(15分)钴及其化合物在工业生产中有着广阔的应用前景。
2 3
已知:Co2不易被氧化,Co3具有强氧化性;CoNH 具有较强还原性,CoNH 性质稳定。
3 6 3 6
(1)从锂钴废料(主要成分为LiCoO )分离Co2。
2
学科网(北京)股份有限公司①Co2的电子排布式为______________。
②“酸溶”时不选择浓HCl的理由是:▲
③“净化”时,加NaF固体是将Li转化为沉淀,“净化”后溶液中c F 4.0102molL1。若“过滤
1”后溶液中Li浓度为1.0molL1,则“净化”后c Na ____________。[溶液体积变化忽略不计,不考
虑其他离子影响。25℃时K LiF2.0103]
sp
(2)从由CoCl 制备CoNH Cl 。
2 3 6 3
实验过程:称取研细的CoCl 6H O10.0g和NH Cl50g于烧杯中溶解,将溶液转入三颈烧瓶,分液漏斗中
2 2 4
分别装有25mL浓氨水,5mL30%的H O 溶液,控制反应温度为60℃,打开分液漏斗,反应一段时间后,
2 2
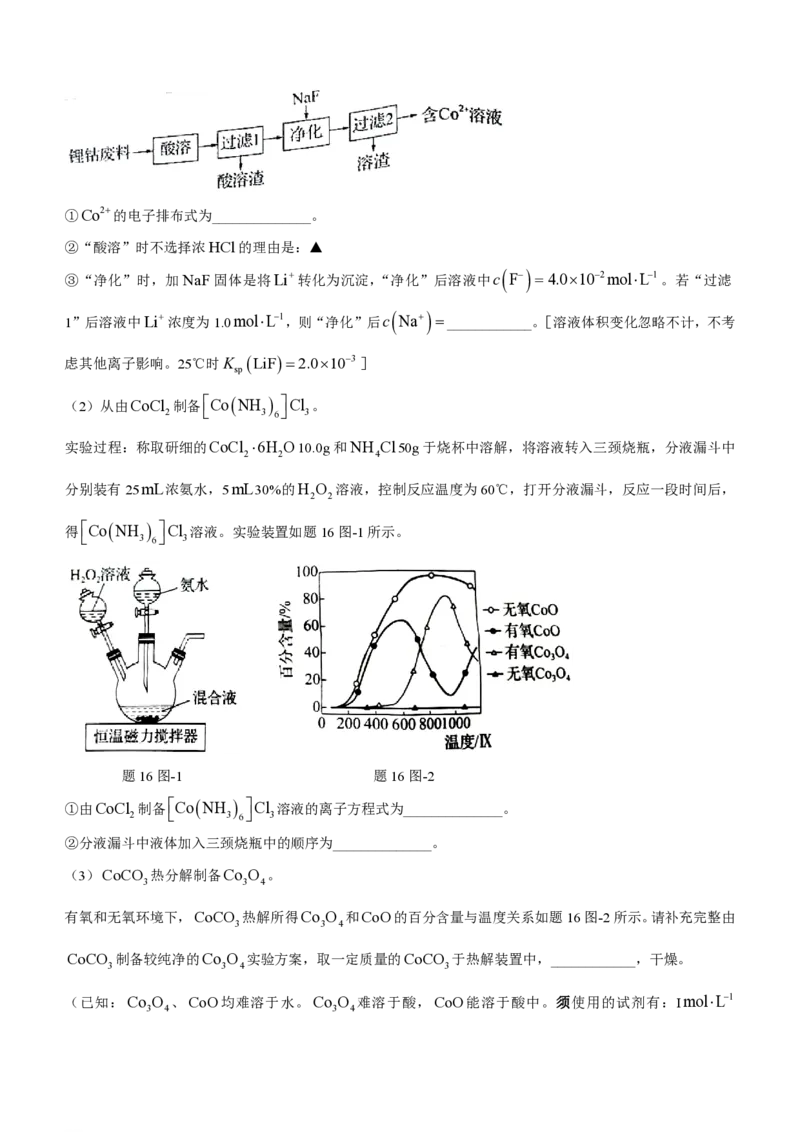
得CoNH Cl 溶液。实验装置如题16图-1所示。
3 6 3
题16图-1 题16图-2
①由CoCl 制备CoNH Cl 溶液的离子方程式为______________。
2 3 6 3
②分液漏斗中液体加入三颈烧瓶中的顺序为______________。
(3)CoCO 热分解制备Co O 。
3 3 4
有氧和无氧环境下,CoCO 热解所得Co O 和CoO的百分含量与温度关系如题16图-2所示。请补充完整由
3 3 4
CoCO 制备较纯净的Co O 实验方案,取一定质量的CoCO 于热解装置中,____________,干燥。
3 3 4 3
(已知:Co O 、CoO均难溶于水。Co O 难溶于酸,CoO能溶于酸中。须使用的试剂有:ImolL1
3 4 3 4
学科网(北京)股份有限公司H SO ,蒸馏水,BaCl 溶液)
2 4 2
17.(16分)将CO 转化为HCOOH能存效减少CO 排放。
2 2
(1)已知:Ⅰ 2COgO g═2CO g ΔH 566.0kJmol1
2 2 1
Ⅱ 2H gO g═2H Og ΔH 483.6kJmol1
2 2 2 2
Ⅲ HCOOHl═CO gH Og ΔH 72.6kJmol1
2 2 3
则CO gH g═HCOOHl H ______________。
2 2 4
(2)325℃时,水在Mn粉表面产生H 和MnO,H 再与CO 反应生产甲酸。
2 2 2
①由H O、Mn、CO 制备甲酸的化学方程式为____________。
2 2
②直接加热H 与CO 难以生成甲酸,该条件下能较快生成甲酸的原因是____________。
2 2
(3)科学家利用CO 在Ru(与Fe同族)基催化剂上加氢成功制得甲酸。其过程如下图所示。
2
①CO 与RuH通过加成形成中间体X,画出中间体X的结构式:____________。
2
②反应过程中加入NaOH或NH 的目的是___________。
3
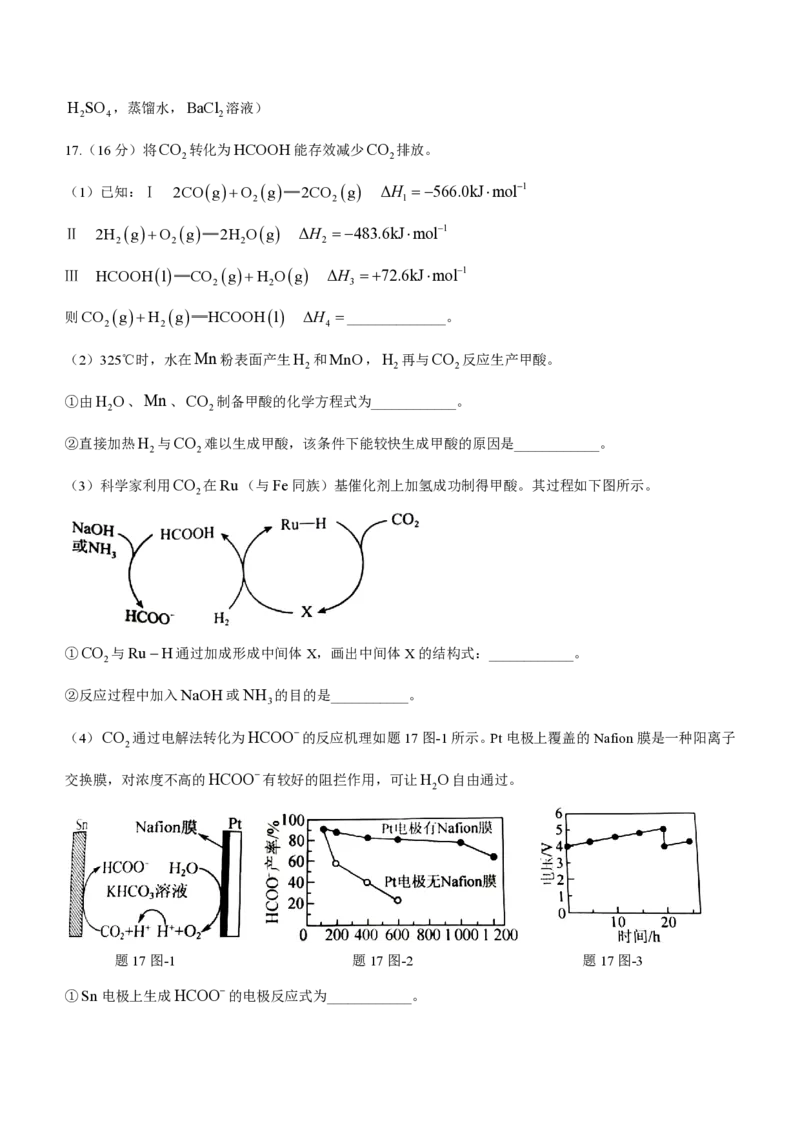
(4)CO 通过电解法转化为HCOO的反应机理如题17图-1所示。Pt电极上覆盖的Nafion膜是一种阳离子
2
交换膜,对浓度不高的HCOO有较好的阻拦作用,可让H O自由通过。
2
题17图-1 题17图-2 题17图-3
①Sn电极上生成HCOO的电极反应式为____________。
学科网(北京)股份有限公司②电路中通过的电量与HCOO产率的关系如题17图-2所示。相同条件下,Pt电极有Nafion膜HCOO产率
明显提高,但电量1000C后又显著下降,可能原因是___________。
③若电解时将Nafon膜置于两个电极中间,保持电流恒定,20h时向阳极区补充KHCO ,电压与时间关系如
3
题17图-3所示。0~20h,电压增大的原因是____________。
高三期初质量检测试卷·化学
参考答案
一、单项选择题:共 13题,每题 3分,共 39分。每题只有一个选项最符合题意。
1.C 2.A 3.B 4.C 5.B 6.D 7.A 8.D 9.B 10.C 11.D 12.B 13.D
二、非选择题:共 4题,共 61分。
14.(15分)
(1)MnO 2Fe2 4H═Mn2 2Fe3 2H O(2分)
2 2
(2)①避免Al(OH) 溶解,防止锰离子沉淀,减少锰元素的损失(2分)
3
②稀释使溶液的pH升高,有利于Fe3 3H
2
O
Fe(OH)
3
3H正向移动(沉淀写FeOOH且配平正确,
也给分)(2分)
(3)①增大空气流速(2分)
②MnO占比降低是由于反应速率ⅱⅰ(或ⅰ已反应完,>的反应速率变快)(2分)
(4)根据元素守恒和得失电子守恒可得关系式:MnO I 2S O2
2 2 2 3
1 1
nMnO n S O2 c S O2 V S O2
2 2 2 3 2 2 3 2 3
1
0.1500molL120.00mL103LmL1
2
1.500103mol (1分)
mMnO 1.500103mol87gmol1 0.1305g (1分)
2
0.1305g
wMnO 100%90.00% (1分)
2 0.1450g
学科网(北京)股份有限公司(5)八面体(答正八面体不扣分)(2分)
15.(15分)
(1)sp2、sp3(2分) (2)取代反应(2分) (3) (2分)
(4) 或 (其他合理答案也给分)(2分)
(5)乙酸和酚酯化需要催化剂、加热等条件,而乙酸酐和酚酯化不需要(或乙酸酐发生酯化反应不生成水,
促进反应正向进行)(2分)
( 6 )
或
(5分)
(其他合理答案也给分)
16.(15分)
(1)①Ar3d7(或1s22s22p63s23d7) (2分)
②浓HCl有还原性,与Co3会发生反应产生Cl ,污染环境(2分)
2
③0.99molL1(2分)
3
(2)①2Co2 2NH H O 10NH H O═2CoNH 12H O(2分)
4 2 2 3 2 3 6 2
②先加浓氨水再加H O 溶液(2分)
2 2
(3)在空气中加热固体(加热时鼓入氧气)(1分),温度在900~1000℃保持一段时间充分反应(1分),取出
固体,冷却;向固体中边搅拌、边加入1molL1 H SO 至固体不再减少(1分),过滤,(1分)用蒸馏水洗
2 4
学科网(北京)股份有限公司涤滤渣至最后一次洗涤液加BaCl 溶液无明显现象(1分)(共5分)
2
17.(16分)
(1)31.4kJmol1
325℃
(2分)①MnCO H O MnOHCOOH(2分)
2 2
②反应生成的MnO是H 与CO 反应的催化剂(2分)
2 2
O
||
(3)①H— C— O— Ru(2分)
②降低浓HCOOH浓度,CO gH g═HCOOHl正向进行程度增大(2分)
2 2
(4)①H CO 2e═HCOO或HCO CO 2e═HCOO CO2(2分)
2 3 2 3
②Nafion膜可以阻止HCOO在阳极放电(1分,答“防止HCOO在阳极被氧化”给分);
电量1000C后,c
HCOO
增大,Nafion膜阻拦作用下降(1分)(共2分)
③阳极区pH减小,HCO浓度下降(1分),K部分迁移至阴极区,阳极区离子浓度下降,导电能力减弱
3
(1分)(共2分)
学科网(北京)股份有限公司