文档内容
2024 北京石景山高三一模
化 学
本试卷共10页,100分。考试时长90分钟。考生务必将答案答在答题卡上,在试卷上作答无效。考
试结束后,将答题卡交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Fe 56 Pd 106
第一部分
本部分共14题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的一项。
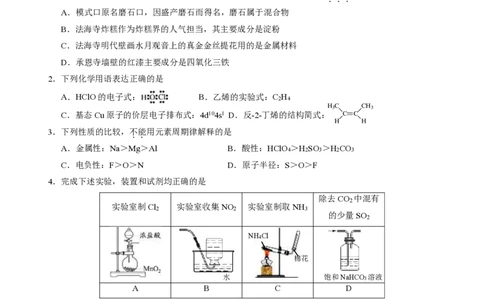
1.石景山模式口历史文化街区已成为北京城市更新的典型案例。下列说法不正确的是
...
A.模式口原名磨石口,因盛产磨石而得名,磨石属于混合物
B.法海寺炸糕作为炸糕界的人气担当,其主要成分是淀粉
C.法海寺明代壁画水月观音上的真金金丝提花用的是金属材料
D.承恩寺墙壁的红漆主要成分是四氧化三铁
2.下列化学用语表达正确的是
A.HClO的电子式: B.乙烯的实验式:C H
2 4
C.基态Cu原子的价层电子排布式:4d104s1 D.反-2-丁烯的结构简式:
3.下列性质的比较,不能用元素周期律解释的是
..
A.金属性:Na>Mg>Al B.酸性:HClO >H SO >H CO
4 2 3 2 3
C.电负性:F>O>N D.原子半径:S>O>F
4.完成下述实验,装置和试剂均正确的是
除去CO 中混有
2
实验室制Cl 实验室收集NO 实验室制取NH
2 2 3
的少量SO
2
A B C D
5.下列离子方程式与所给事实不相符的是
...
A.氨的水溶液显碱性:NH + H O === NH ·H O === NH
3 2 3 2
第1页/共11页
+4 + OH−
B.电解饱和食盐水时阴极析出H
2
:2H
2
O + 2e− === H
2
↑ + 2OH−
C.氯化铁的水溶液显酸性:Fe3+ + 3H O Fe(OH) + 3H+
2 3
D.用加热的方式除去苏打固体中的小苏打:2NaHCO Na CO + H O + CO ↑
3 2 3 2 2
6.利用下列实验药品,能达到实验目的的是
实验目的 实验药品
△
NH4Cl
棉花
饱和NaHCO3 溶液
H C 3
H
C C
C
H
H 3
水A 比较乙酸、碳酸和苯酚的酸性 乙酸、碳酸钠溶液、苯酚钠溶液
B 检验1-溴丁烷中的溴原子 1-溴丁烷、NaOH溶液、AgNO 溶液
3
C 比较镁和铝的金属性强弱 MgCl 溶液、AlCl 溶液、NaOH溶液
2 3
D 证明Ag S比AgCl更难溶 NaCl溶液、AgNO 溶液、硫粉
2 3
7.下列对化学反应速率增大原因的分析错误的是
..
A.有气体参加的化学反应,增大压强使容器容积减小,单位体积内活化分子数增多
B.向反应体系中加入相同浓度的反应物,使活化分子百分数增大
C.升高温度,使反应物分子中活化分子百分数增大
D.加入适宜的催化剂,使反应物分子中活化分子百分数增大
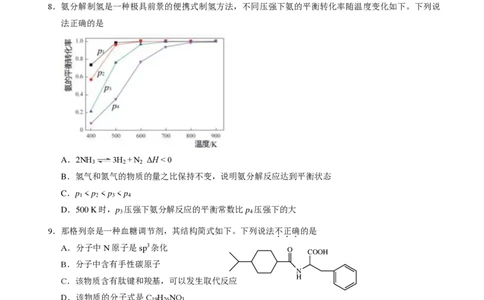
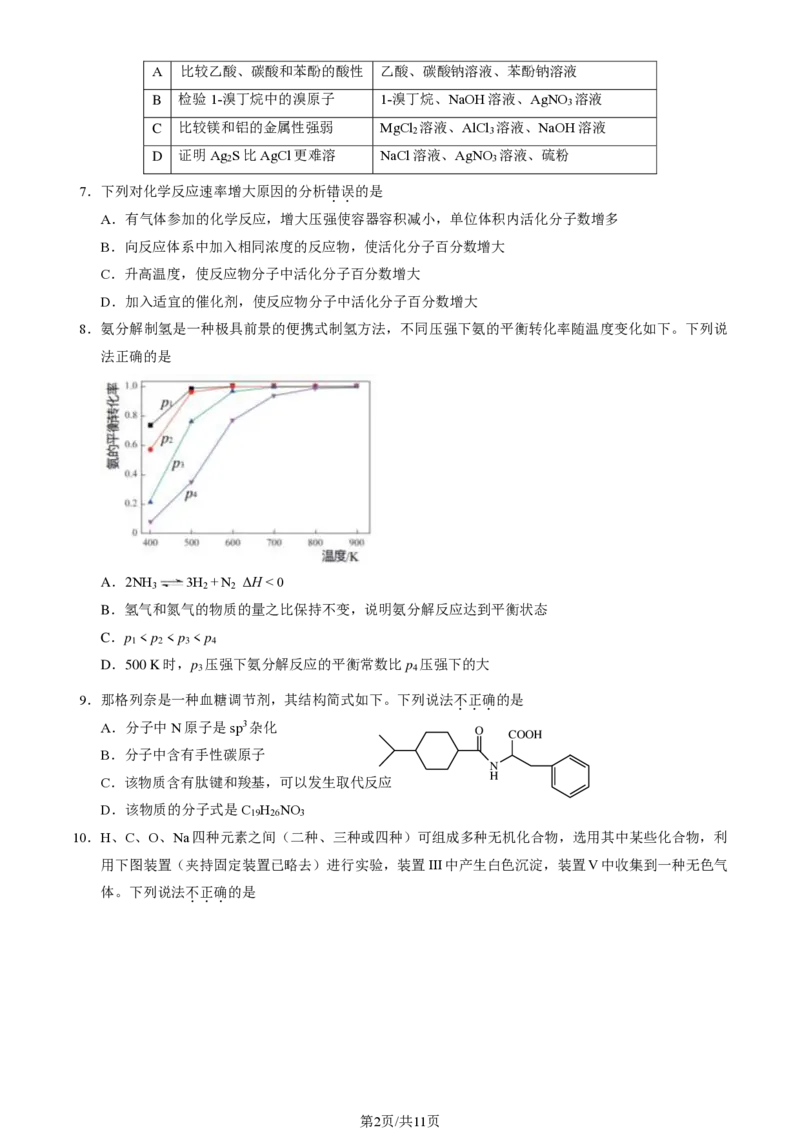
8.氨分解制氢是一种极具前景的便携式制氢方法,不同压强下氨的平衡转化率随温度变化如下。下列说
法正确的是
A.2NH 3H +N ΔH < 0
3 2 2
B.氢气和氮气的物质的量之比保持不变,说明氨分解反应达到平衡状态
C.p < p < p < p
1 2 3 4
D.500 K时,p 压强下氨分解反应的平衡常数比p 压强下的大
3 4
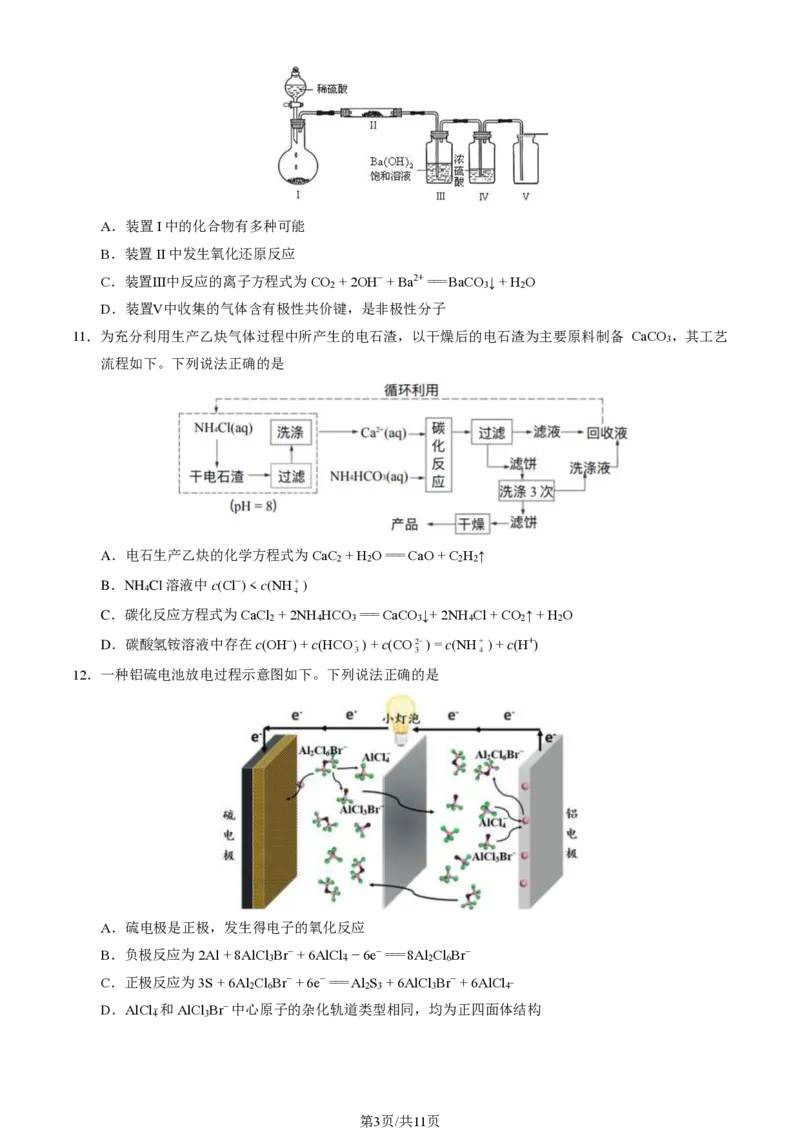
9.那格列奈是一种血糖调节剂,其结构简式如下。下列说法不正确的是
...
A.分子中N原子是sp3杂化
B.分子中含有手性碳原子
C.该物质含有肽键和羧基,可以发生取代反应
D.该物质的分子式是C H NO
19 26 3
10.H、C、O、Na四种元素之间(二种、三种或四种)可组成多种无机化合物,选用其中某些化合物,利
用下图装置(夹持固定装置已略去)进行实验,装置III中产生白色沉淀,装置V中收集到一种无色气
体。下列说法不正确的是
...
第2页/共11页
O
NH
C O O HA.装置I中的化合物有多种可能
B.装置II中发生氧化还原反应
C.装置Ⅲ中反应的离子方程式为CO + 2OH− + Ba2+ === BaCO ↓ + H O
2 3 2
D.装置Ⅴ中收集的气体含有极性共价键,是非极性分子
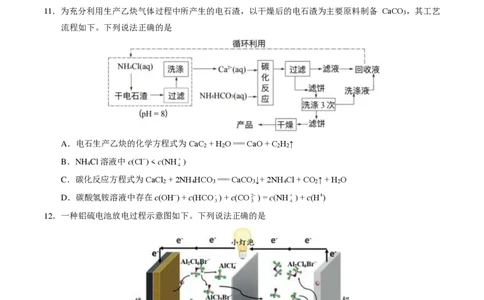
11.为充分利用生产乙炔气体过程中所产生的电石渣,以干燥后的电石渣为主要原料制备 CaCO ,其工艺
3
流程如下。下列说法正确的是
A.电石生产乙炔的化学方程式为CaC + H O === CaO + C H ↑
2 2 2 2
B.NH Cl溶液中c(Cl−) < c(NH
4
第3页/共11页
+4 )
C.碳化反应方程式为CaCl + 2NH HCO === CaCO ↓+ 2NH Cl + CO ↑ + H O
2 4 3 3 4 2 2
D.碳酸氢铵溶液中存在c(OH−) + c(HCO ﹣3 ) + c(CO ﹣23 ) = c(NH +4 ) + c(H+)
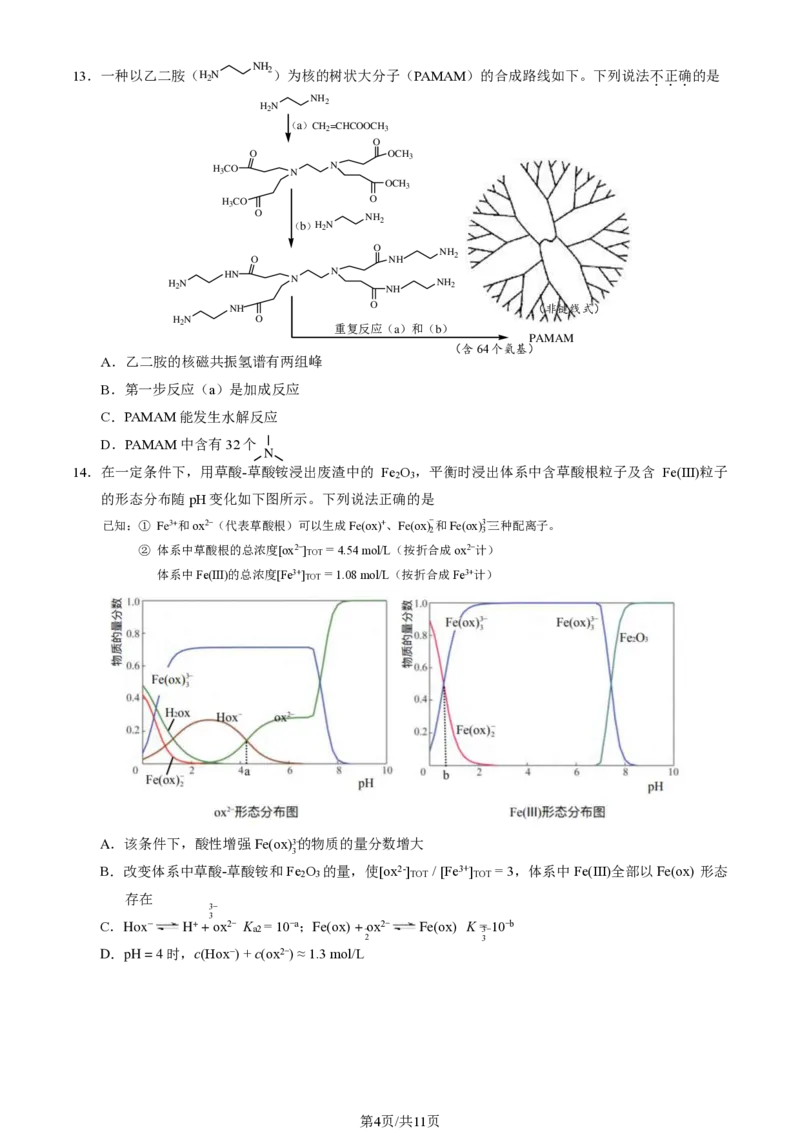
12.一种铝硫电池放电过程示意图如下。下列说法正确的是
A.硫电极是正极,发生得电子的氧化反应
B.负极反应为2Al + 8AlCl
3
Br− + 6AlCl−4 − 6e− === 8Al
2
Cl
6
Br−
C.正极反应为3S + 6Al 2 Cl 6 Br− + 6e− === Al 2 S 3 + 6AlCl 3 Br− + 6AlCl 4−
D.AlCl 4− 和AlCl 3 Br− 中心原子的杂化轨道类型相同,均为正四面体结构13.一种以乙二胺(HN
NH2)为核的树状大分子(PAMAM)的合成路线如下。下列说法不正确的是
2 ...
H2N
NH2
(a)CH2=CHCOOCH3
O
O OCH3
H3CO N N
OCH3
H3CO O
O
NH2
(b)H2N
O
O
NH
NH2
H2N HN N N
NH
NH2
NH O
H2N O
重复反应(a)和(b)
PAMAM
A.乙二胺的核磁共振氢谱有两组峰
B.第一步反应(a)是加成反应
C.PAMAM能发生水解反应
D.PAMAM中含有32个
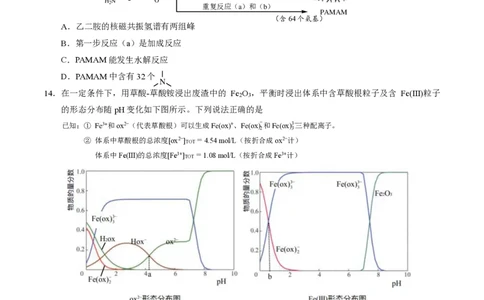
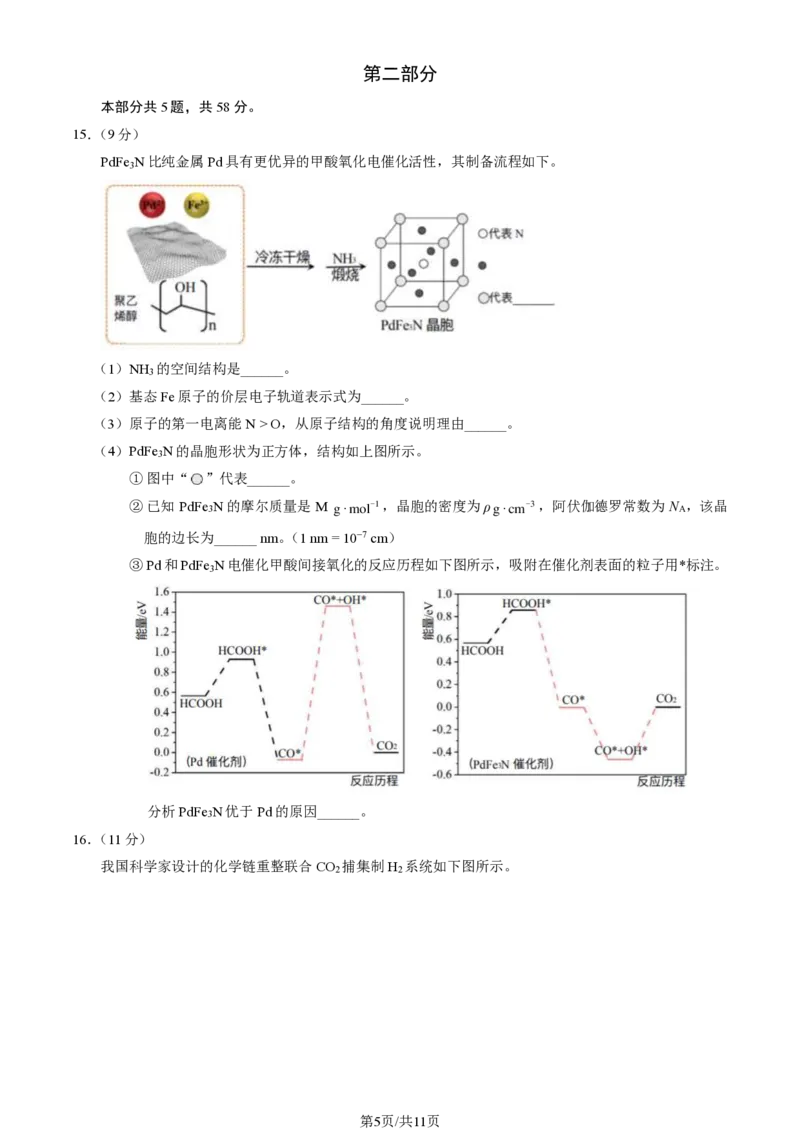
14.在一定条件下,用草酸-草酸铵浸出废渣中的 Fe O ,平衡时浸出体系中含草酸根粒子及含 Fe(Ⅲ)粒子
2 3
的形态分布随pH变化如下图所示。下列说法正确的是
已知:① Fe3+和ox2−(代表草酸根)可以生成Fe(ox)+、Fe(ox) 和Fe(ox) 三种配离子。
② 体系中草酸根的总浓度[ox2−]TOT = 4.54 mol/L(按折合成ox2−计)
体系中Fe(Ⅲ)的总浓度[Fe3+]TOT = 1.08 mol/L(按折合成Fe3+计)
A.该条件下,酸性增强Fe(ox) 的物质的量分数增大
B.改变体系中草酸-草酸铵和Fe
2
O
3
的量,使[ox2-]
TOT
/ [Fe3+]
TOT
= 3,体系中Fe(Ⅲ)全部以Fe(ox) 形态
存在
C.Hox− H+ + ox2− K = 10−a;Fe(ox) + ox2− Fe(ox) K = 10−b
a2
D.pH = 4时,c(Hox−) + c(ox2−) ≈ 1.3 mol/L
第4页/共11页
N
(非键线式)
(含64个氨基)
− 3−
2 3
3−
3
3−
3
− 3−
2 3第二部分
本部分共5题,共58分。
15.(9分)
PdFe N比纯金属Pd具有更优异的甲酸氧化电催化活性,其制备流程如下。
3
(1)NH 的空间结构是______。
3
(2)基态Fe原子的价层电子轨道表示式为______。
(3)原子的第一电离能N > O,从原子结构的角度说明理由______。
(4)PdFe N的晶胞形状为正方体,结构如上图所示。
3
① 图中“ ”代表______。
② 已知 PdFe N的摩尔质量是 M 3
第5页/共11页
g m o l - 1 ,晶胞的密度为 ρ g c m - 3 ,阿伏伽德罗常数为 N ,该晶 A
胞的边长为______ nm。(1 nm = 10−7 cm)
③ Pd和PdFe N电催化甲酸间接氧化的反应历程如下图所示,吸附在催化剂表面的粒子用*标注。
3
分析PdFe N优于Pd的原因______。
3
16.(11分)
我国科学家设计的化学链重整联合CO 捕集制H 系统如下图所示。
2 2(1)空气反应器中发生______反应(填“吸热”或“放热”)。
(2)重整气中有H 、CO、CO 、CH 和H O,燃料反应器中CH 和NiO反应的化学方程式有______。
2 2 4 2 4
(3)CaO吸收反应器中还发生蒸汽变换反应(CO与水蒸气或CH 与水蒸气反应)
4
① 1 mol CH 和水蒸气生成CO 和H 吸收热量165 kJ,1 mol CH 和水蒸气生成CO和H 吸收热
4 2 2 4 2
量206 kJ。CO(g)+H O (g) === H (g)+CO (g) ΔH = ______。
2 2 2
② 反应温度对H
2
产率( 产
燃
品
料
气
中
中
C H
H
4
2
的
的
物
物
质
质
的
的
量
量 )、CO
2
捕集率(1- 产
重
品
整
气
气
中
中
C
C
O
O
2
2
的
的
物
物
质
质
的
的
量
量
)及产品气组成
的影响如下图所示。
结合化学方程式说明图1中温度升高CO 捕集率降低的原因______。
2
解释图2中温度升高H 体积分数降低的原因______。
2
(4)燃料反应器和吸收反应器中加入水蒸气的作用______。
17.(13分)
HO O
3'-prenylgenistein( )是从大豆中分离出来的新型异戊烯基异黄酮,具有
OH O
OH
重要的生物防御活性,其合成路线如下。
第6页/共11页已知: (R为H或烃基)
(1)D中含有的官能团是______。
(2)A → B的目的是保护酚羟基,B中含有酯基,A → B的化学方程式是______。
(3)E的分子式是C H Br。F的结构简式是______。
5 9
(4)下列说法正确的是______(填序号)。
a.B → C和D → F的反应类型均是取代反应
b.含有苯环和 的D的同分异构体有4种
c.G在上述有机合成中的作用是保护酚羟基
(5)G的分子式是C H ClO,I + G → J的化学方程式是______。I和G生成J的产率大于90%,I分子
2 5
中一个羟基未参与反应的主要原因是:I中的分子内氢键降低了其反应活性,在 I的结构中画出存
在的分子内氢键______。
(6)依据K → L的原理,K先“去保护”再“关环”会生成一种含有4个六元环的有机化合物X,其
结构简式是______。
18.(12分)
从铅银渣(含Pb、Ag、Cu等金属元素)中提取银的流程如下。
已知:PbSO4 难溶于水;Ag+可以和SO
第7页/共11页
﹣23 形成[Ag(SO3)2]3−。
(1)“酸浸”时,使用H SO 、NaCl和NaNO 的混合液作为浸出剂。
2 4 3
① 加入NaNO 的作用______。
3
② 固体B含有______。
(2)用氨水和水合肼(N H ·H O)进行“络合浸出”和“还原析银”。
2 4 2
① 氨水“络合浸出”的化学方程式是______。
R 1
O
C R
3
2
A
C H 7
'-p re n
+ R
O 8
y lg
3
e n
H
C
H
O
C
is
O
催 化
te in
O
C
O
剂
O
多
R
步
4
反
B
C H O 9 1 0
O
应
催 化 剂 加 热
2
C
光
O
O
R 1
l2
照
O
R
C
C
2
H 9
R
C
CC
8
O
O
L
3
l2
O
C
O 2
稀
R 4
硫
+
酸
O
H 2 O
O H
C H O
D
C H 8
O
一
I
8
关
定
O
环
E
条
4
件
一
O
定
G
条
F
件
O
O
C
一
1
O
定
H 2
G
条
J
1 6
件
O 6
O H
O
K
C 1 4
加热
HH
1 8
催化剂
O 3
O O
滤液A
铅银渣
氧化焙烧
焙烧渣
酸浸
固体C
络合浸出
固体B
Ag
还原析银
滤液D
滤液E
D② 将水合肼“还原析银”反应的离子方程式补充完整:
□ ______+ N H ·H O === N ↑ + H O + □ ______ + □ ______ + □ NH ↑
2 4 2 2 2 3
(3)用Na SO 和甲醛进行“络合浸出”和“还原析银”。
2 3
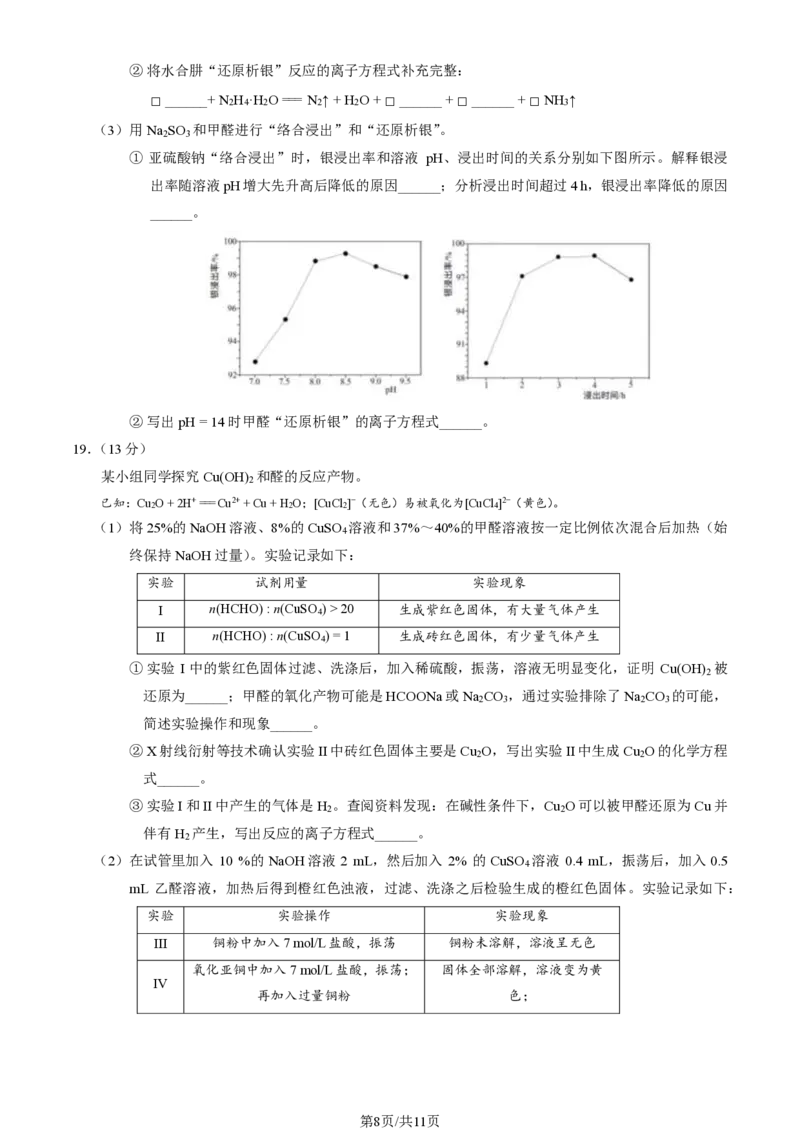
① 亚硫酸钠“络合浸出”时,银浸出率和溶液 pH、浸出时间的关系分别如下图所示。解释银浸
出率随溶液pH增大先升高后降低的原因______;分析浸出时间超过4 h,银浸出率降低的原因
______。
② 写出pH = 14时甲醛“还原析银”的离子方程式______。
19.(13分)
某小组同学探究Cu(OH) 和醛的反应产物。
2
已知:Cu2O + 2H+ === Cu2+ + Cu + H2O;[CuCl2]−(无色)易被氧化为[CuCl4]2−(黄色)。
(1)将25%的NaOH溶液、8%的CuSO 溶液和37%~40%的甲醛溶液按一定比例依次混合后加热(始
4
终保持NaOH过量)。实验记录如下:
实验 试剂用量 实验现象
I n(HCHO) : n(CuSO 4 ) > 20 生成紫红色固体,有大量气体产生
II n(HCHO) : n(CuSO 4 ) = 1 生成砖红色固体,有少量气体产生
① 实验 I 中的紫红色固体过滤、洗涤后,加入稀硫酸,振荡,溶液无明显变化,证明 Cu(OH) 被
2
还原为______;甲醛的氧化产物可能是HCOONa或Na CO ,通过实验排除了Na CO 的可能,
2 3 2 3
简述实验操作和现象______。
② X射线衍射等技术确认实验II中砖红色固体主要是Cu O,写出实验II中生成Cu O的化学方程
2 2
式______。
③ 实验I和II中产生的气体是H 。查阅资料发现:在碱性条件下,Cu O可以被甲醛还原为Cu并
2 2
伴有H 产生,写出反应的离子方程式______。
2
(2)在试管里加入 10 %的NaOH溶液2 mL,然后加入 2% 的CuSO 溶液 0.4 mL,振荡后,加入0.5
4
mL 乙醛溶液,加热后得到橙红色浊液,过滤、洗涤之后检验生成的橙红色固体。实验记录如下:
实验 实验操作 实验现象
Ⅲ 铜粉中加入7 mol/L盐酸,振荡 铜粉未溶解,溶液呈无色
氧化亚铜中加入7 mol/L盐酸,振荡; 固体全部溶解,溶液变为黄
Ⅳ
再加入过量铜粉 色;
第8页/共11页黄色溶液变为无色
Ⅴ 橙红色固体中加入7 mol/L盐酸,振荡 固体全部溶解,溶液变为黄色
① 实验Ⅲ的目的______。
② 用离子方程式解释实验Ⅳ溶液中发生的变化:______。
③ 结合以上实验,小组同学认为橙红色固体只有Cu O,你认为是否合理并说明原因______。
2
第9页/共11页参考答案
第一部分共14题,每题3分,共42分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14
答案 D A B D A C B C D D C B D D
第二部分共5题,共58分。
15.(9分)(其它合理答案酌情给分)
(1)(1分)三角锥
(2)(1分)
(3)(2分)N的电子排布是半充满的,比较稳定,电离能较高
(4)① (1分)Pd
② (2分)3 √ 𝑀 × 107
𝜌∙𝑁𝐴
③ (2 分)Pd 作催化剂时,吸附 OH*需要克服较高的能垒,较难实现;PdFe N作催化剂时,Fe 容易吸
3
附OH*促进CO*的除去。
16.(11分)(其它合理答案酌情给分)
(1)(1分)放热
(2)(2分)CH + NiO 2H + CO + Ni和CH + 2NiO 2H + CO + 2Ni
4 2 4 2 2
(3)① (2分)- 41 kJ/mol
② (2分)CaCO CaO + CO ↑ ,温度升高促进碳酸钙分解
3 2
(2分)CO(g) +H O(g) === H (g) +CO (g) ΔH <0,CO 浓度增大和升高温度均促使平衡逆向移动,
2 2 2 2
H 体积分数降低
2
(4)(2分)通过蒸汽变换等反应增大产品气中H 的产率与体积分数,促进CO 的吸收
2 2
17.(13分)(其它合理答案酌情给分)
(1)(2分)醛基和羟基
(2)(2分)
(3)(2分)
(4)(2分)abc
(5)(2分)
(1分)
第10页/共11页
O
H
O
H C
O
H
O
+
H
O
O
O
O
H
H
O
+
O
2
O
催 化 剂
C l
一 定 条
O
件
O
+
O
O
O
O
O H
O
O
O
H
2 H C l
↑↓ ↑ ↑ ↑ ↑ ↑↓
H
O O
HO OH
△
△ △
3d 4s(6)(2分)
18.(12分)(其它合理答案酌情给分)
(1)① (1分)利用硝酸根在酸性条件下的氧化性,将金属单质氧化
② (1分)AgCl和PbSO
4
(2)① (2分)AgCl + 2NH ·H O === [Ag(NH ) ]Cl + 2H O
3 2 3 2 2
② (2分)4[Ag(NH ) ]+ + N H ·H O === N ↑ + H O + 4Ag↓+ 4NH + 4NH ↑
3 2 2 4 2 2 2 4 3
(3)① (2分)溶液pH增大有利于增大亚硫酸根浓度,进而提高银浸出率;
碱性过高Ag+会生成Ag O,导致浸出率降低
2
(2分)亚硫酸钠既是银的配合剂也是还原剂,会将Ag+还原为Ag
② (2分)2[Ag(SO ) ]3− + HCHO + 3OH− === 2Ag↓+ 4SO + HCOO− + 2H O
3 2 2
19.(13分)(其它合理答案酌情给分)
(1)① (1分)Cu
(2分)取少量反应后的溶液,加入过量盐酸,未产生使澄清石灰水变浑浊的气体
② (2分)HCHO + 2Cu(OH) + NaOH HCOONa + Cu O + 3H O
2 2 2
③ (2分)Cu O + 2HCHO + 2OH− 2Cu + H ↑ + 2HCOO− + H O
2 2 2
(2)① (1分)验证铜粉与7 mol/L盐酸不反应
② (3分)Cu O + 2H+ + 4Cl− === 2[CuCl ]− + H O;
2 2 2
4[CuCl ]− + O + 4H+ + 8Cl− === 4[CuCl ]2− + 2H O;
2 2 4 2
[CuCl ]2− + Cu === 2[CuCl ]−
4 2
③ (2分)不合理;橙红色固体可能是Cu O和Cu的混合物
2
第11页/共11页
H O
O H
O
O
O
+
2−
3
△
△