文档内容
项城三高 2023—2024 学年度上期第一次考试
高 三 化 学 试 卷(宏素班)
(满分 100 分,考试时间:90 分钟)
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,所有答案都写在答题卷上可能
用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 Fe-56 Cu-64 Ba-137
第Ⅰ卷 选择题 (共 48 分)
一、选择题(本题包括16小题,每小题3分,共48分,每小题只 有 一 个 选项符合题
. . . .
意)
1. 化学与生活、社会发展息息相关,下列说法错误的是 ( )
A. 《荷塘月色》中所描绘的月光穿过薄雾形成缕缕光束的美景与胶体性质有关
B. “青蒿一握,以水二升渍,绞取汁”,诗句中体现的屠呦呦对青蒿素的提取属化学变化
C. “熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
D. “千锤万凿出深山,烈火焚烧若等闲”,是指石灰石的分解反应
2.分类是科学研究的重要方法,下列物质分类不
.
正
.
确
.
的是 (
)
A.化合物:干冰、冰水混合物、烧碱 B.同素异形体:石墨、C60、金刚
石C.混合物:漂白粉、矿泉水、空气 D.电解质:熔融 NaCl、硫酸、铜
3.下列条件下,可以大量共存的离子组是( )
A. 含有大量ClO 的溶液中:
B. pH=13 的溶液中:
C.透明溶液中:
D.含有大量 的
溶液:
4. 实验室进行粗盐提纯时,需除去 Ca2+、Mg2+和 ,所用试剂及顺序为( )
A.Na2CO3、BaCl2、HCl、NaOH B.BaCl2、 Na2CO3、NaOH、HCl
C.BaCl2、K2CO3、HCl、NaOH D.BaCl2、Na2CO3、NaOH、HNO35. 下列反应的离子方程式正确的是( )
A.碘化亚铁溶液与等物质的量的氯气:
B.向硫化钠溶液通入足量二氧化硫:
C.将氯气通入冷的石灰乳中制漂白粉:
D.向次氯酸钙溶液通入足量二氧化碳:
6. 关于反应 ,下列说法正确的是( )
A. N 是还原产物 B.氧化剂与还原剂的物质的量之比为 1:4
2
C. N H 既是氧化剂又是还原剂 D.生成 28gN ,转移 4mol 电子
2 4 2
7. 已知含有 15N A 个 Na2SO3 粒子的 Na2SO3 溶液恰好与含有 5N A 个 KRO4 粒子的 KRO4
溶液完全反应转化为 Na2SO4。则 R 元素在产物中的化合价是
A.+1 B.+2 C.+3 D.+4
8. 已知 I-、Fe2+、SO2、Cl-和 H2O2 均有还原性,它们在酸性溶液中的还原性顺序为:
SO2>I->Fe2+>H2O2>Cl-,则下列反应不可能发生的是
9. 用 N A 表示阿伏加德罗常数的数值,下列叙述正确的是
A. 标准状况下,22.4 L H2O 含有的分子数为 N A
B. 通常状况下,O3 和 O2 的混合气体 16 g 所含氧原子数为 N A
C.0.1 mol Na2O2 与足量的 CO2 充分反应转移的电子数为 0.2N
A
D.物质的量浓度为 1 mol·L-1 的 MgCl2 溶液中,含有 Cl-个数为
2N 10.下列叙述正确的是
A
A. 在标准状况下,2.24LSO3 中含有 SO3 分子数目约为6.02 1022
B. 0.1molFe 在 0.1molCl 中充分燃烧,生成0.1molFeCl
2 2C. 在标准状况下, 2.24LO 和 CO 的混合气体中含 C、O 原子共 0.2mol
2
D. 0.1molFeCl 形成 FeOH 胶体, FeOH 胶粒的数目为6.02 1022
3
3
11. 配制 100 mL 0.5 mol·L-1 Na2CO3 溶液,下列操作错误的是
A. 选用 100 mL 容量瓶进行配制
B. 将 Na2CO3 固体溶解并冷却至室温后移至容量瓶中
C. 移液后用蒸馏水洗涤烧杯、玻璃棒两次,洗涤液移至容量瓶中
D. 沿玻璃棒向容量瓶中注入蒸馏水,至溶液的凹液面恰好与容量瓶刻度线相
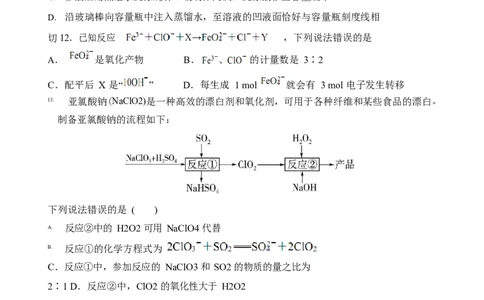
切12.已知反应 ,下列说法错误的是
:
A. 是氧化产物 B. 的计量数是 3∶2
C.配平后 X 是“ ” D.每生成 1 mol 就会有 3 mol 电子发生转移
13. 亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。
制备亚氯酸钠的流程如下:
下列说法错误的是 ( )
A. 反应②中的 H2O2 可用 NaClO4 代替
B. 反应①的化学方程式为
C.反应①中,参加反应的 NaClO3 和 SO2 的物质的量之比为
2∶1 D.反应②中,ClO2 的氧化性大于 H2O2
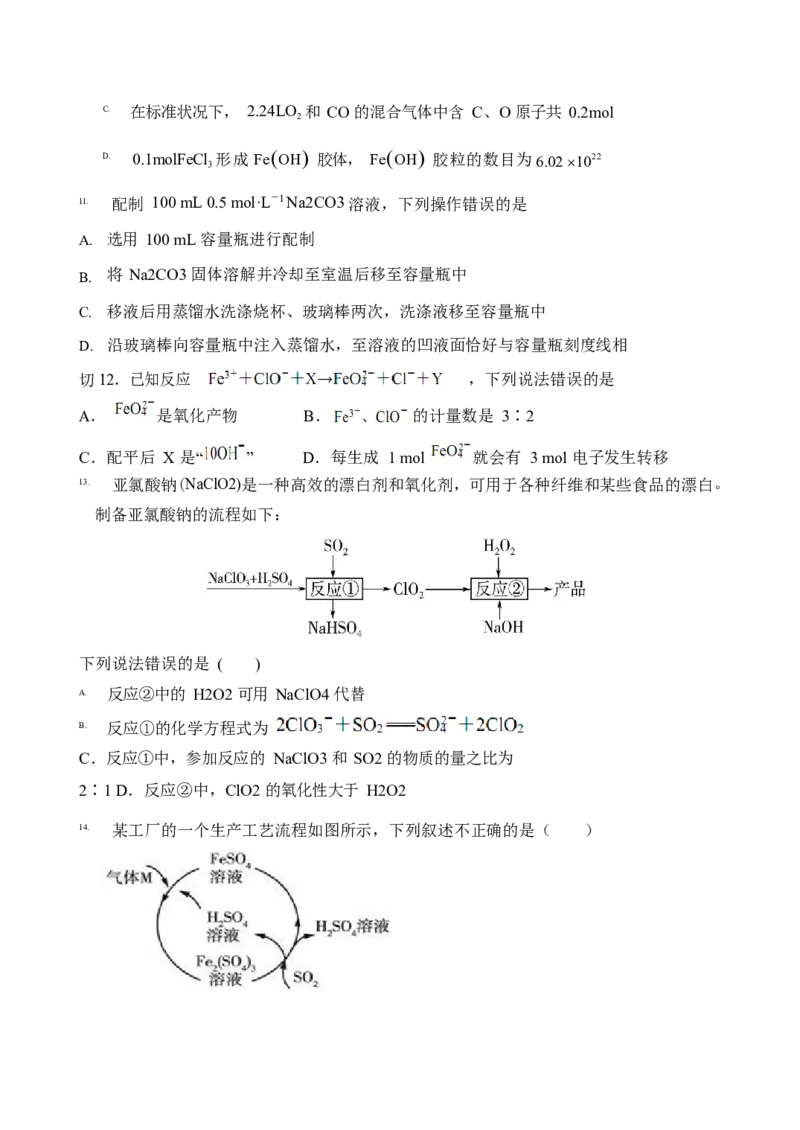
14. 某工厂的一个生产工艺流程如图所示,下列叙述不正确的是( )A.该工艺流程用来制备
H2SO4 B.气体 M 是 O2
C.气体 M 与 FeSO4 溶液发生的反应属于化合反应
D.SO2 与 Fe2(SO4)3 溶液反应时氧化剂和还原剂的物质的量之比是 1:1
15.现有一混合物的水溶液,可能含有以下离子中的若干种:
SO2 。现取两份各 100 mL 溶液进行如下实验:
4
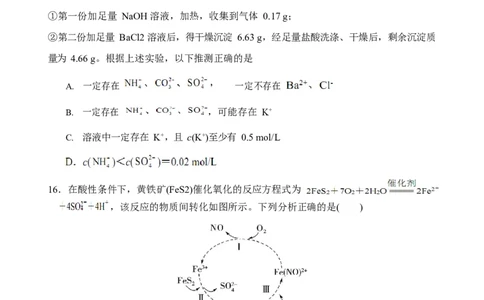
①第一份加足量 NaOH 溶液,加热,收集到气体 0.17 g;
②第二份加足量 BaCl2 溶液后,得干燥沉淀 6.63 g,经足量盐酸洗涤、干燥后,剩余沉淀质
量为 4.66 g。根据上述实验,以下推测正确的是
A. 一定存在 一定不存在
B. 一定存在 ,可能存在 K+
C. 溶液中一定存在 K+,且 c(K+)至少有 0.5 mol/L
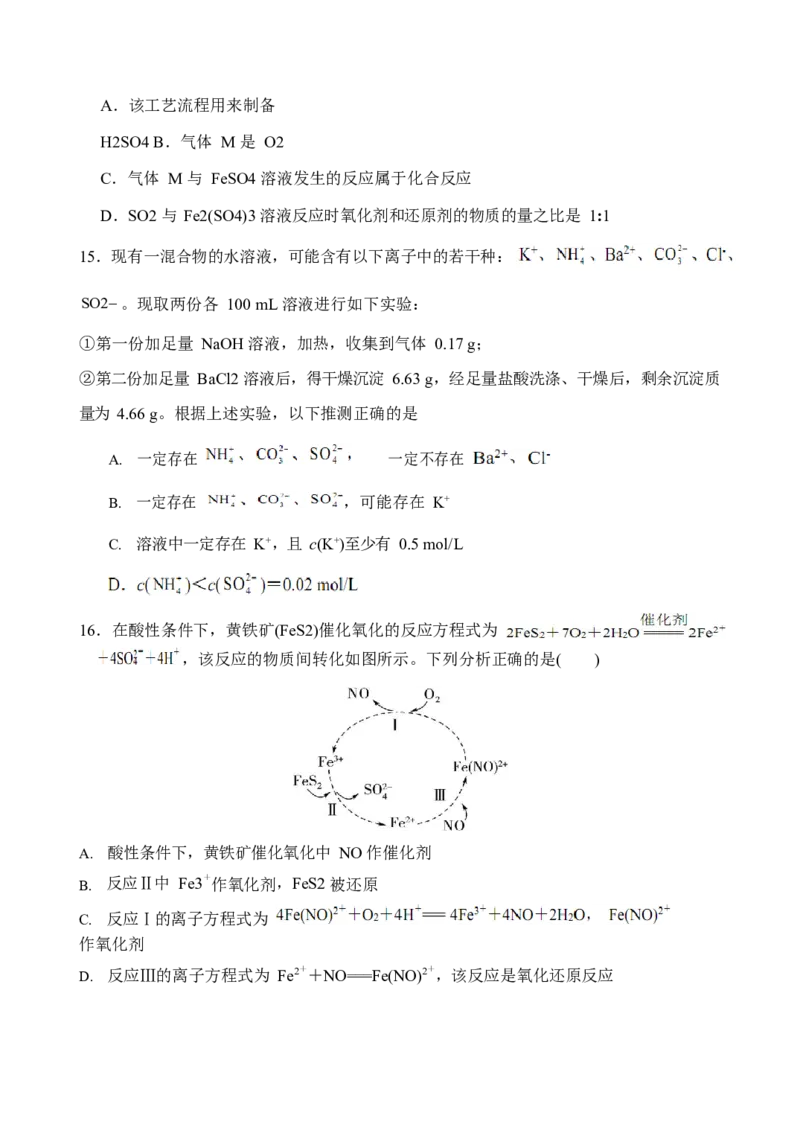
16.在酸性条件下,黄铁矿(FeS2)催化氧化的反应方程式为
,该反应的物质间转化如图所示。下列分析正确的是( )
A. 酸性条件下,黄铁矿催化氧化中 NO 作催化剂
B. 反应Ⅱ中 Fe3+作氧化剂,FeS2 被还原
C. 反应Ⅰ的离子方程式为
作氧化剂
D. 反应Ⅲ的离子方程式为 Fe2++NO===Fe(NO)2+,该反应是氧化还原反应第Ⅱ卷 (非选择题,共 52 分)
二、非选择题(本题包括 4 小题,共 52 分)
17.(12 分)现有下列 10 种物质:①铝,②纯醋酸,③CO2,④H2SO4,⑤NaOH,⑥
硫酸铜溶液,⑦熔融的 NaCl,⑧NaHSO4,⑨硝酸钾晶体,⑩乙醇。
(1)上述物质中属于非电解质的有 (填序号);①②⑥⑦⑨⑩这六种物质中
能导电的有 (填序号)。
(2)向⑥中加入⑤的离子方程式是 。
(3)⑧在水中的电离方程式为 。
(4)上述物质中有两种物质在水溶液中发生的反应可用离子反应 H++OH-=H2O 表示,
请写出该离子反应对应的其中一个化学方程式 。
(5)用双线桥表示 CaH2+2H2O=Ca(OH)2+2H2↑反应电子转移情况:
。
18.(10 分)硫代硫酸钠俗名大苏打,可用以除去自来水中的氧气,也可和稀硫酸发生反应:
Na 2S2O3 H2SO4 =Na 2SO4 S SO2 H2O ,已知某硫代硫酸钠溶液试剂瓶体标签如图
所示,请回答下列问题:
大苏打
【有效成分】 Na 2 S 2 O 3 【规格】1000mL
【质量分数】20% 【密度】1.58g/cm 3
(1)该试剂 Na SO (摩尔质量:158g/mol)溶液的物质的量浓度为 。
2 2 3
(2)某同学欲用Na S O 5H O (摩尔质量:248g/mol )固体配制 60mL 与该试剂物质的量浓度
2 2 3 2
相同的溶液,需要用托盘天平称量 Na S O 5H O 固体的质量为 g。所用到的主要
2 2 3 2
仪器除如图所示外,还需要的玻璃仪器有 。(3)该同学用 98% (密度为1.84g/cm3 )的浓硫酸配制 100mL 2.3mol/L 的稀硫酸用于实验,需
用浓硫酸的体积为 mL。
(4)若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是 (填序号)
①配制前,容量瓶中有少量蒸馏水 ②用量筒量取浓硫酸时俯视刻度线
②定容时俯视容量瓶刻度线 ④加水时超过容量瓶刻度线,再用胶头滴管吸出
19.(15 分)现有四种阳离子 Na+ 、Ba2 、Mg2 、H 和四种阴离子
可分别组成 A、B、C、D 四种易溶于水易电离的物质(离子均不
重复)。
已知:①A 溶液能使紫色石蕊试液变红,且阴阳离子个数比为 1:2;
②B 溶液分别与 A、C、D 溶液混合,均有白色沉淀生成;
③C 溶液能与 A 溶液反应产生无色无味气体。
请填空:
(1)写出下列物质的化学式:B ;D 。
(2)写出下列反应的离子方程式:
①A 溶液与 B 溶液反应的离子方程式: 。
②B 溶液与 D 溶液反应的离子方程式: 。
(3)简述检验 A 中阴离子的方法: 。
(4)C 在水溶液中的电离方程式为 ;向该盐的溶液中加入
足量的 NaOH 溶液,发生反应的离子方程式为 。
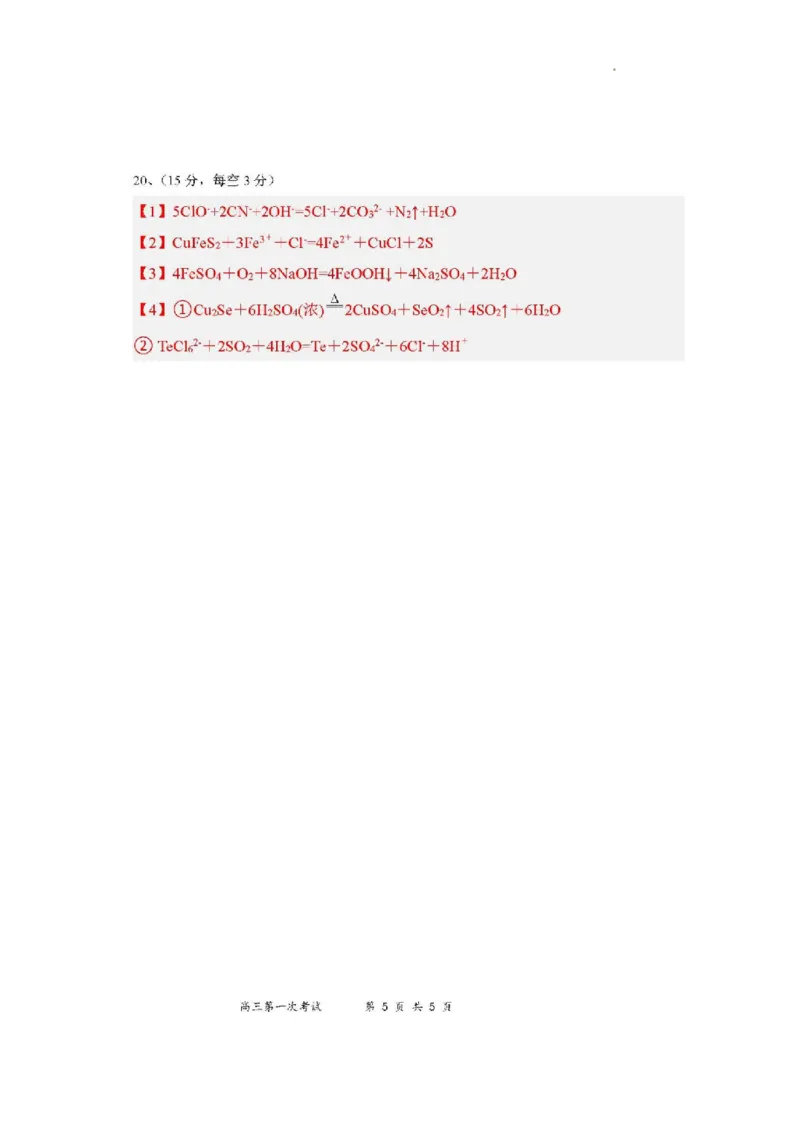
20.(15 分)请按要求书写下列方程式:
(1)由于氰化钠有剧毒,因此需要对“废液”中的氰化钠进行处理,通常选用漂白粉或
漂白液在碱性条件下将其氧化,其中一种产物为空气的主要成分,则在碱性条件下漂白液与氰化钠反应的离子方程式为 。
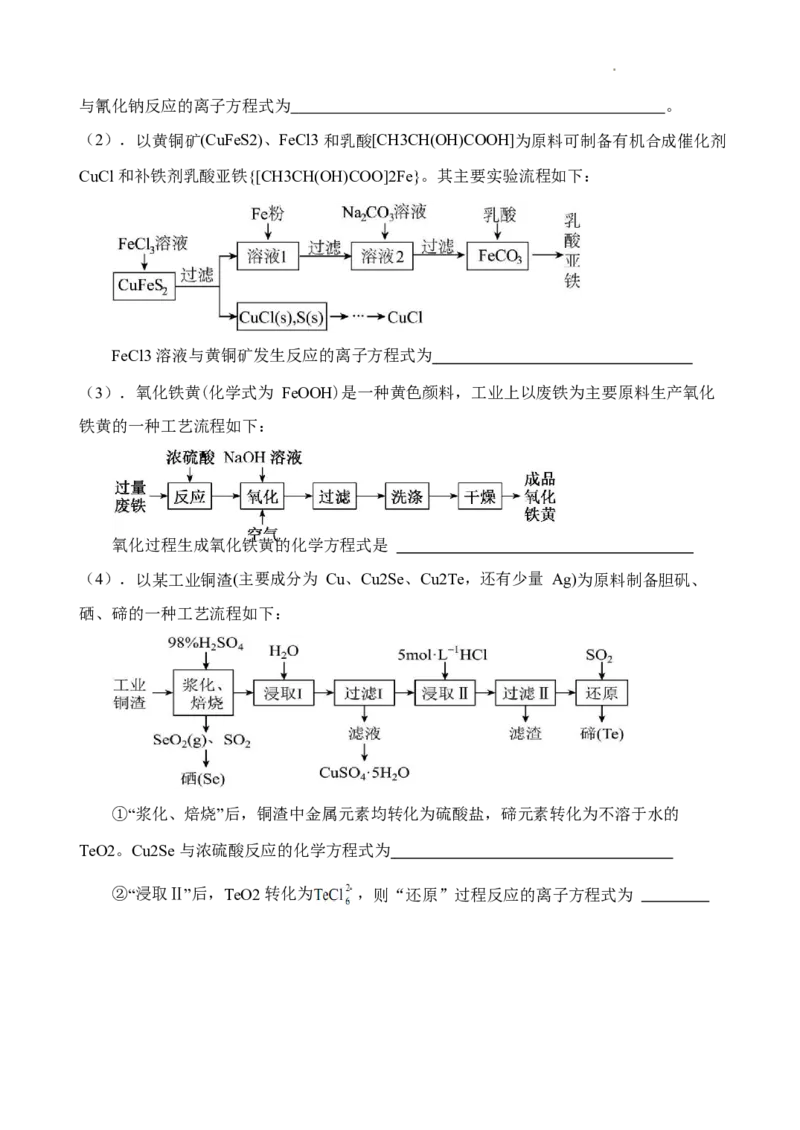
(2).以黄铜矿(CuFeS2)、FeCl3 和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂
CuCl 和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下:
FeCl3 溶液与黄铜矿发生反应的离子方程式为
(3).氧化铁黄(化学式为 FeOOH)是一种黄色颜料,工业上以废铁为主要原料生产氧化
铁黄的一种工艺流程如下:
氧化过程生成氧化铁黄的化学方程式是
(4).以某工业铜渣(主要成分为 Cu、Cu2Se、Cu2Te,还有少量 Ag)为原料制备胆矾、
硒、碲的一种工艺流程如下:
①“浆化、焙烧”后,铜渣中金属元素均转化为硫酸盐,碲元素转化为不溶于水的
TeO2。Cu2Se 与浓硫酸反应的化学方程式为
②“浸取Ⅱ”后,TeO2 转化为 ,则“还原”过程反应的离子方程式为
学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司学科网(北京)股份有限公司