文档内容
湖北省重点高中智学联盟 2023 年秋季高三年级 10 月联考
化学试题
命题学校:湖北省武穴中学 命题人:乐敏 朱李军 审题人:任建华
可能使用到的相对原子质量:
一、选择题:本题共15小题,每题3分,共45分,在每小题给出的四个选项中,只有一项是
符合题目要求的。
1.近年我国材料技术发展迅速,已跻身世界先进国家行列。下列说法不正确的是( )
港珠澳大桥
石墨烯超轻海绵 “祝融号”火星车 光纤内窥镜
A.石墨烯超轻海绵属于 B.港珠澳大桥锚具材料 C.“祝触号”火星车主 D.微创手术所用光纤内
有机高分子材料 ——特殊工艺的低碳钢 体部件采用新型铝基碳 窥镜的光纤属于新型无
属于合金 化硅材料属于复合材料 机非金属材料
A.A B.B C.C D.D
2.水是维持生命过程的必需物质。下列有关说法正确的是( )
A.用电子式表示 的形成过程:
B. 和 互为同素异形体
C.某温度下测得 的蒸馏水显中性
D.冰雪融化时需吸热,是因为该过程破坏了 中的共价键
3.类推(类比迁移)的思维方法可以预测许多物质的性质。但类比是相对的,不能违背客观事实。下列类比
分析结果正确的是( )
A.钠保存在煤油中,则锂也应保存在煤油中
B. 与 反应生成 ,则 与 反应可生成
C. 溶于盐酸生成 和 ,则 溶于氢碘酸生成 和 ;
D.少量 通入 溶液生成 ,则少量 通入 溶液生成
4.下列各组离子在给定溶液中能大量共存的是( )
A.1.0mol/L 盐酸中:B.1.0molL 氨水中:
C.0.1 mol/L 溶液中:
D.0.1 mol/L 溶液中:
5.设 表示阿伏加德罗常数的值。下列说法正确的是( )
A.0.1mol/L 晶体中含有阳离子0.2
B.14g 晶体 中含有共价键数目为2
C.叠氮化铵( )可发生爆炸反应: ,则每收集标准状况下22.4L气体转
移电子数为
D.0.1mol/L NHHCO溶液中含有 数目小于0.1
6.下列叙述对应的离子方程式一定正确的是( )
A.向氧化铝溶液中滴加过量的氨水:
B.向含1mol/L 的溶液中通入1mol :
C.湿润的淀粉碘化钾试纸遇某红棕色气体后,试纸变蓝:
D.向 、 和 浓度之比1:1:1的溶液中加入过量的 溶液:
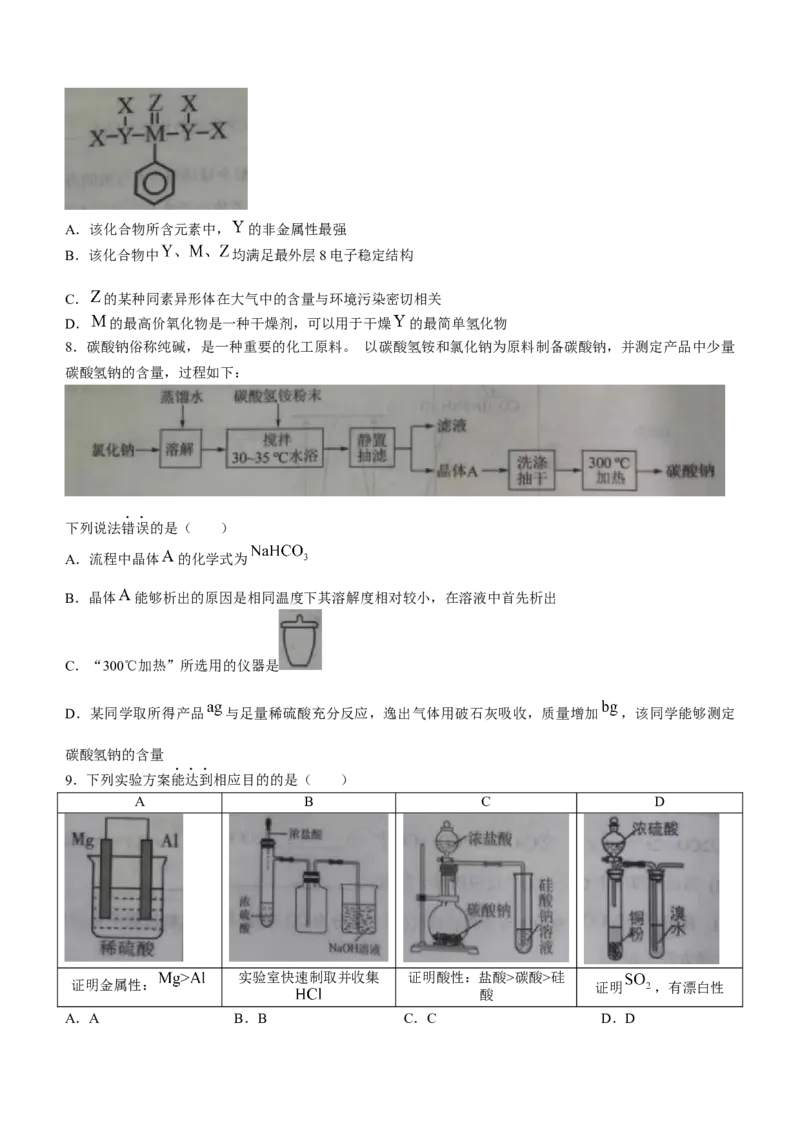
7. 某化合物是一种新型抗肿瘤药的原料, 结构如图,其中 是原子序数依次增大的四种短
周期主族元素,下列说法正确的是( )A.该化合物所含元素中, 的非金属性最强
B.该化合物中 均满足最外层8电子稳定结构
C. 的某种同素异形体在大气中的含量与环境污染密切相关
D. 的最高价氧化物是一种干燥剂,可以用于干燥 的最简单氢化物
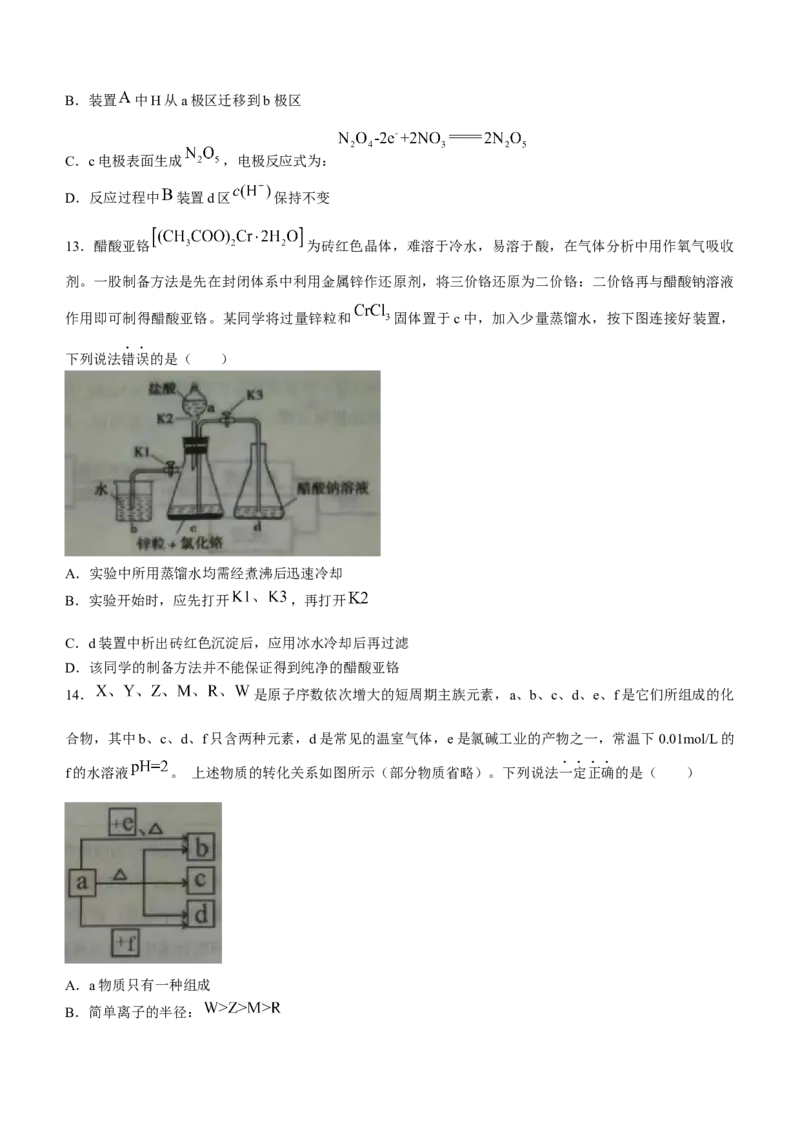
8.碳酸钠俗称纯碱,是一种重要的化工原料。 以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量
碳酸氢钠的含量,过程如下:
下列说法错误的是( )
A.流程中晶体 的化学式为
B.晶体 能够析出的原因是相同温度下其溶解度相对较小,在溶液中首先析出
C.“300℃加热”所选用的仪器是
D.某同学取所得产品 与足量稀硫酸充分反应,逸出气体用破石灰吸收,质量增加 ,该同学能够测定
碳酸氢钠的含量
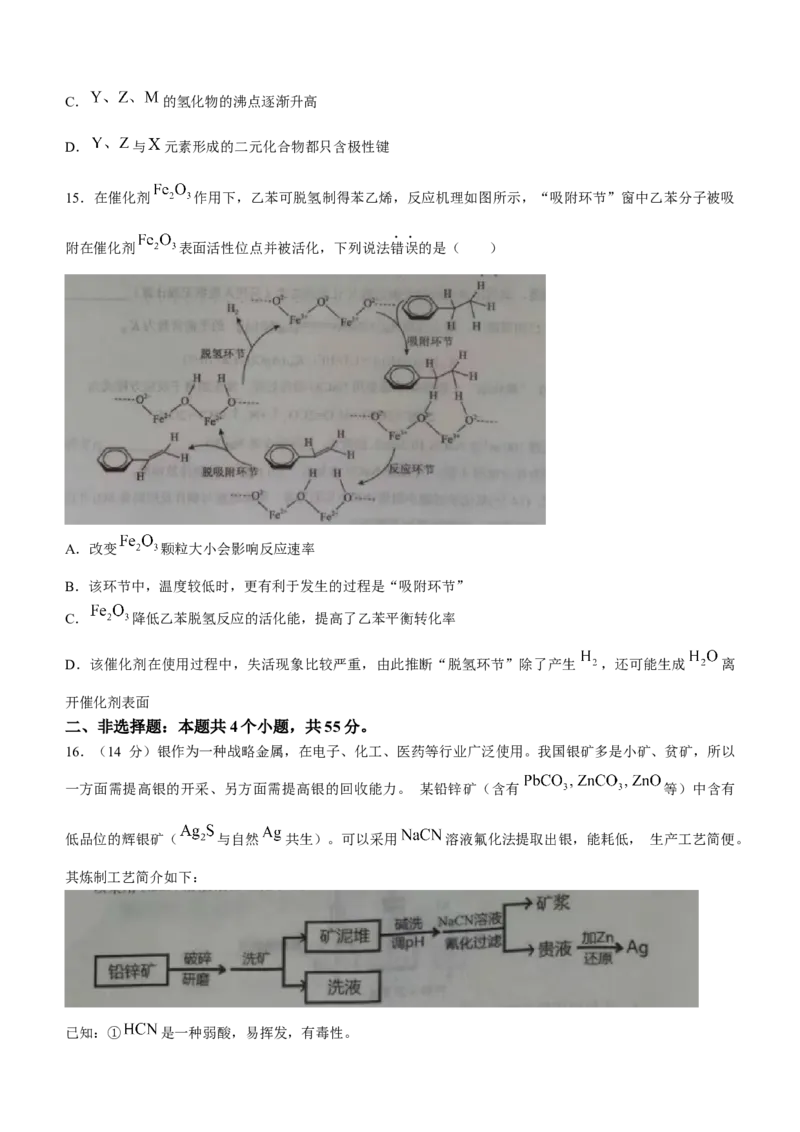
9.下列实验方案能达到相应目的的是( )
A B C D
实验室快速制取并收集 证明酸性:盐酸>碳酸>硅
证明金属性: 证明 ,有漂白性
酸
A.A B.B C.C D.D10.拟卤素是指由二个或二个以上电负性较大的元素的原子组成的原子团,这些原子团在自由状态时,与卤
素单质的性质相似,成为阴离子时与卤素阴离子的性质也相似。硫氰 是一种重要的似卤素,可发生
如下反应:
下列说法错误的是( )
A. 为还原产物
B. 可以和 反应,生成 ;
C.每消耗1mol ,转移 个电子
D. 可以和 反应,可能生成两种盐
11.铁盐、卤素单质及其化合物的很多化学反应存在限度,下列实验或事实对应的结论正确的是( )
选项 实验 结论
向 溶液中滴加 溶液,溶液变红,再加入少量
A 与 的反应不可逆
固体,溶液颜色无明显变化
取两份新制氯水,分别滴加 溶液和淀粉 溶液,
B 氯气与水的反应存在限度
前者生成白色沉淀,后者溶液氯气与水的反应存在限度变
蓝
C 向浓 溶液滴加少量的 溶液,充分反应后,滴加 证明 和 的反应存在限
溶液,溶液变红 度
D 高炉炼铁中增加高炉的高度,炉顶尾气中 的比例没有改 与 和 的反应存在限度
变 有关
A.A B.B C.C D.D
12.硝化剂可在化学反应中向有机化合物中引入硝基、硝酸酯基 是一种绿色硝化剂。有人设想利用工
业废气 ,依据电化学原理制备 和 。装置图如下,下列说法不正确的是( )
A.装置 可将电能转化为化学能B.装置 中H从a极区迁移到b极区
C.c电极表面生成 ,电极反应式为:
D.反应过程中 装置d区 保持不变
13.醋酸亚铬 为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收
剂。一股制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬:二价铬再与醋酸钠溶液
作用即可制得醋酸亚铬。某同学将过量锌粒和 固体置于c中,加入少量蒸馏水,按下图连接好装置,
下列说法错误的是( )
A.实验中所用蒸馏水均需经煮沸后迅速冷却
B.实验开始时,应先打开 ,再打开
C.d装置中析出砖红色沉淀后,应用冰水冷却后再过滤
D.该同学的制备方法并不能保证得到纯净的醋酸亚铬
14. 是原子序数依次增大的短周期主族元素,a、b、c、d、e、f是它们所组成的化
合物,其中b、c、d、f只含两种元素,d是常见的温室气体,e是氯碱工业的产物之一,常温下0.01mol/L的
f的水溶液 。 上述物质的转化关系如图所示(部分物质省略)。下列说法一定正确的是( )
A.a物质只有一种组成
B.简单离子的半径:C. 的氢化物的沸点逐渐升高
D. 与 元素形成的二元化合物都只含极性键
15.在催化剂 作用下,乙苯可脱氢制得苯乙烯,反应机理如图所示,“吸附环节”窗中乙苯分子被吸
附在催化剂 表面活性位点并被活化,下列说法错误的是( )
A.改变 颗粒大小会影响反应速率
B.该环节中,温度较低时,更有利于发生的过程是“吸附环节”
C. 降低乙苯脱氢反应的活化能,提高了乙苯平衡转化率
D.该催化剂在使用过程中,失活现象比较严重,由此推断“脱氢环节”除了产生 ,还可能生成 离
开催化剂表面
二、非选择题:本题共4个小题,共55分。
16.(14 分)银作为一种战略金属,在电子、化工、医药等行业广泛使用。我国银矿多是小矿、贫矿,所以
一方面需提高银的开采、另方面需提高银的回收能力。 某铅锌矿(含有 等)中含有
低品位的辉银矿( 与自然 共生)。可以采用 溶液氟化法提取出银,能耗低, 生产工艺简便。
其炼制工艺简介如下:
已知:① 是一种弱酸,易挥发,有毒性。② 易溶解于 溶液中,且 对游离态和化合态的银均能浸出,氰化过程发生反应之
一为:
③调 过程中, 已经溶解为 ,常温下,
(1) 中 原子均满足8电子稳定结构。写出 的电子式_________
(2)“碱洗”过程中需用生石灰调节矿泥 ,方可进行 溶液喷淋,其目的是_________
(3)矿泥堆要有良好的渗透性和孔隙度,以提供足够的氧。请写出“氧化”过程中自然银 生成
的反应的离子方程式_____________________
(4)提炼过程中发现,矿石中的 对 的“氰化”是有利的,原因是____________
(5)银回收技术中,常用稀硝酸和食盐处理含银废料,得到 固体后,用10%氨水溶解,再通过还原法
得到粗银。
请写出 溶于氨水的化学方程式______________________________,该反应存在一定限度,试列出该反
应的平衡常数 计算表达式(只代入数据无须计算)
(已知常温下,络合反应 的平衡常数为 。
)
(6)“氟化法”中最终矿浆需要用 消毒处理,发生的离子反应方程式为
处理100 含 10.3mg/L的废水,实际至少需 ______g(实际用量应为理论值的4倍).才能
使 含量低于0.5 mg/L,达到排放标准。
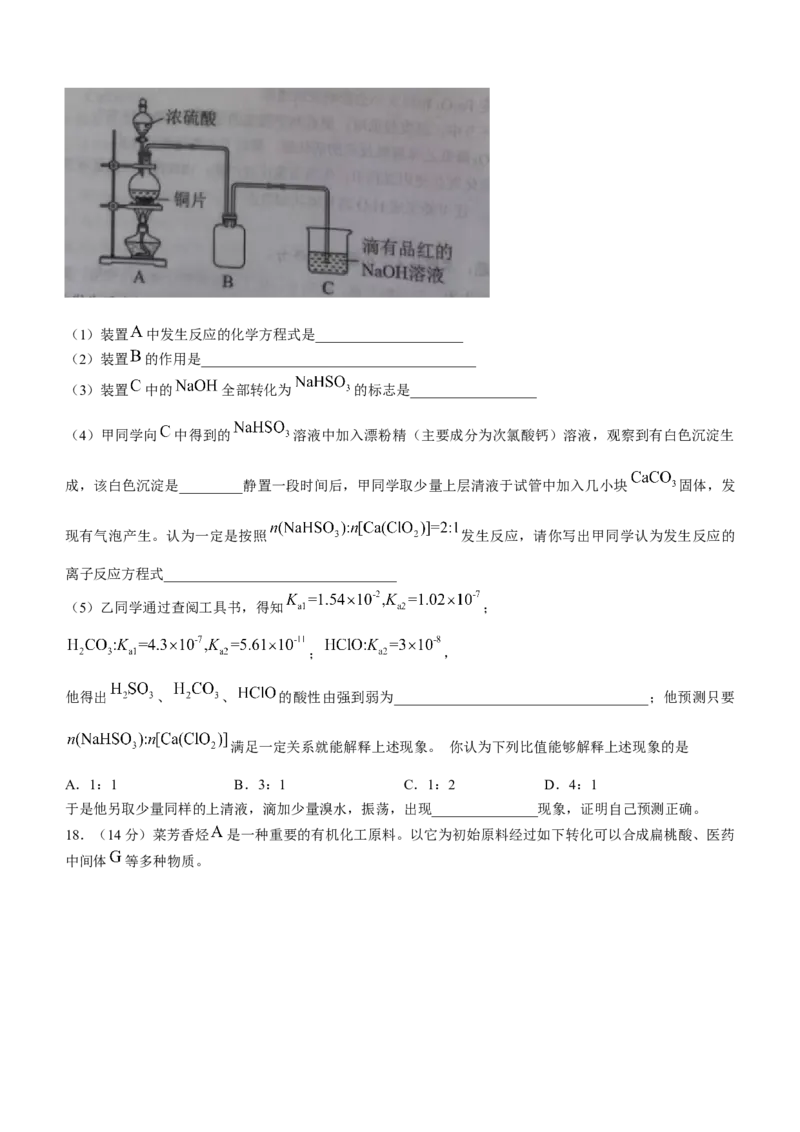
17.(14分)某化学兴趣小组设计如下实验方案,用浓硫酸与钢片反应制备 ,并进行相关实验探究,实
验装置如下图所示:(1)装置 中发生反应的化学方程式是_____________________
(2)装置 的作用是_______________________________________
(3)装置 中的 全部转化为 的标志是__________________
(4)甲同学向 中得到的 溶液中加入漂粉精(主要成分为次氯酸钙)溶液,观察到有白色沉淀生
成,该白色沉淀是_________静置一段时间后,甲同学取少量上层清液于试管中加入几小块 固体,发
现有气泡产生。认为一定是按照 发生反应,请你写出甲同学认为发生反应的
离子反应方程式_________________________________
(5)乙同学通过查阅工具书,得知 ;
; ,
他得出 、 、 的酸性由强到弱为____________________________________;他预测只要
满足一定关系就能解释上述现象。 你认为下列比值能够解释上述现象的是
A.1:1 B.3:1 C.1:2 D.4:1
于是他另取少量同样的上清液,滴加少量溴水,振荡,出现_______________现象,证明自己预测正确。
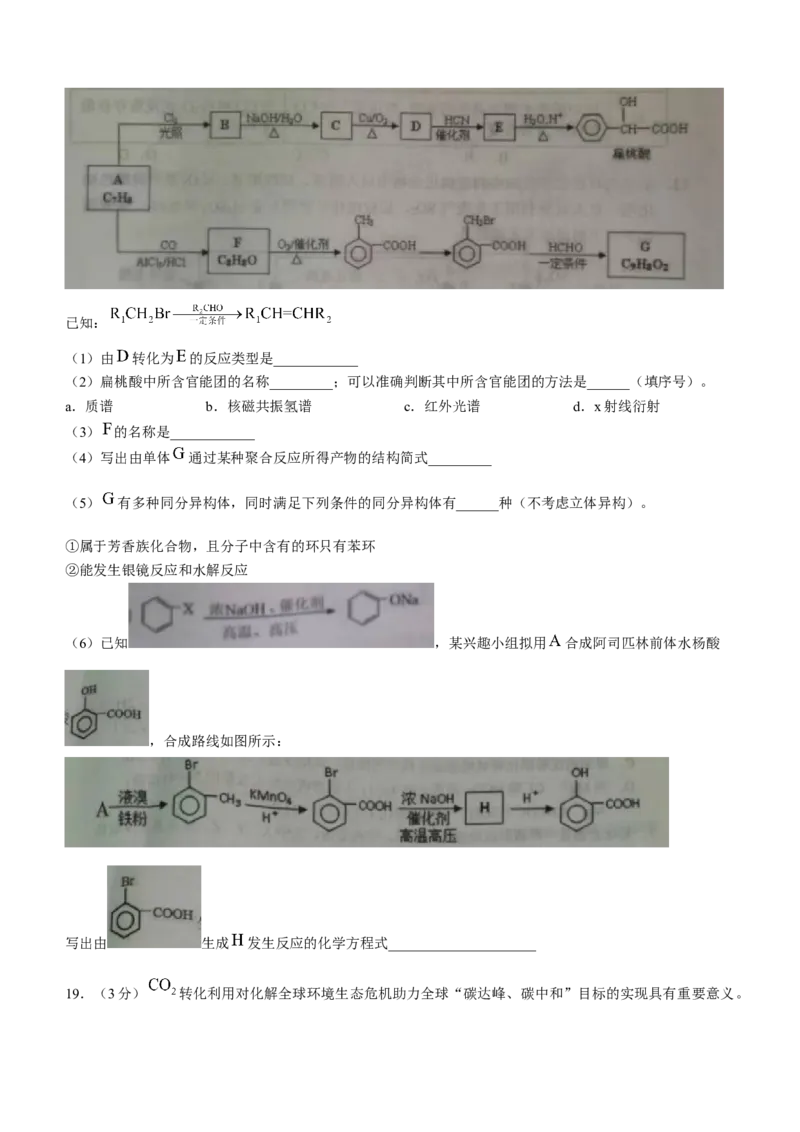
18.(14分)菜芳香烃 是一种重要的有机化工原料。以它为初始原料经过如下转化可以合成扁桃酸、医药
中间体 等多种物质。已知:
(1)由 转化为 的反应类型是____________
(2)扁桃酸中所含官能团的名称_________;可以准确判断其中所含官能团的方法是______(填序号)。
a.质谱 b.核磁共振氢谱 c.红外光谱 d.x射线衍射
(3) 的名称是____________
(4)写出由单体 通过某种聚合反应所得产物的结构简式_________
(5) 有多种同分异构体,同时满足下列条件的同分异构体有______种(不考虑立体异构)。
①属于芳香族化合物,且分子中含有的环只有苯环
②能发生银镜反应和水解反应
(6)已知 ,某兴趣小组拟用 合成阿司匹林前体水杨酸
,合成路线如图所示:
写出由 生成 发生反应的化学方程式_____________________
19.(3分) 转化利用对化解全球环境生态危机助力全球“碳达峰、碳中和”目标的实现具有重要意义。化学工作者致力于将 转化为各种化工原料。
Ⅰ.早在二十世纪初,工业上以 和 为原料在一定温度和压强下合成尿素。反应分两步:
① 和 生成 :② 分解生成尿素。
(1)活化能:反应①______反应②(填“>”、“<” 或“二”) :
(用含 的式子表示)
Ⅱ.我国科学家研究 电池,取得了重大科研成果。 电池中,反应产物为 ;和单质碳,
正极 电还原后与锂离子结合形成 按以下4个步骤进行,
① ② ③_____________________
④
(2)写出步骤③中 与 反应的离子方程式
Ⅲ.利用 和 重整技术可获得合成气(主要成分为 , ),重整过程中反应的热化学方程式如
下:
反应i:
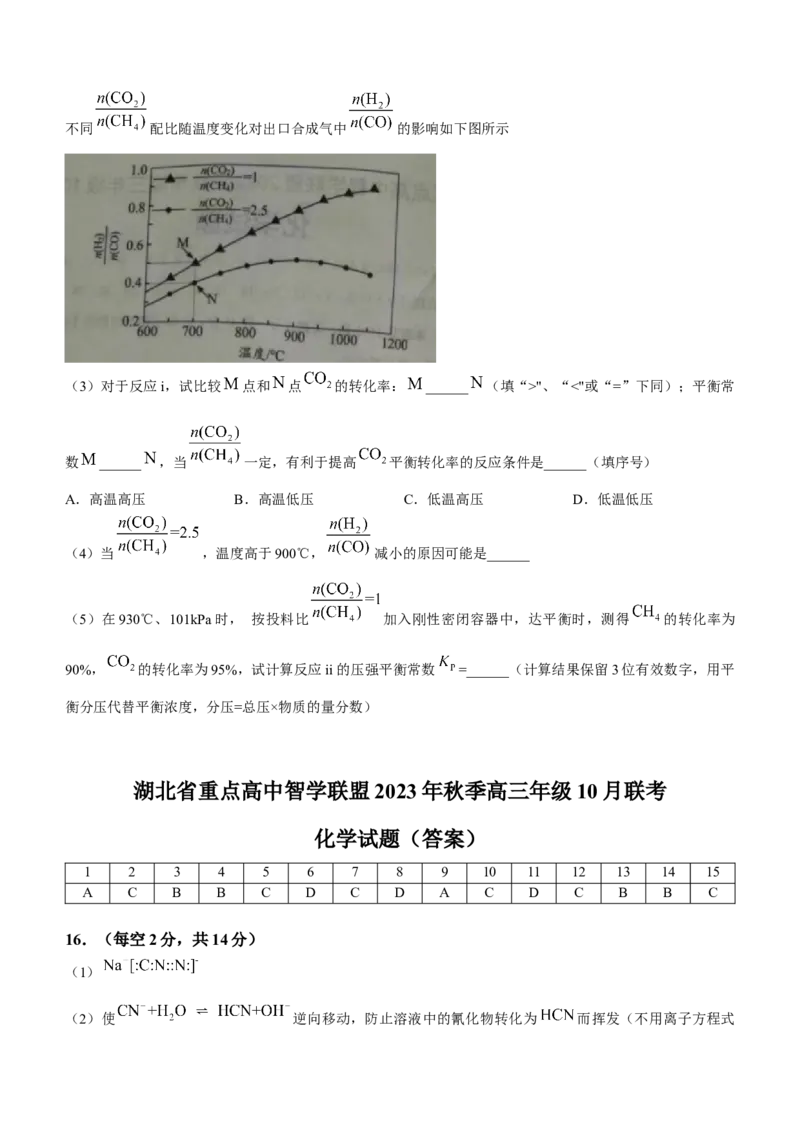
反应ii:不同 配比随温度变化对出口合成气中 的影响如下图所示
(3)对于反应i,试比较 点和 点 的转化率: ______ (填“>"、“<"或“=”下同);平衡常
数 ______ ,当 一定,有利于提高 平衡转化率的反应条件是______(填序号)
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(4)当 ,温度高于900℃, 减小的原因可能是______
(5)在930℃、101kPa时, 按投料比 加入刚性密闭容器中,达平衡时,测得 的转化率为
90%, 的转化率为95%,试计算反应ii的压强平衡常数 =______(计算结果保留3位有效数字,用平
衡分压代替平衡浓度,分压=总压×物质的量分数)
湖北省重点高中智学联盟 2023 年秋季高三年级 10 月联考
化学试题(答案)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
A C B B C D C D A C D C B B C
16.(每空2分,共14分)
(1)
(2)使 逆向移动,防止溶液中的氰化物转化为 而挥发(不用离子方程式解释也给分,如:防止 或 水解生成易挥发的 ,危害健康)
(3)
(4) (铅盐或写成 )与硫化钠反应生成难溶的 ,从而促进 被 溶解浸出。
(5) 或 也给分
( 也给分)
(6)14900
17.(除特殊标注外,每空2分,共14分)
(1) ;
(2)防倒吸(或安全瓶)
(3)溶液由红色变为无色
(4)
(5) (1 分) BD 溴水褪色
18.(每空2分,共14分)
(1)加成反应.
(2)羟基、羧基 cd
(3)邻甲基苯甲醛(2-甲基苯甲醛)
(4) (5) 5
(6) (条件不写全不扣分) .
19.(除特殊标注外,每空2分,共13分)
(1)<(1分) 写成 或 均给分
(2)(3)>(1分) = (1分)
(4)温度高于900℃后体系中发生的反应以反应ii为主, 作为反应物参与反应,导致其浓度减小,而生
成物 的浓度增大,因而导致比值减小。
(5)1.06