文档内容
绝密 启用前 油脂发生皂化反应后所得产物为高级脂肪酸和甘油
★ C.
邯郸市2023届高三年级摸底考试试卷 含棉 毛及合成纤维的废旧衣物燃烧处理时都只生成 和
D. 、 CO2 H2O
下列实验方案合理的是
化学
3. ( )
本试卷共8页 满分100分 考试用时75分钟
, , 。
注意事项:
1答卷前 考生务必将自己的姓名 班级 考场号 座位号 考生号填写在答题卡上
. , 、 、 、 、 。
2回答选择题时 选出每小题答案后 用铅笔把答题卡上对应题目的答案标号涂黑 如 准确量取一
. , , 。 熔 化 探究 对 和 C. 制取少量
A. Na2CO3 B. Cl - Fe 3+ S2O 2 3 - 定体积 D.
需改动 用橡皮擦干净后 再选涂其他答案标号 回答非选择题时 将答案写在答题卡上 固体 反应速率的影响 K2Cr2O7
, , 。 , 。 标准溶液 CO2
写在本试卷上无效 设N 为阿伏加德罗常数的值 下列说法正确的是
。 4. A , ( )
3 . 考试结束后 , 将本试卷和答题卡一并交回 。 A. 标准状况下 ,22.4L 氯气通入水中 , n (HClO)+ n (Cl - )+ n (ClO - )=2 N A
可能用到的相对原子质量
:H1 Li7 C12 N14 O16 Na23 Cl35.5 B. 标准状况下 ,2.24LCH2Cl2 含有的分子数大于 0.1 N A
K39 Cr52 Cu64 C. 室温下 ,pH 为 13 的 NaOH 溶液中 OH - 数目为 0.1 N A
一、单项选择题:本题共9小题,每小题3分,共27分。在每小题给出的四个 选项中 ,只
-1 溶液含有 N 个电子
D.1L1mol·L NaCl 28 A
有一项是符合题目要求的。
榄香素是一种无色油状液体 广泛分布于草药和香料中 主要用于医药麻醉 其结构如
5. , , ,
科技助力冬奥 各种材料大放异彩 下列材料的主要成分不属于有机高分子材料的是
图所示 下列有关榄香素的说法正确的是
1. , 。 。 ( )
( )
冬奥火炬 飞 颁奖礼仪服装
速滑服中的聚氨 B. “ 滑雪板板心木 D.
A. 扬 中的聚硅氮烷 C. 内胆材料 石墨
酯材料 ” 质材料 ———
树脂 烯
下列说法正确的是
2. ( )
聚乳酸是由乳酸发生缩聚反应制得的
A.
食物中的糖类均能被人体吸收
B.
化学试题 第 页 共 页 化学试题 第 页 共 页
1 ( 8 ) 2 ( 8 )
分子式为
A. C9H10O3
O
能发生消去反应
O
B.
苯环上的一氯代物有两种
C.
O
所有碳原子可能共平面
D.
硫氰化铁常被用于电影特技和魔术表演 其制备原理为
6. , FeCl3+3KSCN
已知氯化铁固体的熔点为 沸点为 易升华 下列说
Fe(SCN)3+3KCl。 306℃、 316℃, 。
法正确的是
( )
第一电离能 晶体属于离子晶体
A. :N>S B.Fe(SCN)3
的几何构型为 形 熔点
-
C.SCN V D. :FeCl3>KCl某科学家首次发现在温和的条件下利用 二、不定项选择题:本题共4小题,每小题4分,共16分。在每小题给出的四个选项中,
7.
和 做共同催化剂 卤代烃和炔烃 有一项或两项符合题目要求。若正确答案只包括一个选项,多选时,该小题得0分;
L n Pd CuX ,
发生偶联反应 其偶联反应机理如图 已
若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得4分,但
, 。
知 为烃基 为卤素原子 下列说法
只要选错一个,该小题得0分。
1 2
:R、R ,X ,
绿原酸是咖啡和茶中的主要化合物 具有降血压 抗菌 抗病毒等药理作用 下列有
正确的是 10. , 、 、 。
( )
关绿原酸的说法正确的是
在此偶联反应的机理图中共呈现了 种价态 ( )
A.Pd 3
可与 溶液发生显色反应
每步反应均存在极性键的断裂和形成 A. FeCl3
B. 含有两种含氧官能团
催化剂 B.
该偶联反应的总反应为
1 2 2 1 该分子最多能与 发生反应
C. R—X+R—C≡CH →HX+R—C≡C—R
C.1mol 8molNaOH
若 分别为甲基 乙基 反应除生成 戊炔外 还能生成 丁炔和 己炔
1 2 该分子最多能与 发生反应
D. R、R 、 , 2- , 2- 2-
D.1mol 4molBr2
下列实验操作 现象及所得结论均正确的是 钛酸锂电池由于具有体积小 重量轻 能量密度高 安全稳定 绿色环保等特点 在通信电
8. 、 ( ) 11. 、 、 、 、 ,
源领域具有非常广泛的应用前景 其工作原理如图所示 下列说法正确的是
选项 操作 现象 结论 。 , ( )
向蛋白质溶液中加入饱和
Na2SO4 有沉淀出现 蛋白质发生了变性
A 溶液
向滴有酚酞的 溶液中加入 溶液中存在水解
Na2CO3 红色变浅 Na2CO3
B 固体 平衡
BaCl2
室温下 用 试纸分别测定浓度
, pH 前者
C
为
0.1mol·L -1 HClO
溶液和
大于后
pH
者 HClO
的酸性小于
HF
溶液的 放电时 移向 极
0.1mol·L -1 HF pH A. ,Li + N
加热 固体 并用湿润的 充电时 极接外电源的负极
NH4HCO3 , 试纸变蓝 显碱性 B. ,M
D 红色石蕊试纸检验产物 NH4HCO3
充电时 极的电极反应式
+ -
C. ,N :Ti5O12+4Li +4e Li4Ti5O12
下列 类比 或 对比 合理的是
9. “ ” “ ” ( ) 用该电池电解精炼铜 当 两极质量变化差为 时 理论上可生成 精铜
D. , M、N 14g , 64g
溶液与过量的氨水反应生成 沉淀 则 溶液与过量的氨水反
A.MgCl2 Mg(OH)2 , AlCl3 一种抗甲状腺药物结构简式如图所示 其中 为原子序数依次增大的短周
12. , W、X、Y、Z
应生成 沉淀
Al(OH)3 期元素 分别位于三个周期 原子序数 下列说法错误的是
, , W+X=Y, ( )
在空气中燃烧生成 则 在空气中燃烧生成
B.Na Na2O2, Li Li2O2 原子半径
A. :Z>Y>X
在潮湿的空气中被腐蚀最终生成氧化物 则 在潮湿的空气中被腐蚀最终生
C.Fe , Cu 和 的最高价含氧酸均为强酸
B.Y Z
成氧化物
和 形成的化合物中只含共价键
C.W Y
固体与浓 加热可制 则 固体与浓 加热可制
D.NaCl H2SO4 HCl, NaI H2SO4 HI 该物质中 为 3 杂化
D. Y sp
化学试题 第 页 共 页 化学试题 第 页 共 页
3 ( 8 ) 4 ( 8 )常温下 向 的甘氨酸盐酸盐 化学式为 中逐 装置 中的试剂 是
-1
13. , 10mL0.1mol·L ( HOOCCH2NH3Cl) (3) C X 。
滴加入 的 溶液 滴定过程中溶液的 与 溶液体积的变 装置 的作用为
-1
0.1mol·L NaOH , pH NaOH (4) E 。
化曲线如图所示 已知 甘氨酸盐酸盐与 溶液的反应过程为 无水 易吸水形成暗绿色的 晶体 该配合物的中
。 : NaOH (5) CrCl3 [CrCl2(H2O)4]Cl·2H2O ,
心微粒为 该配合物中含有 键的数目为
+ OH - + - OH - - 下列有 ,1mol σ 。
H3N —CH2—COOH →H3N —CH2—COO →H2N—CH2—COO 。
含量的测定 准确称取m 固体样品 加水配成 溶液 量取
关说法错误的是 (6)CrCl3 : g , 250mL , 25mL
( )
溶液于碘量瓶中 加入一定量的过氧化钠 待溶液由绿色转化为黄色后 充分加热煮
, , ,
沸 冷却后滴加 使溶液显酸性 再向橙色溶液中加入过量
-1
, 2mol·L H2SO4 ,
溶液 其反应的离子方程式为
-1
1mol·L KI ,
充分反应后以淀粉作指示剂 用c
-1
溶液滴定 滴定终点消
, , mol·L Na2S2O3 ,
耗V 溶液 则样品中 的质量分数为 用含cVm 的
mLNa2S2O3 , CrCl3 ( “、、 ”
式子表示 已知 黄色 橙色
+ 的电离平衡常数的数量级为 -3 )[ :2CrO 2 4 - ( )+2H + Cr2O 2 7 - ( )+H2O,I2+2Na2S2O3
A.H3N CH2COOH 10
溶液显酸性 Na2S4O6+2NaI]。
B.NaOOCCH2NH3Cl
分 四钼酸铵晶体 微溶于水和铵盐溶液 在过量浓氨水
时c + c + c - c + - 15.(14 ) [(NH4)2Mo4O13·2H2O] ,
C.pH=9.60 ,(H )+ (H3N CH2COOH)> (OH )+ (H3N CH2COO )
中转化为 溶液 是钼深加工的重要中间品 具有广泛的用途 一种以
时 溶液满足c + c + - (NH4)2MoO4 , , 。
D.pH=7 , (H3N CH2COOH)+ (H3N CH2COO )+
辉钼矿 主要成分是 还含有 和 的氧化物等杂质 为原料生
c - c - ( MoS2, NiS、PbS、SiO2 Fe )
(H2NCH2COO )= (Cl )
产四钼酸铵晶体 的工艺流程如下
三、非选择题:本题共4小题,共57分。 [(NH4)2Mo4O13·2H2O] :
稀硫酸
分 氯化铬 是重要的铬盐 某实验小组利用下图所示装置在实验室制备
空气 稀硫酸 过量浓氨水
14.(14 ) (CrCl3) ,
+H2O2
pH=5一.5系列操作
夹持装置略去 已知 易潮解 易溶于水 铬粉在空气中灼烧生成 辉钼矿 焙↓烧 酸↓浸 除↓杂 结↓晶 四钼酸铵晶体
CrCl3( )。 :CrCl3 , ,
→ → → → →
易与盐酸反应生成氯化亚铬 请回答下列问题 尾↓气 滤↓渣 滤↓渣
Cr2O3, (CrCl2)。 :
Ⅰ Ⅱ
已知 可以将 氧化 故不能存在于水溶液中
3+
:Ni H2O , 。
回答下列问题
:
号元素钼 在周期表中位于第五周期第 族 其价电子排布式为
(1)42 (Mo) ⅥB ,
核外有 种空间运动状态不同的电子
, 。
按照气流由左到右的方向 上述装置合理的连接顺序为 焙烧 时通入过量空气的目的是
(1) , a→ (2)“ ” ,
填仪器接口字母 焙烧 时将 转化为 其反应的化学方程式为
( )。 “ ” MoS2 MoO3,
装置 中橡皮管的作用为
(2) A 。 。
化学试题 第 页 共 页 化学试题 第 页 共 页
5 ( 8 ) 6 ( 8 )酸浸 时 转化为 的作用是 分 以氢气 一氧化碳为主要组分的合成气是一种重要的化工原料 可以合成甲
2+
(3)“ ” ,MoO3 MoO2 ,H2O2 17.(14 ) 、 ,
滤渣 的成分是 填化学式 醇等许多重要的化工产品 回答下列问题
, Ⅰ ( )。 。 :
除杂 时 主要反应的离子方程式为 合成甲醇的热化学方程式为 H
(4)“ ” , ; (1) CO(g)+2H2(g)CH3OH(g) Δ =-90.0
加入 过量浓氨水 使溶液 时剩余杂质元素完全沉淀 已知
“ ” pH≥ 。( : kJ·mol -1 。
当溶液中某离子浓度 -5 -1 时 认为其沉淀完全 常温下 K 已知 相关化学键的键能如表所示 则表中的x 该反应在 填
≤10 mol·L , 。 ,sp[Ni(OH)2] : , = ; (
-16 K -38 高温 低温 或 任何温度 下能自发进行
=1.0×10 ,sp[Fe(OH)3]=8.0×10 。) “ ”“ ” “ ”) 。
结晶 时 滴加稀硫酸调节溶液的 为 的目的是
化学键
(5)“ ” , pH 5.5
C≡O H—H H—O C—O C—H
。 键能 /(kJ·mol -1) x 436 465 351 413
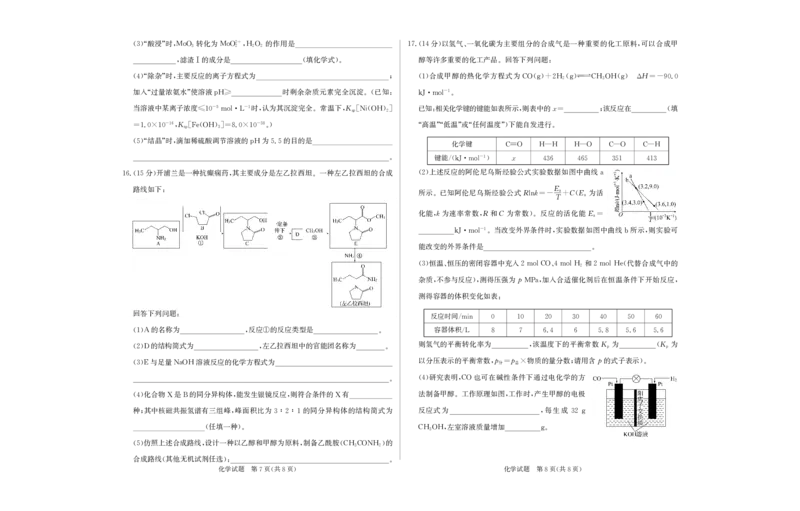
分 开浦兰是一种抗癫痫药 其主要成分是左乙拉西坦 一种左乙拉西坦的合成 上述反应的阿伦尼乌斯经验公式实验数据如图中曲线
16.(15 ) , 。 (2) a
路线如下 E
: 所示 已知阿伦尼乌斯经验公式Rk a CE 为活
。 ln =-T+ (a
化能k为速率常数 R和C为常数 反应的活化能E
, , )。 a=
当改变外界条件时 实验数据如图中曲线 所示 则实验可
-1
kJ·mol 。 , b ,
能改变的外界条件是
。
恒温 恒压的密闭容器中充入 和 代替合成气中的
(3 ) 、 2molCO、4molH2 2molHe(
杂质 不参与反应 测得压强为 加入合适催化剂后在恒温条件下开始反应
p
, ), MPa, ,
测得容器的体积变化如表
:
回答下列问题
反应时间
:
/min 0 10 20 30 40 50 60
的名称为 反应 的反应类型是 容器体积
(1)A , ① 。 /L 8 7 6.4 6 5.8 5.6 5.6
的结构简式为 左乙拉西坦中的官能团名称为 则氢气的平衡转化率为 该温度下的平衡常数K 为 K 为
(2)D , 。 , p (p
与足量 溶液反应的化学方程式为 以分压表示的平衡常数 p分 p总 物质的量分数 请用含 p 的式子表示
(3)E NaOH , = × ; )。
研究表明 也可在碱性条件下通过电化学的方
。 (4) ,CO
化合物 是 的同分异构体 能发生银镜反应 则符合条件的 有 法制备甲醇 工作原理如图 工作时 产生甲醇的电极
(4) X B , , X 。 , ,
种 其中核磁共振氢谱有三组峰 峰面积比为 的同分异构体的结构简式为 反应式为 每生成
; , 3∶2∶1 , 32g
任填一种 左室溶液质量增加
( )。 CH3OH, g。
仿照上述合成路线 设计一种以乙醇和甲醇为原料 制备乙酰胺 的
(5) , , (CH3CONH2)
合成路线 其他无机试剂任选
( ): 。
化学试题 第 页 共 页 化学试题 第 页 共 页
7 ( 8 ) 8 ( 8 )