文档内容
泸县五中高2022级高考适应性考试
化 学
化学试卷分为第一部分(选择题)和第二部分(非选择题)两部分。
满分:100分。考试时间:75分钟。
注意事项:相对原子质量:H-1 O-16 S-32 Fe-56 Cu-64 Cl-35.5 Ag-108
第一部分 选择题(共42分)
一、选择题:本题共14小题,每小题3分,共42分。每小题给出的四个选项中,只有一项是符合题目要
求。
1.化学与生产和生活密切相关,下列过程与水解无关的是
A.明矾净水 B.油脂的皂化
C. 水热法制 D.核苷酸转化为核酸
2.下列化学用语表达正确的是
A.HClO的电子式:
B.CH 分子和CCl 分子的空间填充模型均为
4 4
C.Na S溶液久置后出现浑浊,颜色变深:Na S+2O =Na SO
2 2 2 2 4
D.向FeCl 溶液中滴入K [Fe(CN) ]溶液:K++Fe2++[Fe(CN) ]3-=KFe[Fe(CN) ]↓
2 3 6 6 6
3.下列有关物质用途及性质都正确但是二者不匹配的是
选项 用途 性质
A 做豆腐时加卤水“点卤” 卤水能使蛋白质聚沉
口服小苏打水可缓解服用阿司匹林引发的酸中
B 能与酸反应
毒
C 脲醛塑料(电玉,UF)作电器开关和插座 UF绝缘性好、耐溶剂性好
D 丁基羟基菌香醚(BHA)作脂肪制品的抗氧化剂 BHA具有可燃性
A.A B.B C.C D.D
4.实验室按以下方案从某海洋动物提取具有抗肿瘤活性的天然产物。下列实验方法或仪器错误的是
A.步骤(1)需要过滤装置
B.步骤(2)水层溶液从分液漏斗下口放出
C.步骤(3)需要用到坩埚
D.步骤(4)可利用物质的沸点不同分离
5.设N 为阿伏加德罗常数的值。下列叙述错误的是
A
A.在电解精炼粗铜的过程中,当阴极质量增重32g时转移的电子数为
第 1 页 共 9 页
学科网(北京)股份有限公司B.标准状况下,11.2LSO 分子数目大于
3
C.15g乙烯和20g丙烯的混合气体中含有C—H共价键的数目为
D.4.6gNa与足量O 充分反应,反应中转移的电子数介于 和 之间
2
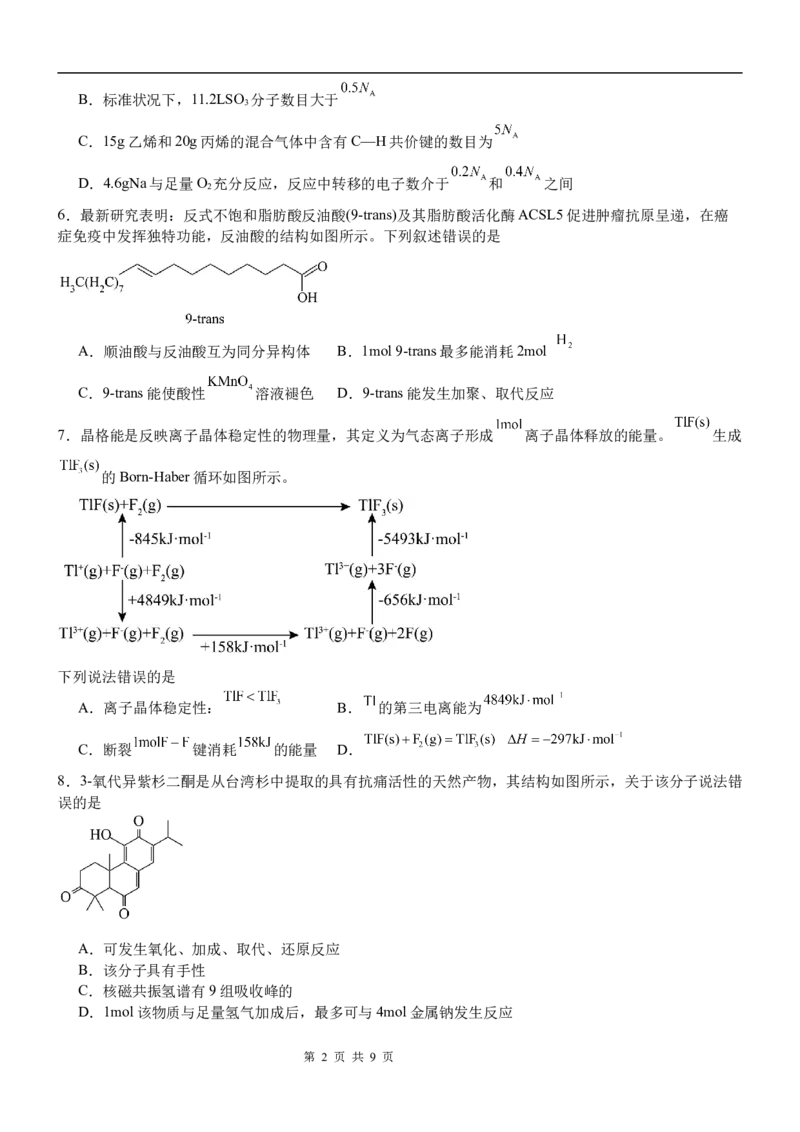
6.最新研究表明:反式不饱和脂肪酸反油酸(9-trans)及其脂肪酸活化酶ACSL5促进肿瘤抗原呈递,在癌
症免疫中发挥独特功能,反油酸的结构如图所示。下列叙述错误的是
A.顺油酸与反油酸互为同分异构体 B.1mol 9-trans最多能消耗2mol
C.9-trans能使酸性 溶液褪色 D.9-trans能发生加聚、取代反应
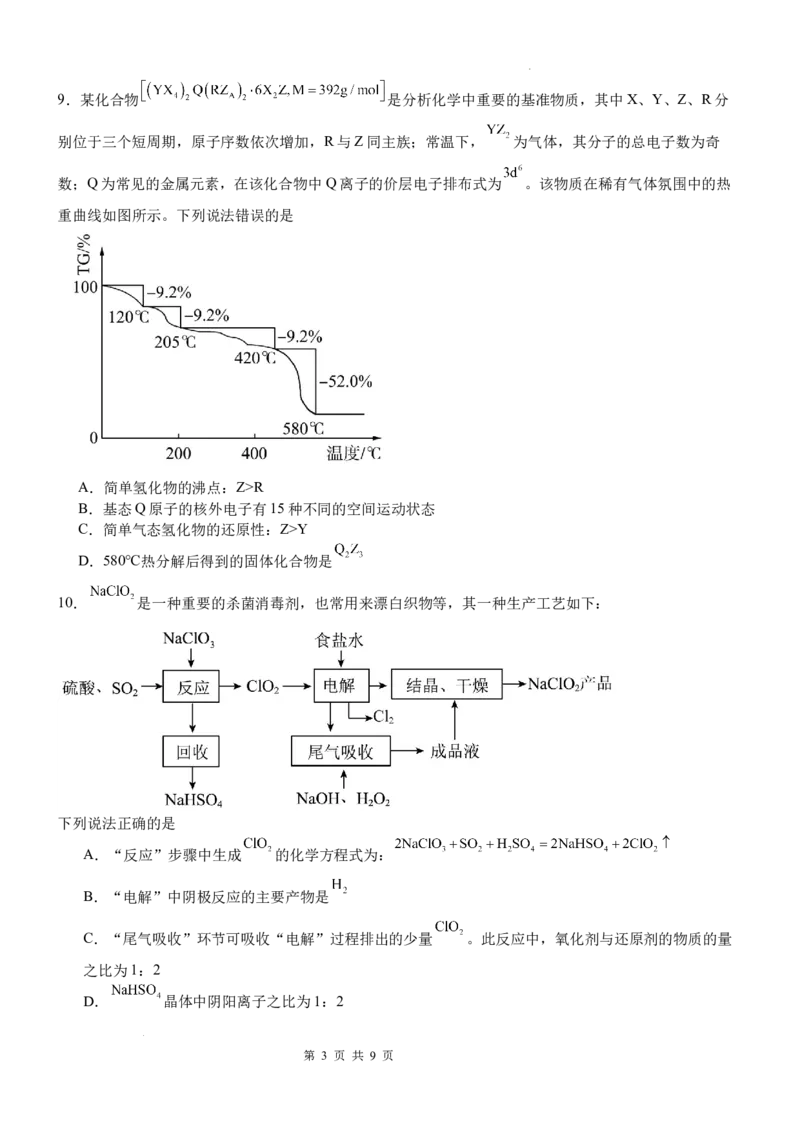
7.晶格能是反映离子晶体稳定性的物理量,其定义为气态离子形成 离子晶体释放的能量。 生成
的Born-Haber循环如图所示。
下列说法错误的是
A.离子晶体稳定性: B. 的第三电离能为
C.断裂 键消耗 的能量 D.
8.3-氧代异紫杉二酮是从台湾杉中提取的具有抗痛活性的天然产物,其结构如图所示,关于该分子说法错
误的是
A.可发生氧化、加成、取代、还原反应
B.该分子具有手性
C.核磁共振氢谱有9组吸收峰的
D.1mol该物质与足量氢气加成后,最多可与4mol金属钠发生反应
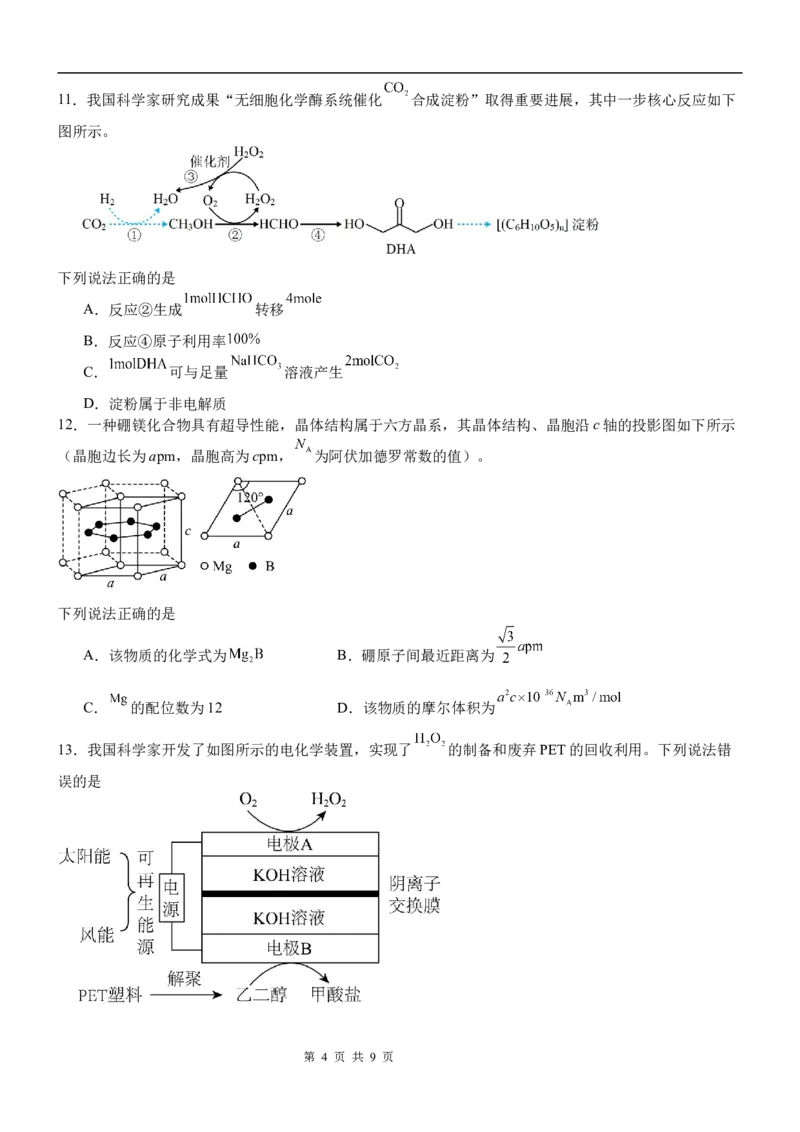
第 2 页 共 9 页9.某化合物 是分析化学中重要的基准物质,其中X、Y、Z、R分
别位于三个短周期,原子序数依次增加,R与Z同主族;常温下, 为气体,其分子的总电子数为奇
数;Q为常见的金属元素,在该化合物中Q离子的价层电子排布式为 。该物质在稀有气体氛围中的热
重曲线如图所示。下列说法错误的是
A.简单氢化物的沸点:Z>R
B.基态Q原子的核外电子有15种不同的空间运动状态
C.简单气态氢化物的还原性:Z>Y
D.580℃热分解后得到的固体化合物是
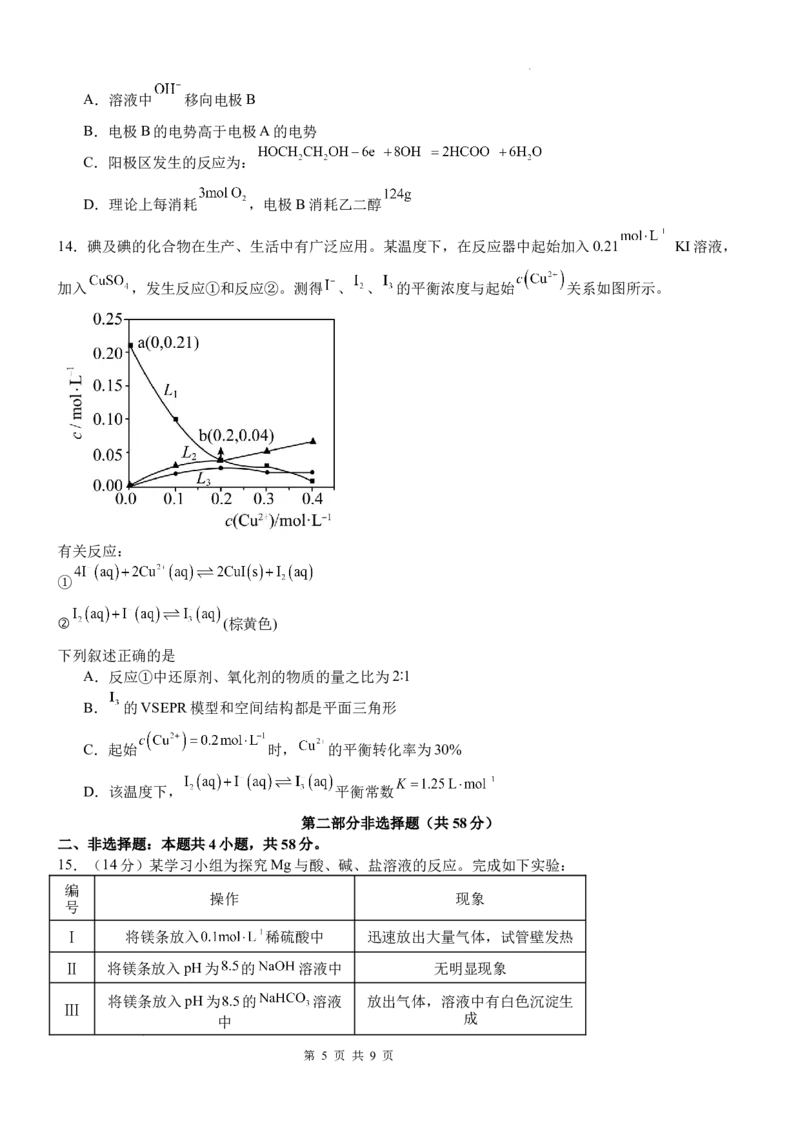
10. 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
下列说法正确的是
A.“反应”步骤中生成 的化学方程式为:
B.“电解”中阴极反应的主要产物是
C.“尾气吸收”环节可吸收“电解”过程排出的少量 。此反应中,氧化剂与还原剂的物质的量
之比为1:2
D. 晶体中阴阳离子之比为1:2
第 3 页 共 9 页
学科网(北京)股份有限公司11.我国科学家研究成果“无细胞化学酶系统催化 合成淀粉”取得重要进展,其中一步核心反应如下
图所示。
下列说法正确的是
A.反应②生成 转移
B.反应④原子利用率
C. 可与足量 溶液产生
D.淀粉属于非电解质
12.一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示
(晶胞边长为apm,晶胞高为cpm, 为阿伏加德罗常数的值)。
下列说法正确的是
A.该物质的化学式为 B.硼原子间最近距离为
C. 的配位数为12 D.该物质的摩尔体积为
13.我国科学家开发了如图所示的电化学装置,实现了 的制备和废弃PET的回收利用。下列说法错
误的是
第 4 页 共 9 页A.溶液中 移向电极B
B.电极B的电势高于电极A的电势
C.阳极区发生的反应为:
D.理论上每消耗 ,电极B消耗乙二醇
14.碘及碘的化合物在生产、生活中有广泛应用。某温度下,在反应器中起始加入0.21 KI溶液,
加入 ,发生反应①和反应②。测得 、 、 的平衡浓度与起始 关系如图所示。
有关反应:
①
② (棕黄色)
下列叙述正确的是
A.反应①中还原剂、氧化剂的物质的量之比为2∶1
B. 的VSEPR模型和空间结构都是平面三角形
C.起始 时, 的平衡转化率为30%
D.该温度下, 平衡常数
第二部分非选择题(共58分)
二、非选择题:本题共4小题,共58分。
15.(14分)某学习小组为探究Mg与酸、碱、盐溶液的反应。完成如下实验:
编
操作 现象
号
Ⅰ 将镁条放入 稀硫酸中 迅速放出大量气体,试管壁发热
Ⅱ 将镁条放入pH为 的 溶液中 无明显现象
将镁条放入pH为 的 溶液 放出气体,溶液中有白色沉淀生
Ⅲ
中 成
第 5 页 共 9 页
学科网(北京)股份有限公司回答下列问题:
(1)实验前除去镁表面氧化物的方法是 。
(2)实验Ⅰ的离子方程式为 。
(3)经实验分析,实验Ⅲ中产生的气体为 和 混合气体。产生 气体的原因是 。
(4)该组同学们比较实验Ⅱ、Ⅲ后,分析认为:实验Ⅲ能快速反应的原因,与溶液中白色沉淀有关。为探究
其成分,设计了如下实验。
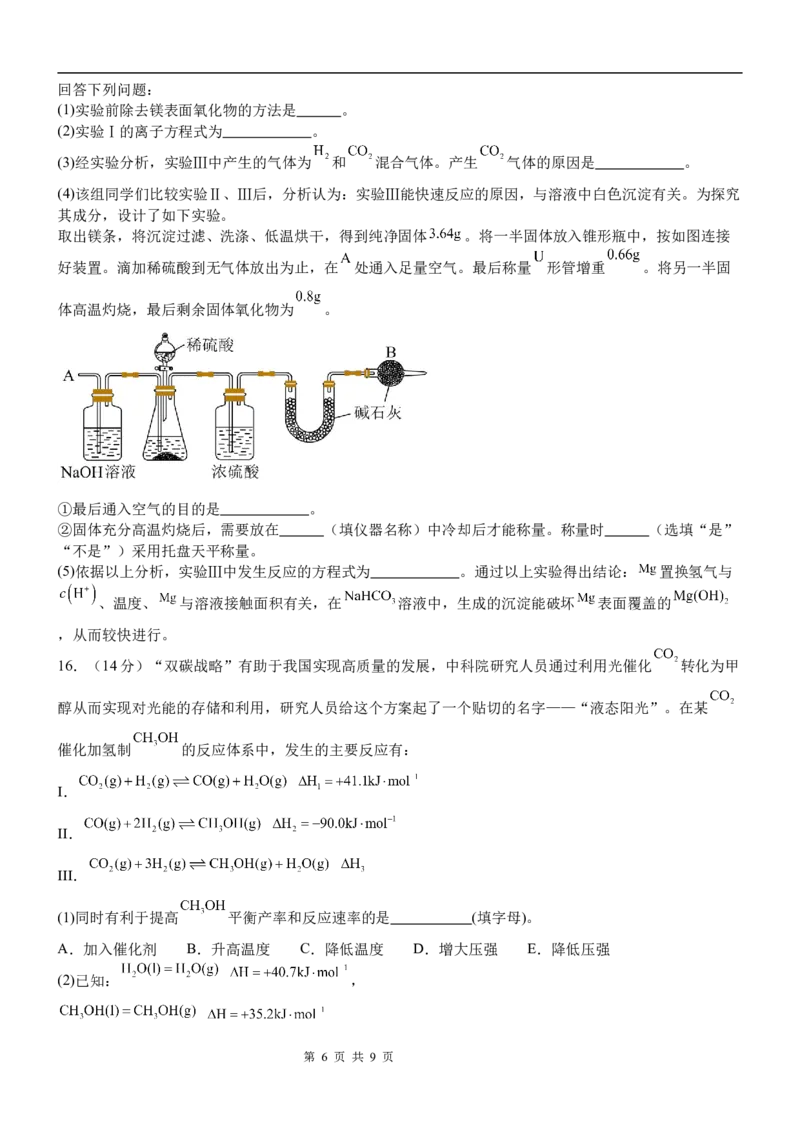
取出镁条,将沉淀过滤、洗涤、低温烘干,得到纯净固体 。将一半固体放入锥形瓶中,按如图连接
好装置。滴加稀硫酸到无气体放出为止,在 处通入足量空气。最后称量 形管增重 。将另一半固
体高温灼烧,最后剩余固体氧化物为 。
①最后通入空气的目的是 。
②固体充分高温灼烧后,需要放在 (填仪器名称)中冷却后才能称量。称量时 (选填“是”
“不是”)采用托盘天平称量。
(5)依据以上分析,实验Ⅲ中发生反应的方程式为 。通过以上实验得出结论: 置换氢气与
、温度、 与溶液接触面积有关,在 溶液中,生成的沉淀能破坏 表面覆盖的
,从而较快进行。
16.(14分)“双碳战略”有助于我国实现高质量的发展,中科院研究人员通过利用光催化 转化为甲
醇从而实现对光能的存储和利用,研究人员给这个方案起了一个贴切的名字——“液态阳光”。在某
催化加氢制 的反应体系中,发生的主要反应有:
I.
II.
III.
(1)同时有利于提高 平衡产率和反应速率的是 (填字母)。
A.加入催化剂 B.升高温度 C.降低温度 D.增大压强 E.降低压强
(2)已知: ,
第 6 页 共 9 页常温常压下,在一密闭钢瓶中通入 和 只发生反应Ⅲ,当生成 的 时放出
的能量。
(3)在实际的生产过程中还会发生副反应,如IV. ,若某温度下,
反应I、Ⅱ的平衡常数分别为 ,则反应IV的平衡常数 (用含 的表达式表
示)。
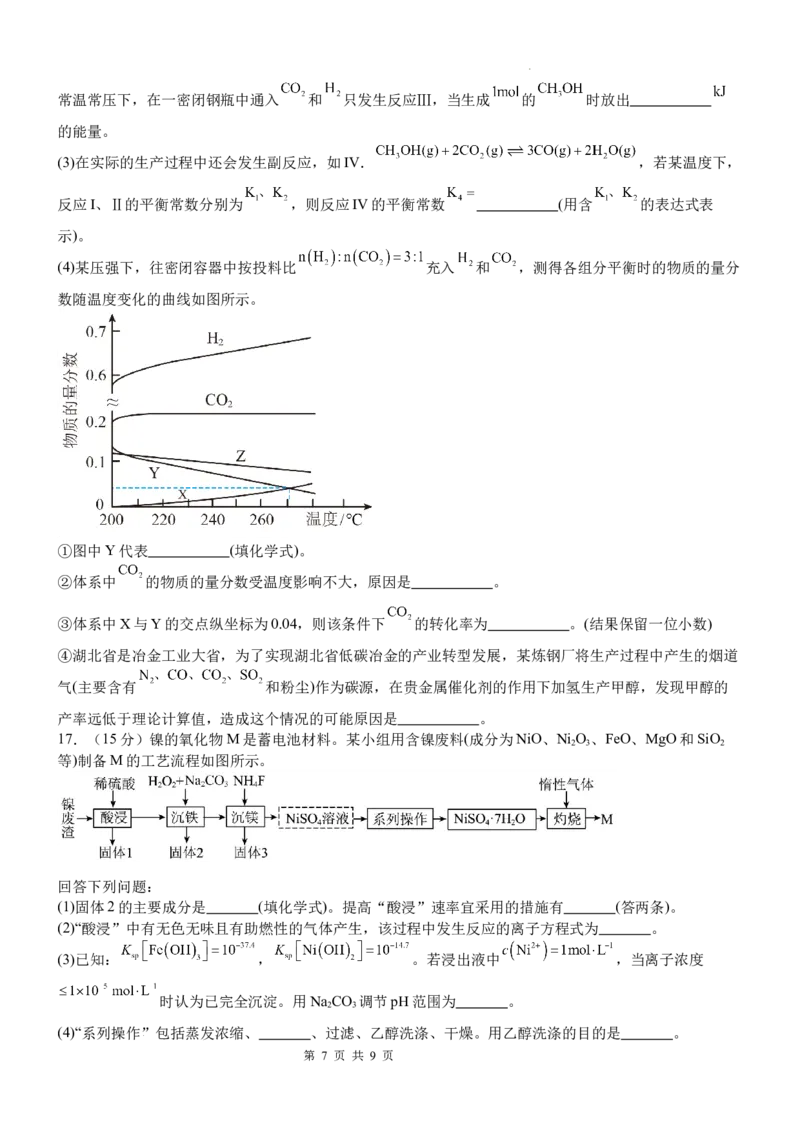
(4)某压强下,往密闭容器中按投料比 充入 和 ,测得各组分平衡时的物质的量分
数随温度变化的曲线如图所示。
①图中Y代表 (填化学式)。
②体系中 的物质的量分数受温度影响不大,原因是 。
③体系中X与Y的交点纵坐标为0.04,则该条件下 的转化率为 。(结果保留一位小数)
④湖北省是冶金工业大省,为了实现湖北省低碳冶金的产业转型发展,某炼钢厂将生产过程中产生的烟道
气(主要含有 和粉尘)作为碳源,在贵金属催化剂的作用下加氢生产甲醇,发现甲醇的
产率远低于理论计算值,造成这个情况的可能原因是 。
17.(15分)镍的氧化物M是蓄电池材料。某小组用含镍废料(成分为NiO、Ni O 、FeO、MgO和SiO
2 3 2
等)制备M的工艺流程如图所示。
回答下列问题:
(1)固体2的主要成分是 (填化学式)。提高“酸浸”速率宜采用的措施有 (答两条)。
(2)“酸浸”中有无色无味且有助燃性的气体产生,该过程中发生反应的离子方程式为 。
(3)已知: , 。若浸出液中 ,当离子浓度
时认为已完全沉淀。用Na CO 调节pH范围为 。
2 3
(4)“系列操作”包括蒸发浓缩、 、过滤、乙醇洗涤、干燥。用乙醇洗涤的目的是 。
第 7 页 共 9 页
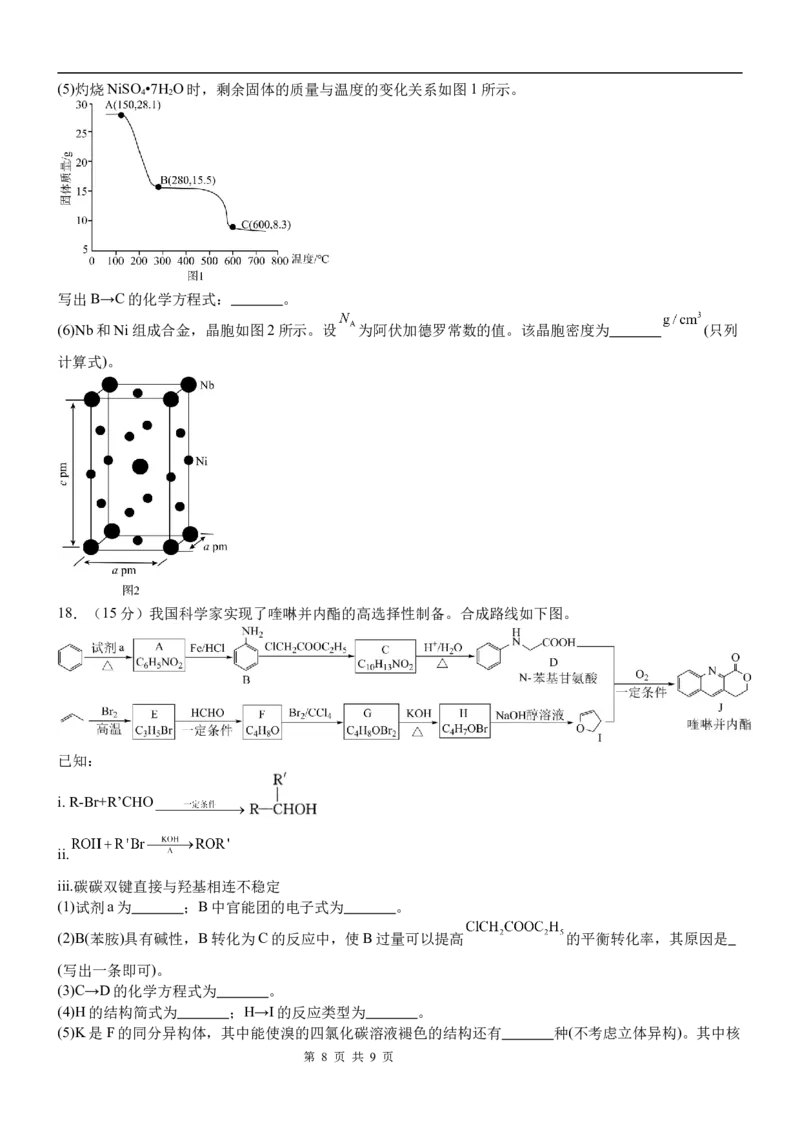
学科网(北京)股份有限公司(5)灼烧NiSO •7H O时,剩余固体的质量与温度的变化关系如图1所示。
4 2
写出B→C的化学方程式: 。
(6)Nb和Ni组成合金,晶胞如图2所示。设 为阿伏加德罗常数的值。该晶胞密度为 (只列
计算式)。
18.(15分)我国科学家实现了喹啉并内酯的高选择性制备。合成路线如下图。
已知:
i. R-Br+R’CHO
ii.
iii.碳碳双键直接与羟基相连不稳定
(1)试剂a为 ;B中官能团的电子式为 。
(2)B(苯胺)具有碱性,B转化为C的反应中,使B过量可以提高 的平衡转化率,其原因是
(写出一条即可)。
(3)C→D的化学方程式为 。
(4)H的结构简式为 ;H→I的反应类型为 。
(5)K是F的同分异构体,其中能使溴的四氯化碳溶液褪色的结构还有 种(不考虑立体异构)。其中核
第 8 页 共 9 页磁共振氢谱有3组峰,峰面积之比为2:3:3的结构简式为 。
(6)D和I转化成J的反应过程中还生成水,理论上该过程中消耗的 与生成的J的物质的量之比为
。
第 9 页 共 9 页
学科网(北京)股份有限公司